用于产生免屠宰肉的营养培养基
文献发布时间:2023-06-19 19:28:50
相关申请的交叉引用
本申请要求于2020年6月5日提交的美国临时专利申请号63/035,661的优先权,其内容通过引用以其整体并入本文。
通过引用序列表并入
本申请包含序列表,该序列表已通过EFS-WEB以ASCII格式提交,并在此通过引用以其整体并入。所述ASCII副本创建于2021年6月7日,名为MPHM_015_01WO_SeqList_ST25.txt,大小为7.97kb。
背景技术
采用通过体外培养后生动物细胞产生的肉类作为从屠宰动物获得的传统动物肉的替代品,势头越来越好。此类肉(在本文中也可互换地称为细胞肉、体外产生的细胞肉、基于细胞培养的肉、体外肉、培养肉、实验室培养的肉或清洁肉)提供了传统肉的可持续替代品并克服了相关的缺点,如微生物污染和暴露于激素和抗生素。它还提供了一些环境效益,包括保护土地和水资源的使用、高热量转换和减少温室气体排放。此外,它还解决了与传统肉产生相关的动物福利问题。
广泛采用细胞肉的一个障碍是其相对较高的成本。细胞肉的产生与其培养中使用的细胞培养基有着错综复杂的联系,目前估计约占最终产品成本的80%。用于细胞肉产生的细胞培养基的配方面临独特的挑战,例如可扩展性、安全和监管考虑以及成本效率。源自动物源性血清,如胎牛血清,是大多数细胞培养基的常见组分,为高效细胞培养提供营养物和蛋白质的基本混合物。然而,动物源性血清目前还没有达到培养细胞肉所需的工业规模。由于其异质的动物来源,使用动物源性血清还可引入批次间可变性和危险病原体,并且因此需要更多涉及的质量控制措施。
随着细胞肉越来越接近市场,如FDA和USDA的机构及其国际同行会被要求提供安全和监管监督。用于细胞肉类培养的细胞培养基及其组分可被FDA视为需要监管监督的食品添加剂。
因此,开发用于产生细胞肉的细胞培养基配方的需求尚未得到满足,该配方满足高安全标准、成本效率、工业规模的适用性,并且含有最少或没有动物源性血清和/或其他动物源性组分。本文提供了用于产生细胞肉的新型细胞培养基组合物和方法,其满足这些及相关需求。
发明内容
本文提供了与用于产生免屠宰肉的营养培养基的产生和使用相关的组合物和方法。
因此,在一个方面,本文提供了一种用于产生免屠宰肉的可食用营养培养基,所述培养基包含多种成分,其中每种成分被批准用于食品和/或等于或低于其ADI值。在一些实施方案中,被批准用于食品的成分是公认安全的(GRAS)。在一些实施方案中,所述成分被FDA、USDA、食品法典、欧洲食品安全局和/或食品化学法典批准用于食品中。
在一些实施方案中,培养基含有不超过10%、9%、8%、7%、6%、5%、4%、3%、2%、1%、0.5%、0.1%、0.05%或不超过0.01%%的动物源性血清。在一些实施方案中,培养基基本上不含动物源性血清或不含动物源性血清。在一些实施方案中,培养基含有不超过10%、9%、8%、7%、6%、5%、4%、3%、2%、1%、0.5%、0.1%、0.05%或不超过0.01%%的动物源性组分。在一些实施方案中,培养基基本上不含动物源性组分或不含动物源性组分。在一些实施方案中,培养基是在化学上定义的。
在一些实施方案中,培养基还包含生长因子。在一些实施方案中,培养基还包含通用生长因子。在一些实施方案中,通用生长因子是FGF-2。在一些实施方案中,通用FGF-2包含SEQ ID NO:3所示的氨基酸序列。在一些实施方案中,通用FGF-2由SEQ ID NO:4所示的核酸序列编码。
在一些实施方案中,通用生长因子是PDGF-BB。在一些实施方案中,通用PDGF-BB包含SEQ ID NO:5所示的氨基酸序列。
在一些实施方案中,通用生长因子是IGF-1。在一些实施方案中,通用IGF-1包含SEQ ID NO:6所示的氨基酸序列。
在一些实施方案中,通用生长因子是VEGF-A。在一些实施方案中,通用VEGF-A包含SEQ ID NO:7所示的氨基酸序列。
在一些实施方案中,培养基用于培养免屠宰肉,并且生长因子是顺式生长因子,其中顺式生长因子与培养中的细胞的属匹配。在一些实施方案中,与非顺式生长因子相比,顺式生长因子的使用允许增强的细胞生长或肉产生。在一些实施方案中,与非顺式生长因子相比允许增强细胞生长的顺式生长因子是顺式原鸡属(Gallus)转铁蛋白。在一些实施方案中,顺式生长因子是培养中细胞的属的相应天然存在的生长因子的变体。在一些实施方案中,顺式生长因子变体是原鸡属LR3-IGF1。在一些实施方案中,原鸡属LR3-IGF1包含SEQ IDNO:1所示的氨基酸序列。
在一些实施方案中,生长因子选自下组:IGF1、LR3-IGF1、FGF-1、FGF-2、PDGF、CTGF、EGF、TGFB、BMP、HGF、转铁蛋白、胰岛素、WNT、白介素、白蛋白、VEGF、同源物、旁系同源物、直向同源物、变体、前体、同源异构体及其组合。在一些实施方案中,生长因子任选地选自表10。在一些实施方案中,生长因子是鸡生长因子、鸭生长因子、牛生长因子、绵羊生长因子、鱼生长因子、猪生长因子、哺乳动物生长因子、禽生长因子、爬行动物生长因子、两栖动物生长因子、蛛形纲动物生长因子或硬骨鱼生长因子。
在一些实施方案中,培养基包含粘附蛋白。在一些实施方案中,粘附蛋白任选地选自表14。
在一些实施方案中,多种成分包含一种或多种氨基酸,其任选地在表1中提供的浓度范围内。
在一些实施方案中,多种成分包含一种或多种碳水化合物,其任选地在表2中提供的浓度范围内。
在一些实施方案中,多种成分包含一种或多种维生素,其任选地在表3中提供的浓度范围内。
在一些实施方案中,多种成分包含一种或多种无机盐,其任选地在表4中提供的浓度范围内。
在一些实施方案中,多种成分包含一种或多种微量金属,其任选地在表5中提供的浓度范围内。
在一些实施方案中,多种成分包含一种或多种脂质,其任选地在表6中提供的浓度范围内。
在一些实施方案中,多种成分包含一种或多种食用油,其任选地在表6中提供的浓度范围内。
在一些实施方案中,多种成分包含一种或多种生长因子,其任选地在表12中提供的浓度范围内。
在一些实施方案中,多种成分包含一种或多种补充成分,其任选地在表8中提供的浓度范围内。
在一些实施方案中,多种成分包含一种或多种TCA循环中间体,其任选地在表7中提供的浓度范围内。
在一些实施方案中,多种成分包含一种或多种糖酵解中间体、铁载体、麦芽酚铁、葡萄糖酸亚铁、剪切保护剂、聚乙二醇、甲基纤维素和水解产物。在一些实施方案中,将培养基与水混合以形成溶液。
在一些实施方案中,培养基包含甲基纤维素。在一些实施方案中,培养基包含氰钴胺,其任选地在1.00E+05g/L至0.0026g/L的浓度范围内。在一些实施方案中,培养基包含西甲硅油。在一些实施方案中,培养基包含柠檬酸铁铵,其任选地在0.01g/L至0.5g/L的浓度范围内。在一些实施方案中,培养基包含食品级植物油。
在另一方面,本文提供了一种组合物,其包含上述任何一种或多种培养基。在一些实施方案中,组合物还包含培养中的非人类细胞。在一些实施方案中,非人类细胞来自家禽、海鲜、野味或家畜。在一些实施方案中,多种成分包含一种或多种氨基酸、镁盐、钠盐、铜盐、锌盐、铁盐和维生素,其任选地在表9中提供的浓度范围内。
在另一个方面,本文提供了工程化生长因子。在一些实施方案中,本文提供了通用FGF-2,其包含SEQ ID NO:3所示的氨基酸序列。在一些实施方案中,本文提供了由SEQ IDNO:4所示核酸序列编码的通用FGF-2。在一些实施方案中,本文提供了通用PDGF-BB,其包含SEQ ID NO:5所示的氨基酸序列。在一些实施方案中,本文提供了通用IGF-1,其包含SEQ IDNO:6所示的氨基酸序列。在一些实施方案中,本文提供了通用的VEGF-A,其包含SEQ ID NO:7中的氨基酸序列。在一些实施方案中,本文提供了原鸡属LR3-IGF1,其包含SEQ ID NO:1所示的氨基酸序列。
在另一方面,本文提供了一种用于产生免屠宰肉的营养培养基的配制方法,其包括:(a)提供多种成分;(b)一个或多个:(i)将一种或多种目前未被批准用于食品的成分替换为一种或多种被批准用于食品的成分;(ii)去除目前未被批准用于食品的一种或多种成分;和(iii)以等于或低于ADI值配制一种或多种目前未被批准用于食品的成分。在一些实施方案中,培养基含有不超过10%、9%、8%、7%、6%、5%、4%、3%、2%、1%、0.5%、0.1%、0.05%或不超过0.01%%的动物源性血清。在一些实施方案中,培养基基本上不含动物源性血清或不含动物源性血清。在一些实施方案中,培养基含有不超过10%、9%、8%、7%、6%、5%、4%、3%、2%、1%、0.5%、0.1%、0.05%或不超过0.01%%的动物源性组分。在一些实施方案中,培养基基本上不含动物源性组分或动物源性组分。在一些实施方案中,培养基是在化学上定义的。
在用于配制产生免屠宰肉的营养培养基的方法的一些实施方案中,将泊洛沙姆替换为甲基纤维素。
在用于配制产生免屠宰肉的营养培养基的方法的一些实施方案中,将氯化钴替换为氰钴胺。
在用于配制产生免屠宰肉的营养培养基的方法的一些实施方案中,将目前未被批准用于食品的消泡剂替换为西甲硅油。
在用于配制产生免屠宰肉的营养培养基的方法的一些实施方案中,将钼酸铵、钼酸钠、偏钒酸铵、偏钒酸钠、氯化铷和六水合氯化锶中的一种或多种替换为柠檬酸铁铵。
在一些实施方案中,用于配制产生免屠宰肉的营养培养基的方法还包括添加本公开中描述的任何一种或多种生长因子。在一些实施方案中,用于配制产生免屠宰肉的营养培养基的方法还包括添加通用FGF-2、通用PDGF-BB、通用IGF-1、通用VEGF-A和/或原鸡属LR3-IGF1中的一种或多种。在一些实施方案中,用于配制产生免屠宰肉的营养培养基的方法还包括添加一种或多种SEQ ID NO.1-7或与其具有至少约50%、至少约60%、至少约70%、至少约80%、至少约90%、至少约95%、至少约96%、至少约96%、至少约97%、至少约98%、至少约99%的序列同一性的序列。
附图说明
图1A显示了在包含公认安全(GRAS)成分的培养基中与在包含非GRAS成分的培养基中培养的贴壁原鸡属细胞的生长的比较。(SF=无血清;ACF=无动物组分)。
图1B显示了在包含GRAS成分的培养基中与在包含非GRAS成分的培养基中培养的悬浮原鸡属细胞的生长的比较。
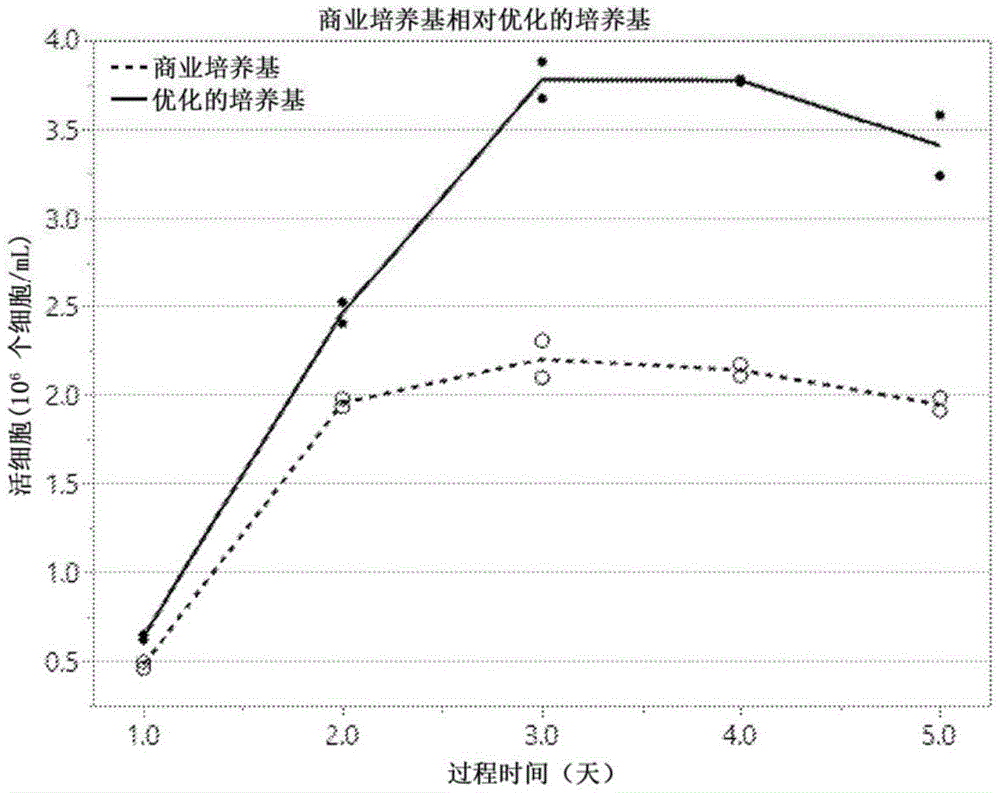
图2显示了在商业培养基中与在优化培养基中培养的悬浮原鸡属细胞的生长的比较。
图3显示了用顺式原鸡属重组FGF-2与用商业人重组FGF-2培养的原鸡属细胞的反应的比较。
图4显示了在用包含顺式原鸡属转铁蛋白的培养基与用包含人重组转铁蛋白的培养基培养的贴壁培养物中原鸡属细胞的生长的比较。
图5显示了多种剪切保护剂的细胞活力随时间的变化的比较。
图6显示了在不存在和以不同浓度存在柠檬酸铁铵的情况下细胞活力随时间的变化。
具体实施方案
本文提供了用于制备和使用细胞培养基的组合物和方法,所述细胞培养基可用于培养细胞肉(可互换地称为本公开的免屠宰肉)。
在详细描述特定实施方案之前,应理解本公开不限于本文描述的特定实施方案,其可以变化。还应理解,本文使用的术语仅出于描述特定示例说明性实施方案的目的,并且不旨在限制,除非另有定义。本说明书中使用的术语通常在本领域、在本公开的上下文中以及在使用每个术语的特定上下文中具有它们的普通含义。某些术语在下文或说明书的其他地方讨论,以在描述本公开的组合物和方法以及如何制造和使用它们时为从业者提供额外的指导。从使用术语的特定上下文中,该术语的任何使用的范围和含义会是显而易见的。因此,本文所阐述的定义旨在为确定本公开的特定实施方案提供示例说明性指导,而不限于特定组合物或生物系统。
标准技术可用于重组DNA、组织培养和转化(例如,电穿孔、脂质转染)。酶促反应和纯化技术可以根据制造商的说明书或如本领域中通常完成的或如本文所述的那样进行。这些和相关的技术和程序通常可以根据本领域公知的常规方法进行,并且如在整个本说明书中引用和讨论的多种一般的和更具体的参考文献中所述。除非提供具体定义,否则本文所述的与分子生物学、分析化学、合成有机化学以及药物和制药化学所使用的相关的命名法和实验室程序和技术是本领域公知的和常用的。标准技术可用于重组技术、分子生物学、微生物学、化学合成、化学分析、药物制备、配制和递送。
如在本公开和所附权利要求中使用的,单数形式“一个”、“一种”和“所述”包括复数引用,除非内容另有明确规定。
在整个本公开和所附权利要求中,除非上下文另有要求,否则词语“包含(comprise)”或诸如“包含(comprises)”或“包含(comprising)”的变形会被理解为暗示包含所陈述的元素或元素组,但不排除任何其他元素或元素组。
如在本公开中所使用的,术语“约”通常应表示测量量的可接受的误差程度。示例性误差程度在值或值范围的20%以内、10%以内和5%以内。
用于获取传统肉类的方式的“屠宰”一词涵盖了传统上用于杀死动物的所有方法,目的是直接收获其肉用于饮食消费。
用于本公开的细胞肉制品的术语“免屠宰”是指生成肉的过程,从培养中的细胞开始,并且该方法不涉及屠宰动物,以直接从该动物身上获得肉用于饮食消费。应当理解,在一些实施方案中,用于细胞培养方法的起始细胞已经可在动物屠宰或活检后获得——尽管用于培养的起始细胞已经可以这种方式获得,细胞培养、收获和可能的后续配制所产生的肉仍然被认为是以免屠宰方式获得的肉。应注意,作为一般事项,如本文所用,免屠宰的细胞肉制品的收获可涉及使用水的缓冲溶液(或其他水溶液)以从肉生长的地方(例如生物反应器的表面,或在包含悬浮培养的细胞的容器中)去除肉,然后可以将肉收集在收集装置(例如网、筛子、滤锅)中。在一些实施方案中,肉可以通过物理方法(例如刮)、酶促方法和/或化学方法收获。在一些实施方案中,肉可以通过任何上述方法收获,随后用缓冲溶液(或其他水溶液)冲洗。
短语“细胞肉”、“免屠宰肉”、“免屠宰细胞肉”、“体外产生的肉”、“体外细胞肉”、“培养肉”、“免屠宰培养肉”、“体外产生的培养肉”、“体外肉”、“体外培养肉”以及其他类似的此类短语在本文中可互换使用,是指从培养中的细胞开始体外生成的肉,以及不涉及屠宰动物以直接从该动物获得肉用于饮食消费的方法。
短语“细胞培养液”、“营养培养基”、“细胞培养基”、“培养基”、“肉汤”、“饲料”和其他类似的短语在本文中可互换使用。如本文所用,“营养培养基”是在从培养中的细胞开始产生细胞肉的上下文中。
免屠宰细胞肉
本公开的免屠宰细胞肉制品通过在培养物中体外培养天然存在的、基因工程的或修饰的动物细胞来产生。
本文提供的方法适用于培养中的任何后生动物细胞。一般而言,细胞来自其组织适合饮食消费的任何后生动物物种。在一些实施方案中,细胞可以展示分化成成熟组织的能力,例如骨骼肌组织、其他肌肉组织或任何细胞、细胞生物质,和/或可以作为肉食用的组织。本公开的方法中使用的细胞可以是原代细胞或细胞系。
在一些实施方案中,细胞衍生自旨在用于人类或非人类饮食消费的任何非人类动物物种(例如鸟类、绵羊、山羊、猪、牛、鱼来源的细胞)(例如家畜、家禽、鸟类、野味或水生物种的细胞)。
在一些实施方案中,细胞来自家畜,例如家牛、猪、绵羊、山羊、骆驼、水牛、兔子等。在一些实施方案中,细胞来自家禽,例如家鸡、火鸡、鸭、鹅、鸽子等。在一些实施方案中,细胞来自野鹿、鹑鸡类的家禽(gallinaceous fowl)、水禽、野兔等野味物种。在一些实施方案中,细胞来自商业上从野生渔业或水产养殖作业或为娱乐而收获的水生物种或半水生物种,包括某些鱼、甲壳类动物、软体动物、头足类动物、鲸目动物、鳄鱼、乌龟、蛙等。
在一些实施方案中,细胞来自外来的、保守的或灭绝的动物物种。在一些实施方案中,细胞来自红原鸡(Gallus gallus)、家鸡(Gallus domesticus)、家牛(Bos taurus)、欧亚野猪(Sous scrofa)、火鸡(Meleagris gallopavo)、绿头鸭(Anas platyrynchos)、大西洋鲑鱼(Salmo salar)、大西洋蓝鳍金枪鱼(Thunnus thynnus)、绵羊(Ovis aries)、西鹌鹑(Coturnix coturnix)、家山羊(Capra aegagrus hircus)或缅因龙虾(Homarusamericanus)。因此,本公开的示例性细胞肉制品包括禽肉制品、鸡肉制品、鸭肉制品和牛肉制品。
在一些实施方案中,细胞是原代干细胞、自我更新干细胞、胚胎干细胞、多能干细胞、诱导多能干细胞或转分化多能干细胞。
在一些实施方案中,细胞可通过基因开关进行修饰,以诱导细胞快速有效地转化为骨骼肌组织、结缔组织、脂肪组织和/或用于培养肉产生的任何其他成熟组织。
在一些实施方案中,细胞是注定要变成肌肉或肌肉样细胞的肌原细胞。在一些实施方案中,肌原细胞是天然的肌原细胞,例如成肌细胞。天然成肌细胞包括但不限于成肌细胞、肌细胞、卫星细胞、侧群细胞、肌肉衍生干细胞、间充质干细胞、成肌周细胞或中成血管细胞(mesoangioblasts)。
在一些实施方案中,细胞属于骨骼肌谱系。骨骼肌谱系的细胞包括成肌细胞、肌细胞和骨骼肌祖细胞,也称为成肌祖细胞,包括卫星细胞、侧群细胞、肌肉来源的干细胞、间充质干细胞、成肌周细胞和中成血管细胞。
在其他实施方案中,细胞不是天然的肌原细胞(例如,在培养基础设施中培养成肌原细胞的非肌原细胞,如成纤维细胞或非肌原干细胞)。
在一些实施方案中,细胞生物质的细胞是体细胞。在一些实施方案中,细胞生物质的细胞不是体细胞。
在一些实施方案中,细胞包含本文所述的细胞群的混合物,例如,共培养中的纤维原细胞和肌原细胞的混合物,例如共培养中的成纤维细胞和成肌细胞的混合物。在一些实施方案中,用于产生细胞肉的细胞是悬浮共培养物中的成纤维细胞和成肌细胞的混合物。在一些实施方案中,用于产生细胞肉的细胞是贴壁共培养物中的成纤维细胞和成肌细胞的混合物。在一些实施方案中,共培养的细胞包含额外的细胞类型,例如脂肪细胞、内皮细胞,并且通常来自中胚层谱系的细胞。
在一些共培养实施方案中,细胞处于悬浮共培养物中,在一些实施方案中,细胞处于贴壁共培养物中,并且在一些实施方案中,培养过程利用这两种技术。本文提供的共培养物包含至少成纤维细胞和成肌细胞的混合物。在一些实施方案中,成纤维细胞与成肌细胞的比例(指定为F和M)在约5F:95M至约95F:5M的范围内。在示例性实施方案中,成纤维细胞与成肌细胞的比例为约5F:95M、10F:90M、15F:85M、20F:80M、25F:75M、30F:70M、35F:65M、40F:60M、45F:55M、50F:50M、55F:45M、60F:40M、65F:35M、70F:30M、75F:25M、80F:20M、85F:15M、90F:10M,甚至约95F:5M。
在一些实施方案中,细胞是非肌原性的,并且这种非肌原细胞可以被编程为肌原性的,例如细胞可以包含被修饰以表达一种或多种肌原转录因子的成纤维细胞。在示例性实施方案中,肌原转录因子包括MYOD1、MYOG、MYF5、MYF6、PAX3、PAX7、旁系同源物、直系同源物和它们的遗传变体。在一些实施方案中,细胞被修饰以表达一种或多种肌原性转录因子,如PCT公开WO/2015/066377中所述,该申请通过引用以其整体并入本文。
在一些实施方案中,细胞被遗传修饰以抑制途径,例如HIPPO信号通路。抑制HIPPO信号通路的示例性方法如PCT申请号PCT/US2018/031276中所述,该申请通过引用以其整体并入本文。
在一些实施方案中,细胞被修饰以表达端粒酶逆转录酶(TERT)和/或抑制细胞周期蛋白依赖性激酶抑制剂(CKI)。在一些实施方案中,细胞被修饰以表达TERT和/或抑制细胞周期蛋白依赖性激酶抑制剂,如PCT公开WO2017/124100中所述,该申请通过引用以其整体并入本文。
在一些实施方案中,细胞被修饰以表达谷氨酰胺合成酶(GS)、胰岛素样生长因子(IGF)和/或白蛋白。示例性修饰细胞以表达GS、IGF和/或白蛋白的方法描述于PCT申请号PCT/US2018/042187中,该申请通过引用以其整体并入本文。
在一些实施方案中,细胞肉制品具有多种特征。细胞肉的示例性特征描述于美国申请号17/033,635和PCT申请号PCT/US2021/016681,该申请通过引用以其整体并入本文。
在一些实施方案中,细胞被遗传编辑、修饰或适应生长而不需要特定成分,所述特定成分包括特定氨基酸、碳水化合物、维生素、无机盐、微量金属、TCA循环中间体、脂质、脂肪酸、补充化合物、生长因子、粘附蛋白和重组蛋白。
在一些实施方案中,细胞可包含本文所述修饰的任何组合。
使用本文提供的细胞培养基配方生成的本公开的细胞肉适合人类和非人类食用。在一些实施方案中,细胞肉适合动物食用,例如家养动物。因此,本文提供的细胞培养基配方支持“宠物食品”,例如狗粮、猫粮等的生长。
细胞培养基配方
本文提供了用于培养和产生免屠宰肉的营养培养基配方和相关组合物和方法。
用于产生用于消费的肉的安全是本公开的细胞培养基的众多优点之一。在一些实施方案中,细胞培养基本身是可食用的,例如如果摄入不会造成任何有害影响。本文提供的培养基配方通常包含各自单独或组合可食用的(例如,食用安全、食品级、食品安全、食品质量、食品可接受、食品相容、食品类别、食品、食品使用、可吃的、可食用的)的成分。本公开的培养基配方的产生是通过将培养基配方设计成包括本质上安全的成分和/或定制要在安全水平下提供的成分的浓度来实现的,如以下讨论的任何一种或多种标准所确定的。
在一些实施方案中,用于产生免屠宰肉的可食用营养培养基包含多种成分,其中每种成分被批准用于食品和/或等于或低于其ADI值。在一些实施方案中,中间形式的细胞培养基可以是可食用的或不可食用的。在一些实施方案中,细胞培养基包含多种成分,其中一种或多种成分被批准用于食品中。在一些实施方案中,细胞培养基包含多种成分,其中每种成分都被批准用于食品中。如在本公开中使用的,“被批准用于食品中”的成分是指被广泛接受的标准,例如国家或国际公认的标准批准用于食品中的成分。这些标准包括但不限于监管机构,例如美国食品药品监督管理局(FDA)、美国农业部(USDA)、世界卫生组织(WHO)、联合国食品和农业组织(FAO)和欧洲食品安全局(EFSA)制定的标准。
因此,在一些实施方案中,本公开的细胞培养基可包含批准用于食品中的成分,这些成分被FDA认可为公认安全(GRAS)。在一些实施方案中,细胞培养基包含GRAS认证成分、非GRAS认证成分或其混合物的成分。在某些实施方案中,细胞培养基仅包含GRAS认证成分。随着FDA更新GRAS物质清单,可修改可用于细胞培养基配方的GRAS认证成分。在一些实施方案中,细胞培养基包含具有当前未知的GRAS状态的成分。预期本文提供的培养基可包含当前具有未知GRAS状态或非GRAS状态但未来可被GRAS认证的成分。
在一些实施方案中,本公开的细胞培养基可以包含如FDA认可的被批准用于食品中的成分。
在一些实施方案中,本公开的细胞培养基可以包含如USDA认可的被批准用于食品中的成分。
在一些实施方案中,本公开的细胞培养基可以包含如FAO认可的被批准用于食品中的成分。
在一些实施方案中,本公开的细胞培养基可以包含如WHO认可的被批准用于食品中的成分。
在一些实施方案中,本公开的细胞培养基可以包含如FAO和WHO在食品法典中认可的被批准用于食品中的成分。
在一些实施方案中,本公开的细胞培养基可以包含如EFSA认可的被批准用于食品中的成分。
在一些实施方案中,本公开的细胞培养基可以包含如食品化学品法典(FCC)认可的被批准用于食品中的成分。
在一些实施方案中,细胞培养基包含配制为或低于供人和/或家养动物食用的安全浓度的成分。在一些实施方案中,如果肉制品中化合物的理论最大量等于或低于平均每日摄入量(ADI)水平,则培养基中的成分可被认为处于人类和/或家养动物食用的安全浓度。平均每日摄入量(ADI)通常是由于亚慢性或急性暴露的适当动物物种的实验得出的无明显不良反应限值(NOAEL)低100倍的安全系数来确定的。本领域的熟练技术人员会了解如何计算NOAEL值。例如,FDA将NOAEL定义为与对照组相比不会产生显著增加不良反应的最高剂量水平。ADI是在适当敏感的物种(通常是啮齿动物)中测定的,报告为mg物质/kg动物体重/24小时周期。计算最终制品中每种培养基化合物的最大理论浓度是通过假设将培养基中的化合物100%掺入制品中来完成的。
在一些实施方案中,细胞培养基包含多种成分,其中一种或多种成分等于或低于其平均每日摄入量(ADI)值。在一些实施方案中,细胞培养基包含多种成分,其中每种成分等于或低于其ADI值。在一些实施方案中,细胞培养基包含多种成分,其中每种成分被批准用于食品和/或等于或低于其ADI值。
在一些实施方案中,细胞培养基包含目前未被批准用于食品的成分和/或目前对于用于食品具有未知状态的成分。在一些实施方案中,目前未被批准用于食品的成分被配制为等于或低于其ADI值。
在一些实施方案中,细胞培养基包含至少一种被批准用于食品的成分和至少一种目前未被批准用于食品的成分的组合。在一些实施方案中,细胞培养基包含至少一种被批准用于食品的成分和至少一种目前未被批准用于食品的成分,其中每种成分被配制为等于或低于其ADI值。
在一些实施方案中,细胞培养基包含被批准以等于或高于其ADI值的浓度配制用于食品的成分。在一些实施方案中,细胞培养基包含目前未被批准以等于或高于其ADI值的浓度配制用于食品的成分。在一些实施方案中,细胞培养基包含至少一种被批准用于食品的成分和至少一种目前未被批准用于食品的成分的组合,其中每种成分被配制为等于或高于其ADI值。
如图1A-B所示和下文实施例1-2详述,当与含有潜在有害的非GRAS成分的细胞培养基相比,本公开的仅包含GRAS成分并缺少动物源性组分的示例性安全细胞培养基显示了贴壁和悬浮细胞的较高生长速度。下文实施例3中详述的图2比较了悬浮细胞在仅包含GRAS成分的本公开的示例性优化无血清培养基与商业培养基中的生长。优化的培养基在细胞活力方面表现出增强的性能。
本公开的细胞培养基的另一个优点是在细胞培养基中不存在动物源性血清和其他动物源性组分,这些成分会带来污染、批次间差异、微生物污染、增加成本和所需的额外的质量控制措施。本文提供的安全培养基配方可以进行优化,以支持以不同培养形式培养多种细胞,在缺乏通常依赖于动物源性血清的营养物质的情况下,这是一项具有挑战性的任务。因此,本文提供的细胞培养基允许在降低动物源性血清浓度的条件下,或甚至在完全不存在动物源性血清的条件下有效培养细胞。在一些实施方案中,细胞培养基包含不超过10%、9%、8%、7%、6%、5%、4%、3%、2%、1%、0.5%、0.1%、0.05%或不超过0.01%动物源性血清。在一些实施方案中,细胞培养基基本上不含动物源性血清。基本上不含是指以等于或低于检测水平存在的动物源性血清的量。熟练的技术人员会知道如何确定检测水平。例如,检测水平可以通过基于质谱的技术、基于PCR的技术、基于抗体的技术、基于ELISA的技术、基于HPLC的技术、和其他公知的化学或生物检测方法。在一些实施方案中,细胞培养基不含动物源性血清。
在一些实施方案中,细胞培养基包含非动物源性血清。非动物源性血清的实例包括合成血清、血清替代品、血清替代物、化学成分确定的血清、KnockOut
同样,本文提供的细胞培养基包含不超过10%、9%、8%、7%、6%、5%、4%、3%、2%、1%、0.5%、0.1%、0.05%或不超过0.01%动物源性组分(包括但不限于动物源性血清)。在一些实施方案中,细胞培养基基本上不含动物源性组分。基本上不含是指以等于或低于检测水平存在的动物源性组分的量。熟练的技术人员会知道如何确定检测水平。例如,检测水平可以通过基于质谱的技术、基于PCR的技术、基于抗体的技术、基于ELISA的技术、基于HPLC的技术和其他公知的化学或生物检测方法来确定。在一些实施方案中,细胞培养基不含动物源性组分。
本公开的细胞培养基是可定制的和模块化的。培养基配方的成分可以根据产生的特定类型的细胞肉进行定制,以获得最佳效果。例如,为了培养鸡细胞,培养基可以包含蛋白质,例如生长因子,它们也来源于鸡。类似地,用于培养牛细胞的培养基可以仅包含牛来源的蛋白质。在一些实施方案中,用于培养鸡细胞的培养基可以包含牛来源的蛋白质,例如生长因子。在一些实施方案中,培养基可以包含用于培养任何类型的细胞肉的通用蛋白质,例如通用生长因子。
通过本公开的细胞培养基产生的细胞肉可以与通过屠宰获得的传统肉相当或可比较的。本公开的细胞培养基允许产生在所有方面,如风味、厚度、硬度、组成等都与其传统获得的对应物相当的细胞肉。例如,核黄素,维生素和辅助因子,当添加到细胞培养基中时,会增加培养中的细胞中的脂肪酸合成。因此,可以调节细胞培养基中核黄素的水平,以使最终细胞肉的脂肪酸含量与传统肉的相匹配,从而使风味与相当的传统肉相匹配。在一些实施方案中,细胞培养基包含核黄素。在一些实施方案中,细胞培养基包含半乳糖、尿苷和锰(GUM)。
本公开的细胞培养基能够调节由其产生的细胞肉的特征标准(standard ofidentity,SOI)性能因子。培养基组分的优化可用于调整性能因子,例如维持细胞活力、最大化生物量/产量、调整风味/味道和/或实现细胞肉的所需组织特性(厚度、硬度等)。在一些实施方案中,性能因子是细胞活力。在一些实施方案中,性能因子是细胞生长。在一些实施方案中,性能因子是最终细胞肉制品的生物量或产量。在一些实施方案中,性能因子是细胞肉的味道或风味。在一些实施方案中,性能因子是例如在组织硬度、厚度等方面测量的细胞肉的质量。
在一些实施方案中,与通过常规培养基产生的细胞肉相比,由本公开的细胞培养基产生的细胞肉的性能因子得到改善。在一些实施方案中,与由含有非GRAS成分的培养基产生的细胞肉相比,由本公开的细胞培养基产生的细胞肉的性能因子得到改善。在一些实施方案中,与由不存在任何未被批准用于食品和/或高于其ADI值的任何成分的常规培养基产生的细胞肉相比,由本公开的细胞培养基产生的细胞肉的性能因子得到改善。
在一些实施方案中,与在传统培养基中培养相比,在本公开的细胞培养基中培养细胞将细胞活力提高至少50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或99%。在一些实施方案中,与在含有非GRAS成分的培养基中培养相比,在本公开的细胞培养基中培养细胞将细胞活力提高至少50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或99%。
在一些实施方案中,与在传统培养基中培养相比,在本公开的细胞培养基中培养细胞将细胞增长率提高至少50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或99%。在一些实施方案中,与在含有非GRAS成分的培养基中培养相比,在本公开的细胞培养基中培养细胞将细胞增长率提高至少50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或99%。
在一些实施方案中,与传统培养基相比,在本公开的细胞培养基中产生细胞肉将最终生物量/产率提高至少50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或99%。在一些实施方案中,与含有非GRAS成分的培养基相比,在本公开的细胞培养基中产生细胞肉将最终生物量/产率提高至少50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或99%。
本公开的细胞培养基的又一个优点是它们以任何所希望的规模以低成本快速应用和配制。例如,它们适用于分批、补料分批、恒化器、灌注和/或强化生物反应器组织培养器过程。
在一些实施方案中,细胞培养基是化学确定的,即其中所有成分及其浓度已知的培养基。在一些实施方案中,可能需要使用化学确定的、不含动物成分的培养基,以最大限度地减少任何潜在的污染物并减少批次间的差异,同时保持高细胞生长、培养肉产生,并将这些细胞肉的相似性与传统肉制品的特征标准相匹配。例如,许多传统的细胞培养基使用动物源性油,例如鱼肝油作为脂质来源,因为鱼肝油中含有许多甲酯脂肪酸。然而,鱼肝油不允许控制细胞肉的脂肪酸组成,并且可给出错误的脂肪酸谱,例如鸡具有鱼谱。在一些实施方案中,细胞培养基不含任何不确定的成分,例如水解物、不确定的血清替代物和动物油(例如鱼肝油)。在一些实施方案中,本文提供了植物源性食用油和/或合成来源的脂肪脂质以提供理想的比例来实现所需的脂肪酸谱。在一些实施方案中,细胞培养基不含染料,例如pH指示剂染料(例如酚红)。酚红通常作为比色pH指示剂存在于经典细胞培养基(如Ham'sF12和DMEM)中。它与一些非甾体雌激素具有结构相似处。雌激素被认为是激素,不被批准用于食品。
在一些实施方案中,细胞培养基可以包含不确定的非动物源性组分,例如植物水解物。
氨基酸
细胞培养基包含一种或多种氨基酸。氨基酸可以是L立体化学、D立体化学或L和D同源异构体的组合,例如外消旋体形式。在示例性实施方案中,氨基酸是L立体化学。在一些实施方案中,氨基酸包括二十种天然存在的规范氨基酸。
本公开的培养基中包含的氨基酸的实例包括丙氨酸、精氨酸、天冬氨酸、天冬酰胺、半胱氨酸、胱氨酸、谷氨酸、谷氨酰胺、甘氨酸、组氨酸、脯氨酸、羟脯氨酸、异亮氨酸、亮氨酸、赖氨酸、甲硫氨酸、苯丙氨酸、丝氨酸、苏氨酸、色氨酸、酪氨酸、缬氨酸和鸟氨酸。
在一些实施方案中,细胞培养基包含一种或多种必需氨基酸、非必需氨基酸、蛋白氨基酸、非蛋白氨基酸和/或支链氨基酸。
在一些实施方案中,细胞培养基包含一种或多种非天然氨基酸、氨基酸类似物、氨基酸衍生物、β-氨基酸、γ氨基酸、氨基酸模拟物和/或寡肽。在一些实施方案中,细胞培养基包含牛磺酸、肌肽、α-氨基丁酸、β-氨基丁酸和γ-氨基丁酸。
在一些实施方案中,细胞培养基包含一种或多种浓度范围如下表1所示的氨基酸。对于本公开的该表和其他表,范围包括列举的最低和最高浓度。
表1:示例性氨基酸和相关化合物
/>
碳水化合物
在一些实施方案中,细胞培养基包含一种或多种碳水化合物。碳水化合物可以包括单糖、二糖、寡糖、多糖和/或多元醇。碳水化合物的实例包括葡萄糖、半乳糖、甘露糖、麦芽糖、岩藻糖、蔗糖、果糖、阿洛糖、阿卓糖、古洛糖、艾杜糖、塔罗糖、阿洛酮糖、山梨糖、塔格糖、乳糖、核糖和肌醇。
在一些实施方案中,细胞培养基包含碳水化合物衍生物和/或合成碳水化合物。实例包括氨基糖、还原糖、氧化糖、人造糖、脱氧糖、葡糖酸、葡糖醛酸、葡糖二酸、甘油、葡糖胺、半乳糖胺、甘露糖胺、岩藻糖和脱氧核糖。
在一些实施方案中,细胞培养基包含一种或多种浓度范围如下表2中所示的碳水化合物。
表2:示例性碳水化合物和相关化合物
维生素
在一些实施方案中,细胞培养基包含一种或多种维生素。维生素的实例包括维生素C、维生素B1、维生素B2、维生素B7、维生素D、维生素B9、维生素B3、维生素B5、维生素B6、维生素B12、维生素E。
在一些实施方案中,细胞培养基包含维生素前体、中间体和代谢物。实例包括烟酰胺、甲萘醌、氯化胆碱和对氨基苯甲酸。
在一些实施方案中,细胞培养基包含如下表3中所示浓度范围的维生素。
表3:示例性维生素和相关化合物
无机盐
在一些实施方案中,细胞培养基包含一种或多种无机盐。无机盐的实例包括氯化钙、氯化钠、磷酸钠、氯化镁、硫酸镁和氯化钾。
在一些实施方案中,细胞培养基包含下表4所示浓度范围如的无机盐。
表4:示例性无机盐和相关化合物
微量金属
在一些实施方案中,细胞培养基包含一种或多种微量金属。
微量金属的实例包括镉、锶、铜、硒、硅、铜、铁、镍和锡。微量金属可能以不同的氧化态、盐、溶剂化物和水合物存在。
在一些实施方案中,细胞培养基包含如下表5所示浓度范围的微量金属。
表5:示例性微量金属和相关化合物
脂质
在一些实施方案中,细胞培养基包含一种或多种脂质。脂质的实例包括脂肪酸、脂肪、油、甘油酯、非甘油酯脂质、鞘脂、糖脂、磷脂、硫脂、类固醇、复合脂质、衍生脂质和脂质混合物。实例包括油酸、亚油酸、花生四烯酸、亚麻酸、肉豆蔻酸、棕榈酸、棕榈油酸、硬脂酸和卵磷脂。在一些实施方案中,细胞培养基包含食用油和食品级植物油。油的实例包括亚麻籽油、菜籽油和海藻油。
在一些实施方案中,细胞培养基包含如下表6所示浓度范围的脂质。
表6:示例性脂质、食用油和相关化合物
TCA循环中间体
在一些实施方案中,细胞培养基包含一种或多种TCA循环中间体。TCA循环中间体的实例包括丙酮酸、琥珀酸、柠檬酸、异柠檬酸、α-酮戊二酸、富马酸、苹果酸、草酰乙酸、乙酰胆碱、乙酰辅酶A和琥珀酰辅酶A。
在一些实施方案中,细胞培养基包含如下表7所示浓度范围的TCA循环中间体。
表7:示例性TCA循环中间体和相关化合物
补充成分
在一些实施方案中,细胞培养基包含一种或多种补充成分。补充化合物的实例包括聚山梨酯
在一些实施方案中,细胞培养基包含下表8中所示浓度范围的补充化合物。
表8:示例性补充成分
在一些实施方案中,细胞培养基包含一组核心成分,这取决于所需的细胞培养物的性质。在示例性实施方案中,细胞培养基的核心成分包括L-精氨酸、L-半胱氨酸、L-胱氨酸、L-谷氨酰胺、L-组氨酸、L-异亮氨酸、L-亮氨酸、L-赖氨酸、L-甲硫氨酸、L-苯丙氨酸、L-脯氨酸、L-色氨酸、L-酪氨酸、L-缬氨酸、D-葡萄糖、烟酸、核黄素、麦角骨化醇、抗坏血酸、铜盐、钠盐、铁盐、镁盐和锌盐中的至少一种、至少两种、至少三种、至少四种、至少五种、至少六种、至少七种、至少八种、至少九种、至少十种、至少十一种、至少十二种、至少十三种、至少十四种、至少十五种、至少十六种、至少十七种、至少十八种、至少十九种、至少二十种、至少二十一种、至少二十二种、至少二十三种、至少二十四种或更多种。
在示例性实施方案中,细胞培养基的核心成分包括L-精氨酸、L-半胱氨酸、L-胱氨酸、L-谷氨酰胺、L-组氨酸、L-异亮氨酸、L-亮氨酸、L-赖氨酸、L-甲硫氨酸、L-苯丙氨酸、L-脯氨酸、L-色氨酸、L-酪氨酸、L-缬氨酸、D-葡萄糖、烟酸、核黄素、麦角骨化醇、抗坏血酸、硫酸铜、亚硒酸钠、柠檬酸铁铵、氯化镁、硫酸镁和硫酸锌中的至少一种、至少两种、至少三种、至少四种、至少五种、至少六种、至少七种、至少八种、至少九种、至少十种、至少十一种、至少十二种、至少十三种、至少十四种、至少十五种、至少十六种、至少十七种、至少十八种、至少十九种、至少二十种、至少二十一种、至少二十二种、至少二十三种、至少二十四种或更多种。
在其他实施方案中,细胞培养基包含L-精氨酸、L-半胱氨酸、L-胱氨酸、L-谷氨酰胺、L-组氨酸、L-异亮氨酸、L-亮氨酸、L-赖氨酸、L-甲硫氨酸、L-苯丙氨酸、L-脯氨酸、L-色氨酸、L-酪氨酸、L-缬氨酸、D-葡萄糖、烟酸、核黄素、麦角骨化醇、抗坏血酸、硫酸铜、亚硒酸钠、柠檬酸铁铵、氯化镁、硫酸镁和硫酸锌。
在一些实施方案中,细胞培养基至少包含下表9中所示的成分。
表9:示例性成分
可以使用本公开中公开的任何细胞培养基成分的盐、溶剂化物、水合物、多晶型物、无水物、酯、同源异构体、代谢物、前体、衍生物和前药。
生长因子
在一些实施方案中,细胞培养基包含一种或多种生长因子。生长因子可以通过本领域已知的多种方法产生。生长因子可以包含天然存在或非天然存在的序列。例如,包含非天然存在的序列的生长因子可以是天然存在的序列的变体。或者,包含非天然存在的序列的生长因子可不类似于具有很多序列相似性但保留相似功能的天然存在的对应物。生长因子可以通过本领域已知的多种方法产生,例如生长因子可以重组产生、分离和纯化或化学合成。本公开的生长因子涵盖同源物、直向同源物和旁系同源物。可包含在本文提供的培养基中的生长因子的实例包括成纤维细胞生长因子、成纤维细胞生长因子1(FGF-1)、成纤维细胞生长因子2(FGF-2)、血小板衍生生长因子、血小板衍生生长因子亚基A(PDGF-A)、血小板衍生生长因子亚基B(PDGF-B)、血小板衍生生长因子-AA (PDGF-AA)、血小板衍生生长因子-BB(PDGF-BB)、胰岛素样生长因子1(IGF-1)、长精氨酸3-IGF-1(LR3-IGF1)、胰岛素、转铁蛋白、血清转铁蛋白、卵转铁蛋白、结缔组织生长因子(CTGF)、表皮生长因子(EGF)、转化生长因子(TGF)、转化生长因子β(TGF-β)、骨形态发生蛋白(BMP)、肝细胞生长因子(HGF)、WNT蛋白、WNT 1、WNT 11、WNT 11B、成肌调节因子、成肌因子6、白介素、IL2、IL2同源异构体XI、IL6、IL6前体、白血病抑制因子(LIF)、LIF同源异构体XI IL3、血管内皮生长因子(VEGF)、变体、热稳定的变体、前体、同源异构体、同系物、旁系同源物、直系同源物及其生物学活性片段。示例性生长因子和蛋白质显示在下表10中。
表10:示例性生长因子和蛋白质
/>
/>
在一些实施方案中,细胞培养基包含长精氨酸3-IGF-1(LR3-IGF1)。LR3肽链为蛋白质提供更高的稳定性。在一些实施方案中,红原鸡LR3-IGF1包含SEQ ID NO:1所示的氨基酸序列或与其具有至少约50%、至少约60%、至少约70%、至少约80%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%的序列同一性的序列。示例性的LR3-IGF1蛋白显示在下表11中。
表11:LR3-IGF1序列
在一些实施方案中,细胞培养基包含一种或多种浓度范围如下表12所示的生长因子。
表12:示例性生长因子和蛋白质
以顺式提供的物种特异性生长因子
在一些实施方案中,可能希望特定属/种的细胞肉与包含源自相同属/种的生长因子的细胞培养基一起培养。目前,只有小鼠和人类来源的生长因子可在商业上广泛获得,并且可能不利于或不适合生长在农业上或营养上重要的动物细胞系,如但不限于鸡肉、牛肉、牲畜、家禽、禽类、野味、或水生物种。用于生长包含高保真物种匹配生长因子的细胞肉的细胞培养基的不可用性,特别是在工业规模上,是一个挑战。
本公开通过提供包含与所培养的细胞肉的属和/或种匹配或顺式的生长因子的细胞培养基解决了这一挑战。如本文所用,顺式生长因子是与培养中细胞的属和/或种相匹配的生长因子。这允许细胞培养基通过仅使用物种和/或属匹配的细胞和生长因子来定制为所培养的细胞肉。例如,在本公开的此类顺式实施方案中,如果细胞培养基用于培养原鸡属细胞,则细胞培养基中使用的相应顺式生长因子会是原鸡属来源的,例如来自红原鸡的FGF-2。顺式生长因子可包含天然存在的序列,例如野生型序列或自发突变,或可包含非天然存在的序列。例如,包含非天然存在的序列的顺式生长因子可以是天然存在的序列的工程化变体。应注意,包含非天然存在的序列的顺式生长因子可能不类似于具有很多序列相似性的天然存在的对应物,但保留相似的功能。顺式生长因子可以通过本领域已知的多种方法产生,例如生长因子可以重组产生、分离和纯化或化学合成。本公开的顺式生长因子包括天然存在的同源物、旁系同源物和直向同源物。任何生长因子都可以以顺式提供;可用作顺式生长因子的示例性生长因子如上表10所示。在一些实施方案中,顺式生长因子是重组顺式生长因子。
在一些实施方案中,变体顺式生长因子是顺式原鸡属LR3-IGF1(SEQ ID NO:1,表11);附加的LR3肽链为蛋白质提供了更高的稳定性。
使用顺式生长因子是本公开的细胞培养基组合物的众多优点之一。目前无法获得源自农业或营养相关动物来源的生长因子,例如鸡FGF或牛IGF,特别是在配制细胞培养基以经济地生长细胞肉所需的工业规模上。顺式重组生长因子可以如下面实施例5所示产生。图3和如实施例6中详述的,显示了用不同浓度的顺式重组原鸡属FGF-2或可商购人重组FGF-2生长的原鸡属细胞的细胞反应。使用两种生长因子观察到相同的反应,表明使用顺式重组原鸡属FGF-2后活性没有损失。
在一些实施方案中,与使用非顺式生长因子时相比,顺式生长因子的使用提供增强的细胞反应、生长、功效和/或活性。例如,与包含非顺式生长因子的培养基相比,在包含顺式生长因子的培养基中培养细胞肉可导致增加的细胞生长速率。如图4所示并在实施例7中详述,与包含人重组转铁蛋白的培养基相比,在包含顺式原鸡属(Gallus)转铁蛋白的培养基中生长的贴壁原鸡属细胞显示出更高的细胞生长。在测试的所有三种浓度的顺式原鸡属转铁蛋白和人重组转铁蛋白中都观察到了增加的增长趋势。这证明了包含顺式生长因子的细胞培养基在产生细胞肉方面优于具有非顺式生长因子的培养基的能力。
通用生长因子
本公开提供了新的生长因子,其支持多个属和/或种的细胞肉的生长并且在本文中被称为通用生长因子。在一些实施方案中,通用生长因子支持任何属和/或种的细胞肉的生长。作为非限制性实例,通用FGF-2、通用PDGF-BB、通用IGF-1或通用VEGF-A可用于细胞培养基中以生长细胞鸡肉、牛肉、家畜、家禽、鸟类、野味或水生物种。含有通用生长因子的细胞培养基具有多种优势,如独立于被培养的细胞的适用性、现成的可用性和降低的成本。
在一些实施方案中,通用生长因子选自下组:通用FGF-2(SEQ ID NO:3)、通用PDGF-BB(SEQ ID NO:5)、通用IGF-1(SEQ ID NO:6)、和通用VEGF-A(SEQ ID NO:7)或与其具有至少约50%、至少约60%、至少约70%、至少约80%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%的序列同一性的序列。
在一些实施方案中,通用生长因子可以是跨界、门、纲、目、科、属和/或种通用的。在一些实施方案中,通用生长因子可以在动物界的后生动物分支中是通用的。
在一些实施方案中,通用生长因子仅在某些界、门、纲、目、科、属和/或种中是通用的。例如,通用生长因子可以在哺乳动物、鸟类、鱼类、爬行动物、两栖动物和节肢动物中的任何一种中通用。在一些实施方案中,通用哺乳动物生长因子可全面用于培养哺乳动物细胞肉。
本公开的通用生长因子可以重组产生、分离/纯化和/或化学合成。在一些实施方案中,通用生长因子如实施例4中所述,在计算机上设计并重组产生。示例性重组通用生长因子显示在表13中。
表13:示例性重组通用生长因子
/>
粘附蛋白
在一些实施方案中,细胞培养基包含一种或多种粘附蛋白。粘附蛋白的实例包括胶原蛋白、胶原蛋白IVα1、纤连蛋白、TPA:纤连蛋白、部分纤连蛋白玻连蛋白、纤维蛋白原变体、前体、同源异构体、同系物、旁系同源物、直系同源物及其生物学活性片段。示例性粘附蛋白显示在下表14中。
表14:示例性粘附蛋白
其他顺式和通用培养基组分
在一些实施方案中,包含在本公开的细胞培养基中的任何蛋白质可以以顺式使用提供。例如,当培养原鸡属细胞时,所使用的粘附蛋白纤连蛋白可以是原鸡属纤连蛋白。顺式粘附蛋白可以重组产生、分离/纯化或化学合成。
在一些实施方案中,包含在本公开的细胞培养基中的任何蛋白质可以是通用的。例如,粘附蛋白纤连蛋白可用于通过本公开中描述的方法开发通用纤连蛋白。
用于配制细胞培养基的方法
本文提供了配制本公开的可用于培养免屠宰肉的细胞培养基(营养培养基)的方法。
在一些实施方案中,本文提供了一种用于配制产生免屠宰肉的营养培养基的配制方法,其包括:(a)提供多种成分;(b)一个或多个:(i)将一种或多种目前未被批准用于食品的成分替换为一种或多种被批准用于食品的成分;(ii)去除目前未被批准用于食品的一种或多种成分;和(iii)以等于或低于ADI值配制一种或多种目前未被批准用于食品的成分。在一些实施方案中,通过该方法产生的细胞培养基是化学确定的。
用于配制产生细胞肉的本公开的细胞培养基的方法是极具挑战性和不可预测的过程。不同于传统的用于制药和生物技术应用的细胞培养基(例如Ham’s F-12、DMEM、培养基199),在开发用于产生细胞肉的本公开的安全和有效的细胞培养基中克服了几个挑战。本公开的细胞培养基是通过一方面平衡安全而开发的,同时保持(如果不超过)用于培养细胞和组织的培养基性能。在大多数情况下,更换、去除和/或减少成分以赋予培养基可食用性会导致细胞培养基性能下降,例如通过细胞活力和细胞生长评估。经过大量实验和新方法,确定了细胞培养基组合物和用于配制细胞培养基的方法。下面讨论了在不影响性能的情况下替换、去除和/或减少低于ADI值的培养基成分的具体实例。此外,下文详述了示例性安全评估框架和3级分类系统,以及表16中成分的具体实例。
举例来说,泊洛沙姆类(poloxamers),例如泊洛沙姆188(Poloxamer 188),是在细胞培养生物过程中用作剪切保护剂的表面活性剂,因此通常在常规细胞培养基中提供。泊洛沙姆类未被批准用于食品。为了找到合适的食品安全替代品,鉴定和筛选了几种具有GRAS批准通知和潜在剪切保护特性的化合物,如聚乙烯醇(PVA)、聚乙烯吡咯烷酮(PVP)和几种甲基纤维素。如图5所示,在各种剪切保护剂存在的情况下,监测性能指标、细胞活力随时间的变化。在没有剪切保护剂(阴性对照)的情况下,细胞活力随时间迅速下降。在PVP存在的情况下,注意到类似的下降,而泊洛沙姆188保持了预期的活力。出乎意料的是,发现羟丙基甲基纤维素(HPMC)在去除泊洛沙姆188后可提供足够的剪切保护以维持细胞活力。然而,单独的有效的剪切保护不足以确定泊洛沙姆的替代品。还必须测试其他关键特性,例如溶解度、粒度、温度效应。发现HPMC具有足够的可溶性和可过滤性,而许多其他食品安全的剪切保护剂则失败了。鉴于泊洛沙姆、PVA、PVP和HPMC的化学结构和物理化学特征大不相同,因此不可能预测所需的性能,例如剪切保护和溶解度等。测试了多种条件以获得本公开的本细胞培养基组合物,例如上述HPMC。在一些实施方案中,所述方法包括去除泊洛沙姆。在一些实施方案中,所述方法包括用甲基纤维素代替泊洛沙姆。在一些实施方案中,所述方法包括用羟丙基甲基纤维素代替泊洛沙姆。在一些实施方案中,所述方法包括将细胞培养基中的泊洛沙姆配方减少至或低于其ADI值。
钴是许多有助于代谢和细胞功能的酶促途径的必需辅助因子营养物质。氯化钴是培养基中常用的钴来源。FDA严禁在食品中使用氯化钴。为了找到合适的替代品,筛选了许多钴化合物。最终,发现了氰钴胺形式的维生素B12,其手性中心含有生物可利用的钴。用氰钴胺素替代氯化钴足以提供钴作为食品安全辅助因子,以促进细胞功能。在一些实施方案中,所述方法包括去除氯化钴。在一些实施方案中,所述方法包括用氰钴胺(Vit B12)代替氯化钴。
几种微量元素对细胞新陈代谢和生长至关重要。为了满足安全标准,这些元素可以从培养基配方中大量减少或完全去除。表15显示了几种不同的成分,它们被调整到低于ADI水平,或完全从培养基配方中去除。作为直接配制微量元素的新替代方案,本公开公开了天然含有微量元素的食品安全复合物的鉴定和测试。例如,柠檬酸铁铵(FAC)是氨、柠檬酸盐和铁的复合物,通常用作食品添加剂/成分。由于FAC的收获和产生过程,已知FAC含有少量的许多微量元素营养物质。细胞研究表明,通过将FAC添加到本公开的培养基中,为细胞提供了稳健细胞生长所需的微量的这些矿物质。如图6所示,与未补充FAC的细胞相比,补充了不同浓度(0.5mg/ml-50mg/ml)的FAC的细胞在一段时间内(长达275小时)保持高活力。因此,在减少/去除表14中的成分后,补充FAC的细胞没有表现出性能下降。
表15:示例性微量元素和其他成分
在一些实施方案中,所述方法包括去除钼酸铵、钼酸钠、偏钒酸铵、偏钒酸钠、氯化铷、氯化锶六水合物、次黄嘌呤、腐胺、胸苷和DL-α硫辛酸中的一种或多种。在其他实施方案中,所述方法包括用柠檬酸铁铵代替钼酸铵、钼酸钠、偏钒酸铵、偏钒酸钠、氯化铷和氯化锶六水合物中的一种或多种。在其他实施方案中,所述方法包括用表1所示浓度范围内的优化氨基酸混合物代替次黄嘌呤、腐胺和胸苷中的一种或多种。在其他实施方案中,所述方法包括用植物衍生油或酵母水解物代替DL-α硫辛酸。在一些实施方案中,所述方法包括将钼酸铵、钼酸钠、偏钒酸铵、偏钒酸钠、氯化铷、氯化锶六水合物、次黄嘌呤、腐胺、胸苷和DL-α硫辛酸中的一种或多种减少至其各自的ADI值或至其各自的ADI值以下。
在一些实施方案中,所述方法包括去除目前未被批准用于食品中的消泡剂。在一些实施方案中,所述方法包括用西甲硅油代替目前未被批准用于食品中的消泡剂。在一些实施方案中,所述方法包括将目前未被批准用于食品中的消泡剂的配方在细胞培养基中减少至其ADI值或至其ADI值以下。
在一些实施方案中,通过所述方法产生的细胞培养基含有不超过10%、9%、8%、7%、6%、5%、4%、3%、2%、1%、0.5%、0.1%或不超过0.01%%的动物源性血清。在一些实施方案中,通过所述方法产生的细胞培养基基本上不含动物源性血清或不含动物源性血清。
在一些实施方案中,通过所述方法产生的细胞培养基不包含任何与血液相关的成分。
在一些实施方案中,通过所述方法产生的细胞培养基含有不超过10%、9%、8%、7%、6%、5%、4%、3%、2%、1%、0.5%、0.1%或不超过0.01%的动物源性组分。在一些实施方案中,通过所述方法产生的细胞培养基基本上不含动物源性组分或不含动物源性组分。
在一些实施方案中,通过所述方法产生的细胞培养基可用于分批、分批补料、恒化器、灌注和/或强化的生物反应器组织培养器过程。
在一些实施方案中,通过所述方法产生的细胞培养基包含本公开中描述的生长因子、通用生长因子和/或顺式生长因子中的任何一种或多种。在一些实施方案中,通过所述方法产生的细胞培养基包含SEQ ID NO:1-7所示的任何一种或多种生长因子。在一些实施方案中,通过所述方法产生的细胞培养基包含本公开中描述的任何一种或多种成分。
本公开还提供了用于评价培养基配方在细胞肉产生中的使用以及用于安全评价的安全评估框架。根据以下概述的程序,对给定细胞培养基的每个成分进行了安全评估。大多数培养基成分是营养物质,并具有多种指定的食品用途的现有监管状态;因此,评价首先要考虑每种化合物的监管状态。根据其类别名称,下文进一步概述了确保培养基成分安全且适用于肉产生的分类框架。表16列出了肉产生过程中使用的培养基成分清单,以及最坏情况暴露估计值和相关权威限制或支持其使用的已公布毒理学/安全数据。
第1类:这些细胞培养基成分是GRAS或联邦法规允许,没有使用限制的食品成分/添加剂。此类别中的示例性化合物包括无害成分,如糖、pH缓冲剂、水溶性维生素和常见的抗氧化剂,如生育酚。
第2类。这些细胞培养基成分是常见的膳食营养物质,预计具有食品使用的GRAS状态或法规允许添加到食品中。此类化合物的实例包括存在于细胞培养基中的大多数无机盐和大量营养剂。如果允许这些化合物以与细胞肉制品中合理预期的预期浓度相当的使用水平直接添加到食品中,,则不会出现安全问题。在家禽细胞肉中存在的大部分营养物质可以很容易地使用常见的经过验证的食品成分测试方法进行测量。可以获得多批次成品的批量分析以验证上述假设。在某些情况下,可以利用从相关权威机构(例如,美国FDA、EFSA、JECFA、FSANZ、U.S.EPA)得出的既定安全水平(例如ADI、UL)来支持安全。如果使用相对于权威参考摄入量值的预期膳食摄入量进行比较,则可以考虑所有膳食来源的添加剂摄入量。在没有权威参考摄入量值的情况下,来自动物毒理学研究的已公布NOAEL可使用食品安全评价的标准科学程序用于评价安全。通常认为,NOAEL与食物暴露的估计膳食摄入量之间的暴露边际(MoE)为100倍或更大足以支持安全。在MoE<100倍的情况下,可能需要进一步减少培养基成分的额外措施,或者可能需要进一步表征种内/种间代谢差异。这些情况还需要根据具体情况仔细考虑监管状态(例如,作为食品添加剂的上市前批准或所需的GRAS评价)。
第3类。这些细胞培养基成分以前没有用于食品产生(例如,没有联邦法规或以前的GRAS状态),但有足够的信息可以得出这些化合物不存在用于食品产生的预期用途的风险的结论。例如,所述化合物在成品中检测不到或在比较食品中以同等水平存在的情况、不耐热且在烹饪过程中会被消化的化合物和/或预期在摄取后被消化为无害化合物的化合物。满足上述条件的化合物的实例会包括重组生长因子和血清成分。对于第3类物质,安全评估过程中的最终考虑可涉及对物质在亚慢性大鼠毒性研究中测量的终点之外产生毒性生物效应的可能性的危害表征。具有生物活性的物质可能需要额外的与生殖和发育毒性或免疫毒性相关的危险特征。还可以评价对过敏原性、对人体的生物学影响(例如,对血压的影响)以及对与其他培养基成分的协同作用的考虑。此类调查最好是基于证据的(即,临床试验的可用性证明某种物质会影响血压),而不是理论上的(即,基于推定的作用机制)。与第2类物质类似,第3类中成分的监管状态会需要对化合物的监管状态进行逐案评价(例如,需要上市前批准或GRAS评价)。第3类成分的实例包括重组蛋白和动物血清。
表16:肉产生过程中使用的细胞培养基成分示例性列表,风险分类和安全信息
/>
/>
/>
/>
/>
/>
/>
/>
Al=充足的摄入量
ADI=可接受的每日摄入量
FNB-IOM=医学研究所食品和营养委员会
FIDT=测试的最高剂量
N/A=不适用
NR=未报告
NS=未指定为没有已知过量摄入的毒性证据
NOAEL=未观察到有害作用水平
UL=可耐受上限
OSL=观察到的安全水平
*作为膳食蛋白质提供时没有上限
**使用培养基成分完全转移到成品的保守假设估计的最大膳食暴露量,以wt/wt为基础。
示例性实施方案
实施方案I-1。一种包含多种成分的细胞培养基,其中每种成分被批准用于食品和/或等于或低于其ADI值。
实施方案I-2。实施方案I-1所述的培养基,其中所述培养基是可食用的。
实施方案I-3。实施方案I-1或1-2所述的培养基,其中被批准用于食品的成分是公认安全的(GRAS)。
实施方案I-4。实施方案I-1至1-3之一所述的培养基,其中所述成分被FDA批准用于食品中。
实施方案I-5。实施方案I-1至1-4之一所述的培养基,其中所述成分被USDA批准用于食品中。
实施方案I-6。实施方案I-1至1-5之一所述的培养基,其中所述成分被食品法典批准用于食品中。
实施方案I-7。实施方案I-1至1-6之一所述的培养基,其中所述成分被欧洲食品安全局批准用于食品中。
实施方案I-8。实施方案I-1至1-7之一所述的培养基,其中所述成分被食品化学品法典批准用于食品中。
实施方案I-9。实施方案I-1至1-8之一所述的培养基,其中所述培养基含有不超过10%、9%、8%、7%、6%、5%、4%、3%、2%、1%、0.5%、0.1%、0.05%或不超过0.01%动物源性血清。
实施方案I-10。实施方案I-1至1-9之一所述的培养基,其中所述培养基基本上不含动物源性血清。
实施方案I-11。实施方案I-1至I-10之一所述的培养基,其中所述培养基不含动物源性血清。
实施方案I-12。实施方案I-1至I-11之一所述的培养基,其中所述培养基含有不超过10%、9%、8%、7%、6%、5%、4%、3%、2%、1%、0.5%、0.1%、0.05%或不超过0.01%动物源性组分。
实施方案I-13。实施方案I-1至1-12之一所述的培养基,其中所述培养基基本上不含动物源性组分。
实施方案I-14。实施方案I-1至1-13之一所述的培养基,其中所述培养基不含动物源性组分。
实施方案I-15。实施方案I-1至1-14之一所述的培养基,其中所述培养基是在化学上定义的。
实施方案I-16。实施方案I-1至1-15之一所述的培养基,其进一步包含生长因子。
实施方案I-17。实施方案I-16所述的培养基,其中所述生长因子是通用生长因子。
实施方案I-18。实施方案I-17所述的培养基,其中所述通用生长因子是FGF-2。
实施方案I-19。实施方案I-18所述的培养基,其中FGF-2包含SEQ ID NO:3所示的氨基酸序列。
实施方案I-20。实施方案I-18所述的培养基,其中FGF-2由SEQ ID NO:4所示的核酸序列编码。
实施方案I-21。实施方案I-17所述的培养基,其中通用生长因子是PDGF-BB。
实施方案I-22。实施方案I-21所述的培养基,其中PDGF-BB包含SEQ ID NO:5所示的氨基酸序列。
实施方案I-23。实施方案I-17所述的培养基,其中所述通用生长因子是IGF-1。
实施方案I-24。实施方案I-23所述的培养基,其中IGF-1包含SEQ ID NO:6所示的氨基酸序列。
实施方案I-25。实施方案I-17所述的培养基,其中所述通用生长因子是VEGF-A。
实施方案I-26。实施方案I-25所述的培养基,其中VEGF-A包含SEQ ID NO:7所示的氨基酸序列。
实施方案I-27。实施方案I-16所述的培养基,其中所述培养基用于培养细胞肉,所述生长因子为顺式生长因子,其中所述顺式生长因子与培养中的细胞的属匹配。
实施方案I-28。实施方案I-27所述的培养基,其中与非顺式生长因子相比,所述顺式生长因子的使用允许增强的细胞生长。
实施方案I-29。实施方案I-28所述的培养基,其中所述顺式生长因子为顺式原鸡属转铁蛋白。
实施方案I-30。实施方案I-27所述的培养基,其中所述顺式生长因子是培养中细胞的属的相应天然存在的生长因子的变体。
实施方案I-31。实施方案I-30所述的培养基,其中所述顺式生长因子变体是原鸡属LR3-IGF1。
实施方案I-32。实施方案I-31所述的培养基,其中原鸡属LR3-IGF1包含SEQ IDNO:1所示的氨基酸序列。
实施方案I-33。实施方案I-16所述的培养基,其中所述生长因子选自下组:IGF-1、LR3-IGF1、FGF-1、FGF-2、PDGF、CTGF、EGF、TGFB、BMP、HGF、转铁蛋白、胰岛素、WNT、白细胞介素、白蛋白、VEGF、同源物、旁系同源物、直向同源物、变体、前体、同源异构体及其组合。
实施方案I-34。实施方案I-16或1-33所述的培养基,其中所述生长因子选自表10。
实施方案I-35。实施方案I-16或1-33所述的培养基,其中所述生长因子是鸡生长因子、鸭生长因子、牛生长因子、绵羊生长因子、鱼生长因子、猪生长因子、哺乳动物生长因子、鸟类生长因子,爬行动物生长因子、两栖动物生长因子、蛛形纲动物生长因子或硬骨鱼生长因子。
实施方案I-36。实施方案I-1至1-35之一所述的培养基,其进一步包含粘附蛋白。
实施方案I-37。实施方案I-36所述的培养基,其中所述粘附蛋白选自表14。
实施方案I-38。实施方案I-1至1-37之一所述的培养基,其中所述多种成分包含一种或多种浓度范围如下所示的氨基酸:
/>
实施方案I-39。实施方案I-1至1-38之一所述的培养基,其中所述多种成分包含一种或多种浓度范围如下所示的碳水化合物:
实施方案I-40。实施方案I-1至1-39之一所述的培养基,其中所述多种成分包含一种或多种浓度范围如下所示的维生素:
实施方案I-41。实施方案I-1至1-40之一所述的培养基,其中所述多种成分包含一种或多种浓度范围如下所示的无机盐:
实施方案I-42。实施方案I-1至1-41之一所述的培养基,其中所述多种成分包含一种或多种浓度范围如下所示的微量金属:
实施方案I-43。实施方案I-1至1-42之一所述的培养基,其中所述多种成分包含一种或多种浓度范围如下所示的脂质:
实施方案I-44。实施方案I-1至1-43之一所述的培养基,其中所述多种成分包含一种或多种如下所示浓度范围的食用油:
实施方案I-45。实施方案I-1至1-44之一所述的培养基,其中所述多种成分包含一种或多种如下所示浓度范围的生长因子:
实施方案I-46。实施方案I-1至1-45之一所述的培养基,其中所述多种成分包含一种或多种如下所示浓度范围的补充成分:
实施方案I-47。实施方案I-1至1-46之一所述的培养基,其中所述多种成分包含一种或多种如下所示浓度范围的TCA循环中间体:
实施方案I-48。实施方案I-1至1-47之一所述的培养基,其中所述多种成分包含一种或多种糖酵解中间体、铁载体、麦芽酚铁、葡萄糖酸亚铁、剪切保护剂、聚乙二醇、甲基纤维素和水解产物。
实施方案I-49。实施方案I-1至1-48之一所述的培养基,其中将所述培养基与水混合以形成溶液。
实施方案I-50。实施方案I-1至1-49之一所述的培养基,其中所述培养基包含甲基纤维素。
实施方案I-51。实施方案I-1至1-50之一所述的培养基,其中所述培养基包含氰钴胺,任选地浓度范围为1.00E+05g/L至0.0026g/L。
实施方案I-52。实施方案I-1至1-51之一所述的培养基,其中所述培养基包含西甲硅油。
实施方案I-53。实施方案I-1至1-52之一的培养基,其中所述培养基包含柠檬酸铁铵,任选地浓度范围为0.01g/L至0.5g/L。
实施方案I-54。实施方案I-1至1-53之一的培养基,其中所述培养基包含食品级植物油。
实施方案I-55。一种组合物,其包含实施方案I-1至1-54之一所述的培养基,其进一步包含培养中的非人细胞。
实施方案I-56。实施方案I-55所述的组合物,其中所述细胞来自家禽、海鲜、野味或家畜。
实施方案I-57。实施方案I-1至1-56之一所述的培养基,其中所述多种成分包含一种或多种氨基酸、镁盐、钠盐、铜盐、锌盐、铁盐和维生素。
实施方案I-58。实施方案I-57所述的培养基,其中所述成分的浓度范围如下所示:
实施方案I-59。一种通用FGF-2,其包含SEQ ID NO:3所示的氨基酸序列。
实施方案I-60。一种通用FGF-2,其由SEQ ID NO:4所示的核酸序列编码。
实施方案I-61。一种通用PDGF-BB,其包含SEQ ID NO:5所示的氨基酸序列。
实施方案I-62。一种通用IGF-1,其包含SEQ ID NO:6所示的氨基酸序列。
实施方案I-63。一种通用VEGF-A,其包含SEQ ID NO:7所示的氨基酸序列。
实施方案I-64。一种原鸡属LR3-IGF1,其包含SEQ ID NO:1所示的氨基酸序列。
实施方案I-65。一种用于配制培养细胞肉的培养基的方法,其包括:
(a)提供多种成分;以及
(b)一个或多个:
(i)将一种或多种目前未被批准用于食品的成分替换为被批准用于食品的成分;
(ii)去除目前未被批准用于食品的一种或多种成分;和
(iii)以等于或低于ADI值配制一种或多种目前未被批准用于食品的成分。
实施方案I-66。实施方案I-65所述的方法,其中所述培养基是可食用的。
实施方案I-67。实施方案I-65或1-66所述的方法,其中所述培养基含有不超过10%、9%、8%、7%、6%、5%、4%、3%、2%、1%、0.5%、0.1%、0.05%或不超过0.01%动物源性血清。
实施方案I-68。实施方案I-65至1-67之一所述的方法,其中所述培养基基本上不含动物源性血清。
实施方案I-69。实施方案I-65至1-68之一所述的方法,其中所述培养基不含动物源性血清。
实施方案I-70。实施方案I-65至1-69之一所述的方法,其中所述培养基含有不超过10%、9%、8%、7%、6%、5%、4%、3%、2%、1%、0.5%、0.1%、0.05%或不超过0.01%动物源性组分。
实施方案I-71。实施方案I-65至1-70之一所述的方法,其中所述培养基基本上不含动物源性组分。
实施方案I-72。实施方案I-65至1-71之一所述的方法,其中所述培养基不含动物源性组分。
实施方案I-73。实施方案I-65至1-72之一所述的方法,其中所述培养基是化学上定义的。
实施方案I-74。实施方案I-65至1-73之一所述的方法,其中将泊洛沙姆替换为甲基纤维素。
实施方案I-75。实施方案I-65至1-74之一所述的方法,其中将氯化钴替换为氰钴胺。
实施方案I-76。实施方案I-65至1-75之一所述的方法,其中将目前未被批准用于食品的消泡剂替换为西甲硅油。
实施方案I-77。实施方案I-65至1-76之一所述的方法,其中将钼酸铵、钼酸钠、偏钒酸铵、偏钒酸钠、氯化铷和氯化锶六水合物中的一种或多种替换为柠檬酸铁铵。
实施方案I-78。实施方案I-65至1-77之一所述的方法,其进一步包括添加实施方案I-59至1-64中任一项所述的生长因子。
实施方案II-1。一种用于产生免屠宰肉的可食用营养培养基,所述培养基包含多种成分,其中每种成分被批准用于食品和/或等于或低于其ADI值。
实施方案II-2。实施方案II-1所述的培养基,其中被批准用于食品的成分是公认安全的(GRAS)。
实施方案II-3。实施方案II-1所述的培养基,其中所述培养基基本上不含动物源性组分。
实施方案II-4。实施方案II-1所述的培养基,其中所述培养基基本上不含动物源性血清。
实施方案II-5。实施方案II-1所述的培养基,其进一步包含生长因子。
实施方案II-6。实施方案II-5所述的培养基,其中所述生长因子是选自下组的通用生长因子:通用FGF-2(SEQ ID NO:3)、通用PDGF-BB(SEQ ID NO:5)、通用IGF-1(SEQ IDNO:6)和通用VEGF-A(SEQ ID NO:7),或与它们具有至少约50%、至少约60%、至少约70%、至少约80%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%的序列同一性的序列。
实施方案II-7。实施方案II-6所述的培养基,其中所述培养基包含顺式生长因子,其中所述顺式生长因子与所产生肉的来源的属(genus)匹配。
实施方案II-8。实施方案II-7所述的培养基,其中与非顺式生长因子相比,所述顺式生长因子的使用允许增强的肉产生。
实施方案II-9。实施方案II-8所述的培养基,其中所述顺式生长因子是顺式原鸡属(Gallus)转铁蛋白。
实施方案II-10。实施方案II-7所述的培养基,其中所述顺式生长因子是所产生肉的属的相应天然存在的生长因子的变体。
实施方案II-11。实施方案II-10所述的培养基,其中所述顺式生长因子变体是原鸡属LR3-IGF1,任选地包含SEQ ID NO:1所示的氨基酸序列。
实施方案II-12。实施方案II-5所述的培养基,其中所述生长因子选自下组:IGF-1、LR3-IGF1、FGF-1、FGF-2、PDGF、CTGF、EGF、TGFB、BMP、HGF、转铁蛋白、胰岛素、WNT、白细胞介素、白蛋白、VEGF、同源物、旁系同源物、直向同源物、变体、前体、同源异构体及其组合。
实施方案II-13。实施方案II-5所述的培养基,其中所述生长因子选自表10。
实施方案II-14。实施方案II-5所述的培养基,其中所述生长因子是鸡生长因子、鸭生长因子、牛生长因子、绵羊生长因子、鱼生长因子、猪生长因子、哺乳动物生长因子、鸟类生长因子、爬行动物生长因子,两栖类生长因子、蛛形纲动物生长因子或硬骨鱼生长因子。
实施方案II-15。实施方案II-1所述的培养基,其进一步包含选自表14的粘附蛋白。
实施方案II-16。实施方案II-1所述的培养基,其中所述多种成分包含一种或多种浓度范围如下所示的氨基酸:
实施方案II-17。实施方案II-1所述的培养基,其中所述多种成分包含一种或多种浓度范围如下所示的碳水化合物:
实施方案II-18。实施方案II-1所述的培养基,其中所述多种成分包含一种或多种浓度范围如下所示的维生素:
/>
实施方案II-19。实施方案II-1所述的培养基,其中所述多种成分包含一种或多种浓度范围如下所示的无机盐:
实施方案II-20。实施方案II-1所述的培养基,其中所述多种成分包含一种或多种浓度范围如下所示的微量金属:
/>
实施方案II-21。实施方案II-1所述的培养基,其中所述多种成分包含一种或多种浓度范围如下所示的脂质:
实施方案II-22。实施方案II-1所述的培养基,其中所述多种成分包含一种或多种如下所示浓度范围的食用油:
实施方案II-23。实施方案II-1所述的培养基,其中所述多种成分包含一种或多种浓度范围如下所示的生长因子:
实施方案II-24。实施方案II-1所述的培养基,其中所述多种成分包含一种或多种如下所示浓度范围的补充成分:
实施方案II-25。实施方案II-1所述的培养基,其中所述多种成分包含一种或多种如下所示浓度范围的TCA循环中间体:
实施方案II-26。实施方案II-1所述的培养基,其中所述多种成分包含一种或多种糖酵解中间体、铁载体、麦芽酚铁、葡萄糖酸亚铁、剪切保护剂、聚乙二醇、甲基纤维素、西甲硅油、食品级植物油和水解产物。
实施方案II-27。实施方案II-1所述的培养基,其中所述成分的浓度范围如下所示:
/>
实施方案II-28。一种通用生长因子,其选自下组:通用FGF-2(SEQ ID NO:3)、通用PDGF-BB(SEQ ID NO:5)、通用IGF-1(SEQ ID NO:6)和通用VEGF-A(SEQ ID NO:7)或与其具有至少约50%、至少约60%、至少约70%、至少约80%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%的序列同一性的序列。
实施方案II-29。一种原鸡属LR3-IGF1,其包含SEQ ID NO:1所示的氨基酸序列或与其具有至少约50%、至少约60%、至少约70%、至少约80%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%的序列同一性的序列。
实施方案II-30。一种用于配制产生免屠宰肉的营养培养基的方法,其包括:
(a)提供多种成分;以及
(b)一个或多个:
(i)将一种或多种目前未被批准用于食品的成分替换为一种或多种被批准用于食品的成分;
(ii)去除目前未被批准用于食品的一种或多种成分;和
(iii)以等于或低于ADI值配制一种或多种目前未被批准用于食品的成分。
实施方案II-31。实施方案II-30所述的方法,其中所述将一种或多种目前未被批准用于食品的成分替换为一种或多种被批准用于食品的成分,包括一种或多种:
a.其中将泊洛沙姆替换为甲基纤维素;
b.其中将氯化钴替换为氰钴胺;
b.其中将目前未被批准用于食品的消泡剂替换为西甲硅油;以及
c.其中将钼酸铵、钼酸钠、偏钒酸铵、偏钒酸钠、氯化铷和氯化锶六水合物中的一种或多种替换为柠檬酸铁铵。
实施方案II-32。实施方案II-30所述的方法,其中将泊洛沙姆替换为甲基纤维素。
实施方案II-33。实施方案II-30所述的方法,其中将氯化钴替换为氰钴胺。
实施方案II-34。实施方案II-30所述的方法,其中将目前未被批准用于食品的消泡剂替换为西甲硅油。
实施方案II-35。实施方案II-30所述的方法,其中将钼酸铵、钼酸钠、偏钒酸铵和偏钒酸钠中的一种或多种替换为柠檬酸铁铵。
实施例
实施例1在含有GRAS与非GRAS成分的细胞培养基中贴壁原鸡属细胞的生长
将贴壁原鸡属细胞解冻并以5000个细胞/cm
图1A显示了随时间计数的活贴壁细胞的平均数。在GRAS-ACF培养基中生长的细胞显示出比在非GRAS SF培养基中生长的细胞更快的生长速率。在阴性对照中观察到最小的细胞生长。
实施例2在含有GRAS与非GRAS成分的细胞培养基中悬浮原鸡属细胞的生长
将悬浮原鸡属细胞解冻并以0.25x10
图IB显示了随时间计数的活悬浮细胞的平均数。与实施例1中描述的贴壁细胞相似,在GRAS-ACF培养基中生长的悬浮细胞显示出比在非GRAS SF培养基中生长的悬浮细胞更高的生长速率。在非GRAS SF培养基中生长的细胞在第4天观察到细胞活力急剧下降,而在GRAS-ACF培养基中观察到持续生长。
实施例1和2证明了与包含潜在危险的非GRAS认证成分的细胞培养基相比,包含GRAS认证成分的本公开的示例性无动物组分细胞培养基支持贴壁细胞和悬浮细胞生长的能力。
实施例3可商购培养基与优化的培养基中悬浮细胞生长的比较
将悬浮原鸡属细胞解冻并以0.25x10
图2显示了5天内在优化的培养基中与在商业培养基中生长的活细胞的数量。对于在优化的培养基中生长的细胞,观察到活细胞数量明显增加。较高的细胞活力一直持续到实验结束,这表明本公开的优化的细胞培养基相对于可商购的细胞培养基具有增强的细胞生长性能。
实施例4通用重组生长因子的生成
例如,下文描述了通用重组FGF-2、PDGF-BB、VEGF-A和IGF-1的产生。
通用FGF-2
根据Uniprot比对程序https://www.uniprot.org/,使用每个位点最常见的氨基酸残基构建通用FGF-2。FGF-2序列选自几种常见的哺乳动物、两栖动物和鸟类,包括小鼠、大鼠、鸡、牛、人、黑猩猩、绵羊、非洲爪蟾、狗、雪貂、猫和马。反映每个位置最常见的氨基酸选择的典型氨基酸显示在SEQ ID NO:3所示的氨基酸序列中(表13)。
在Soleyman et al.High-level Expression and Purification of ActiveHuman FGF-2in Escherichia coli by Codon and Culture Condition OptimizationIran Red Crescent Med J.2016February;18(2):e21615之后,将通用FGF-2克隆到大肠杆菌表达载体pET32a(+)中。氨基酸序列针对大肠杆菌BL21(DE3)表达进行了密码子优化。通用FGF-2的DNA序列(SEQ ID NO:4,表13)已提交用于全基因合成,包括由NEB Builder设计的PCR核苷酸序列,以按照制造商的说明使用
通用PDGF-BB
使用与上述通用FGF-2相同的方法构建通用PDGF-BB。通用PDGF-BB的氨基酸序列显示在SEQ ID NO:5(表13)中。
通用IGF-1和通用VEGF-A
使用与上述通用FGF-2类似的方法构建通用IGF-1和通用VEGF-A,具有一些变化。通用IGF-1和通用VEGF-A的氨基酸序列分别显示在SEQ ID NO.6和SEQ ID NO.7(表13)中。使用了Clustal Omega多序列比对程序,https://www.ebi.ac.uk/Tools/msa/clustalo/。IGF-1和VEGF-A序列选自包括人、牛、猪、绵羊、山羊和鸡在内的物种。通用生长因子序列由EMBOSS Cons工具确定,以确定每个位置的共有氨基酸残基,https://www.ebi.ac.uk/Tools/msa/emboss_cons/。
实施例5种特异性顺式重组生长因子的产生
用于生长相同属/种的培养肉目的的种特异性顺式生长因子在大肠杆菌或哺乳动物细胞中重组产生。例如,下文描述了用于培养细胞鸡的原鸡属FGF-2的重组产生。
编码原鸡属FGF-2的DNA针对细菌表达进行了密码子优化。然后将DNA插入细菌表达载体,例如PET32a。携带编码顺式生长因子基因的载体在大肠杆菌中表达,并针对蛋白质产生和纯化进行了优化。纯化蛋白质的生物活性通过在生长因子敏感细胞(例如NIH3T3成纤维细胞)中的增殖测定来确定。然后将纯化的生长因子用于细胞培养,以促进细胞肉的产生。
实施例6与商业人重组FGF-2相比,顺式重组原鸡属FGF-2的细胞反应
将贴壁原鸡属细胞解冻并以5000个细胞/cm
图3显示了与不含生长因子的培养基(空白)相比,10μg/L和100μg/L的顺式原鸡属FGF-2和商业人FGF-2的细胞反应。结果表明,在两种测试的浓度下,用顺式原鸡属FGF-2培养的原鸡属细胞的活性与用商业人FGF-2培养的细胞的活性相当。这些结果证明了本公开的重组生长因子对于生长物种匹配的顺式细胞肉的适用性,与广泛可得的商业生长因子相比,没有任何功能损失。
实施例7在包含顺式原鸡
将贴壁的原鸡属细胞解冻并以5000个细胞/cm
图4是条形图,将细胞计数显示为每个条件的对照百分比。与在培养基中用人重组转铁蛋白生长的细胞相比,在所有测试浓度下,用顺式原鸡属转铁蛋白在培养基中生长的原鸡属细胞明显显示出更高的细胞计数。
序列表
<110> 阿普賽德食品公司
<120> 用于产生免屠宰肉的营养培养基
<130> PF02717A
<150> US 63/035,661
<151> 2020-06-05
<160> 7
<170> PatentIn version 3.5
<210> 1
<211> 83
<212> PRT
<213> 原鸡
<400> 1
Met Phe Pro Ala Met Pro Leu Ser Ser Leu Phe Val Asn Gly Pro Arg
1 5 1015
Thr Leu Cys Gly Ala Glu Leu Val Asp Ala Leu Gln Phe Val Cys Gly
202530
Asp Arg Gly Phe Tyr Phe Ser Lys Pro Thr Gly Tyr Gly Ser Ser Ser
354045
Arg Arg Leu His His Lys Gly Ile Val Asp Glu Cys Cys Phe Gln Ser
505560
Cys Asp Leu Arg Arg Leu Glu Met Tyr Cys Ala Pro Ile Lys Pro Pro
65707580
Lys Ser Ala
<210> 2
<211> 83
<212> PRT
<213> 智人
<400> 2
Met Phe Pro Ala Met Pro Leu Ser Ser Leu Phe Val Asn Gly Pro Arg
1 5 1015
Thr Leu Cys Gly Ala Glu Leu Val Asp Ala Leu Gln Phe Val Cys Gly
202530
Asp Arg Gly Phe Tyr Phe Asn Lys Pro Thr Gly Tyr Gly Ser Ser Ser
354045
Arg Arg Ala Pro Gln Thr Gly Ile Val Asp Glu Cys Cys Phe Arg Ser
505560
Cys Asp Leu Arg Arg Leu Glu Met Tyr Cys Ala Pro Leu Lys Pro Ala
65707580
Lys Ser Ala
<210> 3
<211> 155
<212> PRT
<213> 人工序列
<220>
<223> 通用FGF-2
<400> 3
Met Ala Ala Gly Ser Ile Thr Thr Leu Pro Ala Leu Pro Glu Asp Gly
1 5 1015
Gly Ser Gly Ala Phe Pro Pro Gly His Phe Lys Asp Pro Lys Arg Leu
202530
Tyr Cys Lys Asn Gly Gly Phe Phe Leu Arg Ile His Pro Asp Gly Arg
354045
Val Asp Gly Val Arg Glu Lys Ser Asp Pro His Ile Lys Leu Gln Leu
505560
Gln Ala Glu Glu Arg Gly Val Val Ser Ile Lys Gly Val Cys Ala Asn
65707580
Arg Tyr Leu Ala Met Lys Glu Asp Gly Arg Leu Leu Ala Ser Lys Cys
859095
Val Thr Asp Glu Cys Phe Phe Phe Glu Arg Leu Glu Ser Asn Asn Tyr
100 105 110
Asn Thr Tyr Arg Ser Arg Lys Tyr Ser Ser Trp Tyr Val Ala Leu Lys
115 120 125
Arg Thr Gly Gln Tyr Lys Leu Gly Ser Lys Thr Gly Pro Gly Gln Lys
130 135 140
Ala Ile Leu Phe Leu Pro Met Ser Ala Lys Ser
145 150 155
<210> 4
<211> 471
<212> DNA
<213> 人工序列
<220>
<223> 通用FGF-2
<400> 4
atggcagcag gtagtattac tacgcttccc gcccttcccg aagacggggg ttcaggtgcc 60
ttcccgccgg ggcattttaa agacccgaag cgcctttact gtaagaatgg gggctttttc 120
ttgcgtatcc acccagacgg ccgcgtggac ggtgtgcgtg aaaaatccga tccacatatt 180
aaacttcagc ttcaagcaga agagcgtggt gtggtttcca tcaagggggt gtgtgccaac 240
cgctatcttg cgatgaagga ggacggtcgt ctgctggctt cgaaatgtgt taccgacgag 300
tgttttttct tcgagcgcct ggaatcaaat aattacaaca cctaccgcag ccgcaaatat 360
tcttcatggt acgtggcttt gaagcgcaca ggtcagtata aattgggcag taaaacgggt 420
ccaggacaga aggcgattct tttcttaccg atgtcagcta aaagctaatg a 471
<210> 5
<211> 108
<212> PRT
<213> 人工序列
<220>
<223> 通用PDGF-BB
<400> 5
Ser Leu Gly Ser Leu Ala Ala Ala Glu Pro Ala Val Ile Ala Glu Cys
1 5 1015
Lys Thr Arg Thr Glu Val Phe Glu Ile Ser Arg Arg Leu Ile Asp Arg
202530
Thr Asn Ala Asn Phe Leu Val Trp Pro Pro Cys Val Glu Val Gln Arg
354045
Cys Ser Gly Cys Cys Asn Asn Arg Asn Val Gln Cys Arg Pro Thr Gln
505560
Val Gln Asp Arg Pro Val Gln Val Arg Lys Ile Glu Ile Val Arg Lys
65707580
Lys Pro Ile Phe Lys Lys Ala Thr Val Thr Leu Glu Asp His Leu Ala
859095
Cys Lys Cys Glu Thr Val Val Ala Arg Ala Val Thr
100 105
<210> 6
<211> 153
<212> PRT
<213> 人工序列
<220>
<223> 通用IGF-1
<400> 6
Met Gly Lys Ile Ser Ser Leu Pro Thr Gln Leu Phe Lys Cys Cys Phe
1 5 1015
Cys Asp Phe Leu Lys Val Lys Met His Val Thr Ser Ser Ser His Leu
202530
Phe Tyr Leu Ala Leu Cys Leu Leu Thr Phe Thr Ser Ser Ala Thr Ala
354045
Gly Pro Glu Thr Leu Cys Gly Ala Glu Leu Val Asp Ala Leu Gln Phe
505560
Val Cys Gly Asp Arg Gly Phe Tyr Phe Asn Lys Pro Thr Gly Tyr Gly
65707580
Ser Ser Ser Arg Arg Ala Pro Gln Thr Gly Ile Val Asp Glu Cys Cys
859095
Phe Arg Ser Cys Asp Leu Arg Arg Leu Glu Met Tyr Cys Ala Pro Leu
100 105 110
Lys Pro Ala Lys Ser Ala Arg Ser Val Arg Ala Gln Arg His Thr Asp
115 120 125
Met Pro Lys Ala Gln Lys Glu Val His Leu Lys Asn Thr Ser Arg Gly
130 135 140
Ser Ala Gly Asn Lys Asn Tyr Arg Met
145 150
<210> 7
<211> 190
<212> PRT
<213> 人工序列
<220>
<223> 通用VEGF-A
<400> 7
Met Asn Phe Leu Leu Ser Trp Val His Trp Ser Leu Ala Leu Leu Leu
1 5 1015
Tyr Leu His His Ala Lys Trp Ser Gln Ala Ala Pro Met Ala Glu Gly
202530
Gly Gln Lys Pro His Glu Val Val Lys Phe Met Asp Val Tyr Gln Arg
354045
Ser Phe Cys Arg Pro Ile Glu Thr Leu Val Asp Ile Phe Gln Glu Tyr
505560
Pro Asp Glu Ile Glu Phe Ile Phe Lys Pro Ser Cys Val Pro Leu Met
65707580
Arg Cys Gly Gly Cys Cys Asn Asp Glu Ser Leu Glu Cys Val Pro Thr
859095
Glu Glu Phe Asn Ile Thr Met Gln Ile Met Arg Ile Lys Pro His Gln
100 105 110
Ser Gln His Ile Gly Glu Met Ser Phe Leu Gln His Asn Lys Cys Glu
115 120 125
Cys Arg Pro Lys Lys Asp Lys Ala Arg Gln Glu Asn Pro Cys Gly Pro
130 135 140
Cys Ser Glu Arg Arg Lys His Leu Phe Val Gln Asp Pro Gln Thr Cys
145 150 155 160
Lys Cys Ser Cys Lys Asn Thr Asp Ser Arg Cys Lys Ala Arg Gln Leu
165 170 175
Glu Leu Asn Glu Arg Thr Cys Arg Cys Asp Lys Pro Arg Arg
180 185 190
