一种抗衰老片的多成分定量分析方法
文献发布时间:2024-04-18 19:58:30
技术领域
本发明涉及医药技术领域,尤其是涉及一种抗衰老片的多成分定量分析方法。
背景技术
衰老一直是医学领域令人困惑的一个问题,是一个多因素的过程,导致细胞、组织和有机体水平的渐进式功能下降。中药抗衰老历史悠久、优势显著,已成为当前中药领域的研究热点。抗衰老片粉末是在明永乐太医院宫廷方“益寿永贞膏”基础上开发的中成药复方制剂,具有益气养阴、补血生津、宁心安神的功效,由生地黄、红参、麦冬、天冬、地骨皮、茯苓六味药材制备而成。抗衰老片中含有大量的人参皂苷等活性小分子组分和多糖组分,其质量控制成为必要的一环。鉴于至今未有报导全面和快速的抗衰老片多成分检测方法,建立灵敏、快速、操作简单且能较全面和直接反映抗衰老片中有效成分的定量分析方法,是抗衰老片的质量标准研究和有效成分控制的趋势。
发明内容
本发明所要解决的技术问题在于提供一种抗衰老片的多成分定量分析方法。
本发明采用的技术方案是:
一种抗衰老片的多成分定量分析方法,以含乙腈-甲酸的水溶液为流动相,使用色谱柱进行目标化合物分离,采用电喷雾电离三重四级杆质谱在MRM模式下对抗衰老片中的13种活性成分同时进行含量测定,所述13种活性成分为毛蕊花糖苷、异毛蕊花糖苷、松果菊苷、焦地黄苯乙醇苷A1、人参皂苷Rb1、人参皂苷Rb2、人参皂苷Rc、人参皂苷Rd、人参皂苷Re、人参皂苷Rf、人参皂苷Rg1、人参皂苷Rg2和人参皂苷Rg3。
优选的,上述抗衰老片的多成分定量分析方法,所述流动相为含乙腈-0.1%甲酸的水溶液。
优选的,上述抗衰老片的多成分定量分析方法,所述色谱柱为HSS T3色谱柱。
优选的,上述抗衰老片的多成分定量分析方法,所述抗衰老片为抗衰老片浸膏粉,该抗衰老片浸膏粉经50%乙醇超声提取90min后,提取液离心并通过微孔滤膜过滤作为供试液。
优选的,上述抗衰老片的多成分定量分析方法,采用HSS T3色谱柱的色谱条件如下:
色谱柱:Waters UPLC ACQUITY HSS T3(1.8μm,2.1mm×100mm);流动相:乙腈(A)—0.1%甲酸水溶液(B),梯度洗脱程序,柱温40℃,流速0.3mL/min,进样体积4μL。梯度洗脱程序如下:0–2.5mi,20–30%(A);2.5–10min,30–60%(A);10–10.5min,60–98%(A);10.5–13min,98–98%(A);13–13.5min,98–20%(A);13.5–15min,20–20%(A)。
优选的,上述抗衰老片的多成分定量分析方法,采用电喷雾电离三重四级杆质谱的质谱条件如下:
离子源为电喷雾离子源(ESI),采用负离子扫描检测模式,负离子模式下:毛细管电压2.0kv,锥孔电压37V,脱溶剂温度350℃;正离子模式下毛细管电压3.0kv,锥孔电压30V,脱溶剂温度350℃,采用多重反应监测模式(MRM)。
本发明的有益效果是:
上述抗衰老片的多成分定量分析方法,是综合考虑抗衰老片所含的活性成分和特征成分,首次建立同时测定抗衰老片中毛蕊花糖苷、异毛蕊花糖苷、松果菊苷、焦地黄苯乙苷A1、人参皂苷Rb1、人参皂苷Rb2、人参皂苷Rc、人参皂苷Rd、人参皂苷Re、人参皂苷Rf、人参皂苷Rg1、人参皂苷Rg2和人参皂苷Rg3 13种化学成分的UPLC/QQQ-MS方法,通过对该同时测定抗衰老片多成分含量的方法学进行考察,其专属性、线性、准确度、精密度、稳定性和加样回收率均符合要求,为同时测定抗衰老片中多成分的含量提供了新的技术思路。
上述抗衰老片中的多成分定量分析方法可同时定量抗衰老片中的13种成分,所述13种活性成分中毛蕊花糖苷、异毛蕊花糖苷、松果菊苷、焦地黄苯乙醇苷A1、人参皂苷Rg2和人参皂苷Rg3的线性范围为0.4-100ng/mL,人参皂苷Rb1、人参皂苷Rb2、人参皂苷Rc、人参皂苷Rd、人参皂苷Re、人参皂苷Rf、人参皂苷Rg1的线性范围为4-1000ng/mL,该方法灵敏度高,专属性强,重现性好,实现了对抗衰老片中13种活性成分的同时定量分析。
附图说明
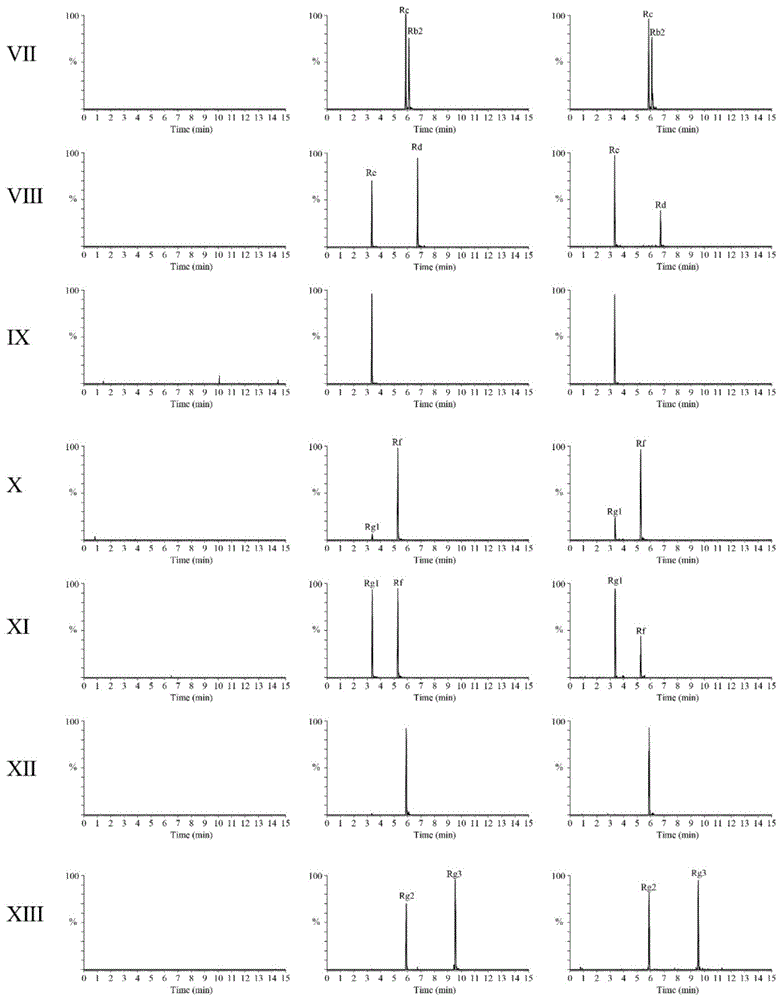
图1为混合对照品溶液和供试品溶液的质谱图。
其中,A空白溶液;B对照品溶液;C供试品溶液。
图中:Ⅰ毛蕊花糖苷;Ⅱ异毛蕊花糖苷;Ⅲ松果菊苷;Ⅳ焦地黄苯乙醇苷A1;Ⅴ人参皂苷Rb1;Ⅵ人参皂苷Rb2;Ⅶ人参皂苷Rc;Ⅷ人参皂苷Rd;Ⅸ人参皂苷Re;Ⅹ人参皂苷Rf;Ⅺ人参皂苷Rg1;Ⅻ人参皂苷Rg2;ⅩⅢ人参皂苷Rg3。
具体实施方式
为了使本领域的技术人员更好的理解本发明的技术方案,下面结合附图及具体实施方式对本发明所述技术方案作进一步的详细说明。
实施例1
1、实验仪器
ACQUITY UPLC超高效液相色谱仪(美国waters公司);Waters Xevo TQ-S三重四级杆质谱仪(美国waters公司);Waters UPLC ACQUITY HSS T3(1.8μm,2.1mm×100mm);AX–205十万分之一电子天平(瑞士Mettler Toledo公司);SB–5200DTS超声波清洗器(宁波新芝生物科技股份有限公司);VX-200涡旋混匀器(Labnet International公司);旋转蒸发仪(瑞士BUCHI公司,型号:R-220SE);冷冻干燥机(EYELA东京理化器械株式会社,型号:FDU-2100);高速离心机(德国Eppendorf股份公司,型号22331Hamburg);Milli–Q纯水仪(美国Millipore公司)。
2、标准品母液的配制及多反应检测(MRM)扫描方式的建立
精密称取毛蕊花糖苷、异毛蕊花糖苷、松果菊苷、焦地黄苯乙醇苷A1、人参皂苷Rb1、人参皂苷Rb2、人参皂苷Rc、人参皂苷Rd、人参皂苷Re、人参皂苷Rf、人参皂苷Rg1、人参皂苷Rg2、人参皂苷Rg3等对照品各1mg,加入50%乙醇配成1mg/mL的对照品溶液,取各对照品溶液适量逐级稀释至毛蕊花糖苷、异毛蕊花糖苷、松果菊苷、焦地黄苯乙醇苷A1、人参皂苷Rg2、人参皂苷Rg3 2μg/mL,人参皂苷Rb1、人参皂苷Rb2、人参皂苷Rc、人参皂苷Rd、人参皂苷Re、人参皂苷Rf、人参皂苷Rg1 20μg/mL。取适量20μg/mL的单一标准品母液,加50%乙醇逐级稀释至终浓度为200ng/mL溶液,待用。
基于QQQ质谱分析仪MRM扫描方式的建立过程:将200ng/mL的毛蕊花糖苷、异毛蕊花糖苷、松果菊苷、焦地黄苯乙醇苷A1、人参皂苷Rg2、人参皂苷Rg3,人参皂苷Rb1、人参皂苷Rb2、人参皂苷Rc、人参皂苷Rd、人参皂苷Re、人参皂苷Rf、人参皂苷Rg1单一标准品溶液逐个插入A调谐口,使针管尽可能在液面以下,点击Infurion,在ACQUITY UPLC SYSTEM下的XevoTQ-S MSDetector,设置分子式,正负离子模式,文件保存路径,进样体积等信息后,采集离子对信息。详细的离子对信息见表2。
3.标准曲线工作溶液的配制
通过50%的乙醇将13种活性成分中的毛蕊花糖苷、异毛蕊花糖苷、松果菊苷、焦地黄苯乙醇苷A1、人参皂苷Rg2和人参皂苷Rg3配制成线性范围为0.4-100ng/mL的标准曲线工作溶液;将人参皂苷Rb1、人参皂苷Rb2、人参皂苷Rc、人参皂苷Rd、人参皂苷Re、人参皂苷Rf、人参皂苷Rg1配制成线性范围为4-1000ng/mL的标准曲线工作溶液。
4、提取与配制供试品的方法
精密称取抗衰老片浸膏粉0.1g,加入50%乙醇10mL,超声提取90min,取适量提取液,12000g/min离心10min,经0.22μm微孔滤膜过滤,精密量取1mL续滤液于100mL容量瓶中,加50%乙醇定容至刻度线,混匀,即得100μg/mL的供试液。取适量供试液装进进样小瓶进行分析。
5、含量测定
采用所述检测体系对标准品进行检测,以各待测化合物的浓度为横坐标,待测化合物峰面积为纵坐标,建立各待测化合物的标准曲线
采用所述检测体系对供试液进行检测,每个条件平行制备三份样品,进LC-MS分析,测定供试品溶液中各成分的峰面积,并计算其含量,结果见表3。
色谱条件
色谱柱:Waters UPLC ACQUITY HSS T3(1.8μm,2.1mm×100mm);流动相:乙腈(A)—0.1%甲酸水溶液(B),梯度洗脱程序见表1,柱温40℃,流速0.3mL/min,进样体积4μL。梯度洗脱程序见表1。
表1梯度洗脱程序
质谱条件
离子源为电喷雾离子源(ESI),采用负离子扫描检测模式,负离子模式下:毛细管电压2.0kv,锥孔电压37V,脱溶剂温度350℃;正离子模式下毛细管电压3.0kv,锥孔电压30V,脱溶剂温度350℃,采用多重反应监测模式(MRM)。13个化合物的质谱分析条件见表2。
表2质谱分析条件参数
表3含量测定结果
实施例2
方法学结果考察
1、专属性
取空白溶液(50%乙醇)、混合对照品溶液和供试品溶液分别进样分析,记录其质谱图,如图1所示。
2、线性关系
对照品母液的配制
精密称取毛蕊花糖苷、异毛蕊花糖苷、松果菊苷、焦地黄苯乙醇苷A1、人参皂苷Rb1、人参皂苷Rb2、人参皂苷Rc、人参皂苷Rd、人参皂苷Re、人参皂苷Rf、人参皂苷Rg1、人参皂苷Rg2、人参皂苷Rg3等对照品各1mg,加入50%乙醇配成1mg/mL的对照品溶液,取各对照品溶液适量逐级稀释至毛蕊花糖苷、异毛蕊花糖苷、松果菊苷、焦地黄苯乙醇苷A1、人参皂苷Rg2、人参皂苷Rg3 2μg/mL,人参皂苷Rb1、人参皂苷Rb2、人参皂苷Rc、人参皂苷Rd、人参皂苷Re、人参皂苷Rf、人参皂苷Rg1 20μg/mL。
线性工作液的配制
取各标品稀释液50μL加350μL 50%乙醇涡旋混匀得含有毛蕊花糖苷、异毛蕊花糖苷、松果菊苷、焦地黄苯乙醇苷A1、人参皂苷Rg2、人参皂苷Rg3 100ng/mL,人参皂苷Rb1、人参皂苷Rb2、人参皂苷Rc、人参皂苷Rd、人参皂苷Re、人参皂苷Rf、人参皂苷Rg1 1000ng/mL的混合标准品母液,采用50%乙醇逐级稀释即得毛蕊花糖苷、异毛蕊花糖苷、松果菊苷、焦地黄苯乙醇苷A1、人参皂苷Rg2、人参皂苷Rg3的8个浓度点为100ng/mL、50ng/mL、20ng/mL、10ng/mL、4ng/mL、2ng/mL、0.8ng/mL、0.4ng/mL,人参皂苷Rb1、人参皂苷Rb2、人参皂苷Rc、人参皂苷Rd、人参皂苷Re、人参皂苷Rf、人参皂苷Rg1的8个浓度点为1000ng/mL、500ng/mL、200ng/mL、100ng/mL、40ng/mL、20ng/mL、8ng/mL、4ng/mL。
制备的系列混合线性工作液,以对照品浓度x(ng/mL)为横坐标,以各对照品化合物相应的峰面积y为纵坐标,绘制标准曲线,对标准曲线进行线性回归,得到线性回归方程及相关系数,结果如表4所示。
表4抗衰老片13个成分线性回归方程
由表4可知,毛蕊花糖苷、异毛蕊花糖苷、松果菊苷、焦地黄苯乙醇苷A1、人参皂苷Rb1、人参皂苷Rb2、人参皂苷Rc、人参皂苷Rd、人参皂苷Re、人参皂苷Rf、人参皂苷Rg1、人参皂苷Rg2和人参皂苷Rg3在各自浓度范围内线性关系良好。
3、定量限与检测限
将混合对照品溶液继续稀释进样分析,以信噪比为10时各成分的浓度作为其定量限;信噪比为3时各成分的浓度作为其检测限。结果表明,毛蕊花糖苷、异毛蕊花糖苷、松果菊苷、焦地黄苯乙醇苷A1、人参皂苷Rg2、人参皂苷Rg3、人参皂苷Rb1、人参皂苷Rb2、人参皂苷Rc、人参皂苷Rd、人参皂苷Re、人参皂苷Rf、人参皂苷Rg1的定量限分别为0.08ng/mL、0.08ng/mL、0.2ng/mL、0.2ng/mL、0.2ng/mL、0.2ng/mL、2ng/mL、0.8ng/mL、2ng/mL、2ng/mL、0.8ng/mL、0.8ng/mL、0.8ng/mL,检测限分别为0.02ng/mL、0.02ng/mL、0.06ng/mL、0.06ng/mL、0.06ng/mL、0.06ng/mL、0.6ng/mL、0.24ng/mL、0.6ng/mL、0.6ng/mL、0.24ng/mL、0.24ng/mL、0.24ng/mL。
4、准确度与精密度
分别取各线性工作液适量,用50%乙醇稀释,配制混合标准工作液低、中、高三个浓度的质控(QC)样品,平行制备3份,连续测定3天,按检测条件进行分析测定,通过随行标准曲线,根据样品色谱峰面积计算得到各QC样品的所测浓度,并计算批内和批间准确度与精密度,准确度用(RE%)表示,精密度用相对标准偏差(RSD%)表示,结果见表5。
表5
由表5可知,毛蕊花糖苷、异毛蕊花糖苷、松果菊苷、焦地黄苯乙醇苷A1、人参皂苷Rb1、人参皂苷Rb2、人参皂苷Rc、人参皂苷Rd、人参皂苷Re、人参皂苷Rf、人参皂苷Rg1、人参皂苷Rg2和人参皂苷Rg3的日内准确度和日间准确度RE值均小于等于4.78%,日内精密度和日间精密度RSD值均小于等于7.16%,表明该方法准确度良好,仪器精密度良好。
5、稳定性
分别取各线性工作液适量,用50%乙醇稀释,配制混合标准工作液低、中、高三个浓度的质控(QC)样品,置于10℃自动进样器,于0、2、4、8、12、24h按检测条件进行分析测定,通过随行标准曲线,根据样品色谱峰面积计算得到各QC样品的所测浓度及其RSD值,结果见表6。
表6
由表6可知,毛蕊花糖苷、异毛蕊花糖苷、松果菊苷、焦地黄苯乙醇苷A1、人参皂苷Rb1、人参皂苷Rb2、人参皂苷Rc、人参皂苷Rd、人参皂苷Re、人参皂苷Rf、人参皂苷Rg1、人参皂苷Rg2和人参皂苷Rg3的RSD均小于等于4.75%,表明在10℃样品盘温度下,各待测指标在24h内稳定性良好。
6、加样回收率
精密称取同一已知待测成分含量的抗衰老片浸膏粉供试品3份,每份约50mg,分别加入毛蕊花糖苷、异毛蕊花糖苷、松果菊苷、焦地黄苯乙醇苷A1、人参皂苷Rb1、人参皂苷Rb2、人参皂苷Rc、人参皂苷Rd、人参皂苷Re、人参皂苷Rf、人参皂苷Rg1、人参皂苷Rg2、人参皂苷Rg3对照品适量,按“2.1项”下方法制备供试品溶液,并稀释至各成分在线性范围内,计算加样回收率及其RSD值,结果见下表7。
表7
/>
/>
由表7可知,毛蕊花糖苷、异毛蕊花糖苷、松果菊苷、焦地黄苯乙醇苷A1、人参皂苷Rb1、人参皂苷Rb2、人参皂苷Rc、人参皂苷Rd、人参皂苷Re、人参皂苷Rf、人参皂苷Rg1、人参皂苷Rg2和人参皂苷Rg3的平均加样回收率在87.12%-97.35%之间,RSD值均小于等于8.03%,表明该方法加样回收率良好。
综上,上述抗衰老片的多成分定量分析方法基于UPLC/QQQ-MS技术,综合考虑抗衰老片所含的活性成分和特征成分,首次建立了抗衰老片中毛蕊花糖苷、异毛蕊花糖苷、松果菊苷、焦地黄苯乙醇苷A1、人参皂苷Rb1、人参皂苷Rb2、人参皂苷Rc、人参皂苷Rd、人参皂苷Re、人参皂苷Rf、人参皂苷Rg1、人参皂苷Rg2和人参皂苷Rg3 13种化学成分同时检测的方法,可实现全面和快速地控制抗衰老片的质量。尽管这13种成分含量各不相同,但通过配制不同稀释倍数的供试品溶液,可实现对这13种成分的快速检测,对该13个化学成分进行方法学考察及含量测定,方法学结果表明各成分的线性关系、准确度、精密度、稳定性和加样回收率等均符合2020年版《中国药典》9101分析方法验证指导原则。
以上所述实施例仅仅是对本发明的优选实施方式进行描述,并非对本发明的范围进行限定,在不脱离本发明设计精神的前提下,本领域普通工程技术人员对本发明的技术方案作出的各种变形和改进,均应落入本发明的权利要求书确定的保护范围内。
- 一种苗药红禾麻的多成分含量测定方法
- 一种荷丹片的多成分含量测定方法
- 一种正气片及其制备工艺与其中多成分定量定性的测定方法
- 一种正极极片活性物质的定量分析方法和用途
