SOCS3作为生物标志物在制备肝衰竭预后预测产品中的应用及检测试剂盒
文献发布时间:2024-04-18 19:59:31
技术领域
本发明涉及生物医学技术领域,尤其涉及SOCS3作为生物标志物在制备肝衰竭预后预测产品中的应用及检测试剂盒。
背景技术
公开该背景技术部分的信息仅仅旨在增加对本发明的总体背景的理解,而不必然被视为承认或以任何形式暗示该信息构成已经成为本领域一般技术人员所公知的现有技术。
肝衰竭中,慢加急性肝衰竭(acute-on-chronic liver failure,ACLF)是指在慢性肝病基础上,短期内出现急性肝功能失代偿和肝功能衰竭,临床主要表现为黄疸和凝血功能障碍,是严重危害人体健康的症候群。在我国,慢性乙型肝炎(CHB)病毒感染是肝衰竭发展的重要危险因素,乙肝相关慢加急性肝衰竭(acute-on-chronic hepatitis B liverfailure,ACHBLF)占ACLF的80%以上,且死亡率为50-90%。ACHBLF患者除了现存的肝脏疾病以外,还会出现肝外并发症,累及多系统。由于及时的临床干预可以阻止甚至逆转ACHBLF的进展,并且提高患者的生存率。所以,迫切需要及早诊断并且有效地评判ACHBLF患者的预后,延缓甚至逆转病情发展仍是医学难题。因此,当前急需找到能够正确评估ACHBLF患者的严重程度和有效预测其预后的生物标志物,建立有效的综合评估预后标准,制订有效的治疗方案具有重大意义。
研究表明,表观遗传学是仅影响基因表达与表型表现,但DNA序列却不发生任何变化,不改变遗传信息。其主要包括DNA甲基化、组蛋白修饰及非编码RNA的表达等现象。当前DNA甲基化是表观遗传学领域的重要研究方向,在肝衰竭发展过程中发挥重要作用,已逐渐成为医学领域的研究热点。DNA甲基化是指通过DNA甲基转移酶(DNMTs)催化作用,以S-腺苷蛋氨酸作为甲基的供体,将DNA鸟嘌呤(G)旁的胞嘧啶(C)(CpG二核苷酸)通过甲基化作用修饰成为5’-甲基胞嘧啶的过程。基因启动子区的甲基化可抑制相应基因的转录,从而影响细胞或组织特异性基因的表达。有研究表明,感染HBV的宿主存在CpG二核苷酸甲基化表达异常且DNMT表达活性变化的现象。
在肝衰竭发生过程中,肝脏组织受到多重打击,包括原发性免疫损伤、组织缺血缺氧和内毒素血症。免疫损伤和炎症反应在肝衰竭的发生发展过程中发挥重要作用。其中细胞因子大量激活并共同参与介导肝脏损伤,与肝衰竭过程中的免疫性损伤和疾病临床预后密切相关,并参与了肝细胞的凋亡及再生抑制,这直接影响了ACHBLF病情的恶化。细胞因子信号传导抑制分子3(SOCS3)作为SOCS家族中的一员,是SOCS家族中负性调控细胞因子的JAK/STAT信号转导通路作用最强的抑制蛋白之一,其基因启动子上含有JAK2/STAT3信号途径的结合位点。SOCS3作为JAK/STAT信号传导途径的特异性内源性抑制物,能够通过直接与JAK2位点和STAT3磷酸化络氨酸残基结合以及募集链接泛素化酶等途径抑制细胞因子的过度激活。因此,在肝衰竭的炎症损伤过程中,SOCS3在细胞因子信号转导途径中作为抑制性调控因子,参与细胞因子介导的炎症反应。
目前肝衰竭的预后预测方法常用MELD评分、SOFA评分等,仍有其局限性,许多肝衰竭新的预后标记物及评估体系正被研究。但由于肝衰竭的发病机制复杂,病情发展迅速,影响预后因素较多,肝衰竭的精准预测较为困难。因此,亟需一种可以评估肝衰竭预后的生物学标志物,实现对肝衰竭病情早期、灵敏和稳定的预测,以便及时、有效的治疗。
发明内容
本发明提供了SOCS3作为生物标志物在制备肝衰竭预后预测产品中的应用及检测试剂盒,通过检测样本中SOCS3的甲基化率,可以对受试者肝衰竭预后进行预测评估,提供更加及时的临床策略,从而辅助临床治疗,解决了现有技术中存在的问题。
本发明所采用的技术方案之一是:
检测样本中SOCS3的甲基化程度的试剂在制备肝衰竭预后预测或辅助预后预测产品中的应用。
进一步地,所述样本为包括但不限于外周血的受试者血液;当样本中SOCS3呈现高甲基化程度时,受试者肝衰竭预后不良。
进一步地,所述试剂为定量检测样本中SOCS3的甲基化率的试剂;当SOCS3甲基化率≥57.37%时,受试者肝衰竭预后不良,当SOCS3甲基化率<57.37%时,受试者肝衰竭预后良好;所述样本为外周血单个核细胞。
进一步地,所述试剂包括引物、探针、抗体、核酸芯片或蛋白质芯片。
进一步地,所述试剂包括甲基化特异性多连接依赖性探针扩或甲基化特异性PCR检测SOCS3甲基化率的试剂。
进一步地,所述试剂包括定量甲基化特异性PCR检测SOCS3基因甲基化程度的引物对。
进一步地,所述引物对的上游引物序列如SEQ ID NO.1所示,所述引物对的下游引物序列如SEQ ID N0.2所示;SOCS3-Taqman荧光探针序列如SEQ ID N0.3所示。
进一步地,SOCS3-Taqman荧光探针在5’端和3’端分别设置有荧光基团和淬灭基团。
进一步地,所述荧光基团为Fam,所述淬灭基团为BHQl。
进一步地,所述肝衰竭为乙肝相关肝衰竭;所述预后预测或辅助预后预测产品为监测或预测乙肝相关肝衰竭患者预后的产品。
进一步地,所述产品包括芯片或试剂盒;所述肝衰竭为慢加急性肝衰竭。
进一步地,所述慢加急性肝衰竭为乙肝相关慢加急性肝衰竭。
本发明所采用的技术方案之二是:
提供一种用于肝衰竭预后预测或辅助预后预测的检测试剂盒,所述试剂盒为特异性定量检测SOCS3甲基化率的甲基化特异性PCR试剂盒。
进一步的,所述甲基化特异性PCR试剂盒至少包括针对目的基因SOCS3启动子的甲基化特异性引物对和Taqman荧光探针;所述引物对的上游引物序列如SEQ ID NO.1所示,所述引物对的下游引物序列如SEQ ID N0.2所示;SOCS3-Taqman荧光探针序列如SEQ ID N0.3所示。
进一步的,所述甲基化特异性PCR试剂盒包括内参基因的特异性引物对和Taqman荧光探针;所述内参基因为GPADH;内参基因特异性引物对的上游引物序列如SEQ ID NO.4所示,内参基因特异性引物对的下游引物序列如SEQ ID NO.5所示;内参基因Taqman荧光探针序列如SEQ ID NO.6所示。
进一步地,GPADH-Taqman荧光探针在5’端和3’端分别设置有荧光基团和淬灭基团。
进一步地,所述检测试剂盒还包括阳性对照、阴性对照;所述阳性对照为重亚硫酸盐修饰的100%甲基化的人基因组DNA,所述阴性对照为水,优选为高压的双蒸馏水。
进一步地,所述检测试剂盒还包括提取血液(包括外周血)基因组DNA的试剂,对血液基因组DNA进行重亚硫酸盐修饰的试剂和预混PCR反应体系液等。
本发明所采用的技术方案之三是:
提供一种用于预测或辅助预测肝衰竭预后的系统,包括定量检测单元和分析单元;所述定量检测单元包括:采用如上所述检测试剂盒进行实时定量甲基化特异性聚合酶链式反应;所述分析单元包括对定量检测单元获得的结果进行分析,检测待测样本SOCS3的DNA甲基化率,判断受试者预后情况。
本发明的有益效果:
1、本发明提供的生物标志物SOCS3的甲基化程度能为肝衰竭预后预测评估提供依据,可辅助临床治疗,提供更及时的临床策略,消除了现有评分方法的局限性。
2、本发明以患者外周血单个核细胞中SOCS3的甲基化率的检测,能够检测到人体外周血单个核细胞中极微量的DNA,灵敏度高,特异性强。采用基于Taqman荧光探针的实时定量甲基化特异性PCR检测相较于甲基化特异性聚合酶链反应MSP-PCR定性检测方法,可更好的消除非特异性扩增,更好的避免DNA污染对结果的影响,确保检测结果的特异度。
3、本发明采用试剂盒组装,相较其他检测技术,具有取材简便、检测快速、结果精确等优点,可作为辅助临床医师对乙肝相关慢加急性肝衰患者预后的预测依据,具有深远的临床意义,适于大规模推广应用。利用试剂盒做到由采血到定量检测与肝衰竭预后相关的SOCS3基因甲基化程度的全过程,方便、快捷、适用,具有良好的实际应用之价值。
附图说明
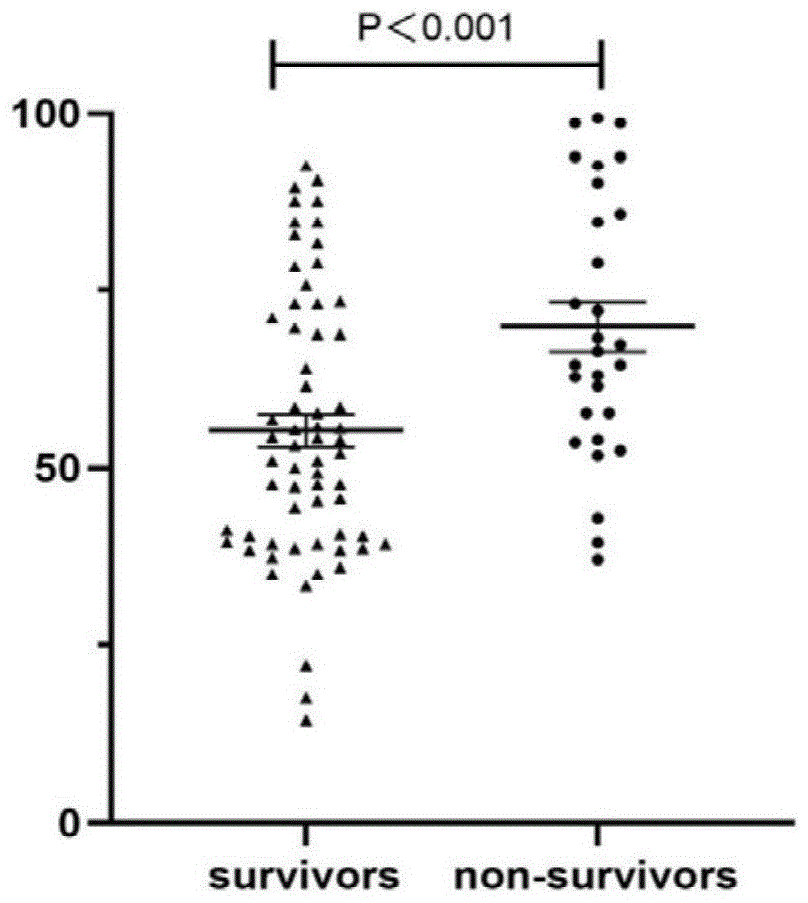
图1为本发明实施例乙肝相关慢加急性肝衰患者生存者与死亡者SOCS3基因启动子甲基化程度的比较;
图2为本发明实施例肝衰竭qPCR特异性检测结果示意图;
图3为本发明实施例肝衰竭患者SOCS3基因启动子甲基化率与血清MELD评分的受试者特征工作曲线。
其中,图1中,survivors:生存者;non-survivors:死亡者;
图2中,纵坐标表示校正荧光强度值,横坐标表示荧光定量扩增的循环数,ct值为达到阂值线所需要的循环数;SOCS3表示肝衰竭阳性样本甲基化检测结果;ACTB扩增表示样本含量正常;
图3中,MELD Score:终末期肝脏病模型评分;PMR:甲基化率;Sensitivity:敏感性;Specificity:特异性。
具体实施方式
为能清楚说明本方案的技术特点,下面通过具体实施方式,结合附图,对本发明进行详细阐述。本发明的范围并不限于下述实施例。本领域的专业人员能够理解,在不背离本发明的精神和范围的前提下,可以对本发明进行各种变化和修饰。
下述实施例中所涉及的仪器、试剂、材料等,若无特别说明,均为现有技术中已有的常规仪器、试剂、材料等,可通过正规商业途径获得。
实施例
一、实验方法
1.样本DNA的提取:
从肝衰竭患者抽取血液后,可以按照下列步骤提取患者的DNA,也可以用其他方法提取DNA。
(1)准备试剂:TRIzol试剂,乙醇,柠檬酸钠,氢氧化钠,三氯甲烷,Tris-EDTA溶液及HEPES,PBS溶液;
(2)离心收集细胞,每(5-10)×10
(3)每使用1ml的TRIzol加入0.3ml三氯甲烷,剧烈振荡30-60秒,室温放置2-5分钟;
(4)2-8℃条件下以12000×g离心力离心10-20分钟;样品分为三层:底层为红色有机相,上层为无色水相和一个中间层;
(5)移去上层水相,用乙醇沉淀中间层和有机相中的DNA,每使用1ml的TRIzol加0.3ml无水乙醇混匀,室温放置3-5分钟,2-8℃14800×g的离心力离心5分钟;
(6)移去上清,用含10%乙醇与PBS溶液的0.lmol/L柠檬酸钠洗涤DNA沉淀;每用1ml的TRIzol加入1ml的0.lmol/L柠檬酸钠(含10%乙醇与PBS溶液),室温震荡20-30分钟,停止震荡后静置5-15分钟,2-8℃14800×g的离心力离心5分钟,弃上清,重复五次;
(7)用75%乙醇再洗一遍DNA沉淀,每用1ml的TRIzol加入1.5-2ml的75%乙醇,室温震荡10-20分钟,2-8℃条件下14800×g离心5分钟,弃上清液,重复两次;
(8)用无水乙醇再洗一遍DNA沉淀,每用1ml的TRIzol加入1.5-2m1的无水乙醇,室温震荡10-20分钟,2-8℃条件下14800×g离心5分钟,弃上清液,重复三次;
(9)室温放置5-15分钟晾干DNA,用8mmol/L氢氧化钠溶解DNA;从10
2.重亚硫酸盐修饰
采用重亚硫酸盐对提取的基因组DNA进行甲基化修饰,将非甲基化的胞嘧啶转化为尿嘧啶,用作扩增模板,即:用重亚硫酸盐处理和转化提取的基因组DNA样品(采用甲基化DNA转化试剂盒EZ DNAMethylation-Gold Kit货号:D5005)。步骤如下:
(1)配制转化剂:将900μl水、300μl稀释缓冲液和50μl溶解缓冲液加入到转化剂管中,涡旋振动混匀;
(2)将130μl转化剂加入到20μl DNA样本中;
(3)将样本放在PCR仪中,98℃孵育10分钟,72℃孵育2.5小时,可4℃贮存;
(4)将600μl结合缓冲液加入离心柱中,置于收集管中;
(5)将来自第2步的样本加入装有结合缓冲液的离心柱中,盖紧管盖反复颠倒混匀一分钟;
(6)13400×g离心30秒,弃掉滤液;
(7)将100μl洗涤缓冲液加入上述离心柱中,13400×g离心30秒;
(8)将200μl脱磺化缓冲液加入离心柱中室温孵育15-20分钟,13400×g离心30秒;
(9)将200μl洗涤缓冲液加入离心柱中,13400×g离心30秒;再加入200μl洗涤缓冲液13400×g离心30秒,重复两次;
(10)将离心柱加入1.5ml EP管中,向离心柱中加入20μl洗脱缓冲液,最高速离心30秒以洗脱DNA;
(11)分光光度计法测DNA浓度和纯度,保存于-20℃。
3.实时定量甲基化特异性聚合酶链式反应
针对目的基因SOCS3启动子的甲基化特异性引物对和探针、内参基因的特异性引物对和Taqman荧光探针;实时定量甲基化特异性PCR方法对目的基因SOCS3启动子和内参基因进行扩增。
(1)引物设计:
SOCS3-上游引物:5'TTTAGGTTTATAGCGTTTGTATTTC 3'(SEQ ID NO.1);SOCS3-下游引物:5'TCATCTTATCCCCAAATAAACTATATAAT 3'(SEQ ID NO.2);
SOCS3-探针:5'Fam AATGTTATTGAGGTAGTTTTCGGGTGTTTT 3'BHQ1(SEQ ID NO.3);
GPADH-上游引物:5'TGGTGATGGAGGAGGTTTAGTAAGT 3'(SEQ ID NO.4);
GPADH-下游引物:5'AACCAATAAAACCTACTCCTCCCTTAAA 3'(SEQ ID NO.5);
GPADH-探针:5'Fam ACCACCACCCAACACACAATAACAAACACA'BHQl(SEQ ID NO.6)。
(2)实时定量甲基化特异性聚合酶链式反应检测SOCS3启动子甲基化程度:分别用目的基因SOCS3启动子及内参基因的甲基化特异性引物对和Taqman荧光探针序列探针,对处理过的DNA进行实时定量聚合酶链式(PCR)反应,其中阴性对照是将体系中DNA模板替换为双蒸馏水,阳性对照是将体系中DNA模板替换为100%甲基化的人基因组DNA,即从健康人白细胞中提取的DNA,通过CpG甲基化转移酶进行体外甲基化后,通过重亚硫酸盐修饰获得。
实时定量甲基化特异性PCR反应体系试剂如下表1:
表1
其中,上游引物和下游引物指的是:目的基因SOCS3和内参基因的特异性引物对。即:前述SOCS3-上游引物、SOCS3-下游引物;GPADH-上游引物、GPADH-下游引物;探针指的是目的基因SOCS3和内参基因的荧光探针,即:前述SOCS3-探针和GPADH探针。
(3)5×预混PCR反应体系为市场出售产品,其中含有热启动Taq聚合酶、三磷酸脱氧核糖核普、氯化镁、反应缓冲液PCR反应的增强剂、优化剂以及稳定剂。
(4)反应条件如下:加热至95℃,保温1-15分钟,共1个循环;加热至95℃,保温15秒,在58-64℃的温度下,退火40-60秒,35-60个循环。
4.数据计算
对待测样本进行实时定量结果分析,检测待测样本DNA甲基化程度。通过荧光PCR仪配套软件获得各PCR反应管的甲基化反应的阂值循环值(Cp值,每个反应管内的荧光信号到达设定阂值时所经历的循环数),按照以下计算公式计算得到SOCS3甲基化程度。
甲基化率=100%×2exp-[△Cp(样品SOCS3 Cp值-样品GPADH Cp值)-△Cp(阳性对照SOCS3 Cp值-阳性对照GPADH Cp值)]。
将甲基化率(PMR)≥57.37定义为阳性结果(甲基化),预测肝衰竭患者预后不良;PMR<57.37定义为阴性结果(非甲基化),预测肝衰竭患者预后良好。
二、比较乙肝相关肝衰竭生存者及死亡者SOCS3甲基化程度
1.收集乙肝相关肝衰竭患者病例
收集自2022年6月至2023年10月期间,在山东大学齐鲁医院肝病科收集93例乙肝相关慢加急性肝衰竭患者病例及预后情况,其中64例生存者,39例死亡者。病例情况如下(见表2):
表2:病例情况
2.收集上述患者外周血样本,进行如前实验方法的基因组DNA提取、DNA浓度测定、重亚硫酸盐转化、实时定量甲基化特异性PCR反应体系、反应条件及甲基化程度计算方法均与“一”中的相同。
3.结果分析
64例乙肝相关慢加急性肝衰竭生存者的SOCS3基因甲基化指数为52.67(四分位数间距31.13),显著低于乙肝相关肝衰竭死亡者的SOCS3基因甲基化指数66.47(四分位数间距32.09)(P<0.001),参见图1。
如图3所示,并结合下表3结果可知,SOCS3甲基化指数判断肝衰竭预后情况的受试者工作特征曲线(ROC)下面积为0.714(95%可信区间:0.604-0.823),敏感性为0.759,特异性为0.625,选取截断点为甲基化率57.37%,敏感性为0.759,特异性为0.625。且相较于MELD评分受试者工作特征曲线(ROC)下面积为0.688(95%可信区间:0.570-0.806),敏感性为0.793,特异性为0.516,说明本发明应用的SOCS3甲基化指数判断肝衰竭预后具备优异的敏感性和高特异性特点。
表3
综上,通过患者血液样本中SOCS3基因启动子在预后不良的乙肝相关肝衰竭患者中呈高甲基化状态,表明SOCS3基因启动子甲基化程度可以用来预测乙肝相关肝衰竭患者的预后,可为辅助医师临床预测和后续治疗效果的参考依据。
上述具体实施方式不能作为对本发明保护范围的限制,对于本技术领域的技术人员来说,对本发明实施方式所做出的任何替代改进或变换均落在本发明的保护范围内。
本发明未详述之处,均为本技术领域技术人员的公知技术。
