用于新型冠状病毒核酸检测的标准物质
文献发布时间:2024-04-18 19:59:31
技术领域
本发明涉及生物技术领域,特别涉及一种用于新型冠状病毒核酸检测的标准物质。
背景技术
新冠病毒是一种负链RNA病毒,RT-qPCR实时荧光定量是最常用的新冠病毒核酸检测方法。在荧光定量检测过程中,为确保样本采集、核酸提取、RT-qPCR扩增过程准确无误,需要使用核酸检测第三方质控品(属于标准物质种类)来质控荧光定量PCR的整个过程。
新城疫(Newcastle disease virus,NDV)病毒属于副粘病毒科Avulavirus属,是一种负链RNA病毒,其基因组包含N、P、M、F、HN和L六大基因以及非编码调控序列,目前,NDV病毒主要是作为重组疫苗的载体进行应用,未见作为质控品的载体的报道。
天然病毒能够最真实的模拟核酸提取和RT-qPCR过程,但由于新冠病毒潜在的传染危险性,需要在BSL-III级以上生物安全实验室获取,目前不会使用新冠病毒作为质控物质。市场上的新冠病毒核酸荧光定量检测的第三方质控品主要包括新冠核酸、慢病毒、噬菌体假病毒几大种类。但都存在一定不足,其中,新冠核酸不易制备,不能监控样本采集过程;慢病毒及噬菌体假病毒制备过程复杂,产能有限,且常常存在质粒残留,不能满足标准物质要求。
发明内容
本发明的目的在于解决现有质控品存在的上述问题,提供一种用于新型冠状病毒核酸检测的标准物质,不存在质粒DNA残留,能完整的质控从核酸提取到荧光定量PCR扩增的整个过程。
本发明解决其技术问题所采用的技术方案是:
一种用于新型冠状病毒核酸检测的标准物质,所述标准物质是以NDV病毒为载体,插入外源新冠病毒基因序列形成NDV重组病毒载体,NDV重组病毒载体经病毒拯救形成重组NDV病毒,随后利用灭活型病毒保存液将重组NDV病毒稀释5倍以上,测定拷贝数后形成标准物质。
标准物质为质控品或阳性参考品。
所述灭活型病毒保存液为市售产品,可以采用无胍盐灭活病毒保存液或者含胍盐灭活病毒保存液。
作为优选,插入的外源新冠病毒基因序列总长度在60bp-15000bp。可以插入不同长度的序列。
作为优选,插入的外源新冠病毒核苷酸序列见SEQ ID No.1所示。
作为优选,外源新冠病毒基因序列插入在NDV病毒载体的P基因和M基因之间、插入在NDV病毒载体的M基因和F基因之间或插入在NDV病毒载体的HN基因和L基因之间。
一种NDV重组病毒载体,以NDV病毒为载体,插入外源新冠病毒基因序列形成。
一种重组NDV病毒,是由NDV重组病毒载体经病毒拯救形成。本发明所形成的重组NDV病毒可以在鸡胚稳定连续传代至少5代。
重组NDV病毒的应用,将重组NDV病毒灭活后作为RNA类病毒核酸检测的标准物质的应用。
本发明的有益效果是:
(1)一次制备病毒后可连续传代生产,成本低廉;
(2)本发明的标准物质原液可以直接传代,在生产过程中无需质粒参与,不存在质粒DNA残留;
(3)能完整的质控从核酸提取到荧光定量PCR扩增的整个过程。
附图说明
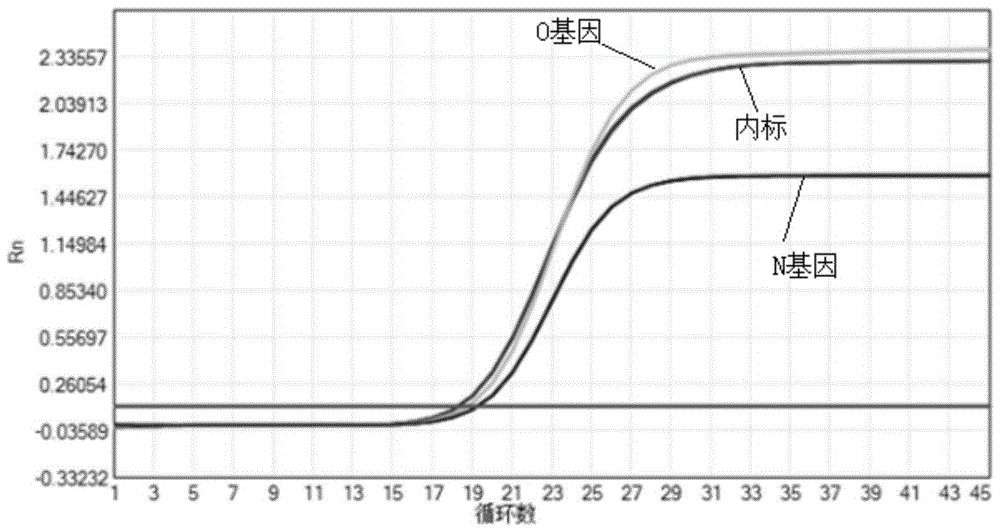
图1是稀释到10
图2是稀释到10
图3是稀释到10
图4是稀释到10
图5是稀释到10
图6是稀释到10
具体实施方式
下面通过具体实施例,对本发明的技术方案作进一步的具体说明。
本发明中,若非特指,所采用的原料和设备等均可从市场购得或是本领域常用的。下述实施例中的方法,如无特别说明,均为本领域的常规方法。
在本发明中,NDV病毒优选新城疫LaSota病毒株,新城疫LaSota病毒株是在申请号202010542477.8、名称为一种重组新城疫病毒载体新型冠状病毒疫苗候选株及其构建方法和应用的专利公开的新城疫LaSota病毒株。
一种用于新型冠状病毒核酸检测的标准物质(质控品/阳性参考品),所述标准物质是以NDV病毒为载体,插入外源新冠病毒基因序列形成NDV重组病毒载体,NDV重组病毒载体经病毒拯救形成重组NDV病毒,随后利用可灭活病毒保存液将重组NDV病毒稀释,测定拷贝数后形成标准物质。
本发明插入的外源新冠病毒基因序列总长度在60bp-15000bp;插入的外源新冠病毒基因核苷酸序列见SEQ ID No.1所示。
本发明中,外源新冠病毒基因序列可插入在NDV病毒载体的P基因和M基因之间、可插入在NDV病毒载体的M基因和F基因之间或可插入在NDV病毒载体的HN基因和L基因之间。
实施例1NDV为载体的新冠质控品构建
1.1重组NDV载体的构建
获取SARS-COV-2的基因组序列(GenBank序列号NC_045512.2),选择N基因、E基因、orf1ab基因的部分序列,以及人源RPP30基因的一部分通过杭州擎科生物有限公司进行基因合成,合成外源新冠病毒基因序列坐标为:Gene Bank No NC_045512.2(2082-2147,7959-8043,9093-9238,12577-15910,20880-20967,26245-26472,28274-29530),人源RNase P基因序列坐标为:Gene Bank No NM_006413(28-92)。设计引物(表1),按照
表1引物序列表
。
1.2病毒拯救
将以上重组NDV-Allin病毒载体和病毒拯救辅助质粒pCI-NP、pCI-P和pCI-L,经Nanodrop测定质粒浓度后,转染BHK21-T7细胞(已公开在CN112011521A)。转染后72h,反复冻融细胞3次,并将混合物接种9~11日龄SPF鸡胚,0.2~0.3mL/胚,37℃培养24h。弃去24h内的死胚,收获72h内存活的鸡胚尿囊液并测量血凝价。将有血凝价且存活的P1代鸡胚尿囊液离心后分装,RT-PCR测序确保插入序列完全正确。为保证尿囊液病毒无质粒残留,将病毒稀释1000倍后,继续接种9~11日龄SPF鸡胚,收获72h后的P2代鸡胚尿囊液,混匀后测定血凝价,冻存于-80℃冰箱保存待用。所收获病毒血凝价一般大于6。
1.3验证灭活效果
取NDV-Allin重组病毒原液,用灭活型病毒保存液分别稀释5倍和10倍,取0.1~0.2mL接毒9~11日龄SPF鸡胚,每种浓度接三只,72h后,收获鸡胚尿囊液测量血凝价。检测结果为均无血凝,可见病毒在用灭活型病毒保护液稀释5倍时候即被灭活,实际生产会使用更高倍数的稀释,确保了最终产品的安全性。
1.4荧光定量检测梯度稀释重组病毒原液
使用灭活型病毒保存液将NDV-Allin病毒原液梯度稀释6个数量级(若收获病毒血凝价高,则可以稀释到更高的数量级),分别随机抽取稀释后不同浓度的病毒原液各6管,按照Axygen体液病毒DNA/RNA提取试剂盒说明书提取核酸,按照达安生物新型冠状病毒核酸检测试剂盒说明书操作对提取核酸样本进行检测。检测结果如表2和图1-图6,由扩增曲线和循环数CV值可知,本重组病毒经过稀释后浓度高度均一,同一批产品批内差异极小。有成为优秀标准物质潜能。
表2不同稀释度灭活重组病毒扩增结果
。
1.5质粒残留验证
按照Axygen体液病毒DNA/RNA提取试剂盒说明书提取稀释了10
表3
。
1.6数字PCR定量拷贝数浓度
将以上按照QIAamp Viral RNA Mini Kit说明书,取稀释了10
根据仪器输出结果计算平均拷贝数浓度,结果如表4。由结果可知,我们的产品在稀释到10
表4
。
1.7稳定性研究
将稀释到10
表5
表6
。
实施例2NDV为载体的新冠质控品构建
本实施例与实施例1的1.1和1.2节不同之处在于:将合成的基因片段通过同源重组方式插入到NDV载体的M基因和F基因之间,形成重组NDV-Allin病毒载体。其它同实施例1。
实施例3NDV为载体的新冠质控品构建
本实施例与实施例1的1.1和1.2节不同之处在于:将合成的基因片段通过同源重组方式插入到NDV载体的HN基因和L基因之间,形成重组NDV-Allin病毒载体。
实施例4验证是否可质控核酸提取过程
4.1主要实验材料和仪器
现有产品1(新型冠状病毒核酸标准品,市售),现有产品2(新型冠状病毒假病毒非定值质控品,市售),现有产品3(新型冠状病毒假病毒第三方质控品,市售),本发明实施例1生产的质控品(病毒拷贝数浓度1000copies/ml),Axygen体液病毒DNA/RNA提取试剂盒,达安生物新型冠状病毒核酸检测试剂盒(荧光PCR法),宏石SLAN-96P荧光定量PCR扩增仪。
4.2实验方法
取200μl质控品,按照Axygen体液病毒DNA/RNA提取试剂盒说明书要求,提取以上新冠质控品核酸样品,最终使用60μl TE Buffer进行洗脱。将提取到的新冠质控品核酸样品以及未经过提取的新冠质控品样品按照达安生物新型冠状病毒核酸检测试剂盒(荧光PCR法)说明书要求配置反应体系和设置扩增程序,并进行PCR反应。
4.3实验结果
4.3.1现有产品2分别参与提取和不提取过程扩增结果
。
4.3.2现有产品3分别参与提取和不提取过程扩增结果
。
4.3.3现有产品1分别参与提取和不提取过程扩增结果
。
4.3.4本发明分别参与提取和不提取过程扩增结果
。
4.4结果汇总
。
根据以上实验结果可知,现有产品1含有质粒残留;现有产品1-3均存在不提取核酸可以扩增情况。提取各个厂家的质控品核酸样品,使用达安生物新型冠状病毒核酸检测试剂盒(荧光PCR法)进行扩增,扩增结果显示,本发明新冠质控品N基因,orf1ab基因以及内标基因的扩增CT值更加接近,在相同扩增效率情况下,表明各基因拷贝数浓度水平相当。综合以上,认为本发明质控品可以更加真实的质控新型冠状病毒核酸检测从样本核酸提取到PCR扩增的整个流程。
以上所述的实施例只是本发明的一种较佳的方案,并非对本发明作任何形式上的限制,在不超出权利要求所记载的技术方案的前提下还有其它的变体及改型。
