含季鏻盐结构的哒嗪酮衍生物及其制备方法和应用
文献发布时间:2024-04-18 20:00:50
技术领域
本发明属于创新药物研究领域,特别涉及含季鏻盐结构的哒嗪酮衍生物及其制备方法和应用。
背景技术
多聚腺苷二磷酸核糖聚合酶-1(Poly ADP-ribose polymerase-1,PARP-1)是一种参与损伤DNA修复的酶,广泛分布于细胞核和线粒体中。有研究表明,多种原因导致神经细胞线粒体中PARP-1活性增加时,线粒体的损伤会加剧,会加速细胞死亡,抑制线粒体中PARP-1的活性可能起到保护线粒体继而保护神经细胞的作用,具有重要的临床价值,特别是对阿尔兹海默症等神经退行性的治疗可能有重要意义。
AZD2461(结构如下所示)是一种公开报道的PARP-1强抑制剂,哒嗪酮是其发挥PARP-1抑制活性的主要结构,但是,其不具有线粒体靶向性。本发明对其进行化学结构改造,通过酯键引入具有靶向细胞线粒体的季鏻盐结构,所得化合物有望进入受损伤神经细胞的线粒体中,抑制PARP-1活性,改善线粒体功能,减少细胞损伤。因此,该类化合物可应用于治疗此类神经细胞损伤疾病。本发明正是基于此进行的研究。
发明内容
本发明提供了含季鏻盐结构的哒嗪酮衍生物及其制备方法和应用,化合物的制备所需原料易得,反应条件温和,操作简单,制备成本低。
为达到上述目的,本发明采用以下技术方案:
本发明提供了含季鏻盐结构的哒嗪酮衍生物,所述哒嗪酮衍生物具有如式(I)表示的结构:
其中,n=1-4。
优选地,n=4。
本发明还提供了上述哒嗪酮衍生物的制备方法,其特征在于:所述制备方法通过以下步骤实现:
式(IV)中,n=1-4。
在以上技术方案中,所述制备方法的具体步骤为:
步骤(1),将式(II)所示化合物加入二氯甲烷中,搅拌呈混悬液,滴加DIPEA,在冰浴条件下加入HATU,搅拌反应,再向反应液中加入4-羟基哌啶,撤冰浴,室温搅拌,经硅胶柱层析分离得到式(III)所示化合物;
步骤(2),式(III)所示化合物再分别与3-溴丙酰氯、4-溴丁酰氯、5-溴戊酰氯和6-溴己酰氯发生酯化反应,得到式(IV)所示化合物;
步骤(3),式(IV)所示化合物再与三苯基膦加热反应,得到式(I)所示化合物。
本发明还提供了上述哒嗪酮衍生物在制备治疗神经细胞损伤疾病的药物中的应用。
优选地,所述神经细胞损伤疾病包括但不限于阿尔兹海默症。
本发明还提供了上述哒嗪酮衍生物应用于增加D-半乳糖损伤的PC12细胞存活率。
本发明的有益效果在于:
本发明以AZD2461(通式II化合物)为先导化合物,合成制备了4种以通式I为代表的化合物,通式中n=1-4。化合物I的三苯基季鏻盐结构将化合物定向地富集到细胞线粒体中,再通过酯酶作用断开酯键,释放具有PARP-1抑制活性的AZD2461去甲基化产物(4-[4-氟-3-[(4-羟基哌啶-1-基)羰基]苄基]酞嗪-1(2H)-酮)从而保护受损伤的神经细胞。通过D-半乳糖诱导的PC12神经细胞损伤模型证实,其中化合物(n=4)能显著性减少D-半乳糖诱导的PC12细胞死亡,对损伤的PC12神经细胞就有保护作用。本发明化合物I的制备所需原料易得,反应条件温和,操作简单,制备成本低。
附图说明
图1是化合物I
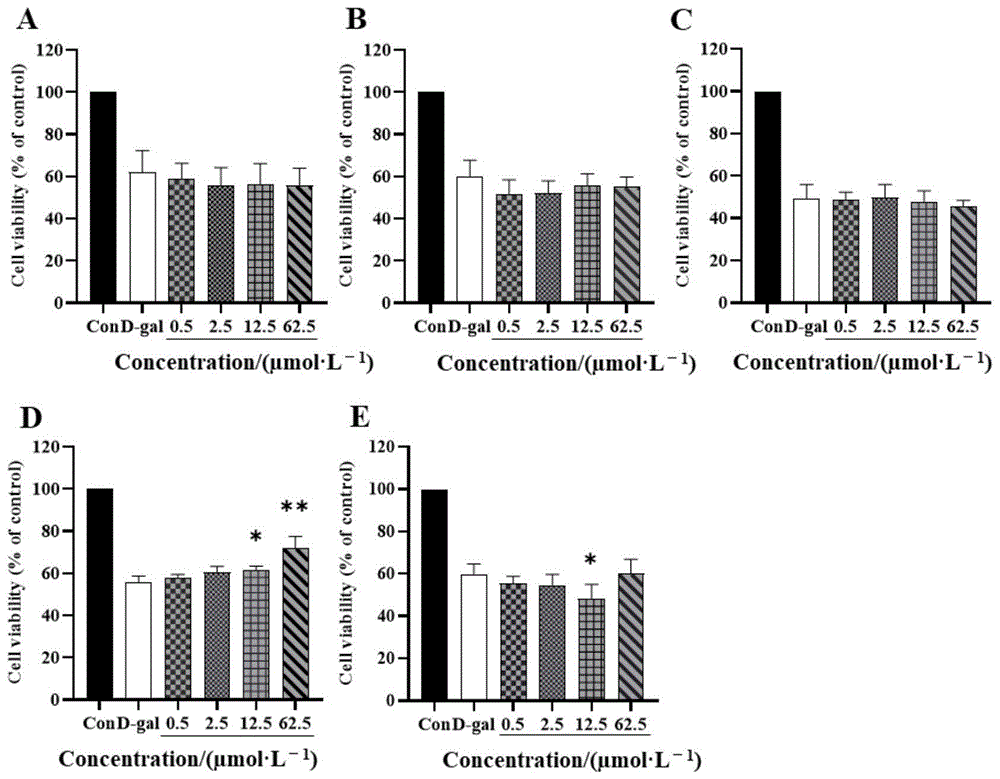
图A-E:不同浓度的化合物I
具体实施方式
为了更好地说明本发明的目的、技术发明和优点,下面将结合具体实施例对本发明做进一步描述。本发明可以以许多不同的形式实施,而不应该被理解为限于在此阐述的实施例。相反,提供这些实施例,使得本公开将是彻底和完整的,并且将把本发明的构思充分传达给本领域技术人员,本发明将仅由权利要求来限定。
本发明提供了含季鏻盐结构的哒嗪酮衍生物,哒嗪酮衍生物具有如式(I)表示的结构:
其中,n=1-4。
上述哒嗪酮衍生物的制备方法通过以下步骤实现:
式(IV)和式(I)中,n=1-4,且两式中n相等。
作为其中一种实施例,上述哒嗪酮衍生物的制备方法具体为:将1.0g(3.4mmol)2-氟-5-[(4-氧代-3,4-二氢酞嗪-1-基)甲基]苯甲酸(II)加入30mL二氯甲烷中,搅拌呈混悬液,滴加N,N-二异丙基乙胺(DIPEA)0.7g(5.0mmol),在冰浴条件下加入2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(HATU)1.9g(5.0mmol),搅拌反应10min,再向反应液中加入4-羟基哌啶0.5g(5.0mmol),撤冰浴,室温搅拌18h,经硅胶柱层析分离得到化合物III。化合物III再分别与3-溴丙酰氯、4-溴丁酰氯、5-溴戊酰氯和6-溴己酰氯发生酯化反应,得到化合物IV,化合物IV再与三苯基膦加热反应,得到化合物I。
将化合物I用PC12细胞进行药理活性试验测试。PC12细胞(Pheochromocytomacells)为大鼠肾上腺髓质嗜铬细胞瘤克隆化的细胞株,系神经峭源性,具可传代特点,广泛应用于神经生理和神经药理学研究。60mmol/L的D-半乳糖能造成PC12细胞氧化应激损伤,线粒体功能紊乱,最终可导致细胞死亡。本发明用不同浓度(0.5μmol/L、2.5μmol/L、12.5μmol/L及62.5μmol/L)的化合物I和AZD2461预先加入PC12细胞处理2h后,再加入60mmol/L的D-半乳糖,结果发现化合物I
实施例1
3-溴化三苯基膦基丙酸-{[2-氟-5-[(3,4-二氢-4-氧代-1-酞嗪基)甲基]苯甲酰基]哌啶-4-醇}酯(I
步骤一:4-[4-氟-3-[(4-羟基哌啶-1-基)羰基]苄基]酞嗪-1(2H)-酮(III)的合成
在100mL圆底烧瓶中加入2-氟-5-[(4-氧代-3,4-二氢酞嗪-1-基)甲基]苯甲酸(II)1.0g(3.4mmol)和30mL二氯甲烷,搅拌呈混悬液,滴加DIPEA 0.7g(5.0mmol),在冰浴条件下加入HATU 1.9g(5.0mmol),搅拌反应10min,再向反应液中加入4-羟基哌啶0.5g(5.0mmol),撤冰浴,室温搅拌18h。反应结束,用30mL×3水洗涤,无水硫酸钠干燥,浓缩,用乙酸乙酯/石油醚(v/v)=5:1作为流动相进行柱层析,得白色固体0.5g,产率39%,熔点:151.8-152.3℃。
步骤二:1-{2-氟-5-[(3,4-二氢-4-氧代-1-酞嗪基)甲基]苯甲酰基}哌啶-4-基-3-溴丙酸酯(IV
在25mL圆底烧瓶中加入化合物III 1.0g(2.6mmol),10mL二氯甲烷,搅拌至完全溶解,滴加0.3mL(3.9mmol)吡啶和0.4mL(3.9mmol)3-溴丙酰氯,室温反应6h,TLC跟踪反应。反应结束后,用10mL×3水洗涤,无水硫酸钠干燥,浓缩,用乙酸乙酯/石油醚(v/v)=1:1作为流动相进行硅胶柱柱层析,得白色固体0.8g,产率51%,熔点:161.9-163.1℃。
步骤三:在25mL圆底烧瓶中加入三苯基膦3.0g(11.4mmol)和1.9mmol化合物IV
实施例2
4-溴化三苯基膦基丁酸-{[2-氟-5-[(3,4-二氢-4-氧代-1-酞嗪基)甲基]苯甲酰基]哌啶-4-醇}酯(I
步骤一:同实施例1的步骤一。
步骤二:1-{2-氟-5-[(3,4-二氢-4-氧代-1-酞嗪基)甲基]苯甲酰基}哌啶-4-基-4-溴丁酯(IV
在25mL圆底烧瓶中加入化合物III 1.0g(2.6mmol),10mL二氯甲烷,搅拌至完全溶解,滴加0.3mL(3.9mmol)吡啶和0.4mL(3.9mmol)4-溴丁酰氯,室温反应6h,TLC跟踪反应。反应结束后,用10mL×3水洗涤,无水硫酸钠干燥,浓缩,用乙酸乙酯/石油醚(v/v)=1:1作为流动相进行硅胶柱柱层析,得淡黄色固体,产率46%,熔点:137.2-138.7℃。
步骤三:在25mL圆底烧瓶中加入三苯基膦3.0g(11.4mmol)和1.9mmol化合物IV
实施例3
5-溴化三苯基膦基戊酸-{[2-氟-5-[(3,4-二氢-4-氧代-1-酞嗪基)甲基]苯甲酰基]哌啶-4-醇}酯(I
步骤一:同实施例1的步骤一。
步骤二:1-{2-氟-5-[(3,4-二氢-4-氧代-1-酞嗪基)甲基]苯甲酰基}哌啶-4-基-5-溴戊酯(IV
在25mL圆底烧瓶中加入化合物III 1.0g(2.6mmol),10mL二氯甲烷,搅拌至完全溶解,滴加0.3mL(3.9mmol)吡啶和0.4mL(3.9mmol)5-溴戊酰氯,室温反应6h,TLC跟踪反应。反应结束后,用10mL×3水洗涤,无水硫酸钠干燥,浓缩,用乙酸乙酯/石油醚(v/v)=1:1作为流动相进行硅胶柱柱层析,得淡黄色固体,产率43%,熔点:116.8-118.6℃。
步骤三:在25mL圆底烧瓶中加入三苯基膦3.0g(11.4mmol)和1.9mmol化合物IV
实施例4
6-溴化三苯基膦基己酸-{[2-氟-5-[(3,4-二氢-4-氧代-1-酞嗪基)甲基]苯甲酰基]哌啶-4-醇}酯(I
步骤一:同实施例1的步骤一。
步骤二:1-{2-氟-5-[(3,4-二氢-4-氧代-1-酞嗪基)甲基]苯甲酰基}哌啶-4-基-6-溴己酸酯(IV
在25mL圆底烧瓶中加入化合物III 1.0g(2.6mmol),10mL二氯甲烷,搅拌至完全溶解,滴加0.3mL(3.9mmol)吡啶和0.4mL(3.9mmol)6-溴己酰氯,室温反应6h,TLC跟踪反应。反应结束后,用10mL×3水洗涤,无水硫酸钠干燥,浓缩,用乙酸乙酯/石油醚(v/v)=1:1作为流动相进行硅胶柱柱层析,得淡黄色固体,产率为40%,熔点:129.4-131.2℃。
步骤三:在25mL圆底烧瓶中加入三苯基膦3.0g(11.4mmol)和1.9mmol化合物IV
实施例5
以下是本发明代表化合物对D-半乳糖诱导的PC12神经细胞损伤模型的保护实验及实验结果:
取传代三次以上的PC12细胞,经0.25%胰蛋白酶消化后,于细胞计数板中进行计数。根据计数结果,向其中加入含有10%胎牛血清的完全培养基制备成细胞悬液,调整细胞密度为3×10
空白组为不含PC12细胞、待测化合物和D-半乳糖的含10%胎牛血清的完全培养基;
正常对照组(CON组,图1)用含10%胎牛血清的完全培养基培养PC12细胞;
模型组细胞(D-gal组,图1)用含60mmol/L D-半乳糖的完全培养基培养PC12细胞;
药物组的PC12细胞经终浓度分别为0.5μmol/L、2.5μmol/L、12.5μmol/L及62.5μmol/L的待测化合物分别预处理2h,随后加入浓度为60μmol/L的含D-半乳糖的完全培养基处理PC12细胞。每组药物浓度设置6个复孔,将其放置于细胞培养箱(37℃,95%O
在给药后的PC12细胞中,每孔避光加入用完全培养基稀释的浓度为5mg/mL的MTT20μL,在细胞培养箱(37℃,95%O
结果如图1所示,与模型组相比,给药浓度为0.5-62.5μmol/L时,化合物I
本发明的药理实验结果表明化合物I
显然,上述实施例仅仅是为清楚地说明所作的举例,而并非对实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。而由此所引伸出的显而易见的变化或变动仍处于本发明创造的保护范围之中。
