用于预测肿瘤进展及预后的基因标志物组合、试剂盒及系统
文献发布时间:2024-04-18 20:01:55
相关专利
本申请是申请号为2022110946885,申请日为2022年09月03日,发明名称为“用于预测肿瘤进展及预后的基因标志物组合、试剂盒及系统”的中国发明专利申请的分案申请。
技术领域
本发明属于医学分子生物学领域,具体地,涉及用于预测肿瘤进展及预后的基因标志物组合、试剂盒及系统。
背景技术
胶质母细胞瘤(Glioblastoma,GBM)是成人中最常见的侵入性脑肿瘤。由于肿瘤的恶性进展,改善GBM的预后具有巨大的挑战性。标准治疗方案下,GBM患者的中位生存期约为15个月,然而,大多数患者在初次治疗后会在十个月内快速复发。
当前,已有技术构建了几种方法模型来探索GBM的发病和进展。例如,Ozawa等人分析了人类GBM数据,发现染色体改变可能是GBM的起因(Ozawa,Tatsuya,et al."Most humannon-GCIMP glioblastoma subtypes evolve from a common proneural-like precursorglioma."Cancer cell 26.2(2014):288-300.)。还有一些技术研究在纵向样本模型上探索了GBM的时空变化。GBM的进展是从成对的原发性和复发性样本中预测的,以上技术显示了由治疗驱动的GBM患者的基因组特征。
尽管已有技术加深了本领域对GBM进展的认知,增进了对治疗失败的理解,但其主要基于治疗后的基因组变化。总体来讲,目前仍缺少预测自然疾病进展过程中肿瘤细胞如何进展的合适模型和方法。
发明内容
为了解决上述技术问题中的至少一个,本发明通过获得肿瘤组织的RNA样本,通过全转录组高通量测序获得转录组测序数据,对下机数据进行预处理后,将数据对比至人类参考基因组上,进行表达定量分析,获得表达谱信息。进一步利用表达谱数据获得了能够用于预测肿瘤进展和/或预后的基因标志物组合。通过对多种肿瘤样本进行同样的分析,意外地获得了适用于多种肿瘤进展和/或预后的基因标志物组合,从而完成了本发明。
在本发明中,所述高通量全转录组测序(whole transcriptome resequencing)指一次对几十万到几百万条RNA分子进行序列测定。转录组测序的研究对象为特定细胞在某一功能状态下所能转录出来的所有RNA的总和,主要包括mRNA和非编码RNA。转录组研究是基因功能及结构研究的基础和出发点,通过新一代高通量测序,能够全面快速地获得某一物种特定组织或器官在某一状态下的几乎所有转录本序列信息,已广泛应用于基础研究、临床诊断和药物研发等领域。
在本发明中,所述基因表达谱(gene expression profile)指构建处于某一特定状态下的细胞或组织的非偏性cDNA文库,通过大规模的cDNA测序,收集cDNA序列片段、定性、定量分析其mRNA群体组成,从而描绘该特定细胞或组织在特定状态下的基因表达种类和丰度信息,这样编制成的数据表就称为基因表达谱。
在本发明中,高通量测序获得的reads都是300-500bp的序列片段,无法直接进行下游分析。因此,需要将mRNA测序得到的reads与人类参考基因组进行比较,由此确定mRNA的序列片段来源于参考基因组上的哪个基因。
在本发明中,所述人类参考基因组是指2001年2月12日,由6国的科学家共同参与的国际人类基因组公布了人类基因组图谱及初步分析结果。目前,参考序列可以是人类基因组hg38、hg19或其它版本的序列。在本发明的实施方案中,所述人类参考基因组是指hg19。
本发明的采用的技术方案如下:
本发明第一方面提供一种基因标志物组合,所述基因标志物组合包括S100A10、FOSL2、SPP1、CAV1、ANXA1、VIM、CD44、SERPINH1、LGALS3、CEBPB、ATF5和LGALS1中的至少一个基因。
在本发明中,术语“基因标志物”、“基因标记”和“特征分子”具有等同的含义,均指与肿瘤进展和/或预后有关的基因。
S100A10(S100 Calcium Binding Protein A10,S100A10)基因编码的蛋白质是含有2个EF手钙结合基序的S100蛋白质家族的成员之一。S100钙结合蛋白位于多种细胞的细胞质和/或细胞核中,并参与许多细胞过程的调节,例如细胞周期进程和分化。S100基因包括至少13个成员,它们以簇的形式位于染色体1q21上。
FOSL2(FOS Like 2,AP-1Transcription Factor Subunit,FOSL2)是Fos基因家族成员,其余成员包括:FOS、FOSB和FOSL1。这些基因编码的亮氨酸拉链蛋白可以与JUN家族的蛋白质二聚化,从而形成转录因子复合物AP-1。因此,FOS蛋白被认为是细胞增殖、分化和转化的调节剂。
SPP1(Secreted Phosphoprotein 1)基因编码的蛋白质参与破骨细胞与矿化骨基质的附着。SPP1蛋白被分泌并以高亲和力结合羟基磷灰石。破骨细胞玻连蛋白受体存在于细胞膜中,可能参与与SPP1蛋白的结合。SPP1蛋白也是一种上调干扰素-γ和白细胞介素-12表达的细胞因子。
CAV1(Caveolin 1)基因编码的支架蛋白是在大多数细胞类型中发现的细胞膜穴样膜的主要成分。CAV1蛋白将整合素亚基与酪氨酸激酶FYN连接起来,这是将整合素与Ras-ERK途径偶联并促进细胞周期进程的起始步骤。CAV1基因是肿瘤抑制基因候选者和Ras-p42/44丝裂原活化激酶级联的负调节剂。CAV1和CAV2在7号染色体上彼此相邻,并表达形成稳定异源寡聚体复合物的共定位蛋白。
ANXA1(Annexin A1)基因编码一种与磷脂结合的膜定位蛋白。ANXA1蛋白抑制磷脂酶A2并具有抗炎活性。
VIM(Vimentin)基因编码一种III型中间丝蛋白。中间丝与微管和肌动蛋白微丝一起构成细胞骨架。VIM蛋白负责维持细胞形状和细胞质的完整性,并稳定细胞骨架相互作用。VIM蛋白参与神经发生和胆固醇转运,并作为许多其他关键蛋白质的组织者发挥作用,这些蛋白质参与细胞附着、迁移和信号传导。
CD44(CD44 Molecule)基因编码的蛋白质是一种细胞表面糖蛋白,参与细胞间相互作用、细胞粘附和迁移。CD44蛋白是透明质酸(HA)的受体,还可以与其他配体相互作用,例如骨桥蛋白、胶原蛋白和基质金属蛋白酶(MMP)。CD44蛋白参与多种细胞功能,包括淋巴细胞活化、再循环和归巢、造血和肿瘤转移。
SERPINH1(Serpin Family H Member 1)基因编码丝氨酸蛋白酶抑制剂中丝氨酸超家族的成员之一。SERPINH1蛋白定位于内质网,并作为胶原蛋白特异性分子伴侣在胶原蛋白生物合成中发挥作用。SERPINH1基因的核苷酸多态性可能与胎膜早破引起的早产有关,该基因的假基因位于9号染色体的短臂上。
LGALS3(Galectin 3)基因编码碳水化合物结合蛋白的半乳凝素家族成员之一。该蛋白质家族的成员对β-半乳糖苷具有亲和力。LGALS3蛋白的特征在于N末端富含脯氨酸的串联重复结构域和单个C末端碳水化合物识别结构域。LGALS3蛋白可以通过N端结构域自缔合,使其与多价糖配体结合。LGALS3蛋白定位于细胞外基质、细胞质和细胞核,在许多细胞功能中发挥作用,包括细胞凋亡、先天免疫、细胞粘附和T细胞调节。
CEBPB(CCAAT Enhancer Binding Protein Beta)是一种无内含子的基因,其编码的转录因子包含一个基本的亮氨酸拉链(bZIP)结构域。CEBPB蛋白作为同型二聚体发挥作用,但也可以与CCAAT/增强子结合蛋白α、δ和γ形成异二聚体。CEBPB蛋白的活性在调节涉及免疫和炎症反应的基因以及其他过程中很重要。
ATF5(Activating Transcription Factor 5)基因启用多种功能,包括DNA结合转录激活剂活性、RNA聚合酶II特异性;RNA聚合酶II转录调控区序列特异性DNA结合活性和微管蛋白结合活性。并且参与多个过程,包括脂肪细胞分化;细胞周期过程的调节和转录调控。
LGALS1(Galectin 1)基因编码碳水化合物结合蛋白的半乳凝素家族成员之一。LGALS1蛋白可以作为调节细胞增殖的自分泌负生长因子。
上述基因标志物组合中的各基因在预测肿瘤进展和/或预后中均具有一定的价值,本领域技术人员可以选择任一组合,例如其中任意1个基因、任意2个基因、任意3个基因、任意4个基因、任意5个基因、……、任意10个基因、任意11个基因进行预测。尽管本发明实施例仅示例性给出单个基因和部分组合预测肿瘤进展的结果,但实际上上述任一组合均可以取得良好的预测效果。
在本发明的一些实施方案中,所述基因标志物组合包括FOSL2、ANXA1和SERPINH1。在本发明的另一些实施方案中,所述基因标志物组合包括FOSL2、ANXA1、SERPINH1VIM和CAV1。在本发明的又一些实施方案中,所述基因标志物组合包括S100A10、FOSL2、SPP1、CAV1、ANXA1、VIM、CD44、SERPINH1、LGALS3、CEBPB、ATF5和LGALS1。
本发明的第二方面提供本发明第一方面所述的基因标志物组合的表达水平检测试剂在制备用于预测肿瘤进展和/或预后的试剂盒中的应用。
在本发明中,获得所述基因标志物组合的表达水平是指获得所述基因标志物组合中各基因的表达水平。在本发明一些实施方案中,所述表达水平为相对表达水平,即相对于内参基因的表达水平。所述内参基因可以是本领域公知或通用的任意内参基因。所述内参基因的表达水平可以是一个内参基因的表达水平,也可以是多个内参基因的表达水平的平均值、众值或中位值。
在本发明的一些实施方案中,所述基因标志物组合的表达水平检测试剂为引物和/或探针。进一步地,利用包括全转录组测序、捕获测序和qRT-PCR的组中的至少一种方法获得所述基因标志物组合的表达水平。例如,本领域技术人员可以针对所述基因标志物组合中各基因设计探针,并将探针制备成基因芯片,利用基因芯片进行捕获测序。再如,可以针对所述基因标志物组合中各基因设计引物,进行PCR扩增后进行测序。又如,可以针对所述基因标志物组合中各基因设计引物和探针,利用qRT-PCR方法检测各基因的表达水平。特别地,也可以直接进行全转录组高通量测序,获得测序数据后,与人类参考基因组进行比较,并进行表达定量,获得表达谱信息。当然,本领域技术人员也可以利用其他任意方法获得所述基因标志物组合中各基因的表达水平。
在本发明中,所述表达水平基于RNA样本进行检测。具体地,可以在获得生物样本后,提取RNA样本进行检测,例如通过全转录组测序、捕获测序或qRT-PCR进行检测。在本发明的另一些实施方案中,也可以利用单细胞RNA测序(scRNA-seq)获得单个肿瘤细胞中所述各基因的表达水平。
在本发明的一些实施方案中,所述生物样本为组织、器官或体液。所述体液包括但不限定血液、血清、血浆、组织液、淋巴液、胸膜腔液、腹腔液、脑脊液、尿液、唾液、泪液、精液、阴道液。值得说明的是,对于不同的肿瘤,适用的组织或者体液可能不同,例如对于GBM,可以选择血液、脑脊液和脑组织的任意一种;对于本领域技术人员可能通过实践选择最适合的样本,但都落入本发明的保护范围。本发明第三方面提供一种预测肿瘤进展和/或预后的试剂盒,所述试剂盒包括权利要求1所述的基因标志物组合的表达水平检测试剂。
在本发明的一些实施方案中,还包括RNA提取试剂。
本发明的第四方面提供一种预测肿瘤进展和/或预后的系统,包括:
数据输入模块,用于获得本发明第一方面所述的基因标志物组合中各基因的表达水平;
预测模块,与所述数据输入模块连接,用于根据所述各基因的表达水平,利用单样本基因集富集分析方法预测肿瘤进展和/预后。
在本发明的一些实施方案中,所述预测模块中,利用单样本基因集富集分析方法获得所述基因标志物组合的富集分数,富集分数越高,肿瘤进展越晚期;肿瘤进展越晚期,对包括手术、化疗、放疗等治疗手段更容易产生抗性,也就意味着其预后越差。一般来说,
所述单样本基因集富集分析(single sample gene set enrichment analysis,ssGSEA)是GSEA方法的扩展,主要是针对单个样本无法做GSEA而设计。
在本发明的一些实施方案中,所述各基因的表达水平是基于RNA样本通过选自包括全转录组测序、捕获测序和qRT-PCR的组中的至少一种方法获得的。
在本发明的一些实施方案中,还包括参数存储模块,与所述预测模块连接,用于存储所述富集分数参考值。所述富集分数参考值是多个区间数值范围,落入某个区间数值范围内,意味着肿瘤处于某个进展期。例如,对于GBM,可分为早期(younger)、中期(middle)和晚期(older)三个进展期,对应三个区间数值范围:第一区间、第二区间、第三区间。当预测模块得到样本的富集分数后,与所述参数存储模块中的富集分数参考值进行比较,若富集分数落入第一区间,则表示来源肿瘤样本处于早期,预后良好;若富集分数落入第二区间,则表示来源肿瘤样本处于中期,预后一般;若富集分数落入第三区间,则表示来源肿瘤样本处于晚期,预后较差。
在本发明的一些具体实施方案中,所述富集分数参考值是利用群体样本得到的。在本发明的一些优选实施方案中,所述群体样本包括20个以上样本,例如30个、50个、80个、100个、150个、200个、300个、500个或更多。
在本发明的一些实施方案中,所述参数存储模块中的富集分数参考值根据所述预测模块中的预测结果进行更新。具体地,将富集分数和实际进展和/或预后数据与群体数据一起作为训练集,重新训练得到富集分数参考值。
在本发明中,所述肿瘤包括但不限于人肉瘤和癌,如纤维肉瘤、肌肉瘤、脂肪肉瘤、软骨肉瘤、成骨肉瘤、脊索瘤、血管肉瘤、内皮肉瘤、淋巴管肉瘤、淋巴管内皮肉瘤、滑膜瘤、间皮瘤、尤因瘤、平滑肌肉瘤、横纹肌肉瘤、结肠癌、胰腺癌、前列腺癌、鳞状细胞癌、基底细胞癌、腺癌、汗腺癌、皮脂腺癌、乳头状癌、乳头腺癌、囊腺癌、髓样癌、支气管癌、肝细胞瘤、胆管癌、绒毛膜癌、精原细胞瘤、胚胎癌、肾母细胞瘤、宫颈癌、睾丸瘤、肺癌、小细胞肺癌、上皮癌、胶质瘤、星形细胞瘤、髓母细胞瘤、颅咽管瘤、室管膜瘤、松果体瘤、成血管细胞瘤、听神经瘤、少突神经胶质瘤、脑膜瘤、黑素瘤、神经母细胞瘤、胶质母细胞瘤、视网膜母细胞瘤;白血病,如急性淋巴细胞性白血病和急性成髓细胞性白血病(成髓细胞、前髓细胞、髓单核细胞、单核细胞和红细胞白血病);慢性白血病(慢性髓细胞(粒细胞)白血病和慢性淋巴细胞性白血病);和真性红细胞增多、淋巴瘤(霍奇金病和非霍奇金病)、多发性骨髓瘤、瓦尔登斯特伦巨球蛋白血症和重链病。
在本发明的一些实施方案中,肿瘤为胶质母细胞瘤、膀胱癌、结直肠癌、食管癌、卵巢癌、胃癌、非小细胞肺癌、乳腺癌、肝癌或胰腺癌。
本发明的有益效果
相对于现有技术,本发明具有以下有益效果:
本发明利用转录组测序研发GBM,获得了GBM肿瘤的进展和预测的基因标志物组合,实现了肿瘤自然进化过程的前所未有的高分辨率表征。
利用本发明的基因标志物组合、试剂盒或系统,能够对包括GBM在内的多种肿瘤的进展和/或预后进行预测,普适性强,准确性高,具有非常在的临床应用价值。
利用本发明的基因标志物组合、试剂盒或系统,不仅能够利用肿瘤样本进行检测,还能够利用如外周血在内的其他生物样本进行检测,应用前景广泛。
附图说明
图1示出了12个基因在不同肿瘤细胞簇中的表达分布。其中,肿瘤细胞簇根据进展状态被分为早期(younger)、中期(intermediated)和晚期(older)三组。
图2示出了本发明肿瘤进展及预后预测系统的富集评分与患者预后的相关性。
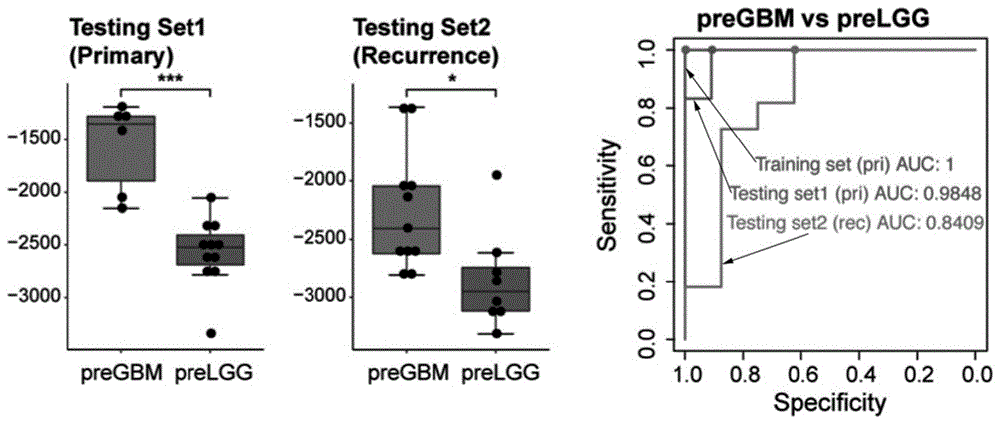
图3示出了利用本发明肿瘤进展及预后预测系统基于术前外周血样本的预测结果。preGBM代表高级别GBM的术前外周血样本,preLGG代表低级别LGG术前外周血样本。
具体实施方式
除非另有说明、从上下文暗示或属于现有技术的惯例,否则本申请中所有的份数和百分比都基于重量,且所用的测试和表征方法都是与本申请的提交日期同步的。在适用的情况下,本申请中涉及的任何专利、专利申请或公开的内容全部结合于此作为参考,且其等价的同族专利也引入作为参考,特别这些文献所披露的关于本领域中的相关术语的定义。如果现有技术中披露的具体术语的定义与本申请中提供的任何定义不一致,则以本申请中提供的术语定义为准。
本申请中的数字范围是近似值,因此除非另有说明,否则其可包括范围以外的数值。数值范围包括以1个单位增加的从下限值到上限值的所有数值,条件是在任意较低值与任意较高值之间存在至少2个单位的间隔。
术语“包含”,“包括”,“具有”以及它们的派生词不排除任何其它的组分、步骤或过程的存在,且与这些其它的组分、步骤或过程是否在本申请中披露无关。
为了使本发明所解决的技术问题、技术方案及有益效果更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。
实施例
以下例子在此用于示范本发明的优选实施方案。本领域内的技术人员会明白,下述例子中披露的技术代表发明人发现的可以用于实施本发明的技术,因此可以视为实施本发明的优选方案。但是本领域内的技术人员根据本说明书应该明白,这里所公开的特定实施例可以做很多修改,仍然能得到相同的或者类似的结果,而非背离本发明的精神或范围。
除非另有定义,所有在此使用的技术和科学的术语,和本发明所属领域内的技术人员所通常理解的意思相同,在此公开引用及他们引用的材料都将以引用的方式被并入。
那些本领域内的技术人员将意识到或者通过常规试验就能了解许多这里所描述的发明的特定实施方案的许多等同技术。这些等同将被包含在权利要求书中。
下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的仪器设备,如无特殊说明,均为实验室常规仪器设备;下述实施例中所用的试验材料,如无特殊说明,均为自常规生化试剂商店购买得到的。
实施例1基于转录组测序获得GBM肿瘤进展特征分子
本实施例首先对原发性GBM肿瘤样本进行RNA提取,然后进行全转录组测序,进一步对下机测序数据进行预处理,接着进行序列比对和基因表达定量,最终获得基因表达谱。具体步骤如下:
1.RNA提取及转录组测序
对每个肿瘤样本进行RNA提取,获取总RNA:每个肿瘤样本先分别获得第一病灶和第二病灶(影像上看相互隔离的病灶)的总RNA样本。
将RNA逆转录成cDNA;通过超声破碎将cDNA片段过于大的样本打断至200-350碱基对;对片段化的cDNA分子执行末端修复、添加嘌呤、连接文库接头等操作;在高通量测序仪上进行测序。
2.下机数据预处理
获得相应的高通量测序数据后,采用本领域通用方法对数据进行预处理,以过滤掉接头序列及不合格序列。
3.序列比对和基因表达定量
首先通过STAR内置函数genomeGenerate算法对要比对的参考基因组建立索引,然后通过STAR对样本进行比对,生成BAM文件。通过HTseq工具对BAM文件进行处理,得到样本基因表达矩阵。最后,通过FPKM算法对表达矩阵进行标准化。
4.肿瘤进展特征分子的鉴定
为了剖析与GBM肿瘤进展相关的分子特征,也即GBM肿瘤进展相关的基因标志物或叫基因标记物,发明人鉴定了肿瘤样本中第一病灶和第二病灶的肿瘤细胞中差异表达基因,保留在第一病灶和第二病灶的肿瘤细胞之间表达的绝对差异大于5%的基因。为了便于后续描述,第一病灶和第二病灶的差异表达基因分别表示为oDEG和yDEG。
为了识别进展较老和较年轻的肿瘤簇,发明人首先使用以下公式计算每个肿瘤簇的潜进展状态(称为PE):
其中O
发明人进一步通过PE得分对每个肿瘤簇进行从高到低排序,选择前20%和后20%分别作为较老簇和较年轻簇。
发明人利用第一个病灶的较老簇和第二个病灶的较年轻簇建立表达谱,并基于该表达谱进行差异表达分析。差异表达分析使用的标准包括:
(1)差异倍数(Fold Change,FC)≥1.5;
(2)Wilcoxon秩和检验矫正p值<10
(3)每组中表达的基因百分比≥10%。
由此,得到6083个基因,可作为潜在的肿瘤进展候选特征分子。
为确保肿瘤进展特征分子(基因)适用各种GBM,发明人在每个病灶以及另外4个GBM患者的样本中进行验证。同样用以下标准鉴定出显著的差异表达基因:
(1)FC≥1.5;
(2)Wilcoxon秩和检验矫正p值<10
(3)每组中表达的基因百分比≥10%。
将所有分析中获得的差异表达基因取交集,得到12个基因,这12个基因都称为肿瘤进展特征分子,也称为肿瘤进展预测基因标志物。12个基因分别是:S100A10、FOSL2、SPP1、CAV1、ANXA1、VIM、CD44、SERPINH1、LGALS3、CEBPB、ATF5和LGALS1,其在不同进展期的表达如图1所示。利用上述基因标志物组合或其子集,可用于预测肿瘤进展情况,进一步,由于肿瘤进展与预后密不可分,利用上述基因标志物组合或其子集还可用于预测肿瘤预后。
为了验证上述基因标志物组合的子集也能够用于肿瘤进展及预后的预测,发明人针对单个基因及少于31个基因的组合对GBM进行预测,结果如表1所示:
表1肿瘤进展预测基因标志物组合子集预测结果
由此可见,本实施例筛选鉴定的基因标志物组合中任一子集也可用于肿瘤进展和预后的预测,并且均具有非常高的准确率。
实施例2肿瘤进展或预后预测系统
本实施例建立一种预测肿瘤进展或预后的计算机系统,包括数据输入模块和预测模块。数据输入模块可获得实施例1获得的基因标志物组合中各基因的表达水平,预测模块使用单样本基因集富集分析(single sample gene set enrichment analysis,ssGSEA)方法(Barbie,D.,Tamayo,P.,Boehm,J.et al.Systematic RNA interference reveals thatoncogenic KRAS-driven cancers require TBK1.Nature 462,108-112(2009).)预测肿瘤进展或预后。
ssGSEA算法概括来说就是首先对给定样本的基因表达值进行秩次标准化,然后利用经验累积分布函数计算富集分数(ES)。R语言GSVA包可实现ssGSEA分析,GSVA包发布在Bioconductor上。
具体地,利用ssGSEA获得基因标志物组合的富集分数来预测肿瘤进展或预后,富集分数越高,肿瘤进展越晚期,预后越差。
对于GBM预后的预测如图2所示,从图2中可以看出,通过The Cancer GenomeAtlas(TCGA)、Gravendeel等人(Gravendeel,Lonneke AM,et al."Intrinsic geneexpression profiles of gliomas are a better predictor of survival thanhistology."Cancer research 69.23(2009):9065-9072.)、以及Chinese Glioma GenomeAtlas(CGGA)的数据分析表明,该系统能够有效预测GBM患者预后,富集分数高的患者生存时间更短。
实施例3肿瘤进展或预后预测系统的应用
为了验证实施例2系统的准确性和可靠性,以及对除GBM外的其他肿瘤的适用性,发明人收集了TCGA、International Cancer Genome Consortium(ICGC)数据库全基因组测序(whole exome sequencing,WES)的公共数据以及公开文献中多种样本测序数据。通过实施例2的系统计算每个样本的肿瘤进展得分并预测其预后。
结果如表2所示:
表2肿瘤进展或预后预测系统在多种肿瘤样本中的应用
从结果来看,本发明肿瘤进展及预后预测系统在多种肿瘤样本中均取得了较高的准确度。其中,对膀胱癌、结直肠癌、食管癌、卵巢癌进展及预后的预测,AUC都超过90%,准确度非常高。对胃癌和非小细胞肺癌进展的预测,AUC均超过80%,准确度也相对非常高;对乳腺癌、肝癌以及胰腺癌进展及预后的预测,AUC也都超过了75%,具有显著的临床价值。
实施例4肿瘤进展或预后预测系统的在基于外周血的应用
为了进一步验证实施例2系统可用于除肿瘤组织外的其他样本进行预测。发明人获得术前GBM和低级别胶质瘤(low-grade glioma,LGG)的外周血样本,分别进行预测。结果如图3所示。可以看到,无论在初发组(Primary)中还是复发组(Recurrence)中,GBM的富集分数均显著高于LGG,表示实施例2系统基于外周血样本也可以很好的预测肿瘤进展。进一步拓宽了实施例2系统应用前景。
在本发明提及的所有文献都在本申请中引用作为参考,就如同每一篇文献被单独引用作为参考那样。此外应理解,在阅读了本发明的上述讲授内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。
