一种生理参数的计算方法及相应的医疗设备
文献发布时间:2023-06-19 11:24:21
技术领域
本发明涉及生理参数监测领域,尤其涉及一种生理参数的计算方法及相应的医疗设备。
背景技术
人体的新陈代谢过程是生物氧化过程,而新陈代谢过程所需要的氧,是通过呼吸系统进入人体血液,与血液红细胞中的还原血红蛋白(Hb),结合成氧合血红蛋白(HbO2),再输送到人体各部分组织细胞中。当机体氧供与氧耗之间出现不平衡,就意味着缺氧情况的发生。缺氧对机体有着巨大的影响。故,动脉血氧浓度的实时监测在临床救护中非常重要。
血氧饱和度(SpO2)是血液中氧合血红蛋白(HbO2)容量占总血红蛋白(Hb+HbO2)容量的百分比,即血液中血氧的浓度。血氧饱和度(SpO2)作为动脉血氧饱和度(SaO2)的间接反映,以其无创、简单、准确、快速等特点,迅速被各大应用领域采纳和使用。
脉搏血氧技术应用的如此广泛,随之而来,对脉搏血氧准确性的要求也水涨船高。本领域人员可知,评价脉搏血氧性能的优劣性,有两大关键因素:弱灌注性能和运动性能。如果被测患者存在弱灌注性能差或及运动性能差的情形,则对脉搏血氧性能的准确性和稳定性要求就更加苛刻。
自1998年Masimo公司推出“运动和弱灌注下准确测量病人血氧饱和度技术”以来,Masimo公司迅速确立了其血氧行业的领先地位。其技术的核心思想是确立系数R
可以理解的是,基于Lambert-Bear定律可知,氧合血红蛋白(HbO2)和去氧血红蛋白(HB)在不同的光波段下吸收特性不同,如图1所示,为现有技术中氧合血红蛋白和还原血红蛋白吸收光谱曲线图;利用该吸收特性,可以进一步评估血氧饱和度参数。
如图2所示,为现有技术中血氧测量工作原理图;利用发光管发射两路光(例如:红光和近红外光)透射机体组织,并利用接收管接收透射机体组织的光信号,从而获得血液搏动成分AC交流量(例如:动脉血)和非搏动成分DC直流量(例如:静脉血、肌肉、骨骼、皮肤等)。分别利用红光和近红外光的AC交流量和DC直流量,即可获得与动脉血氧饱和度(SaO2)的映射曲线比值,即R系数表(如公式1所示方法)。再基于查表法即可获得动脉血氧饱和度(SaO2)的无限逼近值脉搏血氧饱和度(SpO2)。
其中,AC
然而如何能够准确识别采集信号中AC交流成分和DC交流成分,获得准确的R值,却不是那么容易的事情。现有技术中存在两种技术:时域技术和频域技术。
其中,时域技术具有响应速度快、相位信息清晰等特点。由于时域信号是有用信号和噪声信号的混合,生理带宽外的噪声可以通过高通/低通滤波器轻松滤除,而当出现生理带宽内的噪声时,由于噪声的变化性、先验知识的匮乏,时域方法几乎没有办法滤除这部分噪声。因此时域技术在抗运动性能上存在着天然的缺陷。
而频域技术理论上可以分离噪声和有用信号的频带,进而达到区分识别真实信号的目的。按照数字信处理的定义,任何一个波形都是由多个正弦波构成,生理参数的脉搏波也不例外。因此,当生理脉搏波信号转换为频域信号时,该生理参数就会出现基倍频特征。当干扰出现时,干扰频谱和生理参数的基倍频谱混叠在一起,很难识别到真实频谱是哪一个。因此,尽管频域技术存在着先天性的优势,但是想在干扰状态下准确计算血氧相关参数,也非常棘手。
由Parseval定理可知,信号时域的总能量等于频域的总能量。因此,公式1也适用于频域信号,其中AC交流量对应于每个频率点的能量变化。在理想条件下,经过规一化后,脉搏波的红光及红外光频谱如图3所示,主频段及各个倍频段的比值可以看作是此频段下对应的能量比值。该能量比值的意义与公式1中对应的R值的意义完全一致,也即与血氧饱和度唯一对应。在不考虑噪声的理想状态下,各个频段的比值一致,都与当前的血氧饱和度唯一对应,理论上在任何频段都可以得到血氧饱和度参数。
同理,根据信号的构成理论,可知图3中基频峰所在频率即为脉率值。常规检测基频峰频率的方法可以通过识别基倍频峰筛选获得,所依据的理论是基频峰与谐波峰存在能量和频率的比例关系。通过这种比例关系即可识别到生理脉率值。
综上所述,通过检索频域信号中基倍频峰的位置信息和红光与红外光的能量比值,即可获得脉率参数和血氧参数。然而在干扰情况下,红光和红外光的频谱峰信息可能被噪声混淆、湮灭,基频峰频率信息因无法识别或错误识别而导致脉率计算异常;同时红光和红外光的能量比值也因噪声的混入而导致血氧计算偏差较大。如图4所示,给出了一种干扰下的频谱分布示意。从图4中可以看到,红外光和红光的频谱峰能量比值忽大忽小,基频峰几乎被湮没。这种情况下,利用现有的时频域技术正确的识别频谱峰并计算准确的血氧和脉率参数,几乎不可能实现。
发明内容
本发明实施例所要解决的技术问题在于提供一种生理参数的计算方法及相应的医疗设备,可以在弱灌性和运动状态下提升计算生理参数(如脉率值以及血氧参数)的准确度,且计算复杂度低,对运算资源需求低。
为了解决上述技术问题,本发明实施例提供了一种生理参数的计算方法,该方法包括如下步骤:
选择通过采样获得的红光和/或红外光的至少一路信号所对应的一段区间的时域信号,对所述区间的时域信号进行时频域转换,获得相应的频域信号;
在所述频域信号中,选择其中所有合理的频谱峰,计算所选择的合理的频谱峰的能量信息,并构成频谱峰能量比值序列;
根据所述频谱峰能量比值序列构建稳定系数,如果所述的稳定系数偏低,则利用频谱峰能量比值序列构建补偿系数;
使用所述的补偿系数补偿所述的时域信号和/或频域信号的至少一路,基于已补偿的时域信号和/或频域信号计算获得生理参数。
相应地,本发明的另一方面,还提供一种计算生理参数的医疗设备,其包括:
传感器,其包括至少一个发光管和至少一个接收管,所述发光管发射透射生理组织的至少两路不同波长的光信号,所述接收管接收透射生理组织的至少两路光信号,并转为电信号;
模数转换器,与所述传感器连接,将所述电信号转换为数字信号,该数字信号包含了生理组织的至少部分特征;
数字处理器,与所述模数转换器连接,所述数字处理器执行下述处理:
对一段区间的数字信号进行时频域转换,获得对应的频域信号;
在所述频域信号中,选择其中所有合理的频谱峰,计算所选择的合理的频谱峰的能量信息,并构成频谱峰能量比值序列;
根据所述频谱峰能量比值序列构建稳定系数,如果所述的稳定系数偏低,则利用频谱峰能量比值序列构建补偿系数;
使用所述的补偿系数补偿所述一段区间的数字信号和/或对应的频域信号,基于已补偿的数字信号和/或频域信号,计算获得生理参数。
相应地,本发明的另一方面,还提供一种生理参数的计算方法,该方法包括如下步骤:
选择通过采样获得的红光和/或红外光的至少一路信号所对应的一段区间的时域信号,对所述区间的时域信号进行时频域转换,获得至少一路频域信号;
在所述频域信号中,选择其中所有合理的频谱峰,计算所选择的合理的频谱峰的位置信息,并形成频谱峰位置序列;
根据所述的频谱峰位置序列,构建随时间变化的阵列图,随时间变化的每个位置点构建至少一个稳定因子,从而形成稳定因子阵列图;
基于稳定因子阵列图构建稳定系数,如果所述稳定系数偏低,则利用所述的稳定因子阵列图计算得到补偿系数;
使用所述的补偿系数补偿所述的时域信号和/或频域信号的至少一路,基于已补偿的时域信号和/或频域信号计算获得生理参数。
相应地,本发明的另一方面,还提供一种计算生理参数的医疗设备,其包括:
传感器,其包括至少一个发光管和至少一个接收管,所述发光管发射透射生理组织的至少两路不同波长的光信号,所述接收管接收透射生理组织的至少两路光信号,并转为电信号;
模数转换器,与所述传感器连接,将所述电信号转换为数字信号,该数字信号包含了生理组织的至少部分特征;
数字处理器,与所述模数转换器连接,所述数字处理器执行下述处理:
对一段区间的数字信号进行时频域转换,获得对应的频域信号;
选择其中所有合理的频谱峰,计算所选择的合理的频谱峰的位置信息,并形成频谱峰位置序列;
根据所述的频谱峰位置序列,构建随时间变化的阵列图,随时间变化的每个位置点构建至少一个稳定因子,从而形成稳定因子阵列图;
基于稳定因子阵列图构建稳定系数,如果所述稳定系数偏低,则利用所述的稳定因子阵列图计算得到补偿系数;
使用所述的补偿系数补偿所述的所述一段期间的数字信号和/或对应的频域信号,基于已补偿的数字信号和/或频域信号,计算获得生理参数。
相应地,本发明的另一方面,还提供一种生理参数的计算方法,该方法包括如下步骤:
选择通过采样获得的红光和/或红外光的至少一路信号所对应的一段区间的时域信号,对所述区间的时域信号进行时频域转换,获得至少一路频域信号;
在所述频域信号中,选择其中所有合理的频谱峰,计算所选择的合理的频谱峰的能量和/或位置信息,并形成频谱峰能量比值序列和/或频谱峰位置序列;
根据所述频谱峰能量比值序列和/或频谱峰位置序列,构建稳定系数,如果稳定系数偏低,使用所述频谱峰能量比值序列和/或频谱峰位置序列构建补偿系数;
使用所述的补偿系数补偿所述的时域信号和/或频域信号的至少一路,基于已补偿的时域信号和/或频域信号计算获得生理参数。
相应地,本发明的另一方面,还提供一种计算生理参数的医疗设备,其包括:
传感器,其包括至少一个发光管和至少一个接收管,所述发光管发射透射生理组织的至少两路不同波长的光信号,所述接收管接收透射生理组织的至少两路光信号,并转为电信号;
模数转换器,与所述传感器连接,将所述电信号转换为数字信号,该数字信号包含了生理组织的至少部分特征;
数字处理器,与所述模数转换器连接,所述数字处理器执行下述处理:
对一段区间的数字信号进行时频域转换,获得对应的频域信号;
在所述频域信号中,选择其中所有合理的频谱峰,计算所选择的合理的频谱峰的能量和/或位置信息,并形成频谱峰能量比值序列和/或频谱峰位置序列;
根据所述频谱峰能量比值序列和/或频谱峰位置序列构建稳定系数,偏低如果稳定系数偏低偏低,使用所述频谱峰能量比值序列和/或频谱峰位置序列构建补偿系数;
使用所述的补偿系数补偿所述一段区间的数字信号和/或对应的频域信号,基于已补偿的数字信号和/或频域信号,计算获得生理参数。
实施本发明实施例,具有如下的有益效果:
首先,本发明实施例基于频域技术并结合时域技术,能够在弱灌注和运动状态下,大幅度提升了生理参数的计算准确性,为客户带来了卓越的临床性能体验,可极大地提高生理参数(如血氧参数)的应用和推广;
其次,实施本发明,通过将时频域信号的特点与人体生理参数的特征相结合,在出现干扰情况下,采用静脉氧补偿法以及频谱阵列图法,在弱灌性和运动状态下提升计算生理参数(如脉率值以及血氧参数)的准确度。其中,静脉氧补偿法可以消除干扰引起的血氧测量偏差,无限逼近真实生理血氧值,极大的提供了干扰状态下血氧参数计算的准确性;频谱阵列图法方法可以消除干扰引起的脉率测量偏差,即使在长时间的干扰状态下,也能够准确的识别生理频谱信息,极大的提供了干扰状态下脉率参数计算的准确性;
另外,本发明实施例提供的方法,计算复杂度低,对运算资源需求低。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动性的前提下,根据这些附图获得其他的附图仍属于本发明的范畴。
图1为现有技术中氧合血红蛋白和还原血红蛋白吸收光谱曲线图;
图2为现有技术中血氧测量工作原理图;
图3为不存在干扰情形时的一种频谱分布图;
图4为存在干扰情形时的一种频谱分布图;
图5为本发明提供的生理参数的计算方法一个实施例的主流程示意图;
图6为本发明提供的生理参数的计算方法另一个实施例的主流程示意图;
图7为本发明提供的生理参数的计算方法又一个实施例的主流程示意图;
图8为本发明提供的计算生理参数的医疗设备中所采用的数字处理器的一个实施例的结构示意图;
图9为图8中补偿系数构建单元的结构示意图;
图10为本发明提供的计算生理参数的医疗设备中所采用的数字处理器的另一个实施例的结构示意图;
图11为图10中补偿系数构建单元的结构示意图;
图12为本发明提供的计算生理参数的医疗设备中所采用的数字处理器的又一个实施例的结构示意图;
图13为图12中补偿处理单元的结构示意图;
图14是本发明一个实施例中涉及的一种静脉血搏动干扰动脉血搏动的示意图;
图15是本发明一个实施例中补偿系数的计算流程示意图;
图16是本发明一个实施例中在干扰状态下的频谱段血氧分布示意图;
图17本发明一个实施例中静脉氧补偿法框架流程示意图;
图18是本发明一个实施例中进行基倍频率筛选流程示意图;
图19示出了本发明一个实施例中频谱阵列图法的流程示意图;
图20示出了本发明一个实施例中同时采用静脉氧补偿法和频谱阵列图法的流程示意图;
图21为本发明提供的一种计算生理参数的医疗设备的一个实施例的结构示意图。
具体实施方式
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
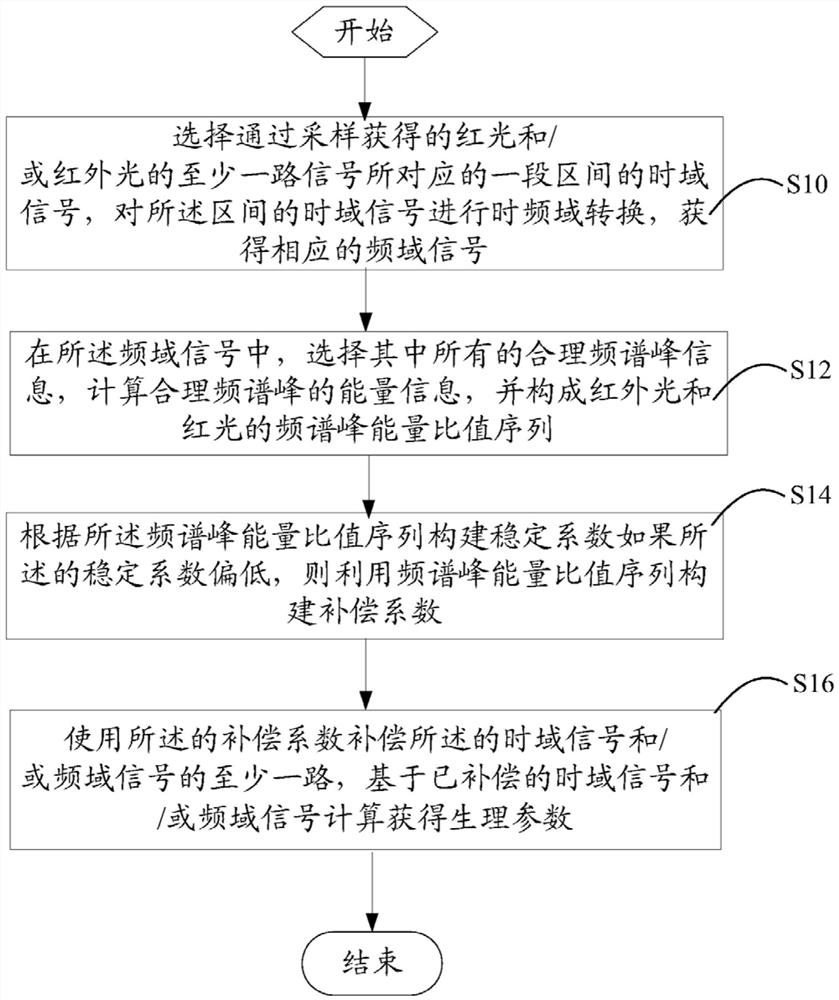
如图5所示,示出了本发明提供的一种生理参数计算准确度的方法的一个实施例的主流程示意图,在该实施例中,示出了静脉氧补偿法(Venous Oxygen Compensation,VOC)的补偿流程,具体地,该方法包括如下的步骤:
步骤S10,选择通过采样获得的红光和/或红外光的至少一路信号所对应的一段区间的时域信号,对所述区间的时域信号进行时频域转换,获得相应的频域信号;
步骤S12,在所述频域信号中,选择其中所有合理的频谱峰信息,计算所选择的合理的频谱峰的能量信息,并构成红外光和红光的频谱峰能量比值序列;其中,所述合理的频谱峰信息为满足频谱能量关系(如,否存在基倍频关系)、频谱幅度关系(幅度是否未低于一个定值)、频谱位置关系、频谱峰形态关系(如,频谱峰的形状对于频点是否左右对称)等因素中的至少一个;
步骤S14,根据所述频谱峰能量比值序列构建稳定系数,如果所述的稳定系数偏低,则利用频谱峰能量比值序列构建补偿系数;其中,所述的稳定系数为基于所述红光和红外光能量比值的偏差统计或基于血氧参数值的偏差统计构建而成,或者为一经验系数。经验系数根据生理状态以及信噪比特征抽象化形成,例如:识别为运动干扰时,生理血氧不可能过低;长时间运动下生理血氧会出现下降趋势;运动干扰剧烈时,当噪声成分远大于信号成分时,血氧趋近于80%,等等。结合血氧系统,即可形成数字化的经验系数值。具体地,将所述稳定系数与一设定阈值对比判断,以确定所述稳定系数是否偏低。在一个例子中,可以利用统计谱峰能量比值偏差序列或血氧偏差序列的均值、标准差、最大值、最小值信息,按照特定算法构建获得所述稳定系数;
在一个例子中,可以采用如下的方法来构建补偿系数:
选取生理参数(如血氧参数)均值作为补偿系数计算公式的分母输入源;选取均值+标准差或均值-标准差作为补偿系数计算公式的分子输入源;
将所述分子输入源和分母输入源代入下述补偿系数计算公式,计算得到相应的补偿系数:
Factorcompensation=tabR(Numerator)/tabR(Denomnator)
其中,tabR(Numerator)为以所述分子输入源作为血氧值,在一预定的血氧与R曲线系数的映射表查询获得的R系数值,而tabR(Denomnator)为以所述分子输入源作为血氧值,在一预定的血氧与R曲线系数的映射表查询获得的R系数值;Factorcompensation为补偿系数。
步骤S16,使用所述的补偿系数补偿所述的时域信号和/或频域信号的至少一路,基于所述的已补偿的时域信号和/或频域信号计算获得生理参数所述生理参数为血氧参数、脉率参数、波形面积参数、灌注指数参数中的至少一个。
下述以生理参数为血氧饱和度参数为例,举例说明图5中的进一步的详细流程图。
首先在步骤S10中,选择通过采样获得的红光和/或红外光的至少一路信号所对应的一段区间的时域信号,对所述区间的时域信号进行时频域转换,获得相应的频域信号;
接着在步骤S12中,在所述频域信号中,选择其中所有合理的频谱峰信息,计算所选择的合理的频谱峰的能量信息,并构成红外光和红光的频谱峰能量比值序列;具体地;根据每一所述合理的频谱峰的血氧饱和度参数,统计分析血氧分布序列,获得多个特征信息;具体地,根据每一所述合理的频谱峰的血氧饱和度参数,至少计算获得所述血氧饱和度的均值vMean、标准差vStd、最大值vMax、最小值vMin;
然后在步骤S14中,根据所述频谱峰能量比值序列构建稳定系数,如果该稳定系数偏低,则利用频谱峰能量比值序列构建补偿系数。具体地,将前述步骤中获得的多个特征信息中,最大值与最小值的差值作为稳定系数,如果所述稳定系统小于或等于一个设定的第一阈值,则确定该稳定系数偏低,需要构建补偿系数;
具体地,在一些实施例中,构建补偿系数的过程可以通过如下方法获得:
如果此时标准差vStd小于一预设的第二阈值,则选取均值作为补偿系数计算公式的分母输入源;如果所述血氧序列中超过均值的血氧个数占序列总数的至少一半,则以最大值+标准差作为补偿系数计算公式的分子输入源,反之以最大值–标准差作为补偿系数计算公式的分子输入源;
如果此时标准差大于一预设的第二阈值,则以预定方式获得重复因子,以所作为补偿系数计算公式的分子输入源,并以所述均值作为补偿系数计算公式的分母输入源;
将所述分子输入源和分母输入源代入下述补偿系数计算公式,计算得到相应的补偿系数:
Factorcompensation=tabR(Numerator)/tabR(Denomnator)...................公式1
其中,tabR(Numerator)为以所述分子输入源作为血氧值,在一预定的血氧与R曲线系数的映射表查询获得的R系数值,而tabR(Denomnator)为以所述分子输入源作为血氧值,在一预定的血氧与R曲线系数的映射表查询获得的R系数值;Factorcompensation为补偿系数。
其中,所述以预定方式获得重复因子的步骤具体为:
统计血氧分布序列中,获得满足一定偏差值(如+2%)的最大血氧参数集合,计算所述最大血氧参数集合的均值,作为重复因子;或者
选取血氧历史趋势中的一定时间范围(如4s~8s)内的稳定段,计算所述稳定段中血氧参数集合的均值,作为重复因子;
最后在步骤S16中,使用所述补偿系数补偿所述红光和/或红外光至少一路所对应的时域信号,使用至少一路已补偿的时域信号进一步计算生理参数。所述生理参数为血氧参数、脉率参数、波形面积参数、灌注指数参数中的至少一个。具体地可以通过如下的两种方式:
一、根据所述补偿后的时域信号,根据时域算法,计算获得最终血氧饱和度参数和脉率值;或者
二、对所述补偿后的时域信号进行时频域变换,获得频域信号,选择频域信号中一个合理的频谱峰,并根据频域算法对所述合理的频谱峰进行计算,获得准确的最终血氧饱和度参数。
如图6所示,示出了本发明提供的一种生理参数计算准确度的方法的另一个实施例的主流程示意图,在该实施例中,示出了频谱阵列图法(Power Spectrum Array,PSA)补偿流程,具体地,该方法包括如下的步骤:
步骤S20,选择通过采样获得的红光和/或红外光的至少一路信号所对应的一段区间的时域信号,对所述区间的时域信号进行时频域转换,获得至少一路频域信号;
步骤S22,在所述频域信号中,选择其中所有合理的频谱峰信息,计算所选择的合理的频谱峰的位置信息,并形成或频谱峰位置序列;其中,所述合理的频谱峰信息为满足频谱能量关系、频谱幅度关系、频谱位置关系、频谱峰形态关系中的至少一个或多个;
步骤S24,根据所述的频谱峰位置序列,构建稳定系数,如果所述稳定系数偏低,则利用所述的频谱峰位置序列构建随时间变化的阵列图,并通过该阵列图计算得到补偿系数;其中,所述稳定系数为基于频谱能量比值偏差、频谱血氧偏差、基倍频组状态、合理的频谱峰个数中至少一个构建而成,可以根据稳定因子的数量和/或权重值判断所述稳定系数是否偏低;
在一个例子中,根据频谱峰位置序列中的基倍频组状态来确定稳定系数;例如,在该频谱峰位置序列中不能识别出基倍频组对时,则认为稳定系数偏低;
具体地,用所述的频谱峰位置序列构建随时间变化的阵列图,并通过该阵列图计算得到补偿系数的步骤包括:
建立缓存以存储频谱峰的相关信息,所述频谱峰的相关信息包括:每一频谱峰位置信息PeakArray;每一频谱峰位置权重信息WeigtedArray;频谱峰存储的数量信息ArrayIndex;
步骤S161,筛选所述频域信号中预定数量的频谱峰,依次填充到所述缓存中,将每一频谱峰的位置信息填写入PeakArray,在WeigtedArray相应的位置权重信息加一,总长度ArrayIndex加一;其中,如果当前筛选的频谱峰与缓存中的一频谱峰相同,则直接将缓存中所述频谱峰位置权重信息WeigtedArray加一。
步骤S162,在所述缓存中,假定每一个频谱峰作为疑似基频峰,遍历所有其它频谱峰,判断其它频谱峰与所述疑似基频峰是否满足频率的倍数关系,如果满足,则消除所述倍频峰在缓存中的相关信息,并将所述倍频峰的位置权重系数按照倍频次数折算并累加到所述相应疑似基频峰的位置权重系数上;反之保留其它频谱峰的相关信息;
步骤S163,在最后保留的所述疑似频谱峰中,选择位置权重系数排在前列的三个频谱峰,确定其中一个作为最终的合理的频谱峰(在一些例子中可以认为是基频峰),并根据所述确定的最终的合理的频谱峰获得脉率值,同样,可以理解的是,可以根据该最终的合理的频谱峰通过能量计算获得对应的血氧饱和度。具体地,该步骤进一步包括:
将所选择的每一频谱峰的位置权重系数分别与一预定的第三阈值进行比较;
如果位置权重系数大于所述的第三阈值的频谱峰个数为一个,则将所述频谱峰确定为最终的合理的频谱峰;
如果权重系数大于所述的第三阈值的频谱峰个数为至少两个,则进一步根据生理特性,确定其中一个频谱峰作为最终的合理的频谱峰,并以后述最终的合理的频谱峰的信息作为补偿系数;
步骤S26,使用所述的补偿系数补偿所述的时域信号和/或频域信号的至少一路,基于所述的已补偿的时域信号和/或频域信号计算获得生理参数;其中,所述生理参数为血氧参数、脉率参数、波形面积参数、灌注指数参数中的至少一个;其中,在一个例子中,使用所述的补偿系数补偿所述的时域信号和/或频域信号的至少一路可以具体为:根据所述补偿系数构建一个带通滤波器,对所述的时域信号和/或频域信号的至少一路进行滤波处理,以实现补偿功能。
如图7所示,示出了本发明提供的一种生理参数计算准确度的方法的另一个实施例的主流程示意图,在该实施例中,综合了静脉氧补偿法(Venous Oxygen Compensation,VOC)和频谱阵列图法(Power Spectrum Array,PSA)补偿流程,具体地,该方法包括如下的步骤:
步骤S30,选择通过采样获得的红光和/或红外光的至少一路信号所对应的一段区间的时域信号,对所述区间的时域信号进行时频域转换,获得至少一路频域信号;
步骤S32,在所述频域信号中,选择其中所有合理的频谱峰信息,计算所选择的合理的频谱峰的能量和或位置信息,并形成频谱峰能量比值序列和频谱峰位置序列;其中,所述合理的频谱峰信息为满足频谱能量关系、频谱幅度关系、频谱位置关系、频谱峰形态关系中的至少一个;所述形成频谱峰能量比值序列和频谱峰位置序列的过程可分别参见前述对图5中步骤S12和对图6中步骤S22的描述;
步骤S34,根据所述频谱峰能量比值序列和频谱峰位置序列的至少一路的信号特征,构建稳定系数,同时判断述序列的至少一路的稳定系数是否偏低,如果稳定系数偏低,使用所述序列的至少一路的信号特征构建补偿系数;其中,所述稳定系数为基于频谱能量比值偏差、频谱血氧偏差、基倍频组状态、合理的频谱峰个数中至少一个构建而成;所述补偿系数为基于频谱能量序列计算得到的能量比值偏差系数或血氧偏差系数,或者为基于频谱位置序列随时间变化而统计得到的位置系数。
其中,根据频谱峰能量比值序构建稳定系数,并构建补偿系数的具体流程可参见前述对图5中步骤S14的描述;
其中,频谱峰位置序列构建稳定系数,并构建补偿系数的具体流程可参见前述对图6中步骤S24的描述;在此不进行详述。
步骤S36,利用所述补偿系数补偿所述的时域信号和/或频域信号;基于所述的已补偿的时域信号和/或频域信号,进一步计算获得生理参数,所述生理参数为血氧参数、脉率参数、波形面积参数、灌注指数参数中的至少一个或多个。
具体地,该步骤包括下述至少一个:利用所述补偿系数,所选择的时域信号做增益处理,以实现补偿;或者
利用所述补偿系数,对所选择的频域信号进行滤波处理,以实现补偿。
相应地,本发明还提供了一种计算生理参数的医疗设备。
可以理解的是,本发明所公开的一种生理参数的计算方法可以功能模块化来实现,作为插件集成于其他辅助诊断设备(如监护设备,除颤仪,AED,自动复苏仪器,心电图机等);也可以做成为单参数医疗器械,用于相关生理参数监测,生理参数包含血氧参数、脉率参数、波形面积参数、灌注指数参数中的至少一个。
如图21所示,示出了本发明公开的一种医疗设备的结构示意图,在该实施例中示出了一个单参数医疗器械;在该实施例中,该医疗设备包括:
至少一个血氧传感器,其用于对受试者的手指、额头、耳垂、脚趾、脚掌等部位的测量。该血氧传感器至少包含一个发光管和一个接收管,发光管发射用于透过受试者人体组织的至少两路不同波长的光信号,在一个例子中,该发光管可发射一路红光和一路红外光信号。接收管接收透过受试者人体组织的至少两路光信号,并转为至少两路电信号,在一个例子中,该两路电信号为红光和红外光信号;
模数转换器,与所述传感器连接,将所述电信号转换为数字信号,该数字信号包含了生理组织的至少部分特征;
数字处理器,与所述模数转换器连接,所述数字处理器执行下述处理:
对一段区间的数字信号进行时频域转换,获得对应的频域信号;
在所述频域信号中,选择其中所有合理的频谱峰,计算所选择的合理的频谱峰的能量信息,并构成频谱峰能量比值序列;
根据所述频谱峰能量比值序列构建稳定系数,如果所述的稳定系数偏低,则利用频谱峰能量比值序列构建补偿系数;
使用所述的补偿系数补偿所述一段区间的数字信号和/或对应的频域信号,基于已补偿的数字信号和/或频域信号计算获得生理参数。
进一步包括:与所述数字处理器连接,显示所述数字处理器计算获得的生理参数;和/或
通信单元,与所述数字处理器连接,发送所述数字处理器计算获得的生理参数。
其中,血氧传感器包括透射式和反射式两种,一般可佩戴于受试者手指、额头、耳垂、脚趾、脚掌等部位进行生理参数测量,包含血氧参数、脉率参数、波形面积参数、灌注指数参数中的至少一个。其中,显示单元可以是本地显示单元,也可以是通过有线/无线方式远程通讯到远程显示单元。显示单元通过字符、数值、波形、棒图、声音提示等为用户提供一个可知觉的参数呈现。
在本发明的其中一个实施例中,所述生理组织的至少部分特征为血液中含氧血红蛋白、去氧血红蛋白、铁氧血红蛋白、总血红蛋白或一氧化碳的光学特征中的一项或多项。
在本发明的其中一个实施例中,所述合理的频谱峰满足频谱能量关系、频谱幅度关系、频谱位置关系、频谱峰形态关系中的至少一个。
在本发明的其中一个实施例中,所述稳定系数为基于所述红光和红外光能量比值的偏差统计构建而成,或者为一经验系数。
在本发明的其中一个实施例中,所述稳定因子依据基倍频组特性、频谱峰形态合理性的至少一个,随时间变化调整其稳定性权重。
在本发明的其中一个实施例中,所述数字处理器利用频谱峰能量比值序列构建补偿系数的处理具体为:
选取所述均值经系数表转换为补偿系数计算公式的分母,选取(均值+标准差)或(均值-标准差)经系数表转换为补偿系数计算公式的分子,求取其比值得到补偿系数。
在本发明的其中一个实施例中,所述生理参数为血氧、脉率、波形面积、灌注指数等的至少一个。
为了更好地理解本实施例中数字处理器的功能及工作原理,下面将结合一个具体的例子进行说明。
如图8所示,示出了本发明提供的一种计算生理参数的医疗设备中所采用的数字处理器的一个实施例的结构示意图,该数字处理器采用静脉氧补偿法(Venous OxygenCompensation,VOC)进行补偿,请一并结合图9所示,具体地,该数字处理器包括:
时频域转换单元11,用于选择通过采样获得的红光和/或红外光的至少一路信号所对应的一段区间的时域信号,对所述区间的时域信号进行时频域转换,获得相应的频域信号;
能量比值序列构建单元12,用于在所述频域信号中,选择其中所有合理的频谱峰信息,计算所选择的合理的频谱峰的能量信息,并构成红外光和红光的频谱峰能量比值序列;其中,所述合理的频谱峰信息为满足频谱能量关系、频谱幅度关系、频谱位置关系、频谱峰形态关系中的至少一个;
补偿系数构建单元13,用于根据所述频谱峰能量比值序列构建稳定系数,如果所述的稳定系数偏低,则利用频谱峰能量比值序列构建补偿系数;所述稳定系数为基于所述红光和红外光能量比值的偏差统计或基于血氧参数值的偏差统计构建而成,或者为一经验系数;将所述稳定系数与一设定阈值对比判断,以确定所述稳定系数是否偏低。
补偿处理单元14,用于使用所述补偿系数补偿所述红光和/或红外光至少一路所对应的时域信号,使用至少一路已补偿的时域信号进一步计算生理参数。
所述补偿系数构建单元13进一步包括:
稳定系数构建子单元130,用于利用统计谱峰能量比值偏差序列或血氧偏差序列的均值、标准差、最大值、最小值信息,按照特定算法构建获得所述稳定系数;
判断单元131,用于判断稳定系数构建子单元130所构建的稳定系数是否偏低;
分子分母选取单元132,用于选取血氧参数均值作为补偿系数计算公式的分母输入源;以及选取均值+标准差或均值-标准差作为补偿系数计算公式的分子输入源;
计算单元134,用于将所述分子分母选取单元所选取的分子输入源和分母输入源代入下述补偿系数计算公式,计算得到相应的补偿系数:
Factorcompensation=tabR(Numerator)/tabR(Denomnator)
其中,tabR(Numerator)为以所述分子输入源作为血氧值,在一预定的血氧与R曲线系数的映射表查询获得的R系数值,而tabR(Denomnator)为以所述分子输入源作为血氧值,在一预定的血氧与R曲线系数的映射表查询获得的R系数值;Factorcompensation为补偿系数。
更多的细节,可参照前述对图5的描述。
相应地,本发明还提供了一种计算生理参数的医疗设备,在该实施例中,该医疗设备包括:
传感器,其包括至少一个发光管和至少一个接收管,所述发光管发射透射生理组织的至少两路不同波长的光信号,所述接收管接收透射生理组织的至少两路光信号,并转为电信号;
模数转换器,与所述传感器连接,将所述电信号转换为数字信号,该数字信号包含了生理组织的至少部分特征;
数字处理器,与所述模数转换器连接,所述数字处理器执行下述处理:
对一段区间的数字信号进行时频域转换,获得对应的频域信号;
在所述频域信号中,选择其中所有合理的频谱峰,计算所选择的合理的频谱峰的位置信息,并形成频谱峰位置序列;
根据所述的频谱峰位置序列,构建随时间变化的阵列图,随时间变化的每个位置点构建至少一个稳定因子,从而形成稳定因子阵列图;
基于稳定因子阵列图构建稳定系数,如果所述稳定系数偏低,则利用所述的稳定因子阵列图计算得到补偿系数;
使用所述的补偿系数补偿所述的时域信号和/或频域信号的至少一路,基于已补偿的时域信号和/或频域信号计算获得生理参数。
进一步包括:显示单元,与所述数字处理器连接,显示所述数字处理器计算获得的生理参数;和/或
通信单元,与所述数字处理器连接,发送所述数字处理器计算获得的生理参数。
在本发明的其中一个实施例中,所述两路光信号,是红光和红外光;
在本发明的其中一个实施例中,所述生理组织的至少部分特征为血液中含氧血红蛋白、去氧血红蛋白、铁氧血红蛋白、总血红蛋白或一氧化碳的光学特征中的一项或多项。
在本发明的其中一个实施例中,所述合理的频谱峰为满足频谱能量关系、频谱幅度关系、频谱位置关系、频谱峰形态关系中的至少一个或多个。
在本发明的其中一个实施例中,所述稳定系数为基于频谱能量比值偏差、频谱血氧偏差、基倍频组状态、合理的频谱峰个数、频谱峰形态合理性中的至少一个构建而成。
在本发明的其中一个实施例中,所述稳定因子依据基倍频组特性、频谱峰形态合理性的至少一个,随时间变化调整其稳定性权重。
在本发明的其中一个实施例中,根据稳定因子的数量和/或权重值判断所述稳定系数是否稳定。
在本发明的其中一个实施例中,所述生理参数为血氧、脉率、波形面积、灌注指数等的至少一个。
更多细节,可以参照前述对图21的描述,同时为了更好地理解本实施例中数字处理器的功能及工作原理,下面将结合一个具体的例子进行说明。
如图10所示,示出了本发明提供的一种计算生理参数的医疗设备中所采用的数字处理器的另一个实施例的结构示意图,该数字处理器采用频谱阵列图法(Power SpectrumArray,PSA)进行补偿,请一并结合图11所示,具体地,该数字处理器包括:
时频域转换单元11,用于选择通过采样获得的红光和/或红外光的至少一路信号所对应的一段区间的时域信号,对所述区间的时域信号进行时频域转换,获得至少一路频域信号;
频谱峰位置序列获得单元15,用于在所述频域信号中,选择其中所有合理的频谱峰信息,计算所选择的合理的频谱峰的位置信息,并形成频谱峰位置序列,所述合理的频谱峰信息为满足频谱能量关系、频谱幅度关系、频谱位置关系、频谱峰形态关系中的至少一个或多个;
补偿系数构建单元16,用于根据所述的频谱峰位置序列,构建稳定系数,如果所述稳定系数偏低,则利用所述的频谱峰位置序列构建随时间变化的阵列图,并通过该阵列图计算得到补偿系数,所述稳定系数为基于频谱能量比值偏差、频谱血氧偏差、基倍频组状态、合理的频谱峰个数中至少一个构建而成;
补偿处理单元17,用于使用所述的补偿系数补偿所述的时域信号和/或频域信号的至少一路,基于所述的已补偿的时域信号和/或频域信号计算获得生理参数,所述生理参数为血氧参数、脉率参数、波形面积参数、灌注指数参数中的至少一个。
其中,补偿系数构建单元16包括:
缓存单元160,用于建立缓存以存储频谱峰的相关信息,所述频谱峰的相关信息包括:每一频谱峰位置信息;每一频谱峰位置权重信息;频谱峰存储的数量信息;
频谱峰信息记录单元162,用于筛选所述频域信号中预定数量的频谱峰,依次填充到所述缓存中,将每一频谱峰的位置信息填写入,在相应的位置权重信息加一,总长度数量信息加一;
遍历处理单元164,用于在所述缓存中,假定每一个频谱峰作为疑似基频峰,遍历所有其它频谱峰,判断其它频谱峰与所述疑似基频峰是否满足频率的倍数关系,如果满足,则消除所述倍频峰在缓存中的相关信息,并将所述倍频峰的位置权重系数按照倍频次数折算并累加到所述相应疑似基频峰的位置权重系数上;反之保留其它频谱峰的相关信息;
补偿系数获得单元166,用于在最后保留的所述疑似频谱峰中,选择位置权重系数排在前列的三个频谱峰,确定其中一个作为最终的合理的频谱峰,以所述合理的频谱峰的信息作为补偿系数。
更多的细节,可参照前述对图6的描述。
相应地,本发明还提供了一种计算生理参数的医疗设备,在该实施例中,该医疗设备包括:
传感器,其包括至少一个发光管和至少一个接收管,所述发光管发射透射生理组织的至少两路不同波长的光信号,所述接收管接收透射生理组织的至少两路光信号,并转为电信号;
模数转换器,与所述传感器连接,将所述电信号转换为数字信号,该数字信号包含了生理组织的至少部分特征;
数字处理器,与所述模数转换器连接,所述数字处理器执行下述处理:
对一段区间的数字信号进行时频域转换,获得对应的频域信号;
在所述频域信号中,选择其中所有合理的频谱峰,计算所选择的合理的频谱峰的能量和/或位置信息,并形成频谱峰能量比值序列和/或频谱峰位置序列;
根据所述频谱峰能量比值序列和/或频谱峰位置序列构建稳定系数,偏低如果所述稳定系数偏低,使用所述频谱峰能量比值序列和/或频谱峰位置序列构建补偿系数;
使用所述的补偿系数补偿所述的时域信号和/或频域信号的至少一路,基于已补偿的时域信号和/或频域信号计算获得生理参数。
在本发明的其中一个实施例中,所述两路光信号,是红光和红外光。
在本发明的其中一个实施例中,所述生理组织的至少部分特征为血液中含氧血红蛋白、去氧血红蛋白、铁氧血红蛋白、总血红蛋白或一氧化碳的光学特征中的一项或多项。
在本发明的其中一个实施例中,所述合理的频谱峰为满足频谱能量关系、频谱幅度关系、频谱位置关系、频谱峰形态关系中的至少一个。
在本发明的其中一个实施例中,所述稳定系数为基于频谱能量比值偏差、频谱血氧偏差、基倍频组状态、合理的频谱峰个数中的至少一个构建而成。
在本发明的其中一个实施例中,所述补偿系数为基于频谱峰能量比值序列计算得到的能量比值偏差系数,或者为基于频谱峰位置序列随时间变化而统计得到的位置系数。
在本发明的其中一个实施例中,使用所述的补偿系数补偿所述的时域信号和/或频域信号的至少一路的处理具体为:
利用所述补偿系数,对所选择的时域信号做增益处理,以实现补偿;或者
利用所述补偿系数,对所选择的频域信号进行滤波处理,以实现补偿。
在本发明的其中一个实施例中,所述生理参数为血氧、脉率、波形面积、灌注指数等的至少一个。
更多细节,可以参照前述对图21的描述,同时为了更好地理解本实施例中数字处理器的功能及工作原理,下面将结合一个具体的例子进行说明。
如图12所示,示出了本发明提供的一种计算生理参数的医疗设备中所采用的数字处理器的另一个实施例的结构示意图,该数字处理器结合了静脉氧补偿法(Venous OxygenCompensation,VOC)以及频谱阵列图法(Power Spectrum Array,PSA)进行补偿,请一并结合图13所示,具体地,该数字处理器包括:
时频域转换单元11,用于选择通过采样获得的红光和/或红外光的至少一路信号所对应的一段区间的时域信号,对所述区间的时域信号进行时频域转换,获得至少一路频域信号;
相应序列构建单元18,用于在所述频域信号中,选择其中所有合理的频谱峰信息,计算所选择的合理的频谱峰的能量和/或位置信息,并形成频谱峰能量比值序列和/或频谱峰位置序列;所述合理的频谱峰信息为满足频谱能量关系、频谱幅度关系、频谱位置关系、频谱峰形态关系中的至少一个;可以理解的是,该相应序列构建单元18同时具有图8中能量比值序列构建单元13和图10中频谱峰位置序列获得单元15的功能,具体的细节可参照前述相应的描述;
补偿系数构建单元16,用于根据所述序列的至少一路的信号特征,构建稳定系数,同时判断述序列的至少一路的稳定系数是否偏低,如果稳定系数偏低,使用所述序列的至少一路的信号特征构建补偿系数;所述稳定系数为基于频谱能量比值偏差、频谱血氧偏差、基倍频组状态、合理的频谱峰个数中至少一个构建而成;补偿系数构建单元16可以基于频谱能量序列计算得到的能量比值偏差系数或血氧偏差系数,或者基于频谱位置序列随时间变化而统计得到的位置系数而构建所述补偿系数。可以理解的是,该补偿系数构建单元16同时具有图8中补偿系数构建单元16和图10中补偿系数构建单元16的功能,具体的细节可参照前述相应的描述;
补偿处理单元17,用于利用所述补偿系数补偿所述的时域信号和/或频域信号;基于所述的已补偿的时域信号和/或频域信号,进一步计算获得生理参数,其中,所述生理参数为血氧参数、脉率参数、波形面积参数、灌注指数参数中的至少一个。
其中,补偿处理单元17进一步包括:
时域补偿单元170,用于利用所述补偿系数,所选择的时域信号做增益处理,以实现补偿;或者
频域补偿单元172,用于利用所述补偿系数,对所选择的频域信号进行滤波处理,以实现补偿。
更多的细节,可参照前述对图7的描述。
为了便于更好地理解本发明,下文中将结合实际的例子来进一步说明前文中涉及的静脉氧补偿法(Venous Oxygen Compensation,VOC)以及频谱阵列图法(Power SpectrumArray,PSA)的原理及实现过程。
一、对于静脉氧补偿法(VOC)
申请人认为,在非干扰状态下,静脉血液由于其生理特性流动相对比较缓慢,可以认为是DC直流量的一部分,静脉血氧饱和度不会对正常的血氧测量产生任何影响。在干扰状态下,静脉血液受到干扰的影响,产生了静脉搏动,该静脉搏动形成的AC交流量就会混入动脉血液搏动所形成的AC交流量中。按照前文的公式1可知,此时计算得到血氧饱和度必然是偏离真实值的;从生理角度,可以理解为动脉波氧饱和度中混入了静脉氧饱和度,导致最终的血氧饱和度偏离血气值。
如图14所示,给出了一种静脉血搏动干扰动脉血搏动的示意图。在无法获取随机干扰源特征的情况下,时域算法几乎没有任何办法准确计算血氧饱和度值;另外,想要获取随机干扰源特征是非常困难的。
在背景技术中提到,频域信号中的每个频谱段都与血氧饱和度唯一对应,理论上每个频谱段都可以计算血氧饱和度;同时由于静脉干扰的随机性,其叠加在不同频段上的干扰也存在轻重之分。本申请所提出的静脉氧补偿法(VOC)即基于这两种假设模型而构建。当每个频谱段之间的血氧值偏差较大时,说明静脉搏动已经干扰到真实血氧结果,通过统计每个频谱段的血氧值偏差变化,得到差异分布特征,并以此构建补偿系数,以消除血氧采样信号中的干扰,最后再以消除了干扰的采样信号重新计算,即可获得无限逼近真实生理血氧的参数结果。
故静脉氧补偿法(VOC)的流程如下:
首先,在完成时频域变换后,统计分析频域信号中每个频谱段血氧饱和度之间的差异变化,从而得到差异分布特征。即从频谱信号中获取满足条件的频谱峰,进而计算每个频谱峰的血氧饱和度,得到血氧饱和度序列。其中,满足条件的频谱峰是指在幅度、能量、宽度、形态等符合纳入统计分析的范围,判断准则是依据生理信号的特征以及数字信号处理的基本方法建立的。基于血氧饱和度序列,统计得到血氧的均值(vMean)、标准差(vStd)、最大值(vMax)、最小值(vMin)等。
其次,构建补偿系数计算公式,基于差异分布特征计算得到补偿系数。
如图13所示,给出了补偿系数的计算流程。
第一步,将vMax与vMin的差值与第一阈值(Threshold1)进行比较,并将vStd值与第二阈值(Threshold2)进行比较,判断选择正常模式还是干扰模式。该第一阈值和第二阈值的选择是根据生理参数特征以及血氧系统特点所得到的经验系数,例如在一个例子中,第一阈值(Threshold1)可以取15%的血氧偏差,第二阈值(Threshold2)可以取5%的血氧偏差。
第二步,如果是正常模式,说明静脉氧引起的波动相对比较小,可以选取均值和标准差作为补偿系数计算公式的输入源。其中,均值作为分母的输入源,如果血氧序列中超过均值的血氧个数占序列总数的至少一半,则以vMean+vStd作为分子,反之以vMean–vStd作为分子。
第三步,与第二步是选择关系,如果是异常模式,需要引入重复因子。重复因子的来源有两种:1)统计血氧序列中满足一定数值(如,±2%)偏差的最大血氧集合,取该集合的均值作为重复因子,其中,此处的±2%为经验系数,可根据实际变化调整;2)选取血氧历史趋势的稳定段,例如4s~8s的稳定趋势,计算该集合的均值作为重复因子,同样该4s~8s时间段也为经验系数,可根据实际变化调整。将该重复因子作为分子输入源,将均值作为分母输入源。
第四步,将分子和分母参数输入下述公式2,计算得到补偿系数。计算公式如下所示,其中tabR是血氧与R曲线系数的映射表(如前文所述),通过输入的血氧值即可反查得到对应的R系数值。补偿系数就是分子血氧的R系数值与分母血氧的R系数值的比值。
Factorcompensation=tabR(Numerator)/tabR(Denominator)......................公式2
Factorcompensation是补偿系数,tabR(Numerator)就是将分子作为输入源后代入血氧与R曲线系数的映射表后查得的R系数值,tabR(Denominator)就是将分母作为输入源后代入血氧与R曲线系数的映射表后查得的R系数值。
其中,下述将结合一个实际的例子来说明如何在静脉氧补偿法(VOC)中如何计算获得补偿系数。如图16所示,给出了一种干扰状态下的频谱段血氧分布示意图,假设频谱信号在生理带宽0.3Hz~5Hz中有A、B、C、D四段频谱峰,并假设该频谱信号受到静脉氧随机搏动的影响,每段频谱峰通过红外光和红光比值换算得到的血氧饱和度值分别为96%、85%、90%、87%,该计算出的四个血氧饱和度值之间存在偏差。通过统计偏差分布特征,分别可以得到:vMean=88.3%,vStd=4.8%,vMax=96%,vMin=85%。判断vMax与vMin的偏差小于第一阈值(例如,15%),且vStd小于第二阈值(例如,5%),故选择正常模式。此时统计大于均值血氧的个数为2,占总血氧序列的50%,故选择分子为vMean+vStd=93.1%,分母为vMean=88.3%。查询血氧与R曲线系数的映射表,分别获得分子与分母对应的R值,代入公式2,即可计算得到修正因子约为1.172。
再次,利用该补偿系数补偿时域信号(频域信号是基于此段信号变换得到)因干扰而受到的损失。即用于频域变换的时域信号乘以补偿系数,得到补偿信号。在本申请的一个例子中,仅针对红光一路信号做补偿,作为示例。但在实际应用中也可以分化补偿系数,实现补偿每一路信号。
最后,利用完成补偿的时域信号再次变换到频域信号,再利用频域信号计算准确的血氧等参数。本发明实施例是基于频域算法给出的示例,实际应用中也可以省略频域方法,基于完成补偿的时域信号,利用时域算法获取准确的血氧等参数。
如图17所示,给出了静脉氧补偿法(VOC)的框架流程示意图。其整个过程为:选择时域信号一段区间,进行时频域转换,将时域信号转换到频域信号。利用生理信号特征以及数字信号处理的基本知识(例如:生理脉搏波频率范围、基倍频原理、形态特征等),选择合理的频谱峰并计算该频谱峰的血氧饱和度参数。按照前述步骤统计分析血氧分布系列,得到一系列特征信息,再根据这些特征信息判断血氧饱和度是否存在偏差(或者小的偏差)。如果没有,则输出血氧参数结果;反之,根据这些特征信息计算补偿系数,并补偿到时域信号中。最后再利用补偿后的时域信号重新做时频域转换,并基于新的频域信号选择合理的频谱峰并计算输出最终血氧饱和度参数。
从中可以看出,静脉氧补偿法(VOC)能够消除干扰引起的血氧测量偏差,无限逼近真实生理血氧值,极大的提供了干扰状态下血氧参数计算的准确性。
二、频谱阵列图法(PSA)
如背景技术中所述,当干扰存在并严重扰乱频谱信号时,从频谱上很难识别出生理频谱信息。例如在图4示出的频谱图中,只依据基倍频原理的能量和频率关系是没有办法识别到基频峰信息的。如何在干扰状态下识别到生理频谱峰?本申请基于噪声随机分布的特性,提出了一种假设理论。任何类型的干扰,例如:弱灌注、肢体擦碰、手指晃动等,在血氧采样信号中,均表现为一种随机干扰成分,干扰的强度与测量端的运动强度正相关。考虑到生理特征状态,绝大多数的干扰都呈现为随机白噪声分布;少数较为规律的干扰(例如:帕金森症等),由于其震动幅度相对较低,震动频率相对较高,而对血氧采样信号没有实质性的影响,即不影响血氧参数的测量。尽管干扰信号扰乱了频谱信号,使得生理频谱无法识别出来,但无论干扰信号怎么变化,生理频谱峰的特征始终存在某一个频点上并且在一定时间内不会发生变化或变化相对缓慢(生理特征);与此同时,干扰噪声是随机分布的,随着时间的变化,频谱特征也随之而发生变化。将每一时刻的频谱按照时间顺序依次排列,并纵向观察频谱信号的特征,就能够发现,绝大部分的频谱峰幅度和位置都在发生变化时,总存在至少一个频谱峰的位置是相对稳定不发生偏移的,这个频谱峰就是生理频谱峰(基频峰)。如果能够采用一种识别算法找出该频谱峰,也就意味找到了正确的脉率值。这就是频谱阵列图法的核心思想。
在本申请中,频谱阵列图法(PSA)的一般流程如下:
首先,建立缓存存储频谱峰的相关信息。例如:频谱峰位置信息,也即所在频率点(PeakArray);频谱峰位置权重信息(WeigtedArray);频谱峰存储的数量信息(ArrayIndex),其中位置信息和权重信息共用数量信息。一般而言,考察的频谱峰数量不能太多,过多会增加算法识别的复杂性和运算量,例如,可以默认选取20作为上限,超出不进行分析。可以理解的是,在实际应用中也可根据系统的需求,选取合适的分析数量。
其次,筛选频域信号中合理的频谱峰,填充到上述缓存中。筛选的准则是根据频谱峰的能量、幅度、形态、位置等信息综合而得到的。记录信息时,将频谱峰的位置信息填写入PeakArray,在WeigtedArray相应的位置权重加一,总长度ArrayIndex加一。以此类推,将一次计算识别到的所有频谱峰添加入缓存中。如果是≧2次记录信息,需要考虑待添加的频谱峰是否已经存于缓存中,如果存在,则WeigtedArray相应位置权重递增,反之按常规方式增加新的频谱峰。假设每一次计算间隔2S,缓存需要累积一定时间的频谱信息,才可以启动生理频谱峰的识别。该时间需要根据系统的实际需求设定,例如可以设定为10次计算,即20S的时间趋势。满足10次信息存储,则启动相关的趋势分析,同时在完成趋势分析之后,消减最早存储的频谱信息。
再次,根据缓存的信息识别真实生理频谱峰。根据基倍频原理,消除PeakArray中的倍频峰,同时倍频峰的权重系数按照倍频次数折算并累加到基频峰的权重系数(例如:基频峰权重系数是3,2次倍频峰权重系数是2,取权重系数2除以倍频次数2,得到调整后的权重系数1,累积到基频峰权重系数,即基频峰权重系数调整为4),同时消除该倍频峰存储在PeakArray和WeigtedArray中的信息,即初始化为0。详细流程如下图18所示,此时可以假定每一个频谱峰为基频峰,遍历所有其它频谱峰,判断其它频谱峰与该假定的基频峰是否满足频率的倍数关系,如果满足则是其倍频峰,消除该倍频峰的相关信息,反之保留。根据基倍频能量衰减的特性以及生理特性,一般倍频超过4倍以上影响相对较小,实际应用时可根据系统的需要选择设置。按照类似操作,遍历每个频谱峰,完成倍频峰的相关信息的消除。最后选择权重系数相对较大的前三个峰作为下一步的输入信息。
最后,判断频谱峰的最大权重系数是否大于或等于设定的阈值(例如:该阈值可设定为8,表示连续16s都存在稳定频谱峰,实际应用时可根据系统的需要选择设置)。如果有2个或以上的频谱峰满足权重系数大于或等于设定阈值,则需要进一步根据生理特性做出判断。例如:在干扰状态下,生理脉率不可能过高也不可能偏低。选择满足设定阈值的最为合理的频谱峰,计算脉率参数并输出,同时根据状态适当优化其它频谱峰的权重系数。
如图19所示,给出了频谱阵列图法(PSA)的流程示意图。从中可以看出,首先建立频谱峰信息缓存,按照时间顺序,填充缓存。当缓存填充满时,按照基倍频原则简化存储的频谱峰,再选择简化的频谱峰中满足设定阈值的频谱峰。如果满足条件的频谱峰大于或等于2个,则根据生理特性转化的准则排除,并最终选择1个合理的频谱峰,基于此频谱峰并计算脉率参数。频谱阵列图法(PSA)能够消除干扰引起的脉率测量偏差,即使在长时间的干扰状态下,也能够准确的识别生理频谱信息,极大的提供了干扰状态下脉率参数计算的准确性。
综上所述,静脉氧修正法(VOC)可以识别静脉氧的干扰并补偿干扰引起的血氧偏差,频谱阵列图法(PSA)可以在连续干扰中准确识别脉率信息。这两种方法各自具备干扰的识别和处理能力,因此,当两种方法结合运用时,可以显著的提升对干扰的识别和抑制,从而获得血氧参数计算准确性和脉率参数准确性的大幅度提升。
如图20所示,示出了本发明提供的方法中两种方案综合应用的示例。在实际应用中可以根据系统需要自适应的增加、删减、调整这些步骤。其大致流程如下:选择指定的一段时域信号,进行时频转换,并基于转换后的频谱信号进行频谱峰的检索和识别,同时计算每个合理的频谱峰的血氧值。统计合理峰的血氧值得到相关的统计信息为VOC做准备,同时也记录本次计算所得到的所有频谱峰的信息为PSA做准备。如果识别到基倍频组对并且基倍频组对中每个频谱峰血氧值相对偏差较小,则直接选择基频峰计算脉率,并输出最终结果的血氧和脉率值。如果基倍频组对不满足,则进入PSA方法并计算得到合理的频谱峰。如果是基于已消除噪声/补偿静脉氧的时域信号,但是血氧值不稳定(例如:和历史趋势结果不匹配),则只计算并输出脉率参数;反之如果血氧值稳定,则计算脉率值并输出最终结果的血氧和脉率值;如果是第一次计算(时域信号没有消除噪声/补偿静脉氧)且血氧值不稳定,则进入VOC识别分支。在VOC识别分支增加了一步基于PSA方法得到的频谱峰的特定滤波器。结合补偿系数和特定滤波器,对时域信号进行补偿和噪声消除,然后重新做时频域变换并计算相关参数。
综上,实施本发明实施例提供的方法以及医疗设备,具有如下的有益效果:
首先,本发明实施例基于频域技术并结合时域技术,能够在弱灌注和运动状态下,大幅度提升了血氧和脉率参数的计算准确性,为客户带来了卓越的临床性能体验,可极大地提高血氧参数的应用和推广;
其次,实施本发明,通过将时频域信号的特点与人体生理参数的特征相结合,在出现干扰情况下,采用静脉氧补偿法以及频谱阵列图法,在弱灌性和运动状态下提升计算脉率值以及血氧参数的准确度。其中,静脉氧补偿法可以消除干扰引起的血氧测量偏差,无限逼近真实生理血氧值,极大的提供了干扰状态下血氧参数计算的准确性;频谱阵列图法方法可以消除干扰引起的脉率测量偏差,即使在长时间的干扰状态下,也能够准确的识别生理频谱信息,极大的提供了干扰状态下脉率参数计算的准确性;
另外,本发明实施例提供的方法,计算复杂度低,对运算资源需求低。
本领域普通技术人员可以理解实现上述实施例方法中的全部或部分步骤是可以通过程序来指令相关的硬件来完成,程序可以存储于一计算机可读取存储介质中,的存储介质,如ROM/RAM、磁盘、光盘等。
以上仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
- 一种生理参数的计算方法及相应的医疗设备
- 一种生理参数的计算方法及相应的医疗设备
