一种Au NPs@WP5/BiOBr复合材料的制备方法和应用
文献发布时间:2023-06-19 12:04:09
技术领域
本发明涉及于光电化学技术领域,尤其涉及一种Au NPs@WP5/BiOBr复合材料的制备方法和应用。
背景技术
血红蛋白(Hb)又称血色素,是人体必需的物质,是红细胞的主要组成部分,能与氧结合,运输氧和二氧化碳。血红蛋白含量能很好地反映贫血程度。人体内血红蛋白的正常范围为:男性 130~175 g/L;女性 115~150 g/L;新生儿 170~200 g/L。血红蛋白减少会引起各种贫血(如再生障碍性贫血、缺铁性贫血、铁粒幼细胞性贫血、巨幼细胞性贫血、溶血性贫血、地中海性贫血等)、大量失血(如外伤大出血、手术大出血、产后大出血、急性消化道出血、溃疡所致的慢性失血等)、白血病、产后、化疗、钩虫病等。因此,有必要找到一种用于临床分析的检测血红蛋白的理想方法。由于牛血红蛋白(BHb)与人血红蛋白的相似度高达90%,而人血红蛋白价格高昂,因此本发明后续实验均用牛血红蛋白代替人血红蛋白进行相关实验。
用于Hb检测的技术很多,包括比重法,比色法,分光光度法,荧光光谱法,Kurt电阻法和电化学法。其中,最有优势的方法是电化学分析,因为它具有高灵敏度,便携性,低成本仪器,快速检测和易于自动化的特点。血红素中心深深地嵌入蛋白质中,导致电极表面与大蛋白质之间电子转移困难,所以血红蛋白难以直接电氧化还原。另外,蛋白质吸附到电极表面上会引发Hb变性和电极钝化。因此本发明利用多巴胺与牛血红蛋白的吸附作用,进而间接检测牛血红蛋白。
BiOBr作为Bi基半导体材料之一,因其独特的层状晶体结构、高效的可见光吸收和电荷转移能力而受到研究人员的关注。这种独特的层状结构为原子和原子轨道的极化提供了充分的可能性,促进了光诱导电子和空穴的分离,从而提高了光电化学性能。然而,BiOBr的带隙约为2.64 ~ 2.91 eV,导致BiOBr在可见光区吸收较弱,限制了BiOBr的潜在应用。为了拓宽BiOBr的应用范围,有必要对其进行改性研究。BiOBr的改性方法包括形貌控制、元素掺杂、金属沉积和形成新的异质结。其中,金属沉积改善了可见光吸收,促进了表面电荷转移,从而提高了光电化学性能。金纳米颗粒的表面等离子体共振能促进BiOBr的光吸附,提高其光电化学性能。金纳米离子因其易于合成、化学稳定性高、易于表面功能化等特点,已成为新型杂化纳米材料的重要组成部分。并且金纳米离子具有良好的生物相容性、优秀的导电性及局域表面等离子共振效应。同时,大环宿主(环糊精、杯芳烃、瓜环等)具有独特的尺寸不可及的腔结构,并表现出特殊的性质。柱[n]芳烃由对苯二酚或其衍生物在其2和5位由亚甲基(- CH2 -)桥连接而成。与冠醚和杯芳烃相比,柱芳烃具有更强的刚性结构;另一方面,与环糊精和葫芦烯相比,柱[n]芳烃更容易改性。作为新兴的大环芳烃宿主家族,柱[n]芳烃以其新颖刚硬的对称柱状结构、疏水性供电子腔、独特而优异的主宾功能和可调功能的边缘等特点受到广泛关注。近年来,贵金属纳米掺杂有机材料的制备因其先进的电子、光学和生物性能而引起了人们的极大兴趣。因此,在BiOBr半导体表面负载AuNPs@WP5不仅提供了一种新型的杂化纳米材料,而且有望带来新的性能、功能和应用。
发明内容
本发明提供一种Au NPs@WP5/BiOBr复合材料的制备方法和应用,解决原有检测技术灵敏度低、检测范围有限、对环境污染严重、仪器昂贵、需要专门操作人员、效率低,速度慢、不易操作等技术问题。
本发明采用以下技术方案:一种Au NPs@WP5/BiOBr复合材料,由溴氧化铋纳米花片层内负载Au NPs@WP5,制备出Au NPs@WP5/BiOBr复合材料。
作为本发明的一种优选技术方案:所述BiOBr纳米花的直径为:400-450 nm。
一种Au NPs@WP5/BiOBr复合材料的制备方法,包括以下步骤:
步骤1,制备溴氧化铋纳米花:将0.485g Bi(NO)
步骤2,采用还原氯金酸的方法制备金纳米颗粒:取150 mL去离子水,加热至沸腾,向其中加入0.9 mL H
步骤3,制备水溶性柱芳烃;
步骤4,Au NPs@WP5的合成:采用超声混合的方法,将金纳米粒子和水溶性柱芳烃(n Au NPs:n WP5 = 1:18)分散在水溶液中,超声1.5 h,制备Au NPs@WP5复合材料;
步骤5,Au NPs@WP5/BiOBr的合成:将步骤1所得的溴氧化铋纳米花分散在水溶液中,并向其中滴加Au NPs@WP5复合材料,保证n BiOBr:n Au NPs@WP5=1:20,搅拌40 min,形成Au NPs@WP5/BiOBr复合材料。
本申请还保护了一种Au NPs@WP5/BiOBr复合材料在光电传感器中的应用,所述光电传感器由Au NPs@WP5/BiOBr滴涂在玻碳电极表面制成。
作为本发明的一种优选技术方案:在氙灯模拟的可见光源的条件下,利用电化学工作站、所述光电传感器用于多巴胺的光电化学分析。
作为本发明的一种优选技术方案:所述光电传感器用于多巴胺的光电化学分析中,多巴胺溶液里依次滴加不同浓度的牛血红蛋白溶液,利用牛血红蛋白和多巴胺的吸附作用来间接的检测牛血红蛋白。
有益效果
本发明所述一种Au NPs@WP5/BiOBr复合材料的制备方法和应用采用以上技术方案与现有技术相比,具有以下技术效果:
1、由于血红蛋白是大分子蛋白质难以用电化学方法直接检测,本发明利用多巴胺与血红蛋白的吸附作用设计一种间接性检测血红蛋白的方法。在可见光照下,溴氧化铋可生成光生电子空穴,金纳米粒子的局域表面等离子共振以及水溶性柱芳烃与多巴胺的主客体络合作用相结合,形成Au NPs@WP5/BiOBr复合材料,并将此材料修饰电极此方法在可见光照下利用电化学方法高效灵敏的检测牛血红蛋白。解决原有检测技术灵敏度低、检测范围有限、对环境污染严重、仪器昂贵、需要专门操作人员、效率低,速度慢、不易操作等技术问题;
2、本文检测范围为10
附图说明
图1是本申请中BiOBr(a)与AuNPs@WP5/BiOBr(b)TEM图。
图2是本申请中BiOBr、Au、Au@WP5、Au@WP5/BiOBr 的XRD粉末衍射图(a)和BiOBr、WP5、Au、Au@WP5、Au@WP5/BiOBr的红外光谱(b)图。
图3是本申请中BiOBr、Au@WP5、Au@WP5/BiOBr 修饰的玻碳电极在5 mM K
图4是本申请中的BiOBr、Au NPs@WP5、和Au NPs@WP5/BiOBr修饰的GCE在可见光照射下检测0.5 mM DA (pH = 7.0)时的DPV曲线图。
图5是本申请中Au NPs@WP5/BiOBr修饰的GCE在检测不同pH 0.5 mM DA时的DPV曲线图。
图6为本申请中Au NPs@WP5改性GCE在用不同扫描速度检测0.5 mM CA时的LSV曲线图。
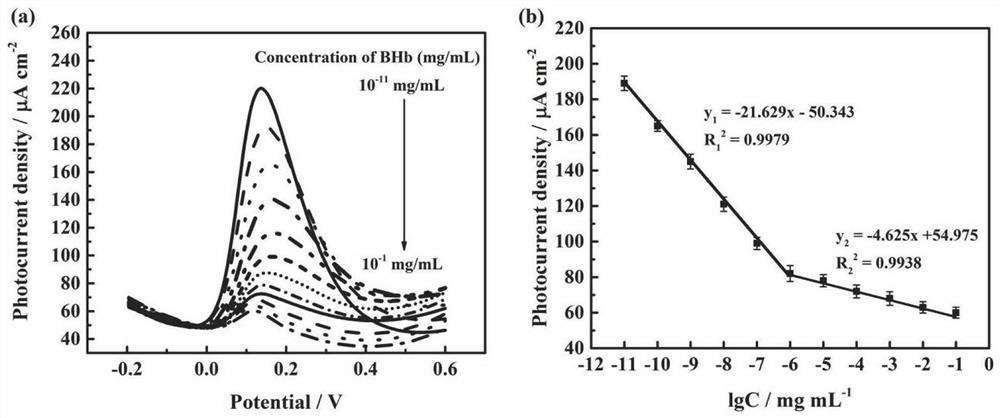
图7为本申请中Au NPs@WP5/BiOBr修饰的GCE在含有0.5 mM DA时,滴加不同牛血红蛋白溶液浓度时(10
图8为本申请中Au NPs@WP5/BiOBr修饰的GCE在含有 0.1 mM DA 的 0.1 M PBS(pH = 7.0) 溶液中的 i-t 曲线。时间间隔为30 s图。
图9为本申请中Au NPs@WP5/BiOBr修饰的GCE对牛血红蛋白、牛血清蛋白、鸡蛋白蛋白、溶酶菌及ATP的选择性,每个化合物的浓度为300 μg/mL图。
图10为本申请中WP5的合成方法图。
具体实施方式
以下结合实例对本发明作进一步的描述,实施例仅用于对本发明进行说明,并不构成对权利要求范围的限制,本领域技术人员可以想到的其他替代手段,均在本发明权利要求范围内。
实施例1:
一种Au NPs@WP5/BiOBr复合材料的制备方法,步骤为:
步骤1,制备溴氧化铋纳米花:将0.485g Bi(NO)
步骤2,采用还原氯金酸的方法制备金纳米颗粒:取150 mL去离子水,加热至沸腾,向其中加入0.9 mL H
步骤3:制备水溶性柱芳烃,如图10所示;
步骤4,Au NPs@WP5的合成:采用超声混合的方法,将金纳米粒子和水溶性柱芳烃(n Au NPs:n WP5 = 1:18)分散在水溶液中,超声1.5 h,制备Au NPs@WP5复合材料。
步骤5,Au NPs@WP5/BiOBr的合成:将步骤1所得的溴氧化铋纳米花分散在水溶液中,并向其中滴加Au NPs@WP5复合材料,保证n BiOBr:n Au NPs@WP5 = 1:20,搅拌40 min,形成Au NPs@WP5/BiOBr复合材料。
实施例2
物理表征:
BiOBr,Au NPs@WP5/BiOBr的形貌测定。
图1的(a)、(b)分别是实施例1中步骤1制备出来的BiOBr纳米花和步骤5中制备出来的Au NPs@WP5/BiOBr的透射电镜图。结果表明,图示(a)中能够观察到合成的BiOBr纳米花直径为400-450 nm,且分散均匀。图示(b)可以看出制备的Au NPs@WP5比较均匀地分散在BiOBr纳米花的片层中,说明Au NPs@WP5/BiOBr复合材料的成功制备。
Au NPs@WP5/BiOBr复合材料的XRD粉末衍射和红外表征。
图2是步骤5中制备出来的BiOBr、Au NPs 、Au NPs@WP5、Au NPs@WP5/BiOBr复合材料的XRD粉末衍射图,从图上可以看出,对于Au NPs@WP5/BiOBr,在21.51° 、25.07°、25.29°、43.90°、57.53°分别为BiOBr的(101)、(102)、(110)、(200)及(212)晶面,在38.34°、42.96°、78.68°存在Au NPs的(111)、(200)及(311)晶面,表明Au NPs@WP5/BiOBr复合材料的成功合成。
实施例3
对多巴胺的电化学性质测试:
将上述实施例1中得到的Au NPs@WP5/BiOBr取10 μL滴涂在GCE表面,使其在50摄氏度的红外灯旁干燥,得到Au NPs@WP5/BiOBr修饰改性的GCE。将多巴胺溶解于PH=7.0的PBS中作为待测物,通过传统的三电极法,利用氙灯模拟可见光源照射GCE电极表面,控制遮光间隔时间作为可调控“开-关”,再用电化学工作站进行光电化学检测。
电化学表征:
如图 3 所示,通过在含有 5.0 mM K
在可见光照下对多巴胺的检测:
图4是BiOBr/GCE、Au NPs@WP5/GCE以及 Au NPs@WP5/BiOBr/GCE电极分别含有0.5mM DA的 0.1 M 的磷酸缓冲溶液 (pH = 7.0) 混合溶液中的差分脉冲曲线图。图4中DA在Au NPs@WP5 和 BiOBr/GCE电极上的氧化峰电流分别是 136 和 164 μA/cm
Au NPs@WP5/BiOBr电极检测多巴胺和尿酸的电化学参数优化:
我们研究了电解质溶液的酸度对 Au NPs@WP5/BiOBr/GCE 检测 DA的影响。如 图5所示,随着溶液的 pH 从 3.0 到 8.0,DA氧化峰电位先上升再下降。当 pH 值增加到 7.0时,氧化峰电流最大。因此,0.1 M pH = 7.0 的 PBS 作为最优 pH 参数应用在实验中。
实验中研究了扫描速率对 DA在 Au NPs@WP5/BiOBr/GCE 电极上的氧化还原反应的影响,如图6所示。图6 b中的线性回归方程为:Ipa(DA) = 1.0866ʋ (mV s
实施例4
对牛血红蛋白的电化学检测:
差式微分脉冲伏安法 (DPV) 被用 Au NPs@WP5/BiOBr/GCE 电极在 0.1 M PBS(pH=7.0) 的磷酸缓冲液中高灵敏性和选择性地检测 DA。在检测过程中, DA的浓度不变,不断的往DA溶液中滴加不同浓度的牛血红蛋白溶液。如图7所示,氧化峰电流随着牛血红蛋白浓度的增加而减弱。这是由于DA的浓度几乎不表,而随着牛血红蛋白的逐渐加入,牛血红蛋白与多巴胺存在吸附作用,溶液中游离的多巴胺将会减少,此时DA地氧化峰电流将会下降。将不同浓度的牛血红蛋白加入到含有 0.5 mM DA 的 50 mL 0.1 M PBS 溶液中检测(图7a), 电压为 -0.2-0.6V, 氧化峰电流和牛血红蛋白的浓度之间有良好的线性关系,分两段,分别为:Ipa(BHb) = -21.629C
实施例5
Au@WP5改性GCE的稳定性、重复性、选择性:
稳定性:
稳定性是评价所制作传感器的一个重要参数,在0.5 mM的DA溶液中,通过对所修饰的Au NPs@WP5/BiOBr/GCE电极进行相应测试。在循环约900秒后,光电流密度几乎没有变化,如图8所示。另外,在室温下放置10天后,PEC传感器上的光电流信号保留了初始光电流值的~90.68%,确认了Au NPs@WP5 BiOBr/GCE传感器的可接受稳定性。
重复性:
在相同条件下,通过在五个平行Au NPs@WP5/BiOBr/GCE电极上测定0.5 mM DA溶液来评估所制备的PEC传感器的重复性。相对标准偏差(RSD)被计算为3.87%,这说明了该传感器的优良重复性。
选择性:
如图9所示,为了评估Au NPs@WP5/BiOBr/GCE对BHb分析的选择性,我们以牛血清蛋白(BSA)、鸡蛋白蛋白(EA)及溶酶菌(Lyz)为对照蛋白,并研究了小分子的物理吸附,如三磷酸腺苷(ATP)。每个分子的浓度是10
上述的对实施例的描述是为便于该技术领域的普通技术人员能理解和使用发明。熟悉本领域技术的人员显然可以容易地对这些实施例作出各种修改,并把在此说明的一般原理应用到其他实施例中而不必经过创造性的劳动。因此,本发明不限于上述实施例,本领域技术人员根据本发明的揭示,不脱离本发明范畴所做出的改进和修改都应该在本发明的保护范围之内。
- 一种Au NPs@WP5/BiOBr复合材料的制备方法和应用
- 一种混晶TiO2/BiOBr复合材料及其制备方法和应用
