一种基于环介导等温扩增的流感病毒H10N3快速检测试剂、试剂盒及使用方法
文献发布时间:2023-06-19 18:37:28
技术领域
本发明涉及生物医学检测技术领域,尤其涉及一种基于环介导等温扩增(LAMP)的流感病毒H10N3快速检测试剂盒。
背景技术
流感是一种呼吸道疾病,其引起的季节性暴发使全球每年感染5%至15%的人口,是全球高死亡率的重要原因之一。根据WHO(World Health Organization)报告,全球每年有高达65万人因流感死亡,仅2019年前5个月,流感上报发病病例已高达177万,超过了过去四年的流感上报人数总和。流感病毒根据核蛋白和基质蛋白不同,分为A、B、C、D(甲、乙、丙、丁)四型。而根据CDC报告的18种不同的血凝素(HA,Hemagglutinin)和11种不同的神经氨酸酶(NA,Neuraminidae)排列组合的198种亚型,其中有131种在流行,目前感染人的主要是甲型流感病毒中的H1N1、H3N2亚型及乙型病。流感病毒毒株的多样性阻碍了对其的特异性检测,因此需要开发一种快速、选择性和灵敏的诊断方法来快速检测流感病毒。尤其是近两个月来,国内外均出现了H10N3流感病毒感染人的病例报告,应该予以重视。目前对流感的检测方法有多种,传统鉴定流感病毒的方法是根据《全国临床检验操作规程》常规分离病毒,这些检测手段不仅需要专业技术人员和复杂的设备仪器,同时鉴定过程耗时长(48h以上),操作复杂,灵敏性低。临床上迫切需要研制一种可以快速有效检测流感病毒的方法。
目前已开发的众多用于流感病毒临床检测方法中,病毒培养最为常规。然而,使用细胞培养检测目标病毒需要长达14天的时间。基于病毒表面抗原检测的直接荧光免疫检测法已被用于快速识别流感病毒,然而,由于免疫测定中使用的抗体其交叉反应性和低检测灵敏度,使其不能同时有效地为流感病毒分型。为了准确识别流感病毒类型,通常使用包括RT-PCR(Reverse Transcription-Polymerase Chain Reaction)的分子实时诊断方法。但是荧光定量PCR是现阶段病毒检测的优选方案,但其存在以下局限性:(1)容易产生气溶胶污染导致结果出现假阳性,需配备经专业培训并执PCR上岗证的技术人员、专业PCR认证实验室与价格昂贵的温度变换控制分析仪器;(2)传统荧光定量PCR样本核酸提取和扩增检测分两步骤进行,从取样到出具检测结果至少需要2-3小时以上。虽然最近已开发出通过单个靶基因的多重PCR实时扩增技术,但其多达90~120分钟的扩增检测过程与对实验设备和实验人员的严苛要求显然不适合于快速检测。
发明内容
本发明的目的在于针对现有技术的不足,提供一种基于LAMP的流感病毒H10N3快速检测试剂、试剂盒及使用方法,本发明具有准确率高、检测速度快的特点,能够特异性的对流感病毒H10N3检测。
为了实现本发明的上述目的,本发明采用以下技术方案或组合:
首先,本发明提供一种基于LAMP的流感病毒H10N3快速检测试剂,所述试剂包括用于检测H10N3病毒引物组,所述引物组包括双基因扩增引物和环引物,所述双基因包括基因NA和基因HA,每条基因均包括多个位点的扩增引物,相对于现有的荧光定量PCR检测法具有准确率高、检测速度快的优势。
所述试剂包括用于检测甲型流感病毒H10N3的引物组和探针;所述引物组包括上游引物和下游引物,其中,
用于扩增NA基因的引物包括四条,分别是引物H10N3-NA-F3、引物H10N3-NA-B3、引物H10N3-NA-FIP和引物H10N3-NA-BIP;其核苷酸序列分别如序列表SEQ ID No.1-4所示,
SEQ ID No.1:CTGTGATAAACAACATAACAACAAC,
SEQ ID No.2:TGTTTAGTTCCTAGCAATGC,
SEQ ID No.3:GTGGAAGGGGAAGAACCCTCTAATAACTGAAGCAGAA AAGCCT,
SEQ ID No.4:GGTGAGAACAAAGATGTCATAGTCACTTGTGCGAGAG CAAAGG。
用于扩增基因HA的引物包括四条,分别是引物H10N3-HA-F3、引物H10N3-HA-B3、引物H10N3-HA-FIP和引物H10N3-HA-BIP;其核苷酸序列分别如序列表SEQ ID No.5-8所示,
SEQ ID No.5:CAAAAAGAGCCTGTTGCTT,
SEQ ID No.6:GTTATTTGATCTATAGCTGCCT,
SEQ ID No.7:ATCCAGCTATTGCTCCAAACAGGGCTACTGGAATGAG GAATGT,
SEQ ID No.8:GGAAGGAATGGTAGATGGTTGGTGAGTACTTTTGTAAT CCGCG。
优选地,所述引物和探针用于检测流感病毒H10N3的NA和HA基因。
优选地,所述目视比色中,FAM为荧光基团,BHQ1为淬灭基团。
进一步地,荧光基团还可以为Texas Red、TAMRA、ROX、HEX和JOE中的一种或多种。
在此基础上,本发明提供一种基于LAMP的流感病毒H10N3快速检测试剂盒,所述试剂盒含有上述的试剂,所述试剂盒还包括缓冲液、LAMP扩增反应体系和RNA提取试剂盒。利用该试剂盒可以对H10N3进行检测,准确率高、速度快,30分钟左右即可取得结果。
优选地,所述LAMP扩增反应体系以50μL计包括:
流感病毒H10N3模板RNA 1.0~10μL;
上游引物1.0~5.0μL;
下游引物1.0~5.0μL;
环引物0.5~5μL;
扩增buffer 25μL;
扩增酶bsu 0.5~2.5μL;
RNase-free水灭菌去离子水补至50μL。
本发明还提供上述试剂盒的使用方法,包括以下步骤:
(1)RNA模板提取:提取待测样品中的RNA;
(2)LAMP扩增反应:以步骤(1)提取的RNA为模板,并采用试剂盒中的LAMP引物与扩增酶,在LAMP反应管中进行LAMP扩增反应;
(3)荧光检测分析LAMP扩增产物。
进一步地,所述待测样品包括H10N3核糖核酸(HIN1 RNA)液体室内质控品中的至少一种。
进一步地,所述待测样品包括鼻咽拭子保存液、口咽拭子保存液、痰液的至少一种。
进一步地,所述LAMP扩增为恒温扩增,扩增反应的温度为63-65℃,扩增时间为1-60min,优选为63℃,扩增3-20min。
在本发明中,荧光检测分析可利用任何一款能识别并采集荧光信号的仪器,且其发光基因包括但不限于FAM通道,还包括Cy3,Cy5,Texas Red,Alexa Flour,ROX,JOE等所有系列等荧光检测基团。
更优选地,恒温反应可选用任意能控温的装置,包括但不限于水浴锅,恒温箱等。
与现有技术相比,本发明的有益效果为:
(1)本发明以H10N3的溶血素基因(hemagglutinin,HA)和神经氨酸酶(Neuramidinase,NA)为检测靶标,设计了LAMP检测引物及探针,进而建立了一种基于恒温扩增的联合检测方法。
(2)本发明的检测多种感染呼吸道病毒的LAMP引物及探针,能够用以完成对临床患者或门诊筛查多种院内感染呼吸道病毒的检测;本发明试剂盒具有特异性、价廉、灵敏、便携使用等特点;采用本发明的试剂盒能够有效、特异性地检测出单反应单拷贝及以上的多种院内感染呼吸道病毒。
(3)使用本发明的LAMP引物及探针进行检测,可以在一个反应里实现检测一至多种不同的荧光信号,还可以对多个样本进行同时检测,有效的简化了系统设计,避免了由于样品光学检验时间不同造成的不准确性等问题。
(4)相对于“金标准”实时荧光定量PCR,采用本发明的试剂盒以LAMP方法进行检测,引物和探针灵敏度高,检测准确率较高、灵敏度较高,30分钟内即可完成检测。
(5)本发明采用H10N3的溶血素基因(hemagglutinin,HA)和神经氨酸酶(Neuramidinase,NA)为检测靶标进行LAMP检测引物及探针设计,进行检测,准确性较高。
(6)本发明采用多酶优化配比并冷冻干燥形成干粉酶与扩增管中,减去了反转录过程,检测时间和操作步骤优化,方法更简便。
(7)本发明LAMP引物及探针,已经过临床真实患者咽拭子样本检测验证,符合率100%,准确性及特异性非常高,更具有临床应用试验效果的说服力。
综上所述,本发明提供的基于环介导等温扩增技术(LAMP)的流感病毒H10N3快速检测试剂盒可以广泛应用于临床上流感病毒H10N3的检测。多重实时RT-LAMP快速检测,于单一体系中对多个待测样本进行定量检测,具有准确率高、检测速度快的优势。并且,本发明将引物探针组整合于单一扩增体系,实现实时快速扩增检测体系的微量化,对未知流感病毒的鉴定提供技术支持,做到早定型、早发现、早治疗。
附图说明
为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
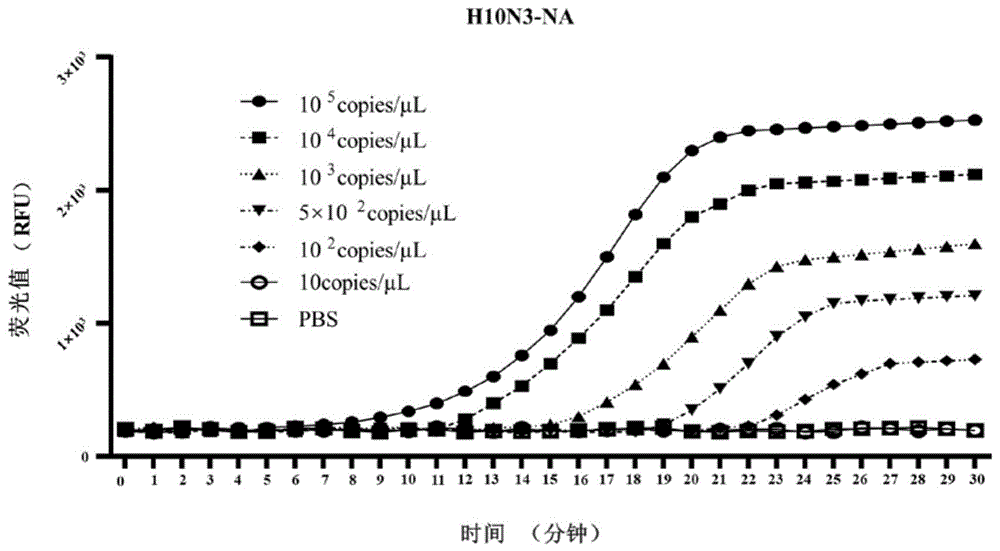
图1是实施例3中H10N3实时RT-LAMP的灵敏度测定曲线图;
图2是实施例3中H10N3实时RT-LAMP的特异性测定曲线图。
具体实施方式
下面将结合实施例对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
在本发明的实施例中,除非有明确的限定,术语靶标基因应做全基因片段理解,基因不局限于引物探针所涉及的片段,还可以是该基因的其他可设计引物的区域。
在本发明中,荧光探针不局限于FAM,还可以为GFP、Texas Red、DAPI、AlexaFluor@488、FITC、Cy3、Cy5、Cy7、ROX、JOE及Alexa Fluor@750等其他荧光激发集团。
在本发明中,所述检测样本可为病毒核酸模板、咽拭子、病毒培养液、含有甲流、乙流病毒的痰液和肺泡灌洗液中的至少一种。对于本领域的普通技术人员或相关检测人员而言,可以根据具体情况理解上述术语在本发明中的具体含义。
在本发明中,所述的聚合酶成分:Bsu RNA聚合酶为市售成品。
以下实施例中,所用的试剂、仪器等都能通过商业途径购得。
实施例1引物及探针设计
根据NCBI已公示的流感病毒H10N3基因组碱基序列,查找比对HA和NA基因碱基序列,按照引物设计原则人工创造性设计引物并分别验证所设计引物的GC含量等参数保证其达最适范围。与此同时,根据LAMP探针引物的设计原则分别设计对应的探针。
获得如下针对流感病毒H10N3其HA和NA基因的引物及环引物:
以上所述引物、环引物可用于检测流感病毒H10N3的HA和NA基因。
将设计完毕的多组引物送至生工生物工程(上海)股份有限公司进行合成,获得引物后添加RNase-free水稀释成10mmol/μL备用。
实施例2LAMP扩增体系
一种基于重组酶聚合酶扩增技术(LAMP)流感病毒H10N3检测试剂盒,所述试剂盒包括实施例1的引物和探针;
所述试剂盒还包括再水化缓冲液、醋酸镁、RNase-free水、灭菌去离子水、RNA提取试剂盒(QIAamp Viral RNA Kits(50))、扩增酶;扩增酶为BSU RNA聚合酶。
需要说明的是,所述RNA提取试剂盒用于提取待测样品中的RNA作为模板;RNA提取试剂盒可以采用常规的市售的RNA提取试剂盒,本实施例中,采用的RNA提取试剂盒为QIAGEN的RNA提取试剂盒QIAamp Viral RNA Kits。
本实施例试剂盒包括如下LAMP扩增反应体系:
用于检测流感病毒H10N3的LAMP扩增反应体系,该反应体系含有实施例1中用于检测流感病毒H10N3的引物探针组;
所述用于检测流感病毒H10N3、的LAMP扩增体系以50μL计包括:
优选地,所述LAMP扩增反应体系以50μL计包括:
流感病毒H10N3模板RNA 1.0~10μL;
上游引物1.0~5.0μL;
下游引物1.0~5.0μL;
环引物0.5~5μL;
扩增buffer 25μL;
扩增酶bsu 0.5~2.5μL;
RNase-free水灭菌去离子水补至50μL。
所述试剂盒的使用方法,包括以下步骤:
(1)RNA模板提取:提取待测样品中的RNA,同时以无RNA酶去离子水为阴性对照;
(2)LAMP扩增反应:以步骤(1)提取的RNA为模板,并采用试剂盒中的LAMP引物与探针,在LAMP反应管中进行LAMP扩增反应。
实施例3LAMP引物的灵敏性检测
(1)提供实施例2的试剂盒,按照如下的反应体系进行各试剂的添加,具体包括:
按照例1所述的组分添加进行扩增。
(2)即时将反应管置于提前设置好的可收集荧光信号的仪器中,LAMP反应条件为63℃,反应40分钟,每30S收集一次荧光信号。
具体灵敏性检测荧光信号图如图1所示,可达检测灵敏度10copies/μL。
实施例4LAMP引物的特异性检测
选取流感病毒H10N3及PBS缓冲液为模板进行LAMP引物的特异性验证。直接利用购买的试剂盒抽提流感病毒H10N3模板RNA后测其浓度并折算成拷贝数,并按10倍稀释为系列浓度梯度,包括10
提供实施例2的试剂盒,按照如下的反应体系进行样本各试剂的添加,具体包括:流感病毒H10N3模板RNA 1.0~10μL;
上游引物1.0~5.0μL;
下游引物1.0~5.0μL;
环引物0.5~5μL;
扩增buffer 25μL;
扩增酶bsu 0.5~2.5μL;
RNase-free水灭菌去离子水补至50μL。
及时将反应管置于提前设置好的可收集荧光信号的仪器中,LAMP反应条件为63℃,反应40分钟,每30S收集一次荧光信号。
具体特异性检测的结果如表1所示,选取已经过鉴定的分离自口腔痰液及呼吸道等常见病毒,包括H1N1、H3N2、鼻病毒、呼吸道合胞病毒等(图2)进行常规培养,并最终进行浓度测定,抽提核酸并换算成拷贝数,使之浓度达10
表1:
上述表格中“+”代表出现扩增,“-”代表未出现扩增。
实施例5LAMP方法与荧光定量PCR方法的比较验证
选取流感病毒H10N3(10
LAMP反应按照如下的反应体系进行各试剂的添加,其中各基因检测引物和探针不混合添加,分别进行扩增,具体包括:流感病毒H10N3模板RNA 1.0~10μL;
上游引物1.0~5.0μL;
下游引物1.0~5.0μL;
环引物0.5~5μL;
扩增buffer 25μL;
扩增酶bsu 0.5~2.5μL;
RNase-free水灭菌去离子水补至50μL。
即时将LAMP反应管置于提前设置好的可收集荧光信号的仪器中LAMP反应条件为63℃,反应40分钟,每30S收集一次荧光信号。
荧光定量PCR反应,按照世卫组织所推荐的检测引物及探针,并利用商品化的定量检测试剂盒进行扩增,反应体系为:
M基因:
反应条件为:PCR酶激活(预变性)15min 95℃;
循环扩增:
图2为本实施例LAMP法检测流感病毒灵敏性分析,由图2可知本方法10分钟之内即可检测出病毒H10N3的存在,30分钟之内即可完成单病毒基因检测;与定量PCR扩增结果准确度拟合性结果分析显示,本实施例LAMP法检测结果和荧光定量PCR检测结果没有显著性差异,拟合率在100%,目前核酸检测金标准还是荧光定量PCR,提示我们建立的方法检测效率和荧光定量PCR检测准确率相同,但检测时间大大缩短。
应用例1LAMP方法临床样本测试分析
选取临床样本抽提核酸60例(咽拭子);
使用实施例2的试剂盒进行临床样本测试分析,具体结果如下,未见扩增条带,经金标准PCR鉴定证实所检测样本不包含H10N3。
最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。
