苯酞类化合物合成酶LcP450、编码其核苷酸序列及应用
文献发布时间:2023-06-19 19:30:30
技术领域
本发明属于生物工程的技术领域,涉及苯酞类化合物合成酶LcP450、编码其核苷酸序列及应用,所述酶可用于3-取代苯酞类化合物(如丁烯基苯酞)的生物合成。
背景技术
苯酞类化合物是从药用植物中分离出来的一类具有药物活性的化合物。药用植物川芎(Ligusticum chuanxiong hort.)是伞形科藁本属植物,以根部入药,在我国主要分布在四川。川芎在传统中药中用于月经不调、闭经痛经、症瘕腹痛、胸胁刺痛、跌扑肿痛、头痛、风湿痹痛等相关疾病的治疗。目前,已有近60种苯酞类化合物从川芎中被分离出来,其中主要包括藁本内酯、丁烯基苯酞等化合物,它们具有舒张血管、抗氧化、抗血栓、抗菌消炎等多种药理作用。不同的修饰位点和不同的取代基使苯酞类化合物具有结构多样性,同时也赋予苯酞类单聚体化合物不同的生理功能和药用价值。其中,丁烯基苯酞在动物模型中,发现其可以有效抑制胶质瘤的生长。同时,丁烯基苯酞也可以作为临床上治疗缺血性脑卒中药物丁基苯酞的合成的前体物质。因此,解析丁烯基苯酞合成通路的研究,对于利用基因工程手段提高川芎中丁烯基苯酞和丁苯酞的含量具有重大意义。
细胞色素p450(Cytochrome p450,CYP450)在生物界中广泛存在,具有单加氧酶活性。CYP450约占植物蛋白编码基因的1%,是参与植物次生代谢活动最多的一类氧化酶超基因家族,具有复杂的底物选择性。细胞色素p450具有广泛的催化活性,在植物中催化多种初级和次级代谢反应,包括萜类、生物碱类、甾醇类、脂肪酸、植物激素、黄酮类等合成和代谢反应,涉及到羟基化、环氧基化、脱氢、烷基化等多种类型的反应。随着分子生物学以及相关技术的不断发展,CYP450在次生代谢途径中的功能逐步得以验证,但在丁苯酞生物合成途径中,目前还没有鉴定到参与苯酞类化合物结构修饰的CYP基因。
发明内容
本发明的目的在于提供川芎中参与丁烯基苯酞生物合成的苯酞类化合物合成酶LcP450、编码其核苷酸序列及应用。
本发明的第一方面提供苯酞类化合物合成酶LcP450,所述苯酞类化合物合成酶LcP450的氨基酸序列包含或由如下序列组成:
a)SEQ ID No.1或SEQ ID No.2所示的氨基酸序列;或
b)与SEQ ID No.1或SEQ ID No.2所示的氨基酸序列具有至少75%序列同一性的功能性同源序列;或
c)在SEQ ID No.1或SEQ ID No.2所示的氨基酸序列中添加、缺失、替换一个或多个氨基酸且具有相同蛋白活性的氨基酸序列。
本发明以伞形科药用植物川芎Ligusticum chuanxiong hort.为研究对象,从中筛选分离出两种编码苯酞类化合物合成酶LcP450的基因,命名为LcCYP72A和LcCYP716E,其获得的编码蛋白具有催化底物藁本内酯生成丁烯基苯酞的功能。
在本发明的一种实施方式中,所述苯酞类化合物合成酶LcP450LcCYP72A、LcCYP716E的氨基酸序列为SEQ ID No.1、SEQ ID No.2所示的氨基酸序列。
在本发明的一种实施方式中,所述苯酞类化合物合成酶LcP450LcCYP72A、LcCYP716E的氨基酸序列为与SEQ ID No.1、SEQ ID No.2所示的氨基酸序列具有至少75%序列同一性的功能性同源序列。所述功能性同源序列包括但不限于与SEQ ID No.1、SEQ IDNo.2所示的氨基酸序列具有约75%或以上、80%或以上、85%或以上、90%或以上、95%或以上、99%或以上、99.5%或以上、99.9%或以上同一性的氨基酸序列。
在本发明的一种实施方式中,所述苯酞类化合物合成酶LcP450LcCYP72A、LcCYP716E的氨基酸序列为在SEQ ID No.1、SEQ ID No.2所示的氨基酸序列中添加、缺失、替换一个或多个(例如可以为1-10个或更多,具体地,可以为1个、2个、3个、4个、5个、6个、7个、8个、9个、10个或更多个)氨基酸且具有相同蛋白活性的氨基酸序列。
本发明的第二方面提供了编码所述苯酞类化合物合成酶LcP450的核苷酸序列。
进一步的,编码苯酞类化合物合成酶LcP450的核苷酸序列包含或由以下序列组成:
1)SEQ ID No.3或SEQ ID No.4所示的核苷酸序列;或
2)SEQ ID No.3或SEQ ID No.4所示的核苷酸序列的互补序列、简并序列或同源序列;或
3)与SEQ ID No.3或SEQ ID No.4所示的核苷酸序列杂交,且能够编码苯酞类化合物合成酶LcP450的核苷酸序列。
在本发明的一种实施方式中,LcCYP72A和LcCYP716E的核苷酸序列为SEQ ID No.3和SEQ ID No.4所示的核苷酸序列。
在本发明的一种实施方式中,LcCYP72A和LcCYP716E的核苷酸序列为SEQ ID No.3和SEQ ID No.4所示的核苷酸序列按照碱基互补配对原则形成的互补序列,互补序列可以为具有编码LcCYP72A和LcCYP716E功能的不完全互补序列或完全互补序列。
在本发明的一种实施方式中,LcCYP72A和LcCYP716E的核苷酸序列为SEQ ID No.3和SEQ ID No.4所示的核苷酸序列的简并序列。简并序列是指改变SEQ ID No.3和SEQ IDNo.4核苷酸某个或多个核苷酸序列后,改变的核苷酸序列位置对应编码的氨基酸种类不变,不会影响LcCYP72A和LcCYP716E基因的功能和表达水平。
在本发明的一种实施方式中,LcCYP72A和LcCYP716E的核苷酸序列为SEQ ID No.3和SEQ ID No.4所示的核苷酸序列的同源序列。所述同源序列包括在SEQ ID No.3和SEQ IDNo.4所示的核苷酸序列中添加和/或取代和/或缺失一个或几个核苷酸而生成的可编码具有苯酞类化合物合成酶LcP450LcCYP72A和LcCYP716E活性的突变基因、等位基因或衍生物。
进一步优选同源序列为与SEQ ID No.3和SEQ ID No.4所示的核苷酸序列约80%或以上、85%或以上、90%或以上、95%或以上、99%或以上、99.5%或以上、或99.9%或以上相似性且具备编码苯酞类化合物合成酶LcP450功能的多核苷酸。
本发明的第三方面提供了所述苯酞类化合物合成酶LcP450或编码所述苯酞类化合物合成酶LcP450的核苷酸序列在合成3-取代苯酞类化合物中的应用,尤其是在合成丁烯基苯酞中的应用。
其中,所述的苯酞类化合物合成酶LcP450在合成丁烯基苯酞中的应用包括以下几个方面:
(1)本发明所提供的LcCYP72A和LcCYP716E氨基酸序列或至少部分去除或替代某些氨基酸之后仍有生物活性甚至有新的生物活性。
(2)涉及丁烯基苯酞的生物合成。
编码所述苯酞类化合物合成酶LcP450的核苷酸序列在合成丁烯基苯酞中的应用包括以下几个方面:
(1)本发明提供的核苷酸序列或至少部分核苷酸序列被修饰或突变,修饰或突变的途径包括插入、缺失、易错PCR,不同序列的重新连接,序列的不同部分与其他来源的同源序列进行定向进化,或者通过化学试剂诱变等。
(2)本发明所提供的核苷酸序列或至少部分核苷酸序列的克隆基因通过某些表达体系在外源宿主或內源宿主中表达以得到相应的酶活其他更高的生物活性活产量。
(3)本发明所提供的核苷酸序列活至少部分核苷酸序列的基因活基因簇可以通过同源重组来构建重组质粒以获得化合物的新的合成途径,也可以通过插入、置换、缺失或失活来获得化合物的新的合成途径。
本发明的第四方面提供了用于扩增核苷酸序列的引物,所述引物的碱基序列如SEQ ID No.5和SEQ ID No.6或SEQ ID No.7和SEQ ID No.8所示。
本发明的第五方面提供了载体,所述载体转入了所述的核苷酸序列
对于载体的种类不作具体限定,可以根据需要选择适合的载体。例如载体包括但不限于pEAQ-HT、pSuper-1300、pET-28a、pET30a、pET24b、pESC-Ura、pESC-Trp、pESC-Leu、pESC-His、pGEX2T、pTAex3、pYMB03,优选pSuper1300和pET24b。
本发明的第六方面提供了遗传工程化的宿主细胞,其包含所述的氨基酸序列,或所述的核苷酸序列,或导入了所述的载体。
进一步,所述宿主细胞包括植物细胞和/或微生物细胞中的至少一种。
进一步,所述植物细胞包括川芎细胞、烟草细胞中的至少一种。这里植物细胞的来源也包括外植体的植物部分,包括但不限于:插条、组织培养物、细胞悬浮液和愈伤组织
进一步,所述微生物细胞包括链霉菌、假单胞菌、芽孢杆菌、酵母细胞、大肠杆菌中的至少一种。
进一步,在体内和体外将编码苯酞类化合物合成酶LcP450的核苷酸序列,或重组质粒,或表达载体引入宿主细胞的方法包括但不限于电穿孔、聚乙二醇(PEG)转化、脂质转染、热休克、磷酸钙沉淀、病毒介导和显微注射。
本发明的有益效果是:
本发明提供了新发现的苯酞类化合物合成酶LcP450,有助于了解苯酞类化合物的合成通路,为利用基因工程手段提高川芎种丁烯基苯酞和丁苯酞的含量提供了新的基因资源,有利于通过定向进化或克隆基因在宿主细胞种表达得到相应的酶或更高的活性产物或产量。
附图说明
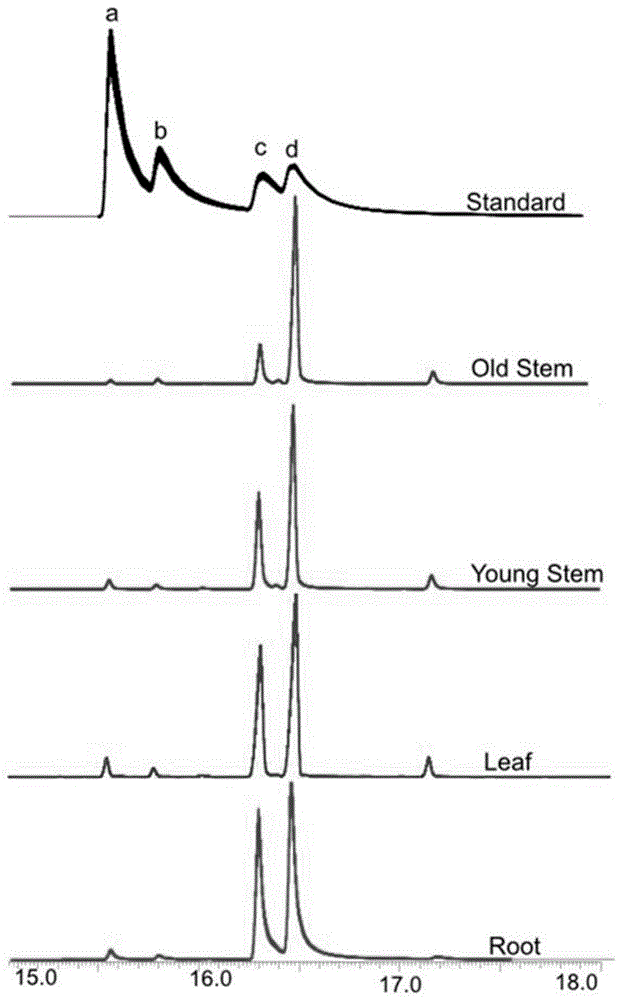
图1为川芎不同组织种苯酞类物质的含量,其中,a为丁基苯酞,b为丁烯基苯酞,c为洋川芎内酯A,d为藁本内酯。
图2为实施例1重组质粒pSuper1300-LcCYP716E和pSuper1300-LcCYP72A的PCR鉴定结果。
图3为实施例2中采用GC-MS检测pSuper1300-LcCYP716E和pSuper1300-LcCYP72A酶促产物的离子色谱图(TIC)。
图4为实施例2中pSuper1300-LcCYP716E和pSuper1300-LcCYP72A主要酶促产物丁烯基苯酞的质谱图,母离子和特征离子分别为m/z188和m/z159。
图5为实施例2中pSuper1300-LcCYP716E和pSuper1300-LcCYP72A催化藁本内酯生成丁烯基苯酞的反应机理示意图。
具体实施方式
本发明种,术语“LcP450”为苯酞类化合物合成酶,具体可以表示藁本内酯氧化酶,或丁烯基苯酞合成酶,具体所指的含义可以结合上下文判断。
下面将结合实施例,对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。实施例均按照常规实验条件或按照厂商说明书建议的条件进行。除非另行定义,本发明中所使用的所有专业术语具有与本领域的技术人员通常理解的相同的含义。此外,任何与所记载内容相似或相同的方法及材料都可用于本发明方法中,基于本发明中的实施例,本领域技术人员在没有付出创造性劳动的前提下所获得的所有其他实施例,都属于本发明保护的范围。
以下实施例中所使用的实验方法如无特殊说明,均采用常规方法。所用的材料、试剂和耗材等,如无特殊说明,均可从商业途径获得。
以下实施例中所涉及的材料及试剂包括:川芎(Ligusticum chuanxiong hort.)植株,由四川省彭州市军乐镇农户购买,公众可从中药材天地网上获得,经单位内植物分类学背景的同事鉴定为商品川芎。OMEGA Plant RNA Kit(Omega),
丁烯基苯酞检测体系的构建
为分析川芎中不同组织部位丁烯基苯酞的分布情况,通过有机溶剂如甲醇、乙酸乙酯或甲基叔丁基醚(MTBE)对川芎的根、茎和叶进行萃取,过0.22μm滤膜后,采用气相色谱和质谱联用测定丁烯基苯酞的含量,测定结果如图1所示。
实施例1川芎中LcCYP72A和LcCYP716E的克隆
1.川芎根的cDNA的合成
取适量川芎根(-80℃冰箱保存),液氮磨碎。采用Trizon法提取川芎总RNA,提取后用DNase I及RNA纯化试剂盒,对所提取的总RNA进行精制,去除RNA中的基因组污染。
根据Novoprotein的第一链cDNA合成试剂盒
(1)去基因组DNA反应:
42℃孵育5min,反应结束后冰上放置。
(2)逆转录反应:
50℃孵育30min,75℃孵育5min,终止反应。
cDNA样品于-20℃保存。
2.LcCYP基因的克隆
以川芎根的cDNA为模板,利用扩增核苷酸序列的引物,引物包含XbaⅠ和KpnⅠ酶切位点序列,采用PCR的方法扩增LcCYP基因,与经XbaⅠ和KpnⅠ双酶切的线性pSuper1300载体重组,采用Fast DNA Assembly Mix试剂盒的方法获得重组质粒,并转入大肠杆菌DH5α后,提取质粒进行PCR鉴定(北京六合华大基因科技有限公司),阳性重组质粒命名为pSuper1300-LcP450,其PCR鉴定结果如图2所示。
其中,LcCYP72A的扩增引物序列如下:
LcCYP72A-Forward:
CTCGATACACCAAATCGACTCTAGA
LcCYP72A-Reverse:
CCCTTGCTCACCATGGTACC
LcCYP716E的扩增引物序列如下:
LcCYP716E-Forward:
CTCGATACACCAAATCGACTCTAGA
LcCYP716E-Reverse:
CCCTTGCTCACCATGGTACC
3.胶回收
取PCR产物与与DNAloading buffer混合,在1%琼脂糖凝胶上以140V电压电泳15分钟;用刀片切割含有DNA片段的凝胶,尽可能靠近DNA片段切割,将切下的胶放入已经称重的1.5mL离心管中并称重,记下回收胶的重量;加入等量的(V:m=1:1)Binging buffer,在50℃的水浴锅中孵育10min,期间颠倒混匀2-3次,促进胶融化,保证胶全部溶解,在上柱前将凝胶混合物快速涡旋混匀一次;转移最多750μL胶混合液到回收纯化柱中,13000rpm离心1min,弃透过液,然后将回收柱放回相同的收集管;加入700μL Wash Buffer到纯化柱中,13000rpm离心1min,弃透过液,然后将纯化柱放回收集管中;在13000rpm 1min,离心空的纯化柱,彻底去除残留的Wash Buffer;将纯化柱移至1.5mL微量离心管,加入30-50μL ddH
实施例2 LcCYP72A和LcCYP716E的烟草异源表达
将实施例1得到的重组载体导入农杆菌GV3101中,使用该重组的农杆菌GV3101侵染本氏烟草叶片,用转入pSuper1300载体的农杆菌作为对照菌株。本氏烟草培养于25℃,16h光照条件下,直到长至6片真叶时用于农杆菌的侵染。将含有重组质粒的农杆菌于28℃下培养OD
表1注射缓冲液配方
采用GC-MS对转基因烟草的丁烯基苯酞含量进行检测,主要采取以下步骤:
样品前处理:烟草通过冷冻干燥后,用研钵磨成粉,每100mg烟草用2mL乙酸乙酯提取,提取物超声处理30min,12000rpm下4℃离心10min,收集上清,真空浓缩至0.5mL,用0.45μm尼龙过滤器将上清过滤至棕色样品瓶中,待进样。
GC-MS条件:GC-MS仪器为安捷伦7890B/7000C(美国Waldbronn安捷伦科技),质谱检测器参数:70eV,氦气流速1.2mL·min
LcCYP72A和LcCYP716E在本氏烟草的异源表达结果如图3和图4所示,图3、4中的结果表明,LcCYP72A和LcCYP716E能够催化藁本内酯生成丁烯基苯酞,催化的反应机理如图5所示。
以上所述仅是本发明的优选实施方式,应当理解本发明并非局限于本文所披露的形式,不应看作是对其他实施例的排除,而可用于各种其他组合、修改和环境,并能够在本文所述构想范围内,通过上述教导或相关领域的技术或知识进行改动。而本领域人员所进行的改动和变化不脱离本发明的精神和范围,则都应在本发明所附权利要求的保护范围内。
