基于苯并半花菁类化合物的荧光探针及其制法和应用
文献发布时间:2023-06-19 19:30:30
技术领域
本发明涉及一种基于苯并半花菁类化合物的荧光探针,还涉及上述荧光探针的制备方法及其在特异性检测过氧化氢、羧酸酯酶和半胱氨酸方面的应用。
背景技术
近红外荧光探针的使用可以降低生物分子的吸收与散射,能够提高荧光成像的信噪比,可以非侵入性地实现细胞及生命体中的生理过程可视化,在荧光成像领域具有广泛应用前景。目前应用于近红外荧光成像的探针主要有生物分子荧光探针、纳米荧光探针和小分子荧光染料。其中,小分子荧光染料具有合成与修饰容易、尺寸小、成本低、成像快速、生物相容性好的优点,是近红外荧光成像领域研究的重点之一。
作为一类特殊的有机染料,半花菁具有独特的供体-π-受体(D-π-A)的共轭体系。通常,半花菁结构带正电荷的氮杂环部分作为电子受体,末端羟基、烷氧基或氨基作为电子给体,它们通过共轭骨架相连。目前半花菁类荧光探针在荧光成像领域得到了较广泛的应用,但其探针分子共轭结构不大,使其吸收和发射波长均局限于可见光区域,因而限制了其在荧光成像尤其是活体荧光成像方面的应用。为了开发新型的半花菁染料分子以调控其吸收和发射光谱,Young-Tae-Chang课题组通过不同吡啶鎓盐与芳香醛的缩合反应,不仅实现了半花菁荧光团的多样化,而且获得的一系列染料分子的发射波长从可见光区域红移到了700nm以后,在2012年,Lin课题组通过间苯二酚处理氯代环己烯取代的七甲川花菁时,意外地获得了一种新型的半花菁染料,所得半花菁分子的吸收和发射波长均位于近红外光区域(700-780nm)。虽然目前开发的荧光探针吸收和发射光谱有所提高,但是由于斯托克斯位移仍然较小,其在荧光成像尤其是活体荧光成像方面的应用依然受到限制。
发明内容
发明目的:本发明目的旨在提供一种既具有近红外发光特性又具有较大斯托克斯位移的荧光探针;本发明另一目的旨在提供上述荧光探针的制备方法及其在特异性检测过氧化氢、羧酸酯酶和半胱氨酸方面的应用。
技术方案:本发明所述的基于苯并半花菁类化合物的荧光探针,其结构通式如下:
其中,R为苯甲酰基、二甲氨基甲酰基或丙烯酰基中的一种。
上述基于苯并半花菁类化合物的荧光探针的制备方法,包括如下步骤:
(1)合成化合物Cy:
在氮气保护下,将4-(1,1,2-三甲基-1H-苯并[e]吲哚-3-基)丁烷-1-磺酸酯、2-氯环己-1-烯-1,3-二甲醛、正丁醇和甲苯混合,置于水分离器中(置于水分离器中的目的是去除体系中的水,水的反应活性高于反应物料),抽真空,抽3次氮气(除去氧气防止反应物与空气中的氧气发生反应),于高温下反应;反应完成后,冷却至室温,然后将反应混合物滴加到乙酸乙酯和石油醚混合液中剧烈搅拌(剧烈搅拌能够防止反应物与大分子的产物聚合粘连,默认看不清磁子形状即为剧烈搅拌),搅拌后过滤、洗涤,收集固体;
(2)合成中间化合物CZX-OH:
在氮气保护下,将化合物Cy、萘-1,3-二醇、碳酸钾和DMF混合,于高温下回流反应,反应后旋转蒸发除去剩余溶剂,然后用硅胶色谱分离纯化得中间化合物CZX-OH;
(3)合成目标化合物:
在氮气保护下,将化合物CZX-OH以及苯甲酰氯、二甲氨基甲酰氯或丙烯酰氯中的一种加入到DIPEA(N,N-二异丙基乙胺)和DMF(二甲基甲酰胺)的混合溶剂中,高温下反应,反应后旋转蒸发除去剩余溶剂,然后用硅胶柱层析得到目标化合物。
其中,步骤(1)中,4-(1,1,2-三甲基-1H-苯并[e]吲哚-3-基)丁烷-1-磺酸酯和2-氯环己-1-烯-1,3-二甲醛的质量比为345:86。
其中,步骤(1)中,反应温度为136~140℃;反应时间为13~14小时。
其中,步骤(1)中,混合液中,乙酸乙酯和石油醚的体积比为2:1,剧烈搅拌时间为0.5~0.6小时。
其中,步骤(2)中,化合物Cy、萘-1,3-二醇和碳酸钾的质量比为155:30:77.53。
其中,步骤(2)中,反应温度为80~85℃;反应时间为6~6.5小时。
其中,步骤(3)中,化合物CZX-OH与苯甲酰氯、二甲氨基甲酰氯或丙烯酰氯的摩尔比为1:5。
其中,步骤(3)中,反应温度为50~55℃;反应时间为12~12.5小时。
上述基于苯并半花菁类化合物的荧光探针在特异性检测过氧化氢、羧酸酯酶和半胱氨酸方面的应用。上述荧光探针可被过氧化氢、羧酸酯酶、半胱氨酸特异性催化并生成水解产物CZX-OH,该水解产物具有荧光发射属性,可采用荧光分光光度仪对产物实现超灵敏迅速检测;产物CZX-OH荧光检测条件为:激发波长为~670nm,在~850nm波长进行荧光发射光谱的检测。
氧化氢、羧酸酯酶、半胱氨酸快速定量检测方法,具体为:在PBS或Tris-HCl缓冲液中,反应温度为20℃~60℃,优选37℃,孵育体系pH值为5.5~10.5,优选pH值为7.4;以基于苯并半花菁类化合物的荧光探针作为特异性探针底物,探针底物浓度为1/10~10Km;反应5~120分钟后终止反应,测定单位时间内水解产物生成量作为过氧化氢、羧酸酯酶和半胱氨酸含量的评价指标。过氧化氢可以特异性催化CZX-H2O2,羧酸酯酶可以特异性地催化CZX-CES2,半胱氨酸可以特异性地催化CZX-Cys,均生成水解产物CZX-OH,该水解产物具有良好的荧光属性,可通过定量检测单位时间内荧光强度的变化测定氧化氢、羧酸酯酶、半胱氨酸的真实含量。
有益效果:与现有技术相比,本发明具有如下显著优点:(1)高特异性:本发明荧光探针可被过氧化氢、羧酸酯酶和半胱氨酸高特异性地代谢成单一代谢产物,其它人体常见水解酶或具有水解活性的蛋白不参与此类化合物(荧光探针)的水解;因此本发明荧光探针能够对过氧化氢、羧酸酯酶和半胱氨酸特异性的定量定性检测;(2)高灵敏度:本发明荧光探针的水解产物CZX-OH具有良好的荧光属性,发射波长处于近红外区域(最大发射波长在850nm),通过在半花菁共轭多个苯环(不高于6个),使荧光探针分子具有大的共轭结构,从而使其发射波长红移到达近红外发射的效果,进而能够减少生物样本自身的背景荧光,增强检测的灵敏度,在生物样本中具有良好的应用前景;(3)通过在半花菁共轭多个苯环,使探针分子具有大的共轭结构的同时还能进一步提高其斯托克位移,使荧光探针分子具有较大的斯托克斯位移,达到~180nm,因此能够很好的消除背景荧光,能够在较苛刻和复杂的环境中对过氧化氢、羧酸酯酶和半胱氨酸的分布进行定量评价;并且在探针分子具有大的斯托克位移的同时还具有良好的柔性,从而具有良好的结构稳定性;(4)良好的水溶性:本发明荧光探针具有良好的水溶性,因此具有好的细胞穿透性,且无细胞毒性,因此可作为一种实时检测生命系统中过氧化氢、羧酸酯酶和半胱氨酸含量的实用工具。
附图说明
图1为本发明荧光探针CZX-CES2的合成路线图;
图2为本发明荧光探针CZX-H
图3为本发明荧光探针CZX-Cys的合成路线图;
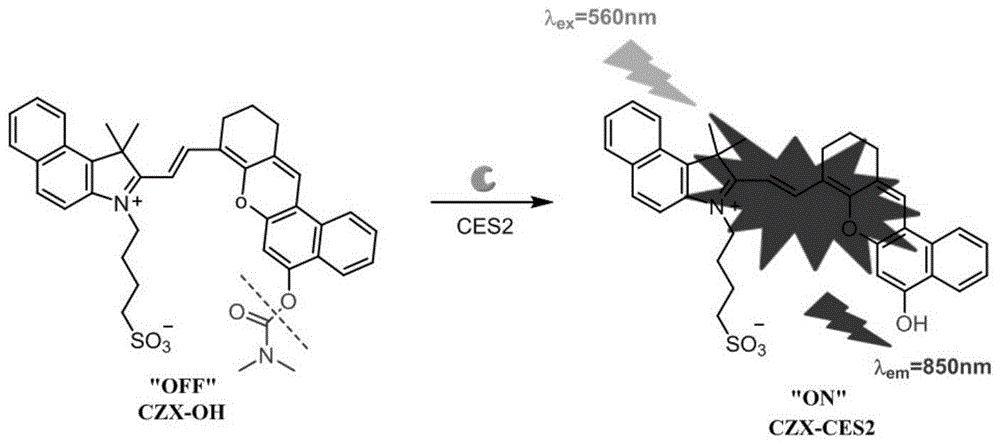
图4为本发明荧光探针的发光机理;
图5为本发明荧光探针CZX-H
图6为本发明荧光探针CZX-Cys的氢谱图;
图7为本发明荧光探针CZX-H
图8为本发明荧光探针CZX-CES2对羧酸酯酶2响应前后的吸收光谱图;
图9为本发明荧光探针CZX-Cys对半胱氨酸响应前后的吸收光谱图;
图10为本发明荧光探针CZX-CES2对羧酸酯酶2响应前后的荧光光谱图;
图11为本发明荧光探针CZX-CES2对羧酸酯酶2不同响应时间的荧光光谱图;
图12为本发明荧光探针CZX-CES2对不同浓度羧酸酯酶2响应的荧光光谱图;
图13为本发明荧光探针CZX-CES2对羧酸酯酶2的特异性响应图;
图14为本发明荧光探针CZX-H
图15为本发明荧光探针CZX-Cys对半胱氨酸的特异性响应图;
图16为荧光探针中间化合物Cy的氢谱图;
图17为荧光探针中间化合物CZX-OH的氢谱图。
具体实施方式
实施例1
本发明荧光探针CZX-H
(1)中间体化合物Cy的合成:
在氮气保护下,将4-(1,1,2-三甲基-1H-苯并[e]吲哚-3-基)丁烷-1-磺酸酯(345mg,1mmol)、2-氯环己-1-烯-1,3-二甲醛(86mg,0.5mmol)、正丁醇(30mL)和甲苯(15mL)加入干燥烧瓶中,置于水分离器中,抽真空,抽3次氮气后,逐渐升温至136℃,反应13小时;反应完成后,冷却至室温,然后将反应混合物滴加到乙酸乙酯和石油醚的混合液(200mL)中剧烈搅拌,混合液中,EA/PE=V/V=2:1;搅拌0.5小时后,过滤,乙酸乙酯洗涤3次,收集固体,最终得到金绿色金属光泽固体4-(2-((E)-2-((E)-2-氯-3-((E)-2-(1,1-二甲基-3-(4-磺酰基丁基)-1,3-二氢-2H-苯并[E]吲哚-2-亚基)亚乙基)环己-1-烯-1-基)乙烯基)-1,1-二甲基-1H-苯并[E]吲哚-3-鎓-3-基)丁烷-1-磺酸盐(化合物Cy);采用氢谱进行化合物Cy的表征,如图16所示;
(2)中间体化合物CZX-OH的合成:
在氮气保护下,将化合物Cy(155mg,0.187mmol)、萘-1,3-二醇(30mg,0.187mmol)、碳酸钾(77.53mg,0.561mmol)和DMF(10mL)加入到干燥的烧瓶中,然后逐渐升温至80℃,6小时后停止回流反应,旋转蒸发除去剩余溶剂,然后用硅胶色谱分离纯化(MeOH:DCM=V/V=1:15)得到蓝绿色固体(化合物CZX-OH);采用氢谱进行化合物CZX-OH的表征,如图17所示;
(3)目标化合物CZX-H
在氮气保护下,将化合物CZX-OH(40mg,0.052mmol)、苯甲酰氯(24μL,0.26mmol)、DIPEA(45.2μL,0.26mmol)和DMF(2mL)加入到干燥烧瓶中,然后逐渐升温至50℃,12小时后停止反应,旋转蒸发除去剩余溶剂,然后用硅胶柱层析(MeOH:DCM=V/V=1:10)得到绿色固体,即为目标产物荧光探针CZX-H
采用氢谱进行化合物CZX-H
实施例2
本发明荧光探针CZX-CES2(检测羧酸酯酶2)的制备方法,包括如下步骤:
(1)中间体化合物Cy的合成同实施例1;
(2)中间体化合物CZX-OH的合成同实施例1;
(3)目标化合物CZX-CES2的合成:
在氮气保护下,将化合物CZX-OH(40mg,0.052mmol)、二甲氨基甲酰氯(24μL,0.26mmol)、DIPEA(45.2μL,0.26mmol)和DMF(2mL)加入到干燥烧瓶中,然后逐渐升温至50℃,12小时后停止反应,旋转蒸发除去剩余溶剂,然后用硅胶柱层析(MeOH:DCM=V/V=1:10)得到绿色固体,即为目标产物荧光探针CZX-CES2;
(600MHz,Methanol-d
(d,J=8.3Hz,1H),7.66(t,J=7.7Hz,1H),7.59–7.52(m,3H),7.45(q,J=6.7,5.4Hz,4H),7.36(t,J=7.2Hz,1H),6.43(d,J=14.8Hz,1H),4.24(t,J=7.4Hz,2H),3.21(t,J=1.8Hz,6H),2.82(t,J=6.3Hz,3H),2.65(t,J=6.2Hz,2H),1.94–1.86(m,2H),1.74(s,6H),1.19(d,J=11.1Hz,6H).HRMS(ESI positive)calcd for[M+H]
采用高分辨质谱对化合物进行表征,其合成路线如图1所示。
实施例3
本发明荧光探针CZX-Cys(检测半胱氨酸)的制备方法,包括如下步骤:
(1)中间体化合物Cy的合成同实施例1;
(2)中间体化合物CZX-OH的合成同实施例1;
(3)目标化合物CZX-Cys的合成:
在氮气保护下,将化合物CZX-OH(40mg,0.052mmol)、丙烯酰氯(24μL,0.26mmol)、DIPEA(45.2μL,0.26mmol)和DMF(2mL)加入到干燥烧瓶中,然后逐渐升温至50℃,12小时后停止反应,旋转蒸发除去剩余溶剂,然后用硅胶柱层析(MeOH:DCM=V/V=1:10)得到绿色固体,即为目标产物荧光探针CZX-Cys。
采用氢谱进行化合物CZX-Cys的表征,如图6所示;其具体合成路线如图3所示。
实施例4
检测过氧化氢荧光探针CZX-H
实施例5
检测羧酸酯酶2荧光探针CZX-CES2响应前后的吸收光谱:以水为溶剂配制浓度为1M的荧光探针母液,测试之前,用磷酸盐缓冲液(10mM,p H7.4)稀释至荧光探针浓度为10μM,得到测试溶液,并设置对照。控制空白样中荧光探针浓度为10μM,其中不加入羧酸酯酶2作为对照组,测试样中荧光探针浓度为10μM,并控制最终羧酸酯酶2浓度为2μg/mL,在37℃温育15min,之后分别检测500nm到900nm之间的吸收光谱结果,如图8所示。
实施例6
检测半胱氨酸荧光探针CZX-Cys响应前后的吸收光谱:以水为溶剂配制浓度为1M的荧光探针母液,测试之前,用磷酸盐缓冲液(10mM,p H7.4)稀释至荧光探针浓度为10μM,得到测试溶液,并设置对照。控制空白样中荧光探针浓度为10μM,其中不加入半胱氨酸作为对照组,测试样中荧光探针浓度为10μM,并控制最终半胱氨酸浓度为2μg/mL,在37℃温育15min,之后分别检测500nm到900nm之间的吸收光谱结果,如图9所示。
实施例7
检测羧酸酯酶2荧光探针CZX-CES2响应前后的吸收光谱:以水为溶剂配制浓度为1M的荧光探针母液,测试之前,用磷酸盐缓冲液(10mM,p H7.4)稀释至荧光探针浓度为10μM,得到测试溶液,并设置对照。控制空白样中荧光探针浓度为10μM,其中不加入羧酸酯酶2作为对照组,测试样中荧光探针浓度为10μM,并控制最终羧酸酯酶2浓度为2μg/mL,在37℃温育15min,之后分别检测500nm到900nm之间的荧光光谱结果,如图10所示。
实施例8
荧光探针CZX-CES2对羧酸酯酶2不同响应时间的荧光光谱测试:羧酸酯酶2浓度为2μg/mL,荧光探针浓度为10μM时,荧光强度随时间的变化结果如图11所示。
实施例9
荧光探针CZX-CES2对不同浓度羧酸酯酶2响应的荧光光谱:配制羧酸酯酶2浓度分别为0、2、4、6、8、10μg/mL,探针浓度为10μM的PBS缓冲液(pH=7.4),温度为37℃,响应时间为20min,分别测定每组测试样在波长670nm的激发波长下的荧光光谱图,测试结果如图12所示。本发明制得的荧光探针对酶促反应体系中的羧酸酯酶2有较好的检测效果,随着羧酸酯酶2浓度(0-10μg/m L)的增加在30min内反应充分,响应前后荧光变化明显,说明利用该荧光探针可对多种生物体系中羧酸酯酶2的分布和功能进行定量评价。
实施例10
荧光探针CZX-CES2对羧酸酯酶2的特异性响应:配制总体积为100μL的混合溶液,包含98μL PBS缓冲溶液,1μL荧光探针母液(浓度为1mM)和1μL羧酸酯酶2(1mg/mL)。将混合液在37℃孵育30min,然后加入到100μL乙腈中来淬灭反应。荧光探针和羧酸酯酶2的最终浓度分别为10μM和5μg/mL。在条件不变的情况下,分别用羧酸酯酶1、乙酰胆碱酯酶、丁酰胆碱酯酶、人血清蛋白、牛血清蛋白、氯化钾、氯化锌、氯化镁、氯化钙、葡萄糖、维生素C、酪氨酸、甘氨酸、谷氨酸、精氨酸、丙氨酸和赖氨酸来替换混合溶液中的羧酸酯酶2,得到不同的溶液,测定荧光强度。如图13所示,羧酸酯酶2溶液的荧光强度远远高于其他溶液的荧光强度,荧光探针中的酯键会被羧酸酯酶2催化水解并转化为羟基,导致荧光被打开(图4)。结果表明本发明荧光探针CZX-CES2可以选择性地检测羧酸酯酶2。
实施例11
荧光探针CZX-H
实施例12
荧光探针CZX-Cys对半胱氨酸的特异性响应:配制总体积为100μL的混合溶液,包含98μL PBS缓冲溶液,1μL荧光探针母液(浓度为1mM)和1μL半胱氨酸(1mg/mL)。将混合液在37℃孵育30min,然后加入到100μL乙腈中来淬灭反应。荧光探针和半胱氨酸的最终浓度分别为10μM和5μg/mL。在条件不变的情况下,分别用羧酸酯酶1、乙酰胆碱酯酶、丁酰胆碱酯酶、人血清蛋白、牛血清蛋白、氯化钾、氯化锌、氯化镁、氯化钙、葡萄糖、维生素C、酪氨酸、甘氨酸、谷氨酸、精氨酸、丙氨酸和赖氨酸来替换混合溶液中的半胱氨酸,得到不同的溶液,测定荧光强度。如图14所示,半胱氨酸溶液的荧光强度远远高于其他溶液的荧光强度,荧光探针中的酯键会被半胱氨酸催化水解并转化为羟基,导致荧光被打开(图4)。结果表明本发明荧光探针CZX-Cys可以选择性地检测半胱氨酸。
