用于动脉粥样硬化治疗的靶向纳米载体及其制备方法
文献发布时间:2024-04-18 19:58:26
技术领域
本发明属于药物载体领域,具体涉及一种用于动脉粥样硬化治疗的靶向纳米载体及其制备方法。
背景技术
动脉粥样硬化是一类易引起缺血性心脏病和脑卒中等严重心血管疾病的慢性疾病。动脉内壁的脂质沉积和由此形成的泡沫细胞共同加重了动脉粥样硬化病变的进展,并促进脂质在斑块内的进一步积聚,从而形成恶性循环加速病情恶化。目前,降脂治疗仍是动脉粥样硬化药物治疗的主要途径。以他汀类药物为代表的降脂药物因其并发症较少而在临床上得到广泛应用。然而,尽管他汀类药物能在一定程度延缓疾病进展,该药物仍不足以从单一途径实现对动脉粥样硬化的抑制。科研工作者们发现,由肝X受体介导的转录重编程以增强胆固醇流出等手段可在一定程度上实现动脉粥样硬化斑块的消退,但其非特异性分布导致的药物副作用也限制了临床价值。为了降低药物不良反应,近年来,基于纳米载体的高效药物递送策略得到了科研工作者们广泛的关注及研究。
随着纳米递送系统的不断开发和进步,优良的封装能力和富集特性使其在心血管疾病的治疗方面显示出巨大的临床应用潜力。由于动脉粥样硬化病变处的内皮损伤及局部炎症,纳米载体可实现在动脉粥样硬化病灶处的特异性富集,为具有治疗活性的分子提供了理想的运输效率。此外,科研工作者们发现,接枝胆固醇基团的两亲性聚合物展现出溶解大量游离胆固醇的能力,这为实现动脉粥样硬化病变的胆固醇逆向转运提供了新的治疗思路。因此,在两亲性纳米载体中引入稳定的胆固醇结构,可以实现对斑块内泡沫细胞中游离胆固醇的移除。
因此,构建兼具动脉粥样硬化斑块特异性靶向特性和多途径联合胆固醇移除治疗策略的纳米载体,对早期动脉粥样硬化的抑制及已形成斑块的消退和逆转具有重要的临床价值。
发明内容
针对现有技术中的上述不足,本发明提供一种用于动脉粥样硬化治疗的靶向纳米载体及其制备方法,其基于表面修饰氧化透明质酸的共价连接胆固醇基团的聚赖氨酸纳米胶束,由基于共价连接胆固醇基团的聚赖氨酸通过负载LXR激动剂T0901317,并于表面包覆氧化透明质酸自组装而成。在通过静脉注射进入血液循环后,该纳米载体可实现在动脉粥样硬化病灶处的精准富集,并可在溶酶体酸性环境下实现高效逃逸。纳米载体通过其胆固醇结合能力并释放负载的促进胆固醇逆向转运药物的联合胆固醇移除策略,实现对动脉粥样硬化的治疗作用。
本发明的目的通过如下的技术方案来实现:
一种用于动脉粥样硬化治疗的靶向纳米载体,其基于表面修饰氧化透明质酸的共价连接胆固醇基团的聚赖氨酸纳米胶束,由基于共价连接胆固醇基团的聚赖氨酸通过负载LXR激动剂T0901317,并于表面包覆氧化透明质酸自组装而成;
所述基于表面修饰氧化透明质酸的共价连接胆固醇基团的聚赖氨酸纳米胶束的结构式如式I所示:
其中,a、b、c为三种聚合单元的聚合度。
一种用于动脉粥样硬化治疗的靶向纳米载体的制备方法,该方法包括如下步骤:
步骤一:将胆固醇琥珀酸酯、1-(3-二甲氨基丙基)-3-乙基碳二亚胺和N-羟基琥珀酰亚胺溶解于第一有机溶剂中,室温搅拌,使其充分反应;其中,胆固醇琥珀酸酯、1-(3-二甲氨基丙基)-3-乙基碳二亚胺和N-羟基琥珀酰亚胺的摩尔比为10:12:11;
步骤二:向步骤(1)所得混合溶液中加入聚赖氨酸,加入的聚赖氨酸与所述胆固醇琥珀酸酯的质量比为2:1,室温搅拌,使其充分反应;所得溶液在去离子水中充分透析除去有机溶剂,然后冷冻干燥;
步骤三:将步骤二所得物与肝X受体激动剂T0901317按照质量比为10:1的比例溶解在第二有机溶剂中,然后将混合溶液滴入磷酸盐缓冲液,室温搅拌,在溶液中自组装形成纳米颗粒;所述混合溶液和磷酸盐缓冲液的体积比为1:10-1:3;
步骤四:按照质量体积比为25:0.1mg/ml的比例将氧化透明质酸溶解于磷酸盐缓冲液,并将此时的混合溶液滴入到步骤三所得的混合溶液中,室温搅拌,充分反应;然后用磷酸盐缓冲液进行充分透析,最终制得用于动脉粥样硬化治疗的靶向纳米载体。
进一步地,所述步骤一和步骤二中的搅拌时间为12-48h,所述步骤三中的搅拌时间为2-24h,步骤四中的搅拌时间为4-24h,从而让构成纳米颗粒的各组分间充分反应,且在水中充分自组装形成纳米颗粒。
进一步地,所述第一有机溶剂和第二有机溶剂相同,可同时溶解各组分。
进一步地,所述第一有机溶剂和第二有机溶剂选用二甲基亚砜或四氢呋喃,可更好的促进各组分溶解,促进反应高效进行。
本发明的有益效果如下:
(1)本发明构建的靶向纳米载体表面包覆透明质酸外壳,具有良好的动脉粥样硬化靶向性,可以实现动脉粥样硬化斑块病变处的精准递药。
(2)纳米载体中的亚胺键可以在溶酶体酸性条件下发生敏感性断裂,使得表面电荷由负电性向正电性转变,可以实现纳米载体释放药物并负载胆固醇后的溶酶体逃逸。
(3)本发明制备得到的纳米载体中引入的胆固醇结构可以实现对细胞内游离胆固醇的结合与移除,进而起到动脉粥样硬化治疗效果。
(4)本发明制备得到的纳米载体在稳定性、药物释放特性、胆固醇结合能力、动脉粥样硬化斑块靶向性上均具有显著提高。
(5)本发明制备得到的纳米载体可以实现对早期动脉粥样硬化病灶的高效抑制以及逆转。
附图说明
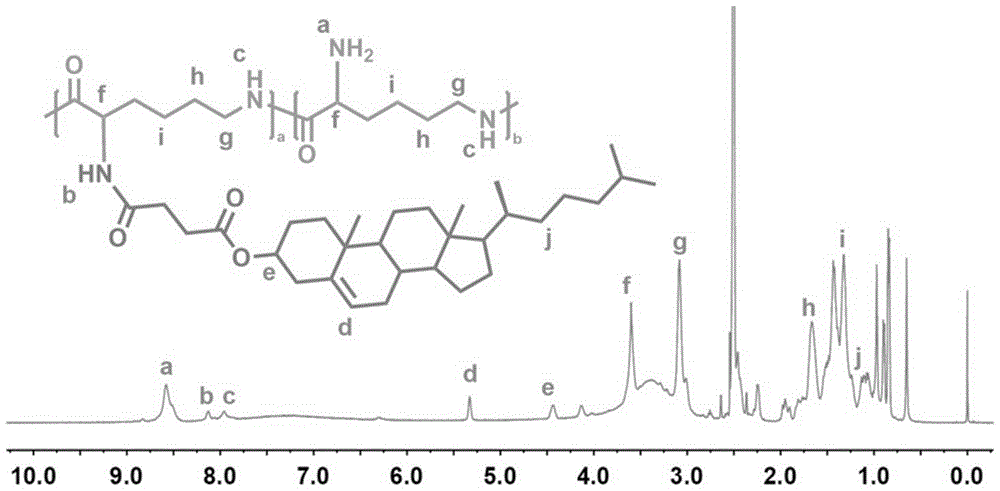
图1为接枝胆固醇基团的聚赖氨酸纳米胶束的核磁共振氢谱图谱;
图2为纳米载体的粒径分布图和透射电镜图;
图3为不同条件下纳米载体的粒径和表面电位变化图;
图4为纳米载体在不同条件下的体外药物释放结果图;
图5为纳米载体在不同条件下的体外胆固醇溶解能力结果图;
图6为纳米载体对体外泡沫细胞形成的抑制结果图;
图7为动物实验中纳米载体对动脉粥样硬化的靶向性能结果图;
图8为动物试验中纳米载体对动脉粥样硬化治疗的结果图。
具体实施方式
下面根据附图和优选实施例详细描述本发明,本发明的目的和效果将变得更加明白,应当理解,此处所描述的具体实施例仅用以解释本发明,并不用于限定本发明。
实施例1
(1)将胆固醇琥珀酸酯(0.243g,0.5mmol)、1-(3-二甲氨基丙基)-3-乙基碳二亚胺(0.113g,0.6mmol)和N-羟基琥珀酰亚胺(0.063g,0.55mmol)溶解于1mL二甲基亚砜中,室温搅拌24h;
(2)将聚赖氨酸(0.486g)溶解后加入至步骤(1)所得溶液中,室温下反应24h后,将所得溶液在去离子水(MCWO=3500)中透析48h,冷冻干燥后,得到大分子聚合物骨架;
上述制得的大分子聚合物骨架的核磁共振氢谱图谱见图1,由其出峰位置以及积分比例可知大分子聚合物骨架成功合成。
(3)将步骤(2)所得化合物(50mg)和肝X受体激动剂T0901317(5mg)溶解在1mL二甲基亚砜中,并滴加至4mL磷酸盐缓冲液中,室温搅拌2h;
(4)将氧化透明质酸(25mg)溶解于0.1mL磷酸盐缓冲液,并滴加至步骤(3)所得混合溶液,室温搅拌5h后,在磷酸盐缓冲液(MCWO=3500)中透析48h,制得纳米载体溶液。
纳米载体粒径图及透射电镜图见图2,图2中的图A为纳米载体粒径图,图B为透射电镜图;由图可知纳米载体可自组装形成具有纳米尺寸的均一颗粒,推测其为具有核-壳结构的纳米胶束。
实施例2
(1)将胆固醇琥珀酸酯(0.243g,0.5mmol)、1-(3-二甲氨基丙基)-3-乙基碳二亚胺(0.113g,0.6mmol)和N-羟基琥珀酰亚胺(0.063g,0.55mmol)溶解于1mL四氢呋喃中,室温搅拌24h;
(2)将聚赖氨酸(0.486g)溶解后加入至步骤(1)所得溶液中,室温下反应24h后,将所得溶液在去离子水(MCWO=3500)中透析48h,冷冻干燥;
(3)将步骤(2)所得化合物(25mg)和肝X受体激动剂T0901317(2.5mg)溶解在1mL四氢呋喃中,并滴加至4mL磷酸盐缓冲液中,室温搅拌2h;
(4)将氧化透明质酸(12.5mg)溶解于0.05mL磷酸盐缓冲液,并滴加至步骤(3)所得混合溶液,室温搅拌5h后,在磷酸盐缓冲液(MCWO=3500)中透析48h,制得纳米载体溶液。
实施例3
(1)将胆固醇琥珀酸酯(0.486g,1.0mmol)、1-(3-二甲氨基丙基)-3-乙基碳二亚胺(0.226g,1.2mmol)和N-羟基琥珀酰亚胺(0.126g,1.1mmol)溶解于2mL二甲基亚砜中,室温搅拌24h;
(2)将聚赖氨酸(0.972g)溶解后加入至步骤(1)所得溶液中,室温下反应24h后,将所得溶液在去离子水(MCWO=3500)中透析48h,冷冻干燥;
(3)将步骤(2)所得化合物(50mg)和肝X受体激动剂T0901317(5mg)溶解在1mL二甲基亚砜中,并滴加至4mL磷酸盐缓冲液中,室温搅拌2h;
(4)将氧化透明质酸(25mg)溶解于0.1mL磷酸盐缓冲液,并滴加至步骤(3)所得混合溶液,室温搅拌5h后在磷酸盐缓冲液(MCWO=3500)中透析48h,制得纳米载体溶液。
实施例4
(1)将胆固醇琥珀酸酯(0.243g,0.5mmol)、1-(3-二甲氨基丙基)-3-乙基碳二亚胺(0.113g,0.6mmol)和N-羟基琥珀酰亚胺(0.063g,0.55mmol)溶解于1mL二甲基亚砜中,室温搅拌24h;
(2)将聚赖氨酸(0.486g)溶解后加入至步骤(1)所得溶液中,室温下反应24h后,将所得溶液在去离子水(MCWO=3500)中透析48h,冷冻干燥;
(3)将步骤(2)所得化合物(50mg)和肝X受体激动剂T0901317(5mg)溶解在1mL二甲基亚砜中,并滴加至9mL磷酸盐缓冲液中,室温搅拌2h;
(4)将氧化透明质酸(50mg)溶解于0.2mL磷酸盐缓冲液,并滴加至步骤(3)所得混合溶液,室温搅拌5h后,在磷酸盐缓冲液(MCWO=3500)中透析48h,制得纳米载体溶液。
实施例5
(1)将胆固醇琥珀酸酯(0.243g,0.5mmol)、1-(3-二甲氨基丙基)-3-乙基碳二亚胺(0.113g,0.6mmol)和N-羟基琥珀酰亚胺(0.063g,0.55mmol)溶解于1mL二甲基亚砜中,室温搅拌24h;
(2)将聚赖氨酸(0.486g)溶解后加入至步骤(1)所得溶液中,室温下反应24h后,将所得溶液在去离子水(MCWO=3500)中透析48h,冷冻干燥后得到大分子聚合物骨架;
(3)将步骤(2)所得化合物(100mg)和肝X受体激动剂T0901317(10mg)溶解在1mL二甲基亚砜中,并滴加至4mL磷酸盐缓冲液中,室温搅拌2h;
(4)将氧化透明质酸(50mg)溶解于0.2mL磷酸盐缓冲液,并滴加至步骤(3)所得混合溶液,室温搅拌12h后在磷酸盐缓冲液(MCWO=3500)中透析48h,制得纳米载体溶液。
试验例1纳米载体酸性环境响应性的研究
将实施例1制得的纳米载体置于37℃,不同pH值(7.4、6.5和5.5)的磷酸盐缓冲液条件下,每隔一段时间用动态光散射DLS测定其粒径和Zeta电位变化,粒径变化结果见图3中的A,Zeta电位变化结果见图3中的B。
由图3可知,本发明制备的纳米载体在pH 7.4环境下表现出良好的稳定性,而随着环境酸性增加,测得的粒径显著增大,Zeta电位呈现出由负向正的电荷转换,表明其具有酸性条件下的特异性响应能力。
试验例2纳米载体体外药物释放行为的研究
将实施例1制得的纳米载体制成浓度为1mg/mL的溶液,然后取2mL转移到截留分子量为3500的透析袋中,将透析袋密封后置于500mL不同环境下的磷酸盐缓冲液中(pH 7.4、pH 6.5、pH 5.5和pH 5.5+6μM胆固醇),于37℃避光条件下持续振荡孵育,在不同时间点取出2mL溶液,用高效液相色谱仪测药物释放量,其结果如图4所示。
由图4可知,纳米载体在pH 7.4环境下结构稳定,药物泄露极少,随着环境酸性增加,释放药物能力显著增加,而在胆固醇共存条件下,药物的释放效率得到进一步提升。
试验例3纳米载体体外溶解胆固醇能力的研究
将实施例1制得的纳米载体置于不同pH环境下(7.4、6.5和5.5)的具有0.3mg/mL胆固醇的溶液中,于不同时间点过滤溶液,并在等体积的10%二甲基亚砜溶液中(MCWO=1000)中透析24h,用高效液相色谱仪测定透析液中胆固醇含量,其结果如图5所示。
由图5可知,在酸性条件下,纳米载体显示出良好的胆固醇溶解能力,且随着环境酸性增加,溶解胆固醇能力显著提升。
试验例4纳米载体对体外泡沫细胞形成的抑制作用
在被脂多糖(500ng/mL)激活并加入氧化低密度脂蛋白(1mg/mL)诱导的巨噬细胞中,加入实施例1制得的纳米载体或未搭载LXR激动剂的纳米载体,于37℃环境下共培养24h,对细胞进行油红O染色,并在光学显微镜下观察油红O阳性区域信号。
由图6可知,与未搭载LXR激动剂的纳米载体相比,使用制得的纳米载体干预后的巨噬细胞具有更小的油红O阳性区域面积,表明其降脂能力更强。
试验例5动物试验验证纳米载体对动脉粥样硬化病变斑块靶向性能
建立动脉粥样硬化小鼠模型。由尾静脉分别注射由罗丹明B标记的纳米载体或未包覆氧化透明质酸的纳米载体。药物的药量为每只小鼠100mg/kg。分别于6、12、24h后处死小鼠并分离主动脉。用IVIS光谱系统测定荧光强度。
由图7可知,完整纳米载体在动脉粥样硬化斑块处具有更多的特异性富集,且随着时间延长,富集的纳米载体显著增加,表明其对动脉粥样硬化斑块的靶向性能更佳。
试验例6动物试验验证纳米载体对动脉粥样硬化病变斑块治疗效果
建立动脉粥样硬化小鼠模型。由尾静脉分别隔日注射纳米载体、未搭载LXR激动剂的纳米载体、未包覆氧化透明质酸的纳米载体或等体积的生理盐水。药物的药量为每只小鼠100mg/kg/次。连续4周饲喂高脂饮食或正常饮食。治疗结束后分离小鼠主动脉进行油红O染色,并制备主动脉弓切片进行油红O染色,实验结果见图8。
由图8可知,与不完整纳米载体相比,实施例1制得的纳米载体具有更好的抑制动脉粥样硬化形成效果,并可以逆转已形成的动脉粥样硬化斑块。
本领域普通技术人员可以理解,以上所述仅为发明的优选实例而已,并不用于限制发明,尽管参照前述实例对发明进行了详细的说明,对于本领域的技术人员来说,其依然可以对前述各实例记载的技术方案进行修改,或者对其中部分技术特征进行等同替换。凡在发明的精神和原则之内,所做的修改、等同替换等均应包含在发明的保护范围之内。
- 用于结直肠癌靶向治疗的介孔钌纳米粒子及其制备方法和应用
- 岩藻糖与环糊精修饰多肽靶向动脉粥样硬化相关巨噬细胞纳米载体系统及其制备方法和应用
- 靶向动脉粥样硬化巨噬细胞树状纳米载体系统及制备方法
