肝癌特异性生物标志物
文献发布时间:2023-06-19 10:22:47
技术领域
本发明涉及肝癌特异性生物标志物,更加详细地,涉及一种使用其表达针对肝细胞癌特异性改变的基因作为用于检测及诊断肝癌细胞的生物标志物。
背景技术
在癌症中,肝癌被公知为是世界上最致命的癌症之一,据报道,尤其是在亚洲和撒哈拉以南的非洲每年有超过约50万人死于肝癌。肝癌大致可分为由肝细胞自身引起的原发性肝癌(肝细胞癌;hepatocellular carcinoma)和由其他组织的癌症转移到肝脏而引起的转移性肝癌,其中,约90%以上肝癌为原发性肝癌。
肝细胞癌(Hepatocellular carcinoma,HCC)是世界上第五大最常见的肿瘤,每年有50万人死于肝癌(Okuda 2000)。在过去20年中,肝癌细胞患者的生存率并未提高,其发病率大约等于死亡率(Marrero、Fontana et al 2005)。由乙型肝炎病毒或丙型肝炎病毒感染以及暴露于诸如黄曲霉毒素B1(aflatoxin B1)等致癌物引起的慢性肝炎被公知为是肝癌细胞的主要危险因素(Thorgeirsson and Grisham 2002),尽管已经有报道称从细胞周期机制进展到G1阶段的细胞周期调节物质的变化与肝癌的形成有关(Hui et al,Hepatogasteroenterology 45:1635-1642,1998),但尚不清楚与肝癌的发病和进展有关的细胞内分子机制。根据以往的研究,当诸如各种生长因子基因之类的原癌基因(protooncogene)因各种原因而突变为癌基因(oncogene)且过表达或过度活跃,或者诸如Rb蛋白或p53蛋白之类的肿瘤抑制基因(tumor suppressor gene)因各种原因而突变且表达不足或丧失功能时,据报道,会引起包括肝癌在内的各种肝癌的发病和进展。除此之外,据报道,在肝癌患者组织中确认到DNA突变和基因表达的遗传变异(genetic alteration)等(Park et al,Cancer Res 59:307-310,1999;Bjersing et al,J Intern Med 234:339-340,1993;Tsopanomichalou et al,Liver 19:305-311,1999;Kusano et al,Hepatology29:1858-1862,1999;Keck et al,Cancer Genet Cytogenet 111:37-44,1999)。近年来,人们认识到包括肝癌在内的大多数癌症的发病及进展并非由特定的几个基因引起,而是由与细胞周期、信号传导等有关的各种基因的复合性相互作用引起,因此,需要对各种基因或蛋白质进行全面研究,而不是仅关注单个基因或蛋白质的表达或功能。
另一方面,尚未开发出可以在正常人群中早期准确检测出肝癌的生物标志物检测方法,用于诊断高危人群的非侵入性早期肝癌的检测方法为血清甲胎蛋白检测。开发当时提出了将20ng/mL作为可以同时达到优异的甲胎蛋白(AFP)的敏感性和特异性的参考值,但在此情况下,敏感性仅为60%,当根据国际协会的肝癌诊断指南,以200ng/mL的标准诊断出肝癌时,虽然特异性提高,但敏感性仅为22%。根据以往的研究其结果,甲胎蛋白被公知为总体上具有约66%的敏感性和82%的特异性,因此在诊断所有肝癌患者方面存在局限性。另外,虽然尚未建立诊断标准,但有助于肝癌诊断的血清标志物包括脱羧凝血酶原(Descarboxyprothrombin,DCP)、维生素K缺乏Ⅱ诱导的凝血酶原Ⅱ(Prothrombin Inducedby Vitamin K Absence Ⅱ,PIVKA-Ⅱ)、糖基化甲胎蛋白与总甲胎蛋白(L3 fraction))分布、岩藻糖苷酶(alpha fucosidase)、磷脂酰肌醇蛋白聚糖(glypican)3、热激蛋白(HSP)-70等。但是,它们中的大多数具有作为预后因子的含义,当单独使用时,其准确性低,因此尚不能用于筛选检测,并且肝癌的早期诊断被判断为已达到极限。在可进行诸如实际手术或高频热疗等治愈性治疗阶段被诊断出的患者仅限于所有肝癌患者的30%左右。
发明内容
技术问题
本发明的目的在于,开发出具有改善的特异性和敏感性的新的诊断标志物,其可以在能够根治肝癌的阶段最大限度地实现早期诊断。
技术手段
为了实现上述目的,本发明提供用于诊断肝癌的生物标志物。
并且,本发明提供用于诊断肝癌的组合物。
并且,本发明提供肝癌诊断试剂盒。
同时,本发明提供诊断肝癌所需信息的提供方法。
技术效果
根据本发明,作为本发明生物标志物的透明质酸介导的运动受体(HMMR,hyaluronan-mediated motility receptor)、神经亲和素4(NXPH4,neurexophilin 4)、成对同源异型域1(PITX1,paired-like homeodomain 1)、血小板反应蛋白4(THBS4,thrombospondin 4)或泛素结合酶E2T(UBE2T,ubiquitin-conjugating enzyme E2T)会针对肝细胞癌特异性地改变其表达,因此具有如下效果:可将它们用作肝细胞癌特异性标志物,若将它们分别单独使用或与甲胎蛋白(α-fetoprotein)一同使用或另外组合,则可以更加特异性和准确地诊断肝细胞癌。
附图说明
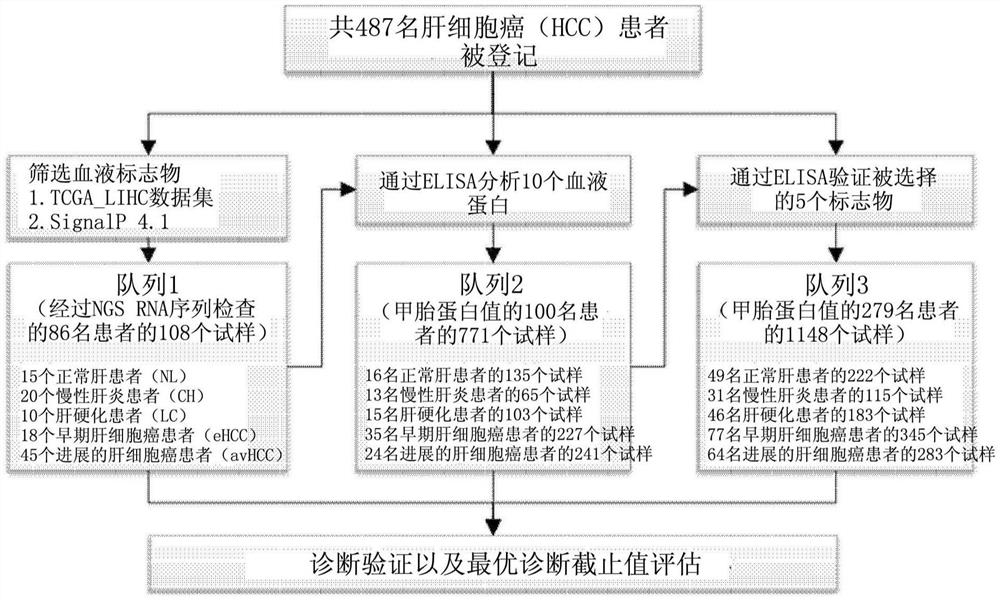
图1是示出本发明的肝细胞癌特异性标志物的衍生过程的示意图。
图2是示出仅在肝细胞癌中过表达的2502个前癌症基因组(Pre-Cancer Genome)的衍生过程的图。
图3是通过分析癌症基因组图谱(Cancer Genome Atlas)肝细胞癌(TCGA_LIHC)数据及基因表达综合(Gene Expression Omnibus,GEO)数据库来对在两个数据库中均过表达的737个基因进行层次聚类分析的结果的图。
图4a-图4d是确认在GSE114564数据队列和GSE6764中均表现出过表达的10个候选标志物基因的图。
图5a-图5d示出分别分析源自TCGA_LIHC数据集及ICGC_LIRI数据集的肝癌细胞患者的非肿瘤组织及肿瘤组织的10个标志物基因的表达水平的结果。
图6a-6b示出利用GSE77314数据集来比较分析上述10个标志物基因的表达水平的结果。
图7是在独立的肝病患者队列(100名患者的771个试样)中确认作为肝癌细胞癌症标志物的甲胎蛋白值的图。
图8a-8b是通过酶联免疫吸附试验(ELISA)分析10个选定的标志物基因的表达水平的结果。
图9a-9b是使用10个标志物基因的酶联免疫吸附试验值进行受试者工作特征(ROC)曲线分析的结果。
图10是在独立的肝病患者队列(279名患者的1148个试样)中确认作为肝癌细胞癌症标志物的甲胎蛋白值的图。
图11a-11b通过酶联免疫吸附试验分析10个标志物基因的表达水平的结果。
图12a-12b是使用标志物基因的透明质酸介导的运动受体、神经亲和素4、成对同源异型域1、血小板反应蛋白4及泛素结合酶E2T的酶联免疫吸附试验值进行受试者工作特征曲线分析的结果。
图13a-13g是通过酶联免疫吸附试验分析确认在使用甲胎蛋白验证的队列中的透明质酸介导的运动受体、神经亲和素4、成对同源异型域1、血小板反应蛋白4及泛素结合酶E2T的敏感性、特异性及准确性的图。
图14a-14d是根据甲胎蛋白、透明质酸介导的运动受体、神经亲和素4、成对同源异型域1、血小板反应蛋白4及泛素结合酶E2T中的两种标志物的组合(甲胎蛋白与透明质酸介导的运动受体、神经亲和素4、成对同源异型域1、血小板反应蛋白4或泛素结合酶E2T的组合;或者透明质酸介导的运动受体、神经亲和素4、成对同源异型域1、血小板反应蛋白4及泛素结合酶E2T中的两种标志物的组合)或三种标志物的组合(甲胎蛋白与透明质酸介导的运动受体、神经亲和素4、成对同源异型域1、血小板反应蛋白4及泛素结合酶E2T中的两种标志物的组合;或者透明质酸介导的运动受体、神经亲和素4、成对同源异型域1、血小板反应蛋白4及泛素结合酶E2T中的三种标志物的组合)的肝细胞癌诊断效果的比较图。
最优实施方式
以下,将参照附图来通过本发明的实例对本发明进行详细描述。然而,以下实例是作为本发明的例示来提出的,当判断为针对本发明所属技术领域的普通技术人员所公知的技术或结构的具体描述有可能不必要地混淆本发明主旨的情况下,可以省略对其的详细描述,并且本发明不限于此。在下述发明要求保护范围的记载以及由此解释的等同范围内,本发明能够进行各种变形及应用。
并且,本说明书中使用的术语(terminology)是用于适当地表达本发明的优选实施例而使用的术语,其可根据使用者或操作者的意图或本发明所属领域的惯例等而变化。因此,应当基于整个说明书中的内容来对这些术语下定义。在整个说明书中,当表示某个部分“包括”某个结构要素时,只要没有特别相反的记载,这并不意味着排除其他结构要素,而是意味着还可包括其他结构要素。
除非另有指示,否则核酸从左到右沿5'→3'方向记录。说明书中例举的数值范围包括用于定义范围的数字,并且包括定义范围内的每个整数或任何非整数分数。
除非另有定义,否则本说明书中使用的所有技术术语和科学术语具有与本发明所属技术领域的普通技术人员通常所理解的含义相同的含义。可在用于测试本发明的实践中使用与本说明书中描述的内容类似或等同的任何方法和材料,但是本文中描述了优选的材料和方法。
在本发明中,术语“受试体”或“患者”是指需要治疗的任何单个个体,包括人、猿、猴、牛、狗、豚鼠、兔、鸡、昆虫等。并且,对象包括参加临床研究试验且未显示任何疾病临床表现的的任何对象或参加力学研究的对象或用作对照组的对象。
在本发明中,术语“试样(样品)”是指从对象或患者获取的生物试样。生物试样的供给源可以是新鲜、冷冻和/或保存的器官或组织样品或从活检或引物产生的固体组织;血液或任意血液组分;对象的怀孕或发育中任意时间点的细胞。在本发明的一实施例中,将血液或任意血液组分用作试样。
除非另有定义,否则本发明中使用的所有技术术语均以本发明所属技术领域的普通技术人员通常在本发明的相关领域中理解的含义相同的含义来使用。并且,在本发明中记载了优选的方法或试样,但是与其相似或等同物也包括在本发明的范畴之内。本说明书中作为参考文献记载的所有出版物的内容被并入本发明。
在一方面中,本发明涉及用于诊断肝癌的生物标志物,其包含针对肝癌表现出特异性表达变化的选自由甲胎蛋白(α-fetoprotein)、透明质酸介导的运动受体(HMMR,hyaluronan-mediated motility receptor)、神经亲和素4(NXPH4,neurexophilin 4)、成对同源异型域1(PITX1,paired-like homeodomain 1)、血小板反应蛋白4(THBS4,thrombospondin 4)及泛素结合酶E2T(UBE2T,ubiquitin-conjugating enzyme E2T)组成的组中的一种以上的基因或从上述基因表达的蛋白质。在本发明的一实施例中,图1中示出了对肝癌特异性生物标志物的识别顺序的示意图。
在一实例中,肝癌可以是肝细胞癌(hepatocellular carcinoma,HCC),并且可以是早期肝细胞癌或进展的肝细胞癌。
在一实例中,本发明的生物标志物基因的表达可以肝癌特异性地增加。
在一方面中,本发明涉及用于诊断肝癌的组合物,其包含用于在mRNA或蛋白质水平上测量选自由甲胎蛋白、透明质酸介导的运动受体、神经亲和素4、成对同源异型域1、血小板反应蛋白4及泛素结合酶E2T组成的组中的一种以上的生物标志物基因的表达量的制剂。
在一实例中,上述组合物可以包含用于在mRNA或蛋白质水平上测量选自由甲胎蛋白及透明质酸介导的运动受体、甲胎蛋白及神经亲和素4、甲胎蛋白及成对同源异型域1、甲胎蛋白及血小板反应蛋白4、甲胎蛋白及泛素结合酶E2T、透明质酸介导的运动受体及神经亲和素4、透明质酸介导的运动受体及成对同源异型域1、透明质酸介导的运动受体及血小板反应蛋白4、透明质酸介导的运动受体及泛素结合酶E2T、神经亲和素4及成对同源异型域1、神经亲和素4及血小板反应蛋白4、神经亲和素4及泛素结合酶E2T、成对同源异型域1及血小板反应蛋白4、成对同源异型域1及泛素结合酶E2T、血小板反应蛋白4及泛素结合酶E2T组成的组中的一种以上的生物标志物基因集的表达量的制剂。
在一实例中,上述组合物可以包含在mRNA或蛋白质水平上测量选自由甲胎蛋白、透明质酸介导的运动受体及神经亲和素4;甲胎蛋白、透明质酸介导的运动受体及成对同源异型域1;甲胎蛋白、透明质酸介导的运动受体及血小板反应蛋白4;甲胎蛋白、透明质酸介导的运动受体及泛素结合酶E2T;甲胎蛋白、神经亲和素4及成对同源异型域1;甲胎蛋白、神经亲和素4及血小板反应蛋白4;甲胎蛋白、神经亲和素4及泛素结合酶E2T;甲胎蛋白、成对同源异型域1及血小板反应蛋白4;甲胎蛋白、成对同源异型域1及泛素结合酶E2T;甲胎蛋白、血小板反应蛋白4及泛素结合酶E2T;透明质酸介导的运动受体、神经亲和素4及成对同源异型域1;透明质酸介导的运动受体、神经亲和素4及;透明质酸介导的运动受体、神经亲和素4及血小板反应蛋白4;透明质酸介导的运动受体、神经亲和素4及泛素结合酶E2T;透明质酸介导的运动受体、成对同源异型域1及血小板反应蛋白4;透明质酸介导的运动受体、成对同源异型域1及泛素结合酶E2T;透明质酸介导的运动受体、血小板反应蛋白4及泛素结合酶E2T;神经亲和素4、成对同源异型域1及血小板反应蛋白4;神经亲和素4、成对同源异型域1及泛素结合酶E2T;及神经亲和素4、血小板反应蛋白4及泛素结合酶E2T组成的组中的一种以上的生物标志物基因集的表达量的制剂。
在一实例中,用于在mRNA水平上测量上述生物标志物基因的表达量的制剂可以包含标志物的核酸序列、上述核酸序列互补的核酸序列、特异性识别上述核酸序列及互补序列的片段的引物对、探针、或者引物对和探针,可通过选自由聚合酶链反应、实时荧光定量逆转录多聚酶链反应(Real-time RT-PCR)、逆转录聚合酶链反应、竞争性聚合酶链反应(Competitive RT-PCR)、核酸酶(Nuclease)保护分析(RNase,S1 nuclease assay)、原位杂交法、核酸微阵列、RNA印迹或DNA芯片组成的组中的方法进行上述测量。
在一实例中,上述生物用于在蛋白质水平上测量标志物基因的表达量的制剂可以包含特异性识别上述标志物的蛋白质全长或其片段的抗体、抗体片段、适体(aptamer)、高亲和性多聚体(avidity multimer)或拟肽(peptidomimetics),可通过选自由免疫印迹、酶联免疫吸附试验(enzyme linked immunosorbent assay)、放射免疫分析(RIA:Radioimmunoassay)、放射免疫扩散法(radioimmunodiffusion)、免疫电泳、组织免疫染色、免疫沉淀分析法(Immunoprecipitation assay)、补体固定分析法(Complement FixationAssay),荧光激活细胞分选(FACS)、质量分析或蛋白质微阵列组成的组中的方法进行上述测量。
本发明中使用的术语“检测”或“测量”是指量化被检测或测量的对象的浓度。
在本发明中,术语“引物”是指短核酸序列,其具有短的游离3羟基(free 3hydroxyl group)的核酸序列,能够与互补的模板(template)形成碱基对(base pair),其充当用于模板链复制的起点。引物可以在适当的缓冲液及温度下,在用于聚合反应(即,DN聚合酶或逆转录酶)的试剂及不同的4种核苷三磷酸的存在下诱发DNA合成。
在本发明中,术语“探针”是指对应于能够特异性结合mRNA的数个碱基至数百个碱基的核酸片段,例如RNA或DNA等。由于被标记,因而可以确认是否存在特定的mRNA。探针能够以寡核苷酸(oligonucleotide)探针、单链DNA(single stranded DNA)探针、双链DNA(double stranded DNA)探针、RNA探针等形式制造。在本发明中,利用与上述甲胎蛋白、透明质酸介导的运动受体、神经亲和素4、成对同源异型域1、血小板反应蛋白4和/或泛素结合酶E2T基因互补的探针进行杂交,并且可通过是否杂交来诊断上述基因的表达水平。可以基于本技术领域中公知的技术来更改用于合适探针的选择及杂交条件,在本发明中,对此没有特别限制。
本发明的引物或探针可以使用亚磷酰胺固相载体方法或其他公知的方法化学合成。这种核酸序列可以利用本领域中公知的多种手段来进行变形。这种变形的非限制性例包括甲基化、封装、天然核苷酸的一种以上的同源物的取代以及核苷酸之间的变形,例如,变形为不带电的连接体(例:膦酸甲酯、磷酸三酯、氨基磷酸酯、氨基甲酸酯等)或带电的连接体(例:硫代磷酸酯,二硫代磷酸酯等)。
在本发明中,可通过优化步骤在一系列过程中确定使探针与cDNA分子杂交的合适条件。该步骤由本领域普通技术人员通过一系列过程进行,以建立用于在研究室中使用的协议。例如,温度、成分浓度、杂交及洗涤时间、缓冲液成分及其pH以及离子强度等条件取决于探针的长度、GC量及靶核苷酸序列等各种因素。用于杂交的详细条件可从“JosephSambrook,et al.,Molecular Cloning,A Laboratory Manual,Cold Spring HarborLaboratory Press,Cold Spring Harbor,N.Y.(2001);以及M.L.M.Anderson,NucleicAcidHybridization,Springer-Verlag New York Inc.N.Y.(1999)”中确认。例如,在上述严格条件中的高严格条件是指在65℃下在0.5M NaHPO4、7%十二烷基硫酸钠(SDS,sodium dodecyl sulfate)、1mM EDTA中进行杂交,并且在68℃下在0.1×标准柠檬酸盐水(SSC,standard saline citrate)/0.1%十二烷基硫酸钠中进行洗涤。或者,高严格条件是指在48℃下在6×标准柠檬酸盐水/0.05%焦磷酸钠中进行洗涤。低严格条件是指例如在42℃下在0.2×标准柠檬酸盐水/0.1%十二烷基硫酸钠中进行洗涤。
在本发明中,术语“抗体”是本领域中公知的术语,是指针对抗原性位点指示的特异蛋白分子。为了本发明的目的,抗体是指与作为本发明标志物的甲胎蛋白、透明质酸介导的运动受体、神经亲和素4、成对同源异型域1、血小板反应蛋白4和/或泛素结合酶E2T基因中表达的蛋白质特异性结合的抗体,上述抗体可以使用公知的方法来制备。其中包括可以由上述蛋白质制成的部分肽。对本发明的抗体的形式没有特别限制,如果多克隆抗体,单克隆抗体或具有抗原结合特性的任何一种,则其一部分也包括在本发明的抗体中,并且包括所有的免疫球蛋白抗体。进而,本发明的抗体还包括特殊抗体,例如人源化抗体。
在一方面中,本发明涉及包含用于诊断肝癌的组合物的肝癌诊断试剂盒。
在一实例中,上述试剂盒还可包含用于从受试者或患者收集生物试样的工具和/或试剂,以及用于从其试样准备基因组DNA、cDNA、RNA或蛋白质的工具和/或试剂。例如,可以包含用于扩增基因组DNA的相关区域的PCR引物。上述试剂盒可包含可用于药物基因组分析的遗传因子的探针。并且,当使用这种试剂盒时,可以使用被标记的寡核苷酸来在分析过程中轻松识别。
在一实例中,上述试剂盒可进一步含有标记物质,例如DNA聚合酶、dNTP(dGTP、dCTP、dATP及dTTP)、荧光物质等。
在本发明中,术语“肝癌诊断试剂盒”是指包含本发明的用于诊断肝癌的组合物的试剂盒。因此,上述表述“肝癌诊断试剂盒”可以与“用于诊断肝癌的组合物”互换或混合使用。在本说明书中,术语“诊断”包括判断一个对象对特定疾病或病症的敏感性(susceptibility)、判断一个对象当前是否患有特定疾病或病症、判断患有特定疾病或病症的一个对象的预后(prognosis)(例如,识别前转移性或转移性癌症状、确定癌症的阶段或癌症对治疗的反应性)、或者治疗指标(therametrics)(例如,监控对象的状态以提供与治疗功效有关的信息)。
在本发明中,术语“诊断用生物标志物、用于诊断的生物标志物或诊断标志物(diagnosis marker)”是一种能够与正常细胞或组织分开来诊断是否存在肝癌细胞或组织的物,包括与正常细胞相比,在具有肝癌细胞的细胞或组织中表达增加或减少状态的诸如多肽或核酸(例:mRNA等)、脂质、糖脂、糖蛋白、糖(单糖,二糖,寡糖等)之类的有机生物分子等。为了本发明的目的,上述肝癌检测或诊断生物标志物是选自由基因甲胎蛋白、透明质酸介导的运动受体、神经亲和素4、成对同源异型域1、血小板反应蛋白4及泛素结合酶E2T组成的组中的一种以上,并且是在肝癌中mRNA表达或蛋白质表达水平特异性增加的基因。这些标志物不仅包括基因,还包括与一种标志物互补的DNA或mRNA,并且优选为包括两种以上的这些标志物的复合标志物,更优选为选自由甲胎蛋白及透明质酸介导的运动受体;甲胎蛋白及神经亲和素4;甲胎蛋白及成对同源异型域1;甲胎蛋白及血小板反应蛋白4;甲胎蛋白及泛素结合酶E2T;透明质酸介导的运动受体及神经亲和素4;透明质酸介导的运动受体及成对同源异型域1;透明质酸介导的运动受体及血小板反应蛋白4;透明质酸介导的运动受体及泛素结合酶E2T;神经亲和素4及成对同源异型域1;神经亲和素4及血小板反应蛋白4;神经亲和素4及泛素结合酶E2T;成对同源异型域1及血小板反应蛋白4;成对同源异型域1及泛素结合酶E2T;血小板反应蛋白4及泛素结合酶E2T;甲胎蛋白、透明质酸介导的运动受体及神经亲和素4;甲胎蛋白、透明质酸介导的运动受体及成对同源异型域1;甲胎蛋白、透明质酸介导的运动受体及血小板反应蛋白4;甲胎蛋白、透明质酸介导的运动受体及泛素结合酶E2T;甲胎蛋白、神经亲和素4及成对同源异型域1;甲胎蛋白、神经亲和素4及血小板反应蛋白4;甲胎蛋白、神经亲和素4及泛素结合酶E2T;甲胎蛋白、成对同源异型域1及血小板反应蛋白4;甲胎蛋白、成对同源异型域1及泛素结合酶E2T;甲胎蛋白、血小板反应蛋白4及泛素结合酶E2T;透明质酸介导的运动受体、神经亲和素4及成对同源异型域1;透明质酸介导的运动受体、神经亲和素4及;透明质酸介导的运动受体、神经亲和素4及血小板反应蛋白4;透明质酸介导的运动受体、神经亲和素4及泛素结合酶E2T;透明质酸介导的运动受体、成对同源异型域1及血小板反应蛋白4;透明质酸介导的运动受体、成对同源异型域1及泛素结合酶E2T;透明质酸介导的运动受体、血小板反应蛋白4及泛素结合酶E2T;神经亲和素4、成对同源异型域1及血小板反应蛋白4;神经亲和素4、成对同源异型域1及泛素结合酶E2T;及神经亲和素4、血小板反应蛋白4及泛素结合酶E2T组成的组中的一种以上。
在一方面中,本发明涉及抗癌候选物质的筛选方法,其包括:步骤(a),测量肝癌细胞的甲胎蛋白、透明质酸介导的运动受体、神经亲和素4、成对同源异型域1、血小板反应蛋白4或泛素结合酶E2T基因的表达水平;步骤(b),向上述肝癌细胞给予抗癌候选物质并测量甲胎蛋白、透明质酸介导的运动受体、神经亲和素4、成对同源异型域1、血小板反应蛋白4或泛素结合酶E2T基因的表达水平;以及步骤(c),当步骤(a)中的甲胎蛋白、透明质酸介导的运动受体、神经亲和素4、成对同源异型域1、血小板反应蛋白4或泛素结合酶E2T基因的表达水平大于步骤(b)中的甲胎蛋白、透明质酸介导的运动受体、神经亲和素4、成对同源异型域1、血小板反应蛋白4或泛素结合酶E2T基因的表达水平时,判断上述抗癌候选物质为有效抗癌物质。
在一方面中,本发明涉及诊断肝癌所需信息的提供方法,其包括:步骤(a),在从受试体分离的生物试样中测量选自由甲胎蛋白、透明质酸介导的运动受体、神经亲和素4、成对同源异型域1、血小板反应蛋白4及泛素结合酶E2T组成的组中的一种以上的生物标志物基因的表达量;步骤(b),与正常对照组试样的对应标志物的相应结果进行比较;以及步骤(c),当步骤(a)中的生物标志物基因的表达量大于步骤(b)中的生物标志物基因的表达水平时,判断为上述受试体可能是肝癌。
在一实例中,上述方法可以进一步包括根据生物标志物基因的表达变化水平来区分早期肝癌和进展的肝癌的步骤。
在一实例中,测量上述生物标志物基因的mRNA或其蛋白质的表达水平的具体方法如下:可以在mRNA水平或蛋白质水平上检测上述基因的表达,可以使用公知工序从生物试样中分离mRNA或蛋白质,并且可以通过逆转录聚合酶链反应(reverse transcriptase-polymerase chain reaction)或实时聚合酶链反应(real time-polymerase chainreaction)来确认基因的表达水平。
在一实例中,生物试样可以包括诸如组织、细胞、全血、血清、血浆、唾液、痰液、脑脊液或尿液之类的试样等,更优选为全血、血清或血浆。
将通过以下实施例更详细地描述本发明。但是,以下实施例仅用于具体描述本发明的内容,而本发明不限于此。
具体实施方式
实施例1.利用数据库进行的血液标志物筛选
从独立的肝病患者队列(86名患者的108个试样)的血液试样(15个正常肝患者试样(Normal liver,NL);20个慢性肝炎患者试样(Chronic hepatitis,CH);10个肝硬化患者试样(Liver Cirrhosis,LC);18个早期肝细胞癌患者试样(Early HCC,eHCC);以及45个进展的肝细胞癌患者试样(Advanced HCC,avHCC))中选择3个独立组,并利用TRIzol试剂提取总RNA之后,利用RNA Library Prep Kit for Illumina(Cat#E7420L)制备测序文库,并通过Illumina HiSeq 2000来根据Illumina公司的标准方法进行了测序。在利用STAR及Gencode v.25绘制经过分析的肝的整个转录组(transcriptome)后,用FPKM值替换表达谱,然后用Gencode v.25分类基因类型,并用SignalP 4.1衍生了12654个信号肽。产生的所有数据均记录在开放的Omix数据库GEO中。之后衍生仅在肝细胞癌中过表达的2502个前癌症基因组(Pre-Cancer Genome)之后(图2),通过癌症基因组图谱(Cancer Genome Atlas)肝细胞癌(TCGA_LIHC)数据及基因表达综合(Gene Expression Omnibus)(GEO)数据库进行分析,从而通过层次聚类分析了这两个数据库中均过表达的737个基因。其结果,GSE114564数据库示出了分为正常肝、慢性肝炎(CHB)、肝硬化、早期肝细胞癌及进展型肝细胞癌等5个子类的系统图,TCGA_LIHC数据库示出了分为正常肝及进展型肝细胞癌等2个子类的系统图(图3)。当在2个数据集中对计算出的737个基因的表达状态进行比较时,确认到与正常肝组织相比,其进展为肝癌或在进展型肝癌中的表达变化存在显著差异。并且,为了对其进行具有两类的基因数据的分析,利用基因集富集分析(Gene set enrichiment analysis,GSEA)进行了分析,上述基因集富集分析用于在基于生物学特征组成的各种基因集中提取两类表达值在统计学上表现出显著差异的重要的基因集。分析结果,可以确认到与以往众所周知的一种肝癌队列基因集CHANG_LIVER_CANCER的数据集有非常密切的关联性(平均凝集指数NES=1.88,NES=1.85)。然后,通过确认在上述GSE114564数据队列和GSE6764中均表现出过表达的10个候选标志物基因(图4a-4d),从而筛选出仅在肝细胞癌中其表达特异性增加的10个候选标志物CCNB2、CDT1、COCH、CSMD1、HMMR、NXPH4、OLFML2B、PITX1、THBS4及UBE2T。
为了实现从患者的血清中显著增加的生物标志物,进展型肝癌的中的表达增加率必须在统计学上显著高于正常肝的增加率,在已公开的数据中,基于可准确地测量表达的测序,以及分别分析和验证作为大规模队列的源自TCGA_LIHC数据集及ICGC_LIRI数据集的肝癌细胞患者的非肿瘤组织及肿瘤组织的10个标志物基因的表达水平,结果确认到两种队列中均表现出明显的表达差异(图5a-5d)。
利用GSE77314数据集来对上述10个标志物基因的表达水平进行了比较分析,上述GSE77314数据集是作为中国肝癌患者队列在共50名肝癌患者的周围正常组织和肝癌组织中通过测序方法测得的基因的表达值,其结果,在大多数患者中,确认到与正常肝组织相比,在肝癌组织中其表达显著增加(图6a-6b)。
实施例2.第一次选定的标志物的酶联免疫吸附试验分析
在确认到作为肝癌细胞癌症标志物的甲胎蛋白值的独立的肝病患者队列(100名患者的771个试样)的血液试样(16名正常肝患者的135个试样(Normal liver,NL);13名慢性肝炎患的65个试样(Chronic hepatitis,CH);15名肝硬化患者的103个试样(LiverCirrhosis,LC);35名早期肝细胞癌患者的227个试样(Early HCC,eHCC);以及24名进展的肝细胞癌患者的241个试样(Advanced HCC,avHCC))(图7)中,通过酶联免疫吸附试验分析确认到上述实施例1中选定的10个标志物基因的表达水平(图8a-8b)。
其结果,在CCNB2的情况下,从正常肝患者(NL)平均测出0.02ng/ml,慢性肝炎患者(CH)表现出0.2029ng/ml,肝硬化患者(LC)表现出0.43ng/ml,早期肝细胞癌患者(eHCC)表现出0.27ng/ml,以及进展的肝细胞癌患者(avHCC)表现出0.31ng/ml,因而LC表现出最大值。在CDT1的情况下,从正常肝患者(NL)平均测出167.7pg/ml,CH表现出230.8pg/ml,LC表现出178.2pg/ml,eHCC表现出103.5pg/ml,以及avHCC表现出146.8pg/ml,因而avHCC表现出最大值,总体上,疾病之间未表现出显著差异。在COCH的情况下,从正常肝患者(NL)平均测出1.724ng/ml,CH表现出12.78ng/ml,LC表现出10.03ng/ml,eHCC表现出6.74ng/ml,以及avHCC表现出8.025ng/ml,因此除了正常肝之外,在所有肝病及肝癌阶段均表现出较大值。在CSMD1的情况下,从正常肝患者(NL)平均测出14.8ng/ml,CH表现出11.65ng/ml,LC表现出14.48ng/ml,eHCC表现出14.72ng/ml,以及avHCC表现出15.66ng/ml,因而总体上表现出相似值。在OLFML2B的情况下,NL平均表现出175.2pg/ml,CH表现出658.8pg/ml,LC表现出338.4pg/ml,eHCC表现出284.1pg/ml,以及avHCC表现出349.6pg/ml,因而除了正常肝之外,在所有肝病及肝癌阶段均表现出较大值,尤其在CH中表现出较大值。在HMMR的情况下,从NL平均测出0.21ng/ml,CH表现出0.62ng/ml,LC表现出0.74ng/ml,eHCC表现出1.54ng/ml,以及avHCC表现出1.64ng/ml,因而与测序结果相似,该值随着肝病阶段的进展而增加。在NXPH4的情况下,NL平均表现出3.54ng/ml,CH表现出10.23ng/ml,LC表现出6.52ng/ml,eHCC表现出15.02ng/ml,以及avHCC表现出19.83ng/ml,因而在CH中略高,但与测序结果相似,该值随着肝病阶段的进展而增加。在PITX1的情况下,NL平均表现出2042pg/ml,CH表现出1994pg/ml,LC表现出3238pg/ml,eHCC表现出3314pg/ml,以及avHCC表现出6135pg/ml,因而在CH中表现出比正常值低的值,但与测序结果相似,该值随着肝病阶段的进展而增加。在THBS4的情况下,NL平均表现出45.36ng/ml,CH表现出70.96ng/ml,LC表现出141.8ng/ml,eHCC表现出229.4ng/ml,以及avHCC表现出233.6ng/ml,因而与测序结果相同,该值随着肝病阶段的进展而增加。在UBE2T的情况下,NL平均表现出16.14ng/ml,CH表现出319.9ng/ml,LC表现出426.1ng/ml,eHCC表现出505.5ng/ml,以及avHCC表现出877.2ng/ml,因而与正常肝相比,在肝病中剧增约20倍,并且该值随着肝病阶段的进展而增加。
通过酶联免疫吸附试验值对上述队列中的10个标志物基因进行了受试者工作特征曲线分析。
其结果,CSMD1、HMMR、NXPH4、OPITX1、THBS4及UBE2T与参考线相比具有统计学上显著的值,受试者工作特征曲线分析中表现出曲线下面积(AUC,area under the curve)值与甲胎蛋白相似或更大,这表明具有特性性及敏感性的标志物为HMMR、NXPH4、PITX1、THBS4及UBE2T(图9a-9b)。
实施例3.早期癌症诊断标志物HMMR、NXPH4、PITX1、THBS4及UBE2T的验证
在确认到作为肝癌细胞癌症标志物的甲胎蛋白值的独立的肝病患者队列(279名患者的1148个试样)的血液试样(49名正常肝患者的222个试样(Normal liver,NL);31名慢性肝炎患者的115个试样(Chronic hepatitis,CH);46名肝硬化患者的183个试样(LiverCirrhosis,LC);77名早期肝细胞癌患者的345个试样(Early HCC,eHCC);以及64名进展的肝细胞癌患者的283个试样(Advanced HCC,avHCC))(图10)中,通过酶联免疫吸附试验分析确认到上述实施例1中选定的10个标志物基因的表达水平(图11a-11b)。
其结果,当在验证队列中分别测量5个标志物的蛋白质表达水平时,在HMMR的情况下,通过将共230个试样中的正常组与每个肝病组进行比较的结果,表现出除了肝硬化组之外,有非常显著的差异,并且确认到尤其在早期肝癌中其表达特异性地高。在NXPH4的情况下,与正常组相比,每个肝病阶段组均表现出较大的表达变化,PITX1也表现出同样的结果。在THBS4的情况下,像HMMR一样,除了肝硬化组之外,其表达显著增加,并且在早期肝癌组表现出较大值。在UBE2T的情况下,像测试队列一样,正常组中根本未表达,而在肝病阶段组中表现出表达增加。
对上述队列中的标志物基因HMMR、NXPH4、PITX1、THBS4及UBE2T进行了受试者工作特征曲线分析。
其结果,在HMMR及THBS4的情况下,分别表现出AUC=0.856及AUC=0.772的值,因而确认到其表达水平高于以往的标志物AFP的AUC=0.749(图12a-12b)。
为了确认通过AFP验证的上述HMMR、NXPH4、PITX1、THBS4及UBE2T的敏感性(sensitivity)、特异性(specificity)及准确性(accuracy),对上述队列试样进谢了酶联免疫吸附试验分析。
表1
结果示出于上述表1及图13a-13g。具体地,对于甲胎蛋白以及5个标志物进行了如下步骤:1)在非肝癌试样(正常肝、肝炎、肝硬化试样)及肝癌试样中进行比较;2)在肝病试样(肝炎、肝硬化试样)及肝癌试样中进行比较之后,仅针对早期肝癌,特异性地分别按3)非肝癌试样及4)肝病试样进行了分析。在所有4种情况下,均表现出透明质酸介导的运动受体的敏感性、特异性及准确性最大。当利用MedCal程序求出它们各自标志物的截止值(cut-off value)时,测出透明质酸介导的运动受体为0.8ng/μl,神经亲和素4为7.5ng/μl,成对同源异型域1为2475pg/μl,血小板反应蛋白4为90ng/μl,泛素结合酶E2T为40ng/μl,在截止值增加超过每个截止值的试样的情况下,分为阳性(Positive)或低的阴性(Negative)来进行分析。从正常肝中的阳性率来看,测出甲胎蛋白为2%,透明质酸介导的运动受体为0%,神经亲和素4为6%,成对同源异型域1为23%,血小板反应蛋白4为4%,以及泛素结合酶E2T为0%。在肝炎组在,测出甲胎蛋白为19%,透明质酸介导的运动受体为19%,神经亲和素4为50%,成对同源异型域1为44%,血小板反应蛋白4为44%,以及泛素结合酶E2T为63%。在肝硬化组中,测出甲胎蛋白为39%,透明质酸介导的运动受体为17%,神经亲和素4为48%,成对同源异型域1为57%,血小板反应蛋白4为4%,以及泛素结合酶E2T为70%。在早期肝癌组在,测出甲胎蛋白为33%,透明质酸介导的运动受体为83%,神经亲和素4为64%,成对同源异型域1为72%,血小板反应蛋白4为54%,以及泛素结合酶E2T为54%,因而测出的5个标志物的阳性率显著高于作为肝癌测量标志物的甲胎蛋白。在进展型肝癌组中,表现出甲胎蛋白为73%,透明质酸介导的运动受体为78%,神经亲和素4为87%,成对同源异型域1为89%,血小板反应蛋白4为62%,以及泛素结合酶E2T为67%。然后,当比较肝癌患者中的甲胎蛋白及5个标志物的阳性率时,甲胎蛋白为52%,而剩余标志物表现出高阳性率,尤其当比较甲胎蛋白为阴性的肝癌患者中的每个阳性率时,在HMMR的情况下,测出86%的高阳性率,预计这将能够补充未测出甲胎蛋白为阳性的肝癌患者。在早期肝癌组的情况下,甲胎蛋白表现出33%的阳性率,相反,在HMMR的情况下,表现出83%的高阳性率。并且在甲胎蛋白为阴性的肝癌患者中,也表现出85%的高阳性率。
对于上述实施例3-1的队列,比较了根据甲胎蛋白、透明质酸介导的运动受体、神经亲和素4、成对同源异型域1、血小板反应蛋白4及泛素结合酶E2T中的两种标志物的组合(甲胎蛋白与透明质酸介导的运动受体、神经亲和素4、成对同源异型域1、血小板反应蛋白4或泛素结合酶E2T的组合;或者透明质酸介导的运动受体、神经亲和素4、成对同源异型域1、血小板反应蛋白4及泛素结合酶E2T中的两种标志物的组合)或三种标志物的组合(甲胎蛋白与透明质酸介导的运动受体、神经亲和素4、成对同源异型域1、血小板反应蛋白4及泛素结合酶E2T中的两种标志物的组合;或者透明质酸介导的运动受体、神经亲和素4、成对同源异型域1、血小板反应蛋白4及泛素结合酶E2T中的三种标志物的组合)的肝细胞癌的诊断效果。
表2
结果示出于上述表2及图14a-14d。具体地,当组合2种标志物时,若以所有肝癌患者作为对象,则甲胎蛋白及透明质酸介导的运动受体的组合表现出92%的阳性率,透明质酸介导的运动受体及成对同源异型域1的组合表现出最大的96%的阳性率。若以早期肝癌患者作为对象,则甲胎蛋白及透明质酸介导的运动受体的组合表现出90%的阳性率,透明质酸介导的运动受体及成对同源异型域1的组合表现出最大的99%的阳性率。并且,在将三种标志物组合的情况下,若以所有肝癌患者作为对象,则甲胎蛋白、透明质酸介导的运动受体及成对同源异型域1的组合、透明质酸介导的运动受体、神经亲和素4及成对同源异型域1的组合以及透明质酸介导的运动受体、成对同源异型域1及泛素结合酶E2T的组合表现出100%的阳性率。若以早期肝癌患者作为对象,则甲胎蛋白与透明质酸介导的运动受体及成对同源异型域1的组合、透明质酸介导的运动受体、神经亲和素4及成对同源异型域1的组合、透明质酸介导的运动受体、神经亲和素4及泛素结合酶E2T的组合以及透明质酸介导的运动受体、成对同源异型域1及泛素结合酶E2T的组合表现出100%的阳性率。
进一步地,当对86个非肝癌试样和132个肝癌试样中表现出100%的阳性率的组合进行受试者工作特征分析时,可以确认到,与以往的甲胎蛋白相比,所有组合的曲线下面积值在统计学上均显著增加,在两种组合中,评估出甲胎蛋白及透明质酸介导的运动受体的组合最优秀,在三种组合中,甲胎蛋白、透明质酸介导的运动受体及成对同源异型域1的组合表现出最大值。在诊断分析方面,在两种组合中,对准确性分析的结果,测出了透明质酸介导的运动受体及成对同源异型域1最高,优势比也表现出最高的75.23。在三种组合中,对准确性分析的结果,甲胎蛋白、透明质酸介导的运动受体及成对同源异型域1表现出最高的90.37%,优势比也表现出最高的87.04。并且,当对86个非肝癌试样和69个早期肝癌试样中分别表现出100%的阳性率的组合进行受试者工作特征分析时,可以确认到,与以往的甲胎蛋白相比,所有组合的曲线下面积值在统计学上均显著增加,在两种组合中,评估出透明质酸介导的运动受体及成对同源异型域1的组合最优秀,在三种组合中,甲胎蛋白、透明质酸介导的运动受体及成对同源异型域1的组合表现出最大值。在诊断分析方面,在两种组合中,对准确性分析的结果,测出了透明质酸介导的运动受体及成对同源异型域1为最高的88.39%,优势比也表现出最高的64.75。在三种组合中,对准确性分析的结果,甲胎蛋白、透明质酸介导的运动受体及成对同源异型域1表现出最高的92.75%,优势比也被测出最高的65.83。
- 一种用于诊断原发性肝癌的血清特异性生物标志物及筛选方法与应用
- 用于肝癌的无创诊断的特异性生物标志物组
