一种制备磷酸铁的方法及其应用
文献发布时间:2024-04-18 20:01:23
技术领域
本申请涉及材料生产技术领域,具体涉及一种制备磷酸铁的方法及其应用。
背景技术
磷酸铁锂电池因优异的安全性能、循环寿命长、成本低等特点,在新能源汽车等领域的应用迅猛增长。磷酸铁作为制备磷酸铁锂的主要原材料,对磷酸铁锂的物理和化学性能有着重要影响。
目前磷酸铁的制备主要是用硝酸、盐酸、硫酸等强无机酸对磷矿和铁矿进行消解获得消解液,然后用碱调节消解液pH制备磷酸铁。该方法存在磷酸铁纯度低,副产物难处理等缺陷,从而影响以磷酸铁为原料制备得到的正极活性材料性能的稳定性。
因此,需要提供一种制备高纯度磷酸铁的方法。
发明内容
本申请提供了一种制备磷酸铁的方法及其应用,该方法得到的磷酸铁中杂质含量较低,有利于扩大其应用范围。
第一方面,本申请提供了一种制备磷酸铁的方法,包括以下步骤:
S10:将铁源、磷源和酸混匀,得到前驱混合物;
S20:将所述前驱混合物进行高温烧结,使铁源和磷源中铁元素和磷元素充分氧化,以得到磷酸铁粗品;
S30:将所述磷酸铁粗品进行洗涤,使所述磷酸铁粗品中杂质含量降低,以得到磷酸铁。
根据本申请,通过将铁源和磷源与酸共混作为前驱体进行烧结,其中铁源和磷源氧化生成磷酸铁,同时烧结过程中在酸的作用下,铁源和磷源中的杂质元素可转化为易溶的化合物,从而在洗涤过程中更易去除,进而得到的磷酸铁中杂质元素含量降低,纯度更高,应用范围更广。
在一些实施方式中,所述步骤S10中,所述铁源和所述磷源的总质量与所述酸的质量之比为1.5~3:1。
在一些实施方式中,所述步骤S10中,所述前驱混合物中铁元素和磷元素的摩尔比为1:1~1.1。
在一些实施方式中,所述步骤S10中,所所述步骤S10中,所述铁源包括铁矿石,所述铁矿石包括磁铁矿石、赤铁矿石、钒钛磁铁矿石、褐铁矿石、菱铁矿石中的至少一种;和/或所述磷源包括磷矿石,所述磷矿石包括胶磷矿、碳磷灰石、磷铝石、氟磷灰石中的至少一种;和/或所述酸包括硫酸、盐酸、草酸、柠檬酸、氢氟酸、硝酸、苹果酸、葡萄糖酸、甲酸、乳酸、苯甲酸、丙烯酸、乙酸、丙酸、硬脂酸、次氯酸中的至少一种。
在一些实施方式中,所述步骤S20中,所述高温烧结的条件为:在300~1200℃下烧结5~24h。
在一些实施方式中,所述步骤S30中,所述洗涤包括:将所述磷酸铁粗品分别进行碱洗和酸洗。
在一些实施方式中,所述碱洗具体包括:在20~100℃下,使用质量浓度为5%~50%的碱液洗涤1~5h;和/或所述酸洗具体包括:在20~100℃下,使用质量浓度为1%~30%的酸液洗涤1~5h。
在一些实施方式中,所述碱液包括氢氧化钠水溶液、氢氧化钾水溶液、氢氧化钡水溶液、氢氧化钙水溶液、氨水中的至少一种;和/或所述酸液包括硫酸水溶液、盐酸、草酸水溶液、碳酸水溶液、柠檬酸水溶液、氢氟酸水溶液、硝酸水溶液、苹果酸水溶液、葡萄糖酸水溶液、甲酸水溶液、乳酸水溶液、苯甲酸水溶液、丙烯酸水溶液、乙酸水溶液、丙酸水溶液、硬脂酸水溶液、次氯酸水溶液中的至少一种。
第二方面,本申请提供了一种磷酸铁,根据第一方面任一实施方式所述的方法制备得到。
第三方面,本申请提供了一种正极活性材料,包括以下原料:根据第一方面任一实施方式所述的方法制备得到的磷酸铁或根据第二方面任一实施方式所述的磷酸铁。
附图说明
此处的附图被并入说明书中并构成本说明书的一部分,示出了符合本申请的实施例,并与说明书一起用于解释本申请的原理。
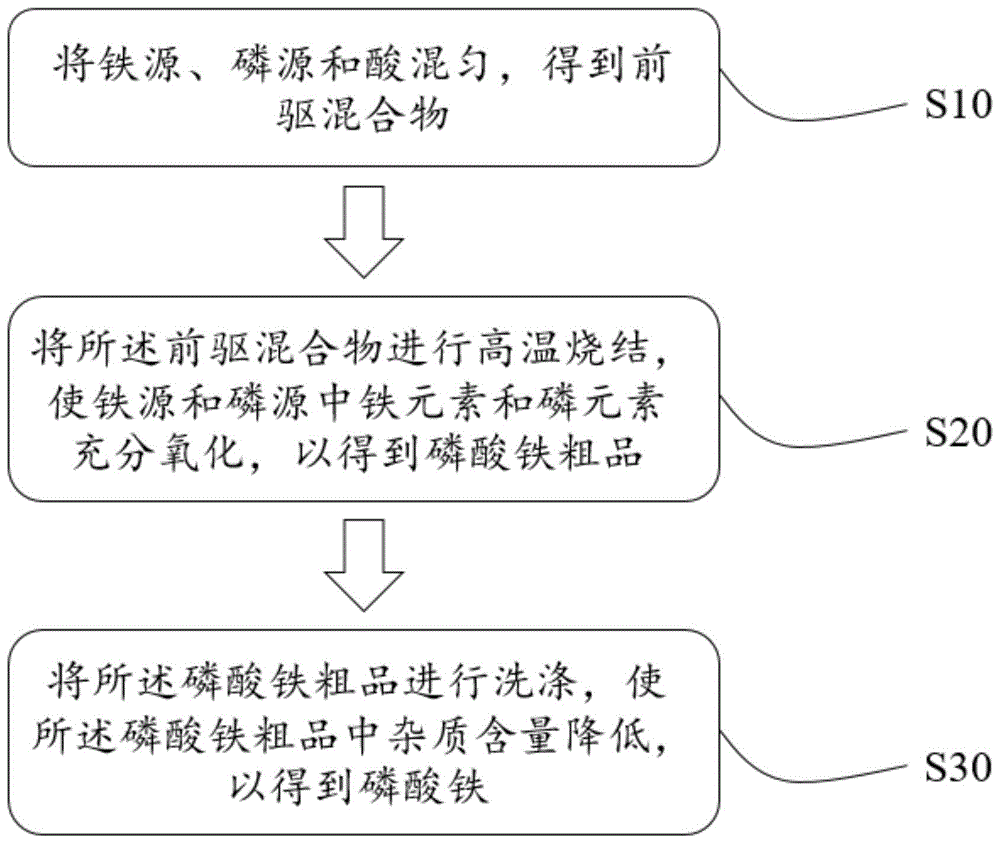
图1为本申请一实施方式的流程示意图。
通过上述附图,已示出本申请明确的实施例,后文中将有更详细的描述。这些附图和文字描述并不是为了通过任何方式限制本申请构思的范围,而是通过参考特定实施例为本领域技术人员说明本申请的概念。
具体实施方式
本说明书中各实施例或实施方案采用递进的方案描述,每个实施例重点说明的都是与其他实施例的不同之处。
在本说明书的描述中,参考术语“一个实施例”、“一些实施例”、“示意性实施例”、“示例”、“具体示例”、或“一些示例”等的描述意指结合实施方式或示例描述的具体特征、结构、材料或者特点包含于本申请的至少一个实施方式或示例中。在本说明书中,对上述术语的示意性表述不一定指的是相同的实施方式或示例。而且,描述的具体特征、结构、材料或者特点可以在任何的一个或多个实施方式或示例中以合适的方案结合。
此外,术语“第一”、“第二”仅用于描述目的,而不能理解为指示或暗示相对重要性或者隐含指明所指示的技术特征的数量。由此,限定有“第一”、“第二”的特征可以明示或者隐含地包括至少一个该特征。在本申请的描述中,“多个”的含义是至少两个,例如两个,三个等,除非另有明确具体的限定。
如上文中背景技术所述,现有的磷酸铁制备工艺中存在磷酸铁纯度低,副产物难处理等问题,会影响磷酸铁在作为正极活性材料原料的应用。
基于此,发明人经过分析,目前磷酸铁的制备工艺一般为:先将铁源和磷源使用过量的强无机酸液溶解得到消解液,然后加碱通过调节pH将磷酸铁进行沉淀,后续经过进一步洗涤得到磷酸铁。在此过程中,由于一般铁源和磷源中存在一定杂质元素,因此在消解液中存在一定的杂质元素,在沉降磷酸铁的过程中,一部分杂质元素也会沉淀析出,同时由于在沉降过程中,体系的水分含量高且粘度大,呈现为类型胶体的状态,对杂质沉淀具有较强的吸附作用,因此沉降得到磷酸铁含有较多的杂质元素,需要进一步洗涤,而由于通过调节pH产生的杂质元素一方面不易溶解,且与磷酸铁结合更加紧密,导致在洗涤过程中不易去除,因此磷酸铁的纯度较低。然而通过降低铁源和磷源中杂质元素的含量,以提高磷酸铁的纯度会导致成本较高,不适合于工业化生产应用。
针对上述问题,本申请提供了一种制备磷酸铁的方法及其应用,该方法通过使用加酸烧结的方法,避免了溶液沉降所带来的问题,可以得到纯度较高的磷酸铁。以下对本申请的具体实施方式进行具体说明。
第一方面,本申请提供了一种制备磷酸铁的方法,包括以下步骤:
S10:将铁源、磷源和酸混匀,得到前驱混合物;
S20:将前驱混合物进行高温烧结,使铁源和磷源中铁元素和磷元素充分氧化,以得到磷酸铁粗品;
S30:将磷酸铁粗品进行洗涤,使磷酸铁粗品中杂质含量降低,以得到磷酸铁。
根据本申请,通过将铁源和磷源与酸共混作为前驱体进行烧结,其中铁源和磷源氧化生成磷酸铁,同时烧结过程中在酸的作用下,铁源和磷源中的杂质元素可转化为易溶的化合物,从而在洗涤过程中更易去除,进而得到的磷酸铁中杂质元素含量降低,纯度更高,应用范围更广。
具体的,图1示出了该方法的具体流程图,步骤S10中,将铁源和磷源与酸混匀得到前驱混合物,其中,铁源和磷源即提供制备磷酸铁的铁元素和磷元素,酸的作用在于提供易产生可溶性盐的阴离子以及氢离子,以使前驱混合物在后续的烧结过程中,铁源和磷源中的杂质元素转化为易溶性的盐或氧化物(在本申请的上下文中,“易溶”并不限于溶于水,还可以是易溶于酸液或碱液),从而更容易在后续的洗涤过程中去除,减少磷酸铁中杂质元素的含量,提高磷酸铁的纯度。
需要说明的是,酸可以是固态的酸单质,由于本申请中酸的作用不在于溶解铁源和磷源得到消解液,因此可以是固体酸与铁源和磷源共混进行烧结,同时由于部分酸需要在水溶液才能稳定存在,如硝酸、盐酸等,因此酸也可以水溶液的状态与铁源和磷源共混,水在后续的烧结过程中去除。
步骤S20中,将前驱体混合物进行高温烧结,在此过程中磷元素和铁元素充分氧化生产磷酸铁化合物,同时铁源和磷源中部分杂质元素在烧结过程中去除,另一部分杂质元素可在酸的作用下发生转化,以易溶的化合物存在于磷酸铁粗品中。由于通过高温烧结的方法制备磷酸铁,避免了在液相中沉降磷酸铁容易吸附杂质元素和容易产生难溶性杂质的问题,有利于在后续的洗涤过程中去除磷酸铁中的杂质元素。
步骤S30中,对磷酸铁粗品进行洗涤,降低其中杂质元素的含量,得到纯度较高的磷酸铁。可以理解的是,由于铁矿和磷矿中可以通过烧结直接去除的杂质元素较少,大部分的杂质元素还是以易溶的化合物存在,因此需要对磷酸铁粗品进行洗涤,以去除大部分杂质元素,提高磷酸铁的纯度。
另外可以理解的是,在相关技术中使用大量强无机酸液对铁源和磷酸溶液得到消解液,再进行调节pH沉降磷酸铁的过程中,虽然有部分杂质元素无法沉降,而在过滤过程中去除,从而沉降得到的磷酸铁中杂质元素相较于本申请中磷酸铁粗品的含量更低,但是部分沉降出的杂质沉淀,会通过吸附作用与磷酸铁紧密结合,且该杂质沉淀也更不易去除,因此在后续洗涤过程中,难以进一步提高磷酸铁的纯度。同时相较于消解沉降法,由于磷酸铁的沉降并不完全,因此本申请提供的方法对铁元素和磷元素的回收率也更高,有利于降低成本。
另一方面,由于本申请中不需要使用大量的强无机酸液制备消解液,仅需要加入适当酸提供易产生可溶性盐的阴离子以及氢离子,因此可以降低生产成本以及减少废液排放,适合于工业化生产应用。
在一些实施方式中,步骤S10中,铁源和磷源的总质量与酸的质量之比为1.5~3:1。
在上述一些实施方式中,铁源和磷源的总质量与酸的质量之比会影响铁源和磷源中杂质元素的转化,在此条件下,铁源和磷源中杂质元素能够更加充分转化为易溶性的化合物,从而更易在后续洗涤过程中去除,从而得到纯度更高的磷酸铁。例如,铁源和磷源的总质量与酸的质量之比可以为1.5:1,1.8:1,2:1,2.2:1,2.5:1,2.8:1,3:1,或上述任意数值所组成的范围内。
在一些实施方式中,步骤S10中,前驱混合物中铁元素和磷元素的摩尔比为1:1~1.1。
在上述一些实施方式中,可以进一步提高铁元素和磷元素利用率,从而可以降低铁源和磷源的用量,进一步减少由于铁源和磷源引入的杂质,进而可以进一步提高磷酸铁的纯度。同时适量过量的磷元素,可以进一步提高铁元素的利用率,进一步降低生产成本。例如,前驱混合物中铁元素和磷元素的摩尔比可以为1:1,1:1.01,1:1.02,1:1.03,1:1.04,1:1.05,1:1.06,1:1.07,1:1.08,1:1.09,1:1.1,或上述任意数值所组成的范围内。
在一些实施方式中,步骤S10中,铁源包括铁矿石,铁矿石包括磁铁矿石、赤铁矿石、钒钛磁铁矿石、褐铁矿石、菱铁矿石中的至少一种。
在上述一些实施方式中,由于本申请提供的方法能够避免沉降制备磷酸铁吸附杂质的缺点,因此铁源可以包括杂质元素含量更高,但价格更低的铁矿石,在保证磷酸铁具有较高纯度的同时,可以进一步降低生产成本。同时可以理解的是,铁矿石包括但不限于上述几种,本领域技术人员可以根据实际需要选择其他已知的铁矿石。
进一步的,铁矿石的平均粒径可以在50μm以下,由于不经过消解,直接进行共混烧结,更小的粒径有利于与其他原料的充分混匀,提高铁元素的利用率,同时促进铁矿石中杂质元素的充分转化。
在一些实施方式中,步骤S10中,磷源包括磷矿石,磷矿石包括胶磷矿、碳磷灰石、磷铝石、氟磷灰石中的至少一种。
在上述一些实施方式中,同样的,本申请对磷源的选择也没有太大的限制,可以选择通过选择价格更低的磷矿石作为磷源,以降低生产成本。可以理解的是,磷矿石包括但不限于上述几种,本领域技术人员可以根据实际需要选择其他已知的磷矿石。
进一步的,磷矿石的平均粒径可以在50μm以下,由于不经过消解,直接进行共混烧结,更小的粒径有利于与其他原料的充分混匀,提高磷元素的利用率,同时促进磷矿石中杂质元素的充分转化。
在一些实施方式中,酸包括硫酸、盐酸、草酸、柠檬酸、氢氟酸、硝酸、苹果酸、葡萄糖酸、甲酸、乳酸、苯甲酸、丙烯酸、乙酸、丙酸、硬脂酸、次氯酸中的至少一种。可以理解的是,酸包括但不限于上述几种,本领域技术人员可以根据实际需要选择其他已知的可将杂质元素转化为可溶性化合物的酸。
在一些实施方式中,步骤S20中,高温烧结的条件为:在300~1200℃下烧结5~24h。在此条件下烧结有利于前驱混合物中磷元素和铁元素充分氧化生成磷酸铁,同时促进杂质元素在酸的作用下转化为可溶性化合物。另外可以理解的是,高温烧结的条件可以根据铁源和磷源的具体种类进行相应优化调整,以保证磷元素和铁元素充分氧化。
在一些实施方式中,步骤S30中,洗涤包括:将磷酸铁粗品分别进行碱洗和酸洗。
在上述一些实施方式中,洗涤可以包括碱洗和酸洗,高温烧结过程中杂质元素在酸的作用下,转化为易溶性的化合物一般是酸溶或是碱溶的,因此分别进行碱洗和酸洗,可以使磷酸铁粗品中的杂质元素进一步降低,从而进一步提高磷酸铁的纯度。
在一些实施方式中,碱洗具体包括:在20~100℃下,使用质量浓度为5%~50%的碱液洗涤1~5h;和/或酸洗具体包括:在20~100℃下,使用质量浓度为1%~30%的酸液洗涤1~5h。
在上述一些实施方式中,具体限定了碱洗和酸洗的条件,在此条件下杂质元素转化的易溶性化合物可以充分溶解,从而进一步降低磷酸铁中杂质元素的含量,提高磷酸铁的纯度。
在一些实施方式中,碱液包括氢氧化钠水溶液、氢氧化钾水溶液、氢氧化钡水溶液、氢氧化钙水溶液、氨水中的至少一种;和/或酸液包括硫酸水溶液、盐酸、草酸水溶液、碳酸水溶液、柠檬酸水溶液、氢氟酸水溶液、硝酸水溶液、苹果酸水溶液、葡萄糖酸水溶液、甲酸水溶液、乳酸水溶液、苯甲酸水溶液、丙烯酸水溶液、乙酸水溶液、丙酸水溶液、硬脂酸水溶液、次氯酸水溶液中的至少一种。可以理解的是,碱液和酸液的种类包括但不限于上述几种,本领域技术人员可以根据实际需要选择其他已知的可用于碱洗或酸洗磷酸铁材料的碱液或酸液。
第二方面,本申请提供了一种磷酸铁,根据第一方面任一实施方式的方法制备得到。
根据本申请,由于该磷酸铁根据第一方面任一实施方式的方法制备得到,因此具有第一方面的有益效果。即通过该方法制备得到的磷酸铁的纯度较高,可以扩大其应用场景。例如用于制备正极活性材料,由于其纯度较高,得到的正极活性材料的性能更加稳定,有利于提高电池的循环稳定性。另外,由于其纯度较高,在以其为原料制备其他产品时,可以无需对其进一步纯化处理,可以节约成本并提高效率。
第三方面,本申请提供了一种正极活性材料,包括以下原料:根据第一方面任一实施方式的方法制备得到的磷酸铁或根据第二方面任一实施方式的磷酸铁。
根据本申请,由于制备该正极活性材料的原料包括根据第一方面任一实施方式的方法制备得到的磷酸铁或根据第二方面任一实施方式的磷酸铁,因此具有第一方面或第二方面的有益效果。即由于第一方面任一实施方式的方法制备得到的磷酸铁或第二方面任一实施方式的磷酸铁具有较高的纯度,因此以此为原料制备的正极活性材料中杂质含量较少,有利于提高正极活性材料的稳定性。
在一些实施方式中,正极活性材料可以包括磷酸铁锂、磷酸铁钠、磷酸锰铁锂、磷酸锰铁钠或基于上述几种材料通过掺杂其他元素的正极活性材料,掺杂元素包括但不限于钒、钛、氮等金属或非金属元素。
以下,说明本申请的实施例。下面描述的实施例是示例性的,仅用于解释本申请,而不能理解为对本申请的限制。实施例中未注明具体技术或条件的,按照本领域内的文献所描述的技术或条件或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规产品。
铁元素含量的测定:称取2.5g(±0.001g)样品于100mL烧杯中,加50mL盐酸溶解至溶液透明,转移液体至250mL容量瓶中定容至刻度线。从容量瓶中移取10mL溶液至250mL锥形瓶中,加入100mL水,滴加3滴10%磺基水杨酸溶液,用0.02mol/L的EDTA标准溶液滴定至溶液呈亮黄色,即为终点,计算铁元素含量。
杂质元素含量的测定:称取0.5g(±0.001g)样品于100mL烧杯中,加50mL盐酸溶解至溶液透明,从烧杯中称量1g(±0.0001g)溶液于100mL容量瓶中,加入5mL硝酸,定容至刻度线,使用ICP光谱仪测试杂质元素Al、Ca、Cr、Mg、Na、Ni、S、Si的含量。
实施例1
一种制备磷酸铁的方法:
(1)取100g磷含量15.5wt%的胶磷矿和42g铁含量65.2wt%磁铁矿石研磨至平均粒径为10μm后加入20g 40wt%硝酸水溶液和30g 50wt%硫酸水溶液混合均匀;
(2)将混合均匀的物料置于烧结炉中,在500℃下烧结12h获得磷酸铁粗品;
(3)磷酸铁粗品加500mL 20wt%氢氧化钠水溶液在50℃下洗涤3h;加500mL水洗涤30min后加600mL 10wt%盐酸在50℃下洗涤3h,再经过干燥得到磷酸铁。
分别对磷酸铁粗品和磷酸铁中杂质元素的含量进行测定,计算磷酸铁粗品和磷酸铁的纯度,如表1所示,其中纯度的计算公式为:纯度(%)=(1-杂质元素的总含量)×100%;同时对磷酸铁中铁元素的含量进行测定,计算铁元素的回收率,其中回收率的计算公式为:铁元素回收率(%)=原料中铁元素的总质量/磷酸铁中铁元素的质量×100%,如表1所示。
另外,磷酸铁中杂质元素的含量如表2所示。
实施例2
一种制备磷酸铁的方法:
(1)取150g磷含量18.4wt%的磷铝石和75g铁含量63wt%赤铁矿石研磨至粒径15μm后加入50g 50wt%硝酸水溶液和30g柠檬酸混合均匀;
(2)将混合均匀的物料置于烧结炉中,在800℃下烧结18h获得磷酸铁粗品;
(3)磷酸铁加600mL 15wt%氢氧化钾水溶液在80℃下洗涤5h;加500mL水洗涤30min后加400mL 30wt%硫酸水溶液在60℃下洗涤4h,再经过干燥得到磷酸铁。
分别对磷酸铁粗品和磷酸铁中杂质元素的含量进行测定,计算磷酸铁粗品和磷酸铁的纯度,如表1所示,其中纯度的计算公式为:纯度(%)=(1-杂质元素的总含量)×100%;同时对磷酸铁中铁元素的含量进行测定,计算铁元素的回收率,其中回收率的计算公式为:铁元素回收率(%)=原料中铁元素的总质量/磷酸铁中铁元素的质量×100%,如表1所示。
另外,磷酸铁中杂质元素的含量如表2所示。
实施例3
一种制备磷酸铁的方法:
(1)取200g磷含量16.5wt%的氟磷灰石和120g铁含量50.4wt%褐铁矿石研磨至粒径8μm后加入100g草酸和50g葡萄糖酸混合均匀;
(2)将混合均匀的物料置于烧结炉中,在1000℃下烧结5h获得磷酸铁粗品;
(3)磷酸铁加1000mL 10wt%氨水溶液在40℃下洗涤6h;加800mL水洗涤30min后加600mL 20wt%硝酸水溶液在80℃下洗涤6h,再经过干燥得到磷酸铁。
分别对磷酸铁粗品和磷酸铁中杂质元素的含量进行测定,计算磷酸铁粗品和磷酸铁的纯度,如表1所示,其中纯度的计算公式为:纯度(%)=(1-杂质元素的总含量)×100%;同时对磷酸铁中铁元素的含量进行测定,计算铁元素的回收率,其中回收率的计算公式为:铁元素回收率(%)=原料中铁元素的总质量/磷酸铁中铁元素的质量×100%,如表1所示。
另外,磷酸铁中杂质元素的含量如表2所示。
对比例1
一种以磷矿和铁矿为原料制备磷酸铁的方法,包括如下步骤:
(1)取100g磷含量15.5wt%的胶磷矿加500mL 20wt%硫酸水溶液在80℃下消解10h获得磷矿消解液;
(2)取42g铁含量65.2wt%磁铁矿石加500mL 40wt%硝酸水溶液在90℃下消解12h获得铁矿消解液;
(3)将上述步骤(1)和步骤(2)所得磷、铁消解液混合均匀,加氢氧化钠调节pH至2沉降磷酸铁,得到磷酸铁粗品,在磷酸铁粗品加500mL 20wt%氢氧化钠水溶液在50℃下洗涤3h;加500mL水洗涤30min后加600mL 10wt%盐酸在50℃下洗涤3h,再经过干燥得到磷酸铁。
分别对磷酸铁粗品和磷酸铁中杂质元素的含量进行测定,计算磷酸铁粗品和磷酸铁的纯度,如表1所示,其中纯度的计算公式为:纯度(%)=(1-杂质元素的总含量)×100%;同时对磷酸铁中铁元素的含量进行测定,计算铁元素的回收率,其中回收率的计算公式为:铁元素回收率(%)=原料中铁元素的总质量/磷酸铁中铁元素的质量×100%,如表1所示。
另外,磷酸铁中杂质元素的含量如表2所示。
表1
表2
根据表1和表2可知,各实施例得到的磷酸铁的纯度显著高于对比例,且各种杂质元素均显著低于对比例,更加有利于作为电极活性材料的原料。同时各实施例中铁元素的回收率也显著高于对比例,有利于降低磷酸铁的生产成本。对比例1中,通过将磷源和铁源消解后经过沉降得到磷酸铁,虽然在消解沉降过程中能够减少杂质含量,因此磷酸铁粗品的纯度相较于实施例较高,但是沉降过程中形成的杂质不易在后续洗涤过程中去除,导致杂质含量较高,同时消解沉降也会导致铁元素的损失,导致铁元素的回收率较低。
最后应说明的是:以上各实施例仅用以说明本申请的技术方案,而非对其限制;尽管参照前述各实施例对本申请进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本申请各实施例技术方案的范围。
- 泡料、瓶片循环均化装置的循环提料机构
- 高粘性复合材料均匀摊料工艺及装置
- 高粘性复合材料高效摊料工艺及装置
