磁性SERS生物传感器及其制备方法和应用
文献发布时间:2023-06-19 11:34:14
技术领域
本发明属于生物传感器制备技术领域,具体涉及一种新型磁性SERS生物传感器,可用于同时检测mRNA和miRNA等多种生物标志物。该传感器在生物医学领域有着广泛的应用前景。
背景技术
MicroRNA(miRNA)在许多生物学过程中起着至关重要的作用,例如细胞分化,细胞凋亡和癌症的发展。此外,已有研究结果表明,超过80%的人类肿瘤中存在miRNA-21过表达,而正常细胞中不存在。由于miRNA体积小、丰度低,其检测是一个具有挑战性的问题。除了miRNA外,mRNA可以翻译成蛋白质,蛋白质也被认为是在各种肿瘤中过表达的重要生物标志物。
一些检测miRNAs的新技术已经开发出来,例如实时定量荧光PCR扩增、表面增强拉曼光谱(SERS)、电化学、比色法和荧光成像检测平台。其中,基于SERS的生物传感器具有成本效益高、灵敏度高、操作简单、甚至可以单分子检测等优点,具有广阔的应用前景。
发明内容
有鉴于此,本发明的目的在于提出了一种磁性SERS生物传感器,可以用于同时检测癌细胞中mRNA和miRNA等多种生物标志物,并且操作简单,具有较高的灵敏性和特异性。
为了实现本发明的目的,一方面,本发明提出一种同时检测多个靶标的磁性SERS生物传感器,包括Fe
在一些实施例中,所述拉曼报告分子选自对氨基苯硫酚(4-ATP)、二硫代双硝基苯甲酸(DTNB)、罗丹明6G(R6G)、结晶紫(CV)、孔雀石绿(MG)或4,4’-联吡啶(44DP)。
在一些实施例中,所述Au@Ag纳米颗粒通过Au-S键与所述捕获探针DNA共价连接。
在一些实施例中,所述Fe
另一方面,本发明提出一种所述磁性SERS生物传感器的制备方法,包括:
将金纳米颗粒分别与不同拉曼报告分子共同孵育,然后在金纳米颗粒的表面上形成银壳,得到分别包含不同拉曼报告分子的多种Au@Ag纳米颗粒;
将多种Au@Ag纳米颗粒分别与不同捕获探针DNA的一端共价连接,得到多种捕获探针DNA-Au@Ag纳米颗粒复合物,将所述复合物混合并将捕获探针DNA的另一端共价连接到Fe
在一些实施例中,通过将所述Au@Ag纳米颗粒与捕获探针DNA一起孵育以使所述Au@Ag纳米颗粒通过Au-S键与所述捕获探针DNA共价连接。
在一些实施例中,所述方法包括将所述Fe
又一方面,本发明提出一种利用所述磁性SERS生物传感器检测样品中多个靶标的方法,包括:
将样品和SERS生物传感器加入含有双链特异性核酸酶(DSN)的缓冲溶液中,在50-60℃下孵育0.5-2小时,洗涤SERS生物传感器并分散到溶液中进行表面增强拉曼光谱检测。
在一些实施例中,双链特异性核酸酶DSN的量为1-5U/mL,优选为3U/mL。
在一些实施例中,所述靶标包括多种mRNA或miRNA。
在磁性SERS生物传感器中,Fe
本发明的生物传感器具有高特异性,能区分RNA序列中的单个碱基,可以检测真实肿瘤细胞系中的RNA,达到实际应用的价值。
与现有技术相比,本发明的磁性SERS生物传感器具有以下的有益效果:
基于稳定的Fe
附图说明
以下附图仅旨在于对本发明做示意性说明和解释,并不限定本发明的范围。其中:
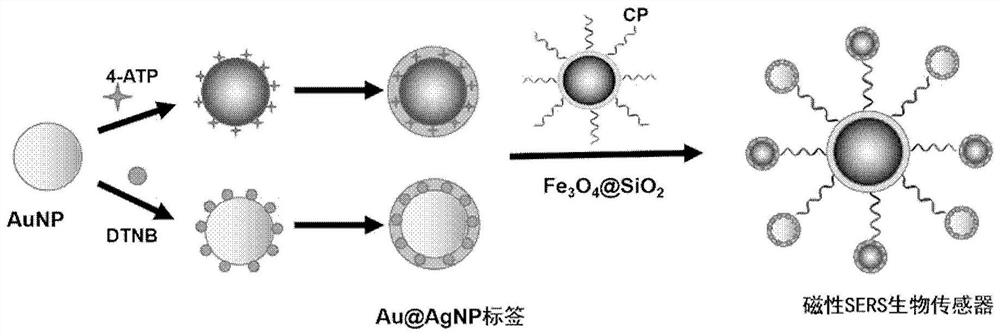
图1为本发明实施例中磁性生物传感器的制备示意图。
图2为本发明实施例中所制备的Fe
图3为本发明实施例中所制备的AuNPs和Au@AgNPs透射电镜图和紫外吸收光谱图。
图4为本发明实施例中所制备的磁性SERS生物传感器的透射电镜图。
图5为本发明实施例1中所制备的磁性SERS生物传感器用于检测p21mRNA的拉曼图谱,其中p21 mRNA的浓度为1fM至1nM。
图6为本发明实施例2中所制备的磁性SERS生物传感器用于检测miRNA-21的拉曼图谱,其中miRNA-21的浓度为1fM至1nM。
图7为本发明实施例3中所制备的磁性SERS生物传感器用于同时检测p21 mRNA和miRNA-21的拉曼图谱,其中p21 mRNA和miRNA-21的浓度为1fM至1nM。
图8为本发明实施例4中所制备的磁性SERS生物传感器用于检测真实癌症细胞中的RNA的拉曼图谱。
具体实施方式
为使本发明的目的、技术方案和优点更加清楚明白,以下结合具体实施例,并参照附图,对本发明作进一步的详细说明。
本发明实施例提供了一种磁性SERS生物传感器,包括Fe
如图1所示,本发明实施例中磁性SERS生物传感器的制备方法包括:
在金纳米颗粒(AuNPs)上分别固定拉曼报告分子对氨基苯硫酚(4-ATP)和二硫代双硝基苯甲酸(DTNB),随后在AuNPs的表面上形成银壳,制备得到包含不同拉曼报告分子的Au@AgNPs SERS纳米标签。
将Au@AgNPs SERS纳米标签和Fe
在本发明实施例中,所述磁性SERS生物传感器中Fe
(1)通过溶剂热反应法合成磁性Fe
通常,室温环境下将1.35g的FeCl
(2)制备核壳Fe
通常,取0.10g Fe
图2为本发明实施例中所制备的Fe
在本发明实施例中,所述磁性SERS生物传感器中SERS纳米标签(Au@AgNPs)通过以下制备方法获得:
(1)通过柠檬酸钠还原法合成直径约为23nm的金纳米颗粒(AuNPs)
首先,将100mL 0.01%(w/v)的HAuCl
(2)包含拉曼报告分子(4-ATP和DTNB)的Au@AgNPs SERS纳米标签的制备如下:
将100μL的1mM 4-ATP和DTNB溶液分别添加入制备好的AuNPs(10mL)溶液中,终浓度为10μM。室温下孵育2h后,以8000rpm的速度离心10min去除多余的拉曼报告分子,所得产物重新分散在10mL超纯水中。随后,为了在AuNPs的表面上形成银壳,将1.5mL(0.1M)抗坏血酸AA和2mL(1mM)AgNO
图3为本发明实施例中所制备的AuNPs和Au@AgNPs透射电镜图和紫外吸收光谱图。从图3的透射图像得出合成均匀的金纳米颗粒(AuNPs),直径大约为23nm。通过种子介导法合成Au@AgNPs,通过透射图像分析得出银壳的厚度估计为8nm。紫外吸收光谱表明Au在520nm处的吸收峰消失,并且8nm厚度的银壳在400nm处出现了新的吸收峰。这些结果证实了Au@AgNPs的成功合成。
在本发明实施例中,新型磁性SERS生物传感器的制备方法如下:
Au@AgNPs纳米标签和Fe
p21mRNA探针:NH2-TTTTTT CGC TGC AGG ACA CAT GGG GAG CCG AGG CAG CGTTTTTT-SH;
miRNA-21探针:NH2-TTTTTT CAA CAT CAG TCT GAT AAG CTA TTTTTT-SH
首先,将10μM CP溶液(p21 mRNA探针和miRNA-21探针)在90℃加热5min并缓慢冷却至室温进行预处理。两种CP溶液分别添加到100μL Au@AgNPs溶液中,并在室温下孵育12h以形成两种CP-Au@AgNPs。随后,将Fe
图4为本发明实施例中所制备的磁性SERS生物传感器的透射电镜图。从图中可以看出,Au@AgNPs纳米标签富集在Fe
在本发明实施例中,所述反应中拉曼报告分子的浓度优选为10μM。
在本发明实施例中,所述RNA检测反应的孵育温度优选为55℃;所述反应的时间优选为1小时,所述双链特异性核酸酶DSN(购于俄罗斯Evrogen公司)的量优选为每毫升3单位(U)。
在本发明实施例中,所述反应中RNA的浓度变化范围优选为1fM至1nM。
在检测反应体系中加入靶标RNA后,捕获探针CP可与靶标RNA杂交形成DNA-RNA异源双链体,被DSN酶特异性切割,使SERS纳米标签从Fe
实施例1
本实施例按照图1所示的路线制备磁性SERS生物传感器。
Au@AgNPs SERS纳米标签中包含的拉曼报告分子为4-ATP。需要说明的是,检测p21mRNA时的拉曼报告分子并不限于4-ATP,还可以选用DTNB、罗丹明6G、结晶紫等其他拉曼报告分子,只需确保一种拉曼报告分子和一种捕获探针仅与一种靶标对应即可。
本实施例1中包含报告分子4-ATP的Au@AgNPs纳米标签和Fe
使用磁性SERS生物传感器检测p21mRNA:
p21 mRNA定量测定步骤如下:在100μL反应溶液中进行p21 mRNA的SERS检测,反应溶液包括1×DSN主缓冲液(50mM Tris-HCl,pH 7.5)、5mM MgCl
图5本发明实施例1定量检测p21 mRNA的拉曼图谱,从图中可以得出,随着p21mRNA浓度的升高,拉曼强度显著降低。
实施例2
本实施例按照图1所示的路线制备磁性SERS生物传感器。
Au@AgNPs SERS纳米标签中包含的拉曼报告分子为DTNB。
本实施例2中包含报告分子DTNB的Au@AgNPs纳米标签和Fe
使用磁性SERS生物传感器检测miRNA-21:
miRNA-21定量测定步骤如下:在100μL反应溶液中进行miRNA-21的SERS检测,反应溶液包括1×DSN主缓冲液(50mM Tris-HCl,pH 7.5)、5mM MgCl
图6本发明实施例2定量检测miRNA-21的拉曼图谱,从图中可以得出,随着miRNA-21浓度的升高,拉曼强度显著降低。
实施例3
本实施例按照图1所示的路线制备磁性SERS生物传感器。
Au@AgNPs SERS纳米标签中包含的两种拉曼报告分子4-ATP和DTNB。
本实施例中包含两种报告分子4-ATP和DTNB的Au@AgNPs纳米标签和Fe
使用磁性SERS生物传感器同时检测p21 mRNA和miRNA-21:
同时检测p21 mRNA和miRNA-21步骤如下:在100μL反应溶液中进行p21 mRNA和miRNA-21的SERS检测,反应溶液包括1×DSN主缓冲液(50mM Tris-HCl,pH 7.5)、5mMMgCl
图7本发明实施例3定量检测p21 mRNA和miRNA-21的拉曼图谱,从图中可以得出,随着p21 mRNA和miRNA-21浓度的升高,拉曼强度显著降低。
实施例4
本实施例按照图1所示的路线制备磁性SERS生物传感器。
Au@AgNPs SERS纳米标签中包含的两种拉曼报告分子4-ATP和DTNB。
本实施例中包含两种报告分子4-ATP和DTNB的Au@AgNPs纳米标签和Fe
非小细胞肺癌细胞系(A549),人肾上皮细胞系(293T)和人宫颈癌细胞系(HeLa)三种人类细胞系来制备生物学样品总RNA。
使用磁性SERS生物传感器检测癌细胞系中的p21 mRNA和miRNA-21:
检测癌细胞系RNA的步骤如下:在100μL反应溶液中进行癌细胞系RNA的SERS检测,反应溶液包括1×DSN主缓冲液(50mM Tris-HCl,pH 7.5)、5mM MgCl
图8本发明实施例4应用于真实的生物样品检测,分别使用了三种细胞系,非小细胞肺癌细胞系(A549),人肾上皮细胞系(293T)和人宫颈癌细胞系(HeLa)用于检测p21 mRNA和miRNA-21。实验结果表明,该磁性SERS传感器能够区别不同癌症细胞系中的RNA的表达水平。通过与传统技术qPCR结果对比,甚至能够定量RNA的浓度。
由以上实施例可知,本发明了一种磁性SERS生物传感器,可同时检测mRNA和miRNA。该SERS生物传感器由Fe
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和修饰,这些改进和修饰也应视为在本发明的保护范围内。
- 磁性SERS生物传感器及其制备方法和应用
- 一种用于铅离子检测的CHA-SERS生物传感器及其制备方法和应用
