一种碳化铌纳米材料的应用及促进细胞增殖的细胞培养基
文献发布时间:2023-06-19 11:30:53
技术领域
本发明属于生物医用材料技术领域,尤其涉及一种碳化铌纳米材料的应用及促进细胞增殖的细胞培养基。
背景技术
细胞培养基是生物制药生产的关键原材料之一。是人工模拟细胞在体内生长的营养环境,提供细胞营养和促进细胞生长增殖的物质基础,可广泛应用于疫苗、单抗等生物制药产业,以及各类生物医药技术研究。
进入21世纪,医用植入物得到了广泛应用,医用植入物引发的细菌感染成为了目前丞待解决的重要临床问题。临床医学研究表明,入侵细菌倾向于迅速粘附到生物活性植入物表面并形成生物膜,从而在存在敌意的宿主环境中生存。生物膜的聚合基质抵抗抗生素和免疫细胞的渗透,与浮游细菌相比表现出极大的抵抗力。考虑到生物被膜的形成是种植体相关感染的主要病理特征,细菌附着是生物被膜形成的主要原因,人们已经做出了广泛的努力来开发含有抗菌剂的植入物。
到目前为止,这些设计主要是抑制细菌粘附,对已经形成的生物膜影响有限。此外,由于银等传统抗菌离子的长期使用,耐银细菌已有报道,这对传统治疗方案可能诱导耐药性发出了警告。而且,银等传统抗菌离子对细胞的增殖一般没有促进作用。
发明内容
本发明实施例的目的在于提供一种碳化铌纳米材料在促进细胞增殖中的应用,旨在解决背景技术中提出的问题。
本发明实施例是这样实现的,一种碳化铌纳米材料在促进细胞增殖中的应用。
作为本发明实施例的一个优选方案,所述细胞为内皮细胞。
作为本发明实施例的另一个优选方案,所述碳化铌纳米材料的粒径为10~90nm。
本发明实施例的另一目的在于提供一种促进细胞增殖的细胞培养基,包括基础培养基和碳化铌纳米材料。
作为本发明实施例的另一个优选方案,所述细胞为内皮细胞。
作为本发明实施例的另一个优选方案,所述碳化铌纳米材料的粒径为10~90nm。
作为本发明实施例的另一个优选方案,所述细胞培养基还包括白蛋白和/或细胞生长因子。
作为本发明实施例的另一个优选方案,所述基础培养基为内皮细胞培养液,所述白蛋白为牛血清白蛋白,所述细胞生长因子为血管内皮生长因子。
作为本发明实施例的另一个优选方案,所述细胞培养基中,白蛋白的体积浓度为5%~20%,细胞生长因子的体积浓度为0.1%~2%。
作为本发明实施例的另一个优选方案,所述细胞培养基中,碳化铌纳米材料的浓度为1~100μg/mL。
本发明实施例提供的一种碳化铌纳米材料在促进细胞增殖中的应用,通过利用碳化铌纳米材料下调细菌能量代谢途径,抑制生物膜的形成,通过激活辅助基因调节来破坏生物膜,促进生物膜的脱落,从而直接消除细菌,可有效降低根除细菌所需的温度,并减轻可能的正常组织损伤,清除感染微环境中过量的活性氧,从而减轻促炎反应。另外,碳化铌纳米材料可显著上调血管内皮生长因子等细胞生长因子的表达,促进血管内皮细胞的增殖、迁移,明显促进血管生成和伤口愈合。
附图说明
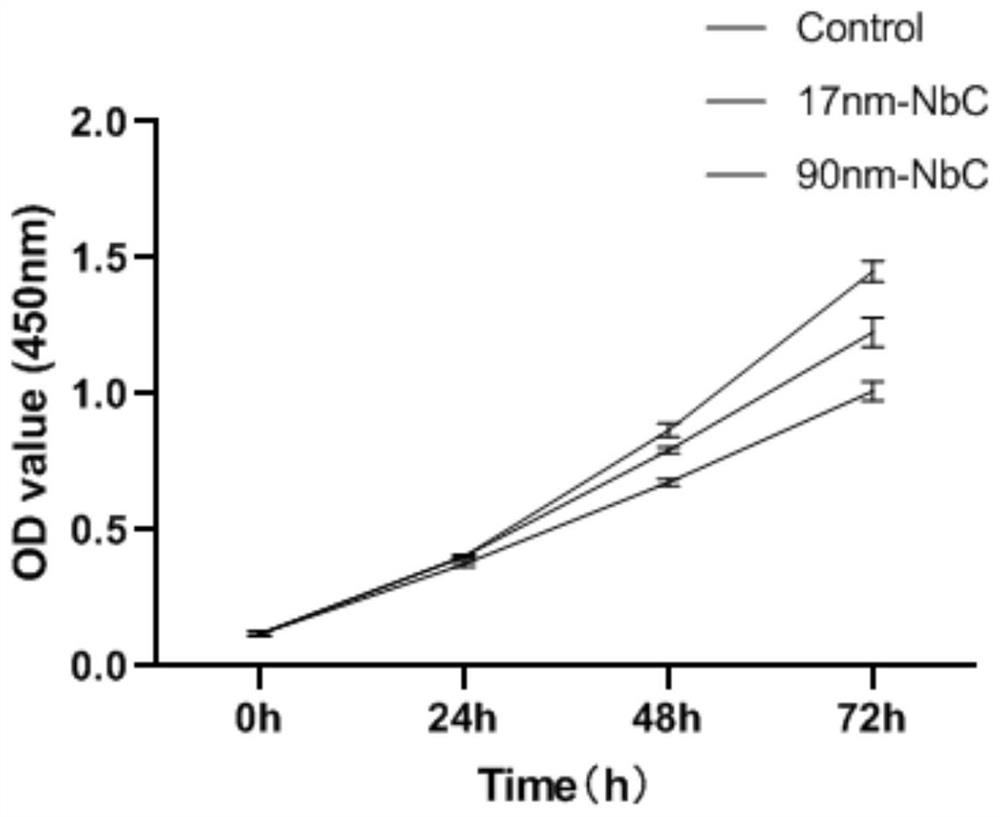
图1为含碳化铌纳米材料的细胞培养基促进内皮细胞增殖实验结果图。
图2为含碳化铌纳米材料的细胞培养基的毒性实验结果图。
图3为细胞增殖实验结果图。
图4为血管内皮生长因子(VEGF)免疫荧光阳性率结果图。
具体实施方式
下面将结合本发明实施例,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
实施例1
该实施例提供了一种促进细胞增殖的细胞培养基,其由不含血清、双抗、生长因子的内皮细胞培养液(ECM基础培养基)和碳化铌纳米材料混合而得,其中,碳化铌纳米材料的质量含量为1%,碳化铌纳米材料的粒径为17nm。
实施例2
该实施例提供了一种促进细胞增殖的细胞培养基,其由不含血清、双抗、生长因子的内皮细胞培养液(ECM基础培养基)和碳化铌纳米材料混合而得,其中,碳化铌纳米材料的质量含量为0.1%,碳化铌纳米材料的粒径为90nm。
实施例3
该实施例提供了一种促进细胞增殖的细胞培养基,其由不含血清、双抗、生长因子的内皮细胞培养液(ECM基础培养基)和碳化铌纳米材料混合而得,其中,碳化铌纳米材料的质量含量为2%,碳化铌纳米材料的粒径为10nm。
实施例4
该实施例提供了一种促进细胞增殖的细胞培养基,其制备方法包括以下步骤:
S1、称取1mL市售的血管内皮生长因子ECGS(Cat.#1052),50mL市售的牛血清白蛋白(FBS,Cat.#0025)以及1mg市售的粒径为10nm的碳化铌纳米颗粒,备用。
S2、将上述血管内皮生长因子ECGS、牛血清白蛋白以及碳化铌纳米颗粒单独添加至适量的内皮细胞培养液(ECM)中,以制得1000mL的细胞培养基。
实施例5
该实施例提供了一种促进细胞增殖的细胞培养基,其制备方法包括以下步骤:
S1、称取20mL市售的血管内皮生长因子ECGS(Cat.#1052),200mL市售的牛血清白蛋白(FBS,Cat.#0025)以及100mg市售的粒径为90nm的碳化铌纳米颗粒,备用。
S2、将上述血管内皮生长因子ECGS、牛血清白蛋白以及碳化铌纳米颗粒单独添加至适量的内皮细胞培养液(ECM)中,以制得1000mL的细胞培养基。
实施例6
该实施例提供了一种促进细胞增殖的细胞培养基,其制备方法包括以下步骤:
S1、称取5mL市售的血管内皮生长因子ECGS(Cat.#1052),100mL市售的牛血清白蛋白(FBS,Cat.#0025)以及20mg市售的粒径为17nm的碳化铌纳米颗粒,备用。
S2、将上述血管内皮生长因子ECGS、牛血清白蛋白以及碳化铌纳米颗粒单独添加至适量的内皮细胞培养液(ECM)中,以制得1000mL的细胞培养基。
实施例7
该实施例提供了一种促进细胞增殖的细胞培养基,其制备方法包括以下步骤:
S1、称取10mL市售的血管内皮生长因子ECGS(Cat.#1052),120mL市售的牛血清白蛋白(FBS,Cat.#0025)以及50mg市售的粒径为50nm的碳化铌纳米颗粒,备用。
S2、将上述血管内皮生长因子ECGS、牛血清白蛋白以及碳化铌纳米颗粒单独添加至适量的内皮细胞培养液(ECM)中,以制得1000mL的细胞培养基。
实施例8
该实施例提供了一种促进细胞增殖的细胞培养基,其制备方法包括以下步骤:
S1、称取15mL市售的血管内皮生长因子ECGS(Cat.#1052)以及80mg市售的粒径为30nm的碳化铌纳米颗粒,备用。
S2、将上述血管内皮生长因子ECGS以及碳化铌纳米颗粒单独添加至适量的内皮细胞培养液(ECM)中,以制得1000mL的细胞培养基。
实施例9
该实施例提供了一种促进细胞增殖的细胞培养基,其制备方法包括以下步骤:
S1、称取150mL市售的牛血清白蛋白(FBS,Cat.#0025)以及30mg市售的粒径为70nm的碳化铌纳米颗粒,备用。
S2、将上述牛血清白蛋白以及碳化铌纳米颗粒单独添加至适量的内皮细胞培养液(ECM)中,以制得1000mL的细胞培养基。
实施例10
该实施例提供了一种促进细胞增殖的细胞培养基,其制备方法包括以下步骤:
S1、称取12mL市售的血管内皮生长因子ECGS(Cat.#1052),80mL市售的牛血清白蛋白(FBS,Cat.#0025)以及60mg市售的粒径为90nm的碳化铌纳米颗粒,备用。
S2、将上述血管内皮生长因子ECGS、牛血清白蛋白以及碳化铌纳米颗粒单独添加至适量的内皮细胞培养液(ECM)中,以制得1000mL的细胞培养基。
实验例:
一、含碳化铌纳米材料的细胞培养基促进内皮细胞增殖实验:
(1)水浴锅提前升温至37℃,将培养基于水浴锅中预热,双抗常温解冻,同时打开超净台紫外灯照射半小时;
(2)未拆封的不含血清、双抗、生长因子的ECM基础培养基于超净工作台内分装为等量4份,其中,1份不做任何处理,标记为空白组培养基A;1份添加1%双抗,标记为对照组培养基B;1份添加质量浓度为1%的粒径为90nm的碳化铌纳米材料,标记为碳化铌-90nm组培养基C;1份添加质量浓度为1%的粒径为17nm的碳化铌纳米材料,标记为碳化铌-17nm组培养基D。
(3)从液氮罐中取出冻存的人脐静脉内皮细胞HUVECs,迅速放置在37℃的水浴锅中使细胞解冻,之后迅速转移到超净工作台里进行如下操作:将冻存管内的细胞液用移液器小心地转移到含有5mL培养基的离心管中,1000rpm离心3分钟,弃上清液,用ECM完全培养基重悬,转移到T75培养瓶中,然后放入37℃含5%CO
(4)第二天观察细胞状态,待细胞状态良好后,传一代培养至细胞密度达到80%~90%时进行下面的实验;
(5)去培养基,10mL PBS清洗2次,加入5mL含0.05%EDTA的胰蛋白酶,轻轻晃动,均匀覆盖,轻敲培养瓶底,于37℃细胞培养箱消化3min,肉眼观察到飘白色絮状物,显微镜下观察大多数细胞悬浮,加入5mL培养基终止胰酶消化,1mL移液枪吹打5~10下至均匀,转移至15mL离心管,1000rpm离心3min,弃上清液,加入1mL ECM完全培养基,用枪吹打均匀,制备混悬液,注意不要产生气泡;用细胞计数板计数为6×10
(6)将细胞重悬液配置为1×10
二、含碳化铌纳米材料的细胞培养基的细胞毒性实验如下:
(1)水浴锅提前升温至37℃,将培养基于水浴锅中预热,双抗常温解冻,同时打开超净台紫外灯照射半小时;
(2)取等量不含血清、双抗、生长因子的ECM基础培养基8份,分别配置0μg/mL,1μg/mL,2.5μg/mL,5μg/mL,10μg/mL,20μg/mL,50μg/mL,100μg/mL8个浓度碳化铌纳米颗粒的培养基。
(3)从液氮罐中取出冻存的人脐静脉内皮细胞HUVECs,迅速放置在37℃的水浴锅中使细胞解冻,之后迅速转移到超净工作台里进行如下操作:将冻存管内的细胞液用移液器小心地转移到含有5mL培养基的离心管中,1000rpm离心3分钟,弃上清液,用ECM完全培养基重悬,转移到T75培养瓶中,然后放入37℃含5%CO
(4)第二天观察细胞状态,待细胞状态良好后,传一代培养至细胞密度达到80%~90%时进行下面的实验;
(5)去培养基,10mL PBS清洗2次,加入5mL含0.05%EDTA的胰蛋白酶,轻轻晃动,均匀覆盖,轻敲培养瓶底,于37℃细胞培养箱消化3min,肉眼观察到飘白色絮状物,显微镜下观察大多数细胞悬浮,加入5mL培养基终止胰酶消化,1mL移液枪吹打5~10下至均匀,转移至15mL离心管,1000rpm离心3min,弃上清液,加入1mL ECM完全培养基,用枪吹打均匀,制备混悬液,注意不要产生气泡;用细胞计数板计数为6×10
(6)将细胞重悬液配置为1×10
图2的结果显示,不同浓度碳化铌纳米颗粒作用48h后,各组细胞的存活率受到不同程度的影响。当浓度为50μg/ml 时,细胞相对活力与Control组比较降低,差异有统计学意义(P<0.001),说明高浓度(>50μg/ml) 碳化铌纳米颗粒抑制细胞增殖,呈浓度依赖性抑制细胞活力。
另外,图3为碳化铌纳米材料促进细胞增殖实验效果,其中,Control柱状图代表HUVECs在不含碳化铌的细胞培养基中培养24小时的细胞数目(设为100%),其他柱状图代表Huvecs在含有17nm-NbC和90nm-NbC培养基中培养24小时后的细胞数目(相对于Control组的百分比),结果显示,含有NbC的培养基中HUVECs的细胞数目均大于Control组,说明碳化铌纳米材料具有促进HUVECs增殖的功能。其中17nm-碳化铌(约140%)效果优于90nm-碳化铌(约120%)。
图4为血管内皮生长因子(VEGF)免疫荧光阳性率结果,其中,17nm-NbC组阳性率为75%,90nm-NbC组阳性率为56%,均远高于Control组,差异有统计学意义(P<0.001),说明碳化铌纳米材料显著上调VEGF的表达,明显促进血管生成和伤口愈合。
综上所述,本发明实施例提供的一种碳化铌纳米材料在促进细胞增殖中的应用,通过利用碳化铌纳米材料下调细菌能量代谢途径,抑制生物膜的形成,通过激活辅助基因调节来破坏生物膜,促进生物膜的脱落,从而直接消除细菌,可有效降低根除细菌所需的温度,并减轻可能的正常组织损伤,清除感染微环境中过量的活性氧,从而减轻促炎反应。另外,碳化铌纳米材料可显著上调血管内皮生长因子等细胞生长因子的表达,促进血管内皮细胞的增殖、迁移,明显促进血管生成和伤口愈合。
此外,应当理解,虽然本说明书按照实施方式加以描述,但并非每个实施方式仅包含一个独立的技术方案,说明书的这种叙述方式仅仅是为清楚起见,本领域技术人员应当将说明书作为一个整体,各实施例中的技术方案也可以经适当组合,形成本领域技术人员可以理解的其他实施方式。
- 一种碳化铌纳米材料的应用及促进细胞增殖的细胞培养基
- 促进CIK细胞增殖分化的人参多糖、培养基、培养方法和应用
