UMI-77在制备抗脓毒症药物中的应用
文献发布时间:2024-04-18 19:52:40
技术领域
本发明涉及脓毒症治疗技术领域,具体地,涉及UMI-77在制备抗脓毒症药物中的应用。
背景技术
脓毒症是以全身感染性炎症反应为特征,是外科患者发病和死亡的主要因素。脓毒症的超炎症反应可在体内释放多种炎症介质,最终导致多个器官功能障碍、凝血甚至死亡。脓毒症的病死率已经超过心肌梗死,成为重症监护病房内非心脏病人死亡的主要原因。
随着脓毒症机制研究地不断深入,针对脓毒症机制特点,也有越来越多的药物被开发用于治疗脓毒症,主要有:(a)抗炎症介质药物:针对TNF-α、IL-1β、IL-6及HMBG-1等细胞因子的细胞因子拮抗剂以及甾体和非甾体抗炎药物;(b)免疫调节剂;(c)模式识别受体拮抗剂:主要针对TLR4受体。虽然,这些药物治疗在动物实验及临床试验中都显现出了一定的效果,但均未能有效降低脓毒症的死亡率。
发明内容
针对现有技术中存在的问题,本发明提供了UMI-77在制备抗脓毒症药物中的应用,能够大大降低脓毒症的死亡率。
为实现上述技术目的,本发明采用如下技术方案:一种UMI-77在制备抗脓毒症药物中的应用。
进一步地,所述UMI-77的给药浓度为5mg/kg-10mg/kg,所述UMI-77的给药量为0.1mL/20g体重-0.2mL/20g体重。
进一步地,所述UMI-77连续给药5天以上。
进一步地,所述UMI-77的给药方式为腹腔注射。
与现有技术相比,本发明具有如下有益效果:本发明首次公开了UMI-77在制备抗脓毒症药物中的应用,揭示了UMI-77抗脓毒症主要跟应激反应、凝血反应以及防御反应等相关,从而通过调控相应的蛋白如凝血因子12、C4b等抑制机体内炎症风暴因子如:KC、RANTES、LIX、TNF RI、IL-6、TARC、IL-1β、MCP-5、G-CSF、MCP-1、TNF-α、MIG、ICAM-1、TIMP-M-1和IL-10的释放,从而减少脓毒症机体各器官病理损伤起到保护脑神经元、改善肺组织肺泡增厚情况、改善心肌充血以及改善小鼠肠道结构损伤的作用,大大提高了脓毒症患者的存活机率。
附图说明
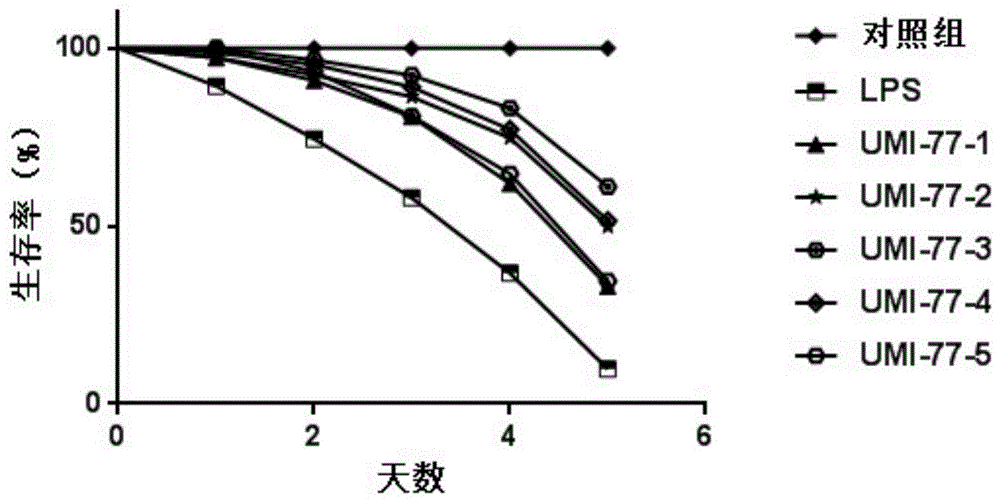
图1为本发明中患有脓毒症的小鼠在UMI-77治疗后的生存率预测图;
图2为空白组1、LPS组1、UMI-77-1组、UMI-77-3组、UMI-77-5组BALB/c小鼠的脑、肺、心、小肠的形态学变化图;
图3为空白组1、LPS组1、UMI-77-1组、UMI-77-3组、UMI-77-5组BALB/c小鼠的肝、脾、肾的形态学变化图;
图4为UMI-77-3组中BALB/c小鼠对脓毒症炎症因子风暴的影响示意图;
图5为空白组1、LPS组1、UMI-77-3组的PCA分析示意图;
具体实施方式
下面结合附图和实施例对本发明的技术方案作进一步地解释说明。
本发明提供了一种UMI-77在制备抗脓毒症药物中的应用,通过给药浓度为5mg/kg-10mg/kg、给药量为0.1mL/20g体重-0.2mL/20g体重,并连续腹腔注射给药5天以上,腹腔注射的药效比口服给药的药效更快,更适用于脓毒症这种急性病的治疗。本发明首次提出UMI-77在制备抗脓毒症药物中的应用,揭示了UMI-77抗脓毒症的作用机理,UMI-77的使用,能够显著降低脓毒症的死亡率。
实施例1
本实施例通过内毒素LPS来验证UMI-77对脓毒症的影响:
(1)取BALB/c小鼠105只,每只BALB/c小鼠的体重为20±2g,将BALB/c小鼠随机等分为7组,分别为空白组1、LPS组1、UMI-77-1组、UMI-77-2组、UMI-77-3组、UMI-77-4组、UMI-77-5组;
(2)先采用尾静脉注射方式为除去空白组的其余5组BALB/c小鼠注射内毒素LPS,每只BALB/c小鼠注射的内毒素LPS的浓度为18mg/kg、剂量为0.1mL/20g体重;
(3)UMI-77-1组、UMI-77-2组、UMI-77-3组、UMI-77-4组、UMI-77-5组在注射内毒素LPS后分别腹腔注射浓度为3.5mg/kg、5.0mg/kg、7.0mg/kg、10.0mg/kg、14.0mg/kg的UMI-77,且UMI-77的腹腔注射剂量为0.1mL/20g体重,连续腹腔注射给药5天;空白组和LPS组给予相应剂量的基质;
(4)空白组1、LPS组1、UMI-77-1组、UMI-77-2组、UMI-77-3组、UMI-77-4组、UMI-77-5组的BALB/c小鼠分笼饲养,给等量、充足的饲料和水,观察并记录各组BALB/c小鼠在5天内的一般情况(精神状态、食欲、活动度和对刺激的反应)、存活数量及具体死亡时间;
(5)第5天给药后24h内将各组BALB/c小鼠全部处死,取材备用。
根据5天对各组BALB/c小鼠的存活数量记载,可知:第五天给药后,对照组1的BALB/c小鼠全部存活,存活率为100%,说明该组的BALB/c小鼠是正常的;LPS组1的BALB/c小鼠只存活4只,存活率为26.27%;UMI-77-1组的BALB/c小鼠存活8只,存活率为53.33%,UMI-77-2组的BALB/c小鼠存活10只,存活率为66.67%,UMI-77-3组的BALB/c小鼠存活11只,存活率为73.33%,UMI-77-4组的BALB/c小鼠存活10只,存活率为66.67%,UMI-77-5组的BALB/c小鼠存活8只,存活率为53.33%。根据上述存活率可知,患有脓毒症的小鼠在不进行药物干预的情况下,存活率非常低,但是经过UMI-77进行治疗后的小鼠的第五天存活率由26.27%上升到53.33%以上,患有脓毒症的BALB/c小鼠通过UMI-77的给药治疗后,BALB/c小鼠的存活率大幅度提升,说明UMI-77对脓毒症具有一定的疗效,同时,UMI-77-2组、UMI-77-3组、UMI-77-4组中BALB/c小鼠的第五天存活率超过60%,说明5mg/kg-10mg/kg的UMI-77给药浓度具有更好的抗脓毒症效果。
本发明还通过GraphPad Prism 7软件对7组BALB/c小鼠的五天生存率进行生存分析,如图1所示,发现空白组1BALB/c小鼠的生存率为100%;而LPS组1BALB/c小鼠从第1天至第5天的生存率分别为89.333%、74.444%、57.901%、36.671%和9.779%;UMI-77-1组BALB/c小鼠从1天至第5天的生存率分别为97.333%、90.844%、80.751%、61.909%和33.018%;UMI-77-2组BALB/c小鼠从1天至第5天的生存率分别为97.333%、92.467%、86.302%、74.795%和49.864%;UMI-77-3组BALB/c小鼠从1天至第5天的生存率分别为100.0%、96.667%、92.370%、83.133%和60.964%;UMI-77-4组BALB/c小鼠从1天至第5天的生存率分别为98.667%、95.378%、89.019%、77.150%和51.433%;UMI-77-1组BALB/c小鼠从1天至第5天的生存率分别为100.0%、93.333%、80.889%、64.711和34.513%;由此可知,UMI-77-1组、UMI-77-2组、UMI-77-3组、UMI-77-4组、UMI-77-5组中的BALB/c小鼠的生存率明显高于LPS组1BALB/c小鼠生存率,说明UMI-77能够对脓毒症具有一定的抑制作用,而其中UMI-77-2组、UMI-77-3组、UMI-77-4组小鼠的最终生存率都接近或大于50%,进一步证明,给药浓度为5mg/kg-10mg/kg的UMI-77具有更好的抗脓毒症效果;UMI-77-1组的第五天存活率仅为33.018%,说明UMI-77的给药浓度过低,不能够很好的抑制炎症因子的释放,从而导致死亡率上升;UMI-77-5组的第五天存活率仅为34.513%,说明UMI-77的给药浓度过高,会产生大量的副作用,从而加重死亡率。此外,从图1上可以看出LPS组、UMI-77-1组、UMI-77-2组、UMI-77-3组、UMI-77-4组、UMI-77-5组中的5天内的死亡变化率均呈现逐步上升的趋势,符合脓毒症中炎症因子反复发作的过程。
如图2,探究了空白组1、LPS组1、UMI-77-1组、UMI-77-3组、UMI-77-5组BALB/c小鼠的脑、肺、心、小肠的形态学变化,可以看出LPS组1BALB/c小鼠脑组织中部分神经元和胶质细胞形态结构改变,细胞间隙明显大于空白组;肺组织肺泡腔增厚断裂,炎症细胞浸润较空白组明显;心脏组织心肌毛细血管轻度充血,LPS组1BALB/c小鼠心肌细胞间隙内炎症细胞浸润明显大于空白组;LPS组1BALB/c小鼠的小肠组织较空白组肠道结构损伤严重,腺体紊乱,每层结构边界模糊,有大量炎症细胞浸润;而从UMI-77-1组、UMI-77-3组、UMI-77-5组可以看出UMI-77能抑制脑、心、肺和小肠中的炎症细胞浸润,减少炎症反应,减少各器官病理损伤从而起到保护脑神经元、改善肺组织肺泡增厚情况、改善心肌充血以及改善小鼠肠道结构损伤的作用,其中UMI-77-3组表现最为显著,与其它两组具有明显差异。如图3探究了空白组1、LPS组1、UMI-77-1组、UMI-77-3组、UMI-77-5组BALB/c小鼠的肝、脾、肾的形态学变化,可以看出各组的肝、脾和肾组织均无显著差异,表明该剂量下的LPS和UMI-77对BALB/c小鼠的肝、脾、肾均无明显影响。
根据生存分析和病理观察结果显示,给药浓度为7.0mg/kg的UMI-77治疗脓毒症的效果最好,因此,将该剂量的UMI-77用于进一步的研究,如图4所示,LPS组1中KC、RANTES、LIX、TNF RI、IL-6、TARC、IL-1β、MCP-5、G-CSF、MCP-1、TNF-α、MIG、ICAM-1、TIMP-M-1、IL-10的水平显著升高(p<0.05),而7.0mg/kg UMI-77可显著降低除IL-10外上述细胞因子的水平。这些结果表明,UMI-77治疗脓毒症可能最终通过抑制特征性炎症风暴相关细胞因子。
如图5,通过空白组1、LPS组1、UMI-77-3组进行蛋白组学分析,将该三组BALB/c小鼠小鼠血浆进行分析鉴定到共1151个蛋白,保留Protein FDR置信度高(FDR<1%)的蛋白,并排除污染蛋白、protein groups的蛋白,最终还剩下866个蛋白,整体数据缺失率为0。对三组进行PCA分析发现三个组别相互之间明显区分,说明LSP组1和空白组1具有显著差异,经过UMI-77干预后的UMI-77-3组与LSP组1之间的蛋白也具有显著差异。进一步对866个蛋白进行GO分析发现UMI-77抗脓毒症主要跟应激反应、凝血反应以及防御反应等相关,并对GO分析里的关键蛋白与UMI-77进行分子对接,发现UMI-77与这些关键蛋白的自由结合能均<-5kcal/mol,表明UMI-77具有与这些关键蛋白结合的能力,如表1所示。
表1:与UMI-77自由结合的关键蛋白
/>
实施例2
本实施例用于探究UMI-77给药量对脓毒症的影响。
(1)取BALB/c小鼠105只,每只BALB/c小鼠的体重为20±2g,将BALB/c小鼠随机等分为7组,分别为空白组2、LPS组2、UMI-77-6组、UMI-77-7组、UMI-77-8组、UMI-77-9组、UMI-77-10组;
(2)先采用尾静脉注射方式为除去空白组的其余5组BALB/c小鼠注射内毒素LPS,每只BALB/c小鼠注射的内毒素LPS的浓度为18mg/kg、剂量为0.1mL/20g体重;
(3)UMI-77-6组、UMI-77-7组、UMI-77-8组、UMI-77-9组、UMI-77-10组在注射内毒素LPS后分别腹腔注射UMI-77的腹腔注射剂量为0.05mL/20g体重、0.1mL/20g体重、0.15mL/20g体重、0.2mL/20g体重、0.25mL/20g体重,且给药浓度均为7.0mg/kg,且连续腹腔注射给药5天;空白组2和LPS组2给予相应剂量的基质;
(4)空白组2、LPS组2、UMI-77-6组、UMI-77-7组、UMI-77-8组、UMI-77-9组、UMI-77-10组的BALB/c小鼠分笼饲养,给等量、充足的饲料和水,观察并记录各组BALB/c小鼠在5天内的一般情况(精神状态、食欲、活动度和对刺激的反应)、存活数量及具体死亡时间。
根据5天对各组BALB/c小鼠的存活数量记载,可知:第五天给药后,对照组2的BALB/c小鼠全部存活,存活率为100%,说明该组的BALB/c小鼠是正常的;LPS组2的BALB/c小鼠只存活4只,存活率为26.27%;UMI-77-6组的BALB/c小鼠存活8只,存活率为53.33%,UMI-77-7组的BALB/c小鼠存活11只,存活率为73.33%,UMI-77-8组的BALB/c小鼠存活12只,存活率为80.0%,UMI-77-9组的BALB/c小鼠存活10只,存活率为66.67%,UMI-77-10组的BALB/c小鼠存活8只,存活率为53.33%。根据上述存活率可知,患有脓毒症的小鼠在不进行药物干预的情况下,存活率非常低,但是经过UMI-77进行治疗后的小鼠的第五天存活率由26.27%上升到53.33%以上,患有脓毒症的BALB/c小鼠通过UMI-77的给药治疗后,BALB/c小鼠的存活率大幅度提升,说明UMI-77对脓毒症具有一定的疗效,同时,UMI-77-7组、UMI-77-8组、UMI-77-9组中BALB/c小鼠的第五天存活率超过60%,说明0.1mL/20g体重-0.2mL/20g体重的UMI-77给药量具有更好的抗脓毒症效果。
以上仅是本发明的优选实施方式,本发明的保护范围并不仅局限于上述实施例,凡属于本发明思路下的技术方案均属于本发明的保护范围。应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理前提下的若干改进和润饰,应视为本发明的保护范围。
