一种Ag3PO4/Mxene-PEG-FA-TPP纳米粒子及其制备方法和应用
文献发布时间:2024-04-18 19:58:21
技术领域
本发明属于纳米材料抗肿瘤药物技术领域,特别涉及具有靶向肿瘤细胞线粒体,通过光热效应及光动力学效应抗肿瘤纳米粒子、制备方法及在抗肿瘤中的应用。
背景技术
全球范围内癌症是导致人类死亡的重要原因,也是影响人群预期寿命的重要障碍。据统计仅2020年,全球癌症新增病例约1.93千万,死亡病例约1千万。针对癌症的治疗目前主要是手术治疗、放射治疗、化学药物治疗、免疫治疗等,但现有的治疗效果有限,且伴随较强的毒、副反应,迫切需要开发新的药物。
纳米材料是生物医药领域抗肿瘤的一颗新星,由于纳米材料稳定性强、安全性高、比表面积大及易修饰等特点成为肿瘤治疗新的替代方案。纳米材料本身可通过高渗透长滞留(permeability and retention effect,EPR)效应在肿瘤组织处积蓄。在近红外光的照射下,纳米材料可以产生高热通过热消融的方式杀死肿瘤细胞。同时,纳米材料在近红外光的照射下发生电子的跃迁,产生活性氧(reactive oxygen species,ROS)也可抑制肿瘤细胞。因此,纳米材料新型抗肿瘤药物研发具有较好的应用前景。
虽然纳米材料具有很多抗肿瘤治疗优势,但仅通过纳米材料的被动靶向能力治疗肿瘤还不足以取得令人满意的靶向治疗效果,需提高其靶向性。由于部分纳米材料仅具有光热效应或仅具有光动力学效应,对肿瘤细胞的杀伤能力有限。研究表明联合光热和光动力疗法(PTT/PDT)较单一的光热治疗方式具有显著的疗效优势,PTT引起的局部高温增加了肿瘤的血流量和氧合,提高了PDT的疗效;PDT过程中产生的细胞毒性活性氧物种可以增强肿瘤细胞对PTT的敏感性。此外,部分纳米材料的生物相容性差,毒性问题也限制了纳米材料的使用。面对临床对更精准高效纳米药物的需求,研究开发具有精准靶向、高光热及光动力学效应及安全性高的纳米药物是纳米治疗技术的发展趋势。
发明内容
为了解决背景技术中存在的技术问题,本发明的目的是提供一种具有高效低毒靶向宫颈癌细胞的Ag
本发明目的是通过以下方式实现:
本发明提供一种Ag
(1)合成Mxene纳米材料:将Ti
(2)合成Ag
(3)合成Ag
(4)合成Ag
(5)合成Ag
基于上述技术方案,进一步地,步骤(1)中HF水溶液中HF的浓度为10~40%,溶液中Ti
基于上述技术方案,进一步地,步骤(1)中离心的转速为10000~30000rpm。
基于上述技术方案,进一步地,步骤(1)中得到Mxene纳米材料分别用水和乙醇洗涤1~3次,去除残留的四丙基氢氧化铵。
基于上述技术方案,进一步地,步骤(2)中所述的MXene纳米材料的浓度为0.01~1g/mL,AgNO
基于上述技术方案,进一步地,步骤(2)中所述的磷酸二氢钠溶液的浓度为0.01~0.05g/mL,NaH
基于上述技术方案,进一步地,步骤(3)中所述的有机溶剂包括甲醇和乙醇,Ag
基于上述技术方案,进一步地,步骤(4)中所述的有机溶剂包括甲醇和乙醇,叶酸与Ag
基于上述技术方案,进一步地,步骤(4)中三乙胺与叶酸的摩尔比为20:1~40:1。
基于上述技术方案,进一步地,步骤(5)中所述的有机溶剂包括甲醇和乙醇,3-羧丙基三苯基溴化膦与Ag
基于上述技术方案,进一步地,步骤(5)中三乙胺与3-羧丙基三苯基溴化膦的摩尔比为20:1~40:1。
本发明还提供上述制备方法制得的Ag
本发明还提供上述的Ag
基于上述技术方案,进一步地,所述的肿瘤包括宫颈癌。
本发明相对于现有技术具有的有益效果如下:
1.Mxene纳米材料有良好的电化学性质、光热转换性能但几乎不能产生活性氧,本发明将Ag
2.本发明制备的Ag
3.本发明制备的Ag
附图说明
为了更清楚地说明本发明实施例,下面将对实施例涉及的附图进行简单地介绍。
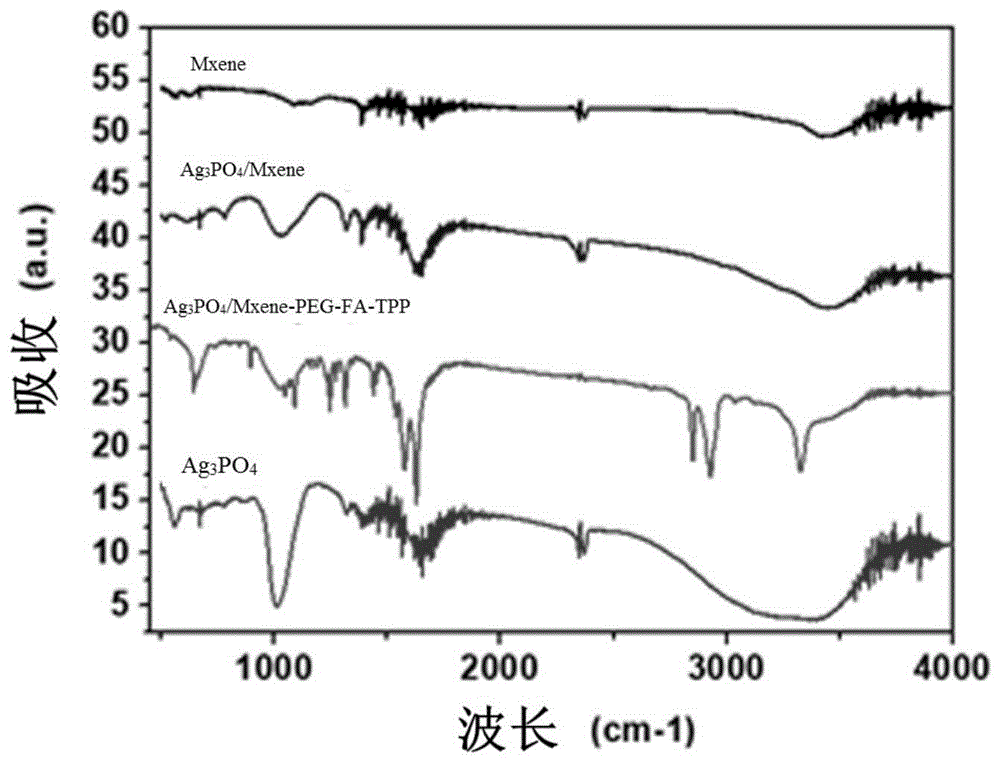
图1为实施例1中纳米粒子Ag
图2为实施例1制备的Ag
图3为实施例2中Ag
图4为实施例2中Ag3PO4/Mxene-PEG-FA-TPP纳米粒子活性氧产生分析图;
图5为实施例3中Ag
图6为实施例3中Ag
图7为实施例4中Ag
图8为实施例4中Ag
图9为实施例4中Ag
图10为实施例5中Ag
具体实施方式
下面结合实施例对本发明进行详细的说明,但本发明的实施方式不限于此,显而易见地,下面描述中的实施例仅是本发明的部分实施例,对于本领域技术人员来讲,在不付出创造性劳动性的前提下,获得其他的类似的实施例均落入本发明的保护范围。
如无特殊说明,本发明所采用的实验方法均为常规方法,所用实验器材、材料、试剂等均可从商业途径获得。
实施例1
Ag
(1)合成Mxene纳米材料
在60mL的HF水溶液(HF的浓度为40%)中加入约10g的Ti
(2)合成Ag
在50mL蒸馏水中加入10g MXene纳米材料并超声15min,超声处理后,添加3.06gAgNO
(3)合成Ag
将1mg Ag
(4)合成Ag
叶酸(FA)含有羧基末端,能有效的连接在PEG的氨基上,我们通过DCC/NHS的活化体系,活化FA分子上的羧基,使其与PEG连接,具体过程如下:
约10mg FA与DCC/NHS在甲醇(2.5mL)中以摩尔比1:1.2:1.2的比例反应,在50℃黑暗中搅拌5h,然后将反应液与上述合成的1mg Ag
(5)合成Ag
3-羧丙基三苯基溴化膦(TPP)含有羧基末端,能有效的连接在FA上富余的氨基上,具体过程如下:
约10mg TPP与DCC/NHS在甲醇(2.5mL)中以摩尔比1:1.2:1.2的比例反应,在50℃黑暗中搅拌5h,然后将反应液与上述合成的1mg Ag
图1a-1c为实施例1制备的纳米粒子Ag
图2为实施例1制备的Ag
实施例2
Ag
(1)光热效应
a.将不同浓度(0,32,63,125,250,500,1000μg/mL)的Ag
b.改变激发功率(0.25,0.5,0.75,1,1.5W/cm
c.将1000μg/mL的Ag
d.取1000μg/mLAg
图3为实施例2中Ag
(2)活性氧检测分析
将Ag
图4为实施例2中Ag
实施例3
Ag
分别将纳米材料Ag
通过小鼠尾静脉注射纳米材料Ag
图5为实施例3中Ag
图6为实施例3中Ag
实施例4
Ag
体外研究采用四甲基偶氮唑盐比色(MTT)法、Calcein-AM/PI活死细胞染色、划痕实验和流式细胞术检测纳米材料近红外光触发的抗肿瘤作用。
MTT实验
(1)在96孔板中每个孔铺8000个SIHA细胞,6h贴壁后,加入Mxene-Ag
(2)在96孔板中每个孔铺8000个SIHA细胞,6h贴壁后,加入(6,12.5,25,50,100,200μg/mL)的Ag
Calcein-AM/PI活死细胞染色
在96孔板中每个孔铺8000个SIHA细胞,6h贴壁后,加入Mxene-Ag
划痕实验
(1)在96孔板中铺8000个宫颈癌SIHA细胞,置于含5% CO
(2)在SIHA细胞中加入100μg/mL的纳米材料,对照组加PBS缓冲液,培养12h;
(3)用PBS清洗3遍,加入新鲜完全培养基,近红外光照射3min,在孔板中进行划痕操作,用PBS清洗1-2遍,重新加入培养基;
(4)倒置显微镜拍照记录0-24h乳腺癌细胞SIHA细胞迁移情况。
流式细胞术
(1)将SIHA细胞以2×10
(2)培养12h后吸出培养基,并用PBS缓冲液清洗三次。
(3)使用不含EDTA的0.25%胰酶消化使SIHA细胞离壁,将SIHA细胞在PBS缓冲液中清洗两次后使用Annexin V-FITC/PI kit进行染色;
(4)加入500μL Annexin V结合缓冲液重悬细胞,并使用Annexin V-FITC和PI各5μL对SIHA细胞进行染色,在避光室温条件染色30min后,使用Calibur流式细胞仪收集检测>10
图7为实施例4中Ag
图8为实施例4中Ag
图9为实施例4中Ag
实施例5
Ag
体内研究通过雌性Balb/c小鼠皮下接种宫颈癌SIHA细胞移植瘤,尾静脉注射复合纳米材料Ag
将宫颈癌SIHA细胞传代后离心,得到细胞沉淀,用5%葡萄糖溶液混匀进行细胞计数,按照每只小鼠5×10
图10为实施例5中Ag
最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。
- 一种Si衬底上InGaN纳米柱@Au纳米粒子复合结构及其制备方法与应用
- 一种金纳米粒子/三维氧化锰/聚吡咯修饰玻碳电极的制备方法及应用
- 一种联烯修饰的金纳米粒子及其制备方法与应用
- 一种具有pH响应性的席夫碱共聚物包覆的介孔二氧化硅载药纳米粒子及其制备方法和应用
- 一种精油和PLGA复合的壳核结构纳米粒子的制备方法及应用
- 一种负载铁基纳米粒子的碳纳米管的制备方法及其负载铁基纳米粒子的碳纳米管和应用
- 一种负载铁基纳米粒子的碳纳米管的制备方法及其负载铁基纳米粒子的碳纳米管和应用
