用于预测生物制剂的药代动力学和脑渗透性的体外基于细胞的测定
文献发布时间:2024-04-18 19:58:26
相关申请的交叉引用
本申请要求2021年4月14日提出申请的美国临时申请第63/174,913号和2021年5月12日提出申请的美国临时申请第63/187,750号的权益,此处将这些申请的内容以全文引用的方式并入本文。
序列表
本申请包含序列表,该序列表已经以ASCII格式以电子方式提交,并以引用方式以其全部内容并入本文。该ASCII副本创建于2022年3月15日,命名为“P36572-WO_SL.txt”,大小为16,584字节。
技术领域
本公开涉及用于测量细胞层对分子的再循环的方法和组合物。特别地,本公开涉及用于评估与FcRn(例如,治疗性抗体、Fc融合分子和与白蛋白连接的分子)相互作用的分子的体内药代动力学特征(例如,清除率和/或半衰期)和组织渗透性的体外受体依赖性再循环测定以及再循环和转胞吞作用测定。
背景技术
治疗性单克隆抗体(mAb)因其在治疗多种疾病方面的有效性和其理想药理学特性而已成为全球主要的医药产品类别。mAb药物的有利药理学特性之一是其循环半衰期通常较长。生物治疗产品的延长半衰期可能允许降低给药频率和/或减少药物剂量,这可能会降低护理成本、提高患者依从性和/或减少浓度依赖性细胞毒性/不良反应。
在理解mAb药物在动物和人类中的药代动力学(PK)特征方面取得了重大进展。尽管许多mAb药物表现出与内源性IgG相似的PK行为,但仍普遍观察到mAb药物在人类中的非特异性清除率存在显著异质性。因此,针对理想PK特性评估和选择临床候选药物是药物开发过程中的重要早期步骤。已采用涉及计算机、体外和体内分析的广泛技术来评估和/或预测mAb在人类中的PK行为(Dostalek等人,2017,MAbs 9(5):756-766)。然而,PK数据从动物到人类以及从体外测定到体内读数的转换对于药物开发人员来说仍然难以捉摸(Vugmeyster等人,2012,World J Biol Chem3(4):73-92)。此外,虽然一些动物模型如人类FcRn转基因小鼠(Avery等人,2016,MAbs,8(6),1064-1078)和非人灵长类动物(Deng等人,2011,Drug Metab Dispos 38(4):600-605)已成功用于预估mAb的人类PK,这些研究通常耗时、成本高且涉及动物牺牲。
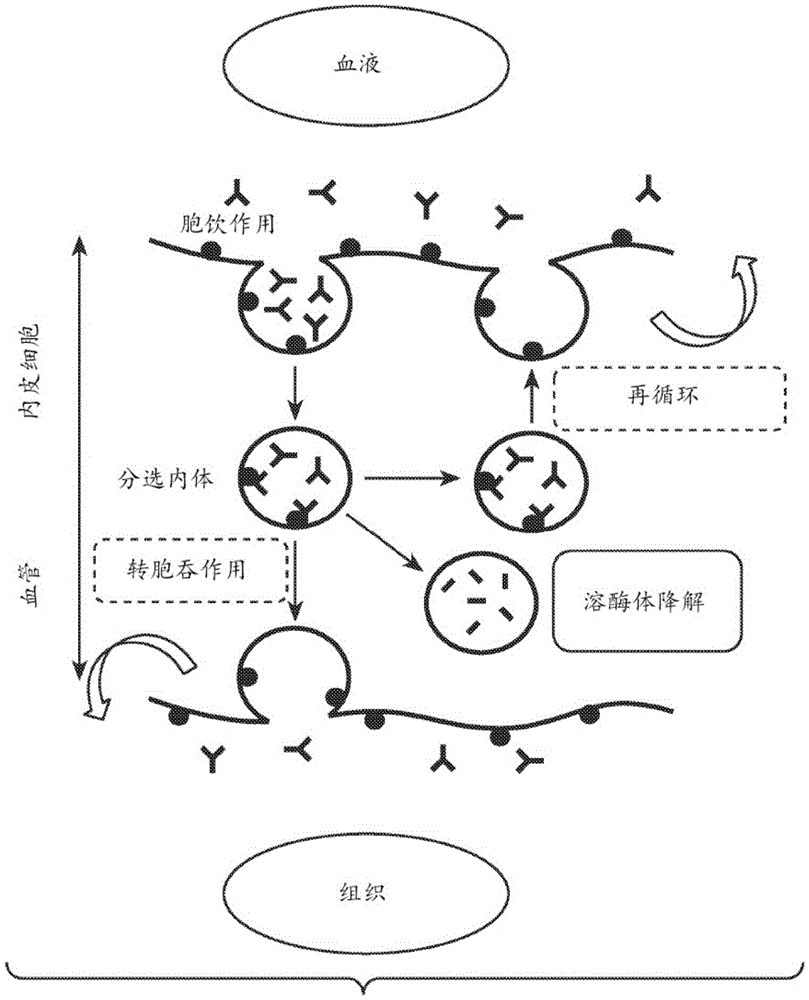
从动物研究和体外测定中预测mAb的人类PK存在许多复杂性。已知靶标介导的药物处置(TMDD)会影响mAb的剂量依赖性PK行为,从而导致非线性分布和消除。在没有TMDD的情形下,mAb预计会表现出线性消除和非特异性清除率,这反映了靶标无关分子特异性药物分解代谢。mAb的非特异性清除主要由网状内皮系统中的溶酶体降解介导,其中新生儿Fc受体(FcRn)介导的补救途径起主要作用。结构上,FcRn是异源二聚体,其由与主要组织相容性复合体(MHC)I类样分子同源的跨膜重链(FCGRT)和可溶性轻链β2微球蛋白(B2M)组成。FcRn在酸性pH(小于6.5)下与内源性IgG的Fc结构域结合,但在中性或碱性pH(大于7.0)下仅最低限度地结合。该独特特性使FcRn能够保护含有Fc的分子免于降解,方法是在它们被吸收到细胞中后在酸性内体中与它们结合,然后将它们运输回细胞表面并在生理pH下将它们释放到循环中。相反,不与FcRn结合的内化分子被引导至溶酶体进行降解(参见图1和Roopenian等人,Nat Rev Immunol.2007年9月;7(9):715-25)。
虽然FcRn在延长含Fc蛋白的半衰期方面的作用已得到广泛认可(Roopenian等人,2003,J Immunol,170(7),3528-3533),但有报道称FcRn结合与人体内的mAb药物的PK之间缺乏相关性(Suzuki,2010;Zheng,2011;Hotzel,2012),报道表明与FcRn的结合亲和力不是含Fc的蛋白的消除率的唯一决定因素。鉴于FcRn在细胞内运输方面的功能,含有Fc的分子/FcRn复合体的内体分选和运输动力学可能会影响FcRn介导的补救机制的整体效率,从而影响分子的非特异性清除率。此外,通过胞饮作用或内吞作用的细胞吸收过程以及溶酶体中的降解过程也可以在确定mAb降解的速率和程度方面发挥作用(Junghans&Anderson,1996,PNAS 93(11),5512-5516)。最后,据报道,电荷/pI、疏水性、非特异性结合和其他因素等生化特性会影响mAb处置(Datta-Mannan等人,2015,MAbs 7(3),483-493;Igawa等人,2010Protein Eng Des Sel 23(5),385-392;Sharma等人,2014PNAS 111(52);Hotzel等人,2012MAbs 4(6),753-760)。这些分子特征本身可能会影响mAb结构,从而在体内改变与FcRn的“真实”相互作用,或者可能有助于改变内化模式/速率和FcRn介导的细胞内运输途径(包括再循环和转胞吞作用)的相对比例的非特异性细胞表面结合。
在啮齿动物和非人类灵长类动物中进行的体内动物研究通常用于预测人类中治疗性抗体的PK(Avery等人,MAbs,2016,8(6),1064-1078;Deng等人,MAbs 2011,3(1),61-66)。这些方法涉及牺牲动物,成本效益较低,并且不能以高处理量方式进行。根据经验比例法,在某些情况下,动物研究中的PK无法准确预测人类中的PK并显示了跨物种的PK差异,其可能是由于FcRn结合、靶标介导的药物处置和触发差异免疫应答中的物种差异(Wang等人,2016,Biopharm Drug Dispos,37(2),51-65)。体外测定方面的努力已被用于评估PK,所通过的方法的时间和成本消耗更少,并且节省了动物。这些方法中的大多数都考虑了可能影响PK的分子特性中的一种或子集,诸如非特异性结合(Hotzel等人,MAbs 2012,4(6),753-760)、FcRn相互作用(Schlottauer等人,MAbs 2013,5(4),576-586;Souders等人,MAbs2015,7(5),912-921)、以及与肝素或细胞外基质的结合(de Ridder等人,Cerebrovasc Dis2013,35(1),60-63;Kraft等人,MAbs2020,12(1))。这些方法通常依赖临界阈值,有时在直接PK预测中成效有限,并且必须与另一种方法结合来提高预测准确度。
在脑渗透性的背景下,缺乏针对抗体的真实世界行为的体外模型是一个特别挑战。中枢神经系统(CNS)疾病是一种严重的健康负担,几十年来一直在大力推动开发针对CNS疾病的有限治疗方法。血脑屏障是高度特化的组织,由具有紧密连接的内皮细胞(以及其他细胞)组成,其调节分子进入大脑的穿行,包括阻止绝大多数当前治疗物从血流进入CNS。虽然存在不同的方法用以改进分子的脑渗透性,但在没有稳健模型来评估其有效性的情形下,将这些方法应用于临床前药物开发非常具有挑战性。由于现有模型与体内效果之间的相关性较差,潜在疗法的脑渗透性通常必须进行经验测试,这既耗时又费用昂贵。
已经开发和评估了一种经过修饰以表达人类FcRn的人类微血管内皮细胞(HMEC1)系,发现再循环/残留mAb比率与其在人类FcRn转基因小鼠中的血清半衰期相关(Grevys等人,Nat Commun 2018,9(1),621)。然而,数据集仅限于具有大大增强的FcRn结合亲和力的工程化IgG,但不包括更常用于治疗性抗体的正常IgG框架。此外,细胞在常规细胞培养板中培养,这可能对于细胞极化不理想,并可能导致转胞吞成分进入再循环样品造成污染。
因此,仍然需要预测治疗性分子的体内PK特性(例如清除率、半衰期或其他)和脑渗透性的方法,这些方法可以在短时间内以合理的成本进行,以帮助评估和选择治疗性分子。
发明内容
本公开涉及用于测量目标分子进出细胞膜的运动或运输(包括目标分子的再循环和目标分子的再循环和转胞吞作用)的方法、测定、测定系统、试剂盒和组合物。特别地,本公开提供评估与分子运输受体(例如,FcRn)相互作用的分子(包括治疗性抗体、Fc融合分子和与白蛋白连接的分子等分子)的药代动力学特征(包括例如体内清除率(CL)、分布体积(Vd)、曲线下面积(AUC)、生物利用度、最大/最小血浆浓度(Cmax/Cmin))的体外受体依赖性转胞吞作用和再循环测定。与其他方法相比,本文提供的方法和测定可以更好地涵盖可能影响测试分子(包括抗体)的体内PK行为的多种因素,诸如非特异性结合和与细胞表面的相互作用、pH依赖性结合(例如,FcRn结合)和细胞内运输途径。与其他方法相比,本文提供的方法和测定可以更好地预测和/或模拟目标分子(包括抗体)的体内组织渗透率(诸如脑渗透率)。与其他方法和/或测定相比,所提供的方法和测定可进一步提供改善的细胞顶-底侧极化,和/或对再循环成分与转胞吞作用成分的更清楚评估。
在某些实施例中,本公开涉及确定多个分子的再循环的方法。例如,确定可以包括:将多个分子引入第一腔室,其中:第一腔室与第二腔室通过细胞层分隔,并且第一腔室和第二腔室包含水溶液;在第一腔室中孵育多个分子;更换第一腔室和第二腔室中的水溶液;以及测量从细胞层释放到第一腔室中的多个分子的量;其中水溶液处于生理pH,并且细胞层包含表达介导分子输运的受体的细胞。
在某些实施例中,该方法进一步包括测量多个分子跨细胞层的转胞吞作用。在某些实施例中,测量转胞吞作用包括:在更换水溶液后,测量第二腔室中多个分子的量。
在某些实施例中,该方法包括在第一腔室中在试剂的存在下孵育多个分子,并确定试剂是否影响多个分子的再循环。
在某些实施例中,本公开涉及一种确定多个分子的组织渗透率的方法,包括:a)将多个分子引入第一腔室,其中第一腔室与第二腔室通过细胞层分隔,并且第一腔室和第二腔室包含水溶液;其中水溶液处于生理pH,并且细胞层包含表达介导分子输运的受体的细胞;b)测量从第一腔室再循环到细胞层并返回到第一腔室的多个分子的量;c)测量从第一腔室转胞吞到第二腔室的多个分子的量;以及d)基于转胞吞分子与再循环分子的比率确定多个分子的组织渗透率。在一些实施例中,组织渗透率为脑渗透率。
在某些实施例中,测量经再循环的多个分子包括:在将多个分子引入第一腔室之后,在第一腔室中孵育多个分子;更换第一腔室和第二腔室中的水溶液;以及测量从细胞层释放到第一腔室中的多个分子的量。
在某些实施例中,测量经转胞吞的多个分子包括:在将多个分子引入第一腔室之后,在第一腔室中孵育多个分子;更换第一腔室和第二腔室中的水溶液;以及测量从细胞层释放到第二腔室中的多个分子的量。
在某些实施例中,测量经再循环的多个分子的量和测量经转胞吞的多个分子的量独立地包括使用酶联免疫吸附测定(ELISA)、液体闪烁计数(LSC),定量PCR、荧光读取器系统、质谱法或其任意组合。在某些实施例中,组织渗透率为脑渗透率。
在某些实施例中,该方法包括在第一腔室中在试剂的存在下孵育多个分子,并确定试剂是否影响多个分子的组织渗透率。
在某些实施例中,本公开涉及一种确定多个分子的药代动力学(PK)参数的方法,包括:a)将多个分子引入第一腔室,其中第一腔室与第二腔室通过细胞层分隔,并且第一腔室和第二腔室包含水溶液;其中水溶液处于生理pH,并且细胞层包含表达介导分子输运的受体的细胞;b)测量从第一腔室再循环到细胞层并返回到第一腔室的多个分子的量;c)基于经再循环的多个分子的量来确定PK参数。
在某些实施例中,测量经再循环的多个分子包括:在将多个分子引入第一腔室之后,在第一腔室中孵育多个分子;更换第一腔室和第二腔室中的水溶液;以及测量从细胞层释放到第一腔室中的多个分子的量。
在某些实施例中,细胞表达异源FcRn。在某些实施例中,测量经再循环的多个分子的量包括使用酶联免疫吸附测定(ELISA)、液体闪烁计数(LSC)、定量PCR、荧光读取器系统或质谱法。
在某些实施例中,PK参数是多个分子的体内清除率、分布体积、曲线下面积(AUC)、生物利用度或体内半衰期的量度。
在某些实施例中,该方法包括在第一腔室中在试剂的存在下孵育多个分子,并确定试剂是否影响多个分子的PK参数。
在某些实施例中,多个分子为多个单一分子。在某些实施例中,多个分子为多个不同分子。在某些实施例中,细胞层包括细胞单层。在某些实施例中,介导分子输运的受体为介导分子的胞内输运的受体。在某些实施例中,介导分子输运的受体为转铁蛋白受体、Fc受体、巨蛋白或立方蛋白。在某些实施例中,介导分子输运的受体为新生儿Fc受体(FcRn)。
在某些实施例中,细胞为真核细胞、哺乳动物细胞或肾细胞。在某些实施例中,细胞为马丁达比犬肾(MDCK)细胞。
在某些实施例中,测量从细胞层释放的多个分子的量包括使用酶联免疫吸附测定(ELISA)、液体闪烁计数(LSC)、定量PCR、荧光读取器系统或质谱法。
在某些实施例中,将多个分子在第一腔室中孵育约1小时至约48小时。在某些实施例中,将多个分子在第一腔室中孵育约1小时至约30小时。在某些实施例中,更换水溶液包括清洗第一腔室。在某些实施例中,该方法进一步包括在测量之前用更换水溶液孵育第一腔室和第二腔室。在某些实施例中,在测量之前,用更换水溶液孵育第一腔室和第二腔室1小时至6小时。在某些实施例中,孵育在约35℃至约39℃之间的温度下进行。
在某些实施例中,多个分子为含有Fc的分子。在某些实施例中,含有Fc的分子为受体Fc融合分子。在某些实施例中,多个分子为抗体。在某些实施例中,抗体为单克隆抗体。在某些实施例中,FcRn选自由人类RcRn、小鼠FcRn、大鼠FcRn和食蟹猕猴FcRn组成的组。
在某些实施例中,生理pH为约7.4。
在某些实施例中,本公开涉及一种测定系统,包括:a)第一腔室和第二腔室,其中每个腔室包括处于生理pH的水溶液;b)细胞层,该细胞层将第一腔室和第二腔室分隔,其中细胞层可以介导分子从第一细胞层再循环到细胞层中并返回到第一腔室中;c)检测器,该检测器用于检测第一腔室中分子的存在;其中测定系统配置成确定检测器分子的再循环,其中该确定包括:将多个分子引入该第一腔室;在第一腔室中孵育多个分子;更换第一腔室和第二腔室中的水溶液;以及测量从细胞层释放到第一腔室中的多个分子的量。
在某些实施例中,测定系统进一步包括:检测器,该检测器用于检测第二腔室中分子的存在;细胞层可以介导分子从第一腔室到第二腔室的转胞吞作用;并且其中测定系统配置成确定多个分子跨细胞层的转胞吞作用,其中确定转胞吞作用包括:在已经替换水溶液之后,测量该第二腔室中多个分子的量。
在某些实施例中,本公开涉及一种试剂盒,该试剂盒包括本公开的测定系统和/或方法。
附图说明
图1描绘了FcRn的作用机制的示意图,该作用机制涉及pH依赖性捕获和释放,以及包括再循环、转胞吞作用和溶酶体降解的细胞内运输途径。
图2描绘了本公开的再循环测定的特定实施例的示意图。
图3A描绘了用于定量如实例中所述的再循环的灵敏人类IgG特异性酶联免疫吸附测定(ELISA)的示意图。
图3B提供了图3A中描述的ELISA测定的标准曲线,展示了检测的下限。
图4示出了具有差异Fc-FcRn结合亲和力的各种人源化IgG1抗体的再循环和转胞吞输出量受人类FcRn影响。
图5A至图5B提供了时间依赖性再循环测量的比较,展示了四种治疗性抗体中相似的再循环动力学。图5A提供了非归一化数据,而图5B提供了归一化数据。
图6示出了野生型(WT)BACE-1抗体分子和几个序列变体的转胞吞作用/再循环(T/R)比率。
图7示出了针对五种抗BACE1 mAb变体的食蟹猕猴中转胞吞作用/再循环(T/R)比率与脑血清比率之间的关系。
图8A至图8D提供了与计算出的pI(图8A)、Fv电荷(图8B)、HI总和(图8C)以及根据本文描述的方法和测定进行的(一组治疗性抗体的)归一化再循环测定的输出量相比,人体中的清除率。在图8A至图8C中,清除率与所比较的参数之间的相关性很低或没有相关性。图8D展示了清除率与归一化再循环输出量的相关性。
具体实施方式
在实践当前所公开的主题时,使用了分子生物学、微生物学、细胞生物学、生物化学和免疫学中的许多常规技术。这些技术在以下出版物中进行了更详细的描述:例如,Molecular Cloning:Laboratory Manual第3版,J.F.Sambrook和D.W.Russell编辑,ColdSpring Harbor Laboratory Press2001;Recombinant Antibodies for Immunotherapy,Melvyn Little编辑,Cambridge University Press 2009;“Oligonucleotide Synthesis”(M.J.Gait编辑,1984);“Animal Cell Culture”(R.I.Freshney编辑,1987);“Methods inEnzymology”(Academic Press,Inc.);“Current Protocols in Molecular Biology”(F.M.Ausubel等人编辑,1987,以及定期更新);“PCR:The Polymerase Chain Reaction”,Mullis等人编辑,1994);“APractical Guide to Molecular Cloning(Perbal BernardV.,1988)《噬菌体展示:实验室手册》(“Phage Display:A Laboratory Manual”,Barbas等人,2001年)。这些参考文献和包含标准协议的其他参考文献的内容,包括制造商的说明书,被本领域技术人员所熟知和依赖,据此以引用方式并入本文作为本公开的一部分。
1.定义
除非另有定义,否则本文中使用的所有技术术语、符号和其他科学术语旨在具有本公开所属领域的技术人员通常理解的含义。在某些情况下,为了清楚和/或易于参考,本文定义了具有通常理解的含义的术语,并且在本文中包括此类定义不应解释为表示与本领域通常理解的定义具有实质性区别。
如本文所用,术语“包含”、“包括”、“具有(having、has)”、“可”、“含有”及其变体旨在作为不排除其他行为或结构的可能性的开放式过度短语、术语或字。除非上下文另外明确指示,否则单数形式“一(a、an)”和“该(the)”包括多个提及物。本公开还涵盖“包含”本文所呈现的实施例或组件、“由其组成”和“基本上由其组成”的本文所呈现的实施例或组件,无论是否明确陈述。
如本文中所使用,术语“约”或“大约”是指特定值处于如由本领域技术人员所确定的特定值的可接受误差范围内,其部分地取决于如何测量或判定该值,即取决于测量系统的局限性。例如,根据业内的实践,在某些实施例中,“约”可意指3倍或3倍以上的标准偏差。可替代地,在某些实施例中,“约”可以意指至多20%、至多10%、至多5%或至多1%的给定值的范围。可替代地,特别是关于生物系统或过程,该术语意指数值的一个数量级内,例如在数值的5倍以内,或在数值的2倍以内。
如本文所用,术语“培养基”和“细胞培养基”是指用于生长或维持细胞的营养源。如本领域技术人员所理解,营养源可以含有细胞生长和/或存活所需的成分,或者可以含有有助于细胞生长和/或存活的成分。维生素、必需或非必需氨基酸(例如,半胱氨酸和胱氨酸)和微量元素(例如,铜)为培养基成分的实例。本文提供的任何培养基也可以补充有胰岛素、植物水解产物和动物水解产物中的任何一种或多种。
如本文所用,短语“药代动力学(PK)参数”是指本领域已知的多种PK参数中的任何一种,包括但不限于多个分子的体内清除率(CL)、分布体积(Vd)、曲线下面积(AUC)、生物利用度、最大/最小血浆浓度(Cmax/Cmin)或体内半衰期(t
如本文所用,术语“清除率”是指分子或多肽从动物血流中清除的速率。动物可以为例如哺乳动物,诸如啮齿动物(小鼠、大鼠、仓鼠、豚鼠或其他啮齿动物)、非人灵长类动物(诸如食蟹猕猴)、狗或人类。
如本文所用,术语“生理pH”是指约6.5至约8.0的pH。在某些实施例中,生理pH值是介于约6.5与约8.0之间的任何值,例如,约6.6、约6.7、约6.8、约6.9、约7.0、约7.1、约7.2、约7.3、约7.4、约7.5、约7.6、约7.7、约7.8、或约7.9,或者是约6.5至约8.0的范围内的任何范围。
“培养”细胞是指使细胞与细胞培养基在适于存活和/或生长和/或增殖细胞的条件下接触。
如本文所用,“分子”通常是指作为测定对象的分子。例如,但不作为限制,分子可以为任何与FcRn天然结合的分子(例如,多肽、抗体、含有Fc的分子等)或已被工程化以结合FcRn,诸如但不限于含白蛋白的分子、经工程化以经由肽标签或其他氨基酸序列结合FcRn的分子、抗体、抗体片段、或如下定义的多克隆或单克隆抗体。此类多肽、蛋白质、抗体、抗体片段或多克隆或单克隆抗体可以包括非天然存在的方面,包括但不限于非天然存在的氨基酸、非氨基酸接头或间隔物,并且可以包括与其他组合物的缀合物,例如小分子或大分子治疗剂。
如本文所用,“多肽”通常是指具有多于约十个氨基酸的肽和蛋白质。多肽可以与宿主细胞同源,或者是与被利用的宿主细胞异源,即,外来的,诸如由中国仓鼠卵巢细胞所产生或由哺乳动物细胞所产生的酵母多肽的人蛋白。在某些实施例中,使用哺乳动物多肽(最初来自哺乳动物生物体的多肽),并且在某些实施例中,本公开的多肽直接分泌到培养基中。
术语“蛋白质”是指链长度足以产生三级和/或四级结构的更高程度的氨基酸序列。这是用于区别“肽”或其他没有此类结构的小分子量药物。典型地,本文的蛋白质可具有至少约15-20kD,以及在某些实施例中,至少约20kD的分子量。涵盖于本文定义内的蛋白质的实例包括所有哺乳动物蛋白(尤其治疗蛋白和诊断蛋白,例如治疗抗体和诊断抗体)以及通常含有一个或多个二硫键的蛋白质(包括含有一个或多个链间和/或链内二硫键的多链多肽)。
本文中所用的术语“抗体”为在最宽广意义上使用且涵盖各种类型的抗体和抗体结构,包括但不限于多克隆抗体或单克隆抗体、人类、人源化或嵌合抗体、多特异性抗体(例如双特异性抗体)和抗体片段,其展示出期望的抗原结合活性。
本文所用的“抗体片段”、抗体的“抗原结合部分”(或简称为“抗体部分”)或抗体的“抗原结合片段”是指除完整抗体外的分子,其包含完整抗体中结合完整抗体的结合抗原和/或表位的部分。抗体片段的实例包括(但不限于)Fv、Fab、Fab’、Fab’-SH、F(ab’)2、二价抗体、线性抗体、单链抗体分子(例如scFv)和从多特异性(例如双特异性)抗体形成的抗体片段。
如本文所用的术语“单克隆抗体”或“mAb”是指获自实质上同源抗体群体的抗体,即包含群体的个别抗体是相同的和/或结合相同的表位,除了例如含有天然生成的突变或在单克隆抗体制剂生产过程中产生的可能的变体抗体之外,此类变体通常是以少量存在。与通常包括针对不同决定位(表位)的不同抗体的多克隆抗体制剂相反,单克隆抗体制剂的每个单克隆抗体是针对于抗原上的单一决定位。因此,修饰词“单克隆”表示抗体的特征是获自实质上同质的抗体群体,并且不应解释为需要通过任何特定方法产生抗体。例如,待根据本文所公开的主题使用的单克隆抗体可通过多种技术来制造,其包括但不限于杂交瘤方法、重组DNA方法、噬菌体展示方法、和利用包含全部或部分人免疫球蛋白基因座的转基因动物的方法,本文描述此类方法以及用于制备单克隆抗体的其他示例性方法。
术语“杂交瘤”是指通过融合免疫来源的永生细胞系和抗体产生细胞所产生的杂合细胞系。该术语涵盖异源杂合骨髓瘤融合体的子代,该融合体是融合人类细胞和鼠类骨髓瘤细胞系且随后与浆细胞(通常称为三源杂交瘤细胞系)融合的结果。另外,该术语旨在包括产生抗体的任何永生化杂合细胞系,例如四源杂交瘤。例如参见Milstein等人,Nature,537:3053(1983)。
如本文所用,术语“细胞”指动物细胞、哺乳动物细胞、经培养细胞、宿主细胞、重组细胞和重组宿主细胞。此类细胞一般是从哺乳动物组织获得或衍生的细胞系,当置于含有适当营养物和/或生长因子的培养基中时,其能够生长和存活。
如本文所用,术语“异源基因”是指编码对所利用的宿主细胞外源的蛋白的基因,诸如编码由中国仓鼠卵巢细胞产生的人蛋白的基因,或编码哺乳动物细胞中产生的酵母多肽的基因。
如本文所用,“多个分子”包括多个单一分子和多个不同分子。多个单一分子例如可以为相同抗体的两个或更多个物理分子、相同抗体片段的两个或更多个物理分子、相同多肽的两个或更多个物理分子、或相同含有Fc的分子的两个或更多个物理分子或另一种目标分子的两个或更多个物理分子。多个不同分子可包括一种分子类型(例如,至少两种不同抗体的物理分子、至少两种不同抗体片段的物理分子、至少两种不同多肽的物理分子、或至少两种含有Fc的分子的物理分子)的混合物,但也可以包括分子类型之间的混合物(例如,一种或多种抗体和一种或多种多肽的物理分子;或一种或多种抗体片段、一种或多种多肽和一种或多种含有Fc的分子等)。
如本文所用,“测试分子”和“目标分子”是指本文所述的测定、方法、试剂盒和系统中评估的多个分子的同一性。如针对多个分子所描述,此类术语既涵盖单一类型的分子(例如,一种抗体、抗体片段、多肽或含有Fc的分子),又涵盖两种或更多种类型的分子(例如,两种或更多种抗体、抗体片段、多肽或含有Fc的分子,或该类别的组合)。
如本文所用,“小分子”是指除蛋白质或多肽之外的分子,其分子量为约2000道尔顿(dalton)或更小,或较佳地约500道尔顿或更小。
2.概述
本公开涉及用于测量目标分子进出细胞膜的运动或运输(诸如目标分子的再循环(如图1所描绘))的方法、测定、测定系统、试剂盒和组合物。本公开进一步涉及用于测量目标分子的转胞吞作用和再循环(如图1所描绘)的方法测定、测定系统、试剂盒和组合物。特别地,本公开涉及用于评估治疗性抗体分子的PK参数(诸如清除率和/或半衰期)的体外受体依赖性再循环和转胞吞测定。如本文中所详细公开,通过本公开的方法测量的目标分子(例如,抗体、抗体片段、多肽或含有Fc的分子)的再循环(任选地与转胞吞进一步组合)可能与细胞的PK特性,诸如该分子的体内清除率高度关联。因此,所要求保护的用于测量目标分子的再循环以及在某些情况下转胞吞作用和再循环的组合的方法可用于评估该分子的体内清除率和其他PK参数,诸如多个分子的半衰期、体积分布(Vd)、曲线下面积(AUC)、生物利用度和最大/最小血浆浓度(Cmax/Cmin)。更进一步地,通过本公开的方法测量的目标分子(例如抗体或其抗体片段)的再循环(任选地与转胞吞作用进一步结合)可以与该目标分子的体内组织渗透率高度相关。因此,在一些实施例中,所要求保护的用于测量目标分子的再循环以及在某些情况下转胞吞作用和再循环的组合的方法可用于评估该目标分子的体内组织渗透率。组织渗透率可以包括例如脑渗透率。
在某些实施例中,方法包括:通过测量一个或多个分子从第一腔室中的溶液中的吸收以及在原始溶液已被第二溶液替换后这些分子到第一腔室的返回,测量多个相同目标分子从第一腔室到相同腔室的跨细胞再循环,其中第一腔室和第二腔室中的每一者都具有生理pH值(例如,pH=约7.4)。在一些实施例中,还评估了多个相同目标分子从第一腔室到第二腔室的跨细胞输运。在其他实施例中,方法包括:测量多个不同目标分子(例如,两种、三种、四种、五种或更多种类型的目标分子)的跨细胞再循环,其任选地可包括评估多个不同目标分子从第一腔室到第二腔室的跨细胞输运。使用分隔第一腔室和第二腔室的细胞层进行该测定的使用。在某些实施例中,细胞层稳定地表达一种或多种介导分子输运的受体。此类受体可以为任何目标受体,包括但不限于转铁蛋白受体、Fc受体、巨蛋白或立方蛋白。
因此,例如,在一个方面,本文提供了一种基于细胞的测定,该测定采用稳定表达人类FcRn和β2-微球蛋白基因的MDCK细胞来测量多肽、抗体或其他FcRn结合分子的再循环效率,以及进一步任选的转胞吞作用,测量是在与FcRn介导的IgG补救途径相关的条件下进行。该转胞吞作用和再循环测定是在生理pH条件下进行的,并且旨在评估IgG与细胞的非特异性结合、其经由胞饮作用的吸收、其与FcRn的pH依赖性相互作用以及细胞内运输和分类过程的动力学中的两者或更多者的组合效应的结果。在该特定实施例中,FcRn的表达是促进测定中测试分子的转胞吞作用和再循环所必需的,并且直接有助于所观察到的相关性。进一步地,诸如本文所提供的测定能够正确排列临床前物种中含有Fc的分子的电荷或糖基化变体的清除率。实例中所提供的结果支持本文所公开的测定作为用于评估多肽、抗体或其他FcRn结合分子(包括在先导选择和优化以及针对期望药代动力学特性的工艺开发过程中的候选抗体药物)的节省成本、节省动物的筛选工具。
本公开还涉及用于通过确定多个分子的转胞吞作用/再循环(T/R)比率来确定多个分子的组织渗透率的方法和组合物。在某些实施例中,方法包括基于转胞吞分子与再循环分子的比率确定多个分子的脑渗透率。所要求保护的用于测量转胞吞作用和再循环以及确定目标分子的T/R比率的方法可用于评估分子的脑渗透率以及其他PK参数,诸如半衰期。诸如本文所提供的体外测定显示了与临床前物种中含有Fc的分子的脑渗透率的相关性。因此,实例中所提供的结果支持本文所公开的测定作为用于在导联选择和优化以及针对期望组织渗透率特性的工艺开发过程中,评估多肽、抗体或其他FcRn结合分子(包括候选抗体药物)的节省成本、节省动物的筛选工具。
本公开涉及本文所提供的方法、测定、测定系统、试剂盒和组合物,其可用于评估多个相同目标分子(例如,相同类型的抗体、抗体片段、多肽或含有Fc的分子)或多个两种或更多种目标分子(例如,选自抗体、抗体片段、多肽、含有Fc的分子或其任何混合物的两种或更多种目标分子)的运动或输运(例如,再循环或再循环和转胞吞作用)、一个或多个PK参数和/或组织渗透率(例如,脑渗透率)。
3.再循环以及再循环和转胞吞作用测定
再循环是指大分子从细胞一侧到同一侧的囊泡输运。再循环是一种跨细胞输运机制,其中细胞将细胞外物质包裹在细胞膜内陷中形成囊泡,然后在细胞内移动囊泡以通过相反的过程将该物质透过同一细胞膜排出。参见图1。
转胞吞作用是指大分子从细胞一侧到另一侧的囊泡输运,其为多细胞生物体在不改变两种环境的独特组成的情形下选择性地在这两种环境之间移动物质所使用的策略。转胞吞作用是一种跨细胞输运机制,其中细胞将细胞外物质包裹在细胞膜内陷中形成囊泡,然后跨细胞移动囊泡以通过相反的过程将物质透过相对的细胞膜排出。参见图1。
在典型FcRn介导的转胞吞作用测定中,表达FcRn的MDCK细胞在转运孔板中的滤膜上生长至汇合,并且在测定之前,通过用酸性测定缓冲剂(pH<6.0)填充内腔室以及用碱性测定缓冲剂(pH>7.4)填充外腔室来产生pH梯度。该测定设计利用FcRn的pH依赖性结合特性,以通过在酸性pH下与细胞表面上的FcRn结合和在碱性pH下释放测试分子(这两者都提高了测定的稳健性和灵敏度),促进细胞对测试分子的吸收。然而,可以改进使用该测定对测试分子的PK行为进行的预测评估。所转染的细胞通常在细胞表面上表达高水平的FcRn,并且测试抗体在酸性环境中与细胞一起孵育,因此认为在酸性pH下对FcRn表现出高结合亲和力的测试分子(诸如抗体)容易结合FcRn并经由FcRn介导的内吞作用进入细胞。这与通常在体内发生的情形形成对比,其中多肽或抗体在生理pH值下与细胞表面FcRn结合最少,并且细胞吸收主要通过非特异性液相胞饮作用来介导。因此,不受理论的束缚,认为pH梯度转胞吞作用测定的输出会受到多肽或抗体在酸性pH下的FcRn结合亲和力的严重影响,因此可能并不总是充分反映其他影响PK的因素(诸如静电相互作用和细胞内运输参数)的贡献。此外,人为pH条件可能本质上对细胞有害,限制了测定的持续时间并可能产生额外的人为测定结果。
因此,如实例中所更详细描述,本文提供了一种用于评估分子在细胞环境中的输运的改进方法,该方法可进一步用于更准确地确定或测量一个或多个PK参数(例如,体内清除率(CL)、分布体积(Vd)、曲线下面积(AUC)、生物利用度、最大/最小血浆浓度(Cmax/Cmin)或体内半衰期(t
在本文所提供的方法、测定和系统的某些实施例中,生理pH值为约6.5至约8.0。在某些实施例中,生理pH值是介于约6.5与约8.0之间的任何值,例如,约6.6、约6.7、约6.8、约6.9、约7.0、约7.1、约7.2、约7.3、约7.4、约7.5、约7.6、约7.7、约7.8、或约7.9,或者是约6.5至约8.0的范围内的任何范围。在某些实施例中,只要两个腔室都具有生理pH,每个腔室的pH就可以不同。例如但不作为限制,第一腔室可以具有6.5的pH,而第二腔室可以具有8.0的pH,或反之亦然。在某些实施例中,生理pH可以为约7.4。
在某些实施例中,本公开涉及一种确定多个分子(包括例如抗体、抗体片段、多肽或含有Fc的分子)的药代动力学(PK)参数的方法,包括:a)将多个分子引入第一腔室,其中第一腔室与第二腔室通过细胞层分隔,并且第一腔室和第二腔室包含水溶液;其中水溶液处于生理pH,并且细胞层包含表达介导分子输运的受体的细胞;b)测量从第一腔室再循环到细胞层并返回到第一腔室的多个分子的量;c)基于经再循环的多个分子的量来确定PK参数。在某些实施例中,测量经再循环的多个分子(包括例如抗体、抗体片段、多肽或含有Fc的分子)包括:在将多个分子引入第一腔室之后,在第一腔室中孵育多个分子;更换第一腔室和第二腔室中的水溶液;以及测量从细胞层释放到第一腔室中的多个分子的量。在某些实施例中,多个分子(包括例如抗体、抗体片段、多肽或含有Fc的分子)在第一腔室中孵育约1小时至约48小时、约1小时至约30小时、约1小时至约24小时、约1小时至约12小时、约1小时至约6小时、或约1小时至约4小时,或它们中的任何值,诸如约1小时、约2小时、约4小时、约6小时、约8小时、约12小时或约18小时。在某些实施例中,更换水溶液包括清洗第一腔室。在某些实施例中,该方法进一步包括在测量之前用更换水溶液孵育第一腔室和第二腔室。在某些实施例中,第一腔室和第二腔室在测量之前用更换水溶液孵育约10分钟至约12小时、约20分钟至约12小时、约30分钟至约6小时、约20分钟至约5小时或约1小时至约4小时,或它们中的任何值,诸如30分钟、1小时、2小时、3小时或4小时。在某些实施例中,孵育在约35℃至约39℃之间的温度(诸如约37℃)下进行。在一些实施例中,使用具有至少200pg/mL、至少100pg/mL、至少50pg/mL或个位数pg/mL的较低水平定量下限(LLOQ)的定量方法。此类方法可包括例如使用高亲和力捕获试剂的ELISA,该试剂可以为例如生物素化小鼠抗人IgG-Fc,诸如生物素-R10Z。在某些实施例中,多个分子为多个相同分子(例如,相同类型的抗体、抗体片段、多肽或含有Fc的分子),而在其他实施例中,多个分子为多个分子(例如,一个或多个不同抗体、抗体片段、多肽或含有Fc的分子,或其混合物)的混合物。
在某些实施例中,再循环的量度可通过以下方法来确定:测量从第一腔室中的溶液中一个或多个分子(包括,例如,抗体、抗体片段、多肽或含有Fc的分子)的吸收以及在原始溶液被第二溶液替换后这些分子到第一腔室的返回。在其中还评估了转胞吞作用的一些实施例中,转胞吞作用的量度可以通过测量一个或多个分子(包括例如抗体、抗体片段、多肽或含有Fc的分子)从第一腔室中的溶液到第二腔室中的溶液的转胞吞作用来确定其中第一腔室和第二腔室由细胞单层分隔,并且每个腔室中的溶液处于生理pH。在某些实施例中,该细胞或多个细胞是真核的,诸如哺乳动物的,例如源自啮齿动物(诸如小鼠、大鼠、豚鼠、仓鼠或其他哺乳动物)、狗、非人灵长类动物(诸如食蟹猕猴)或人类。本文更详细地描述了可以使用的细胞。在某些实施例中,该细胞或多个细胞可以为马丁达比犬肾(MDCK)细胞。在一些实施例中,该细胞或多个细胞为野生型。在其他实施例中,它们表达一种或多种目标异源受体。在某些实施例中,该细胞包含至少一种异源基因。在某些实施例中,该至少一种异源基因可以选自由FCGRT基因和B2M基因组成的组。在某些实施例中,该细胞可以表达异源细胞表面蛋白。在某些实施例中,异源细胞表面蛋白可以包含新生儿Fc受体(FcRn)。在某些实施例中,测量分子的再循环和任选的转胞吞作用包括使用酶联免疫吸附测定(ELISA)、液体闪烁计数(LSC)、定量PCR或荧光读取器系统。在一些实施例中,测量分子的再循环和任选的转胞吞作用包括使用能够评估目标分子的亚纳摩尔浓度的定量方法。在一些实施例中,使用具有至少200pg/mL、至少100pg/mL或至少50pg/mL的较低水平定量下限(LLOQ)的定量方法。此类方法可包括例如使用高亲和力捕获试剂的ELISA,该试剂可以为例如生物素化小鼠抗人IgG-Fc,诸如生物素-R10Z。在本公开的实例部分中描述了此类敏感ELISA方法。在一些实施例中,此类敏感定量方法用于测量再循环,但不太敏感的(例如,纳摩尔浓度下具有LLOQ的)方法用于评估转胞吞作用。在一些实施例中,使用(例如来自Quanterix、Gyrolab或Singulex的)敏感自动化免疫测定平台来定量经再循环的分子和/或经转胞吞的分子。在某些实施例中,本公开的方法可进一步包括基于所测量的分子数量,确定多个分子的体内清除率(CL)、分布体积(Vd)、曲线下面积(AUC)、生物利用度、最大/最小血浆浓度(Cmax/Cmin),或体内半衰期(t
在某些实施例中,本公开涉及一种测定系统,包括:a)第一腔室和第二腔室,其中每个腔室包括处于生理pH的水溶液;b)细胞层,该细胞层将第一腔室和第二腔室分隔,其中细胞层可以介导分子从第一细胞层再循环到细胞层中并返回到第一腔室中;c)检测器,该检测器用于检测第一腔室中分子的存在;其中测定系统配置成确定检测器分子的再循环,其中该确定包括:将多个分子(包括例如抗体、抗体片段、多肽或含有Fc的分子)引入第一腔室;在第一腔室中孵育多个分子;更换第一腔室和第二腔室中的水溶液;以及测量从细胞层释放到第一腔室中的多个分子的量。形成细胞层的细胞可以为可以稳定生长以形成细胞层的任何细胞,如本文所进一步描述。在某些实施例中,可以将细胞以约1×10
在某些实施例中,可以将测试分子(包括例如抗体、抗体片段、多肽或含有Fc的分子)添加到跨孔测定的外腔室或内腔室中,并且可以通过以下方法测量再循环:在适当孵育时段之前测量在同一腔室(例如,分别为外腔室或内腔室)中存在的测试分子的量、清除培养基并更换它(追踪步骤)。在一些实施例中,还通过测量存在于相对腔室(例如,分别为内腔室或外腔室)中的测试分子的量来检测测试分子的转胞吞作用。在某些实施例中,测试分子从暴露于细胞的顶端膜的腔室再循环回到同一腔室。在一些实施例中,测试分子从暴露于细胞的底侧膜的腔室再循环回到同一腔室。在更进一步的实施例中,将测试分子从暴露于细胞的顶膜的腔室转胞吞至暴露于细胞的底侧膜的腔室。
在某些实施例中,本公开提供了用于确定或预测一种或多种分子(包括例如抗体、抗体片段、多肽或含有Fc的分子)的PK参数的方法,包括:a)引入分子进入两个腔室中的第一腔室,其中第一腔室与第二腔室由一个或多个细胞分隔,并且其中第一腔室和第二腔室中的每一者都具有生理pH值;以及b)测量从第一腔室循环到第一腔室的分子的数量。在某些实施例中,生理pH为约6.5至约8.0。在某些实施例中,生理pH值是介于约6.5与约8.0之间的任何值,例如,约6.6、约6.7、约6.8、约6.9、约7.0、约7.1、约7.2、约7.3、约7.4、约7.5、约7.6、约7.7、约7.8、或约7.9,或者是约6.5至约8.0的范围内的任何范围。在某些实施例中,只要两个腔室都具有生理pH,每个腔室的pH就可以不同。例如但不作为限制,第一腔室可以具有6.5的pH,而第二腔室可以具有8.0的pH,或反之亦然。在某些实施例中,生理pH可以为约7.4。在一些实施例中,PK参数为体内清除率(CL)、分布体积(Vd)、曲线下面积(AUC)、生物利用度、最大/最小血浆浓度(Cmax/Cmin)或体内半衰期(t
在某些实施例中,测定系统进一步包括:检测器,该检测器用于检测第一腔室中分子的存在;细胞层可以介导分子从第一腔室到第二腔室的再循环;并且其中测定系统配置成确定多个分子从细胞层进入第一腔室的再循环,其中确定再循环包括:在已经替换水溶液之后,测量第一腔室中多个分子的量。在一些实施例中,还测量转胞吞作用。在某些实施例中,测定系统进一步包括:检测器,该检测器用于检测第二腔室中分子的存在;细胞层可以介导分子从第一腔室到第二腔室的转胞吞作用;并且其中测定系统配置成确定多个分子跨细胞层的转胞吞作用,其中确定转胞吞作用包括:在已经替换水溶液之后,测量该第二腔室中多个分子的量。在一些实施例中,用于检测第一腔室中分子的存在的检测器能够评估一种或多种目标分子(包括,例如,抗体、抗体片段、多肽或含有Fc的分子)的亚纳摩尔浓度,诸如具有至少200pg/mL、至少100pg/mL或至少50pg/mL的LLOQ。在一些实施例中,用于检测第二腔室中分子的存在的检测器具有相似敏感度。在其他实施例中,该检测器没有,例如,其可具有纳摩尔浓度范围内的LLOQ。
在某些实施例中,本公开提供用于测量多个相同分子或多个不同分子的跨细胞输运的测定,包括第一腔室和第二腔室,第一腔室和第二腔室中的每一者都具有生理pH值,其中第一腔室接收多个分子并配置成允许分子转胞吞到第二腔室并且允许分子再循环回到第一腔室。在某些实施例中,生理pH为约6.5至约8.0。在某些实施例中,生理pH值是介于约6.5与约8.0之间的任何值,例如,约6.6、约6.7、约6.8、约6.9、约7.0、约7.1、约7.2、约7.3、约7.4、约7.5、约7.6、约7.7、约7.8、或约7.9,或者是约6.5至约8.0的范围内的任何范围。在某些实施例中,只要两个腔室都具有生理pH,每个腔室的pH就可以不同。例如但不作为限制,第一腔室可以具有6.5的pH,而第二腔室可以具有8.0的pH,或反之亦然。在某些实施例中,生理pH可以为约7.4。
在某些实施例中,本公开提供用于确定或预测一种或多种分子的一个或多个PK参数的测定,包括第一腔室和第二腔室,第一腔室和第二腔室中的每一者都具有生理pH值,其中第一腔室接收多个分子并且配置成允许分子从第一腔室再循环回到第一腔室,并且任选地配置成允许分子从第一腔室转胞吞到第二腔室。在某些实施例中,生理pH值为约7.4。在一些实施例中,PK参数为体内清除率(CL)、分布体积(Vd)、曲线下面积(AUC)、生物利用度、最大/最小血浆浓度(Cmax/Cmin)或体内半衰期(t1/2)。在一些实施例中,PK参数为体内清除率。
在某些实施例中,第一腔室可以包含细胞单层。在某些实施例中,测定中所使用的细胞选自下文标题为“细胞”的第4节中提供的列表。在某些实施例中,用于在测定中的细胞为真核细胞。在一些实施例中,该细胞为哺乳动物细胞。在某些实施例中,该细胞为肾细胞。在一些实施例中,该肾细胞是啮齿动物、非人灵长类动物、人类或犬科动物的细胞。在一些实施例中,该细胞为MDCK细胞。在某些实施例中,在本公开中所描述的方法中使用的细胞可以包含至少一种异源基因。在某些实施例中,该至少一种异源基因可以选自由FCGRT基因和B2M基因组成的组。在某些实施例中,在本公开中所描述的方法中使用的细胞可以表达细胞表面蛋白。在某些实施例中,细胞表面蛋白包含Fc受体(FcR)。在某些实施例中,细胞表面蛋白包含新生儿Fc受体(FcRn)。
在某些实施例中,分子可以被标记或未被标记。所标记的分子的非限制性实例包括3H标记的、荧光标记的分子或放射性同位素,例如I-125和P-32。
在某些实施例中,本公开的方法包括测量经再循环的分子和任选的跨细胞输运的分子的数量。在某些非限制性实施例中,可通过酶联免疫吸附测定(ELISA)、液体闪烁计数(LSC)、定量PCR、荧光读取器系统、共聚焦显微镜或活细胞成像系统、或其任意组合来进行测量经再循环或跨细胞输运的分子的数量。设想使用不同检测方法来检测经再循环的分子与经转胞吞的分子。在一些实施例中,测量方法为能够评估一种或多种目标分子(包括例如抗体、抗体片段、多肽或含有Fc的分子)的亚纳摩尔浓度的测量方法,其LLOQ诸如至少为200pg/mL、至少100pg/mL、或至少50pg/mL。在一些实施例中,检测器系统包括使用高亲和力捕获试剂的ELISA测定,该试剂可以为例如生物素化小鼠抗人IgG-Fc,诸如生物素-R10Z。在某些实施例中,使用不同方法,其中用于测量再循环的方法能够评估亚纳摩尔浓度,而用于测量转胞吞作用的方法则不能够进行评估。使用(例如来自Quanterix、Gyrolab或Singulex的)敏感自动化免疫测定平台来定量经再循环的分子和/或经转胞吞的分子。
在某些实施例中,本公开提供了用于在类似于FcRn介导的IgG补救途径的条件下,通过表达人类FcRn和B2M的MDCK细胞,测量目标分子(例如,一种或多种抗体、抗体片段、多肽或含有Fc的分子)的再循环和任选的转胞吞作用的FcRn依赖性基于细胞的测定。在某些实施例中,该测定的输出不仅涉及生理条件下的Fc-FcRn相互作用,还涉及与目标分子的体内PK行为有关的非特异性结合、细胞吸收、分选和细胞内运输过程。在一些实施例中,目标分子为IgG mAb,诸如本文别处所描述的那些。在一些实施例中,该测定测量另外两种目标分子的再循环和任选的转胞吞作用。
在某些实施例中,本公开提供了用于将再循环与动物(具有不同结构、功能和药理特性的目标分子)中一个或多个PK特性相关联的方法和测定。在某些实施例中,PK特性为体内清除率(CL)、分布体积(Vd)、曲线下面积(AUC)、生物利用度、最大/最小血浆浓度(Cmax/Cmin)或体内半衰期(t
在某些实施例中,可能需要表达FcRn以促进测定中mAb等目标分子(包括例如抗体、抗体片段、多肽或含有Fc的分子)的再循环和任选的转胞吞作用(如果也被评估),并有助于被评估的再循环和PK参数或组织渗透率之间的所观察到的关联性。在某些实施例中,本公开中所描述的方法和测定能够对临床前物种中含有Fc的分子的电荷或糖基化变体的清除率进行排序。在某些实施例中,本公开中所描述的方法和测定可用作用于在导联选择和优化以及针对期望药代动力学特性的工艺开发过程中,评估候选药物(包括例如抗体、抗体片段、多肽或含有Fc的分子)的高时效、节省成本且节省动物的工具。
在某些实施例中,本公开提供了基于细胞的测定和方法,其在生理相关条件下测量药物(包括例如抗体、抗体片段、多肽或含有Fc的分子)的再循环效率。在某些实施例中,稳定表达人类FcRn和β2-微球蛋白基因的MDCK细胞与本文所述的测定结合使用。
在某些实施例中,本公开提供了在生理pH下在补充有胎牛血清的正常细胞培养基中进行的方法和测定,该胎牛血清提供已知与人类FcRn结合的牛白蛋白(Chaudhury C.等人,2003,J.Exp.Med.197,315–322)。
在某些实施例中,本公开提供了方法和测定,其中分子通过非特异性胞饮作用被细胞吸收,在白蛋白的存在下与人类FcRn相互作用并在与FcRn介导的作用机制相关的条件下被细胞再循环。在一些实施例中,至少一部分该分子被再循环回到细胞层的该分子被从其吸收的侧面。在一些实施例中,至少一部分该分子经转胞吞至细胞层的相对侧面。在某些实施例中,本公开提供了用于确定或预测哺乳动物中的目标分子(包括例如抗体、抗体片段、多肽或含有Fc的分子)的清除率(由于方法和/或测定能够评估与细胞的非特异性结合、经由胞饮作用的吸收、与FcRn的pH依赖性相互作用和/或细胞内运输和分选过程的动力学的综合效应)的方法和测定。在一些实施例中,该哺乳动物为非人灵长类动物,诸如食蟹猕猴。在一些实施例中,哺乳动物为人。
在某些实施例中,本公开提供了用于确定或预测目标分子(包括例如抗体、抗体片段、多肽或含有Fc的分子)的组织渗透率的方法和测定。在某些实施例中,组织为脑组织。在某些实施例中,本公开提供了用于通过确定分子的T/R比率来确定或预测目标分子的组织渗透率的方法和测定。在某些实施例中,本公开提供了用于确定或预测哺乳动物中的目标分子(包括例如抗体、抗体片段、多肽或含有Fc的分子)的组织渗透率(由于方法和/或测定能够评估与细胞的非特异性结合、经由胞饮作用的吸收、与FcRn的pH依赖性相互作用和/或细胞内运输和分选过程的动力学的综合效应)并确定目标分子的T/R比率的方法和测定。在一些实施例中,该哺乳动物为非人灵长类动物,诸如食蟹猕猴。在一些实施例中,哺乳动物为人。
在某些实施例中,本公开提供了用于关联再循环(和进一步任选的转胞吞作用)输出量的方法和测定,该输出量是通过哺乳动物中目标分子(包括例如抗体、抗体片段、多肽或含有Fc的分子)的PK参数而获得。在一些实施例中,PK参数为体内清除率(CL)、分布体积(Vd)、曲线下面积(AUC)、生物利用度、最大/最小血浆浓度(Cmax/Cmin)或体内半衰期(t
在又进一步的实施例中,本公开提供了用于确定除测试分子之外的一种或多种试剂对测试分子(包括例如抗体、抗体片段、多肽或含有Fc的分子)的再循环、转胞吞作用、组织渗透率、PK参数或其他特性的影响。此类试剂(也可以称为二级分子)可以为例如小分子(例如,不是蛋白或多肽),诸如小分子药物,或者可以为肽,或者可以为多肽,或者可以为抗体或其片段,或此类分子的多个或组合。此类试剂可以为以下试剂:该试剂与测试分子结合;或者怀疑与测试分子结合;或者调节测试分子与介导分子输运的受体的结合,诸如调节测试分子与FcRn的结合;或者是被评估系统中目标受体的配体(例如,由细胞层的一种或多种细胞表达的受体的配体);或者已知或怀疑与测试分子或细胞层所表达的受体相互作用。该试剂可以为治疗性分子,诸如处方药或非处方(OTC)药;或者为膳食补充剂、维生素、研究试剂、成像试剂或其他目标试剂。治疗剂可包括用于治疗免疫系统、心血管系统、内分泌系统、胃肠道、肾系统、呼吸系统或中枢神经系统的疾病或病症的那些,或用于治疗癌症或其他恶性肿瘤(包括化疗药物和免疫治疗药物)、病毒感染、细菌感染、真菌感染或寄生虫感染的那些。也可以评估两种或更多种目标试剂的组合。因此,在一些实施例中,本文所提供的方法包括在一种或多种试剂的存在下评估测试分子的再循环或再循环和转胞吞作用。一种或多种试剂可以包括在第一腔室中但不包括在第二腔室中,或者包括在第二腔室中但不包括在第一腔室中,或者包括在两个腔室中,或者包括在第一腔室的第一溶液中但随后在溶液被替换时不存在,或其组合。在一些实施例中,在不存在一种或多种试剂的情形下,进一步将测定输出与再循环或再循环和转胞吞作用进行比较。根据本文所述的方法和测定评估一种或多种试剂对测试分子的再循环或再循环和转胞吞作用的影响的能力可用于例如确定一种或多种药物可如何影响测试分子的一个或多个PK参数,或者如何影响测试分子的组织渗透率(例如,脑渗透率)。例如,本文所述的方法和测定可用于了解共同施用的药物对目标分子的PK参数和/或组织渗透率的影响。例如,本文所述的方法和测定可用于研究跨细胞输运机制、PK参数和/或组织渗透率。
本公开还提供了用于确定环境条件下一种或多种变化对测试分子(包括例如抗体、抗体片段、多肽或含有Fc的分子)的再循环、转胞吞作用、组织渗透率、PK参数或其他特性的影响的方法和测定。此类环境条件可以包括例如一种或多种细胞培养基成分的存在、不存在或浓度、或温度、或pH、或氧化、或其组合。在一些实施例中,组织渗透率为脑渗透率。
在某些实施例中,选择本公开的方法和测定的测试分子(包括例如抗体、抗体片段、多肽或含有Fc的分子)可以基于临床级材料的可用性,该动物PK数据和/或动物组织渗透率数据来自可靠源(诸如但不限于处方信息)、基于群体PK或组织渗透率模型的发表报告、或生成线性PK或组织渗透率数据的内部临床试验。在某些实施例中,使用临床级材料可以确保测试材料的质量可以与在生成人PK或组织渗透率数据的临床研究中所使用的那些一致。
在某些实施例中,本公开中所描述的方法和测定可用作体外评估候选药物(包括例如抗体、抗体片段、多肽或含有Fc的分子)的非特异性清除率的潜在倾向的工具以支持导联选择和优化,目的是对候选进行排序并减少在动物模型中所测试的分子的数量,和/或减少所需动物模型的数量。
在某些实施例中,本公开中所描述的方法和测定可用于支持研究表现出非期望或非典型PK或组织渗透率行为的目标分子(包括例如抗体、抗体片段、多肽或含有Fc的分子),或开发新型药物(包括例如抗体、抗体片段、多肽或含Fc药物),其具有改善的再循环特性,适用于特定应用,诸如穿过血脑屏障以增强脑暴露或增强在肿瘤微环境中的处置以用于改善肿瘤靶向。此类“改善的再循环特性”可包括与另一种分子相比再循环的升高,这在一些实施例中可以延长血清半衰期。在某些实施例中,本公开中所描述的方法和测定可用于支持研究表现出非期望或非典型PK或组织渗透率行为的目标分子(包括例如抗体、抗体片段、多肽或含有Fc的分子)或开发新型药物,其具有改善的转胞吞特性,适用于特定应用,诸如穿过血脑屏障以增强脑暴露或增强在肿瘤微环境中的处置以用于改善肿瘤靶向。此类“改善的转胞吞特性”可包括与另一种分子相比转胞吞作用的增强。更进一步地,在某些实施例中,本公开中所描述的方法和测定可用于支持研究表现出非期望或非典型PK或组织渗透率行为的目标分子(包括例如抗体、抗体片段、多肽或含有Fc的分子)或开发新型药物,其具有改善的转胞吞特性,适用于特定应用,诸如穿过血脑屏障以增强脑暴露或增强在肿瘤微环境中的处置以用于改善肿瘤靶向。此类“改善的转胞吞特性”可包括与另一种分子相比转胞吞作用的增强。进一步设想使用本文所述的测定来支持开发与另一种分子相比具有改善的转胞吞作用与再循环比率的新型药物(包括例如抗体、抗体片段、多肽或含有Fc的分子)。此类“改善的转胞吞作用与再循环比率”(T/R比率)可包括比另一种分子更高的比率,例如由于转胞吞作用增强、再循环减少,或两者。与另一种分子相比,更高T/R比率可导致更佳的组织渗透率,诸如更佳的脑渗透率。在一些实施例中,目标分子和/或药物为mAb。
在某些实施例中,本公开中所描述的方法和测定可用于开发改善的基于机制的PK模型以支持临床研究中最佳剂量和给药方案的设计。在某些实施例中,本公开中所描述的方法和测定可用于显示测试分子(包括例如抗体、抗体片段、多肽或含有Fc的分子)的体外读数和体内PK数据之间的相关性。此类PK模型和/或数据可涉及体内清除率(CL)、体内半衰期(t
在某些实施例中,目标分子、测试分子和/或多个分子可以为抗体。在某些实施例中,抗体可以为单克隆或多克隆抗体。在某些实施例中,抗体可以具有不同结构组成(嵌合、人源化和完全人源化)。在某些实施例中,抗体可以由不同重链和轻链序列(IgG1、IgG2和IgG4重链、κ和λ轻链)组成。在某些实施例中,抗体可以识别不同类型的(膜结合和可溶性)靶标。在某些实施例中,抗体可以发挥不同治疗作用机制(激动、拮抗和细胞毒性)。在某些实施例中,抗体可以并且经由不同途径(例如,静脉内、肌内或皮下)给予患者。在某些实施例中,该抗体为抗IgE抗体、抗VEGF抗体、抗整合素抗体(例如抗α4β7整合素抗体)、抗IL-6抗体、抗TNFa抗体、抗BACE1抗体、或抗gD抗体,或其片段。在一些实施例中,该抗体为奥马珠单抗(omalizumab)、贝伐珠单抗(bevacizumab)、维多珠单抗(vedolizumab)、托珠单抗(tocilizumab)、阿达木单抗(adalimumab)、抗BACE1 WT、抗BACE1变体YEY(突变:M252Y;N286E;N434Y)、抗BACE1变体YQAY(突变:M252Y;T307Q;Q311A;N434Y)、抗BACE1变体YPY(突变:M252Y;V308P;N434Y)、抗BACE1变体YY(突变:M252Y;N434Y)、抗BACE1变体YLY1(Q6)(突变:M252Y;M428L;N434Y;Y436I)、或抗BACE1变体YIY(T3)(突变:M252Y;Q311I;N434Y),或其片段。在一些实施例中,评估了两种或更多种抗体。
在某些实施例中,目标分子、测试分子和/或多个分子可以携带可以改变其效应子功能的工程化突变(诸如但不限于阿特珠单抗(atezolizumab)、德瓦鲁单抗(durvalumab)),使得双特异性半抗体(诸如但不限于艾美赛珠单抗(emicizumab))能够结合,或者使IgG4 Fab臂(诸如但不限于纳武单抗(nivolumab)、派姆单抗(pembrolizumab))稳定。
在某些实施例中,目标分子、测试分子和/或多个分子可以为表现出极高FcRn结合亲和力的抗体。在某些实施例中,在哺乳动物(例如非人灵长类动物或人类)中所观察到的再循环读数与PK参数之间的相关性可适用于携带典型Fc区的广泛抗体。在某些实施例中,测试分子可以为经工程化以具有改变的FcRn结合活性的抗体。在某些实施例中,目标分子、测试分子和/或多个分子可以为含有白蛋白的分子,或经工程化以经由肽标签或重组蛋白结合FcRn的任何分子。在某些实施例中,目标分子、测试分子和/或多个分子可以为天然结合FcRn的分子。在某些实施例中,目标分子、测试分子和/或多个分子可以为经工程化以结合FcRn的分子。
在某些实施例中,本公开中所描述的方法和测定可用于指示在再循环或再循环和转胞吞测定中是否需要表达人类FcRn以进行高效再循环,以及在一些实施例中的再循环和转胞吞。
在某些实施例中,本公开的方法和测定可用于检测和/或指示与FcRn的相互作用有助于观察到的测试分子的再循环读数和PK参数之间的相关性。在一些实施例中,体内清除率(CL)、体内半衰期(t
在某些实施例中,本公开的方法和测定可用于分析目标分子、测试分子和/或多个分子与受体的结合。在某些实施例中,受体可以为FcRn受体。在某些实施例中,测试分子可以为抗体。在某些实施例中,受体可以为转铁蛋白受体。在某些实施例中,受体为人类、小鼠、大鼠或食蟹猕猴转铁蛋白受体。在某些实施例中,受体为转铁蛋白1或转铁蛋白2受体。在某些实施例中,受体为在UNIPROT P02786(TFR1_HUMAN)、UNIPROT Q9UP52(TFR2_HUMAN)、UNIPROT A0A2K5X958(A0A2K5X958_MACFA,cyno)、UNIPROT Q62351(TFR1_MOUSE)、UNIPROTQ9JKX3(TFR2_MOUSE)、UNIPROT Q99376(TFR1_RAT)或UNIPROT B2GUY2(TFR2_RAT)中描述的转铁蛋白受体。在一些实施例中,受体描述于UNIPROT P02786(TFR1_HUMAN)或UNIPROTQ9UP52(TFR2_HUMAN)中。在某些实施例中,受体可以为巨蛋白受体。在某些实施例中,受体为在UNIPROT P98164(LRP2_HUMAN)、UNIPROT A2ARV4(LRP2_MOUSE)或UNIPROT P98158(LRP2_RAT)中描述的巨蛋白受体。在某些实施例中,受体可以为立方蛋白受体。在一些实施例中,受体为在UNIPROT O60494(CUBN_HUMAN)、UNIPROT Q9JLB4(CUBN_MOUSE)、UNIPROTO70244(CUBN_RAT)或UNIPROTA0A2K5USK6(A0A2K5USK6_MACFA,cyno)中描述的立方蛋白受体。
在某些实施例中,本发明的方法、测定、测定系统和试剂盒的FcRn受体为人类FcRn受体。
在某些实施例中,本发明的方法、测定、测定系统和试剂盒的人类FcRn受体的重链具有如下序列:AESHLSLLYHLTAVSSPAPGTPAFWVSGWLGPQQYLSYNSLRGEAEPCGAWVWENQVSWYWEKETTDLRIKEKLFLEAFKALGGKGPYTLQGLLGCELGPDNTSVPTAKFALNGEEFMNFDLKQGTWGGDWPEALAISQRWQQQDKAANKELTFLLFSCPHRLREHLERGRGNLEWKEPPSMRLKARPSSPGFSVLTCSAFSFYPPELQLRFLRNGLAAGTGQGDFGPNSDGSFHASSSLTVKSGDEHHYCCIVQHAGLAQPLRVELESPAKSSVLVVGIVIGVLLLTAAAVGGALLWRRMRSGLPAPWISLRGDDTGVLLPTPGEAQDADLKDVNVIPATA(SEQ ID NO:1)。
在某些实施例中,本发明的方法、测定、测定系统和试剂盒的人类FcRn受体的轻链具有如下序列:MSRSVALAVLALLSLSGLEAIQRTPKIQVYSRHPAENGKSNFLNCYVSGF HPSDIEVDLLKNGERIEKVEHSDLSFSKDWSFYLLYYTEFTPTEKDEYACR VNHVTLSQPKIVKWDRDM(SEQ ID NO:2)。
在某些实施例中,本发明的方法、测定、测定系统和试剂盒的FcRn受体为小鼠FcRn受体。
在某些实施例中,本发明的方法、测定、测定系统和试剂盒的小鼠FcRn受体的重链具有如下序列:SETRPPLMYHLTAVSNPSTGLPSFWATGWLGPQQYLTYNSLRQEADPCGAWMWENQVSWYWEKETTDLKSKEQLFLEALKTLEKILNGTYTLQGLLGCELASDNSSVPTAVFALNGEEFMKFNPRIGNWTGEWPETEIVANLWMKQPDAARKESEFLLNSCPERLLGHLERGRRNLEWKEPPSMRLKARPGNSGSSVLTCAAFSFYPPELKFRFLRNGLASGSGNCSTGPNGDGSFHAWSLLEVKRGDEHHYQCQVEHEGLAQPLTVDLDSSARSSVPVVGIVLGLLLVVVAIAGGVLLWGRMRSGLPAPWLSLSGDDSGDLLPGGNLPPEAEPQGANAFPATS(SEQ ID NO:3)。
在某些实施例中,本发明的方法、测定、测定系统和试剂盒的小鼠FcRn受体的轻链具有如下序列:MARSVTLVFLVLVSLTGLYAIQKTPQIQVYSRHPPENGKPNILNCYVTQF HPPHIEIQMLKNGKKIPKVEMSDMSFSKDWSFYILAHTEFTPTETDTYACR VKHDSMAEPKTVYWDRDM(SEQ ID NO:4)。
在某些实施例中,本发明的方法、测定、测定系统和试剂盒的FcRn受体为大鼠FcRn受体。
在某些实施例中,本发明的方法、测定、测定系统和试剂盒的大鼠FcRn受体的重链具有如下序列:AEPRLPLMYHLAAVSDLSTGLPSFWATGWLGAQQYLTYNNLRQEADPCGAWIWENQVSWYWEKETTDLKSKEQLFLEAIRTLENQINGTFTLQGLLGCELAPDNSSLPTAVFALNGEEFMRFNPRTGNWSGEWPETDIVGNLWMKQPEAARKESEFLLTSCPERLLGHLERGRQNLEWKEPPSMRLKARPGNSGSSVLTCAAFSFYPPELKFRFLRNGLASGSGNCSTGPNGDGSFHAWSLLEVKRGDEHHYQCQVEHEGLAQPLTVDLDSPARSSVPVVGIILGLLLVVVAIAGGVLLWNRMRSGLPAPWLSLSGDDSGDLLPGGNLPPEAEPQGVNAFPATS(SEQ ID NO:5)。
在某些实施例中,本发明的方法、测定、测定系统和试剂盒的大鼠FcRn受体的轻链具有如下序列:MARSVTVIFLVLVSLAVVLAIQKTPQIQVYSRHPPENGKPNFLNCYVSQF HPPQIEIELLKNGKKIPNIEMSDLSFSKDWSFYILAHTEFTPTETDVYACRV KHVTLKEPKTVTWDRDM(SEQ ID NO:6)。
在某些实施例中,本发明的方法、测定、测定系统和试剂盒的FcRn受体为食蟹猕猴(cyno)FcRn受体。
在某些实施例中,本发明的方法、测定、测定系统和试剂盒的cyno FcRn受体的重链具有如下序列:AESHLSLLYHLTAVSSPAPGTPAFWVSGWLGPQQYLSYDSLRGQAEPCGAWVWENQVSWYWEKETTDLRIKEKLFLEAFKALGGKGPYTLQGLLGCELSPDNTSVPTAKFALNGEEFMNFDLKQGTWGGDWPEALAISQRWQQQDKAANKELTFLLFSCPHRLREHLERGRGNLEWKEPPSMRLKARPGNPGFSVLTCSAFSFYPPELQLRFLRNGMAAGTGQGDFGPNSDGSFHASSSLTVKSGDEHHYCCIVQHAGLAQPLRVELETPAKSSVLVVGIVIGVLLLTAAAVGGALLWRRMRSGLPAPWISLRGDDTGSLLPTPGEAQDADSKDINVIPATA(SEQ ID NO:7)。
在某些实施例中,本发明的方法、测定、测定系统和试剂盒的cyno FcRn受体的轻链具有如下序列:MSPSVALAVLALLSPSGLEAIQRTPKIQVYSRHPPENGKPNFLNCYVSGFH PSDIEVDLLKNGEKMGKVEHSDLSFSKDWSFYLLYYTEFTPNEKDEYAC RVNHVTLSGPRTVKWDRDM(SEQ ID NO:8)。
在某些实施例中,本发明的方法、测定、测定系统和试剂盒可用于评估多种因素(诸如但不限于内化、分选和细胞内运输的动力学以及胞吐作用)对测试分子(包括例如抗体、抗体片段、多肽或含有Fc的分子)的回收过程的总效率的贡献。在某些实施例中,本公开的方法和测定可用于识别和/或检测涉及FcRn介导的补救途径的多个参数,以用于确定或预测测试分子(包括例如抗体、抗体片段、多肽或含有Fc的分子)的PK。
在某些实施例中,本公开的方法、测定、测定系统和试剂盒可用于检测测试分子(包括例如抗体、抗体片段、多肽或含有Fc的分子)的体外再循环和体内清除率之间的相关性。在某些实施例中,与BV ELISA或Fv电荷/pI相比,本公开的测定可用于检测分子的体外再循环和体内清除率的相关性。
在某些实施例中,本公开的方法、测定、测定系统和试剂盒可用于评估和/或研究糖基化在体内对测试分子(包括例如抗体、抗体片段、多肽或含有Fc的分子)的分布和分解代谢的作用。在某些实施例中,分子可以为糖型变体。
在某些实施例中,本公开的方法、测定、测定系统和试剂盒可用于评估向分子添加唾液酸对细胞内运输参数的作用。在某些实施例中,它们可用于分析其他机制在体内清除分子的高甘露糖和高度唾液酸化糖型变体方面的参与。
在某些实施例中,本公开的方法、测定、测定系统和试剂盒可以用作研究FcRn介导的转胞吞作用和再循环的工具,其作为测试分子(包括例如抗体、抗体片段、多肽或含有Fc的分子)的与其PK有关的消除机制。
在某些实施例中,本公开的方法、测定、测定系统和试剂盒可以用作研究和阐明控制复合FcRn的IgG的分布的分子机制的工具。
在某些实施例中,本公开的方法、测定、测定系统和试剂盒可以提供反映在人体中具有典型FcRn结合亲和力的测试分子(包括例如抗体、抗体片段、多肽、或含有Fc的分子)的靶标非相关、非特异性清除机制的输出。
在某些实施例中,本公开的方法、测定、测定系统和试剂盒可用于分析不同组的含有Fc的分子并响应已知影响PK的因素。
在某些实施例中,本实施例的方法、测定、测定系统和试剂盒可用于剖析涉及再循环测定以及再循环和转胞吞作用测定的因素,以了解这些因素如何与体内清除率相关并定义该相关性的定量性质。
在某些实施例中,本实施例的方法、测定、测定系统和试剂盒可用于剖析涉及再循环测定以及再循环和转胞吞作用测定的因素,以了解这些因素如何与组织渗透率相关并定义该相关性的定量性质。在一些实施例中,组织渗透率为脑渗透率。
在某些实施例中,本公开的方法、测定、测定系统和试剂盒可用于研究所胞饮或内化的测试分子(包括例如抗体、抗体片段、多肽或含有Fc的分子)在各种细胞类型/组织区室中在再循环、转胞吞作用和降解途径之间的分布,并研究控制参与清除IgG的细胞中的此类分布的分子机制。
在某些实施例中,本公开涉及再循环测定系统。在某些实施例中,本公开涉及再循环和转胞吞作用测定系统。例如但不作为限制,此类系统可以包括:第一腔室和第二腔室,其中第一腔室和第二腔室中的每一者均包括处于生理pH的水溶液;细胞层,该细胞层将第一腔室和第二腔室分隔,使得细胞层可以介导引入第一腔室的分子再循环到细胞层中并返回到第一腔室;以及检测器,该检测器用于检测第一腔室中分子的存在。在某些实施例中,本文所公开的测定系统采用真核细胞的细胞层,该真核细胞诸如哺乳动物细胞,例如啮齿动物、犬科动物、非人灵长类动物或人类的细胞。在一些实施例中,本文所公开的测定系统采用肾细胞的细胞层。在一些实施例中,本文所公开的测定系统采用MDCK细胞的细胞层。在一些实施例中,细胞层为单细胞层。在某些实施例中,本文所公开的测定系统采用包含至少一种异源基因的细胞。在某些实施例中,本文所公开的测定系统采用包含至少一种选自FCGRT基因和B2M基因的异源基因的细胞。在某些实施例中,本文所公开的测定系统采用表达异源细胞表面蛋白的细胞。在某些实施例中,本文所公开的测定系统采用表达异源细胞表面蛋白的细胞,其中异源细胞表面蛋白包含新生儿Fc受体(FcRn)。在某些实施例中,本文所公开的测定系统可经由使用酶联免疫吸附测定(ELISA)、液体闪烁计数(LSC)、定量PCR、荧光读取器系统、自动化免疫测定平台(例如Quanterix、Gyrolab和Singlex)、荧光成像或质谱法来测量经再循环的分子的数量。在某些实施例中,本文所公开的测定系统可以使用具有至少200pg/mL、或至少100pg/mL、或至少50pg/mL的LLOQ的方法(诸如使用高亲和力捕获试剂(例如,生物素化小鼠抗人IgG-Fc,诸如生物素R10Z)的ELISA测定)来测量经再循环的分子的数量。在某些实施例中,在本公开的再循环和转胞吞测定系统中,细胞层可以介导分子从第一腔室到第二腔室的转胞吞作用。在一些实施例中,测定系统进一步包括检测器,该检测器用于检测分子在第二腔室中的存在。此类检测器可以与用于检测第一腔室中分子的存在的检测器相同类型和/或具有相同LLOQ,或者该检测器可以具有另一种类型和/或不同敏感度,例如敏感度较低的类型(例如,具有纳摩尔浓度范围内的LLOQ)。
4.细胞
要用于本公开的方法、测定、测定系统或试剂盒的合适细胞包括如本文所述的原核或真核细胞。
在某些实施例中,也可以使用脊椎动物细胞。可用的哺乳动物细胞系的非限制性实例为:由SV40(COS-7)转化的猴肾CV1系;原代人内皮细胞;人脐静脉内皮细胞(HUVEC);人脑微血管内皮细胞(HBMEC);血管内皮细胞(EA.hy926);人真皮微血管内皮细胞(HMEC);人胚胎肾系(如Graham等人,J.Gen Virol.36:59(1977)中所阐述的293或293细胞);幼仓鼠肾细胞(BHK);小鼠赛托利(sertoli)细胞(如Mather,Biol.Reprod.23:243-251(1980)中所阐述的TM4细胞);猴肾细胞(CV1);非洲绿猴肾细胞(VERO-76);人子宫颈癌细胞(HELA);犬肾细胞(MDCK);Buffalo大鼠肝细胞(BRL 3A);人肺细胞(W138);人肝细胞(Hep G2);小鼠乳腺肿瘤(MMT 060562);TRI细胞,如Mather等人,Annals N.Y.Acad.Sci.383:44-68(1982)中所阐述;MRC 5细胞;以及FS4细胞。可用的哺乳动物细胞系的其他非限制性实例包括中国仓鼠卵巢(CHO)细胞,包括DHFR-CHO细胞(Urlaub等人,Proc.Natl.Acad.Sci.USA 77:4216(1980))。在某些实施例中,本公开的方法可以使用杂交瘤细胞。例如但不作为限制,杂交细胞系可以属于任何物种,包括人类和小鼠。在某些实施例中,本公开的方法可以使用原代和已建立的内皮细胞和/或上皮细胞。例如但不作为限制,内皮细胞和/或上皮细胞可以为caco-2、T-84、HMEC-1、MHEC 2.6、HUVEC和诱导的多能干细胞(iPSC)衍生细胞(参见,例如,Lidington,E.A.,D.L.Moyes,等人(1999),“A comparison of primary endothelialcells and endothelial cell lines for studies of immune interactions”TransplImmunol7(4):239-246;或Yamaura,Y.,B.D.Chapron等人(2016),“Functional Comparisonof Human Colonic Carcinoma Cell Lines and Primary Small Intestinal EpithelialCells for Investigations ofIntestinal Drug Permeability and First-PassMetabolism”,Drug Metab Dispos 44(3):329-335)。
在某些实施例中,用于所公开的方法、测定、测定系统或试剂盒的细胞可以包含编码分子(例如受体)的核酸。在某些实施例中,该核酸可以以一种或多种载体存在,例如表达载体。一种载体的类型为“质粒”,其是指环状双链DNA环圈,可在其中连接其他DNA片段。另一种载体的类型为病毒载体,其中其他DNA片段可连接至病毒基因组。某些载体能够在引入他们的细胞(例如具有细菌复制起始点的细菌载体,和附加型哺乳动物载体)中自主复制。其他载体(例如,非附加型哺乳动物载体)在导入细胞后经嵌入到细胞的基因组中,并且从而与宿主基因组一起复制。此外,某些载体(表达载体)能够指导与其可操作连接的基因的表达。通常来说,在重组DNA技术中有用的表达载体通常为质粒(载体)的形式。用于本公开中的表达载体的其他非限制性实例包括提供等效功能的病毒载体(例如复制缺陷型反转录病毒、腺病毒和腺相关病毒)。
在某些实施例中,可以将编码分子(例如受体)的核酸引入细胞中。在某些实施例中,导入核酸至细胞中可以通过任何本领域已知的方法来进行,本领域已知的方法包括但不限于转染、电穿孔、显微注射、用含有核酸序列的病毒或噬菌体载体感染、细胞融合、染色体介导的基因转移、微细胞介导的基因转移、球形质粒融合等。在某些实施例中,该细胞为真核的,例如MDCK细胞。
5.腔室
本公开的方法、测定、测定系统或试剂盒需要第一腔室和第二腔室,其中第一腔室和第二腔室由细胞层分隔。可以使用能够将水溶液保持在沿细胞层相交的两个单独区室中的任何合适配置的腔室。该腔室的材料可以包括例如塑料(例如聚碳酸酯)、玻璃、陶瓷、涂覆材料(例如增塑金属)或其混合物。该腔室可以是完全封闭的,或者可以具有暴露的一侧或多侧,只要它们可以在两个腔室中保持足够水溶液并维持分隔该腔室的细胞层。该腔室可进一步包括其中一个腔室的体积小于另一个腔室并例如配合在另一个腔室的三维空间内(例如,作为插入件)(由细胞层分隔)的配置。在一些实施例中,较小的腔室(其也可以被描述为“内腔室”)为第一腔室,较大的腔室(其也可以被描述为“外腔室”)为第二腔室。然而,此类术语并不意味着将当前描述的测定和系统的使用限制为替代性腔室组合(例如,外腔室可以用作第一腔室,而内腔室可以用作第二腔室)。测试分子被引入第一腔室,无论使用哪种腔室配置。在一些实施例中,腔室为转移系统。可用于本公开的方法、测定、测定系统或试剂盒的合适转移系统包括但不限于:Boyden腔室、细胞迁移测定、细胞侵袭测定、微流体迁移装置、体外划痕测定(in vitro scratch assay)、细胞外基质(ECM)蛋白测定。本公开的方法可以利用多种测定平台(例如,12孔、24孔或96孔多孔阵列)来进行,包括“通用”转移平台。测定平台的非限制性实例包括
示例性实施例
E1.一种方法,其包含确定多个分子的再循环,其中该确定包含:
将该多个分子引入第一腔室中,其中:
该第一腔室通过细胞层与第二腔室分隔,并且
该第一腔室和该第二腔室包含水溶液;
在该第一腔室中孵育该多个分子;
更换该第一腔室和该第二腔室两者中的该水溶液;以及
测量从该细胞层释放至该第一腔室中的该多个分子的量;
其中该水溶液处于生理pH,并且该细胞层包含表达介导分子输运的受体的细胞。
E2.根据E1所述的方法,其中多个分子为多个单一分子。
E3.根据E1所述的方法,其中多个分子为多个不同分子。
E4.根据E1至E3中任一项所述的方法,其中该细胞层包含细胞单层。
E5.根据E1至E4中任一项所述的方法,其中介导分子输运的受体为介导分子的细胞内输运的受体。
E6.根据E1至E4中任一项所述的方法,其中介导分子输运的该受体为转铁蛋白受体、Fc受体、巨蛋白或立方蛋白。
E7.根据E1至E6中任一项所述的方法,其中介导分子输运的该受体为新生儿Fc受体(FcRn)。
E8.根据E1至E7中任一项所述的方法,其中该细胞为真核细胞或哺乳动物细胞。
E9.根据E1至E7中任一项所述的方法,其中该细胞为马丁达比犬肾(MDCK)细胞。
E10.根据E1至E9中任一项所述的方法,其中测量从细胞层释放的多个分子的量包括使用酶联免疫吸附测定(ELISA)、液体闪烁计数(LSC)、定量PCR、荧光读取器系统或质谱法。
E11.根据E1至E10中任一项所述的方法,其中多个分子在第一腔室中孵育约1小时至约48小时。
E12.根据E1至E11中任一项所述的方法,其中多个分子在第一腔室中孵育约1小时至约30小时。
E13.根据E1至E12中任一项所述的方法,其中更换水溶液包括清洗第一腔室。
E14.根据E1至E13中任一项所述的方法,其进一步包括在测量之前,用更换水溶液孵育第一腔室和第二腔室。
E15.根据E14所述的方法,在测量之前,用更换水溶液孵育第一腔室和第二腔室1小时至6小时。
E16.根据E1至E15中任一项所述的方法,其中孵育在约35℃至约39℃之间的温度下进行。
E17.根据E1至E15中任一项所述的方法,其中多个分子为含有Fc的分子。
E18.根据E17所述的方法,其中含有Fc的分子为受体Fc融合分子。
E19.根据E1至E15中任一项所述的方法,其中多个分子为抗体。
E20.根据E19所述的方法,其中该抗体为单克隆抗体。
E21.根据E20所述的方法,其中抗体为抗IgE抗体、抗VEGF抗体、抗整合素抗体、抗IL-6抗体、抗TNFa抗体、抗BACE1抗体或抗gD抗体。
E22.根据E20所述的方法,其中该抗体为奥马珠单抗、贝伐珠单抗、托珠单抗、抗BACE1 WT、抗BACE1变体YEY、抗BACE1变体YQAY、抗BACE1变体YPY、抗BACE1变体YY、抗BACE1变体YLY1(Q6)或抗BACE1变体YIY(T3)。
E23.根据E7所述的方法,其中FcRn选自由人类RcRn、小鼠FcRn、大鼠FcRn和食蟹猕猴FcRn组成的组。
E24.根据E1至E23中任一项所述的方法,其中该生理pH为约7.4。
E25.根据E1至E24中任一项所述的方法,其进一步包括测量多个分子跨细胞层的转胞吞作用。
E26.根据E25所述的方法,其中测量转胞吞作用包括:
在已更换该第一腔室和该第二腔室两者中的该水溶液后,测量该第二腔室中的该多个分子的量。
E27.根据E1至E26中任一项所述的方法,其包括在试剂的存在下在第一腔室中孵育多个分子,以及确定试剂是否影响多个分子的再循环。
E28.根据E27所述的方法,其中该试剂为小分子或多肽。
E29.一种确定多个分子的组织渗透率的方法,其包含:
a)将该多个分子引入第一腔室中,其中该第一腔室通过细胞层与第二腔室分隔,并且该第一腔室和该第二腔室包含水溶液;
其中该水溶液处于生理pH,并且该细胞层包含表达介导分子输运的受体的细胞;
b)测量从该第一腔室再循环至该细胞层中并且返回至该第一腔室的该多个分子的量;
c)测量从该第一腔室转胞吞至该第二腔室的该多个分子的量;以及
d)基于转胞吞分子与再循环分子的比率,确定该多个分子的该组织渗透率。
E30.根据E29所述的方法,其中测量经再循环的多个分子包括:
在将多个分子引入第一腔室后,在第一腔室中孵育多个分子;
更换该第一腔室和该第二腔室两者中的该水溶液;以及
测量从该细胞层释放至该第一腔室中的该多个分子的量。
E31.根据E29或E30所述的方法,其中测量经转胞吞的多个分子包括:
在将多个分子引入第一腔室后,在第一腔室中孵育多个分子;
更换该第一腔室和该第二腔室两者中的该水溶液;以及
测量从该细胞层释放至该第二腔室中的该多个分子的量。
E32.根据E30或E31所述的方法,其中多个分子在第一腔室中孵育至少约1小时至约48小时。
E33.根据E30或E31所述的方法,其中多个分子在第一腔室中孵育约1小时至约30小时。
E34.根据E30至E33中任一项所述的方法,其中更换水溶液包括清洗第一腔室。
E35.根据E29至E34中任一项所述的方法,其进一步包括在测量之前通过水溶液孵育第一腔室和第二腔室。
E36.根据E35所述的方法,在测量之前,用更换水溶液孵育第一腔室和第二腔室1小时至6小时。
E37.根据E29至E36中任一项所述的方法,其中孵育在约35℃至约39℃之间的温度下进行。
E38.根据E29至E36中任一项所述的方法,其中多个分子为多个单一分子。
E39.根据E29至E36中任一项所述的方法,其中多个分子为多个不同分子。
E40.根据E29至E39中任一项所述的方法,其中该细胞层包含细胞单层。
E41.根据E29至E40中任一项所述的方法,其中介导分子输运的受体为介导分子的细胞内输运的受体。
E42.根据E29至E41中任一项所述的方法,其中介导分子输运的该受体为转铁蛋白受体、Fc受体、巨蛋白或立方蛋白。
E43.根据E29至E42中任一项所述的方法,其中介导分子输运的该受体为新生儿Fc受体(FcRn)。
E44.根据E29至E43中任一项所述的方法,其中该细胞为真核细胞或哺乳动物细胞。
E45.根据E29至E44中任一项所述的方法,其中该细胞为马丁达比犬肾(MDCK)细胞。
E46.根据E29至E45中任一项所述的方法,其中测量经再循环的多个分子的量和测量经转胞吞的多个分子的量独立地包括使用酶联免疫吸附测定(ELISA)、液体闪烁计数(LSC)、定量PCR、荧光读取器系统、质谱法或其任意组合。
E47.根据E29至E46中任一项所述的方法,其中多个分子为含有Fc的分子。
E48.根据E47所述的方法,其中含有Fc的分子为受体Fc融合分子。
E49.根据E29至E48中任一项所述的方法,其中多个分子为抗体。
E50.根据E47所述的方法,其中该抗体为单克隆抗体。
E51.根据E50所述的方法,其中抗体为抗IgE抗体、抗VEGF抗体、抗整合素抗体、抗IL-6抗体、抗TNFa抗体、抗BACE1抗体或抗gD抗体。
E52.根据E50所述的方法,其中该抗体为奥马珠单抗、贝伐珠单抗、托珠单抗、抗BACE1 WT、抗BACE1变体YEY、抗BACE1变体YQAY、抗BACE1变体YPY、抗BACE1变体YY、抗BACE1变体YLY1(Q6)或抗BACE1变体YIY(T3)。
E53.根据E29至E52中任一项所述的方法,其中该生理pH为约7.4。
E54.根据E29至E53中任一项所述的方法,其中组织渗透率为脑渗透率。
E55.根据E29至E54中任一项所述的方法,其包括在试剂的存在下在第一腔室中孵育多个分子,以及确定试剂是否影响多个分子的组织渗透率。
E56.根据E55所述的方法,其中该试剂为小分子。
E57.一种确定多个分子的药代动力学(PK)参数的方法,其包括:
a)将该多个分子引入第一腔室中,其中该第一腔室通过细胞层与第二腔室分隔,并且该第一腔室和该第二腔室包含水溶液;
其中该水溶液处于生理pH,并且该细胞层包含表达介导分子输运的受体的细胞;
b)测量从该第一腔室再循环至该细胞层中并且返回至该第一腔室的该多个分子的量;以及
c)基于经再循环的该多个分子的量,确定该PK参数。
E58.根据E57所述的方法,其中测量经再循环的多个分子包括:
在将多个分子引入第一腔室后,在第一腔室中孵育多个分子;
更换该第一腔室和该第二腔室两者中的该水溶液;以及
测量从该细胞层释放至该第一腔室中的该多个分子的量。
E59.根据E58所述的方法,其中多个分子在第一腔室中孵育至少约1小时至约48小时。
E60.根据E58所述的方法,其中多个分子在第一腔室中孵育约1小时至约30小时。
E61.根据E58至E60中任一项所述的方法,其中更换水溶液包括清洗第一腔室。
E62.根据E54至E57中任一项所述的方法,其进一步包括在测量之前通过水溶液孵育第一腔室和第二腔室。
E63.根据E62所述的方法,在测量之前,用更换水溶液孵育第一腔室和第二腔室至少约1小时至约6小时。
E64.根据E58至E63中任一项所述的方法,其中孵育在约35℃至约39℃之间的温度下进行。
E65.根据E57至E63中任一项所述的方法,其中多个分子为多个单一分子。
E66.根据E57至E64中任一项所述的方法,其中多个分子为多个不同分子。
E67.根据E57至E66中任一项所述的方法,其中该细胞层包括细胞单层。
E68.根据E57至E67中任一项所述的方法,其中该细胞表达异源FcRn。
E69.根据E57至E68中任一项所述的方法,其中该细胞为马丁达比犬肾(MDCK)细胞。
E70.根据E57至E68中任一项所述的方法,其中测量经再循环的多个分子的量包括使用酶联免疫吸附测定(ELISA)、液体闪烁计数(LSC)、定量PCR、荧光读取器系统或质谱法。
E71.根据权利要求57至70中任一项所述的方法,其中多个分子为含有Fc的分子。
E72.根据E71所述的方法,其中含有Fc的分子为受体Fc融合分子。
E73.根据E57至E72中任一项所述的方法,其中多个分子为抗体。
E74.根据E73所述的方法,其中该抗体为单克隆抗体。
E75.根据E74所述的方法,其中抗体为抗IgE抗体、抗VEGF抗体、抗整合素抗体、抗IL-6抗体、抗TNFa抗体、抗BACE1抗体或抗gD抗体。
E76.根据E74所述的方法,其中该抗体为奥马珠单抗、贝伐珠单抗、托珠单抗、抗BACE1 WT、抗BACE1变体YEY、抗BACE1变体YQAY、抗BACE1变体YPY、抗BACE1变体YY、抗BACE1变体YLY1(Q6)或抗BACE1变体YIY(T3)。
E77.根据E57至E76中任一项所述的方法,其中该生理pH为约7.4。
E78.根据E57至E77中任一项所述的方法,其中该PK参数为多个分子的体内清除率、分布体积、曲线下面积(AUC)或体内半衰期的量度。
E79.根据E57至E78中任一项所述的方法,其包括在试剂的存在下在第一腔室中孵育多个分子,以及确定试剂是否影响多个分子的PK参数。
E80.根据E79所述的方法,其中该试剂为小分子。
E81.一种测定系统,其包含:
a)第一腔室和第二腔室,其中每一腔室包含处于生理pH的水溶液;
b)细胞层,该细胞层将该第一腔室和该第二腔室分隔,其中该细胞层可介导分子从该第一腔室至该细胞层中并且返回至该第一腔室中的再循环;
c)用于检测该第一腔室中的分子的存在的检测器;
其中该测定系统配置成确定多个分子的再循环;其中该确定包括:
将该多个分子引入该第一腔室中;
在该第一腔室中孵育该多个分子;
更换该第一腔室和该第二腔室两者中的该水溶液;以及
测量从该细胞层释放至该第一腔室中的该多个分子的量。
E82.根据E81所述的测定系统,其中:
该测定系统进一步包含用于检测该第二腔室中的分子的存在的检测器;
该细胞层可介导分子从该第一腔室至该第二腔室的转胞吞作用;并且
其中该测定系统配置成确定多个分子跨该细胞层的该转胞吞作用,其中确定转胞吞作用包含在已更换该水溶液后,测量该第二腔室中的该多个分子的量。
E83.根据E81或E82所述的测定系统,其中第一腔室和第二腔室为96孔转运孔板的组件。
E84.一种试剂盒,其包括根据E81至E83中任一项所述的测定系统,以及使用说明书。
实例
以下实例仅为对本文所公开的主题的说明,并且不应被视为以任何方式作为限制。
材料和方法
表达人类FcRn的MDCK细胞系
如前所述,生成了稳定表达人类FcRn重链(FCGRT)和轻链(B2M)的克隆细胞系(Chung,S.等人,2019,MAbs,11(5),942-955)。简而言之,将两种基因FCGRT(UniProtKB–P55899,FCGRTN_HUMAN)和B2M(UniProtKB–P61769,B2MG_HUMAN)的cDNA通过修饰的pPRK质粒引入MDCK细胞,然后通过嘌呤霉素选择并通过荧光激活细胞分选(FACS)进行分选。基于FCGRT和B2M蛋白的显著表达水平选择用于测定的最终克隆。将MDCK-hFcRn细胞保持在Dulbecco改良的最小必需培养基(DMEM)中,并添加GlutaMAX(Thermo Fisher Scientific,Waltham,MA),其辅助添加有10% FBS(HyClone,Logan,UT)、5μg/mL嘌呤霉素和1%青霉素-链霉素(Thermo Fisher Scientific)。将细胞在37℃和5% CO
测试分子
测试分子包括一组人源化IgG1抗体(一组在人体研究中具有记录或公布的清除率值的七种治疗性抗体)以及抗单纯疱疹病毒糖蛋白D野生型(抗gD WT),其两种变体具有改变Fc-FcRn结合亲和力的工程化突变(抗-gD HAHQ和抗-gD YTE)。在7种治疗性抗体中,5种为上市药品,2种(维多珠单抗和阿达木单抗)购自厂家。其余治疗性抗体(贝伐珠单抗、奥马珠单抗、托珠单抗、mAbX和mAbY)以及抗gD变体在基因泰克公司(加利福尼亚州南旧金山)的工程化中国仓鼠卵巢(CHO)细胞中产生。
再循环测定
将MDCK-hFcRn细胞以6X10
取自内腔室的样品表示再循环成分,取自外腔室的样品表示转胞吞作用成分。将样品冷冻在-70℃以使用ELISA进行定量。
可以使用该过程的变形形式。例如,任选地,对于再循环成分(内腔室)的洗涤过程,可以使用电子移液器的最低速度来对在过滤器上孵育的细胞层的干扰/损坏最小化。任选地,免疫测定的两位数定量下限可用于确保敏感度足够严格以检测抗体的低浓度。任选地,细胞可以在达到超过95%的存活率的条件下孵育。任选地,可以依据所使用的细胞的类型和/或所评估的测试分子来调整细胞培养基。任选地,可以使用大转运孔板(例如,12孔或24孔)。可以进行额外的变化。
ELISA方法
使用作为捕获分子的生物素化小鼠抗人IgG-Fc(生物素-R10Z,基因泰克制备)、作为检测分子的辣根过氧化物酶(HRP)缀合的山羊抗人Fab(ImmunoResearch Laboratories,West Grove,PA)以及用于显色的3,3',5,5'-四甲基联苯胺(TMB)溶液(Kirkegaard&PerryLaboratories,Gaithersburg,MD)的半同源桥接酶联免疫吸附测定(ELISA),其用于评估样品。具体地,将标准品、对照品和样品在细胞培养基中稀释至其最终浓度,并在测定稀释剂(PBS/0.5% BSA/0.05%聚山梨醇酯20/0.05% ProClin 300,pH 7.4±0.1)中制备其他试剂。连续稀释每个治疗分子标准品从4ng/mL至31.25pg/mL(孔内浓度)。对于该测定,将60μL/孔的经稀释的标准品、对照品或样品在环境温度下通过60μL/孔的1μg/mL生物素-R10Z在密封96孔聚丙烯板中轻轻搅拌孵育过夜。过夜孵育后,将100μL/孔的混合物添加到链霉亲和素包被和预封闭的板(Roche Diagnostics Corporation,Indianapolis,IN)。将该板密封并在环境温度下搅拌孵育1小时。每次循环用400μL/孔的洗涤缓冲剂(PBS/0.05%聚山梨醇酯20,pH7.34)将该板洗涤4次。接下来,添加100μL/孔的0.1μg/mL HRP缀合的山羊抗人抗体,将该板密封并在环境温度下孵育1小时。每次循环用300μL/孔的洗涤缓冲剂洗涤该板4次后,加入100μL/孔的过氧化物酶底物溶液B和TMB过氧化物酶底物混合物(Kirkegaard&Perry Laboratories,Gaithersburg,MD)并将该板孵育15至20分钟以进行显色。为了停止显色,向每个孔中加入100μL的1M H
实例1:再循环测定的开发
使用经过工程化以表达人类FcRn重链(FCGRT)和轻链(B2M)的克隆MDCK细胞系(MDCK-hFcRn)来开发FcRn依赖性再循环测定。表达水平、亚细胞共定位和功能读数先前已得到说明,指示MDCK细胞系中的功能性人类FcRn(Chung,S.等人,2019,MAbs,11(5),942-955)。再循环测定是在脉冲追踪实验过程中设计的(图2),并且是在允许细胞更完全的顶-底侧极化的转移培养系统中设计的。将MDCK-hFcRn细胞接种到96孔转运孔板中并培养三天直至汇合。对于脉冲步骤,将抗体添加到内腔室并孵育两小时,以提供时间使抗体被细胞内化并在细胞内途径之间分布和达到稳态(再循环、转胞吞作用和降解)。在清洗内腔室和外腔室以清除现有或经转胞吞的抗体后,将新鲜培养基添加到两个腔室中并将细胞孵育4小时。在该追踪步骤中,可能有三种可能结果:细胞内的抗体要么被再循环回到内腔室中,要么经转胞吞进入外腔室,要么在细胞内降解。出现在内腔室中的抗体表示经再循环的分子。因此,收集内腔室溶液用于分析。任何经转胞吞进入外腔室的抗体都被排除在样品之外,避免FcRn介导的转胞吞作用对再循环测定造成任何污染。在每个实验结束时评估单层的完整性,并从分析中排除来自受损单层的数据。
由于在96孔测定形式下从细胞中释放的经再循环的抗体的数量很小,因此开发了一种敏感人类IgG特异性酶联免疫吸附测定(ELISA)。该夹心ELISA使用了生物素化小鼠抗人IgG-Fc作为捕获物,HRP缀合的山羊抗人Fab作为检测物,以及用于显色的TMB溶液(图3A),定量下限(LLOQ)达到50pg/mL,这允许对再循环输出量的亚纳摩尔浓度进行定量(图3B)。
实例2:人源化IgG1抗体的再循环输出量很大程度上依赖于表达FcRn的细胞中FcRn介导的机制
为了说明再循环测定中FcRn介导的机制的参与,将人源化IgG1抗体(抗单纯疱疹病毒糖蛋白D(抗gD)野生型(WT))与携带改变Fc-FcRn结合亲和力的Fc突变的两种变体进行比较。其中一种变体,抗gD HAHQ,携带消除FcRn结合的H310A/H435Q突变,而另一变体,抗gDYTE,携带增强FcRn结合的突变M252Y/S254T/T256E。抗gD HAHQ的再循环输出量为0.6ng/mL,显著低于抗gD WT(1.2ng/mL),而抗gD YTE的再循环输出量提高(1.9ng/mL)(图4)。这些结果表明,该系统中循环输出量所反映的主要机制由FcRn介导,并支持使用该测定来评估FcRn介导的IgG稳态。
接下来,通过使用一组常规人源化治疗性抗体(包括奥马珠单抗、贝伐珠单抗、维多珠单抗和托珠单抗)评估再循环测量的动力学。在追踪步骤中的不同时间点(从20分钟到4小时)采集再循环样品。对于每个单独分子,观察到再循环的累积增加,在20分钟时再循环输出量最低,在4小时处输出量最高(图5A)。三种经评估的抗体呈现大约为0.4至0.5ng/ml的最大再循环量,而托珠单抗具有更高的再循环值,4小时的时候达到1.09ng/ml。尽管四种分子之间的再循环输出量存在差异,但再循环的动力学相似,在整个追踪步骤的时间过程中几乎没有变化(图5B;再循环输出量被归一化为同一分子的4小时数据点;数据列于表1B中)。在每个时间点进一步检查了四种分子的再循环输出量的排序,并归一化为贝伐珠单抗的再循环输出量。四个时间点的排序和归一化再循环输出量都相似(表1A,归一化至贝伐珠单抗),表明无论追踪时间如何,再循环输出量的相关性都一致。每个分子在四个时间点(20、30、60和240分钟)的变异系数(CV)小于20%,表明具有不同绝对再循环值的抗体的相对再循环输出量在4-小时追踪期间一致。相应地,选择4-小时脉冲步骤作为该系统的标准测定过程,因为更高的再循环输出量使定量更可信,并且决定使用贝伐珠单抗作为内部对照品,以对通过其他测试分子测量的再循环输出量进行归一化。
表1A.在每个时间点处归一化至贝伐珠单抗的再循环输出量。
表1B.对于每种抗体,更早时间点处的平均再循环输出量归一化至在240分钟时的最大值。每个时间点处计算四种抗体的经归一化的输出量的均值和SD。
实例3:食蟹猕猴中转胞吞作用/再循环(T/R)比率与体内脑血清比率的相关性
在转胞吞/再循环双重测定中测试了一组7种抗BACE1变体,包括野生型(WT)分子和六种变体。WO2020/132230A2中进一步描述了抗BACE1抗体。六种变体在其Fc区携带突变,其在中性pH下显著增强对FcRn的结合亲和力,pH 7.4下Kd降低了13.3-78.1倍(表1)。对FcRn的更高结合亲和力将导致mAb受更多保护,引导mAb更多地朝向FcRn介导的再循环和转胞吞途径。与WT分子相比,pH 7.4变体的再循环和转胞吞输出量两者均显示出显著增加。该发现可能归因于通过FcRn受体介导的吸收针对pH 7.4变体增强mAb内化。此外,在pH7.4变体中,转胞吞作用和再循环之间的比率显著增加。WT分子的T/R比率为0.026,而pH7.4变体的比率范围为0.074至0.191(表2和图6),表明突变引入了对转胞吞途径的偏向,这可能促进抗体跨细胞层的输运。
表2.
然后分析来自cyno研究的测定输出和体内脑穿透结果之间的潜在相关性(5种分子的可用cyno数据;表3)。单独的转胞吞作用输出或再循环输出与脑血清比率没有显著相关性。然而,T/R比率与脑血清比率呈现很强的相关性(皮尔逊相关系数0.837)。较高的T/R比率指示有利于转胞吞作用的细胞内途径发生偏向,并且与体内较高的脑穿透行为相关(图7)。因此,T/R比率为预测治疗候选的脑穿透能力的有意义的生物学参数。
表3:获得如WO2020/132230A2中所述的五种分子的Cyno数据
实例3:体外再循环输出量与人体内mAb的体内清除率的相关性
测试了七种治疗性抗体,包括五种已上市药物和两种先前正在开发的药物,并评估其与人体中体内清除率的潜在相关性。该七种分子为IgG1/κ同型的人源化抗体,并且反映了多种特性,包括作用机制、靶标特性和施用途径,但没有一种分子携带用于修饰PK特性或FcRn相互作用的Fc突变。根据药物的处方信息和以前的出版物,清除率值范围为2.2至8.5mL/天/kg。已提出类似抗体同型之间观察到的非特异性清除率差异是由分子特性(诸如pI、电荷或疏水性)引起(Hotzel,I.等人,(2012),MAbs,4(6),753-760)。使用已确立的基于序列的算法,我们计算了分子参数,包括(i)pI值,(ii)pH5.5下的净Fv电荷,以及(iii)CDRL1、L3、H2和H3上疏水性指数值的总和(HIsum)(Sharma,V.K.等人,(2014),PNAS,111(52),18601-18606)。已表明,这些参数的极值指示抗体具有更快的清除速率,然而,与先前的发现一致,没有观察到这些参数与清除率之间的明显相关性趋势(图8A至图8C;表4)。为了探索再循环与清除率之间的相关性,在再循环测定中评估了七种分子,以获得对FcRn介导的再循环过程的定量测量。通过返回内腔室的抗体的浓度测量的每种分子的再循环输出量被归一化至在同一96孔转运孔板上作为对照品运行的贝伐珠单抗的再循环值。表4示出了这些分子的再循环测定的结果,以及它们的所公布的在人体中的清除率。所有七种分子都表现出可测量的再循环输出量,清除率值显示更快速率的分子表现出更高的再循环输出量。示出了再循环输出量与人体中的清除率呈现强正相关性(对于再循环,R
表4.经评估的抗体的归一化再循环输出量和计算出的PI、Fv和HIsum
iv-静脉;sc-皮下
七种经评估的抗体,每一种都具有常规Fc区,无论Fab区的不同特性如何,都说明了人体中的再循环输出量与清除率之间存在显著的相关性。具有相同Fc区的IgG的Pk特性可能有很大差异,这归因于Fab臂的Fv电荷,其可能会影响与FcRn的相互作用,并可能影响内化过程中的液相胞饮作用。在该研究中,针对每个分子在4小时处归一化至最大值后,经测试的四种人源化治疗性抗体(奥马珠单抗、贝伐珠单抗、维多珠单抗和托珠单抗)之间的再循环动力学曲线几乎没有变化。尽管托珠单抗表现出更高的再循环输出值(在4小时处为其他三种抗体的约两倍),但再循环的速率(每个时间点有倾斜)相同。不受理论束缚,相似再循环动力学可表明,对于具有常规Fc区的mAb,穿过再循环途径的FcRn介导的输运可能相似,因此所测得的再循环输出量的差异可能由FcRn介导的输运的上游机制造成。该四种抗体在pH 6.0下对FcRn具有相当的结合亲和力,但托珠单抗的计算出的PI值和Fv电荷更高。这可以解释托珠单抗的高再循环值和更快的清除速率,因为正电荷可以通过与细胞表面的阴离子硫酸肝素蛋白多糖的静电相互作用来增强非特异性结合。这些相互作用可通过液相胞饮作用增强托珠单抗的内化。先前的工作表明,FcRn无关机制可在调节具有相同Fc但具有不同Fab区的mAb的PK行为中发挥作用。
不受理论束缚,鉴于再循环已被认为是使IgG免于溶酶体降解并将其护送回血液的补救机制,最初预计高再循环输出量可能与清除速率负相关。令人惊讶的是,观察到了相反的结果:更高的再循环输出量对应更快的清除速率。不受理论束缚,清除率与FcRn介导的再循环之间的该正相关可与抗体在每个内化事件期间经历消除机制的部分有关。再循环过程从循环中获取抗体并将它们返回到同一个区室,但不会影响血药浓度的净量,因为它本身是唯一因素。然而,之前已说明,再循环事件可伴随着一小部分抗体的损失,这归因于溶酶体的降解(Grevys等人,2018)。在目前描述的转移培养系统中,转胞吞作用也可以作为引导抗体远离再循环的消除途径。不受理论束缚,推测每次再循环事件的此类损失(由降解和转胞吞作用引起)可能会减少返回循环的再循环量。因此,对于高再循环分子,损失被夸大了,并且其可能有助于更快地降低血药浓度,并更快地测量清除率。有趣的是,对于FcRn结合变体组,观察结果似乎相反,表明Fc工程化抗gD变体的再循环输出量和清除率之间存在负相关趋势。与WT相比,显示较慢清除速率的YTE突变的再循环输出量更高(参见实例2)。不受理论束缚,对FcRn的显著增强结合可能已成为主要的生物学因素,其可能导致保护水平增高并且溶酶体降解减少,这延长了抗体的血清半衰期。为了解释常规和Fc工程化mAb之间的差异,影响PK行为的主要因素可能在两种情形下有所不同,具体取决于分子的设计。因此,在解释该体外系统的结果时,应考虑抗体的生化特性和Fc工程化。
所评估的七种mAb指示,作为没有Fc修饰的mAb的PK特性的预测因子,本文所描述的再循环测定优于使用抗体的pI、电荷或疏水性参数(特别是来自人体中循环的清除率)的其他模型。测定设计使用了三区室体外模型系统(内腔室、细胞和外腔室)来模拟体内情形(血液区室、囊泡内皮细胞和组织区室),并结合了可能影响抗体的细胞代谢的多种生物事件。再循环测定提供了对可能影响抗体的细胞代谢的多种生物因素的整体评估,并且因此与仅考虑单一因素或因素子集的其他已发表测定相比,可以更好地预测一个或多个PK特性,例如非特异性结合、与细胞外基质的结合和FcRn相互作用。
此外,不受理论束缚,两个转移腔室中使用的中性pH可能为成功预测PK特性的关键,因为这在生理学上与抗体在中性pH下在细胞表面被捕获和释放的体内情形更相关。这可以解释其他FcRn介导的基于细胞的测定的有限应用,其中酸性缓冲剂用于将抗体加载到细胞中以利用酸性pH下FcRn结合的增强(Chung等人,(2018),J Immunol Methods,462,101-105;Jaramillo等人,2017,MAbs,9(5),781-791;Sockolosky、JT等人,2012,PNAS,109(40),16095-16100;Ying等人,2015,MAbs,7(5),922-930)。其中一些方法预测了具有增强FcRn结合的Fc工程化分子的清除率或半衰期,但预测常规mAb的PK行为的能力有限,其中FcRn结合的变化更加微小。此外,细胞极化可能被认为是一个重要因素,因为再循环和转胞吞作用都被固有地极化,并且至少部分地在极化内皮细胞顶和底侧表面由独立过程进行(Dickinson等人,1999,J Clin Invest,104(7),903-911;Tzaban、S.等人,2009,J CellBiol,185(4),673-684)。与在常规细胞培养板上进行的其他再循环测定相比,本文所描述的利用转移细胞培养系统的测定可允许更好的极化和再循环与转胞吞成分的分离,这在评估常规mAb时可能更准确(Grevys,A.Nat Commun,9(1)621)。
本文所引用的所有出版物、专利和其他参考文献通过引用整体并入本公开中。
序列表
<110>基因泰克公司
<120>用于预测生物制剂的药代动力学和脑渗透性的体外基于细胞的测定
<130>P36572-WO
<140>
<141>
<150>63/187,750
<151>2021-05-12
<150>63/174,913
<151>2021-04-14
<160>8
<170>PatentIn 版本 3.5
<210>1
<211>342
<212>PRT
<213>智人
<400>1
Ala Glu Ser His Leu Ser Leu Leu Tyr His Leu Thr Ala Val Ser Ser
1 5 1015
Pro Ala Pro Gly Thr Pro Ala Phe Trp Val Ser Gly Trp Leu Gly Pro
202530
Gln Gln Tyr Leu Ser Tyr Asn Ser Leu Arg Gly Glu Ala Glu Pro Cys
354045
Gly Ala Trp Val Trp Glu Asn Gln Val Ser Trp Tyr Trp Glu Lys Glu
505560
Thr Thr Asp Leu Arg Ile Lys Glu Lys Leu Phe Leu Glu Ala Phe Lys
65707580
Ala Leu Gly Gly Lys Gly Pro Tyr Thr Leu Gln Gly Leu Leu Gly Cys
859095
Glu Leu Gly Pro Asp Asn Thr Ser Val Pro Thr Ala Lys Phe Ala Leu
100 105 110
Asn Gly Glu Glu Phe Met Asn Phe Asp Leu Lys Gln Gly Thr Trp Gly
115 120 125
Gly Asp Trp Pro Glu Ala Leu Ala Ile Ser Gln Arg Trp Gln Gln Gln
130 135 140
Asp Lys Ala Ala Asn Lys Glu Leu Thr Phe Leu Leu Phe Ser Cys Pro
145 150 155 160
His Arg Leu Arg Glu His Leu Glu Arg Gly Arg Gly Asn Leu Glu Trp
165 170 175
Lys Glu Pro Pro Ser Met Arg Leu Lys Ala Arg Pro Ser Ser Pro Gly
180 185 190
Phe Ser Val Leu Thr Cys Ser Ala Phe Ser Phe Tyr Pro Pro Glu Leu
195 200 205
Gln Leu Arg Phe Leu Arg Asn Gly Leu Ala Ala Gly Thr Gly Gln Gly
210 215 220
Asp Phe Gly Pro Asn Ser Asp Gly Ser Phe His Ala Ser Ser Ser Leu
225 230 235 240
Thr Val Lys Ser Gly Asp Glu His His Tyr Cys Cys Ile Val Gln His
245 250 255
Ala Gly Leu Ala Gln Pro Leu Arg Val Glu Leu Glu Ser Pro Ala Lys
260 265 270
Ser Ser Val Leu Val Val Gly Ile Val Ile Gly Val Leu Leu Leu Thr
275 280 285
Ala Ala Ala Val Gly Gly Ala Leu Leu Trp Arg Arg Met Arg Ser Gly
290 295 300
Leu Pro Ala Pro Trp Ile Ser Leu Arg Gly Asp Asp Thr Gly Val Leu
305 310 315 320
Leu Pro Thr Pro Gly Glu Ala Gln Asp Ala Asp Leu Lys Asp Val Asn
325 330 335
Val Ile Pro Ala Thr Ala
340
<210>2
<211>119
<212>PRT
<213>智人
<400>2
Met Ser Arg Ser Val Ala Leu Ala Val Leu Ala Leu Leu Ser Leu Ser
1 5 1015
Gly Leu Glu Ala Ile Gln Arg Thr Pro Lys Ile Gln Val Tyr Ser Arg
202530
His Pro Ala Glu Asn Gly Lys Ser Asn Phe Leu Asn Cys Tyr Val Ser
354045
Gly Phe His Pro Ser Asp Ile Glu Val Asp Leu Leu Lys Asn Gly Glu
505560
Arg Ile Glu Lys Val Glu His Ser Asp Leu Ser Phe Ser Lys Asp Trp
65707580
Ser Phe Tyr Leu Leu Tyr Tyr Thr Glu Phe Thr Pro Thr Glu Lys Asp
859095
Glu Tyr Ala Cys Arg Val Asn His Val Thr Leu Ser Gln Pro Lys Ile
100 105 110
Val Lys Trp Asp Arg Asp Met
115
<210>3
<211>344
<212>PRT
<213>小家鼠
<400>3
Ser Glu Thr Arg Pro Pro Leu Met Tyr His Leu Thr Ala Val Ser Asn
1 5 1015
Pro Ser Thr Gly Leu Pro Ser Phe Trp Ala Thr Gly Trp Leu Gly Pro
202530
Gln Gln Tyr Leu Thr Tyr Asn Ser Leu Arg Gln Glu Ala Asp Pro Cys
354045
Gly Ala Trp Met Trp Glu Asn Gln Val Ser Trp Tyr Trp Glu Lys Glu
505560
Thr Thr Asp Leu Lys Ser Lys Glu Gln Leu Phe Leu Glu Ala Leu Lys
65707580
Thr Leu Glu Lys Ile Leu Asn Gly Thr Tyr Thr Leu Gln Gly Leu Leu
859095
Gly Cys Glu Leu Ala Ser Asp Asn Ser Ser Val Pro Thr Ala Val Phe
100 105 110
Ala Leu Asn Gly Glu Glu Phe Met Lys Phe Asn Pro Arg Ile Gly Asn
115 120 125
Trp Thr Gly Glu Trp Pro Glu Thr Glu Ile Val Ala Asn Leu Trp Met
130 135 140
Lys Gln Pro Asp Ala Ala Arg Lys Glu Ser Glu Phe Leu Leu Asn Ser
145 150 155 160
Cys Pro Glu Arg Leu Leu Gly His Leu Glu Arg Gly Arg Arg Asn Leu
165 170 175
Glu Trp Lys Glu Pro Pro Ser Met Arg Leu Lys Ala Arg Pro Gly Asn
180 185 190
Ser Gly Ser Ser Val Leu Thr Cys Ala Ala Phe Ser Phe Tyr Pro Pro
195 200 205
Glu Leu Lys Phe Arg Phe Leu Arg Asn Gly Leu Ala Ser Gly Ser Gly
210 215 220
Asn Cys Ser Thr Gly Pro Asn Gly Asp Gly Ser Phe His Ala Trp Ser
225 230 235 240
Leu Leu Glu Val Lys Arg Gly Asp Glu His His Tyr Gln Cys Gln Val
245 250 255
Glu His Glu Gly Leu Ala Gln Pro Leu Thr Val Asp Leu Asp Ser Ser
260 265 270
Ala Arg Ser Ser Val Pro Val Val Gly Ile Val Leu Gly Leu Leu Leu
275 280 285
Val Val Val Ala Ile Ala Gly Gly Val Leu Leu Trp Gly Arg Met Arg
290 295 300
Ser Gly Leu Pro Ala Pro Trp Leu Ser Leu Ser Gly Asp Asp Ser Gly
305 310 315 320
Asp Leu Leu Pro Gly Gly Asn Leu Pro Pro Glu Ala Glu Pro Gln Gly
325 330 335
Ala Asn Ala Phe Pro Ala Thr Ser
340
<210>4
<211>119
<212>PRT
<213>小家鼠
<400>4
Met Ala Arg Ser Val Thr Leu Val Phe Leu Val Leu Val Ser Leu Thr
1 5 1015
Gly Leu Tyr Ala Ile Gln Lys Thr Pro Gln Ile Gln Val Tyr Ser Arg
202530
His Pro Pro Glu Asn Gly Lys Pro Asn Ile Leu Asn Cys Tyr Val Thr
354045
Gln Phe His Pro Pro His Ile Glu Ile Gln Met Leu Lys Asn Gly Lys
505560
Lys Ile Pro Lys Val Glu Met Ser Asp Met Ser Phe Ser Lys Asp Trp
65707580
Ser Phe Tyr Ile Leu Ala His Thr Glu Phe Thr Pro Thr Glu Thr Asp
859095
Thr Tyr Ala Cys Arg Val Lys His Asp Ser Met Ala Glu Pro Lys Thr
100 105 110
Val Tyr Trp Asp Arg Asp Met
115
<210>5
<211>344
<212>PRT
<213>大鼠
<400>5
Ala Glu Pro Arg Leu Pro Leu Met Tyr His Leu Ala Ala Val Ser Asp
1 5 1015
Leu Ser Thr Gly Leu Pro Ser Phe Trp Ala Thr Gly Trp Leu Gly Ala
202530
Gln Gln Tyr Leu Thr Tyr Asn Asn Leu Arg Gln Glu Ala Asp Pro Cys
354045
Gly Ala Trp Ile Trp Glu Asn Gln Val Ser Trp Tyr Trp Glu Lys Glu
505560
Thr Thr Asp Leu Lys Ser Lys Glu Gln Leu Phe Leu Glu Ala Ile Arg
65707580
Thr Leu Glu Asn Gln Ile Asn Gly Thr Phe Thr Leu Gln Gly Leu Leu
859095
Gly Cys Glu Leu Ala Pro Asp Asn Ser Ser Leu Pro Thr Ala Val Phe
100 105 110
Ala Leu Asn Gly Glu Glu Phe Met Arg Phe Asn Pro Arg Thr Gly Asn
115 120 125
Trp Ser Gly Glu Trp Pro Glu Thr Asp Ile Val Gly Asn Leu Trp Met
130 135 140
Lys Gln Pro Glu Ala Ala Arg Lys Glu Ser Glu Phe Leu Leu Thr Ser
145 150 155 160
Cys Pro Glu Arg Leu Leu Gly His Leu Glu Arg Gly Arg Gln Asn Leu
165 170 175
Glu Trp Lys Glu Pro Pro Ser Met Arg Leu Lys Ala Arg Pro Gly Asn
180 185 190
Ser Gly Ser Ser Val Leu Thr Cys Ala Ala Phe Ser Phe Tyr Pro Pro
195 200 205
Glu Leu Lys Phe Arg Phe Leu Arg Asn Gly Leu Ala Ser Gly Ser Gly
210 215 220
Asn Cys Ser Thr Gly Pro Asn Gly Asp Gly Ser Phe His Ala Trp Ser
225 230 235 240
Leu Leu Glu Val Lys Arg Gly Asp Glu His His Tyr Gln Cys Gln Val
245 250 255
Glu His Glu Gly Leu Ala Gln Pro Leu Thr Val Asp Leu Asp Ser Pro
260 265 270
Ala Arg Ser Ser Val Pro Val Val Gly Ile Ile Leu Gly Leu Leu Leu
275 280 285
Val Val Val Ala Ile Ala Gly Gly Val Leu Leu Trp Asn Arg Met Arg
290 295 300
Ser Gly Leu Pro Ala Pro Trp Leu Ser Leu Ser Gly Asp Asp Ser Gly
305 310 315 320
Asp Leu Leu Pro Gly Gly Asn Leu Pro Pro Glu Ala Glu Pro Gln Gly
325 330 335
Val Asn Ala Phe Pro Ala Thr Ser
340
<210>6
<211>119
<212>PRT
<213>大鼠
<400>6
Met Ala Arg Ser Val Thr Val Ile Phe Leu Val Leu Val Ser Leu Ala
1 5 1015
Val Val Leu Ala Ile Gln Lys Thr Pro Gln Ile Gln Val Tyr Ser Arg
202530
His Pro Pro Glu Asn Gly Lys Pro Asn Phe Leu Asn Cys Tyr Val Ser
354045
Gln Phe His Pro Pro Gln Ile Glu Ile Glu Leu Leu Lys Asn Gly Lys
505560
Lys Ile Pro Asn Ile Glu Met Ser Asp Leu Ser Phe Ser Lys Asp Trp
65707580
Ser Phe Tyr Ile Leu Ala His Thr Glu Phe Thr Pro Thr Glu Thr Asp
859095
Val Tyr Ala Cys Arg Val Lys His Val Thr Leu Lys Glu Pro Lys Thr
100 105 110
Val Thr Trp Asp Arg Asp Met
115
<210>7
<211>342
<212>PRT
<213>食蟹猴
<400>7
Ala Glu Ser His Leu Ser Leu Leu Tyr His Leu Thr Ala Val Ser Ser
1 5 1015
Pro Ala Pro Gly Thr Pro Ala Phe Trp Val Ser Gly Trp Leu Gly Pro
202530
Gln Gln Tyr Leu Ser Tyr Asp Ser Leu Arg Gly Gln Ala Glu Pro Cys
354045
Gly Ala Trp Val Trp Glu Asn Gln Val Ser Trp Tyr Trp Glu Lys Glu
505560
Thr Thr Asp Leu Arg Ile Lys Glu Lys Leu Phe Leu Glu Ala Phe Lys
65707580
Ala Leu Gly Gly Lys Gly Pro Tyr Thr Leu Gln Gly Leu Leu Gly Cys
859095
Glu Leu Ser Pro Asp Asn Thr Ser Val Pro Thr Ala Lys Phe Ala Leu
100 105 110
Asn Gly Glu Glu Phe Met Asn Phe Asp Leu Lys Gln Gly Thr Trp Gly
115 120 125
Gly Asp Trp Pro Glu Ala Leu Ala Ile Ser Gln Arg Trp Gln Gln Gln
130 135 140
Asp Lys Ala Ala Asn Lys Glu Leu Thr Phe Leu Leu Phe Ser Cys Pro
145 150 155 160
His Arg Leu Arg Glu His Leu Glu Arg Gly Arg Gly Asn Leu Glu Trp
165 170 175
Lys Glu Pro Pro Ser Met Arg Leu Lys Ala Arg Pro Gly Asn Pro Gly
180 185 190
Phe Ser Val Leu Thr Cys Ser Ala Phe Ser Phe Tyr Pro Pro Glu Leu
195 200 205
Gln Leu Arg Phe Leu Arg Asn Gly Met Ala Ala Gly Thr Gly Gln Gly
210 215 220
Asp Phe Gly Pro Asn Ser Asp Gly Ser Phe His Ala Ser Ser Ser Leu
225 230 235 240
Thr Val Lys Ser Gly Asp Glu His His Tyr Cys Cys Ile Val Gln His
245 250 255
Ala Gly Leu Ala Gln Pro Leu Arg Val Glu Leu Glu Thr Pro Ala Lys
260 265 270
Ser Ser Val Leu Val Val Gly Ile Val Ile Gly Val Leu Leu Leu Thr
275 280 285
Ala Ala Ala Val Gly Gly Ala Leu Leu Trp Arg Arg Met Arg Ser Gly
290 295 300
Leu Pro Ala Pro Trp Ile Ser Leu Arg Gly Asp Asp Thr Gly Ser Leu
305 310 315 320
Leu Pro Thr Pro Gly Glu Ala Gln Asp Ala Asp Ser Lys Asp Ile Asn
325 330 335
Val Ile Pro Ala Thr Ala
340
<210>8
<211>119
<212>PRT
<213>食蟹猴
<400>8
Met Ser Pro Ser Val Ala Leu Ala Val Leu Ala Leu Leu Ser Pro Ser
1 5 1015
Gly Leu Glu Ala Ile Gln Arg Thr Pro Lys Ile Gln Val Tyr Ser Arg
202530
His Pro Pro Glu Asn Gly Lys Pro Asn Phe Leu Asn Cys Tyr Val Ser
354045
Gly Phe His Pro Ser Asp Ile Glu Val Asp Leu Leu Lys Asn Gly Glu
505560
Lys Met Gly Lys Val Glu His Ser Asp Leu Ser Phe Ser Lys Asp Trp
65707580
Ser Phe Tyr Leu Leu Tyr Tyr Thr Glu Phe Thr Pro Asn Glu Lys Asp
859095
Glu Tyr Ala Cys Arg Val Asn His Val Thr Leu Ser Gly Pro Arg Thr
100 105 110
Val Lys Trp Asp Arg Asp Met
115
- 阿西替尼的药代动力学判定方法和基于阿西替尼的药代动力学预测阿西替尼治疗效果的方法
- 一种基于肠芯片的体外模拟药代动力学特征的体系及应用
