一种整合素α6靶向荧光分子探针及其使用
文献发布时间:2024-04-18 20:01:23
技术领域
本发明涉及靶向性荧光探针技术领域,尤其涉及一种整合素α6靶向荧光分子探针及其使用。
背景技术
整合素是一种跨膜的异质二聚体,它由两个非共价结合的跨膜亚基(α亚基和β亚基)组成。细胞外球形结构域可以与细胞外基质蛋白结合,细胞内的尾部则与肌动蛋白相连。具有联系细胞内外结构的作用。能够作为靶向探针或靶向性治疗药物的靶点,在临床肿瘤成像和治疗中已有应用。整合素α6是整合素的一种α亚基,在细胞中可分别与整合素β1亚基和整合素β4亚基组成整合素α6β1或α6β4。在肝癌、胰腺癌、乳腺癌、黑色素瘤等多种肿瘤细胞表面高表达,与肿瘤发生、发展、侵袭、转移等行为密切相关。此外,相关文献表明,整合素α6表达水平高的肿瘤患者,其生存时间显著较短。因此,整合素α6是肿瘤进展和患者预后的重要标志物,对于肿瘤的诊断具有重要意义。
中国专利CN113817021A公开了一种整合素α6靶向多肽及其应用,其基序为RWYD,对整合素α6具有更强的亲和力,平衡解离常数KD可达到nM级别。且无生物毒性,在体内稳定且分布合理。可作为靶向配体用于荧光分子探针的合成。
但是仍然存在较低的肿瘤信背比,特异性低的问题,为了更高的效果连接PEG形成二倍体或多倍体也增加了合成的难度和结构的复杂性。
发明内容
本申请实施例通过提供一种整合素α6靶向荧光分子探针及其使用,解决了现有技术中较低的肿瘤信背比,特异性低的问题,实现了一种信背比,高特异性的荧光探针。
本申请的一种整合素α6靶向荧光分子探针,其基序为RWYD-Cy7;
进一步的,是由整合素α6靶向性多肽RWYD和荧光分子Cy7脱水缩合而成。
进一步的,具体制备过程为:(1)脱水缩合反应:将sulfo Cy7-SE与RWYD多肽溶于PBS缓冲溶液中,通过脱水缩合反应得到含有RWYD-Cy7荧光分子探针的混合物;(2)纯化:将混合物经柱层析纯化后得到荧光分子探针RWYD-Cy7。
进一步的,所述探针利用产生1000-1700nm谱段的NIR-II荧光进行成像。
进一步的,一种整合素α6靶向荧光分子探针肝癌术中在体荧光成像和手术导航和术中获取组织的离体快速病理染色应用
本申请实施例中提供的一个或多个技术方案,至少具有如下技术效果或优点:
其一,本发明提供了一种靶向整合素α6的靶向性NIR-II荧光分子探针。利用对整合素α6具有高亲和力的多肽RWYD,和具有NIR-II荧光信号的小分子荧光染料Cy7,构建能够高特异性靶向肝癌肿瘤细胞表面整合素α6的NIR-II荧光分子探针,且无生物毒性。探针在体内分布稳定且分布合理,能够实现肿瘤在体和离体水平的NIR-II荧光分子成像,实时检测肿瘤整合素α6表达水平。进一步能够作为肿瘤术中NIR-II荧光成像和NIR-II荧光手术导航的荧光分子探针。
其二,本发明的NIR-II荧光分子探针RD-Cy7通过在中性缓冲液中进行温和的脱水缩合反应即可实现,制备工艺较为简单,成本较低。
其三,Cy7是一种小分子花菁类染料,在NIR-II具有荧光拖尾,且不与正常肝脏细胞结合,由此两种分子反应合成的RD-Cy7荧光分子探针具有较高肿瘤信背比,且穿透深度更高,能够辅助肝癌肿瘤的全面精准切除。
以下将结合实施例对本发明的构思及产生的技术效果进行清楚、完整地描述,以充分地理解本发明的目的、特征和效果。显然,所描述的实施例只是本发明的一部分实施例,而不是全部实施例,基于本发明的实施例,本领域的技术人员在不付出创造性劳动的前提下所获得的其他实施例,均属于本发明保护的范围。
附图说明
图1为本发明的整合素α6的肿瘤细胞的靶向性检测WB曝光结果;
图2为共聚焦实验结果图;
图3为RD-Cy7荧光分子探针对肝癌原位模型肿瘤NIR-II荧光成像结果;
图4为图3结果的定量分析折线统计图;
图5为肝癌皮下/原位模型RD-Cy7荧光分子探针特异性检测结果;
图6为竞争组探针组上肿瘤与肝脏的荧光图;
图7为竞争组探针组上肿瘤与组织的荧光图;
图8为图5的量化柱状图;
图9为图6的量化柱状图;
图10为探针组肿瘤与肝脏对比图;
图11为竞争组肿瘤与肝脏对比图;
图12为离体组织成像组图。
其中:
图1中:1、LO2人肝细胞;2、HepG2人肝癌细胞;3、BEL-7402人肝癌细胞;4、Huh7人肝癌细胞;5、MHCC-97H人肝癌细胞;6、HCCLM3人肝癌细胞;7、LX2人肝星状细胞;
图2中:a为DAPI染色细胞核分布图;b为探针分布图;c为细胞核和探针共定位图;
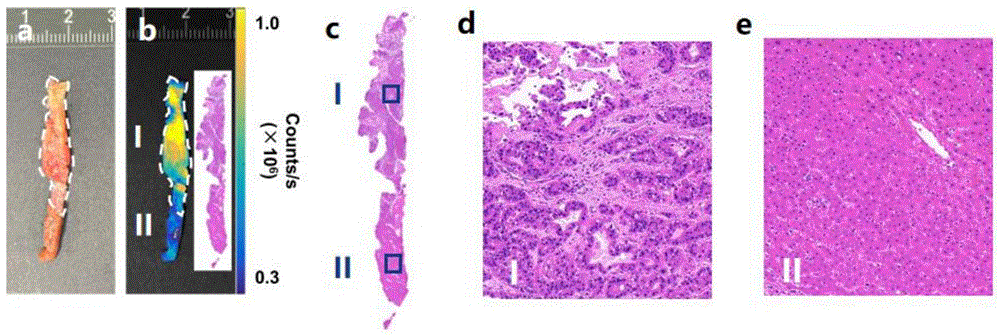
图12中:a为离体组织图;b为离体组织荧光图与离体组织染色图对比;c为离体组织染色图;d为c图中Ⅰ处放大图;e为Ⅱ处放大图。
具体实施方式
为了便于理解本发明,下面将参照相关附图对本申请进行更全面的描述;附图中给出了本发明的较佳实施方式,但是,本发明可以以许多不同的形式来实现,并不限于本文所描述的实施方式;相反地,提供这些实施方式的目的是使对本发明的公开内容理解的更加透彻全面。
一种整合素α6靶向荧光分子探针的制备方法包括以下步骤:
(1)脱水缩合反应:将sulfo Cy7-SE与RWYD多肽在常温条件下溶于中性ph6.8-7的PBS缓冲溶液中,通过脱水缩合反应得到含有RWYD-Cy7荧光分子探针的混合物;
(2)纯化:将混合物经柱层析纯化后得到荧光分子探针RWYD-Cy7,以下简称RD-Cy7。
一种整合素α6靶向荧光分子探针在肝癌术中在体荧光成像和手术导航应用。
除非另有定义,本文所应用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同;本文中在本发明的说明书中所应用的术语只是为了描述具体的实施方式的目的,不是旨在于限制本发明;本文所应用的术语“和/或”包括一个或多个相关的所列项目的任意的和所有的组合。
实施例一
整合素α6对于肿瘤细胞的靶向性检测;
通过蛋白质印迹(Western Blot,WB)检测人肝癌细胞系HCCLM3、Huh-7、Bel7402、Hep3B等和人正常肝脏细胞LO2的整合素α6表达量。选择整合素α6高表达的HCCLM3细胞系进行细胞水平的探针靶向性检测,具体操作如下:
铺板:将HCCLM3培养至对数生长期,均匀铺在共焦显微镜(confocal)皿中过夜,待细胞生长至占皿底90%时,开始实验。
冲洗:弃去confocal皿中的培养基,用PBS冲洗,重复3次。
孵育:用PBS作为溶剂配置探针溶液(10μg/ml),加入confocal皿中(1ml),细胞孵箱中培养2h(37℃,5%CO2,避光)。
冲洗:弃去confocal皿中的探针溶液,加入PBS,confocal皿置于避光容器,摇床冲洗5min,弃去PBS,重复3次。
固定:confocal皿中加入多聚甲醛(4%,1ml),避光孵育10min。
冲洗:弃去confocal皿中的多聚甲醛,加入PBS,confocal皿置于避光容器,摇床冲洗5min,弃去PBS,重复3次。
染核:加入DAPI染色试剂(即用型,1ml),避光孵育10min。
冲洗:冲洗:弃去confocal皿中的DAPI染色试剂,加入PBS,confocal皿置于避光容器,摇床冲洗5min,弃去PBS,重复3次。
采集:Thunder imager 3D assay成像,DAPI通道采集细胞核荧光信号,Cy7通道采集探针信号。
处理:将同一视野的DAPI荧光图像和探针荧光图像赋予伪彩并叠加。
从图1和图2可以看出RD-Cy7荧光分子探针对于人肝癌细胞的靶向性较高,远超人肝细胞,其中HCCLM3细胞系表达量最高,探针能结合在细胞膜上,证明整合素α6确实可以作为肝癌进程的标志物。
实施例二
RD-Cy7荧光分子探针对肝癌皮下模型肿瘤近红外二区(the Second near-infrared window,NIR-II)荧光成像;
利用HCCLM3肝癌细胞系和免疫缺陷Balb/c nude品系的小鼠,构建肝癌小鼠皮下模型,并利用RD-Cy7荧光分子探针,结合小动物NIR-II荧光成像设备,开展肝癌皮下模型的NIR-II荧光成像。
模型构建成功后,通过尾静脉向小鼠模型体内注射RD-Cy7荧光分子探针,浓度为0.5mg/ml,体积为100ul。
其中,荧光分子探针溶于PBS溶液中,PBS的ph为6.8-7,溶液温度为37℃。
注射探针后,间隔不同时间(1h、2h、4h、8h、12h、24h、48h)对肿瘤模型小鼠进行全身NIR-II荧光成像。
如图3-4成像结果表明,RD-Cy7荧光分子探针能够特异性的靶向肝癌皮下模型。探针注射后8h,肿瘤开始出现较强的荧光,注射后24h,肿瘤成像对比度达到最佳。且RD-Cy7荧光分子探针除了肾脏和膀胱有少量摄取,其它脏器的背景更低,尤其是肝脏处,其荧光信号更低,说明RD-Cy7荧光分子探针在肝脏组织中的非特异性分布较低,适用于肝癌的荧光分子成像。
实施例三
肝癌皮下/原位模型RD-Cy7荧光分子探针特异性检测
利用HCCLM3肝癌细胞系和免疫缺陷Balb/c nude品系的小鼠,构建肝癌小鼠原位模型,并利用RD-Cy7荧光分子探针,结合小动物NIR-II荧光成像设备,开展肝癌原位模型的NIR-II荧光成像。
模型构建成功后,通过尾静脉向小鼠模型体内注射RD-Cy7荧光分子探针,浓度为0.5mg/ml,体积为100ul。
其中,荧光分子探针溶于PBS溶液中,PBS的ph为6.8-7,溶液温度为37℃。
注射探针后24h,利用3%的异氟烷将小鼠麻醉,打开腹腔暴露肿瘤和部分肝脏。利用小动物NIR-II荧光成像设备进行成像。
如图5成像结果表明,RD-Cy7荧光分子探针注射24h后,能够特异性的靶向肝癌原位模型,且与肝脏相比,肿瘤的荧光信号强度可达10倍。能够实现较高对比度的肝癌NIR-II荧光成像。
实施例四
竞争结合实验探针靶向性检测;
利用HCCLM3肝癌细胞系和免疫缺陷Balb/c nude品系的小鼠,构建肝癌小鼠皮下/原位模型,并利用RD-Cy7荧光分子探针,结合小动物NIR-II荧光成像设备,开展肝癌原位模型的NIR-II荧光成像,同时利用未标记荧光染料的RD多肽,开展竞争结合实验,在小动物水平验证探针特异性。
模型构建成功后,将皮下/原位模型小鼠分为探针组和竞争组。对于探针组,直接通过尾静脉向小鼠模型体内注射RD-Cy7荧光分子探针,浓度为0.5mg/ml,体积为100ul。
其中,荧光分子探针溶于PBS溶液中,PBS的ph为6.8-7,溶液温度为37℃。
对于竞争组,通过尾静脉先向小鼠体内注射浓度为50mg/ml,体积为100ul未标记荧光染料的RD多肽,0.5h后,注射浓度为0.5mg/ml,体积为100ul的RD-Cy7荧光分子探针。注射探针后24h,利用小动物NIR-II荧光成像设备进行成像。
如图6-11成像结果表明,探针组的肿瘤具有较强的NIR-II荧光信号,而竞争组小鼠的肿瘤荧光信号强度和成像对比度都显著低于探针组。
实验结果表明RD-Cy7荧光分子探针通过RD多肽靶向肿瘤表面的整合素α6,标记荧光染料Cy7不影响RD的靶向性。
实施例五
RD-Cy7荧光分子探针对肝癌手术离体组织整合素α6表达量术中检测
手术获取的肝癌组织,先用PBS冲洗掉血细胞,利用浓度为80nM的RD-Cy7荧光分子探针溶液完全浸泡孵育5min,随后使用PBS缓冲液或生理盐水重复冲洗3次,每次冲洗5min。
其中,荧光分子探针溶于PBS溶液中,PBS的ph为6.8-7,溶液温度为37℃。
孵育结束后,利用NIR-II荧光成像系统对组织进行NIR-II荧光成像,根据荧光强度可半定量判断组织的整合素α6表达量。
如图12,肿瘤处荧光强度远超过肝脏组织处,荧光强度高低范围清晰可见。
以上所述仅为本发明的优选实施方式,并不用于限制本发明,对于本领域技术人员来说,本发明可以有各种更改和变化。凡在本发明精神和原则内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
