一种脓毒症相关性脑病模型及应用
文献发布时间:2023-06-19 19:38:38
技术领域
本发明属于器官芯片模型技术领域,具体涉及一种脓毒症相关性脑病模型及应用。
背景技术
脓毒症相关性脑病(sepsis-associated encephalopathy,SAE)又称脓毒症脑病,是脑以外其他部位感染所致的脓毒症引起的一种弥漫性脑功能障碍。近年来,脓毒症的发病率不断增加。研究表明超过50%脓毒症患者合并SAE,且脓毒症一旦合并SAE死亡率明显升高,随着SAE严重程度的增加,死亡率可升高至70%。目前,SAE已成为一个重要的威胁健康,影响社会发展的公共卫生问题,亟待解决。SAE是多因素、多种病理机制参与并行,如血脑屏障破坏、星形胶质细胞激活、小胶质细胞激活等均可导致神经元损伤,从而出现认知功能障碍。然而目前为止,其病理生理及潜在分子机制仍不完全清楚。
现阶段,开展SAE发病机制研究仍存在较大难度,突出难点在于SAE模型的建立。目前最常用小鼠模型及2D细胞培养模型。然而,小鼠模型在遗传背景、生理构造等方面与人体存在一定差异;SAE发病过程为外周炎症反应通过破坏的血脑屏障进入脑实质引发的一系列病理生理过程,而2D细胞培养模型,细胞缺乏器官病理生理微系统,因此一种人源化、具有病理生理微系统的仿生模型亟待建立。体器官芯片(organs-on-chips)是一种在芯片上构建的器官生理微系统,可以通过在微通道内实现三维细胞培养和精确的流体操控,在体外模拟近生理的组织细胞微环境,在一定程度上弥补传统2D细胞培养和动物模型难以体现人体组织器官复杂生理功能的缺陷。
器官芯片——作为一门迅速发展起来的科学技术,由多学科技术交叉汇聚而成,已经在生物医学领域展现了其独特的优势。该技术主要基于微流控芯片,集合微加工、细胞生物学、材料和生物组织工程等学科技术,在体外构建仿生的3D人体器官模型,包含多种活细胞、功能组织界面、生物流体等。该模型具有接近人体水平的生理功能,同时还能精确地控制多个系统参数。研究人员可以更加直观地研究机体行为,预测或再现疾病中的病理反应、药理反应。在生命科学研究、疾病模拟和新药研发及精准医疗等领域拥有广阔的应用前景。
微流控芯片作为细胞培养载体,有几大优势:首先,借助微流控芯片技术可根据实际应用设计不同的通道尺寸,提供一定的空间限制即物理因素控制,并维持细胞的三维生长状态。其次,流体控制有助于促进营养物质和氧气的交换,为细胞培养提供良好的生存环境。最后,PDMS作为微流控芯片的制作材料,具有良好的透光和透气性,可进行细胞的实时监测和观察并有利于细胞对氧气的充分利用,维持细胞的生长状态。但是目前将微流控技术与人源化SAE体外模型相结合,优化体外SAE模型及操作尚属空白。
现有技术中对双通道夹膜芯片建立人源化、具有器官病理生理微系统特征的三维立体脓毒症相关性脑病微流控仿生模型还属于技术空白,待研究人员的开发研究。
发明内容
为了解决现有技术存在的问题,本发明提供一种脓毒症相关性脑病模型及应用,在体外三维水平探究脓毒症对脑影响的新方法。本发明构建了一种体外人源化、三维立体脓毒症相关性脑病仿生模型体系,基于该器官芯片模型系统可以模拟脓毒症时机体炎症反应对脑的病理损伤过程,探究脓毒症过程中脑损伤的发生机制,填补了该研究领域的空白。
本发明提供了一种脓毒症相关性脑病模型,包括夹膜芯片,所述夹膜芯片包括由上至下顺次设置的上层基底、多孔膜和下层基底,所述上层基底包括上层通道,所述下层基底包括下层通道,所述多孔膜位于所述上层通道和所述下层通道之间;
所述夹膜芯片为BBB芯片;
所述BBB芯片为在所述多孔膜的靠近所述下层通道的一侧接种星形胶质细胞和周细胞,在所述下层通道的底面接种小胶质细胞;在所述多孔膜的靠近所述上层通道的一侧接种人脑微血管内皮细胞。
进一步地,所述多孔膜包括PET多孔膜或PDMS多孔膜等。
进一步地,所述多孔膜的孔径为1-10μm。
进一步地,所述上层基底和所述下层基底的材质包括PDMS。
进一步地,所述上层通道的两端分别设有上层细胞入口和上层细胞出口,所述下层通道的两端分别设有下层细胞入口和下层细胞出口。所述上层通道和下层通道的尺寸均为:1.5mm宽、0.2mm高。
进一步地,所述上层通道的培养基为脓毒症相关性脑病患者血清。
进一步地,所述下层通道的培养基为等体积混合的星形胶质细胞培养基、周细胞培养基和小胶质培养基。
本发明还提供了上述的脓毒症相关性脑病模型在体外人源化、三维水平探究脓毒症相关性脑病对于脑的影响中的应用。
本发明还提供了上述的脓毒症相关性脑病模型在脓毒症相关性脑病时,对脑内多种细胞状态和功能障碍进行实时监测,以及监测对于个体化治疗反应性中的应用。
本发明还提供了一种脓毒症相关性脑病模型的评价方法,具体过程如下:
(1)BBB芯片构建
将星形胶质细胞和周细胞按照2:1添加比制备成2,000细胞/μL的细胞悬液,取20μL细胞悬液注入芯片下层通道,并将芯片倒置放于37℃培养箱中,贴壁培养2小时。
将小胶质细胞制备成2,000细胞/μL的细胞悬液。将芯片通道中残留的星形胶质细胞培养基吸干,取20μL小胶质细胞悬液注入芯片下层通道。将人脑微血管内皮细胞制成2×10
将注射泵联通到芯片的上、下层通道入口处,流速100μL/h,37℃培养箱中灌流培养3天。
(2)芯片功能检测
通过血管内皮细胞钙粘蛋白VE-cadherin和紧密连接蛋白ZO-1免疫荧光染色检测BBB芯片屏障的完整性。采用FITC标记的右旋糖苷(FITC-dextran)监测BBB芯片通透性。利用跨膜电阻仪监测BBB芯片跨膜电阻值。
(3)脓毒症相关性脑病患者外周血收集
收集符合Sepsis-3.0诊断标准的脓毒症患者、符合脓毒症相关性脑病诊断标准的SAE患者分别于入院1d、3d、7d采集患者外周血,给予3000转/分离心10分钟后收集上清,-80℃保存。
同时对患者进行疾病严重程度评估(APACHE II、SOFA评分)及认知功能障碍评估(MMSE、MoCA),为患者个体化治疗做准备。
(4)脓毒症相关性脑病患者血清处理BBB芯片
将收集的脓毒症相关性脑病患者血清注入到BBB芯片的上层微血管通道。37℃培养4天,每隔2天换液一次。
(5)脓毒症相关性脑病患者血清灌注BBB芯片后,BBB损伤检测
在BBB芯片灌注脓毒症相关性脑病患者血清后,可以通过FITC标记的右旋糖苷的渗透性,评估BBB完整性变化。通过内皮细胞外连接(例如ZO-1、Occludin、Claudin-5、VE-cadherin)免疫荧光染色评估脑微血管内皮完整性变化。通过星形胶质细胞特异性标记物(GFAP、S100β)和小胶质细胞特异性标记物(IBA1、CD11b)检测两种胶质细胞的活化状态。通过细胞因子阵列试剂盒检测上下通道培养基中炎症因子水平。
有益效果:
本发明建立一种探究脓毒症对脑损伤影响的模型方法。该模型体系由人源化的脑微血管内皮细胞、周细胞、星形胶质细胞、小胶质细胞和夹膜芯片构成。通过收集脓毒症相关性脑病患者血清注入BBB芯片的脑微血管内皮通道,构建脓毒症引发的脑损伤模型。
本发明提供的脓毒症相关性脑病仿生模型,不仅模拟脓毒症相关性脑病发病过程,对脑屏障的功能损伤进行实时检测,还能对脑微血管内皮细胞、周细胞及胶质细胞在脓毒症引发的脑损伤中的作用进行实时动态体外检测及研究。
本发明提供的脓毒症相关性脑病仿生模型,可采用生物学上常用的细胞检测手段对BBB屏障损伤、多种细胞状态和炎症因子水平进行检测,包括FITC-dextran渗透性检测、细胞活力检测、细胞免疫荧光染色、qRT-PCR、细胞因子阵列检测等。
本发明利用器官芯片技术,具有良好生物相容性、透光性的PDMS和PET多孔膜为细胞的成像观察提供极大便利。该装置适用于检测病毒感染后检测屏障组织水平的变化(血脑屏障)及脑内各种细胞的行为及变化,例如mRNA变化、蛋白表达变化、细胞因子分泌、细胞死亡等。
附图说明
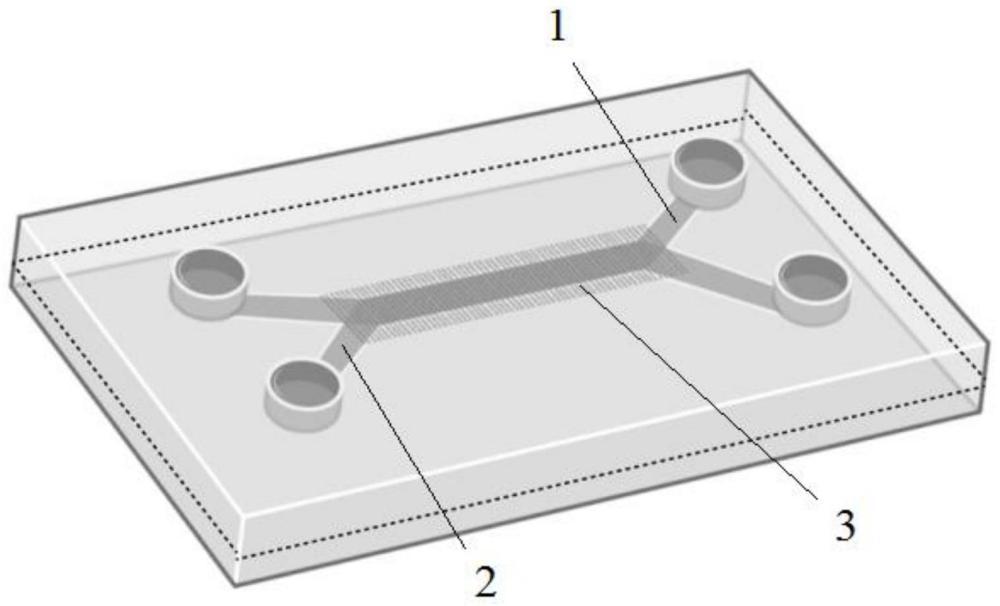
图1为本发明荚膜芯片结构示意图。
其中1为上层通道,2为下层通道,3为PET多孔膜。
图2为本发明脓毒症相关性脑病模型的结构及功能分区示意图。
图3为本发明脓毒症相关性脑病模型的3D立体图片。
图4为本发明脓毒症相关性脑病模型中各种细胞状态观察。
图5为脓毒症患者血清作用下脓毒症相关性脑病模型中各种细胞变化。
具体实施方式
下面的实施例将对本发明予以进一步的说明,但并不因此而限制本发明。
实施例1
利用夹膜芯片构建BBB芯片。
PDMS通道芯片制作:芯片模板成型后,测量模板通道的参数并对芯片进行硅烷化修饰。使用Sylgard184单体和PDMS引发剂按照10:1的体积比配制后倒入围好的芯片模板上,真空除气20min,在干燥箱中80℃烘干30min,使PDMS固化,取出。自然冷却,使用刀片将固化的芯片从模板上剥离,然后将PDMS芯片分割至适宜的大小,并用保鲜膜包裹,使用打孔器打出入口和出口。
夹膜芯片组装:将2μm孔径的PET多孔膜裁剪成合适尺寸,并将其贴附于上层通道芯片上。将下层通道和贴附有多孔膜的上层通道放入等离子封接机中打氧等,并将上下通道对齐粘贴在一起。将粘贴好的夹膜芯片放入60℃烘箱30min,使夹膜芯片充分粘贴牢固。
如图1-2所示,所述夹膜芯片由上层基底和下层基底粘合封接而成,上层基底和下层基底之间设有PET多孔膜。所述上层基底上设有上层通道,下层基底上设有下层通道。所述上层通道上设有上层细胞入口和上层细胞出口,所述下层通道上设有下层细胞入口和下层细胞出口。当夹膜芯片组装后,上层通道和下层通道呈现“x”形。所述上层通道和下层通道的尺寸均为1.5mm宽、0.2mm高。所述PET多孔膜孔径为2μm。所述上层基底和下层基底的材料为PDMS。
所述BBB芯片为在处于所述夹膜芯片的下层通道侧的PET多孔膜上接种星形胶质细胞和周细胞,在所述夹膜芯片的下层通道的底面接种小胶质细胞,在处于所述夹膜芯片的上层通道侧的PET多孔膜上接种人脑微血管内皮细胞。
实施例2
一种基于器官芯片技术,在体外、三维水平探究脓毒症对于脑影响的方法。具体过程如下:
(1)夹膜芯片灭菌及包被
将夹膜芯片放于6cm培养皿中,将培养皿开盖放置于超净台中紫外照射过夜。
在夹膜芯片的上层通道和下层通道各注满50μg/mL纤连蛋白(Fibronectin)溶液,并放置于37℃培养箱中过夜。接种细胞前,吸干纤连蛋白溶液,并用PBS清洗三次。
(2)构建BBB芯片:
将星形胶质细胞和周细胞按照2:1体积比制备成2,000细胞/μL的细胞悬液,取20μL细胞悬液注入芯片夹膜芯片下层通道,并将夹膜芯片倒置放于37℃培养箱中,贴壁培养2小时,使星形胶质细胞和周细胞贴壁于位于下层通道侧的PET多孔膜上。将小胶质细胞制备成2,000细胞/μL的细胞悬液。将夹膜芯片下层通道中残留的星形胶质细胞和周细胞培养基吸干,取20μL小胶质细胞悬液注入夹膜芯片下层通道,使小胶质细胞贴壁于下层通道的底面。将人脑微血管内皮细胞制成2×10
(3)芯片功能检测
通过血管内皮细胞钙粘蛋白VE-cadherin和紧密连接蛋白ZO-1免疫荧光染色检测BBB芯片屏障的完整性,分别对星形胶质细胞(GFAP、S100β、AQP4)、周细胞(HBVP-GFAP)、小胶质细胞(Iba1)进行免疫荧光染色,观察芯片上神经细胞状态完好(见图4)。采用FITC标记的右旋糖苷(FITC-dextran)监测BBB芯片通透性。利用跨膜电阻仪监测BBB芯片跨膜电阻值。
(4)构建脓毒症相关性脑病仿生模型:
由于SAE发病过程为外周血炎症因子通过血脑屏障进入脑实质内引发的一系列反应,因此灌流3天后分别用SAE患者血清灌流脑微血管内皮通道24h,完成脓毒症相关性脑病仿生模型构建。
在第四天,通过免疫荧光分别检测BBB芯片上四种细胞,发现脑微血管内皮细胞外连接(ZO-1指示紧密连接、VE-cadherin指示黏着连接)在SAE组显著减弱;周细胞覆盖率明显下降(α-SMA指示周细胞)星形胶质细胞明显激活(GFAP显著上调);小胶质细胞明显激活(IBA1显著上调),说明脓毒症引起的全身炎症反应可以导致患者神经系统损伤,进而引起临床中出现的神经症状。结果如图5所示。
以上所揭露的仅为本发明较佳实施例而已,当然不能以此来限定本发明之权利范围,因此依本发明权利要求所作的等同变化,仍属本发明所涵盖的范围。
- 一种防治脓毒症脑病的组合物及其应用
- 一种Cyp1a1基因敲除小鼠模型的构建方法及其在脓毒症中的应用
