医疗装置检测系统和方法
文献发布时间:2023-06-19 11:55:48
本申请要求于2018年11月21日提交的标题为“医疗装置检测系统和方法(DETECTION SYSTEMS AND METHODS FOR MEDICAL DEVICES)”的第62/770,676号美国临时专利申请以及因上述申请而产生的任何其它美国、国际或国家阶段专利申请的权益。前述申请以其全文引用的方式并入本文,限制为任何与本文的明确公开相反的主题均不被并入。
技术领域
本公开涉及用于检测生物物质和区分身体介质的系统和方法。更具体地,本公开涉及与可被推入患者体内的医疗装置相结合的用于检测生物物质和区分身体介质的系统和方法。
背景技术
改善尤其是脊柱外科手术的外科手术效果和成本结构的努力已使得微创手术的使用增加。这些手术通常使用图像引导模式,例如荧光透视、CT、神经刺激器以及近年来的多普勒超声。尽管微创脊柱手术、疼痛管理手术、神经阻滞、超声引导介入、活检、经皮穿刺放置或开放性术中放置的风险通常比外科手术小,但仍然存在无效结果和医源性损伤的风险,例如由于各种结构(包含但不限于器官、软组织、血管结构和例如致命性的脊髓等神经组织)的穿透而导致的感染、中风、瘫痪和死亡。无论执业医生的经验如何,损伤都可能发生,因为外科手术器械必须穿过多层身体组织和体液才能到达椎管中的所需腔。
为了说明这一点,在其中施用许多药物的脊柱区域的鞘内(或蛛网膜下)腔容纳神经根和脑脊髓液(CSF),并位于包裹中枢神经系统的三层膜中的两层之间。中枢神经系统的最外层膜是硬脑膜,第二层膜是蛛网膜,且第三层即最内层膜是软脑膜。鞘内腔位于蛛网膜与软脑膜之间。为了到达此区域,外科手术器械可能需要首先穿过皮肤层、脂肪层、棘间韧带、黄韧带、硬膜外腔、硬脑膜、硬膜下腔和鞘内腔。另外,对于用于施用药物的针,整个针孔必须在蛛网膜下腔内。
由于将外科手术器械插入鞘内腔中所涉及的复杂性,已知脊髓和神经组织的穿透容易引起微创脊柱手术和脊柱外科手术的并发症。另外,一些手术需要使用较大的外科手术器械。例如,其中可以将小导线插入脊髓硬膜外腔的呈微创脊柱手术形式的脊髓刺激可能需要将14号针引入硬膜外腔以穿过刺激器引线。这种规格的针在技术上更难控制,从而造成更高的发病风险。并发症可能包含硬脑膜撕裂、脊髓液渗漏、硬膜外静脉破裂导致的继发血肿,以及直接穿透脊髓或神经导致的瘫痪。当执业医生无法检测到针或外科手术设备尖端在关键解剖结构中的位置时,可能会发生这些和其它高风险情况,例如脊柱介入和射频消融。
目前,此类结构的检测依赖于操作者,其中操作者利用触觉、造影剂、解剖标志触诊和图像引导模式下的可视化。患者的安全性可能依赖于执业医生在触觉和图像解释方面的训练和经验。即使额外的训练和经验可能对执业医生有所帮助,但医源性损伤也可能独立于执业医生的经验和技巧而发生,因为解剖变异性可能是自然产生的,也可能是呈瘢痕组织形式的重复手术而引起的。一些手术(例如射频消融术)的专科训练可能不够严格因而无法确保能力;即使经过训练,手术的结果也会有很大的不同。在硬膜外注射和脊柱外科手术的情况下,黄韧带厚度、硬膜外腔宽度、硬膜扩张、硬膜外脂肪增多症、硬膜间隔和瘢痕组织的变化都会给传统的验证方法带来挑战,即使对于经验丰富的操作者也是如此。另外,当神经再生时(通常是一年或更长时间后)重复进行射频手术通常效果不佳且难度更大,因为再生后神经的分布会产生额外的解剖变异性。
发明内容
鉴于这些考虑,需要提供能提供实时反馈以帮助将外科手术器械精确放置到患者解剖结构中的系统和方法。
在一个方面,公开了一种生物标志物检测系统,其包含生物系统中的目标生物标志物。所公开的生物标志物检测系统包含流体分配系统,所述流体分配系统包含具有远端的递送装置。流体分配系统与目标生物标志物接触并且包含管腔和流体通道。生物标志物发光材料与递送装置的远端接触。所公开的生物标志物检测系统还包含与生物标志物发光材料光学连通的光学系统,其中所述光学系统包括光学接收器和光学检测器。在一些实施例中,光学系统可以包含光纤、光学耦合器或两者。
在另一方面,公开了一种生物标志物检测系统,其包含生物系统中的目标生物标志物和流体分配系统。流体分配系统包含递送装置,所述递送装置具有远端。流体分配系统与目标生物标志物接触并且递送装置包含管腔和流体通道。所公开的生物标志物检测系统与目标生物标志物连通。检测系统使用依赖于电导率、折射率或声音的属性的方法来检测目标生物标志物的存在。
在又一方面,公开了一种向患者递送药用流体的方法,所述方法包含使用生物标志物检测系统来定位患者体内目标生物标志物的存在。生物标志物检测系统包含流体分配系统,所述流体分配系统包含递送装置,所述递送装置具有远端。流体分配系统与目标生物标志物接触,且递送装置包含管腔和流体通道,并且生物标志物发光材料与递送装置的远端接触。生物标志物检测系统还包含与生物标志物发光材料光学连通的光学系统。光学系统包含光学接收器和光学检测器。所述方法进一步包含将药用流体递送到患者并且通知临床医生已检测到目标生物标志物。
在本公开中,术语:
“光学接收器”是指被构造和配置成检测沿从生物发光装置到光学检测器的光路返回的光的光检测装置;
“光学检测器”是指感测且可以测量其光路中的光量的装置;
“光学耦合器”是指被构造和配置成在流体通道与至少一个光纤之间耦合光的装置;以及
“滤光器”是指接收光并且仅允许具有例如波长、极性、强度等特定属性或其它选择性属性的光穿过其中的装置。
附图说明
应参考附图阅读以下描述。不一定按比例绘制的附图描绘了示例,并且无意于限制本公开的范围。考虑以下结合附图对各种示例的描述,可以更完全地理解本公开,附图中:
图1是根据本公开的生物标志物检测系统的一部分的说明性示例的示意性半截面图;
图2是根据本公开的生物标志物检测系统的一部分的另一说明性示例的示意性半截面图;
图3A是根据本公开的生物标志物检测系统的一部分的组件的又另一说明性示例的示意性截面图;
图3B是提供示出图3A系统的一些组件的细节的放大图的示意性截面图;
图4是根据本公开的生物标志物检测系统的部分的组件的又另一说明性示例的示意性截面图;
图5A是根据本公开的生物标志物检测系统的一部分的再另一说明性示例的示意性截面图;
图5B是提供示出图5A系统的一些组件的细节的放大图的示意性截面图;
图6A是根据本公开的检测配置中描绘的生物标志物检测系统的一部分的再另一说明性示例的示意性截面图;
图6B是呈检测后流体递送配置的图6A的系统的示意性截面图。
图7A是根据本公开的生物标志物检测针的实施例的示意性截面图;
图7B是从如图7A所描绘的针的左侧观察时图7A的针的示意性平面图;
图8A、8B、8C和8D是沿根据本公开的针的孔向下的示意性截面图,所述针的孔沿其长度提供光纤和管腔;
图9是适用于所提供的公开的用于区分空气和液体的光纤传感器的实施例的示意性截面图;
图10是沿可结合所公开的光纤空气传感器的针系统的说明性示例的孔向下的示意性截面图;
图11是可结合声波空气传感器的针系统的实施例的示意性截面图;
图12A是可结合电空气传感器的针系统的实施例的说明性示例的示意性平面图;
图12B是图12A的针系统的示意性侧视截面图;
图12C是沿图12A的针系统的孔向下的示意性截面图;
图13A是可结合电空气传感器的针系统的另一实施例的说明性示例的示意性侧视截面图;
图13B是沿图13A的针系统的一个配置的孔向下的示意性截面图;以及
图13C是沿图13A的针系统的另一配置的孔向下的示意性截面图。
所公开的生物标志物检测系统可以改善本领域中的一些缺点。它的使用可以改善外科手术效果和成本结构,尤其是脊柱手术和其它微创外科手术。所公开的生物标志物检测装置可以消除操作者对寻找目标生物标志物材料的依赖性,而不是依赖于触觉、造影剂、解剖标志触诊和图像引导模式下的可视化,从而提高了需要生物标志物识别的手术的安全性和有效性。
具体实施方式
本公开涉及用于检测生物物质(例如体液和组织,包含血液)以及用于区分身体介质(例如液体和空气)的系统和方法。将参考附图详细描述系统和方法的各种实施例,其中在整个若干视图中类似参考标号可以表示类似部件和组合件。对各种实施例的参考不限制本文公开的系统和方法的范围。另外,本说明书中阐述的任何示例不旨在限制性的,且仅阐述用于系统和方法的许多可能实施例中的一些。应理解,当情势所趋或因时制宜时,设想等效物的各种省略和替代,但是这些省略和替代意图在不背离本公开的精神或范围的情况下包括申请或实施例。此外,应理解本文所使用的措词和术语是出于描述的目的且不应被视为是限制性的。
本公开提供被构造成、配置成和/或能够经由生物标志物与一种或多种检测材料的相互作用来检测一种或多种生物标志物以及所述相互作用的光学检测的系统和方法。在一些示例中,生物标志物与检测材料的相互作用可以导致可被感测的光的发光发射,其中所述对发光的光的感测提供相互作用的证明,并因此提供生物标志物的存在的证明。在这些示例中的一些中,光的发射可以是生物标志物与检测材料之间相互作用的固有化学发光产物。在这些示例中的另一些示例中,当存在生物标志物时,检测材料的外部光源的照明可以导致可被感测到的光的荧光或磷光发射。本公开提供了可以经由感测化学发光、荧光和/或磷光而提供对生物标志物的检测的系统和方法。
尽管在本公开中示出和描述的生物标志物检测系统的多个示例包含针和流体递送系统或可与之结合使用,但是所公开的生物标志物检测系统和方法的应用不限于流体递送应用。在本公开中,可以通过所公开的流体递送系统来递送药用流体。可以采用结合了本公开的检测技术的流体递送系统来递送导线/引线,纳米颗粒以及任何合适的药理学或其它治疗剂,包含再生药品和化疗药物。
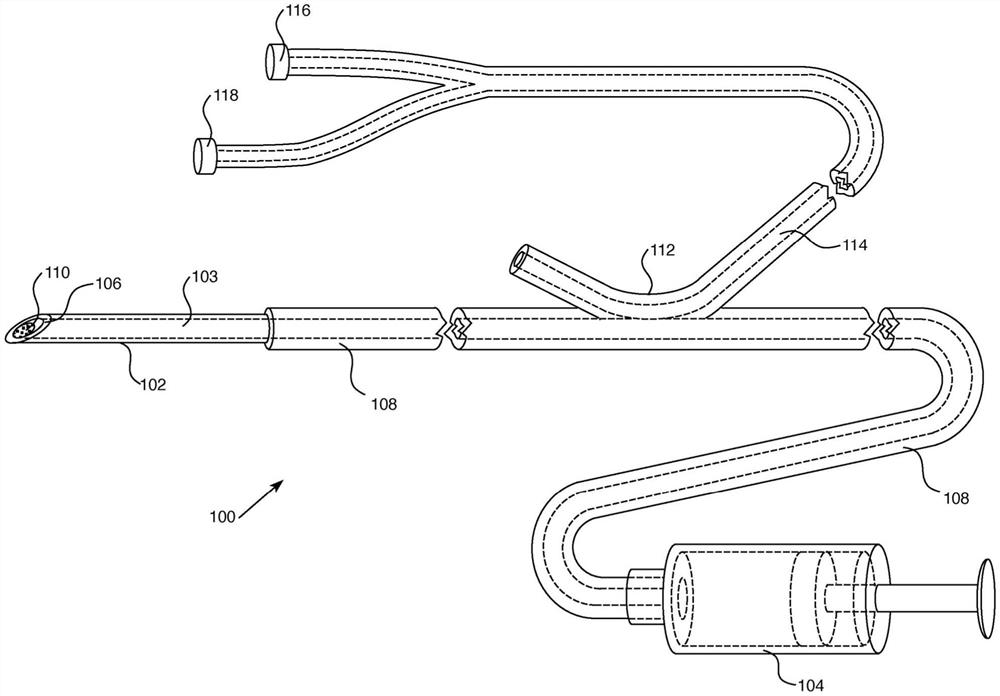
图1示意性地描绘了本公开的生物标志物检测系统100的说明性示例。系统100可以包含具有管腔103的针102,所述管腔可以将来自注射器104或其它合适的流体分配系统的流体经由流体通道108(所述流体通道包含管腔103)递送到所述针的尖端106。可例如经由涂覆工艺将生物标志物发光材料110放置在针102的尖端106处或内部并且邻近所述尖端106。
系统100可以包含光学耦合器112,所述光学耦合器可以被构造和配置成在流体通道108与光纤114之间耦合光。本公开的光学耦合器112和任何其它光学耦合器可以被构造和配置成用作波分复用器,所述波分复用器可以通过例如对到达检测器的光的光谱进行过滤来提高信噪比。可以选择具有折射率大体上接近或基本等于流体通道108中的流体的折射率的芯材料的光纤114,使得光可以容易地在两者之间耦合,同时最小化反射损失和可能由光学失配引起的其它光学问题。替代地或另外,例如,通过选择流体的各种成分(例如葡萄糖、酒精、糖盐和/或任何其它生物相容性流体)的浓度,可以将通道108中的流体的折射率调整为与光纤114的芯的折射率大体上或基本精确匹配。流体通道108可以被构造和配置成使得在存在流体的情况下它可以用作光学波导。
例如二极管激光器或其它合适的光源等光源116可以光学耦合到光纤114,使得来自光源的光可以经由流体通道108所提供的光纤和光波导递送到针102的尖端106,且更具体地,递送到所述尖端处的生物标志物发光材料110。从生物标志物发光材料110发射或以其它方式散射的光可以由流体通道108和光纤114所提供的光路返回到光学接收器118,所述光学接收器可以是光电检测器或被构造和配置成检测沿着从针102的尖端106的光路返回的光的任何其它合适的光检测装置。可以构造、配置和调谐光学耦合器112,使得其可以针对任何相关的光学频率(包含光源116的一个或多个发射频率和生物标志物发光材料110的发光频率)有效地在流体通道108与光纤114之间耦合光。
经由各种机制,来自光源116的光可能例如经由来自组织和其它后向散射途径的后向反射而不期望地到达光学接收器118,从而在接收器118测量来自生物标志物发光材料110的发光发射的信号时增加了所述接收器读取的噪声。可以多种方式抵消这种测量噪声源。如前所述,光学耦合器112可以被构造和配置成用作波分复用器,其可以将入射在光学接收器118上的光的频率选择性地过滤为从生物标志物发光材料110发射的频率。替代地或另外,光学接收器118可以包含滤光器,以选择性地防止除生物标志物发光材料110的发光频率以外的频率到达光学接收器,例如来自光源116的照明光以及环境中可能存在的其它光,例如环境室内照明。可以采取改善信噪比的其它措施,例如过滤室内照明以衰减光学接收器118的灵敏度频率处的发射。这样的波长和频率过滤/灵敏度考虑因素可以应用于本公开的任何相关系统。
可以用来改善信噪比以在光学接收器118处检测从生物标志物发光材料110发射的光的另一种技术是时分复用。通过在时间上将光源116对生物标志物发光材料110的照明与来自所述材料的发光发射的检测分开,可以避免这种噪声源。在说明性示例中,可以用全开、全关的方波来驱动光源116。利用可以足够快地关断的光源116(即,与来自生物标志物发光材料110的发光发射的衰减时间常数相比是快速的),可以对来自光学接收器118的数据收集进行门控以仅在光源116关闭时执行,使得在光学接收器118处没有记录到源自光源116的后向反射/散射光。潜在地,可能不期望地到达光学接收器118的其它光源(例如,可能在外科手术室中采用)也可以用与光源116相同的波形来驱动,以防止其被检测到。在足够高的频率下,人眼无法察觉到这种脉冲。这些时分复用方法可以有利地与本公开的任何兼容系统和方法一起使用。
在系统100的示例使用方法中,临床医生可以将针102推入患者体内,其中光源116被激活以提供对生物标志物发光材料110的照明。具有光学上合适的折射率的流体可以存在于流体通道108(包含管腔103)中。针102可被推入,直到针的尖端106遇到目标生物材料(例如,血液,但也是可能是其它目标生物材料)为止,在此目标生物材料(例如,血液)与生物标志物发光材料110的相互作用结合来自光源116的照明光可以导致来自生物标志物发光材料的光的发射,所述光可以被光学接收器118检测到。可操作地耦合到光学接收器118的通知系统(未示出)可以通知临床医生已检测到目标生物标志物。然后,临床医生可以根据对目标生物材料的检测以及对患者解剖结构的了解(例如,进一步推进、停止推进或缩回针)来对针102的尖端106进行定位。在适当放置针102的尖端106的情况下,可以执行通过流体通道108从流体递送系统递送治疗流体。
图2示意性地描绘了本公开的另一生物标志物检测系统200的另一说明性示例。系统200可以包含针202,所述针可以将来自注射器204或其它合适的流体分配系统的流体经由流体通道208递送到针的尖端206。针202和注射器204可经由一个或多个流体连接器209流体耦合,所述流体连接器可以是任何合适的连接器,例如(但不限于)LUER锁配件。流体通道208可以包含针202的管腔210。在图2所示的系统200的配置中,针202的管腔210可以至少部分地被光纤212占据。光纤212可以包含例如经由涂覆工艺附接到其远侧尖端的生物标志物发光材料214。如图2所示,可以将在其远侧尖端附接有生物标志物发光材料214的光纤212定位在针202的管腔210中,使得生物标志物发光材料定位于针202的尖端206处或附近。在这种配置的一些实施例中,光纤212可以大体上阻挡流体通过针202的管腔210。在一些其它实施例中,存在于管腔210中的光纤可以允许至少部分流体通过。在系统200中,光纤212可以在管腔210内选择性地缩回,使得光纤的远侧尖端可以定位于例如位置216之类的位置处或附近,在所述位置它可以大体上不阻碍流体经由管腔210从注射器204流向针202的尖端206。
系统200可以包含光源218,例如二极管激光器或其它合适的光源,其可以光学地耦合到光纤212,使得来自光源的光可以被递送到光纤的远侧尖端,更具体地,递送到所述尖端处的生物标志物发光材料214。从生物标志物发光材料214发射或以其它方式散射的光可以由光纤212返回到光学接收器220,所述光学接收器可以是光电检测器或被构造和配置成检测由光纤212从光纤的远侧尖端返回的光的任何其它合适的光检测装置。
系统200可以包含光学耦合器222,所述光学耦合器可以被构造和配置成将来自光源218的光传递到光纤212的远侧尖端处的生物标志物发光材料214,并且将从生物标志物发光材料214发射的光透射到光学接收器220。可以将光学耦合器222调谐为例如波分复用器,以选择性地使从生物标志物发光材料214发射的光到光学接收器220的透射最大化,并且使这种发射的光朝着光源218返回的透射最小化。第二光学接收器224可以是光电检测器或可以经由光纤分离器222耦合到系统200的光学系统的任何其它合适的光检测装置。第二光学接收器224可用于感测来自光源218的发射的驱动信号电平,当在光学接收器220解释信号时,其可用于创建差分信号以补偿光源218的强度变化(例如,由于温度变化而引起的漂移)。在一些情况下,也可以使用此布置来实施在光学接收器220处从生物标志物发光材料214接收的信号的相敏检测。
系统200可以在与针对系统100描述的许多方面类似地使用。在操作中,系统200的针202可以通过定位在管腔210中的光纤212推入患者体内,使得在光纤的远侧尖端处的生物标志物发光材料214设置在针202的尖端206处或附近。一旦生物标志物发光材料214接触目标生物材料(例如血液),就可以将这种接触所产生的光沿光纤向上透射至光学接收器220,并将检测结果指示给系统的用户。一旦将针正确地定位(例如,在血液中),光纤212就可以缩回(例如,到216),打开管腔210,使流体从注射器204流动以在针202的尖端206处进行递送。
图3A示意性地描绘了本公开的另一生物标志物检测系统300的组件的另一说明性示例,并且图3B提供了示出图3A所示的一些组件的细节的放大图。系统300可以在与针对用于生物标志物检测和治疗递送的系统100描述的许多方面类似地使用。图3A、3B的系统可以包含针302,所述针可经由流体管线306的流体通道304从流体递送系统(未整体示出)递送流体。图3A、3B的系统300可以包含可将针302与流体递送系统和光学系统(未整体示出)耦合的耦合器308。包含耦合器308的图3A、3B的系统300可以采用任何合适的流体连接器(不一定示出),例如(但不限于)LUER锁配件。光学系统可以包含光纤310和耦合光学器件312,所述耦合光学器件包含一个或多个透镜,并由光学支架314保持光学对准。光学支架314可以通过支撑腹板318保持相对于耦合器壳体316的位置关系。光学支架314、耦合器壳体316和支撑腹板318之间的所描绘的物理布置以及它们之间的物理布置仅是示例,且不应被认为是限制性的。
当相对于光纤310适当地定位和对准时,耦合光学器件312可以将从光纤发射的照明光耦合或聚焦到针302的管腔320中。围绕针302的管腔320的内壁322可以例如通过电化学或其它合适的工艺抛光或以其它方式平滑,使得它们可以用作如此耦合的照明光的波导。在一些示例中,围绕针302的管腔320的内壁322可以涂覆或衬有一层薄的电介质材料,例如玻璃或聚合物,其折射率低于管腔内流体的折射率,使得可以得到类似于光纤的全内反射波导,其中管腔中的较高折射率的流体用作“芯”,且涂覆管腔的壁的较低折射率的薄电介质层用作“包层”。(此波导配置可以潜在地应用于本公开的任何系统中,其中光分别传播通过流体通道,包含系统100、400、500和600的针102、402、502和602中的流体通道)。由任何合适的光源(未示出)(例如二极管激光器)提供的照明光可以经由针302的管腔320的向下传播而递送到其尖端324,生物标志物发光材料326可以例如经由涂覆工艺定位于所述尖端。从生物标志物发光材料326发射或以其它方式散射的光可以通过反向光路(针管腔320的波导,然后通过光学器件312耦合到光纤310)返回到光学接收器(未示出),所述光学接收器可以是光电检测器或被构造和配置成检测由光纤310从针302的尖端324返回的光的任何其它合适的光检测装置。
耦合器308可以包含一个或多个流体通道328,其可在流体管线306的流体通道304与针302的管腔320之间流体连通。光学支架314可以限定或提供空隙330,所述空隙可以从流体递送系统的流体路径(304、328、320)流体地密封,且在其中可以保持稳定折射率的真空或气体气氛,使得可以减少或消除折射率变化对光学耦合的影响。出于相同的原因,透镜312的面向流体的一侧可以是平面表面。
图4示意性地描绘了本公开的另一生物标志物检测系统400的组件的另一说明性示例。图4的系统400可以包含针402,其可将来自流体递送系统(未示出)的流体通过管腔404递送到针402的尖端406。图4的系统400可以包含流体耦合器408,所述流体耦合器可以经由流体连接器410将针402与流体递送系统耦合,所述流体连接器可以是任何合适的流体连接器,例如(但不限于)LUER锁配件。耦合器408和/或针402可以包含或限定一个或多个流体通道411,其可在连接器侧流体通道413与针402的管腔404之间流体连通。
生物标志物发光材料412可以例如经由涂覆工艺而定位于针402的尖端406处。围绕针402的管腔404的内壁可以例如通过电化学或其它合适的工艺抛光或以其它方式平滑,使得它们可以形成波导以有效地将从生物标志物发光材料412发射的光传输到光学接收器414,所述光学接收器可以是光电检测器或被构造和配置成检测从生物标志物发光材料发射的光的任何其它合适的光检测装置。针对生物标志物发光材料412发射的一个或多个波长的光而调谐的波长区分滤光器416可以帮助拒绝杂散光并改善信噪比。光学接收器414可以经由连接418电连接到检测电子器件。
图4的系统400可适于与生物标志物发光材料412一起使用,所述生物标志物发光材料在与目标生物材料(例如,血液)接触时可产生光而无需外部光源的照射。省略照明光源可以使生物标志物检测装置和系统相对简单。可以与图4的系统一起使用的不一定需要外部照明的生物标志物发光材料的一个示例是鲁米诺。
除了省略外部光源对生物标志物发光材料412的照明之外,系统400可以在与针对用于生物标志物检测和治疗递送的系统100描述的许多方面类似地使用。
图5A示意性地描绘了本公开的“独立的”生物标志物检测针系统500的说明性示例,且图5B提供了示出系统500的一些组件的细节的放大图。系统500可以包含具有管腔504和尖端506的针502,生物标志物发光材料508可以例如经由涂覆工艺定位于所述尖端。系统500可以包含支架510,针502可以安装到所述支架上并且经由流体连接器512连接到流体递送系统(未示出),所述流体连接器可以是任何合适的流体连接器,例如(但不限于)LUER锁配件。
支架510可以容纳光学器件和电子器件,以使得能够利用生物标志物发光材料508进行生物检测。在支架510处,系统500可以包含光源514,例如二极管激光器或其它合适的光源;以及光学接收器516,其可以是光电检测器或任何其它合适的光检测装置。支架510的光学系统可以包含光束分离器518和反射镜520。通过这种光学布置,由图5B中的虚线空心箭头表示的来自光源514的照明光可以沿针502的管腔504向下指向针的尖端506,在尖端处它可以照射生物标志物发光材料508。从生物标志物发光材料508发射或以其它方式散射的光可以通过如实线空心箭头所示的反向光路返回到光学接收器516。围绕针502的管腔504的内壁522可以例如通过电化学或其它合适的工艺抛光或以其它方式平滑,使得它们可以用作在针502中传播的光的波导。支架510的光学系统还可以包含光学窗口524,所述光学窗口可以为针502的管腔504中的流体提供屏障,以防止进入支架510的光学/电子空间526。光学窗口524可以制造成选择性地过滤波长(例如,选择性地使来自光源514的照明光和从生物标志物发光材料508发射的光通过,同时阻挡不希望的波长)。选择性过滤也可以在光束分离器518的一个或多个表面处实施。
支架510和/或针502可以包含或限定一个或多个流体通道528,所述流体通道可在连接器侧流体通道530与针502的管腔504之间流体连通,从而提供围绕反射镜520的流体旁路。
光源514和光学接收器516可以电耦合到电路板532,所述电路板可以向装置提供功率和控制信号,并且从装置接收信号或其它信息并进行处理。在图5B中,光源514和光学接收器516均被示为经由引线键合而电耦合到电路板532,但这不是限制性的,并且可以采用装置与电路板之间的任何合适的功能连接(例如表面安装技术)。相对于系统500的元件532所使用的术语“电路板”是通用的,并且不应被认为是限制性的。电路板532可以包含具有多个分立组件的印刷电路板、单芯片处理器或“片上系统”、多个子板、混合系统,或能够用系统500的元件供电和执行生物标志物检测系统功能的任何其它合适的装置。支架510可以容纳或支撑任何合适的用户接口元件534,其可以包含(但不限于)按钮、视觉指示器(例如发光二极管)和音频信号器/扬声器。电路板532可以包含一个或多个无线接口,例如蓝牙接口,其可以结合操作所必需或期望的任何蓝牙功能,例如检测信号、自检、电池状态等。支架510可以容纳能量存储装置536,其可以是电池或任何其它合适的装置,可以为光源514、光学接收器516、电路板532和由支架510承载的其它合适的组件提供操作功率。系统500可以在与针对用于生物标志物检测和治疗递送的系统100描述的许多方面类似地使用。
图6A和6B示意性地描绘了本公开的另一生物标志物检测系统600的组件的另一说明性示例。图6A大体描绘了系统600的检测配置,且图6B大体描绘了检测后流体递送配置。系统600可以包含具有管腔604的针602。在图6A的配置中,设置在针602的尖端608处或附近的半渗透屏障606可以防止存在于管腔604中的生物标志物发光材料流体在针的尖端处离开针,并潜在地进入患者体内。在系统600中使用半渗透屏障606可以使得能够在针602的管腔604中提供生物标志物发光材料流体的大储层,与缺少这种储层的其它布置相比,这提供了更大的照明和更长的灵敏度持续时间。
半渗透屏障606可以对目标生物材料610至少是半渗透的,使得目标生物材料可以与存在于管腔604中的生物标志物发光材料流体接触并反应。在一些示例中,半渗透屏障606可以被构造和配置成使得其选择性地允许铁离子或含铁化合物通过,例如作为血液的成分被发现。存在于管腔604中的生物标志物发光材料流体可以是与这种铁离子或含铁化合物反应的材料。在一些实施例中,血液无限期地保持活跃。一旦血液中存在的任何形式的铁与生物标志物发光材料接触并发出辐射,铁就通常不会在反应中消耗。
在一些实施例中,目标生物材料和生物标志物发光材料流体可以反应,使得通过所述反应产生光子612。如图所示,取决于目标生物材料穿透屏障606并进入管腔的体积中,可以在管腔604内的多个位置中产生此类光子612。在一些实施例中,半渗透屏障606可以是半透明的或至少部分透明的,以允许通过屏障内的反应产生的光子612离开屏障进行检测。
由于目标生物材料610与生物标志物发光材料流体之间的接触而产生的光子612可以在针602的管腔604内传播到光学接收器614,所述光学接收器可以是光电检测器或被构造和配置成检测这种光的任何其它合适的光检测装置。围绕针602的管腔604的内壁616可以例如通过电化学或其它合适的工艺抛光或以其它方式平滑,使得它们可以用作在针中传播的光的波导。
在图6A中以检测配置描绘了生物标志物检测系统600,而在图6B中以流体递送配置描绘了所述系统。在成功检测到目标生物材料之后,可以将系统600从图6A的检测配置重新配置为图6B的流体递送配置,但这不是限制性的,并且这种重新配置不一定取决于成功的生物材料检测。
参考图6B,可以通过经由流体提取端口618从针602的管腔604抽取生物标志物发光材料流体来实现重新配置,所述流体提取端口可以经由提取孔620与针的管腔流体连通。可以通过任何合适的工艺(常规机加工、激光钻孔、蚀刻等)形成提取孔620。箭头622指示生物标志物发光材料流体的抽取,其指示在抽取期间生物标志物发光材料流体的流动方向。半渗透屏障606可以可滑动地配置在针602的管腔604中。当从管腔604抽取生物标志物发光材料流体时,可从其先前的远侧位置(在针602的尖端608处)沿近侧方向(朝图6A和6B的右侧)抽出可滑动的半渗透屏障606。在从管腔大体上完全抽取生物标志物发光材料流体之后,示出了半渗透屏障606在管腔604的近端。在一些替代性示例中,半渗透屏障606可以采取不可滑动的破裂屏障的形式。通常期望这种破裂屏障在破裂时不产生任何颗粒。
利用从针602的管腔604抽取的生物标志物发光材料流体,系统600可以用于经由流体输入端口624从流体递送系统(未示出)递送流体,所述流体输入端口可以经由递送孔626与针的管腔流体连通。可以通过任何合适的工艺(常规机加工、激光钻孔、蚀刻等)形成递送孔626。从流体递送系统进行的流体递送由箭头628指示。
注意,图6A和6B的截面图中的空间630可以例如经由围绕针602的环形空间与流体输入端口624流体连通。类似地,空间632可以与流体提取端口618流体连通。
通过感测由于生物标志物发光材料与目标生物材料之间的接触而产生的发光发射,用于生物标志物检测的其它针配置也是可能的。图7A是生物标志物检测针700的示意性截面图,且图7B是从图7A中的针的左侧观察时针700的示意性平面图。针700在其尖端702处可以包含生物标志物发光材料704。针700可以包含一个或多个光纤706、708。光纤706、708中的一个可用于将照明光从例如二极管激光器或其它合适的光源等光源(未示出)递送到生物标志物发光材料704,而这两个光纤中的另一个可以用于将从生物标志物发光材料发射的光传输到光学接收器(未示出),所述光学接收器可以是光电检测器或任何其它合适的光检测装置。针700可以包含适合于从注射器或其它合适的流体分配系统(未示出)递送流体的管腔710。
针700的配置采用非缩回光纤706、708,用于照明光和由生物标志物发光材料发射的光的高效传输,并且同时提供始终开放以便流体递送到针的尖端702的管腔。相比之下,在图2的系统200中,可能需要将光纤212从尖端206缩回至位置216以打开管腔210进行流体递送。在本公开的一些其它实施例中,例如图1的系统100,针的开放管腔可以用于提供用于光传输的光波导,而没有一个或多个光纤延伸到所述针的远侧尖端。在许多情况下,与针的管腔相比,光纤可以提供更高的光传输效率。
图8A、8B、8C和8D是沿针的孔向下的示意性截面图,所述针的孔沿其长度提供到针的尖端的光纤和管腔,类似于图7A和7B的针700。图8A的针802可以包含五个光纤,其中外部光纤804是将来自光源的照明光递送到生物标志物发光材料的照明光纤,而内部光纤806是用于将从生物标志物发光材料发射的光传输到光学接收器的感测或检测光纤。四个外部照明光纤和一个内部检测光纤的这种布置仅是示例,不应视为限制性的。可以考虑其它光纤布置。针802可以包含一个或多个适于流体递送的管腔808。在一些示例中,可以采用多个管腔来提供更高的流体电导率,以用于从公共流体储层递送流体。在一些其它示例中,可以采用多个管腔来为不同的流体提供独立的递送路径。
图8B的针810可以包含适合于流体递送的三个光纤812和三个管腔814。图8C的针816可以包含两个光纤818和两个管腔820。图8D的针822可以包含单个光纤824和单个管腔826。这些仅是示例,并且可以提供其它数量的光纤和管腔并将其用于本公开中设想的生物标志物检测针。通过使用例如用于处理照明光和检测光利用单个光纤的耦合的光纤分离器(类似于图2的系统200的分离器222),可以将具有单个光纤的针中的光纤用于照明和检测。替代地,具有单个光纤的针中的光纤仅可以用于在不需要照明光的检测布置中将检测光从生物标志物发光材料传输到光学接收器。
在本公开设想的一些示例中,具有多个光纤的器械,类似于(但不限于)图7A、7B、8A、8B和8C中所示的针,可以用于被配置用于检测多种生物标志物和/或其它可检测物质的装置。多个光纤中的每一个都可以用于独立的检测和/或照明通道。例如,可以在针尖的不同检测光纤的末端涂覆不同的生物标志物发光材料,从而可以独立地感测不同的发光检测信号。不同的生物标志物发光材料可具有不同的照明要求,可以通过多个照明光纤来提供所述照明要求。如本文其它地方所讨论的,可以将单独的光纤用于空气/气体检测。
在本公开的系统和方法中用于生物标志物检测的生物标志物发光材料可以利用各种不同的发光现象。一些生物标志物发光材料可以依赖于化学发光,生物标志物发光材料与目标生物标志物之间接触时发生的化学反应可以在没有额外能量输入的情况下产生可被感测为生物标志物的检测信号的光发射。系统400和600(不一定包含光源)可能特别适合与化学发光生物标志物发光材料一起使用,因为它们可能相比包含光源的系统不那么复杂(至少在光学复杂性上)。然而,潜在地系统100、200、300、400、500和600中的任何一个以及针700、802、810、816和822中的任何一个可以与化学发光检测结合使用,尽管在一些所述系统中包含光源可能与化学发光产生的光的检测无关。
一些其它生物标志物发光材料可以采用通过生物标志物发光材料与目标生物材料之间的接触而激活的光致发光(例如,荧光和/或磷光)。用于光致发光的照明光可以由说明性示例系统100、200、300和500的光源提供,并且可以通过系统100、200、300、500的光纤(和/或在一些情况下,其它波导)以及针700、802、810、816和822中的至少一些来传输。
一些生物标志物发光材料在不存在目标生物标志物的情况下可表现出光致发光,并且在暴露于目标生物标志物时,光致发光可以停止或减少。
生物标志物发光材料涂层的物理特性可以反映竞争因素之间的平衡。较薄的涂层可以是足够半透明的以允许照明光穿透并且发射的光逸出以进行检测,而较厚的涂层可以提供更多的生物标志物检测材料和更强的发射信号。涂层可以包含交联的亲水涂层。交联的亲水涂层可以包含生物标志物发光材料作为涂层的一部分,或者可以将其包封或密封到递送装置。可能需要生物标志物发光材料的孔隙率以促进生物标志物与材料之间的相互作用。
本公开进一步考虑了用于区分患者解剖结构内的气体(可以称为“空气”)和液体以帮助在其中精确地放置外科手术器械的实时系统和方法。此类系统可以包含光学、声学和/或电检测,并且可以基于光学、声学和/或电的阻抗的差异。
图9是用于区分空气和液体的光纤传感器900的示意性截面图(在本文中可以称为“光纤空气传感器”)。传感器900可以包含光纤芯902,其可以被包层904包围,而所述包层又可以被缓冲区906包围。缓冲区906可以包含一个或多个缓冲层,例如主要缓冲层和次要缓冲层。光纤空气传感器900可以包含用于强度,保护等的任何其它合适的层(未示出)。
光纤空气传感器900可以被构造和配置成基于在光纤内朝着检测端传播(即,在图9中从左到右)的来自光源(未示出)的光是否在入射到检测端处的光纤芯902的面909上时经历全内反射来区分检测端908处的液体和空气。示例性光线线束被示为在芯902内朝着(在910处)检测端908传播,然后在从面909反射之后远离(在912处)检测端传播。在全内反射的情况下,以比全内反射的临界角浅的入射角入射在面909上的光线可以基本上被完全反射。如果以比临界角更陡的角度入射,则通常光线可以在芯902内部分反射(如在912处)并且部分地折射出光纤,如针对光线914示意性示出的。
面909可以被构造成将在芯902内传播的光线向检测端908回射。它们可以例如相对于芯902的纵轴成45度定向。在一些实施例中,它们可以以立体角配置来布置。相对于芯902的纵轴(基本上是光传播轴)以45度定向的面可以适当地定向以区分空气和液体。对于熔融石英光纤,相对于外部空气介质的全内反射的临界角约为43度,且相对于外部水介质的全内反射的临界角约为67度。因此,沿芯902的纵轴传播并入射在相对于纵轴成45度的面909上的光可以以比空气的临界角浅且比水的临界角陡的方式入射在面上。
在操作中,检测方案可以包含光学接收器(未示出),所述光学接收器可以被适当地配置成检测来自光源的已经从检测端908回射的光。当检测端908的面909暴露于外部空气介质从而产生全内反射时,与当这些面暴露于液体时(因此不会产生全内反射)相比,此回射信号通常可以更亮。面909可以包含涂层以增强其检测效用。面909的内部部分916,包含芯中的光可以入射到的面的部分,可具有疏水涂层,以在检测端908处于空气中时排斥面上的残留液体。面909的外部部分918可以包含亲水涂层,以从内部部分916抽离液体。
图10是沿可结合光纤空气传感器1002的针系统1000的说明性示例的孔向下的示意性截面图可以类似于图9的光纤空气传感器900的传感器1002可设置在模具1008内的皮下注射针1004内。皮下注射针1004可以封闭用于递送药用流体的流体通道1006,但这不是限制性的,并且在其它实施例中,针可以递送或容纳其它治疗有效载荷和/或装置。可以预期的是,光纤空气传感器可以被结合到其它配置的医疗装置中,包含与本文描述的生物标志物检测系统结合。
图11是可结合用于区分空气和液体的声学探头(在本文中可以称为“声学空气传感器”)的针系统1100的示意性截面图。感测杆1102可以经由一个或多个弹性附件1106安装在皮下注射针1104内。感测杆1102可由压电致动器1108相对于反应质量1110以适当频率纵向地(如叠加在其上的箭头所示)驱动。针系统1100的远端处的感测杆1102的尖端1112可以与在其位置处可能存在的任何介质机械接触,无论所述介质是组织、液体还是气体。这些介质中的每一者可对感测杆1102的运动呈现不同的机械阻抗,其中阻抗通常按顺序减小(组织>液体>气体)。声学/机械阻抗可以通过多种方式进行测量,包含但不限于(a)施加恒定驱动力并测量振幅;(b)驱动至恒定振幅并测量驱动力;和/或(c)测量驱动力与运动之间的相移。针系统1100可以封闭用于递送药用流体的流体通道1114,但这不是限制性的,并且在其它实施例中,针可以递送或容纳其它治疗有效载荷和/或装置。可以预期的是,声学空气传感器可以被结合到其它配置的医疗装置中,包含与本文描述的生物标志物检测系统结合。
图12A、12B和12C分别是沿可结合用于区分空气和液体的电传感器(在此可以称为“电空气传感器”)的针系统1200的说明性示例的孔向下的示意性平面图、示意性侧视截面图和示意性截面图。导体1204a、1204b可以模制在位于皮下注射针1202内的绝缘体1206中。皮下注射针1202可以接地,并且导体1204a、1204b可以连接到电驱动和感测设备(未示出)。导体1204a、1204b的末端可以在针1202的远侧尖端处被抛光,使得它们的面1208a、1208b可以与在针的尖端处的任何介质导电接触。通常,导体1204a、1204b的面1208a与1208b之间的电导率可以取决于所述介质。例如,[以(欧姆·厘米)
图13A、13B和13C中示出类似于图12A、12B和12C的系统1200的针系统,图13A、13B和13C分别是可以结合有电空气传感器的针系统1300的说明性示例的示意性侧视截面图,以及沿针系统1300的两个替代配置的孔向下的示意性截面图。在图13A、13B和13C的配置中,与其中导体1204a、1204b模制在针1202的管腔中的绝缘体1206内的针系统1200相比,可以将导线接合在皮下注射针1302的管腔中。图13A、13B和13C的配置的导线各自包含导体1304a、1304b或1304c,其中每个导体由绝缘体1312围绕。可以使用粘合剂1314将导线接合在针管腔内。
在图13B的配置中,可以将具有导体1304a的单个导线接合在针1302内。在此配置中,导体1304a用作一个导体,且针1302用作另一导体,以进行电空气感测。在图13C的配置中,具有导体1304b、1304c的两个导线可以接合在针1302内,并且用作完成空气感测电路所需的两个导体。可以在针的末端放置疏水涂层,以在遇到空气空间时帮助从导体1304a、1304b、1304c的面1308a、1308b、1308c以及针1302的末端1316排出液体。针系统1300可以封闭用于递送药用流体的流体通道1310,但这不是限制性的,并且在其它实施例中,针可以递送或容纳其它治疗有效载荷和/或装置。
在使用具有光学、声学或电空气检测系统的针系统(例如,系统1000、1100、1200或1300中的一个)的示例方法中,临床医生可以将针推入患者体内,其中空气检测系统被激活以向临床医生提供反馈。在将针的尖端推入感兴趣的介质中时,可操作地耦合到空气检测系统的通知系统(未示出)可以通知临床医生已检测到目标介质。然后,临床医生可以根据对目标介质的检测和对患者解剖结构的了解(例如,进一步推进、停止推进或缩回针)来对针的尖端进行定位。在适当放置针的尖端的情况下,可以执行从流体递送系统递送治疗流体(或其它治疗动作)。
与本公开和其主题有关的本领域普通技术人员将认识到,实施例可以包括比通过示例描述的或本文以其它方式设想的任何各个实施例中所示的更少的特征。本文描述的实施例并不意味着是可以组合和/或布置各种特征的方式的详尽呈现。因此,实施例不是特征的互斥组合;相反,如相关领域的普通技术人员所理解的,实施例可以包括从不同的各个实施例中选择的不同的各个特征的组合。而且,即使在此类实施例中没有描述,关于一个实施例描述的元件也可以在其它实施例中实施,除非另有说明。尽管从属权利要求可以在权利要求书中提及与一个或多个其它权利要求的特定组合,但是其它实施例也可以包含从属权利要求与每个其它从属权利要求的主题的组合,或者一个或多个特征与其它从属或独立权利要求的组合。除非指出不意在进行特定的组合,否则在本文中提出了这样的组合。此外,还意在将权利要求的特征包含在任何其它独立权利要求中,即使所述权利要求不是直接从属于所述独立权利要求也是如此。
通过引用上述文件进行的任何合并都是有限的,因此没有违反本文明确公开的主题被合并。上述文献的任何以引用方式的并入进一步受到限制,以使得文献中所包括的权利要求不会以引用的方式并入本文中。上述文献的任何以引用方式的并入更进一步受到限制,以使得除非明确包括于本文中,否则文献中所提供的任何定义不会以引用的方式并入本文中。
- 医疗装置位置检测系统、医疗装置引导系统、医疗装置引导系统的位置检测方法以及医疗装置引导系统的引导方法
- 医疗装置的位置检测系统、医疗装置引导系统及医疗装置的位置检测方法
