一种生物标志物及其在慢性阻塞性肺疾病诊断方面的应用
文献发布时间:2024-01-17 01:26:37
技术领域
本发明涉及生物医学和分子生物学技术领域,具体而言,涉及一种生物标志物及其在慢性阻塞性肺疾病诊断方面的应用。
背景技术
慢性阻塞性肺疾病(Chronic obstructive pulmonary disease,COPD)是最常见的慢性呼吸道疾病,其临床特征表现为持续存在的气流受限和相应的呼吸系统症状,如呼吸道粘液分泌过多、慢性支气管炎和肺气肿等。
根据《慢性阻塞性肺疾病诊治指南(2021年修订版)》,COPD的诊断主要依据危险因素暴露史、症状、体征及肺功能检查等临床资料,并排除可引起类似症状和持续气流受限的其它疾病,综合分析确定。其中,肺功能检查表现为持续气流受限是确诊COPD的必备条件,吸入支气管舒张剂后FEV1/FVC<70%即明确存在持续的气流受限。此外,COPD应与哮喘、支气管扩张症、充血性心力衰竭、肺结核和弥漫性泛细支气管炎等疾病进行鉴别。应注意当哮喘发生气道重塑时,可导致气流受限的可逆性减少,需全面分析患者的临床资料才能做出正确的判断。由此可见,当前临床上COPD的诊断标准复杂且具有异质性。
最新研究表明COPD与肠道菌群密切相关,其中COPD患者或模型动物肠道微生物组成结构明显失调,将COPD患者粪菌移植给健康小鼠,后者能表现出明显的肺功能下降、黏液分泌增多和炎症,说明肠道菌群失调可能是导致COPD发生的因素之一。随后的研究通过粪菌移植、合笼饲养和无菌小鼠等技术进一步证实了肠道菌群失调能促进COPD发生发展。尽管这些研究报道了肠道菌群失调能影响COPD进程,但是肠道菌群是否能区分COPD仍有待研究。
鉴于此,特提出本发明。
发明内容
本发明的目的在于提供一种生物标志物及其在慢性阻塞性肺疾病诊断方面的应用,利用本发明的生物标志物能够实现慢性阻塞性肺疾病的早期诊断,且具有较高的灵敏度和特异性。
本发明是这样实现的:
第一方面,本发明提供了一种生物标志物,其包括普通拟杆菌
更佳地,该生物标志物为普通拟杆菌
经试验证明,普通拟杆菌
上述生物标志物来自受试者的待测样品,其中待测样品包括受试者粪便、唾液、痰液和肺泡灌洗液。
第二方面,本发明还提供了检测上述生物标志物的物质在制备用于诊断受试者是否患有慢性阻塞性肺疾病的产品中的应用。
第三方面,本发明还提供了一种产品,其包括用于检测上述生物标志物的物质,该产品可用于诊断受试者是否患有慢性阻塞性肺疾病。
上述产品包括检测待测样品中生物标志物的丰度的试剂盒,在试剂盒中可包括针对慢性阻塞性肺疾病生物标志物的引物探针组合或其他检测试剂。
上述生物标志物的丰度信息是利用测序方法得到的,包括:从样本中分离得到核酸样本,基于所获得的核酸样本,构建DNA文库, 对DNA文库进行测序,以便获得测序结果,以及基于测序结果,将测序结果与参考基因集进行比对,以确定上述生物标志物的丰度信息。
第四方面,本发明还提供了上述生物标志物作为靶点用于筛选预防或治疗慢性阻塞性肺疾病的药物的应用。
具体地,该应用为:利用候选药物使用前和使用后对生物标志物的影响,从而确定候选药物是否可以用于预防或治疗慢性阻塞性肺疾病。
其中,上述生物标志物包括普通拟杆菌
较佳地,该生物标志物为普通拟杆菌
更佳地,该生物标志物为普通拟杆菌
第五方面,本发明还提供了一种检测慢性阻塞性肺疾病生物标志物含量的试剂在构建预测慢性阻塞性肺疾病风险的计算模型中的应用,其中,计算模型的输入变量为慢性阻塞性肺疾病生物标志物的含量。
具体地,慢性阻塞性肺疾病生物标志物可以是普通拟杆菌
在本发明中,慢性阻塞性肺疾病生物标志物是普通拟杆菌
本发明具有以下有益效果:
本发明首次发现普通拟杆菌
附图说明
为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
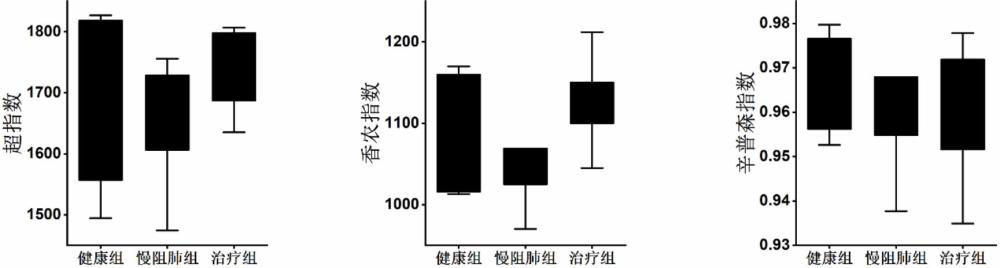
图1为实施例1中健康人群、COPD人群以及药物干预人群三组间肠道菌群多样性的分析结果;
图2为实施例1中健康人群、COPD人群以及药物干预人群三组间肠道菌群门水平组成结果图;
图3为实施例1中健康人群、COPD人群以及药物干预人群三组间肠道菌群属水平上组成结果图;
图4为实施例3中差异菌株与COPD肺功能指标的相关性的结果;
图5为实施例4中菌株组合对COPD的诊断能力的ROC曲线图;
图6为实施例5中菌株组合对COPD诊断能力验证的ROC曲线图。
具体实施方式
为使本发明实施例的目的、技术方案和优点更加清楚,下面将对本发明实施例中的技术方案进行清楚、完整地描述。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
为了评估肠道菌群组成能否作为慢性阻塞性肺疾病的诊断因子,本发明通过收集慢性阻塞性肺疾病患者和健康人的样本,进行全基因组测序以及使用生物信息学进行测序数据的统计,发现与疾病相关的肠道菌群,将肠道菌群与疾病信息整合,最大程度预测慢性阻塞性肺疾病。本发明通过全基因组测序,首次发现普通拟杆菌
当生物标志物在个体中指示异常进程、疾病或其他病症或作为异常进程、疾病或其他病症的标志时,该生物标志物与在个体中指示正常进程、无疾病或其他病症或作为正常进程、无疾病或其他病症的标志的生物标志物的水平或值相比较,通常被描述为含量高的或含量低的。“增加的”、“升高的”和其任何变化形式互换地用来指大于在健康或正常个体中通常检测到的生物标志物的值或水平(或值或水平的范围)的生物样品中的生物标志物的值或水平。
“减少的”、“降低的”和其任何变化形式互换地用来指小于在健康或正常个体中通常检测到的生物标志物的值或水平(或值或水平的范围)的生物样品中的生物标志物的值或水平。
此外,与在个体中指示正常进程或无疾病或其他病症或作为正常进程或无疾病或其他病症的标记的生物标志物的“正常”水平或值相比较,升高的或降低的生物标志物还可称作“差异的”或称作具有“差异水平”或“差异值”。因此,生物标志物的“差异丰度”还可称作生物标志物的“正常”水平的变化形式。
术语“生物标志物”应做广义理解,其包括任何能够反映异常状态的任何可检测生物指标,可以包含基因标志物、物种标志物(种标志物/属标志物)以及功能标志物。其中,基因标志物的含义并不局限于现有可以表达为且有生物活性的蛋白质的基因,还包括任何核酸片段,可以为DNA,也可以为RNA,可以是经修饰的DNA或者RNA,也可以为未经修饰的DNA或者RNA。特别地,本发明的生物标志物为微生物标志物。
本发明可以采用本领域普通技术人员已知的多种核酸以及蛋白技术进行检测微生物标志物的水平。
在本发明中,检测出微生物或测定微生物水平的制剂可以是引物,利用引物的序列扩增的方法可以是例如聚合酶链式反应(PCR)、逆转录-聚合酶链式反应(RT-PCR)、多重PCR、降落PCR、热启动PCR、巢式PCR、增效PCR、实时PCR、差示PCR、cDNA末端快速扩增、反向聚合酶链式反应、载体介导PCR、热不对称交错PCR、连接酶链式反应、修复链式反应、转录-介导的扩增、自主序列复制、目标碱基序列的选择性扩增反应。
在本发明中,术语“引物”是能够形成与模板链互补的碱基对,并且起到用于复制模板链的起始点作用的7~50个核酸序列。引物通常合成而得,但也可以使用自然生成的核酸。引物的序列并不一定需要与模板的序列完全相同,只要充分互补而能够与模板杂交即可。可以混入不改变引物的基本性质的追加特征。作为可以混入的追加特征的例子,有甲基化、带帽、一个以上的核酸被同系物取代和核酸间的修饰,但不限于此。
在本发明中,检测出微生物或测定微生物水平的制剂可以是抗体,通过使用将抗原-抗体反应作为基础的免疫学方法,可以检测出相应微生物或测定微生物水平。作为用于此的分析方法,有蛋白质印迹、酶联免疫吸附分析(ELISA,enzyme linkedimmunosorbentasay)、放射免疫分析(RIA:Radioimmunoassay)、放射免疫扩散法(radioimmunodiffusion)、欧氏(Ouchterlony)免疫扩散法、火箭(rocket)免疫电泳、组织免疫染色、免疫沉淀分析法(Immunoprecipitation assay)、补体结合分析法(ComplementFixation Assay)、荧光活化细胞分选器(FACS,Fluorescence activatedcell sorter)、蛋白芯片(protein chip)等,上述方法只是对抗体-抗原免疫反应的说明,本发明不限于上述方法。
本文中使用的术语“诊断”指的是区分或确定疾病、综合征或病症,或者指的是区分或确定患有特定的疾病、综合征或病症的人。在本发明的说明性实施方式中,基于分析样本中的菌群标志物来诊断对象中的慢性阻塞性肺疾病。
以下结合实施例对本发明的特征和性能作进一步的详细描述。
实施例1
本实施例为COPD患者肠道菌群组成结构的检测实验
1、研究对象和样本收集
本实施例的研究对象为COPD患者24例,COPD患者接受临床药物干预受试者18例,以及健康参与者28例。
COPD患者纳入标准:年龄大于40岁;按照COPD全球倡议(Global initiative forchronic obstructive lung disease, GOLD)颁布的“慢性阻塞性肺疾病诊断、处理和预防全球策略”标准,使用支气管扩张剂后,其1秒强力呼气容积与用力肺活量的比值小于0.7;在广州医科大学附属第一医院就诊。
健康对照纳入标准:年龄与患者匹配的体检正常人群。
排除标准:(1)除了COPD,有其他已知的呼吸道相关疾病的;(2)入组前1个月内COPD恶化者;(3)有肺手术和肺结核历史者;(4)癌症患者;(5)入组前1个月内输血者;(6)自身免疫疾病患者;(7)参与其他药物受试者;(8)入组前1个月服用抗生素或含有益生菌产品的。
COPD患者接受临床药物干预受试者的纳入标准:受试者为主要根据《慢性阻塞性肺疾病诊治指南(2021年修订版)》推荐标准、同时结合每位患者实际临床症状针对性进行药物干预的人群。
所有的受试者均了解本试验的背景、目的和意义,均提供手写的知情同意书。
2、样本收集
以参与研究的所有人员的粪便作为样本。
3、高通量微生物组测序
使用DNA提取试剂盒( 上海美吉生物医药科技有限公司)从样本中提取DNA,操作步骤按说明书进行。然后利用所提取的DNA样本进行高通量微生物组测序,基于测序数据,对各组肠道菌群多样性(超指数、香农指数和辛普森指数)进行分析,并基于相似性≥97%原则在微生物分类学门、属、种水平上进行注释及丰度计算。
物种注释:使用DIAMOND软件将测序获得的基因集蛋白序列与NCBI非冗余蛋白序列数据库进行blastp同源性比对,得到同源物种信息,并基于相似性≥97%原则在微生物分类学门、属、种水平上进行聚类。
丰度计算:利用SAMTOOLS软件统计每个基因被比对上的reads条数,根据基因的长度,计算得到每个基因在样品中的丰度,并汇总成所有样本的基因丰度表。计算公式如下:
其中,r表示比对上基因的reads数目,L为基因的长度。
4、结果
如图1所示,健康人群、COPD人群以及药物干预人群这三组间超指数、香农指数和辛普森指数均无显著性差异,说明三组间肠道菌群多样性没有显著性改变。
如图2所示,在门水平上,共鉴定到15种菌门,其中,厚壁菌门丰度最高为56.47%,其次是拟杆菌门(26.35%)、变形菌门(8.35%)、放线菌门(6.42%)和疣微菌门(1.87%)等,丰度前5的菌门占总基因序列的99.46%。
如图3所示,在属水平上,共鉴定到112种菌属,其中拟杆菌属丰度最高为20.71%,其次是粪杆菌属(11.11%)、志贺菌属(6.29%)、巨单胞菌属(6.26%)、Subdoligranulum(4.74%)和双歧杆菌属(3.60%)等。
在种水平上,共鉴定出151种菌株,其中普通拟杆菌(
表1 在微生物分类学种水平上平均丰度大于0.05的菌株
实施例2
本实施例为实施例1中的肠道差异菌株与COPD的相关性试验
如表1所示,在151种菌株中,普通拟杆菌、梭状芽孢杆菌CIEAF 020和毛螺科菌28-4在三组间丰度明显差异,其中,相较于Control组,普通拟杆菌丰度在COPD组粪便中明显降低,而药物干预后其含量升高。而梭状芽孢杆菌CIEAF 020和毛螺科细菌28-4丰度在COPD人群显著升高,药物干预后明显降低。
如图4所示,利用测序获得差异菌株丰度和受试者肺功能指标(FVC%、FEV1、FEV1%、FEV1/FVC%),基于皮尔森相关性原理,计算差异菌株与受试者肺功能指标间的相关性系数和相关性统计学
实施例3
本实施例为检测实施例2中的差异菌株对COPD诊断能力的试验
基于微生物组学测序数据,本发明对三种差异菌株进行受试者特征曲线(ROC)分析,如表2所示,在健康人群和COPD人群中,普通拟杆菌AUC为0.96,敏感度为1.00,特异性为0.83,95%置信区间为0.90-1.00;梭状芽孢杆菌CIEAF 020的AUC为0.81,敏感度为0.79,特异性为0.92,95%置信区间为0.62-0.99;毛螺科细菌28-4的AUC为0.82,敏感度为1.00,特异性为0.67,95%置信区间为0.57-1.00。
在COPD人群与药物干预人群中,普通拟杆菌AUC为0.96,敏感度为0.92,特异性为0.90,95%置信区间为0.92-1.00;梭状芽孢杆菌CIEAF 020的AUC为0.80,敏感度为0.92,特异性为0.83,95%置信区间为0.70-0.97;毛螺科细菌28-4的AUC为0.68,敏感度为0.67,特异性为0.83,95%置信区间为0.35-1.00。
表2差异菌株对COPD的诊断能力
实施例4
本实施例为普通拟杆菌和梭状芽孢杆菌CIEAF 020的菌株组合对COPD的诊断效果检测
选取上述AUC≥0.80的两种菌(普通拟杆菌和梭状芽孢杆菌CIEAF 020),通过二元回归分析将其进行组合,如图5的ROC分析显示,菌株组合在区分健康人群和COPD人群的AUC为0.98,敏感度为0.86,特异性为1.00,95%置信区间为0.90-1.00;菌株组合在区分COPD人群和药物干预人群的AUC为0.97,敏感度为1.00,特异性为0.83,95%置信区间为0.89-1.00。
实施例5
本实施例为差异菌株对COPD诊断价值的验证试验
本发明选取另一组受试者(健康人群11人、COPD人群10人和COPD药物治疗人群5人)作为验证组,并对其粪便进行高通量测序,计算物种相对丰度,并根据其丰度,利用ROC曲线计算普通拟杆菌和梭状芽孢杆菌CIEAF 020对COPD的诊断能力。其结果如表3和图6所示。
表3差异菌株对COPD的诊断能力验证
如表3所示:在健康人群和COPD人群中,普通拟杆菌AUC为0.87,95%置信区间为0.70-1.00,敏感度为0.91,特异性为0.90;梭状芽孢杆菌CIEAF 020的AUC为0.84,敏感度为0.91,特异性为0.90,95%置信区间为0.62-1.00;如图6A所示,菌株组合的AUC为0.95,敏感度为0.91,特异性为0.90,95%置信区间为0.85-1.00。
如表3和图6B所示:在COPD人群和COPD药物干预组中,普通拟杆菌AUC为0.80,敏感度为0.90,特异性为0.67,95%置信区间为0.57-1.00;梭状芽孢杆菌CIEAF 020的AUC为0.82,敏感度为0.80,特异性为1.00,95%置信区间为0.59-1.00;菌株组合的AUC为0.87,敏感度为0.90,特异性为0.83,95%置信区间为0.68-1.00。
以上结果表明,本发明公开的生物标志物具有较高的准确度和特异性,具有良好的开发为诊断方法的前景,从而为COPD的诊断以及寻找潜在药物靶点提供依据。
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
