一种α-烯基-β-氨基腈化合物的合成方法
文献发布时间:2024-04-18 19:58:30
技术领域
本发明涉及一种化合物及其化学合成方法,是一种具有高区域选择性的
背景技术
β
在过去的二十年里,联烯因为结构独特,被广泛研究。目前,利用联烯在镍催化下与氢氰酸或其替代物能发生氢氰化反应,可以得到有区域选择性的加成产物(
发明内容
本发明的目的是提供一种构建α-烯基-
本发明是采用以下具体技术方案来实现的:
本发明公开了一种存在高区域选择性的氰化产物,结构如下所示:
其中R为苯基,为邻位、对位或间位具有给电子或者吸电子的芳基或烷基。
本发明还公开一种高区域选择性构建α-烯基-
其中所述的R为苯基,为邻位、对位或间位具有给电子或者吸电子的芳基或烷基;镍催化剂为Ni(COD)
作为进一步地改进,具体操作步骤如下:
在手套箱里,干燥的反应管中加入Ni(COD)
反应完成后,将产物进行冷却,浓缩,柱层析提纯获得最终产物。
所述柱层析的洗脱液为石油醚和乙酸乙酯的混合溶剂,石油醚和乙酸乙酯的体积比为2:1。
所述的联烯基胺化合物和镍催化剂的摩尔比为1:0.1。
作为进一步地改进,本发明所述的溶剂为甲苯、二甲基苯、异丙基苯、乙苯、四氢呋喃、甲基叔丁基醚、1,4-二氧六环、乙腈;优选地,为甲苯。
作为进一步地改进,本发明所述的双磷配体为以下结构:
优选地,所述配体为L6。
作为进一步地改进,本发明所述的反应温度为40-80 ℃;优选地,为60 ℃。
作为进一步地改进,本发明所述的联烯基胺化合物和丙酮氰醇的摩尔比为1:1-3;优选地,为1:3。
作为进一步地改进,本发明所述的联烯基胺化合物和配体L6的摩尔比为1:0.1和1:0.2;优选地,为1:0.1。
作为进一步地改进,本发明所述的反应时间为12-18小时;优选地,为12小时。
本发明的优点为:原料试剂简单易得,制备方便;反应条件温和,操作简单,反应活性高,底物普适性广,且有依然保持较高的区域选择性。
附图说明
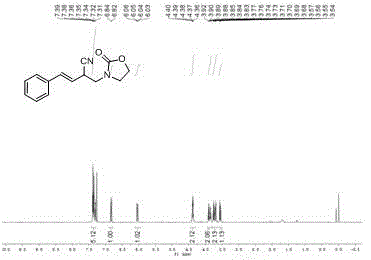
图1和2分别是实施例1所得产物核磁氢谱图和碳谱图;
图3和4分别是实施例2所得产物核磁氢谱图和碳谱图;
图5和6分别是实施例3所得产物核磁氢谱图和碳谱图;
图7和8分别是实施例4所得产物核磁氢谱图和碳谱图;
图9和10分别是实施例5所得产物核磁氢谱图和碳谱图;
图11和12分别是实施例6所得产物核磁氢谱图和碳谱图;
具体实施方式
下面结合具体实施例对本发明作进一步详细地描述,但本发明的实施方式不限于此。
实施例1
在手套箱里,反应管中加入Ni(COD)
1
3a结构为:
实施例2
在手套箱里,反应管中加入Ni(COD)
1
3b结构为:
实施例3
在手套箱里,反应管中加入Ni(COD)
1
3c结构为:
实施例4
在手套箱里,反应管中加入Ni(COD)
1
3d结构为:
实施例5
在手套箱里,反应管中加入Ni(COD)
1
3e结构为:
实施例6
在手套箱里,反应管中加入Ni(COD)
1
3f结构为:
- 一种Z-2-硒氰酸酯基烯基芳基砜化合物及其合成方法
- 一种4-甲基-N-苯基-N-(2-苯基丙-1-烯基)苯磺酰胺类化合物的合成方法
- 氢氧化胆碱促进的一锅法合成2-氨基-3-腈基-7-羟基-4H-色烯衍生物的方法
- 2-氨基-3-腈基-4-硝甲基-4H-色烯及其衍生物的合成方法
