基于人体生理模型的心肺复苏除颤一体机控制系统及方法
文献发布时间:2023-06-19 19:30:30
技术领域
本发明涉及医疗器械技术领域,特别是基于人体生理模型的心肺复苏除颤一体机控制系统及方法。
背景技术
徒手CPR对操作者的要求较高,常常由于按压部位不准、用力方法不对、按压深度掌握不好、按压频率不规律等因素,难以达到理想的效果,甚至造成骨折、气胸、血胸等严重的并发症,因此,只有综合患者血流灌注程度和胸骨骨折危险性才能得到满足患者个体特征的最佳胸外按压深度。但是目前国际上缺乏对胸外按压利弊权衡问题的关注,众多的自动胸外装备的按压深度恒定,并不能依据患者的个体差异进行按压利弊权衡后的优化胸外按压。权衡胸外按压利弊的机制尚未建立。同时口对口进行人工呼吸也有可能在病人与救助者间传染疾病。因此,抢救迅速、定位精准、按压适度的心肺复苏机是有必要的,其及时性和准确性可以显著提高救治效果。
国内外存在一些心肺复苏机的产品,但其成本较高、机器较重,而且未考虑到将除颤加入实现一体化。目前,心肺复苏仪为单独运行,且大部分地区只配备了心肺复苏机或除颤仪之一,然而在急救过程中,心肺复苏机和除颤仪的配合是非常重要的,进行胸外按压的目的是为了手动泵血,把血挤压到全身各个脏器,防止各个脏器因缺血、缺氧而坏死。但是要让患者恢复心跳还得用AED让其紊乱的心脏节律恢复正常。高质量的心肺复苏可以提高除颤的成功率。最主要的是,患者未必一次除颤就可以恢复正常心率,因此AED和心肺复苏交替进行,缺一不可。安装后按照程序设计要求,根据指南标准给予按压,只完成了按压工作,如果患者通过按压出现室颤时,需要给予电除颤,而此时需要将该仪器搬离患者,再给予除颤,除颤后要求为立即按压,这时需要重新安装心肺复苏仪,在搬离、除颤与再安装的过程就是时间的流逝,患者被成功救治的可能性也在大大降低。
发明内容
针对上述缺陷,本发明提出了基于人体生理模型的心肺复苏除颤一体机控制系统及方法,其目的在于解决了现有需要交替更换心肺复苏仪和除颤仪来对患者进行救治,导致患者被成功救治大大降低的问题。
为达此目的,本发明采用以下技术方案:
基于人体生理模型的心肺复苏除颤一体机控制系统,包括
生理信号采集模块,用于采集患者的心电图特征数据和按压特征数据;
发送模块,用于将心电图特征数据和按压特征数据发送至主控模块;
主控模块,用于计算获得心肺特征结果,以及计算BI值、RI值和BRI值,并得到对应的分级级别;
按压判断模块,用于根据分级级别判断患者在按压过程中的心肺复苏效果和骨折风险,如果BRI<5,则继续判断BI和RI,若BI<4.5,则逐渐增加按压力度,直到BI>4.5,若RI>3.4,则逐渐减小按压力度,直到RI<3.4;同时根据心肺特征结果判断是否发生室颤,如果是,则停止按压,进行除颤;
除颤判断模块,用于在除颤过程中根据心肺特征结果判断是否仍然发生室颤,如果是,则继续除颤。
优选地,所述BI值的计算公式如下:
其中,BI代表有益指数,PETCO2代表呼吸末时测量得到的CO
所述RI值的计算公式如下:
其中,RI代表危险指数,Kchest代表胸骨弹性模量,指的是按压单位位移所需要的作用力值,K5代表成人在胸外按压深度为5cm,K6.5代表成人在胸外按压深度为6.5cm;
所述BRI值的计算公式如下:
其中,BRI代表有益危险度综合指数。
优选地,所述按压判断模块包括阻抗控制子模块,所述阻抗控制子模块用于建立阻抗模型;计算获得胸外按压的反作用弹力误差值,所述反作用弹力误差值的计算公式如下:
ΔF(t)=F
其中,ΔF(t)为反作用弹力误差值,F
其中,M
将反作用弹力误差值输入阻抗模型,得到频率域;根据频率域,对反作用弹力信号进行滤波,并将滤波后的反作用弹力信号转化为相应的末端位置的运动信号。
优选地,所述主控模块包括心电信号预处理子模块,所述心电信号预处理子模块用于通过设置自适应阈值,定位QRS群波,其中,自适应阈值的计算公式如下:
/>
其中,THR1为高阈值;mean(peak_buffer)为峰值均值;peak为此刻检测到的信号峰值;THR1_lim为经验常数,代表阈值变化的上界,取值为0.33;THR2为低阈值;peak_buffer为存储此刻峰值之前的8个连续峰值的缓冲值;TRH2_lim也为经验常数,代表阈值变化的下界,取值为0.23。
优选地,所述主控模块还包括心率失常识别子模块,所述心率失常识别子模块用于提取心电信号特征;选取和划分数据集,得到训练集和测试集;对训练集和测试集的数据进行特征归一化处理;训练和测试支持向量机模型,将预处理后心电信号输入支持向量机模型进行分类。
本申请的另一方面提供了基于人体生理模型的心肺复苏除颤一体机控制方法,包括以下步骤:
步骤S1:采集患者的心电图特征数据和按压特征数据;
步骤S2:根据心电图特征数据和按压特征数据,计算获得心肺特征结果,以及BI值、RI值和BRI值对应的分级级别;
步骤S3:根据分级级别判断患者在按压过程中的心肺复苏效果和骨折风险,如果BRI<5,则继续判断BI和RI,若BI<4.5,则逐渐增加按压力度,直到BI>4.5,若RI>3.4,则逐渐减小按压力度,直到RI<3.4;同时根据心肺特征结果判断是否发生室颤,如果是,则停止按压,进行除颤;
步骤S4:在除颤过程中根据心肺特征结果判断是否仍然发生室颤,如果是,则继续除颤。
优选地,在步骤S3中,具体包括阻抗控制子步骤:
步骤S31:建立阻抗模型;
步骤S32:计算获得胸外按压的反作用弹力误差值,所述反作用弹力误差值的计算公式如下:
ΔF(t)=F
其中,ΔF(t)为反作用弹力误差值,F
其中,M
步骤S33:将反作用弹力误差值输入阻抗模型,得到频率域;
步骤S34:根据频率域,对反作用弹力信号进行滤波,并将滤波后的反作用弹力信号转化为相应的末端位置的运动信号。
优选地,在步骤S2中,具体包括心电信号预处理子步骤:通过设置自适应阈值,定位QRS群波,其中,自适应阈值的计算公式如下:
其中,THR1为高阈值;mean(peak_buffer)为峰值均值;peak为此刻检测到的信号峰值;THR1_lim为经验常数,代表阈值变化的上界,取值为0.33;THR2为低阈值;peak_buffer为存储此刻峰值之前的8个连续峰值的缓冲值;TRH2_lim也为经验常数,代表阈值变化的下界,取值为0.23;
还包括心率失常识别子步骤:提取心电信号特征;选取和划分数据集,得到训练集和测试集;对训练集和测试集的数据进行特征归一化处理;训练和测试支持向量机模型,将预处理后心电信号输入支持向量机模型进行分类。
本申请实施例提供的技术方案可以包括以下有益效果:
1、本方案通过BI值、RI值和BRI值对应的分级级别综合评估判断患者的血流灌注程度和胸骨骨折危险程度,能够更好地预测患者在做心肺复苏过程中的受伤概率,减少患者受伤的机率。
2、在按压过程中根据心肺特征结果,自动判断患者的生理状况是否需要进行除颤操作,这样大大节省了更换心肺复苏仪以及除颤仪的时间,使得患者被成功救治的可能性大大提高。
附图说明
图1是一种基于人体生理模型的心肺复苏除颤一体机的结构示意图;
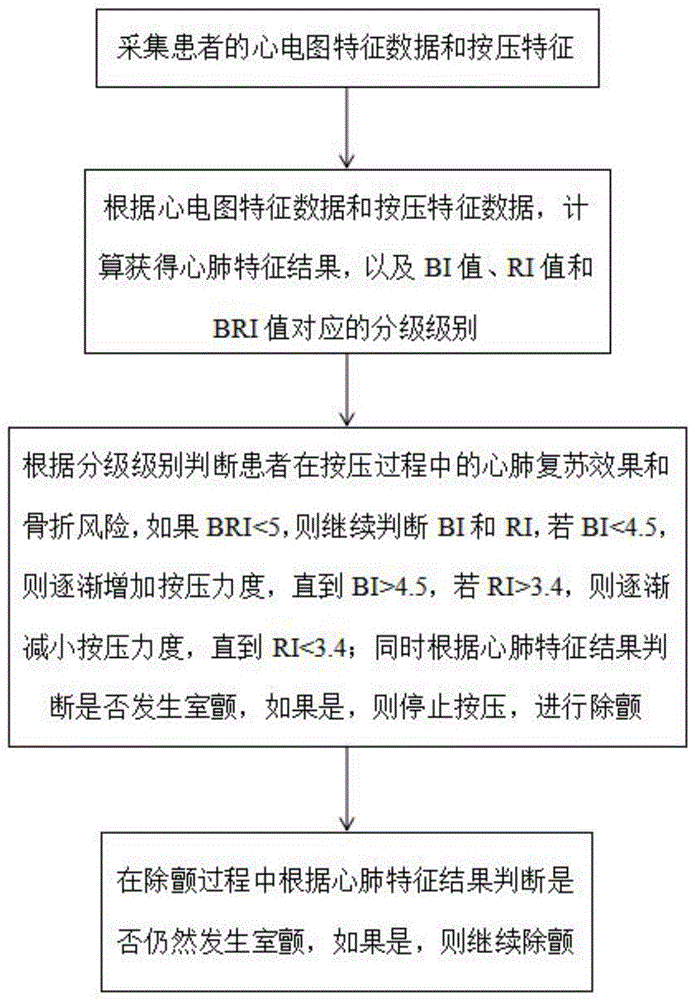
图2是一种基于人体生理模型的心肺复苏除颤方法的步骤流程图。
其中,1、主机外壳;2、显示屏幕;3、电极片;4、推杆;5、按压头;6、垫板;7、绷带。
具体实施方式
下面详细描述本发明的实施方式,实施方式的示例在附图中示出,其中,相同或类似的标号自始至终表示相同或类似的元件或具有相同或类似功能的元件。下面通过参考附图描述的实施方式是示例性的,仅用于解释本发明,而不能理解为对本发明的限制。
基于人体生理模型的心肺复苏除颤一体机控制系统,包括
生理信号采集模块,用于采集患者的心电图特征数据和按压特征数据;
发送模块,用于将心电图特征数据和按压特征数据发送至主控模块;
主控模块,用于计算获得心肺特征结果,以及计算BI值、RI值和BRI值,并得到对应的分级级别;
按压判断模块,用于根据分级级别判断患者在按压过程中的心肺复苏效果和骨折风险,如果BRI<5,则继续判断BI和RI,若BI<4.5,则逐渐增加按压力度,直到BI>4.5,若RI>3.4,则逐渐减小按压力度,直到RI<3.4;同时根据心肺特征结果判断是否发生室颤,如果是,则停止按压,进行除颤;
除颤判断模块,用于在除颤过程中根据心肺特征结果判断是否仍然发生室颤,如果是,则继续除颤。
本方案的基于人体生理模型的心肺复苏除颤一体机控制系统,该系统是以FPGA控制器作为心肺复苏除颤一体机的载体,由于FPGA控制器独特的硬件描述语言以及内部结构,使得各种算法可以并行实现,在延迟方面,FPGA要优于GPU,FPGA在可以提供很高的带宽的同时也可以降低延迟,大大提高了运算速度。如图1所示,心肺复苏除颤一体机除包括FPGA控制器、主机外壳1、显示屏幕2、两个电极片3、推杆4、吸盘式的硅胶按压头5、垫板6和绷带7,所述主机外壳1的内部设置有所述FPGA控制器,所述主机外壳1的外部设置有显示屏幕2,所述显示屏幕2与所述FPGA控制器电性连接。两个所述电极片3均电性连接于所述FPGA控制器。所述主机外壳1的内部还设置有电机和伺服电缸,所述电机的驱动端连接于所述伺服电缸,所述推杆4的一端连接于所述伺服电缸,所述推杆4的另一端连接于所述吸盘式的硅胶按压头5。所述垫板6用于放置患者,所述绷带7用于将患者固定在所述垫板6上。
当患者发生心跳骤停时,救助者迅速帮患者穿戴上心肺复苏除颤一体机,将两个所述电极片3贴至正确的位置,具体的,正极贴在患者的右侧锁骨下,负极贴在患者左侧乳头外下方。打开心肺复苏除颤一体机,心肺复苏除颤一体机控制系统中的生理信号采集模块会采集患者的心电图特征数据和按压特征数据,通过发送模块将心电图特征数据和按压特征数据发送至主控模块,主控模块计算获得心肺特征结果,以及计算BI值、RI值和BRI值,并得到对应的分级级别,其中,BI值、RI值和BRI值为三个量化指标,BI指的是有益指数,用于反映血流灌注程度;RI指的是危险指数,用于辨别胸骨骨折危险程度;BRI指的是有益危险度综合指数,用于综合评估心肺复苏期间胸外按压的利弊特征。得到的心肺特征结果和BI值、RI值和BRI值对应的分级级别会在所述显示屏幕2中显示。心肺复苏除颤一体机进行心肺复苏,具体的,通过启动所述电机,所述电机驱动所述伺服电缸运动,所述伺服电缸驱动所述推杆4上下运动实现按压,其优点是结构简单,重量较轻,减少了患者胸口部位的压力,同时,也可满足AHA中规定的按压深度以及频率。由于所述推杆4连接于所述吸盘式的硅胶按压头5,可以更好的保护患者的胸部不受外部的损伤,并且可以使得患者的胸部充分回弹,达到更好的心肺复苏效果。
心肺复苏除颤一体机控制系统中的按压判断模块会根据分级级别判断患者在按压过程中的心肺复苏效果和骨折风险,如果BRI<5,则继续判断BI和RI,若BI<4.5,则逐渐增加按压力度,直到BI>4.5,若RI>3.4,则逐渐减小按压力度,直到RI<3.4;同时根据心肺特征结果判断是否发生室颤,如果是,则停止按压,进行除颤;除颤判断模块在除颤过程中根据心肺特征结果判断是否仍然发生室颤,如果是,则继续除颤。
本方案中,通过设置按压判断模块,按压判断模块会综合评估判断患者的血流灌注程度和胸骨骨折危险程度,能够更好地预测患者在做心肺复苏过程中的受伤概率,减少患者受伤的机率。通过设置除颤判断模块,除颤判断模块会在按压过程中从心肺特征结果判断的反馈,自动判断患者的生理状况是否需要进行除颤操作,这样大大节省了更换心肺复苏仪以及除颤仪的时间,使得患者被成功救治的可能性大大提高。
优选的,所述BI值的计算公式如下:
其中,BI代表有益指数,PETCO2代表呼吸末时测量得到的CO
所述RI值的计算公式如下:
其中,RI代表危险指数,Kchest代表胸骨弹性模量,指的是按压单位位移所需要的作用力值,K5代表成人在胸外按压深度为5cm,K6.5代表成人在胸外按压深度为6.5cm;
所述BRI值的计算公式如下:
其中,BRI代表有益危险度综合指数。
本实施例中,BI值代表有益指数,反映血流灌注程度。呼吸末二氧化碳含量PETCO2在心肺复苏过程中可以作为检测心肺复苏质量的有效生理指标,正因为PETCO2具有检测简单,使用广泛,与心肺复苏的重要指标血流灌注的程度相关性强的优点,因此用PETCO2作为反馈血流灌注程度的生理参数。为了量化胸外按压有益程度,将PETCO2作为BI值,并将其量化至0-10范围,依照PETCO2反映的血流灌注程度和预测自主循环回复成功的可能性,可将BI分为3级,PETCO2值越大,灌注程度越好,有益等级越高,分数越大,具体的,第一级的PETCO2范围从0mmHg到10mmHg,第二级的PETCO2范围从10mmHg到15mmHg,第三级的PETCO2的范围是从15mmHg到21mmHg,或高于21mmHg。
RI代表危险指数,用于辨识胸骨骨折危险程度。胸骨弹性模量Kchest与胸骨骨折的风险呈负相关性。因此,选择胸骨弹性模量Kchest作为反映胸骨骨折的风险指标,为量化由于胸骨弹性模量Kchest造成的胸骨骨折危险性,依照胸骨弹性模量Kchest的大小将RI量化到0-10的范围,并根据胸骨弹性模量Kchest大小导致胸骨骨折危险程度将其划分为4个等级。2010年AHA心肺复苏和心血管急救指南明确指出,胸外按压深度应使胸骨下陷至少5cm。根据这个要求,按压深度小于5cm的胸外按通常不会对典型的人体胸骨造成危害。临床实践表明,大多数施救人员的胸外按压深度不超过6cm,超过6cm的胸外按压通常被认为是过度按压,容易导致胸骨骨折。因此,在K0-K5范围内的Kchest认为是无危害的,将这一范围内的Kchest划分为第1级,第1级的RI值为0。最高一级的胸骨弹性模量值从K6到K6.5,或在K6.5之上。而在K5到K6之间的胸骨弹性模量被认为是中间级。为了取得更好的RI分辨率,RI的中间级又被分为较大和较小两个危险量等级,第二级的胸骨弹性模量从K5到K5.5,第三级的胸骨弹性模量从K5.5到K6。
为了综合评估心肺复苏期间胸外按压利弊特性,提出了有益危险度综合指数BRI。BRI是评价胸外按压质量的定量指标,可以基于BI和RI得到,若BRI的范围从0到10。若BRI大于5,则利大于弊;若BRI小于5,则弊大于利。
优选的,所述按压判断模块包括阻抗控制子模块,所述阻抗控制子模块用于建立阻抗模型;计算获得胸外按压的反作用弹力误差值,所述反作用弹力误差值的计算公式如下:
ΔF(t)=F
其中,ΔF(t)为反作用弹力误差值,F
其中,M
将反作用弹力误差值输入阻抗模型,得到频率域;根据频率域,对反作用弹力信号进行滤波,并将滤波后的反作用弹力信号转化为相应的末端位置的运动信号。
本实施例中,当按压头5对患者进行按压的过程中,按压头5的按压使患者的胸腔下陷,并会收到胸腔给的一个反作用力。式(3)表示同时考虑位置、速度和加速度的偏差时的模型,在使用阻抗控制时,这一方法表达的是按压过程中环境力的误差和位置误差的关系,胸外按压不仅要实现对按压深度(位置)的控制,也要实现对力度的控制。通过建立阻抗模型;计算获得胸外按压的反作用弹力误差值;将反作用弹力误差值输入阻抗模型,得到频率域;根据频率域,对反作用弹力信号进行滤波,并将滤波后的反作用弹力信号转化为相应的末端位置的运动信号,从阻抗模型中可以看出,通过调节阻抗控制的质量参数、阻尼参数和刚度参数,可以调节按压头末端和胸腔之间弹力和位置的关系。本方案利用阻抗控制对按压头的运动做规划,能够实现按压过程中同时对按压深度和力度进行控制。
优选的,所述主控模块包括心电信号预处理子模块,所述心电信号预处理子模块用于通过设置自适应阈值,定位QRS群波,其中,自适应阈值的计算公式如下:
其中,THR1为高阈值;mean(peak_buffer)为峰值均值;peak为此刻检测到的信号峰值;THR1_lim为经验常数,代表阈值变化的上界,取值为0.33;THR2为低阈值;peak_buffer为存储此刻峰值之前的8个连续峰值的缓冲值;TRH2_lim也为经验常数,代表阈值变化的下界,取值为0.23。
本实施例中,为了完成心电信号预处理中QRS波群的定位,主要通过设置自适应阈值来实现。由于心电信号是非平稳信号,在进行检测时,仅靠固定阈值难以满足所有的QRS波,易造成误检和漏检,而设置自适应阈值能较好地解决这个问题。进一步说明,自适应阈值要跟随波形即时变化,为了让阈值更加准确,采用双阈值的方法,具体是设置一高一低两个阈值。当信号中某个波峰超过设定的低阈值时,就判定一个QRS波,根据高低阈值和波峰振幅之间的关系,调整阈值的大小。为了保持心电信号波形变化的稳健,阈值还需要进行调整,调整的依据是之前检测到的正确波峰振幅变化,保证阈值不会太高或者太低。设置高低两个阈值相比于只有一个阈值来讲,可以在很大的程度上面捕捉到更多层次的波峰。在防“错检”方面,采用了“不应期”方式。当两个波峰距离较近时,只选取较大的波峰。这个过程指的是时间间隔低于0.24s,即不应期的长度;双阈值的数值存在下界,也在某种程度上防止了一些噪声被错检为QRS波。
优选的,所述主控模块还包括心率失常识别子模块,所述心率失常识别子模块用于提取心电信号特征;选取和划分数据集,得到训练集和测试集;对训练集和测试集的数据进行特征归一化处理;训练和测试支持向量机模型,将预处理后心电信号输入支持向量机模型进行分类。
本实施例中,所述心率失常识别子模块的设置有利于提高心电信号分类的敏感度。具体的,提取心电信号特征,首先加载ECG信号数据集,然后对数据集中的每个心拍进行5阶的小波分解,小波函数利用db6小波。经过5阶小波分解和2倍下的采样后,取小波变换系数中原信号的“近似”系数,即5阶分解后的a系数,选取这些系数作为每个心拍的特征值。选取和划分数据集,得到训练集和测试集,其中,训练集和测试集各有10000个样本。随机选取可通过建立randperm函数随机打乱样本索引,然后截取前10000个索引对应的样本作为训练集,剩余的作为测试集来实现。为了加快SVM的收敛,对训练集和测试集的数据进行特征归一化处理,实际操作时,先使用归一化函数的正常模式,对训练集特征归一化到0~1之间,得到归一化后的训练集后,使用归一化函数的apply模式,将训练集得到的归一化信息用至测试集,完成测试集的归一化。训练和测试支持向量机模型,调用libsvmtrain函数和libsvmpredict函数训练和测试模型。Libsvmtrain函数训练的默认核函数为RBF核函数,需要人为设定2个超参数——惩罚因子系数c和核函数参数g,分别将其设定为2和1。不同取值的c和g可能会导致差异较大的结果,如果想要取得更好的效果,必须进行“调参”,减轻欠拟合与过拟合问题。将预处理后心电信号输入支持向量机模型进行分类,当在2s内没有检测到一个完整的QRS波形,便判定为发生了室颤,并立刻停止按压,进行除颤操作。其中,除颤操作要进行三次,第一次除颤能量为200J,除颤完毕后进行判定,倘若仍然发生室颤,则第二次除颤能量为300J,继续判定是否发生室颤,倘若仍然发生室颤,第三次除颤能量为360J,第三次除颤完毕后进行按压操作,过了30s继续判断是否发生室颤。倘若还有室颤发生,则继续上述三次除颤操作。
本申请的另一方面提供了基于人体生理模型的心肺复苏除颤一体机控制方法,包括以下步骤:
步骤S1:采集患者的心电图特征数据和按压特征数据;
步骤S2:根据心电图特征数据和按压特征数据,计算获得心肺特征结果,以及BI值、RI值和BRI值对应的分级级别;
步骤S3:根据分级级别判断患者在按压过程中的心肺复苏效果和骨折风险,如果BRI<5,则继续判断BI和RI,若BI<4.5,则逐渐增加按压力度,直到BI>4.5,若RI>3.4,则逐渐减小按压力度,直到RI<3.4;同时根据心肺特征结果判断是否发生室颤,如果是,则停止按压,进行除颤;
步骤S4:在除颤过程中根据心肺特征结果判断是否仍然发生室颤,如果是,则继续除颤。
本方案中的基于人体生理模型的心肺复苏除颤一体机控制方法,如图2所示,通过BI值、RI值和BRI值对应的分级级别综合评估判断患者的血流灌注程度和胸骨骨折危险程度,能够更好地预测患者在做心肺复苏过程中的受伤概率,减少患者受伤的机率。在按压过程中根据心肺特征结果,自动判断患者的生理状况是否需要进行除颤操作,这样大大节省了更换心肺复苏仪以及除颤仪的时间,使得患者被成功救治的可能性大大提高。
进一步说明,所述BI值的计算公式如下:
其中,BI代表有益指数,PETCO2代表呼吸末时测量得到的CO
所述RI值的计算公式如下:
其中,RI代表危险指数,Kchest代表胸骨弹性模量,指的是按压单位位移所需要的作用力值,K5代表成人在胸外按压深度为5cm,K6.5代表成人在胸外按压深度为6.5cm;
所述BRI值的计算公式如下:
其中,BRI代表有益危险度综合指数。
优选的,在步骤S3中,具体包括阻抗控制子步骤:
步骤S31:建立阻抗模型;
步骤S32:计算获得胸外按压的反作用弹力误差值,所述反作用弹力误差值的计算公式如下:
ΔF(t)=F
其中,ΔF(t)为反作用弹力误差值,F
其中,M
步骤S33:将反作用弹力误差值输入阻抗模型,得到频率域;
步骤S34:根据频率域,对反作用弹力信号进行滤波,并将滤波后的反作用弹力信号转化为相应的末端位置的运动信号。
本实施例中,通过调节阻抗控制的质量参数、阻尼参数和刚度参数,可以调节按压头末端和胸腔之间弹力和位置的关系。本方案利用阻抗控制对按压头的运动做规划,能够实现按压过程中同时对按压深度和力度进行控制。
优选的,在步骤S2中,具体包括心电信号预处理子步骤:通过设置自适应阈值,定位QRS群波,其中,自适应阈值的计算公式如下:
其中,THR1为高阈值;mean(peak_buffer)为峰值均值;peak为此刻检测到的信号峰值;THR1_lim为经验常数,代表阈值变化的上界,取值为0.33;THR2为低阈值;peak_buffer为存储此刻峰值之前的8个连续峰值的缓冲值;TRH2_lim也为经验常数,代表阈值变化的下界,取值为0.23;
还包括心率失常识别子步骤:提取心电信号特征;选取和划分数据集,得到训练集和测试集;对训练集和测试集的数据进行特征归一化处理;训练和测试支持向量机模型,将预处理后心电信号输入支持向量机模型进行分类。
本实施例中,由于心电信号是非平稳信号,在进行检测时,仅靠固定阈值难以满足所有的QRS波,易造成误检和漏检,而设置自适应阈值能较好地解决这个问题,这种基于自适应阈值的心电信号预处理,对消除噪声有明显效果,使得波形特征看起来更单一。本方案还结合基于支持向量机的心率失常识别,能够有效提高心电信号分类的敏感度。
此外,在本发明的各个实施例中的各功能单元可以集成在一个处理模块中,也可以是各个单元单独物理存在,也可以两个或两个以上单元集成在一个模块中。上述集成的模块既可以采用硬件的形式实现,也可以采用软件功能模块的形式实现。所述集成的模块如果以软件功能模块的形式实现并作为独立的产品销售或使用时,也可以存储在一个计算机可读取存储介质中。
尽管上面已经示出和描述了本发明的实施方式,可以理解的是,上述实施方式是示例性的,不能理解为对本发明的限制,本领域的普通技术人员在本发明的范围内可以对上述实施例进行变化、修改、替换和变型。
- 便携式心肺复苏除颤一体机、使用方法及心电图降噪方法
- 一种心肺复苏除颤一体机的控制方法及系统
