含有硝苯地平和利多卡因的局部擦拭物
文献发布时间:2024-04-18 20:01:55
相关申请的交叉引用
本申请根据35U.S.C.§119(e)要求2021年4月1日提交的美国临时专利申请第63/169,768号的优先权,所述申请的名称为“含有硝苯地平和利多卡因的局部擦拭物”,其内容通过引用以其全文特此并入本文中。
技术领域
本发明涉及治疗软组织损伤的领域,并且更具体地涉及用于在肛裂治疗中递送治疗性化合物的局部擦拭物。
背景技术
人体的器官和软组织,通常被定义为未被骨化或钙化硬化的组织,构成了人体组成的大部分。此类组织包括肌肉、肌腱、韧带、脂肪、皮肤等。软组织通常是非常有弹性的材料,能够经受显著的变形而不失效,恢复到它们的自然构造。不管怎样,在某些力和负荷下,即使软组织也会经历失效并可能撕裂。虽然许多此类撕裂是温和的,并且随着时间的推移会自然愈合,但一些撕裂更严重,可以导致不适和疼痛。此外,一些敏感部位的撕裂特别疼,会妨碍日常生活活动。由于禁忌和其他社会态度,身体某些部位的软组织损伤也令患者尴尬或难以讨论。
一个这样的示例是肛裂,通常定义为肛门周围组织的小撕裂。虽然此类撕裂在婴儿中最常见,但它们也可能发生在所有年龄段的人身上,并且大约每350个成人中就有1个出现这种情况。像大多数软组织损伤一样,浅层或表面裂缝通常会自行愈合,并且通过简单的治疗,相关的不适有时可以减轻,且愈合速度加快。然而,在一些情况下,严重的病例可能无法自然愈合,并且需要药物治疗或手术治疗。
已经使用药物如硝酸甘油软膏和钙通道阻滞剂(如硝苯地平、地尔硫卓和吲哚拉明)用于治疗肛裂。Golfam等人.(Acta medica Iranica,第48卷,第5期,2010,第295-299页)用含有0.5%硝苯地平的乳膏治疗慢性肛裂持续四周,并且发现70%的患者经历了愈合。Wise(U.S.10,543,201)用含有0.3%硝苯地平的局部组合物治疗肛门内括约肌和/或盆底肌。肛门内括约肌位于肛管深处(超过肛管1cm以上),并且如果不使用涂抹器装置或通过手指深度穿透,就不能将局部组合物应用到该组织上。凝胶或乳膏通常由患者用手指或用注射器或栓剂应用。患者用保鲜膜或一次性手套覆盖手指,将规定量的软膏挤到覆盖的手指上,然后用手指将软膏涂抹在受影响区域。这种类型的应用并不总是实用或舒适的。一些患者缺乏以这种方式应用软膏的灵活性或灵巧性。那些可以应用药膏的病人经常发现这个过程不舒适。这会导致不适当的或不完全的应用,这会限制治疗的有效性,或者根本阻止患者应用治疗。
发明内容
在一个方面,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计0.15%至7.5%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计0.15%至1.5%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在相关的方面,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计1.5%至7.5%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计0.3至1.5%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在相关的方面,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计0.15%、或0.2%、或0.25%、或0.3%、或0.35%、或0.4%、或0.45%、或0.5%、或0.8%、或1%、或1.2%或1.5%、或1.8%、或2%、或2.2%、或2.5%、或2.8%、或3%、或3.2%、或3.5%、或3.8%、或4%或4.2%、或4.5%或4.8%、或5%、或5.2%、或5.4%、或5.6%、或5.8%、或6%、或6.5%、或6.8%、或7%或7.5%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计0.15%、或0.18%、或0.2%、或0.22%、或.25%、或.28%、或.3%、或0.32%、或0.35%、或0.38%、或0.4%、或0.42%、或0.45%或0.5%、或0.55%、或0.6%、或0.65%、或0.7%、或0.75%、或0.80%、或0.85%、或0.90%、或0.95%、或1%、或1.2%、或1.5%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在相关的方面,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计1.5%、或1.8%、或2%、或2.2%、或2.5%、或2.8%、或3%、或3.2%、或3.5%、或3.8%、或4%或4.2%、或4.5%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计0.15%、或0.18%、或0.2%、或0.22%、或.25%、或.28%、或.3%、或0.32%、或0.35%、或0.38%、或0.4%、或0.42%、或0.45%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少1.5%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少0.3%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少1.5%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少0.2%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少1.5%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少0.1%硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少1.5%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少0.15%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少1.5%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少0.25%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少1.5%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少0.35%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少1.5%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少0.4%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少1.5%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少0.45%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少1.5%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少0.5%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少1.5%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少1%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少1.5%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少1.5%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少0.15%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少0.3%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少0.2%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少0.3%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少0.4%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少0.3%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少0.6%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少0.3%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少0.8%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少0.3%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少1%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少0.3%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少1.5%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少0.3%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少2%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少0.3%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少2.5%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少0.3%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少3%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少0.3%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少4%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少0.3%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少4.5%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少0.3%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少5%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少0.3%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少6%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少0.3%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少6.5%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少0.3%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少7%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少0.3%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在一些实施方案中,本公开提供了局部擦拭物,所述局部擦拭物包含用含有按浓度计至少7.5%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计至少0.3%w/w硝苯地平及其盐的溶液润湿的纤维基质材料。
在本文所述的任何擦拭物的一些实施方案中,包含纤维基质材料的局部擦拭物能够治疗肛裂,将所述纤维基质材料用含有按浓度计约0.15%-7.5%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计约0.3%至1.5%w/w硝苯地平及其盐的溶液润湿。
在本文所述的任何擦拭物的一些实施方案中,包含纤维基质材料的局部擦拭物能够治疗肛裂,将所述纤维基质材料用含有按浓度计约1.5%-5%w/w利多卡因及其盐(示例盐酸利多卡因)和按浓度计约0.15%至0.45%w/w硝苯地平及其盐的溶液润湿。
在本文所述的任何擦拭物的一些实施方案中,所述局部擦拭物还包含防腐剂。在一些实施方案中,所述局部擦拭物还包含抗氧化剂。在一些实施方案中,所述局部擦拭物还包含至少一种赋形剂。在一些实施方案中,赋形剂选自下组,该组由以下组成:抗氧化剂、渗透促进剂、防腐剂、保湿剂、分散剂、湿润剂、乳化剂、增塑剂、表面活性剂、粘度调节剂、润肤剂、成膜剂、拖尾溶剂、共溶剂和/或油。在一些实施方案中,局部擦拭物还包含醇溶剂。
在本文所述的任何擦拭物的一些实施方案中,所述擦拭物还包含渗透促进剂,所述渗透促进剂选自下组,该组由以下组成:苯甲醇、二甲基异山梨醇(DMI)、丙二醇、己二醇、异丙醇、乙醇、苯氧乙醇、油酸、油醇、肉豆蔻酸异丙酯、中链甘油三酯(MCT)和还原二元醇(transcutol)。
在本文所述的任何擦拭物的一些实施方案中,所述擦试物还包含湿润剂,所述湿润剂选自下组,该组由以下组成:丙烯酸酯、甘油、戊二醇、丁二醇、库拉索芦荟汁、提取物、己二醇、透明质酸和乳酸。
在本文所述的任何擦拭物的一些实施方案中,所述擦试物还包含乳化剂,所述乳化剂选自下组,该组由以下组成:聚山梨醇酯(20至80)、Span-80、PEG-40、氢化蓖麻油、十二烷基硫酸钠(SLS)、泊洛沙姆、脱水山梨醇(20-85)和甘油单油酸酯(GMO)。
在本文所述的任何擦拭物的一些实施方案中,所述擦试物还包含表面活性剂,所述表面活性剂选自下组,该组由以下组成:PEG 400、tween-80、油醇、甘油、己二醇和丙二醇。
在本文所述的任何擦拭物的一些实施方案中,所述擦试物还包含抗氧化剂,所述抗氧化剂选自下组,该组由以下组成:丁基化羟基甲苯(BHT)、α-生育酚、没食子酸丙酯、抗坏血酸角鲨烯、抗坏血酸棕榈酸酯、硫代硫酸钠和偏亚硫酸氢钠。
在本文所述的任何擦拭物的一些实施方案中,所述擦拭物还包含生物粘附聚合物,所述聚合物选自下组,该组由以下组成:卡波姆均聚物A型、B型和C型、卡波姆共聚物、互聚物、聚卡波非、pemulens、羟乙基纤维素(HEC)、羟丙基纤维素(HPC)和羟丙基甲基纤维素(HPMC)。
在本文所述的任何擦拭物的一些实施方案中,所述溶液包含选自下组的溶剂,该组由以下组成:水、丙二醇和己二醇。
在本文所述的任何擦拭物的一些实施方案中,所述擦拭物还包含苯甲醇、还原二元醇、丙烯酸酯、聚山梨醇酯80、BHT、PEG 400、甘油和己二醇中的一种或多种。
在本文所述的任何擦拭物的一些实施方案中,所述擦拭物包含按浓度计至少2%苯甲醇。
在本文所述的任何擦拭物的一些实施方案中,所述擦拭物包含按浓度计30%至40%还原二元醇,优选按浓度计30%、35%或40%还原二元醇。
在本文所述的任何擦拭物的一些实施方案中,所述擦拭物包含按浓度计至少4%丙烯酸酯。
在本文所述的任何擦拭物的一些实施方案中,所述擦拭物包含按浓度计至少2%聚山梨醇酯80。
在本文所述的任何擦拭物的一些实施方案中,所述擦拭物包含按浓度计至少0.2%BHT。
在本文所述的任何擦拭物的一些实施方案中,所述擦拭物包含按浓度计30%至60%丙二醇,特别是按浓度计30%、35%、40%、45%、50%、55%或60%丙二醇。
在本文所述的任何擦拭物的一些实施方案中,所述擦拭物包含按浓度计至少15%甘油。
在本文所述的任何擦拭物的一些实施方案中,所述擦拭物包含按浓度计至少10%己二醇。
在本文所述的任何擦拭物的一些实施方案中,擦拭物包含选自下组的制剂,该组由以下组成:制剂I、制剂II、制剂III、制剂IV、制剂V和制剂VI。
在本文所述的任何擦拭物的一些实施方案中,所述局部擦拭物由纤维制成。在一些实施方案中,所述局部擦拭物由非织造纤维制成。在一些实施方案中,所述局部擦拭物由织造纤维制成。
在本文所述的任何擦拭物的一些实施方案中,所述局部擦拭物通常呈矩形形状。在一些实施方案中,所述局部擦拭物被单独包装以供一次性使用。
在另一方面,本公开提供了包含本文所述的多种局部擦拭物的容器。在一些实施方案中,所述容器包括软包装。在一些实施方案中,所述容器包括硬包装。
在另一个方面,本公开提供了药剂盒,所述药剂盒包含本文所述的多种局部擦拭物,这些擦拭物处于单独的单次使用包装中或每个包装至少30个擦拭物。
在另一方面,本公开提供了在有需要的受试者中治疗或改善肛裂的方法,所述方法包括将局部擦拭物应用于所述受试者的肛周区从而提供治疗性缓解的步骤,所述局部擦拭物包含用含有按浓度计至少1.5%盐酸利多卡因和按浓度计至少0.3%硝苯地平的溶液润湿的纤维基质材料。
在另一方面,本公开提供了在有需要的受试者中治疗或改善肛裂的方法,所述方法包括将制剂应用于自所述受试者的肛管1cm内的肛门组织从而提供治疗性缓解的步骤,所述制剂包含按浓度计1.5%至5%盐酸利多卡因,优选至少1.5%盐酸利多卡因和按浓度计0.15%-4.5%硝苯地平,优选至少0.15%硝苯地平。
在另一方面,本公开提供了在有需要的受试者中治疗或改善肛裂的方法,所述方法包括将制剂应用于所述受试者的肛门外括约肌从而提供治疗性缓解的步骤,所述制剂包含按浓度计1.5%-5%盐酸利多卡因,优选至少1.5%盐酸利多卡因和按浓度计0.15%-.45%硝苯地平,优选至少0.15%硝苯地平。
在另一方面,本公开提供了制造包含按浓度计0.15-.45%,优选至少0.3%硝苯地平和按浓度计1.5-5%盐酸利多卡因,优选至少1.5%盐酸利多卡因的局部擦拭物的方法,所述方法包括如下步骤:提供擦拭物;应用包含至少0.15%硝苯地平和至少1.5%盐酸利多卡因的制剂;将所述擦拭物干燥足够的时间,并将所述擦拭物包装在气密容器或小袋中。
在另一方面,本公开提供了使用局部擦拭物的方法,其中所述擦拭物包含按浓度计0.15-.45%硝苯地平,优选至少0.15%硝苯地平和至少1.5%盐酸利多卡因的制剂,所述方法包括如下步骤:将所述擦拭物应用于受试者的肛周,使得所述制剂与所述受试者的肛管1cm内的肛门外括约肌或肛门组织接触,其中所述受试者患有肛裂。
在一些实施方案中,包含至少0.15%硝苯地平和至少1.5%盐酸利多卡因,优选0.3%硝苯地平和1.5%利多卡因的制剂在通过将所述擦拭物应用到肛周区时与肛门外括约肌接触。
在一些实施方案中,包含至少0.15%硝苯地平和至少1.5%盐酸利多卡因,优选0.3%硝苯地平和1.5%利多卡因的制剂,在通过将所述擦拭物应用到肛周区时,与肛门外括约肌和肛门内括约肌接触。
在一些实施方案中,包含至少0.15%硝苯地平和至少1.5%盐酸利多卡因,优选0.3%硝苯地平和1.5%利多卡因的制剂,在通过将所述擦拭物应用到肛周区时,与肛门外括约肌接触,但不与肛门内括约肌接触。
在一些实施方案中,包含至少0.15%硝苯地平和至少1.5%盐酸利多卡因,优选0.3%硝苯地平和1.5%利多卡因的制剂,在通过将所述擦拭物应用到肛周区时,与肛门腔1cm内的肛门组织接触。
现在将描述某些示例性实施方案,以提供对物质组合物(例如,硝苯地平和盐酸利多卡因的制剂)及其制备方法的全面理解。本公开提供了各种成分和/或其组合来配制物质组合物,并进一步提供了可用于组合各种成分和/或其组合以获得物质组合物的各种步骤。本领域技术人员将理解,本文所述的组合物和方法是非限制性的示例性实施方案,并且本公开的范围仅由权利要求限定。除非另有说明,与一个示例性实施方案结合说明或描述的特征通常可以与其他实施方案的特征相结合。例如,鉴于本公开,本领域技术人员将理解一个或多个步骤,这些步骤作为一种制备本文所提供的物质组合物的方法的一部分提供,可用于制备本文所提供的物质组合物或以其他方式在本领域已知的其他方法中。同样地,本领域技术人员将理解,在不脱离本公开的精神的情况下,可以在本文公开的或以其他方式对于本领域技术人员已知的各种方法之间互换的各种步骤,或者鉴于本文公开的以其他方式修改的或以其他方式对于本领域技术人员已知的各种步骤。作为非限制性示例,鉴于本公开,本领域技术人员将理解,替代性技术的使用,无论是在本申请中明确公开的还是鉴于本公开由本领域技术人员已知的,通常仍然保持与本公开相关的发明概念。
在本公开中,许多不同的术语可以互换使用,同时仍能被技术人员理解。通过非限制性示例,短语“选自下组,该组由以下组成”、“选自”等包括特定材料的混合物。当本文陈述数值极限或范围时,包括端点。此外,数值极限或范围内的所有值和子范围都被明确包括在内,就像被明确写出一样。除非特别说明,否则以单数形式提及的元件并不旨在表示“一个且仅一个”,而是“一个或多个”除非特别说明,否则术语如“一些”指一个或多个,并且单数术语如“一个("a"、"an")”、和“该”指一个或多个。
具体实施方式
在一个方面,本公开涉及用于治疗肛裂的方法和组合物,所述方法和组合物通过提供包含治疗剂和能够应用于肛门的局部麻醉剂的含药擦拭物,所述含药擦拭物尤其可以加速或促进治疗,可以有助于疼痛的局部麻木的舒适性,并且可以放松局部肌肉以增加受影响区域的血流,从而促进肛裂的愈合。
擦拭物提供了对现有技术的许多改进,包括用于治疗性化合物和局部麻醉剂的更易于使用和更舒适的递送机制;减轻疼痛、刺激和其他不适的凉爽、舒缓和舒适的效果;以及引起更好加速愈合的化学组成。擦拭物还确保更好地适应局部药物的应用,这与不总是实用或舒适的现有技术的软膏不同。现有技术的软膏通常分散在肛门腔内和/或周围,需要手指插入,而本文使用的局部擦拭物将治疗化合物分散在外部。这有助于患者的舒适性和易用性,因为擦拭动作的机械学模拟了常规的厕所卫生,并且不需要插入。这反过来鼓励遵守治疗方案并改善结果。此外,化合物可以安全地暴露于皮肤,并且因为擦拭物的使用不需要手指的插入,患者可以放弃使用一次性手套或其他卫生覆盖物,并且在使用后只要正确洗手即可。
在一些实施方案中,所述擦拭物中的活性药物化合物实现了相对于靶向组织的有效渗透分布,以提供治疗性缓解。每种化合物的渗透曲线尤其基于每种化合物的物理和化学特性、每种化合物的微观结构特征、局部擦拭物的剂量负荷以及靶组织的特征,这些可以在不同的解剖区域中发生大幅变化。也就是说,已知适用于特定区域(如头皮、腹部或手部)的制剂和现有技术产品可能不适用于本文所述的局部擦拭物。另一个考虑因素是美观,因为可以考虑诸如粘度或感官感觉等属性来选择或优化化合物制剂,这些属性可能会影响产品使用的“脏乱度”(例如,过度饱和的流动化合物可能会在使用前和使用后从擦拭物上过度滴落,或者将过量的制剂转移到未渗透皮肤的受影响区域而必须手动除去)。
在一些实施方案中,用一种或多种局部药剂处理局部擦拭物,所述局部药剂具有有效放松肛门外括约肌和增加血流的治疗特性。通过示例而非限制,一种这样的化合物家族是钙通道阻滞剂。通过另外的示例而非限制,一种这样的钙通道阻滞剂是硝苯地平,C
硝苯地平可溶于有机溶剂,如EtOH(3mg/ml)、DMSO(30mg/ml)和二甲基甲酰胺(30mg/ml),所述有机溶剂应使用惰性气体吹扫。使用硝苯地平的一个挑战是它在水性缓冲液中微溶,尽管它是高度亲脂性的并且可溶于醇。
在另一个实施方案中,局部擦拭物还通过或替代性地用一种或多种具有缓解疼痛或瘙痒特性的局部药剂处理,以有效减轻受影响区域的不适。通过示例而非限制,一种这样的化合物是利多卡因(如下所述)及其盐,例如盐酸利多卡因,C
利多卡因及其盐是一种快速起效的局部麻醉剂,并且高度可溶于醇(4mg/mlEtOH)和氯仿,并且易溶于乙醚和苯。它也能溶解在油中。
在另一个实施方案中,用包含所需化合物(如肌肉松弛剂和/或止痛药)的溶液将局部擦拭物预润湿,然后包装成随时可分配的形式,如软包装或具有顶部开口的硬盖容器,其抑制氧气和其他降解物的引入,保存水分以抑制蒸发,并保护擦拭物免受外部污染物的影响。可以从容器中取出擦拭物,按照规定或需要一次一张立即使用,然后重新密封容器。替代性地或另外地,可以将擦拭物单独包装在一次性容器或软包装中。
在一些实施方案中,用包含按浓度计约1.5%w/w利多卡因和约0.3%w/w硝苯地平的溶液将擦拭物预润湿。在一些实施方案中,用包含按浓度计约2%w/w利多卡因和约0.3%w/w硝苯地平的溶液将擦拭物预润湿。在一些实施方案中,用包含按浓度计约2.5%w/w利多卡因和约0.3%w/w硝苯地平的溶液将擦拭物预润湿。在一些实施方案中,用包含按浓度计约3%w/w盐酸利多卡因和约0.3%w/w硝苯地平的溶液将擦拭物预润湿。在一些实施方案中,用包含按浓度计约3.5%w/w利多卡因和约0.3%w/w硝苯地平的溶液将擦拭物预润湿。在一些实施方案中,用包含按浓度计约4%w/w利多卡因和约0.3%w/w硝苯地平的溶液将擦拭物预润湿。在一些实施方案中,用包含按浓度计约4.5%w/w利多卡因和约0.3%w/w硝苯地平的溶液将擦拭物预润湿。在一些实施方案中,用包含按浓度计约5%w/w利多卡因和约0.3%w/w硝苯地平的溶液将擦拭物预润湿。在一些实施方案中,用包含按浓度计范围在1.5至5%w/w的盐酸利多卡因和约0.3%w/w硝苯地平的溶液将擦拭物预润湿。
这些浓度可以通过添加本文其他地方讨论的其他化合物来改变,包括但不一定限于防腐剂和抗氧化剂。浓度也可以根据其他因素而变化,例如可以根据适用的实际限制(例如典型的处方量、货架间距要求、在普通细节环境中的预期密封货架寿命、打开和使用时的货架寿命以及普通运输条件)合成和/或包装、运输和储存正在讨论的化合物的量和浓度。特别地,应注意在合成或储存过程中可能形成的杂质或化合物相关降解物的引入。
在一些实施方案中,局部擦拭物还包含合适的赋形剂和/或溶剂,通常选择这些赋形剂和/或溶剂以达到所需浓度。例如,硝苯地平和利多卡因都高度溶于醇。可以包括一种或多种赋形剂或赋形剂类,包括但不一定限于抗氧化剂、渗透促进剂、保湿剂、分散剂、粘度调节剂、润肤剂、成膜剂、防腐剂、拖尾溶剂、共溶剂、油等。考虑到任何给定制剂中包含的赋形剂,可以改变或调整所用治疗性化合物的质量和/或体积,以达到本文其他地方所述的所需浓度。可以基于许多因素来选择赋形剂,包括但不一定限于稳定性和与治疗性化合物的潜在相互作用,所述相互作用在预期的剂量水平下会导致抑制的降解或其他抑制的功能。
在一些实施方案中,局部擦拭物包含纤维基质材料,例如天然或合成的纤维或布,优选具有光滑、低摩擦的表面和/或对敏感皮肤温和的饰面。在一些实施方案中,可以使用具有吸收性能的非织造纤维,所述吸收性能有效地负荷所需的药物产品的组合,同时还具有所需的储存特性(例如,负荷药物化合物并将其在储存中保持所需的储存稳定期而不会过度分解或降解的能力)、使用特性(对撕裂或破损的抗性)以及所需的处置特性(例如,可生物降解性、可堆肥性、可冲散、化粪安全性等)。在一些实施方案中,局部擦拭物的组分可有效地提供约两年时间的储存稳定性产品。
在一些实施方案中,擦拭物包括一种或多种防腐剂和/或抗氧化剂。这些化合物的种类和数量或浓度优选能有效确保局部擦拭物在普通运输、零售和消费条件下的所需储存期。通过常规实验和测试确定合适化合物及其量的技术是本领域已知的。
在一些实施方案中,,局部擦拭物通常是正交的,并且优选为矩形,以便于储存和取出。擦拭巾可以单独包装,例如在密封的单个单元包或小袋中,或者可以包装成多个。包装优选是可重复密封的,例如通过使用拉链或粘合剂。
在一些实施方案中,局部擦拭物是无摩擦的,并且对敏感皮肤是温和的。
在一些实施方案中,局部擦拭物是可冲散的、一次性的和化粪安全的。
在一些实施方案中,局部擦拭物可储存稳定至少2年。
尽管针对用于治疗人肛裂的特定化合物描述了前述局部擦拭物,但是容易理解的是,相同的考虑和原理也适用于其他区域,并且可以用于治疗非人类哺乳动物或其他动物的组织中的类似类型的损伤,以及用于治疗具有类似医学特性、解剖几何学或社会态度的其他解剖区域中的类似类型的损伤,这些类似医学特性、解剖几何学或社会态度抑制了患者对自我管理治疗的完全依从性。
虽然已经公开了结合某些实施方案描述的本发明,包括目前被认为是优选实施方案的那些实施方案,但是详细描述旨在具有说明性,并且不应该被理解为限制本公开的范围。如本领域普通技术人员将理解的,除了在本文中详细描述的实施方案之外的实施方案也涵盖在本发明中。在不脱离本发明的精神和范围的情况下,可以对所描述的实施方案进行修改和变化。
附图说明
图1显示了测试赋形剂的不同组合和改变浓度以获得适合用于治疗性用途的浸注擦拭物的硝苯地平和利多卡因的制剂的过程。
图2显示了用于产生局部擦拭物的不同浸注方法,所述局部擦拭物包含硝苯地平和利多卡因以及所选赋形剂的制剂。A)将所需量的盐酸利多卡因+硝苯地平溶液置于容器中。B)将擦拭物浸渍或浸泡在活性溶液中持续t分钟。C)在浸泡或浸渍后,将擦拭物干燥t分钟。D)将所需量的盐酸利多卡因+硝苯地平溶液置于喷雾瓶中。E)将擦拭物用活性溶液喷雾t分钟。F)在喷雾后,将擦拭物干燥t分钟。G)将所需量的盐酸利多卡因+硝苯地平溶液置于移液管中。H)通过移液t分钟,将擦拭物用活性溶液润湿(使用移液管将制剂递增添加到擦拭物上)。I)在移液后,将擦拭物干燥t分钟。饱和负荷是擦拭物的最终重量/擦拭物的干重;饱和百分比是擦拭物的最终重量/擦拭物的干重x100;并且浸注制剂的重量是(负荷和干燥后的干擦拭物的重量)–(干擦拭物的皮重)。
图3显示了一致使用的用于干燥所有用不同方法浸注的擦拭物的干燥方法。
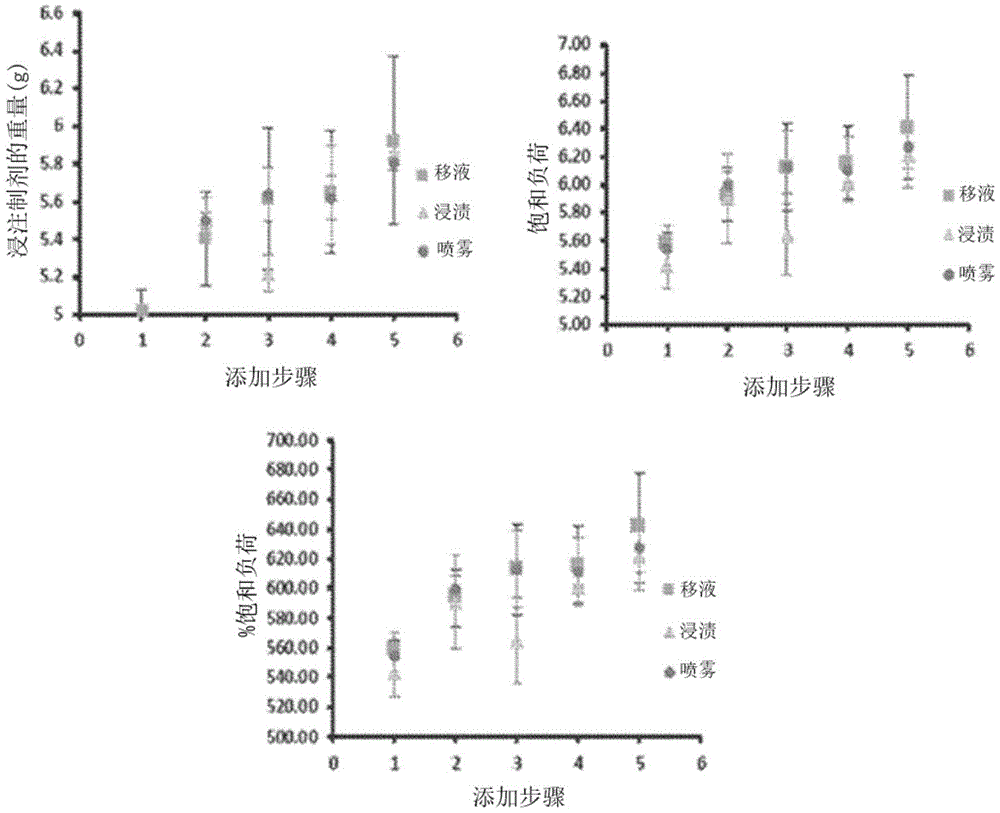
图4显示了浸注溶液的重量、饱和负荷和%饱和负荷与每个递增添加步骤的图。在每个添加步骤后,将擦拭物干燥45分钟。
图5显示了浸注溶液的重量、饱和负荷和%饱和负荷与每个递增添加步骤的图。在每个添加步骤后,将擦拭物干燥15分钟。
图6显示了用不同的擦拭物重量/尺寸获得的校准曲线。
图7显示了在每种类型制剂F1-F3(分别为溶液、擦拭物和软膏)中盐酸利多卡因的平均累积渗透量。
图8显示了在每种类型制剂F1-F3(分别为溶液、擦拭物和软膏)中盐酸利多卡因的平均流量。
图9显示了在每种类型制剂F1-F3(分别为溶液、擦拭物和软膏)中硝苯地平的平均累积渗透量。
图10显示了在每种类型制剂F1-F3(分别为溶液、擦拭物和软膏)中硝苯地平的平均流量。
图11A显示了在每种类型制剂F1-F3(分别为溶液、擦拭物和软膏)中盐酸利多卡因在组织中的平均保留,从组织中回收的总盐酸利多卡因(以ng/cm2片计量);11B显示了所应用的盐酸利多卡因剂量的相应回收率为%回收,并且11C显示了在三种制剂中的组织总保留。
图12A显示了在每种类型制剂F1-F3(分别为溶液、擦拭物和软膏)中硝苯地平在组织中的平均保留,从组织中回收的总硝苯地平(以ng/cm2片计量);12B显示了所应用的硝苯地平剂量的相应回收率为%回收,并且12C显示了在三种制剂中组织的总保留。
图13A显示了肛管和与其相关的各种组织。局部擦拭物优选应用于肛管前1cm内的组织。通过患者应用局部擦拭物将API(硝苯地平和盐酸利多卡因)递送至肛门外括约肌,并有助于治疗肛裂。图13B显示了包括几层的人的皮肤结构。
定义
如本文所用,术语“擦拭物”是指塑料或布的小至中等尺寸的润湿片,为了方便起见或在分配器的情况下,所述润湿片被折叠并单独包装。擦拭物通常出于清洁目的如个人卫生而使用,但当浸注有药物活性化合物如乙醇(抗腐擦拭物)或金缕梅(痔疮擦拭物)等时,也可出于治疗目的而使用。本公开的局部擦拭物浸注有硝苯地平(至少0.3%w/w)和盐酸利多卡因(至少1.5%w/w)的制剂,用于治疗肛裂。擦拭物的尺寸可以根据使用的性质而变化,旅行尺寸的擦拭物通常更小,例如约6英寸x3英寸。常规擦拭物的范围在例如约6英寸x4英寸、约8英寸x8英寸、或9英寸x7英寸。擦拭物的厚度范围在0.5mm至1mm。优选地,擦拭物为6x4英寸,并且由纤维素制成的非织造纤维制成。
擦拭物由诸如聚酯、聚丙烯、棉、木浆或人造丝纤维等材料制成,形成薄片。可以将擦拭物单独包装,或以小包装或散装包装。擦拭物可以由织造纤维和非织造纤维制成。将擦拭物用水和其他惰性成分如表面活性剂和保湿剂润湿,以帮助活性成分更好地发挥作用,并确保用户的依从性。它们可能含有其他成分,如防腐剂,以防止细菌和霉菌的生长。擦拭物可以被制成可生物降解的和可冲散的,因此它可以安全地用于化粪用途。
如本文所用,术语“织造纤维”是指通过相互成直角交织两根或多根线制成的纤维。织造织物或擦拭物可以由天然纤维和合成纤维制成,并且通常由两者的混合物制成。例如,100%棉或80%棉和20%聚酯。
如本文所用,术语“非织造纤维”是指不含交织股线但具有有序内部结构的纤维。这些是通过将纤维放在一起,然后使用热量、化学物质或压力将它们结合成一种粘合的织物状材料制成的。与棉、麻、羊毛和丝等传统材料相反;非织造织物不需要编织。它是通过在溶液中搅动纤维直到它们联锁成致密的织物而制成的。纤维素通常用于制造非织造纤维。
如本文所用,术语“利多卡因”是指由N,N-二乙基甘氨酸与2,6-二甲基苯胺的形式缩合而产生的单羧酸酰胺。它作为局部麻醉剂和抗心律失常药物发挥作用。利多卡因盐的示例是盐酸利多卡因,利多卡因的其他盐也考虑用于本文所述的局部擦拭物中。
如本文所用,术语“盐酸利多卡因”或“盐酸利多卡因”或“2-(二乙氨基)-N-(2,6-二甲基苯基)乙酰胺;盐酸盐”是指利多卡因的盐酸盐,一种氨基乙基酰胺和酰胺类麻醉剂的原型成员。利多卡因与神经细胞膜中的电压门控Na+通道相互作用,并阻断可兴奋膜对Na+渗透性的瞬时增加。这会阻止神经冲动的产生和传导,并产生可逆的感觉丧失。盐酸利多卡因也表现出IB类抗心律失常作用。药剂在动作电位的0相期间减少钠离子流入心肌组织,特别是浦肯野(Purkinje)网络,从而减少去极化、自动性和兴奋性。
如本文所用,术语“硝苯地平”或“2,6-二甲基-4-(2-硝基苯基)-1,4-二氢吡啶-3,5-二羧酸二甲酯”是指二氢吡啶钙通道阻断剂。硝苯地平抑制细胞外钙离子跨膜流入心肌和血管平滑肌细胞,引起主要冠状动脉和全身动脉扩张并降低心肌收缩性。这种药剂也抑制药物外排泵P-糖蛋白,其在一些多药耐药肿瘤中过度表达,并可提高一些抗肿瘤药剂的疗效。硝苯地平碱和硝苯地平的盐也被考虑用于如本文所述的局部擦拭物中。
如本文所用,术语“肛管”是指下胃肠道/大肠的最末端部分,其位于下方会阴中的肛门边缘(肛门口、肛门)和上方直肠之间。
如本文所用,术语“肛裂”是指肛门的薄而脆弱的内层上的切口或撕裂。撕裂经常暴露肛门周围的肌肉,称为肛门括约肌。这种损伤会导致肌肉痉挛,这会更进一步撕开裂缝边缘。痉挛可以引起疼痛并减缓愈合。排便也可以阻止裂缝好转。
如本文所用,术语“肛门外括约肌”是指环绕肛管和肛门开口外壁的随意(横纹)肌肉层。肛门外括约肌从其前端到其后端测量为约8至10cm长,并且与肛门相对约1-2.5cm,排便时括约肌收缩。它由两层组成:表层和深层。浅层,构成肌肉的主要部分,并且起源于狭窄的腱带,从尾骨的尖端延伸到肛门后缘的肛门尾骨缝;它形成两个扁平的肌肉组织平面,这些平面环绕肛门并在前方会合以插入会阴的中央腱点,与会阴浅横肌、肛提肌和球海绵体肌(也称为球海绵体肌)相连。较深层形成肛管的完整括约肌。
如本文所用,术语“肛门内括约肌”是指围绕肛管的平滑肌环。其下缘与肛门外括约肌接触,但与之完全分离。内括约肌由平滑肌组成,并由自主神经系统支配,而外括约肌属于横纹肌,并具有由称为阴部神经的神经提供的躯体(自主)神经支配。
如本文所用,术语“肛周”或“直肠周”是指直肠口或肛管开口周围的区域。通常,擦拭物用于清洁或到达肛周区域。
如本文所用,术语“直肠内”是指直肠或肛管深处的区域。通常需要手指穿透或涂抹棒来进入直肠内区域。
如本文所用,术语“赋形剂”是指用于药物制剂的惰性药物成分。赋形剂可以在药物产品中发挥多种功能作用。每种赋形剂都有特定的用途(例如,粘合剂、崩解剂或pH调节剂),用于保证剂型的适当性能。最终剂型的性质(即稳定性)在很大程度上高度依赖于所选择的赋形剂、它们的浓度以及与活性化合物和彼此之间的相互作用。产品制剂中使用的大多数赋形剂都是药典项目(美国药典(USP)、欧洲药典(EP)、日本药典(JP))。
如本文所用,术语“API”是指活性药物成分.药物成品(FPP)中使用的任何物质或物质组合,旨在提供药理活性或在疾病的诊断、治愈、缓解、治疗或预防中具有直接作用,或在治疗中具有直接作用。本公开中的术语API是指硝苯地平和盐酸利多卡因。
如本文所用,术语“防腐剂”是指防止或抑制微生物生长并延长药物产品储存期的物质。这些系统中常用的防腐剂包括苯甲酸钠、EDTA、山梨酸和对羟基苯甲酸酯。
如本文所用,术语“抗氧化剂”是指减少活性组分因氧化(如自由基引起的氧化)而受损的物质。抗氧化剂的常见的示例包括丁基化羟基甲苯(BHT)、α-生育酚、没食子酸丙酯、β羟基酸(BHA)、角鲨烯、抗坏血酸棕榈酸酯、硫代硫酸钠和偏亚硫酸氢钠。
如本文所用,术语“渗透促进剂”或“渗透促进剂”是指渗透入皮肤并与皮肤构成相互作用以促进药物流量或可逆地降低屏障阻力的药剂。常见的示例包括苯甲醇、二甲基异山梨醇(DMI)、丙二醇、己二醇、异丙醇(IPA)、乙醇、苯氧乙醇、油酸、油醇、肉豆蔻酸异丙酯、中链甘油三酯(MCT)和还原二元醇。也可以使用乙醇或IPA与油酸、油醇、中链甘油三酯(MCT)或肉豆蔻酸异丙酯中的一种或多种的组合。
如本文所用,术语“保湿剂”或“润肤剂”是指在皮肤表面周围形成屏障并防止水分从皮肤细胞流失的物质。常见的示例包括乳木果油、可可脂、矿物油、羊毛脂、凡士林、石蜡、蜂蜡和角鲨烯。
如本文所用,术语“分散剂”是将另一种物质分散在介质如水中以形成胶体溶液的物质。它们的主要功能是减少颗粒间的粘附,并防止絮凝或结块。常见的示例包括十六烷基三甲基氯化铵、PEG-10二甲基硅氧烷、PEG-7甘油椰油酸酯和甘油醚-26。
如本文所用,术语“湿润剂”是一种吸湿材料,其吸收水蒸气并将水结合到皮肤上。湿润剂的水溶液可以降低水分的损失率。这些通常被添加到化妆品中,如水包油型乳膏(雪花膏),以防止干燥。湿润剂的常见示例包括丙烯酸酯和甘油、戊二醇、丁二醇、库拉索芦荟汁/提取物、己二醇、透明质酸及其盐、乳酸及其盐。
如本文所用,术语“乳化剂”是用作乳液稳定剂的化合物或物质,防止通常不混合的液体分离。常见的示例包括聚山梨醇酯80、Span-80硬脂酰乳酸钠、单和双甘油、磷酸铵、PEG-40氢化蓖麻油、十二烷基硫酸钠(SLS)、泊洛沙姆(共嵌段聚合物)、氢化蓖麻油、聚山梨醇酯(20至80)–TWEENS、脱水山梨醇(SPANS(20-85)和甘油单油酸酯(GMO)。
如本文所用,术语“表面活性剂”是指如洗涤剂的物质,当添加至液体时,其降低了表面张力,从而增加了其铺展和润湿性能。表面活性剂在药物中具有若干种用途:i)用于疏水性药物在水性介质中的增溶;ii)作为乳剂的组分;iii)用于口服和透皮药物递送的表面活性剂自组装的媒介物;iv)作为半固体递送系统中的增塑剂;以及v)作为改善药物吸收的药剂。常见的示例包括PEG 400、tween-80、油醇、甘油、己二醇和丙二醇。
如本文所用,术语“粘度调节剂”是指可以改变药物成分的厚度或质地的物质。粘度调节剂可以包括此类药剂,如增稠剂、调质剂、胶凝剂和硬化剂等产品。许多粘度调节剂可用于将液体转化为凝胶、糊状物或粉末,以帮助配方设计师为最终用户创造理想的产品。粘度调节剂可以降低液体的厚度,以改善倾倒能力、在表面上的铺展能力。
如本文所用,术语“成膜剂”是指当应用到毛发或皮肤表面时,在毛发或皮肤上留下柔韧、粘着和连续覆盖物的化合物。这种薄膜具有很强的亲水特性,并且在皮肤上留下光滑的感觉。常见的示例包括聚乙烯吡咯烷酮(PVP)、丙烯酸酯、丙烯酰胺和共聚物。生物粘附聚合物可用作赋形剂,减少含药擦拭物和肛门皮肤之间的摩擦,并产生用于改善擦拭后保留的膜。此类生物粘附聚合物的常见示例包括卡波姆均聚物A型、B型和C型,卡波姆共聚物和互聚物(聚卡波非和Pemulens)、纤维素衍生物,如羟乙基纤维素(HEC)、羟丙基纤维素(HPC)和羟丙基甲基纤维素(HPMC)。
如本文所用,术语“IVPT”是指体外释放测试(IVRT),其需要测量从媒介物释放到受体介质中的药物,所述药物被惰性膜隔开,并用于定量从半固体剂型或擦拭物中释放的活性药物成分(API)的量,并确定其释放速率。关于如何进行IVPT的详细信息可以在RathS,Kanfer I.A Validated IVRT Method to Assess Topical Creams ContainingMetronidazole Using a Novel Approach.Pharmaceutics.2020;12(2):119.Published2020Feb 3.doi:10.3390/pharmaceutics12020119中找到。
如本文所用,术语“TEWL”是指经表皮的水分损失(TEWL),是由于皮肤屏障两侧的水蒸气压力梯度而通过皮肤被动蒸发到外部环境中的水量,并用于表征皮肤屏障功能。人的平均TEWL约为300–400mL/天;然而,它会受到环境和内在因素的影响。经表皮水分损失(TEWL)可以作为角质层屏障性能有效性的一种量度。
擦拭物的生产
用于局部擦拭物的材料可以是类似于在尿布和干燥片所用类型的非织造织物或织造织物。传统的织物(织造纤维)是通过将丝、棉、聚酯、羊毛和类似材料的纤维编织在一起以形成被称为织造织物的联锁矩阵环而制成的。另一方面,非织造织物(非织造纤维)是通过从大量分离的纤维中压制出单片材料的过程制成的。纤维,如棉和人造丝,以及塑料树脂(如聚酯,聚乙烯和聚丙烯)都用在这一过程中。优选地,擦拭物由可从商业来源获得的非织造100%纤维素(木浆)制成(https://pdicontract.com/)。
局部擦拭物可以任选地包含与保湿剂、香料和防腐剂混合的温和洗涤剂。擦拭物可以任选地含有两性表面活性剂,例如擦拭物中使用的二磷乙酸钠和椰油磷脂酰PG-二甲基氯化铵。这些化学物质不会去除皮肤的天然油脂,并且也不会降低皮肤刺激的可能性。温和是首要考虑因素,因为擦拭物会接触肛门和生殖器周围的娇嫩皮肤。可以任选地添加湿润剂如丙二醇和甘油,以防止溶液过早干燥,并有助于皮肤保湿。
此外,可以将诸如矿物油、羊毛脂或硅酮之类的油掺入到有助于软化皮肤的所需制剂(盐酸利多卡因和硝苯地平以及合适的赋形剂)中。增稠剂(例如纤维素衍生物,如羟甲基纤维素)控制最终产品的粘度并保持其正确的稠度。其他成分包括防腐剂,如对羟基苯甲酸甲酯和对羟基苯甲酸丙酯,以确保溶液不支持微生物生长。还可以添加香料来增加消费者的吸引力,并有助于克服体臭。也可以添加已知对皮肤有益的天然成分,如库拉索芦荟或燕麦提取物,以进一步滋养皮肤。
有两种组装非织造织物的主要方法:湿法成网工艺和干法成网工艺。干法成网工艺是“熔喷”法,用于由塑料树脂制造非织造织物。在这种方法中,塑料颗粒被熔化,然后被挤压,或者通过气压被挤压通过微小的孔。当纤维流冷却时,它凝结形成薄片。热金属辊用于压平纤维并将它们粘合在一起。
湿法成网工艺通常用于较软的布,如使用棉混纺的尿布擦拭物。在这种湿法工艺中,将纤维用水和其他化学物质制成液体浆料。得到的糊状物被辊子压成平片,然后进行干燥以形成长卷织物。然后将这些卷进一步加工并切成窄的宽度,然后被穿孔或切割成单独的薄片。将成品布按其至少1.4oz/in2(40g/m2)的干重进行分类。擦拭物的吸收性也是一个重要的要求(优质的擦拭物可以在溶液中吸收其重量的200%到600%)。
一旦制备好,非织造布就从储存辊被输送到涂覆机器上,在那里应用所希望的制剂(盐酸利多卡因和硝苯地平以及合适的赋形剂)。在这个过程中可以采用几种方法。也可以通过使织物穿过溶液槽来添加制剂,或者可以从一系列喷嘴用制剂对织物片喷雾。
可替代地,可以将单个的药巾包装在密封的箔袋中。在这一过程中,层压薄片被送入自动化设备,将它们折叠成小袋,并且热封三边,以形成一个开放的信封。同时,另一条输送线将非织造布送入小袋中。包括延伸穿过填塞棒的导管的液体送料机制在填塞药巾材料的同时将保湿液体注入药巾包中。然后将小袋热封以保持湿度。
擦拭物的尺寸可以根据使用的性质而变化,旅行尺寸的擦拭物通常更小,例如约6英寸x3英寸。常规擦拭物的范围在例如约8英寸x8英寸,或9英寸x7英寸。擦拭物的厚度范围在0.5mm至1mm。擦拭物由诸如聚酯、聚丙烯、棉、木浆或人造丝纤维等材料制成,形成薄片。可以将擦拭物单独包装,或以小包装或散装包装。将擦拭物用水和其他惰性成分如表面活性剂和保湿剂润湿,以帮助活性成分更好地发挥作用,并确保用户的依从性。它们可能含有其他成分,如防腐剂,以防止细菌和霉菌的生长。擦拭物可以被制成可生物降解的和可冲散的,因此它可以安全地用于化粪用途。
实施例
实施例1-使用溶解度测定的溶剂筛选
进行实验来评价硝苯地平和盐酸利多卡因在一系列赋形剂中的视觉溶解度,以确定合适的溶剂系统。通过该过程确定了能够溶解两种组分的溶剂系统。将用于分析的溶剂列在表I中。将等分试样的盐酸利多卡因(例如,20-30mg)添加至闪烁瓶中包含的每种溶剂中。然后将瓶封闭,并在环境条件下放置在多位置搅拌板上,并允许混合持续最少15分钟。然后定期(约1小时)对瓶目视检查浊度的存在或缺失,并且如果药物已经溶解,则添加额外等分试样的盐酸利多卡因,直至达到饱和。按照如上所述的相同方案,使用硝苯地平的等分试样分别重复该过程。
将研究进行24小时,其中将样品保持搅拌,并在第二天进行目视检查。取每个瓶的最终重量,以确定每种赋形剂中的近似溶解度。将视觉溶解度测定的结果列在表II中。
溶解度测定的分析表明硝苯地平本质上是亲脂性的。硝苯地平不容易分配到水和油相中,但可以在溶剂系统如苯甲醇、DMI、丙烯酸酯、还原二元醇(二甘醇单乙醚)和聚山梨醇酯80中分配。还表明盐酸利多卡因本质上是亲水的,并且容易分配到水和乙二醇相,如丙二醇、己二醇、甘油、PEG 400,以及苯甲醇、丙烯酸酯和还原二元醇(二甘醇单乙醚)中。
还原二元醇-P和丙二醇稳定了盐酸利多卡因,并增强了药物从非织造织物的可湿性。它还增强盐酸利多卡因跨粘膜递送至肛周组织,并提高其作为局部麻醉剂的效率。发现聚山梨醇酯80降低了制剂的表面张力,使得包含活性药物组分(硝苯地平和利多卡因)的制剂易于浸注到擦拭物的表面上。聚山梨醇酯80还通过增加含药擦拭物对应用部位的可湿性来增强递送。苯甲醇也充当活性药物组分(硝苯地平和盐酸利多卡因)的防腐剂。丙烯酸酯可用于溶解硝苯地平。丁基化羟基甲苯(BHT)充当盐酸利多卡因和硝苯地平的抗氧化剂和稳定剂。
表1.用于溶解度筛选的赋形剂
表2-溶解度测定的结果
实施例2-药物赋形剂相容性和稳定性研究
药物赋形剂相容性研究通常以选择与治疗性组分(硝苯地平和盐酸利多卡因)相容的剂型组分为主要目标来进行。对各种类型的赋形剂(如抗氧化剂、渗透促进剂、保湿剂、分散剂、粘度调节剂、润肤剂、成膜剂、防腐剂、拖尾溶剂、共溶剂等)与治疗性组分(硝苯地平和盐酸利多卡因)组合进行测试,以评估当暴露于赋形剂时制剂中任何不相容性的可能性。图1示意性地说明了优化每一种类别的赋形剂和最佳浓度以得到含有API(盐酸利多卡因和硝苯地平)的制剂的过程,然后将所述制剂用于浸注擦拭物以产生能够治疗肛裂的局部治疗性擦拭物。
大多数赋形剂没有直接的药理作用,但对于方便施用、调节活性组分的释放和稳定药物以防降解是重要的。药物和赋形剂之间的潜在相互作用对治疗性组分的化学、物理、生物可利用度和稳定性有影响。对于硝苯地平在目标浓度为0.3%w/w下,和/或对于盐酸利多卡因在1.5%w/w浓度下,通过制备由溶解于合适的溶剂(苯甲醇、丙烯酸酯、还原二元醇)中的药物物质组成的溶液来制备药物赋形剂混合物。
为测试创建了四个样本集。每个样品集有17个小瓶,每种赋形剂一个小瓶进行测试,并且一个对照小瓶含有活性化合物但不含有赋形剂。第一样品集(I)仅含有硝苯地平(0.3%w/w)作为治疗性化合物,并且将表III中显示的每种赋形剂单独添加以形成溶液,将所述溶液混合并储存在小瓶中。第二样品集(II)仅含有盐酸利多卡因(1.5%w/w)作为治疗性化合物,并且添加表III中显示的每种赋形剂以形成溶液,将所述溶液混合并储存在小瓶中。第三样品集(III)含有硝苯地平(0.3%w/w)和盐酸利多卡因(1.5%w/w)作为治疗性化合物,并且添加表III中显示的每种赋形剂以形成溶液,将所述溶液混合并储存在小瓶中。第四样品集(IV)是安慰剂对照,它既不含有盐酸利多卡因也不含有硝苯地平,只是将溶剂与表III中显示的每种赋形剂混合以形成溶液,并储存在小瓶中。将来自每个样品集的小瓶分成相同大小的两个更小的瓶(A和B)。然后,在室温下储存后,对来自每个样品集的瓶A进行分析,并且在高温(40℃和75%的相对湿度)条件下储存后,对来自每个样品集的瓶B进行分析。将所述小瓶储存4周,其中在2周和4周的时间段内对小瓶进行分析。
表3.DEC硝苯地平和盐酸利多卡因的赋形剂及其功能类别和根据IID的最大效力限量.
对每批中的A瓶进行(a)监测视觉浊度;(b)在显微镜下监测以观察沉淀或结晶的迹象;和(c)测量pH;和(d)运行HPLC以观察是否有任何降解产物峰(T0测量)。然后将来自每批的小瓶在室温(25℃和60%的相对湿度)下储存2周,然后检查视觉浊度,在显微镜下分析并如上测量pH值(T-2测量)。然后将来自每批的小瓶在室温下再储存2周(总共4周),并重复相同的分析(T-4测量)。将实验重复两次,以确定添加的赋形剂是否与活性组分(硝苯地平和盐酸利多卡因)相容,以及它们在室温下储存2-4周后是否具有稳定的储存期。
对每批中的B瓶进行(a)监测视觉浊度;(b)在显微镜下监测以观察沉淀或结晶的迹象;和(c)测量pH;和(d)运行HPLC以观察是否有任何降解产物峰(T0测量)。然后将来自每批的小瓶在高温(40℃和75%的相对湿度)下储存2周,然后检查视觉浊度,在显微镜下分析并如上测量pH值(T-2测量)。然后将来自每批的小瓶在高温下再储存2周(总共4周),并重复相同的分析。(T-4测量)将实验重复两次,以确定添加的赋形剂是否与活性组分(硝苯地平和盐酸利多卡因)相容,以及它们即使在高温条件下储存2-4周时是否具有稳定的储存期。
第一样品集在两种温度(RT和40℃)下的T0测量显示对照样品(仅硝苯地平)在T0周似乎是稳定的,没有杂质。在T0时,在任何赋形剂组合中均未观察到主要降解(>5%)。第一样品集在两种温度(RT和40℃)下的T4测量显示对照样品(仅硝苯地平)在T4周似乎是稳定的,没有杂质。在还原二元醇、DMI、苯甲醇、油醇、PEG 400和抗坏血酸的DEC组合中观察到主要降解(>5%),表明不相容性。用Tween 80组合也观察到轻微降解。当将抗氧化剂BHT添加至配方时,降解显著减少。
第二样品集在两种温度(RT和40℃)下的T0测量显示对照样品(仅盐酸利多卡因)在T0周似乎是稳定的,没有杂质。在T0时,在任何赋形剂组合中均未观察到主要降解(>5%)。第二样品集在两种温度(RT和40℃)下的T4测量显示对照样品(仅盐酸利多卡因)在T4周似乎是稳定的,没有杂质。在还原二元醇、DMI和PEG 400组合的DEC组合中观察到主要降解(>5%),表明不相容性。用苯甲醇和油醇组合也观察到轻微降解。
第三样品集在两种温度(RT和40℃)下的T0测量显示对照样品(仅硝苯地平和盐酸利多卡因)在T0周似乎是稳定的,没有杂质。在T0时,在任何赋形剂组合中均未观察到主要降解(>5%)。第二样品集在两种温度(RT和40℃)下的T4测量结果显示与第一和第二样品集的结果相似。基于所述样品集的结果,选择六种具有特定浓度的赋形剂的制剂用于进一步分析。
实施例3-制剂的稳定性分析
选择以下六种制剂用于进一步稳定性分析。
制剂I(F-I)
制剂II(F-II)
制剂III(F-III)
制剂4(F-IV)
制剂5(F-V)
制剂6(F-VI)
在三种不同的温度条件(25℃/RH 60%;30℃/RH 65%;40℃./RH 75%),和四个不同的储存时间点(T0、1个月、2个月和3个月)下测试每种制剂。然后对制剂进行(a)监测视觉浊度;(b)在显微镜下监测以观察沉淀或结晶的迹象;和(c)测量pH;和(d)运行HPLC以观察在每个时间点后是否有任何降解产物峰,如实施例2中所述。
T-0测量表明,所有六种制剂均是稳定的,并且在HPLC上没有观察到降解曲线,即使当暴露于不同的温度时(25℃、30℃和40℃)。
T-1个月测量表明,除了制剂-1之外的所有制剂都是稳定的。在F-I制剂中,在约0.75%总量处观察到三种杂质(RRT 0.293、RRT 2.630和RRT 2.796),这在任何其他制剂中都没有观察到。
T-2个月的测量表明F-I制剂表现出了一些降解。在F-I制剂中,在约1.1%总量在40℃下,和在约0.5%总量在25℃下,观察到三种杂质(RRT 0.293、RRT 2.630和RRT2.796),这在任何其他制剂中都没有观察到。同样,在RRT 2.672,在0.1%-0.2%总量、40℃下,F6制剂显示了杂质。
T-3个月的测量表明F-I和F-II制剂表现了一些降解。在F-I和F-II制剂中观察到的RRT 0.106处的杂质与先前的时间点保持一致。在F-I制剂中,在约1.4%总量在40℃下,和在约0.8%总量在25℃下,观察到三种杂质(RRT 0.293、RRT 2.630和RRT 2.796),这在任何其他制剂中都没有观察到。F-III制剂没有观察到的杂质。F-IV、F-V和F-VI制剂显示了自先前的时间点杂质没有显著的增加。
实施例4-擦拭物的饱和负荷能力
选择制剂III来测试其负荷到擦拭物上的能力。可以将该实施例中所述的方案应用到本文公开的任何制剂。使用不含活性物质的制剂组合物3的安慰剂溶液出于建立饱和负荷含量的目的而使用。
如图2所示,通过浸渍、移液或喷雾技术将制剂添加至擦拭物。
浸渍
对于浸渍,将大约6x4英寸的擦拭物的皮干重放入去皮重的容器中,然后在每次添加期间将擦拭物添加至含有大约30g安慰剂制剂的容器中。将擦拭物浸入制剂大约1分钟,之后如图3所示将所述擦拭物干燥。每个干燥步骤花费大约15分钟。基于滴落的量估计干燥时间,在15分钟时几乎没有注意到滴落,并且这被假定为发生至少50%干燥的点。现在,在一个制剂添加步骤后,对擦拭物再次称重以确定擦拭物的干重。
移液
对于移液,将大约6x4英寸的擦拭物的皮干重放入去皮重的容器中,然后在每次添加期间用大约5g安慰剂制剂移液擦拭物。基于先前的研究,确定了5g添加,其中每次超过5g制剂添加显示滴落。将擦拭物浸入制剂大约1分钟,之后如图3所示将所述擦拭物干燥。现在,在一个制剂添加步骤后,对擦拭物再次称重以确定擦拭物的干重。
喷雾
对于喷雾,将大约6x4英寸的擦拭物的皮干重放入去皮重的容器中,然后在每次添加期间使用喷雾瓶,用大约5g安慰剂制剂对所述擦拭物喷雾。将擦拭物浸入制剂大约1分钟,之后如图3所示将所述擦拭物干燥。现在,在一个制剂添加步骤后,对擦拭物再次称重以确定擦拭物的干重。
研究已经表明,干燥时间、添加次数和应用过程在控制或限制擦拭物对制剂的饱和能力方面没有起到显著作用。下表和图(图4&5)给出了研究的细节及其各自对浸注制剂重量、饱和负荷和饱和负荷%的计算。
图4显示浸注制剂的重量范围在4.8g和6.05g之间,其中没有关于添加次数或应用过程的趋势。在称重之前,允许擦拭物干燥超过45分钟。发现饱和负荷在5.5和6.5之间,其中没有关于添加次数或应用过程的趋势。发现饱和负荷百分比的范围为550至650,其中没有关于添加次数或应用过程的趋势。因此,结果表明添加次数和应用过程对制剂浸注或擦拭物的饱和负荷没有任何影响。
重复相同的实验,其中增加的干燥时间为15分钟。实验的结果显示在图5中。在45分钟干燥时间的情况下,浸注制剂的重量范围在3.6g和5.8g之间,其中没有关于添加次数或应用过程的趋势。发现饱和负荷在4.2和6.2之间,其中没有关于添加次数或应用过程的趋势。发现饱和负荷百分比的范围为420至620,其中没有关于添加次数或应用过程的趋势。因此,结果表明添加次数和应用过程对制剂浸注或擦拭物的饱和负荷没有任何影响。
/>
为进一步建立负荷的均匀性,通过使用不同重量和尺寸的擦拭物,并即将其浸渍于制剂中,并使其经受相同的工艺参数来进行校准研究。在负荷制剂之前和之后,测量擦拭物的重量。下表显示了所获得的结果。
表4-导致浸注制剂重量的饱和负荷研究、饱和负荷、%饱和负荷研究及其在每个制剂添加步骤后15分钟干燥时间的各自计算。
图6中的校准曲线显示负荷与不同的擦拭物尺寸一致,表明制剂在擦拭物中均匀分布。
实施例5-治疗性擦拭物的体外渗透测试
体外渗透测试(IVPT)被设计用于确定在明确定义的局部产品中配制的,以进入靶向的人体组织的特定活性药物成分(API)的体外渗透曲线。特定API的渗透曲线不仅取决于API的物理和化学特性(如尺寸、溶解度、亲油性、logP等),还受微观结构特性(粘度、所选择的渗透促进剂、乳化剂等)和局部产品的剂型的影响。因此,IVPT是一个重要的工具,它不仅提供了关于硝苯地平和盐酸利多卡因一起在单一制剂中的可行性的信息和理解,而且还证明了各种制剂原型对API到达预期的作用靶位的能力的影响。
IVPT测试的方案在Santos等人.(Santos LL,Swofford NJ,Santiago BG.InVitro Permeation Test(IVPT)for Pharmacokinetic Assessment of TopicalDermatological Formulations.Curr Protoc Pharmacol.2020Dec;91(1):e79.)中公开。
进行体外渗透测试(IVPT)以比较包含制剂III的局部溶液,其在擦拭物上的相应溶液,和含有1.5%盐酸利多卡因和0.3%硝苯地平在的软膏制剂穿过离体冷冻保存的人尸体肛周组织的皮肤穿透。可以根据本文公开的相同程序用其他制剂(I-II和IV-VI)重复实验。
试剂和材料
a)1.5%盐酸利多卡因和0.3%硝苯地平,制剂III
i.制剂III作为溶液,(F1)
ii.浸注在擦拭物上的制剂III(根据实施例4中的方案)(F2)
iii.制剂III作为软膏(F3)
b)冷冻保存的人尸体肛周组织(500±250μm,厚度),
c)使用每种制剂4次重复
d)1X磷酸盐缓冲盐水(PBS,pH 7.4)
e)均化溶液(50/50甲醇/LCMS级水)
f)20mL闪烁瓶
g)带陶瓷珠的6.0mL均化瓶
h)用于质谱分析的96孔板
i)洗涤溶剂(70%v/v乙醇)
设备
a)自动化、垂直流通池(PermeGear Collector FC 33,3.1版)
b)容积式移液管
c)卡尺/测量规
d)蒸发仪(Delfin Technologies)
e)红外/激光温度计
f)探针温度计
g)组织均化器
h)60℃实验室烘箱
i)质谱仪
j)离心机
冷冻保存的人尸体肛周组织从商业来源获得,并在到达时储存在-80℃。将皮肤组织在室温下解冻,并检查是否有任何可见的孔、损伤、大范围拉伸或疤痕。经表皮水分损失(TEWL或TWL)通常用于表征皮肤组织屏障功能。使用蒸发仪测量每个皮肤组织样品的TEWL值,以评估组织完整性。低TEWL值通常是完整组织屏障功能的特征。在应用制剂(F1-F3)之前,测量并记录每个扩散池(Franz扩散池)的TEWL。
使用自动化、直排流通扩散池系统(PermeGear Collector FC 33,3.1版)以评估在组织渗透实验中的药物/API。贯穿IVPT研究,维持环境控制的实验室温度范围为21℃±2℃,并且湿度范围为50%±20%相对湿度。流通扩散池系统与受体介质平衡。
调整加热器和循环器,使皮肤样品维持在32℃±1℃。将扩散池放置在系统移动臂的支架上并加热,以维持皮肤表面温度(在32℃±1℃)。将池连接到多通道蠕动泵上,并且引导扩散池的出口滴入20mL闪烁瓶中。将皮肤组织切片切成1.5x1.5cm的切片,并安装在扩散池中,其中表皮层/角质层面朝上。将供体隔室块放置在皮肤组织上(角质层上的供体室),并用不锈钢夹钳固定以提供防漏密封。通过倒置扩散池去除气泡,并通过扩散池下侧的玻璃窗进行视觉确认。调节泵,以使流速维持在—30μL/min(1.8mL/h),以提供足够的下沉条件。
允许扩散池平衡大约30分钟。从分析中除去在组织顶部显示水积聚的任何池。平衡后,使用红外线或合适的温度计测量每个池的温度。使皮肤表面温度稳定维持在32℃±1℃。在给药30分钟之前,按—30μL/min(1.8mL/h)收集T'0'样品。
使用容积式移液管,将每种制剂(F1、F2、F3)以交替顺序均匀地分配到皮肤组织表面上的连续扩散池中,设定为递送约10μL体积。供体室保持接近环境条件。按照方案中指示的时间间隔收集馏分,持续最长24小时时间点。在研究结束时,收集未给药的皮肤样品,随后收集经处理的皮肤。
将洗涤和胶带剥离的皮肤置于铝箔上,其中真皮面朝下。如果适用,将肛周组织样品放置在设定为60℃的烘箱中大约2.0分钟。镊子被用来分离表皮与真皮。将经清洁的组织置于各自预称重的带标签的小瓶中,并记录组织的重量。首先处理未给药的皮肤样品,并且置于小瓶中,随后处理皮肤。
将经清洁的表皮和真皮组织置于各自预称重的带标签的小瓶中,并记录组织的重量。按照以下的方案,使用Omni Prep均化器将表皮和真皮组织样品均化:
a)使用新鲜的手术刀片将组织适当且均匀地切碎。
b)将2000μL均化溶剂(50:50,v/v甲醇/LC-MS级水)添加至含有皮肤样品的带标签的管中。
c)将组织按4.5m/s,3x30秒,45秒停歇时间进行均化。
d)均化完成后,使用800μL乙腈,将200μL该等分试样用于API(硝苯地平和盐酸利多卡因)提取,短暂涡旋,然后在水浴中超声处理10分钟。
e)在5℃下,将小瓶以10,000RPM离心5分钟。
f)上清液将用于质谱分析,以确认API的存在并定量(LC/MS)其量。
通过用1个干棉签、1个浸渍在70%乙醇(v/v)洗涤溶剂中的湿棉签和1个干棉签,随后用一个连续的胶带条清洁,进行皮肤组织表面上制剂的回收。将棉签和胶带条收集在带标签的小瓶中用于分析。然后使组织经受均化和蛋白质破碎,以提取吸附的制剂。首先将未给药的皮肤样品进行清洁,随后在干净的解剖板上对经处理的皮肤进行清洁。
a)将10mL ACN添加至收集的胶带条和棉签中,置于搅拌板上,并以600RPM搅拌过夜。
b)将200μL等分试样的上清液用于质谱分析。
将所有样品在2℃-8℃下短期储存(少于一周)或在-20℃下长期储存(超过一周),直到通过LC-MS/MS进行分析。分析表明当与基于擦拭物的递送制剂(F2)和基于软膏的递送制剂(F3)相比时,对于基于溶液的递送制剂(F1),盐酸利多卡因通过组织的累积渗透量更高。
用于计算累积渗透量的公式是每次收集的分析物浓度x样品体积,然后将其添加至在先前时间点的相同收集物中。Jmax是研究期间由每次重复所达到的经计算的最大流量值。用数学方法计算Jmax的公式是分配系数Kp(以cm/h表示),这是分析物的扩散特性乘以水饱和溶解度Csat-max(用mg/L表示)。Jmax=Kp x Csat-max。
有意思的是,当与基于软膏的递送制剂(F3)相比时,对于基于擦拭物的递送制剂(F2),盐酸利多卡因通过组织的累积渗透量更高。(参见图7)。类似的趋势在当与F2和F3相比时,F1中平均流量测量更高的情况下观察到。同样,相比F3,F2的平均流量更高。(参见图8)。
分析还表明,当与基于擦拭物的递送制剂(F2)和基于软膏的递送制剂(F3)相比时,对于基于溶液的递送制剂(F1),硝苯地平通过组织的累积渗透量更高。有意思的是,当与基于软膏的递送制剂(F3)相比时,对于基于擦拭物的递送制剂(F2),硝苯地平通过组织的累积渗透量更高。(参见图9)。类似的趋势在当与F2和F3相比时,F1中平均流量测量更高的情况下观察到。同样,相比F3,F2的平均流量更高。(参见图10)。
图11中显示了对于三种类型的递送制剂,盐酸利多卡因在组织中的保留。当与基于擦拭物的递送制剂(F2)和基于软膏的递送制剂(F3)相比时,在基于溶液的递送制剂(F1)中盐酸利多卡因在组织中的保留更高。同样,与基于软膏的递送制剂(F3)相比,在基于擦拭物的递送制剂(F2)中盐酸利多卡因在组织中的保留更高。
图12中显示了对于三种类型的递送制剂,硝苯地平在组织中的保留。当与基于擦拭物的递送制剂(F2)和基于软膏的递送制剂(F3)相比,在基于溶液的递送制剂(F1)中,硝苯地平在组织中的保留更高。同样,与基于软膏的递送制剂(F3)相比,在基于擦拭物的递送制剂(F2)中,硝苯地平在组织中的保留更高。
实验表明,硝苯地平和盐酸利多卡因的基于擦拭物的递送比基于软膏的递送更有效。通过擦拭物递送的硝苯地平和盐酸利多卡因的制剂能够穿透肛周组织长达24小时,并且通过IVPT研究进行观察。局部溶液呈现了药物分子在作用部位的绝对可利用性,但是从患者使用和依从性的角度来看并不实用。
通过引用并入
本文提及的所有出版物和专利都通过引用以其全文特此并入,就好像每个单独的出版物或专利都被具体和单独地指出通过引用并入一样。
其他实施方案
虽然已经讨论了主题的具体实施方案,但是以上说明是说明性的而非限制性的。在通过综述本说明书和下面的权利要求,许多变化对于本领域技术人员来说将变得显而易见。本发明的全部范围应当通过参考权利要求及其等同物的全部范围、说明书及其此类变化来确定。
