用于进行NHEJ介导的基因组编辑的组合物和方法
文献发布时间:2023-06-19 12:14:58
本申请要求于2018年10月30日提交的美国临时专利申请序列号62/752,959的优先权权益,所述申请的全部内容通过引用以其整体(包含任何附图)明确并入本文中。
所附序列表中的材料特此通过引用并入到本申请中。名称为052984-528001WO_Sequence Listing.txt的所附序列表文本文件创建于2019年10月28日并且大小为24,932字节。
技术领域
本公开涉及用于通过同源非依赖性机制在细胞中进行基因组编辑的组合物和方法。进一步提供了使用此类工程化细胞的方法,如用于治疗各种疾病和病状。
背景技术
重症综合性免疫缺陷是罕见的基因病症,最常见的原因是与淋巴发育相关的基因(例如,IL2Rg、RAG1和IL7R)或与淋巴细胞增殖和代谢相关的基因(例如,ADA和PNP)的突变。疾病的表型的特征在于缺乏T细胞和/或B细胞,因此导致无法抵抗感染。
当前,针对SCID的最常见的治愈是为可以发现足够接近匹配的那些患者进行骨髓移植。虽然接受骨髓移植的患者中有80%存活,但是他们会终生受到免疫抑制。已经尝试用γ-逆转录病毒进行基因疗法,但是白血病的高发生率已使工作停止。
大多数SCID患者的特定基因座具有突变,所述突变已经是SCID的筛选的一部分。一旦被鉴定,就可以收集来自患者的骨髓的造血干细胞(HSC)以通过基因置换或基因校正来对一个或多个引起SCID的突变基因进行靶向基因组编辑。然而,当前用于在HSC中进行基因编辑的技术不能产生持续足够长以产生有效治疗益处的经编辑的HSC。因此,需要用于与HSC一起使用的改进的基因编辑技术。
发明内容
一方面,本文提供了一种用于在造血干细胞(HSC)中的靶基因座处进行基因组修饰的方法,所述方法包括:(a)将核酸酶或对所述核酸酶进行编码的核酸引入到所述HSC中,其中所述靶基因座包括所述核酸酶的第一识别序列;以及(b)将双链供体核酸引入到所述HSC中,其中所述双链核酸包括外源核酸序列并且被配置成通过同源非依赖性机制插入到所述靶基因座中。在一些实施例中,所述HSC是长期移植HSC(LT-HSC)或SCID重新填充细胞。在一些实施例中,所述HSC的特征在于以下标志物:Lin
另一方面,本文中提供了一种用于在静止T细胞中的靶基因座处进行基因组修饰的方法,所述方法包括:(a)将核酸酶或对所述核酸酶进行编码的核酸引入到所述静止T细胞中,其中所述靶基因座包括所述核酸酶的第一识别序列;以及(b)将双链供体核酸引入到所述静止T细胞中,其中所述双链核酸包括外源核酸序列并且被配置成通过同源非依赖性机制插入到所述靶基因座中。在一些实施例中,所述静止T细胞是未经活化的T细胞。
另一方面,本文中提供了一种用于在HDR缺陷细胞中的靶基因座处进行基因组修饰的方法,所述方法包括:(a)将核酸酶或对所述核酸酶进行编码的核酸引入到所述HDR缺陷细胞中,其中所述靶基因座包括所述核酸酶的第一识别序列;(b)将双链供体核酸引入到所述HDR缺陷细胞中,其中所述双链核酸包括外源核酸序列并且被配置成通过同源非依赖性机制插入到所述靶基因座中;以及(c)培养所述HDR缺陷细胞持续足以将所述双链供体核酸整合到所述靶基因座中的时间,其中步骤(a)、(b)和(c)被执行使得所述双链供体核酸的插入效率为至少约4%。在一些实施例中,所述双链供体核酸的插入效率为至少约8%。
在一些实施例中,根据上文所描述的用于进行基因组修饰的方法中的任何方法,所述双链供体核酸进一步包括侧接所述外源核酸序列的第一末端的所述核酸酶的第二识别序列。在一些实施例中,所述双链供体核酸进一步包括侧接所述外源核酸序列的第二末端的第三识别序列。在一些实施例中,所述双链供体核酸在引入到所述细胞中之后在所述第二识别序列和/或所述第三识别序列处被切割。
在一些实施例中,根据上文所描述的用于进行基因组修饰的方法中的任何方法,所述双链供体核酸被配置成使得经切割的双链供体核酸以期望的朝向插入到所述靶基因座中不会在经修饰的靶基因座中产生所述核酸酶的识别序列,并且所述经切割的双链供体核酸以其它朝向插入到所述靶基因座中在所述经修饰的靶基因座中产生所述核酸酶的识别序列。
在一些实施例中,根据上文所描述的用于进行基因组修饰的方法中的任何方法,所述核酸酶是RNA引导的核酸内切酶(RGEN),所述靶基因座和所述双链供体核酸中的所述核酸酶的所述识别序列中的每个识别序列是原间隔子序列,并且所述方法进一步包括将靶向所述原间隔子序列中的一个或多个原间隔子序列的一个或多个gRNA引入到所述细胞中。在一些实施例中,所述方法包括将包括靶向所述靶基因座和所述供体核酸中的原间隔子的间隔子的gRNA引入到所述细胞中。在一些实施例中,所述靶基因座中的所述原间隔子处于正向朝向,所述双链供体核酸中的所述外源核酸处于正向朝向,并且所述双链供体核酸中的所述原间隔子处于反向朝向。在一些实施例中,所述靶基因座和所述供体核酸中的所述原间隔子是相同的。在一些实施例中,所述靶基因座和所述供体核酸中的所述原间隔子中的至少一个原间隔子是与gRNA间隔子不完全匹配的延迟作用原间隔子(DAP)。在一些实施例中,所述DAP:i)其长度比所述gRNA间隔子短至少约1个核苷酸;和/或ii)其包括与所述gRNA间隔子错配的至少约1个核苷酸。在一些实施例中,所述供体核酸中的所述原间隔子是DAP,并且所述靶基因座中所述原间隔子与所述gRNA间隔子完全匹配。在一些实施例中,所述双链供体核酸包括侧接所述外源核酸序列的两个DAP。在一些实施例中,所述供体核酸中的所述原间隔子与所述gRNA间隔子完全匹配,并且所述靶基因座中的所述原间隔子是DAP。
在一些实施例中,根据上文所描述的用于采用RGEN进行基因组修饰的方法中的任何方法,所述RGEN是Cas9核酸酶。
在一些实施例中,根据上文所描述的使用RGEN的用于进行基因组修饰的方法中的任何方法,所述方法包括将包括所述RGEN和所述一个或多个gRNA的核糖核蛋白(RNP)引入到所述细胞中。
在一些实施例中,根据上文所描述的使用RGEN的用于进行基因组修饰的方法中的任何方法,所述方法包括将对所述RGEN进行编码的mRNA引入到所述细胞中。
在一些实施例中,根据上文所描述的用于进行基因组修饰的方法中的任何方法,所述双链供体核酸是双链病毒基因组。在一些实施例中,所述双链病毒基因组是腺病毒基因组、慢病毒基因组或腺相关病毒(AAV)基因组。在一些实施例中,所述AAV基因组是自身互补AAV(scAAV)基因组。在一些实施例中,所述scAAV基因组是scAAV6基因组。
在一些实施例中,根据上文所描述的用于进行基因组修饰的方法中的任何方法,所述核酸酶或对所述核酸酶进行编码的核酸在所述供体核酸被引入到所述细胞中之前被引入到所述细胞中。在一些实施例中,所述核酸酶或对所述核酸酶进行编码的核酸在所述供体核酸被引入到所述细胞中之前不超过1小时被引入到所述细胞中。在一些实施例中,所述核酸酶或对所述核酸酶进行编码的核酸在所述供体核酸被引入到所述细胞中之前不超过5分钟被引入到所述细胞中。
在一些实施例中,根据上文所描述的用于进行基因组修饰的方法中的任何方法,所述细胞在缺氧条件下进行培养。
在一些实施例中,根据上文所描述的用于进行基因组修饰的方法中的任何方法,所述细胞在将所述核酸酶或对所述核酸酶进行编码的核酸和所述供体核酸引入到所述细胞前不超过约48小时进行培养。在一些实施例中,所述细胞在将所述核酸酶或对所述核酸酶进行编码的核酸和所述供体核酸引入到所述细胞前不超过约24小时进行培养。在一些实施例中,所述细胞在将所述核酸酶或对所述核酸酶进行编码的核酸和所述供体核酸引入到所述细胞前不超过约2小时进行培养。
在一些实施例中,根据上文所描述的用于进行基因组修饰的方法中的任何方法,所述细胞在存在Notch配体的情况下进行培养。在一些实施例中,所述Notch配体是δ样Notch配体(DLL)、锯齿状1、锯齿状2或其缀合物。在一些实施例中,所述δ样Notch配体是DLL1、DLL3或DLL4。在一些实施例中,所述Notch配体是Fc-DLL1、Fc-DLL3、Fc-DLL4、Fc-锯齿状1或Fc-锯齿状2。
另一方面,一种用于将包括插入在靶基因座处的外源核酸序列的经编辑的HSC移植在个体中的方法,所述方法包括:(a)对从所述个体获得的HSC的输入群体执行根据上文所描述的实施例中的任何实施例的用于进行基因组修饰的方法以产生包括经编辑的HSC的群体的HSC的输出群体,所述经编辑的HSC包括插入在所述靶基因座处的所述外源核酸序列;以及(b)向所述个体施用所述经编辑的HSC的群体,使得所述经编辑的HSC移植在所述个体中(例如,使得所述经编辑的HSC在所述个体中存在至少约1周、2周、3周、4周、5周、6周、7周、8周、9周、10周、11周、12周、13周、14周、15周、16周或更多周中的任何一个)。在一些实施例中,所述个体中的经编辑的HSC的移植量等于或大于使用同源依赖性机制制备的对应的经编辑的HSC的移植量。在一些实施例中,从所述个体获得的所述HSC的输入群体包括HSC的混合群体,所述HSC的混合群体包括LT-HSC和短期移植HSC(ST-HSC),并且移植的所述经编辑的HSC的群体包括经编辑的LT-HSC。在一些实施例中,向所述个体施用所述经编辑的HSC的群体包括向所述个体施用所述HSC的输出群体。
另一方面,本文中提供了一种工程化HSC,其包括:(a)包括核酸酶的第一识别序列的靶基因座;(b)所述核酸酶或对所述核酸酶进行编码的核酸;以及(c)包括外源核酸序列的双链供体核酸,其中所述双链供体核酸被配置成通过同源非依赖性机制插入到所述靶基因座中。在一些实施例中,所述HSC是LT-HSC或SCID重新填充细胞。在一些实施例中,所述HSC的特征在于以下标志物:Lin
另一方面,本文中提供了一种工程化HSC,其通过根据上文所描述的实施例中的任何实施例的用于在细胞中的靶基因座处进行基因组修饰的方法来制备。在一些实施例中,所述方法包括:(a)将核酸酶或对所述核酸酶进行编码的核酸引入到输入HSC中,其中所述靶基因座包括所述核酸酶的第一识别序列;以及(b)将双链供体核酸引入到所述输入HSC中,其中所述双链核酸包括外源核酸序列并且被配置成通过同源非依赖性机制(例如,NHEJ)插入到所述靶基因座中。在一些实施例中,所述HSC是LT-HSC或SCID重新填充细胞。在一些实施例中,所述HSC的特征在于以下标志物:Lin
另一方面,本文中提供了一种工程化静止T细胞,其包括:(a)包括核酸酶的第一识别序列的靶基因座;(b)所述核酸酶或对所述核酸酶进行编码的核酸;以及(c)包括外源核酸序列的双链供体核酸,其中所述双链供体核酸被配置成通过同源非依赖性机制插入到所述靶基因座中。在一些实施例中,所述静止T细胞是未经活化的T细胞。
另一方面,本文中提供了一种工程化静止T细胞,其通过根据上文所描述的实施例中的任何实施例的用于在细胞中的靶基因座处进行基因组修饰的方法来制备。在一些实施例中,所述方法包括:(a)将核酸酶或对所述核酸酶进行编码的核酸引入到输入静止T细胞中,其中所述靶基因座包括所述核酸酶的第一识别序列;以及(b)将双链供体核酸引入到所述输入静止T细胞中,其中所述双链核酸包括外源核酸序列并且被配置成通过同源非依赖性机制(例如,NHEJ)插入到所述靶基因座中。在一些实施例中,所述静止T细胞是未经活化的T细胞。
在一些实施例中,根据上文所描述的工程化细胞中的任何工程化细胞,所述双链供体核酸进一步包括侧接所述外源核酸序列的第一末端的所述核酸酶的第二识别序列。在一些实施例中,所述双链供体核酸进一步包括侧接所述外源核酸序列的第二末端的第三识别序列。
在一些实施例中,根据上文所描述的工程化细胞中的任何工程化细胞,所述双链供体核酸被配置成使得经切割的双链供体核酸以期望的朝向插入到所述靶基因座中不会在经修饰的靶基因座中产生所述核酸酶的识别序列,并且所述经切割的双链供体核酸以其它朝向插入到所述靶基因座中在所述经修饰的靶基因座中产生所述核酸酶的识别序列。
在一些实施例中,根据上文所描述的工程化细胞中的任何工程化细胞,所述核酸酶是RNA引导的核酸内切酶(RGEN),所述靶基因座和所述双链供体核酸中的所述核酸酶的所述识别序列中的每个识别序列是原间隔子序列,并且所述工程化细胞进一步包括对所述靶基因座和所述双链供体核酸中的所述核酸酶的每个不同的识别序列具有特异性的一个或多个gRNA。在一些实施例中,所述工程化细胞包括包括靶向所述靶基因座和所述供体核酸中的原间隔子的间隔子的gRNA。在一些实施例中,所述靶基因座中的所述原间隔子处于正向朝向,所述双链供体核酸中的所述外源核酸处于正向朝向,并且所述双链供体核酸中的所述原间隔子处于反向朝向。在一些实施例中,所述靶基因座和所述供体核酸中的所述原间隔子是相同的。在一些实施例中,所述靶基因座和所述供体核酸中的所述原间隔子中的至少一个原间隔子是与gRNA间隔子不完全匹配的延迟作用原间隔子(DAP)。在一些实施例中,所述DAP:i)其长度比所述gRNA间隔子短至少约1个核苷酸;和/或ii)其包括与所述gRNA间隔子错配的至少约1个核苷酸。在一些实施例中,所述供体核酸中的所述原间隔子是DAP,并且所述靶基因座中所述原间隔子与所述gRNA间隔子完全匹配。在一些实施例中,所述双链供体核酸包括侧接所述外源核酸序列的两个DAP。在一些实施例中,所述供体核酸中的所述原间隔子与所述gRNA间隔子完全匹配,并且所述靶基因座中的所述原间隔子是DAP。
在一些实施例中,根据上文所描述的包括RGEN的工程化细胞中的任何工程化细胞,所述RGEN是Cas9核酸酶。
在一些实施例中,根据上文所描述的包括RGEN的工程化细胞中的任何工程化细胞,所述工程化细胞包括核糖核蛋白(RNP),所述RNP包括所述RGEN和所述一个或多个gRNA。
在一些实施例中,根据上文所描述的包括RGEN的工程化细胞中的任何工程化细胞,所述工程化细胞包括对所述RGEN进行编码的mRNA。
在一些实施例中,根据上文所描述的工程化细胞中的任何工程化细胞,所述双链供体核酸是双链病毒基因组。在一些实施例中,所述双链病毒基因组是腺病毒基因组、慢病毒基因组或腺相关病毒(AAV)基因组。在一些实施例中,所述AAV基因组是自身互补AAV(scAAV)基因组。在一些实施例中,所述scAAV基因组是scAAV6基因组。
另一方面,本文中提供了一种治疗受试者的疾病或病状的方法,其中所述疾病或病状的特征在于功能性蛋白质的缺陷表达,所述方法包括向所述受试者施用根据上文所描述的实施例中的任何实施例的工程化细胞,其中所述外源核酸对可以在所述工程化细胞中表达的所述蛋白质的功能性形式进行编码。在一些实施例中,所述疾病或病状是SCID,并且其中所述外源核酸包括在涉及淋巴发育或淋巴细胞增殖和/或代谢的所述个体中突变的基因的功能性形式。在一些实施例中,所述外源核酸对IL2Rg、RAG1、IL7R、ADA或PNP的功能性形式进行编码。在一些实施例中,所述疾病或病状是高雪氏病(Gaucher disease)、法布里病(Fabry disease)、黏多糖贮积症I-IX型或肾上腺脑白质营养不良。
附图说明
图1A示出了如通过在存在或不存在Cas9/gRNA RNP的情况下用所指示浓度的pCR2.1-TOPO-psSCRAM-SA-P2A-H2Bj-Venus-BGHpA-psSCRAM(0切口载体质粒)或pCR2.1-TOPO-psAAVS1-SA-P2A-H2Bj-Venus-BGHpA-psSCRAM(1切口载体质粒)处理的K562细胞中的GFP表达测定的NHEJ介导的靶向整合的第14天(D14)时的流式细胞术结果,其中pCR2.1-TOPO是载体质粒主链,psSCRAM是用PAM加扰的原间隔子序列,psAAVS1是用PAM切割Cas9/gRNARNP的基因组DNA序列相同的原间隔子序列,SA是剪接受体,P2A是肽切割信号序列,H2Bi-Venus是与使细胞核中的GFP稳定的组蛋白H2B融合的经修饰的GFP,并且BGHpA是牛生长激素聚腺苷酸化序列。
图1B示出了图1A的流式细胞术研究在第7天(D7)和第14天(D14)时的定量。
图2示出了在存在或不存在Cas9/gRNA RNP的情况下对K562细胞中的所指示浓度的0切口载体质粒或1切口载体质粒的靶向供体整合进行的PCR分析。
图3A示出了通过HDR、NHEJ或HDR和NHEJ两者在经活化的T细胞中进行的靶向整合的流式细胞术结果。
图3B示出了图3A的流式细胞术研究的定量。
图4示出了在通过使用分别递送HDR供体、scAAV6 2切口NHEJ供体或两者的AAV6通过HDR、NHEJ或HDR和NHEJ两者进行靶向整合的情况下,经活化的T细胞的CD4/CD8分布的流式细胞术结果。
图5A示出了通过使用分别递送HDR供体、scAAV6 2切口NHEJ供体或两者的AAV6通过HDR、NHEJ或HDR和NHEJ两者在未经活化的T细胞中进行的靶向整合的流式细胞术结果。
图5B示出了图5A的流式细胞术研究的定量。
图5C示出了在通过NHEJ进行靶向整合的情况下,未经活化的T细胞的CD4/CD8分布的流式细胞术结果。
图6示出了使用方案1或方案2在人CD34
图7A示出了使用方案1或方案2在人CD34
图7B示出了在来自两个不同的供体与scAAV6 2切口供体的人CD34
图8A示出了使用方案1或方案2在人CD34
图8B示出了在来自两个不同的供体与scAAV6 2切口供体的人CD34
图9A示出了当在D1时进行编辑时,使用方案1或方案2在人CD34
图9B示出了当在D1时进行编辑时,使用方案1或方案2在人CD34
图9C示出了当在D1时进行编辑时,使用方案1或方案2在人CD34
图9D示出了当在D1时进行编辑时,使用方案1或方案2在人CD34
图10A示出了当在D1时在SFEM II培养基中进行编辑时,在人CD34
图10B示出了当在D1时在SCGM培养基中进行编辑时,在人CD34
图11A示出了当在D1时在缺氧或常氧条件下用scAAV6 2切口供体进行编辑时,在人CD34
图11B示出了当在D1时在缺氧或常氧条件下用scAAV6 2切口供体进行编辑时,在人CD34
图11C示出了当在D1时在缺氧或常氧条件下用scAAV6 2切口供体进行编辑时,在人CD34
图11D示出了当在D1时在缺氧或常氧条件下用scAAV6 2切口供体进行编辑时,在人CD34
图12A示出了当在D1或D2时用scAAV6 2切口供体进行编辑时,在人CD34
图12B示出了当在D1或D2时用scAAV6 2切口供体进行编辑时,在人CD34
图12C示出了当在D1或D2时用scAAV6 2切口供体进行编辑时,在人CD34
图13示出了当在H1(第1个小时)或D1时用scAAV6 2切口供体进行编辑时,在人CD34
图14A示出了当在D1时使用RNP Lonza 4-D核转染方案DZ-100或RNP Lonza 4-D核转染方案CA-137进行编辑时,在人CD34
图14B示出了当在D1时使用RNP Lonza 4-D核转染方案DZ-100或RNP Lonza 4-D核转染方案CA-137进行编辑时,在人CD34
图14C示出了当在D1时使用RNP Lonza 4-D核转染方案DZ-100或RNP Lonza 4-D核转染方案CA-137进行编辑时,在人CD34
图15示出了当在D1时使用SpyFi Cas9或GeneArt Cas9进行编辑时,在人CD34
图16示出了当在D1时使用低(+)或高(+++)量的RNP和低(+)或高(+++)量的AAV进行编辑时,在人CD34
图17示出了在存在或不存在Cas9/gRNA RNP的情况下由Ad5/35以5000vp/细胞在CD34
图18A示出了使用在生腱蛋白C(TenC)、Fc-DLL1(DLL1)或生腱蛋白C+Fc-DLL1涂层或无涂层上培养的scAAV60切口供体在人CD34
图18B示出了使用在生腱蛋白C(TenC)、Fc-DLL1(DLL1)或生腱蛋白C+Fc-DLL1涂层或无涂层上培养的scAAV6 0切口供体在人CD34
图19示出了来自在D2时注射了通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图20A示出了来自在D2时注射了通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图20B示出了在D1时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图21示出了通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1的H1(新鲜解冻)编辑的人CD34
图22A示出了i)在D2时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图22B示出了i)在D1时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图22C示出了i)在D2时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图22D示出了i)在D2时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图23A示出了i)在D2时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图23B示出了i)在D1时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图23C示出了i)在D2时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图23D示出了i)在D2时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图24A示出了i)在D2时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图24B示出了i)在D1时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图24C示出了i)在D2时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图24D示出了i)在D2时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图25A示出了i)在D2时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图25B示出了i)在D1时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图25C示出了i)在D2时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图25D示出了i)在D2时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图26A示出了i)在D2时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图26B示出了i)在D1时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图26C示出了i)在D2时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图26D示出了i)在D2时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图27A示出了i)在D2时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图27B示出了i)在D1时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图28A示出了i)在D2时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图28B示出了i)在D2时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图28C示出了i)在D2时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图29A示出了i)在D2时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图29B示出了i)在D2时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
图29C示出了i)在D2时用通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
具体实施方式
申请人已经发现了用于在进行同源性定向修复(HDR)较差的细胞中的靶基因座处进行基因组修饰的系统和方法。具体地,申请人已经证实了长期移植造血干细胞(LT-HSC)和其它静止细胞(包含静止(静息)T细胞)中的改进的编辑以及制备和使用工程化细胞的方法和可用于此类方法的组合物。
先前的数据已经示出了,经历HDR的HSC是已经丧失长期移植潜能的那些HSC,从而使得经校正的HSC无法对疾病进行永久性治疗校正。相反,保留长期移植潜能的HSC是不分裂的并且因此并未有效地经历HDR。相比之下,非同源末端连接(NHEJ)是在所有细胞类型(包含静止细胞,如LT-HSC)中起作用的DNA双链断裂(DSB)修复机制。申请人发现了,可以操纵这个途径来介导静止LT-HSC和静止T细胞中的转基因的靶向整合,所述靶向整合允许经编辑的细胞的长期移植和转基因的持续表达。例如,使用CRISPR/Cas9系统对人CD34
除非另外定义,否则本文使用的所有技术术语和科学术语具有与本公开所属领域的普通技术人员通常所理解的含义相同的含义。除非另有说明,否则本文所引用的所有专利、申请、公开的申请和其它出版物通过引用以其整体明确并入本文中。在本文中所用术语存在多个定义的情况下,除非另外说明,否则以在这个部分中的那些定义为主。
如本文中所使用的,“一个(a)”或“一种(an)”可以意指一个或多于一个。
当根据说明书阅读时,“约”具有其简单和普通的含义,并且可以例如在提及可测量值时使用并且可以意指涵盖相较于指定值的±20%或±10%、更优选地±5%、甚至更优选地±1%以及仍更优选地±0.1%的变化。
如本文中所使用的,“蛋白质序列”是指氨基酸的多肽序列,其是蛋白质的一级结构。如本文中所使用的,“上游”是指多核苷酸上的定位的位置5′以及朝向多肽上的定位的N端的位置。如本文中所使用的,“下游”是指核苷酸上的定位的位置3′以及朝向多肽上的定位的C端的位置。因此,术语“N端”是指朝向多肽上的定位的N端的多核苷酸上的元件或定位的位置。
“核酸”或“核酸分子”是指多核苷酸(如脱氧核糖核酸(DNA)或核糖核酸(RNA))、寡核苷酸、通过聚合酶链反应(PCR)产生的片段以及通过连接、断裂、核酸内切酶作用和核酸外切酶作用中的任何一个产生的片段。核酸分子可以由是天然存在的核苷酸(如DNA和RNA)的单体或天然存在的核苷酸的类似物(例如,天然存在的核苷酸的对映异构形式)或两者的组合构成。经修饰的核苷酸可以在糖部分中和/或在嘧啶或嘌呤碱基部分中具有改变。糖修饰包含例如用卤素、烷基、胺和叠氮基置换一个或多个羟基,或者糖可以被官能化为醚或酯。此外,整个糖部分可以被空间和电子类似的结构(如氮杂糖和碳环糖类似物)置换。碱基部分中的修饰的实例包含烷基化的嘌呤和嘧啶、酰化的嘌呤或嘧啶或其它众所周知的杂环取代基。核酸单体可以通过磷酸二酯键或此类连接的类似物连接。磷酸二酯键的类似物包含硫代磷酸酯、二硫代磷酸酯、硒代磷酸酯、二硒代磷酸酯、硫代苯胺磷酸酯、苯胺磷酸酯、氨基磷酸酯等。术语“核酸分子”还包括所谓的“肽核酸”,其包括附着到聚酰胺主链的天然存在或经修饰的核酸碱基。核酸可以是单链或双链的。在一些实施例中,提供了对融合蛋白进行编码的核酸序列。在一些实施例中,核酸是RNA或DNA。
本文中所使用的“编码(coding for)”或“编码(encoding)”是指多核苷酸(如基因、cDNA或mRNA)中的特定核苷酸序列充当用于合成其它大分子(如所定义的氨基酸序列)的模板的特性。因此,如果与基因相对应的mRNA的转录和翻译在细胞或其它生物系统中产生蛋白质,则所述基因对蛋白质进行编码。
“对多肽进行编码的核酸序列”包括彼此为简并形式并且对相同氨基酸序列进行编码的所有核苷酸序列。在一些实施例中,提供了核酸,其中所述核酸对融合蛋白进行编码。
“载体”、“表达载体”、“供体”或“构建体”是用于将异源核酸引入到细胞中的核酸,其具有调节元件以提供异源核酸在细胞中的表达。载体包含但不限于质粒、微环、酵母和病毒基因组。在一些实施例中,载体是质粒、微环、酵母或病毒基因组。在一些实施例中,载体是病毒载体。在一些实施例中,病毒载体是慢病毒。在一些实施例中,载体是腺相关病毒(AAV)载体。在一些实施例中,载体是用于在细菌系统(如大肠杆菌)中进行蛋白质表达。如本文中所使用的,术语“表达”或“蛋白质表达”是指转录的RNA分子翻译成蛋白质分子。蛋白质表达的特征可能在于过其时间、空间、发育或形态学性质以及在于定量或定性指示。在一些实施例中,一个或多个蛋白质的表达使得蛋白质在存在配体的情况下被定位用于二聚化。
如本文中所使用的,术语“调节元件”是指具有基因调节活性的DNA分子,例如具有影响可操作地连接的可转录DNA分子的转录和/或翻译的能力的DNA分子。调节元件(如启动子、前导区、内含子和转录终止区)是具有基因调节活性并在基因在活细胞中的整体表达中发挥重要作用的DNA分子。因此,在植物中起作用的分离的调节元件(如启动子)对于通过基因工程化方法修饰植物表型而言是有用的。
如本文中所使用的,术语“可操作地连接”是指第一分子连接到第二分子,其中分子的此种布置使得第一分子影响第二分子的功能。两个分子可以是单个连续分子的一部分并且可以是相邻的。例如,如果启动子调节细胞中的所关注的可转录DNA分子的转录,则所述启动子可操作地连接到所述可转录DNA分子。
“启动子”是引发特定基因的转录的DNA的区域。启动子可以位于基因的转录起始位点附近、在同一条链上以及在DNA的上游(有义链的5′区域)。启动子可以是条件型启动子、诱导型启动子或组成型启动子。启动子可以对细菌、哺乳动物或昆虫细胞蛋白质表达具有特异性。在一些实施例中,其中提供了对融合蛋白进行编码的核酸,所述核酸进一步包括启动子序列。在一些实施例中,启动子对细菌、哺乳动物或昆虫细胞蛋白质表达具有特异性。在一些实施例中,启动子是条件型启动子、诱导型启动子或组成型启动子。
如本文中所使用的,“受试者”是指作为治疗、观察或实验的对象的动物。“动物”包括冷血和温血脊椎动物和无脊椎动物,如鱼、甲壳类动物、爬行动物,并且特别是哺乳动物。“哺乳动物”包括但不限于小鼠、大鼠、兔子、豚鼠、狗、猫、绵羊、山羊、牛、马、灵长类动物(如猴、黑猩猩和猿,并且特别是人)。在一些替代性中,受试者是人。
一方面,本文中提供了一种用于生成工程化细胞(例如,工程化造血干细胞,如LT-HSC)的系统,所述系统包括外源核酸的靶向整合,其中所述外源核酸通过非同源末端连接(NHEJ)插入到靶基因座中。所述系统包括:(a)核酸酶或对所述核酸酶进行编码的核酸,其中所述核酸酶能够在包括所述核酸酶的第一识别序列的靶基因座处进行介导性基因组编辑;以及(b)双链供体核酸,其中所述双链供体核酸包括外源核酸序列并且被配置成通过NHEJ插入到所述靶基因座中。在一些实施例中,所述系统进一步包括要编辑的细胞。尤其还提供了用于使用离体基因组编辑治疗患有或疑似患有与功能性靶蛋白缺陷相关的病症或健康病状的受试者的系统。例如,在一些实施例中,所述受试者患有由靶细胞中的靶蛋白的功能性缺陷(例如,靶蛋白的缺陷表达和/或活性)导致的疾病,并且所述系统能够介导靶细胞或其祖细胞中的基因组编辑,所述基因组表达允许靶蛋白或其功能性衍生物在所述受试者中的经基因组编辑的细胞或其后代中充分表达,使得疾病被治疗。在一些实施例中,所述靶细胞或其祖细胞进行离体编辑并且施用于所述受试者。
在一些实施例中,根据本文中所描述的包括双链供体核酸的系统中的任何系统,所述双链供体核酸进一步包括侧接所述外源核酸序列的第一末端的所述核酸酶的第二识别序列。例如,在一些实施例中,所述核酸酶的所述第二识别序列紧邻所述外源核酸序列的所述第一末端或远离所述外源核酸序列的所述第一末端约5个或更多个(如约10个、20个、50个、100个、200个、500个、1000个或更多个中的任何一个)碱基。在一些实施例中,所述双链供体核酸进一步包括侧接所述外源核酸序列的第二末端的第三识别序列。例如,在一些实施例中,所述核酸酶的所述第三识别序列紧邻所述外源核酸序列的所述第二末端或远离所述外源核酸序列的所述第二末端约5个或更多个(如约10个、20个、50个、100个、200个、500个、1000个或更多个中的任何一个)碱基。在一些实施例中,所述双链供体核酸被配置成使得经切割的双链供体核酸以期望的朝向插入到所述靶基因座中不会在经修饰的靶基因座中产生所述核酸酶的识别序列,并且所述经切割的双链供体核酸以其它朝向插入到所述靶基因座中在所述经修饰的靶基因座中产生所述核酸酶的识别序列。
在一些实施例中,根据本文中所描述的包括双链供体核酸的系统中的任何系统,所述双链供体核酸是双链病毒基因组。在一些实施例中,所述双链病毒基因组是腺病毒基因组、慢病毒基因组(例如,慢病毒RNA基因组的dsDNA中间体)或腺相关病毒(AAV)基因组。在一些实施例中,所述AAV基因组是自身互补AAV(scAAV)基因组。在一些实施例中,所述scAAV基因组是scAAV6基因组。在一些实施例中,所述慢病毒基因组是整合酶缺陷型慢病毒基因组。
在一些实施例中,根据本文中所描述的包括核酸酶或对所述核酸酶进行编码的核酸的系统中的任何系统,所述核酸酶是RNA引导的核酸内切酶(RGEN)。在一些实施例中,所述RGEN是Cas9核酸酶。在一些实施例中,所述系统进一步包括能够引导所述RGEN切割所述靶基因座中的所述第一识别序列的gRNA。在一些实施例中,所述gRNA能够引导所述RGEN切割所述供体核酸中的一个或多个识别序列。在一些实施例中,所述系统包括包括所述RGEN和所述gRNA的核糖核蛋白(RNP)。在一些实施例中,所述系统包括对所述RGEN进行编码的核酸。在一些实施例中,对所述RGEN进行编码的所述核酸是mRNA或质粒。
在一些实施例中,根据本文中所描述的包括RGEN或对所述RGEN进行编码的核酸的系统中的任何系统,所述靶基因座和所述双链供体核酸中的所述核酸酶的所述识别序列中的每个识别序列是原间隔子序列。在一些实施例中,所述系统进一步包括靶向所述原间隔子序列中的一个或多个原间隔子序列的一个或多个gRNA。在一些实施例中,所述靶基因座和所述双链供体核酸中的所述原间隔子中的每个原间隔子是相同的,并且所述系统包括靶向所述原间隔子序列的一个gRNA。
在一些实施例中,本文中所描述的系统包括:i)第一核酸,所述第一核酸包括第一原间隔子;以及ii)gRNA,所述gRNA包括间隔子,其中所述第一原间隔子与所述间隔子不完全匹配,并且其中所述第一原间隔子与所述间隔子匹配的程度足以允许在所述第一原间隔子处对所述第一核酸进行修饰。与对应的gRNA有关的此种原间隔子在本文中也被称为“延迟作用原间隔子”或“DAP”。此类系统允许通过改变DAP与间隔子之间的匹配程度来对在第一原间隔子处对第一核酸进行的RGEN介导的切割进行时间控制。在一些实施例中,所述DAP的长度比所述间隔子短至少约1个(如至少约2个、3个或更多个中的任何一个)核苷酸。在一些实施例中,所述DAP包括与所述间隔子的至少约1个(如至少约2个、3个或更多个中的任何一个)核苷酸错配。例如,所述gRNA可以包括来自SEQ ID NO:8的多核苷酸序列的间隔子,并且所述第一原间隔子可以包括来自SEQ ID NO:16-28中任何一个的多核苷酸序列的原间隔子。在一些实施例中,所述系统进一步包括包括第二原间隔子的第二核酸,其中所述第二原间隔子与所述间隔子完全匹配。例如,所述gRNA可以包括来自SEQ ID NO:8的多核苷酸序列的间隔子,并且所述第二原间隔子可以包括来自SEQ ID NO:9的多核苷酸序列的原间隔子。此类系统允许使用单个gRNA在其相应的原间隔子处对所述第一和第二核酸进行的RGEN介导的切割的不同时间分布,相较于与所述gRNA间隔子不完全匹配的所述第一原间隔子处的所述第一核酸的切割的开始,与所述gRNA间隔子完全匹配的所述第二原间隔子处的所述第二核酸的切割的开始较快。
DAP存在于核酸(如靶核酸或供体模板)中以促进靶位点切割的时间控制具有若干优点。一方面,DAP存在于此类核酸中允许对在多个基因座处进行的靶位点切割进行时间控制,而不需要在不同时间时施用的每个基因座的多个gRNA。进而,这允许将基因组编辑系统包装在相对较小的空间中,并且使用较少的gRNA可以减少脱靶效应的机会。对于本领域技术人员而言,本公开的实施例的另外的优点将是显而易见的。
在一些实施例中,根据本文中所描述的系统中的任何系统,所述系统包括:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割外源核酸要插入其中的靶基因座中的第一原间隔子;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在一侧或两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述第一原间隔子和所述第二原间隔子与所述gRNA间隔子完全匹配。在一些实施例中,所述靶基因座中的所述第一原间隔子与所述gRNA间隔子完全匹配,并且所述供体核酸中的所述第二原间隔子是与所述gRNA间隔子不完全匹配的DAP。在一些实施例中,所述靶基因座中的所述第一原间隔子是与所述gRNA间隔子不完全匹配的DAP,并且所述供体核酸中的所述第二原间隔子与所述gRNA间隔子完全匹配。在一些实施例中,所述供体核酸包括所述第二原间隔子侧接在两侧上的所述外源核酸。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。例如,在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。在一些实施例中,所述系统进一步包括包括所述靶基因座的细胞。在一些实施例中,所述细胞缺乏同源性定向修复(HDR)所必需的机制。在一些实施例中,所述细胞是造血干细胞(HSC),如长期移植造血干细胞(LT-HSC)。在一些实施例中,所述细胞是SCID重新填充细胞。在一些实施例中,所述细胞的特征在于以下标志物中的一个或多个(如2个、3个、4个或5个中的任何一个)标志物:Lin
在一些实施例中,根据本文中所描述的系统中的任何系统,所述系统包括:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割外源核酸要插入其中的靶基因座中的第一原间隔子,并且其中所述第一原间隔子与所述gRNA间隔子完全匹配;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,其中所述第二原间隔子是与所述gRNA间隔子不完全匹配的DAP,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。在一些实施例中,所述系统进一步包括包括所述靶基因座的细胞。
在一些实施例中,根据本文中所描述的系统中的任何系统,所述系统包括:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割外源核酸要插入其中的靶基因座中的第一原间隔子,并且其中所述第一原间隔子是与所述gRNA间隔子不完全匹配的DAP;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,其中所述第二原间隔子与所述gRNA间隔子完全匹配,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。在一些实施例中,所述系统进一步包括包括所述靶基因座的细胞。
一方面,本文中提供了一种用于在细胞中的靶基因座处进行基因组修饰的方法,所述方法包括:(a)将核酸酶或对所述核酸酶进行编码的核酸引入到所述细胞中,其中所述靶基因座包括所述核酸酶的第一识别序列;以及(b)将双链供体核酸引入到所述细胞中,其中所述双链核酸包括外源核酸序列并且被配置成通过NHEJ插入到所述靶基因座中。
在一些实施例中,根据上文所描述的用于在细胞中进行基因组修饰的方法中的任何方法,所述细胞缺乏同源性定向修复(HDR)所必需的机制。在一些实施例中,所述细胞是造血干细胞(HSC),如长期移植造血干细胞(LT-HSC)。在一些实施例中,所述细胞是SCID重新填充细胞。在一些实施例中,所述细胞的特征在于以下标志物中的一个或多个(如2个、3个、4个或5个中的任何一个)标志物:Lin
在一些实施例中,根据本文中所描述的使用双链供体核酸的方法中的任何方法,所述双链供体核酸进一步包括侧接所述外源核酸序列的第一末端的所述核酸酶的第二识别序列。在一些实施例中,所述双链供体核酸进一步包括侧接所述外源核酸序列的第二末端的第三识别序列。在一些实施例中,所述双链供体核酸在引入到所述细胞中之后在所述第二识别序列和/或所述第三识别序列处被切割。在一些实施例中,所述双链供体核酸被配置成使得经切割的双链供体核酸以期望的朝向插入到所述靶基因座中不会在经修饰的靶基因座中产生所述核酸酶的识别序列,并且所述经切割的双链供体核酸以其它朝向插入到所述靶基因座中在所述经修饰的靶基因座中产生所述核酸酶的识别序列。
在一些实施例中,根据本文中所描述的使用双链供体核酸的方法中的任何方法,所述双链供体核酸是双链病毒基因组。在一些实施例中,所述双链病毒基因组是腺病毒基因组、慢病毒基因组(例如,慢病毒RNA基因组的dsDNA中间体)或腺相关病毒(AAV)基因组。在一些实施例中,所述AAV基因组是自身互补AAV(scAAV)基因组。在一些实施例中,所述scAAV基因组是scAAV6基因组。在一些实施例中,所述慢病毒基因组是整合酶缺陷型慢病毒基因组。
在一些实施例中,根据本文中所描述的使用核酸酶或对所述核酸酶进行编码的核酸的方法中的任何方法,所述核酸酶是RNA引导的核酸内切酶(RGEN)。在一些实施例中,所述RGEN是Cas9核酸酶。在一些实施例中,所述方法进一步包括将能够引导所述RGEN切割所述靶基因座中的所述第一识别序列的gRNA引入到所述细胞中。在一些实施例中,所述gRNA能够引导所述RGEN切割所述供体核酸中的一个或多个识别序列。在一些实施例中,所述方法包括将包括所述RGEN和所述gRNA的核糖核蛋白(RNP)引入到所述细胞中。在一些实施例中,所述方法包括将对所述RGEN进行编码的核酸引入到所述细胞中。在一些实施例中,对所述RGEN进行编码的所述核酸是mRNA或质粒。
在一些实施例中,根据本文中所描述的采用RGEN或对所述RGEN进行编码的核酸的方法中的任何方法,所述靶基因座和所述双链供体核酸中的所述核酸酶的所述识别序列中的每个识别序列是原间隔子序列。在一些实施例中,所述方法进一步包括将靶向所述原间隔子序列中的一个或多个原间隔子序列的一个或多个gRNA引入到所述细胞中。在一些实施例中,所述靶基因座和所述双链供体核酸中的所述原间隔子中的每个原间隔子是相同的,并且所述方法包括将靶向所述原间隔子序列的一个gRNA引入到所述细胞中。
在一些实施例中,本文中提供了一种用于将外源核酸整合到细胞中的靶基因座中的方法,其中所述细胞基因组包括所述靶基因座中的第一原间隔子:所述方法包括将以下引入到所述细胞中:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割所述靶基因座中的所述第一原间隔子;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在一侧或两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述第一原间隔子和所述第二原间隔子与所述gRNA间隔子完全匹配。在一些实施例中,所述靶基因座中的所述第一原间隔子与所述gRNA间隔子完全匹配,并且所述供体核酸中的所述第二原间隔子是与所述gRNA间隔子不完全匹配的DAP。在一些实施例中,所述靶基因座中的所述第一原间隔子是与所述gRNA间隔子不完全匹配的DAP,并且所述供体核酸中的所述第二原间隔子与所述gRNA间隔子完全匹配。在一些实施例中,所述DAP的长度比所述gRNA间隔子短至少约1个(如至少约2个、3个或更多个中的任何一个)核苷酸。在一些实施例中,所述DAP包括与所述gRNA间隔子的至少约1个(如至少约2个、3个或更多个中的任何一个)核苷酸错配。在一些实施例中,所述供体核酸包括所述第二原间隔子侧接在两侧上的所述外源核酸。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。在一些实施例中,所述细胞缺乏同源性定向修复(HDR)所必需的机制。在一些实施例中,所述细胞是HSC,如LT-HSC。在一些实施例中,所述细胞是SCID重新填充细胞。在一些实施例中,所述细胞的特征在于以下标志物中的一个或多个(如2个、3个、4个或5个中的任何一个)标志物:Lin
在一些实施例中,本文中提供了一种用于将外源核酸整合到细胞中的靶基因座中的方法,其中所述细胞基因组包括所述靶基因座中的第一原间隔子:所述方法包括将以下引入到所述细胞中:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割所述靶基因座中的所述第一原间隔子,并且其中所述第一原间隔子与所述gRNA间隔子完全匹配;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,其中所述第二原间隔子是与所述gRNA间隔子不完全匹配的DAP,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。
在一些实施例中,本文中提供了一种用于将外源核酸整合到细胞中的靶基因座中的方法,其中所述细胞基因组包括所述靶基因座中的第一原间隔子:所述方法包括将以下引入到所述细胞中:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割所述靶基因座中的所述第一原间隔子,并且其中所述第一原间隔子是与所述gRNA间隔子不完全匹配的DAP;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,其中所述第二原间隔子与所述gRNA间隔子完全匹配,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。
在一些实施例中,根据本文中所描述的基因组修饰的方法中的任何方法,所述核酸酶或对所述核酸酶进行编码的核酸在所述供体核酸被引入到所述细胞中之前被引入到所述细胞中。在一些实施例中,所述核酸酶或对所述核酸酶进行编码的核酸在所述供体核酸被引入到所述细胞中之前不超过1小时被引入到所述细胞中。在一些实施例中,所述核酸酶或对所述核酸酶进行编码的核酸在所述供体核酸被引入到所述细胞中之前不超过5分钟被引入到所述细胞中。在一些实施例中,将所述核酸酶或对所述核酸酶进行编码的核酸引入到所述细胞中包括将包括RGEN和gRNA的RNP引入到所述细胞中。在一些实施例中,所述供体核酸是双链病毒基因组,例如scAAV基因组。
在一些实施例中,根据本文中所描述的基因组修饰的方法中的任何方法,所述方法包括在所述供体核酸被引入到所述细胞中之前将包括RGEN和gRNA的RNP引入到所述细胞中。在一些实施例中,所述RNP在所述供体核酸被引入到所述细胞中之前不超过1小时被引入到所述细胞中。在一些实施例中,所述RNP在所述供体核酸被引入到所述细胞中之前不超过5分钟被引入到所述细胞中。在一些实施例中,所述供体核酸是双链病毒基因组,例如scAAV基因组。
在一些实施例中,根据本文中所描述的基因组修饰的方法中的任何方法,所述细胞在缺氧条件下进行培养。
在一些实施例中,根据本文中所描述的基因组修饰的方法中的任何方法,所述细胞在将所述核酸酶或对所述核酸酶进行编码的核酸和所述供体核酸引入到所述细胞前不超过约48小时进行培养。在一些实施例中,所述细胞在将所述核酸酶或对所述核酸酶进行编码的核酸和所述供体核酸引入到所述细胞前不超过约24小时进行培养。在一些实施例中,所述细胞在将所述核酸酶或对所述核酸酶进行编码的核酸和所述供体核酸引入到所述细胞前不超过约2小时进行培养。在一些实施例中,将所述核酸酶或对所述核酸酶进行编码的核酸引入到所述细胞中包括将包括RGEN和gRNA的RNP引入到所述细胞中。在一些实施例中,所述供体核酸是双链病毒基因组,例如scAAV基因组。
在一些实施例中,根据本文中所描述的基因组修饰的方法中的任何方法,所述细胞在存在Notch配体的情况下进行培养。在一些实施例中,所述Notch配体是δ样Notch配体(DLL)、锯齿状1、锯齿状2或其缀合物。在一些实施例中,所述δ样Notch配体是DLL1、DLL3或DLL4。在一些实施例中,所述Notch配体是Fc-DLL1、Fc-DLL3、Fc-DLL4、Fc-锯齿状1或Fc-锯齿状2。
一方面,本文中提供了一种用于在HSC中的靶基因座处进行基因组修饰的方法,所述方法包括:(a)将核酸酶或对所述核酸酶进行编码的核酸引入到所述HSC中,其中所述靶基因座包括所述核酸酶的第一识别序列;(b)将双链供体核酸引入到所述HSC中,其中所述双链核酸包括外源核酸序列并且被配置成通过NHEJ插入到所述靶基因座中。在一些实施例中,所述HSC是长期移植HSC(LT-HSC)或SCID重新填充细胞。在一些实施例中,所述HSC的特征在于以下标志物中的一个或多个(如2个、3个、4个或5个中的任何一个)标志物:Lin
在一些实施例中,本文中提供了一种用于将外源核酸整合到HSC中的靶基因座中的方法,其中所述HSC基因组包括所述靶基因座中的第一原间隔子:所述方法包括将以下引入到所述HSC中:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割所述靶基因座中的所述第一原间隔子;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在一侧或两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述第一原间隔子和所述第二原间隔子与所述gRNA间隔子完全匹配。在一些实施例中,所述靶基因座中的所述第一原间隔子与所述gRNA间隔子完全匹配,并且所述供体核酸中的所述第二原间隔子是与所述gRNA间隔子不完全匹配的DAP。在一些实施例中,所述靶基因座中的所述第一原间隔子是与所述gRNA间隔子不完全匹配的DAP,并且所述供体核酸中的所述第二原间隔子与所述gRNA间隔子完全匹配。在一些实施例中,所述供体核酸包括所述第二原间隔子侧接在两侧上的所述外源核酸。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。在一些实施例中,所述方法包括将包括所述RGEN和所述gRNA的RNP引入到所述HSC中。在一些实施例中,所述方法包括将对所述RGEN进行编码的核酸引入到所述HSC中。在一些实施例中,对所述RGEN进行编码的所述核酸是mRNA或质粒。在一些实施例中,所述RGEN是Cas9。
在一些实施例中,本文中提供了一种用于将外源核酸整合到HSC中的靶基因座中的方法,其中所述HSC基因组包括所述靶基因座中的第一原间隔子:所述方法包括将以下引入到所述HSC中:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割所述靶基因座中的所述第一原间隔子,并且其中所述第一原间隔子与所述gRNA间隔子完全匹配;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,其中所述第二原间隔子是与所述gRNA间隔子不完全匹配的DAP,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。
在一些实施例中,本文中提供了一种用于将外源核酸整合到HSC中的靶基因座中的方法,其中所述HSC基因组包括所述靶基因座中的第一原间隔子:所述方法包括将以下引入到所述HSC中:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割所述靶基因座中的所述第一原间隔子,并且其中所述第一原间隔子是与所述gRNA间隔子不完全匹配的DAP;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,其中所述第二原间隔子与所述gRNA间隔子完全匹配,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。
一方面,本文中提供了一种用于在静止T细胞中的靶基因座处进行基因组修饰的方法,所述方法包括:(a)将核酸酶或对所述核酸酶进行编码的核酸引入到所述静止T细胞中,其中所述靶基因座包括所述核酸酶的第一识别序列;(b)将双链供体核酸引入到所述静止T细胞中,其中所述双链核酸包括外源核酸序列并且被配置成通过NHEJ插入到所述靶基因座中。在一些实施例中,所述静止T细胞是未经活化的T细胞。
在一些实施例中,本文中提供了一种用于将外源核酸整合到静止T细胞中的靶基因座中的方法,其中所述静止T细胞基因组包括所述靶基因座中的第一原间隔子:所述方法包括将以下引入到所述静止T细胞中:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割所述靶基因座中的所述第一原间隔子;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在一侧或两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述第一原间隔子和所述第二原间隔子与所述gRNA间隔子完全匹配。在一些实施例中,所述靶基因座中的所述第一原间隔子与所述gRNA间隔子完全匹配,并且所述供体核酸中的所述第二原间隔子是与所述gRNA间隔子不完全匹配的DAP。在一些实施例中,所述靶基因座中的所述第一原间隔子是与所述gRNA间隔子不完全匹配的DAP,并且所述供体核酸中的所述第二原间隔子与所述gRNA间隔子完全匹配。在一些实施例中,所述供体核酸包括所述第二原间隔子侧接在两侧上的所述外源核酸。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。在一些实施例中,所述方法包括将包括所述RGEN和所述gRNA的RNP引入到所述静止T细胞中。在一些实施例中,所述方法包括将对所述RGEN进行编码的核酸引入到所述静止T细胞中。在一些实施例中,对所述RGEN进行编码的所述核酸是mRNA或质粒。在一些实施例中,所述RGEN是Cas9。
在一些实施例中,本文中提供了一种用于将外源核酸整合到静止T细胞中的靶基因座中的方法,其中所述静止T细胞基因组包括所述靶基因座中的第一原间隔子:所述方法包括将以下引入到所述静止T细胞中:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割所述靶基因座中的所述第一原间隔子,并且其中所述第一原间隔子与所述gRNA间隔子完全匹配;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,其中所述第二原间隔子是与所述gRNA间隔子不完全匹配的DAP,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。
在一些实施例中,本文中提供了一种用于将外源核酸整合到静止T细胞中的靶基因座中的方法,其中所述静止T细胞基因组包括所述靶基因座中的第一原间隔子:所述方法包括将以下引入到所述静止T细胞中:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割所述靶基因座中的所述第一原间隔子,并且其中所述第一原间隔子是与所述gRNA间隔子不完全匹配的DAP;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,其中所述第二原间隔子与所述gRNA间隔子完全匹配,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。
一方面,本文中提供了一种用于在HDR缺陷细胞中的靶基因座处进行基因组修饰的方法,所述方法包括:(a)将核酸酶或对所述核酸酶进行编码的核酸引入到所述HDR缺陷细胞中,其中所述靶基因座包括所述核酸酶的第一识别序列;(b)将双链供体核酸引入到所述HDR缺陷细胞中,其中所述双链核酸包括外源核酸序列并且被配置成通过NHEJ插入到所述靶基因座中。在一些实施例中,所述方法进一步包括培养所述HDR缺陷细胞持续足以将所述双链供体核酸整合到所述靶基因座中的时间,其中步骤被执行使得所述双链供体核酸的插入效率为至少约4%(如至少约5%、6%、7%、8%、9%、10%或更多中的任何一个)。在一些实施例中,所述HDR缺陷细胞是不分裂的、不复制的并且因此不会表达HDR的机制的任何细胞类型。
在一些实施例中,本文中提供了一种用于将外源核酸整合到HDR缺陷细胞中的靶基因座中的方法,其中所述HDR缺陷细胞基因组包括所述靶基因座中的第一原间隔子:所述方法包括将以下引入到所述HDR缺陷细胞中:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割所述靶基因座中的所述第一原间隔子;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在一侧或两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述第一原间隔子和所述第二原间隔子与所述gRNA间隔子完全匹配。在一些实施例中,所述靶基因座中的所述第一原间隔子与所述gRNA间隔子完全匹配,并且所述供体核酸中的所述第二原间隔子是与所述gRNA间隔子不完全匹配的DAP。在一些实施例中,所述靶基因座中的所述第一原间隔子是与所述gRNA间隔子不完全匹配的DAP,并且所述供体核酸中的所述第二原间隔子与所述gRNA间隔子完全匹配。在一些实施例中,所述供体核酸包括所述第二原间隔子侧接在两侧上的所述外源核酸。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。在一些实施例中,所述方法包括将包括所述RGEN和所述gRNA的RNP引入到所述HDR缺陷细胞中。在一些实施例中,所述方法包括将对所述RGEN进行编码的核酸引入到所述HDR缺陷细胞中。在一些实施例中,对所述RGEN进行编码的所述核酸是mRNA或质粒。在一些实施例中,所述RGEN是Cas9。
在一些实施例中,本文中提供了一种用于将外源核酸整合到HDR缺陷细胞中的靶基因座中的方法,其中所述HDR缺陷细胞基因组包括所述靶基因座中的第一原间隔子:所述方法包括将以下引入到所述HDR缺陷细胞中:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割所述靶基因座中的所述第一原间隔子,并且其中所述第一原间隔子与所述gRNA间隔子完全匹配;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,其中所述第二原间隔子是与所述gRNA间隔子不完全匹配的DAP,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。
在一些实施例中,本文中提供了一种用于将外源核酸整合到HDR缺陷细胞中的靶基因座中的方法,其中所述HDR缺陷细胞基因组包括所述靶基因座中的第一原间隔子:所述方法包括将以下引入到所述HDR缺陷细胞中:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割所述靶基因座中的所述第一原间隔子,并且其中所述第一原间隔子是与所述gRNA间隔子不完全匹配的DAP;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,其中所述第二原间隔子与所述gRNA间隔子完全匹配,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。
一些方面,本文中提供了一种工程化细胞,如工程化哺乳动物细胞(例如,HSC、T细胞),其包括整合在靶染色体基因座处的外源核酸序列,其中所述外源核酸序列已经通过NHEJ整合在所述靶基因座处。在一些实施例中,所述工程化细胞通过本文中所描述的基因组编辑的方法中的任何方法产生。术语“工程化细胞”不仅是指特定受试者细胞,而且还指此种细胞的后代或潜在后代。因为某些修饰可能由于突变或环境影响而在后续世代中发生,所以此类后代实际上可能不与亲本细胞相同,但仍包含在如本文中所使用的术语的范围内。
在一些实施例中,本文中提供了一种工程化细胞(例如,HSC(如LT-HSC)或T细胞(如静止T细胞)),其包括(a)包括核酸酶的第一识别序列的靶基因座;(b)所述核酸酶或对所述核酸酶进行编码的核酸;以及(c)包括外源核酸序列的双链供体核酸,其中所述双链供体核酸被配置成通过同源非依赖性机制(例如,NHEJ)插入到所述靶基因座中。
在一些实施例中,本文中提供了一种工程化细胞(例如,HSC(如LT-HSC)或T细胞(如静止T细胞)),其通过根据本文中所描述的实施例中的任何实施例的用于在细胞中的靶基因座处进行基因组修饰的方法来制备。在一些实施例中,所述方法包括:(a)将核酸酶或对所述核酸酶进行编码的核酸引入到输入细胞中,其中所述靶基因座包括所述核酸酶的第一识别序列;以及(b)将双链供体核酸引入到所述输入细胞中,其中所述双链核酸包括外源核酸序列并且被配置成通过同源非依赖性机制(例如,NHEJ)插入到所述靶基因座中。
在一些实施例中,根据本文中所描述的工程化细胞中的任何工程化细胞,所述细胞缺乏同源性定向修复(HDR)所必需的机制。在一些实施例中,所述细胞是造血干细胞(HSC),如长期移植造血干细胞(LT-HSC)。在一些实施例中,所述细胞是SCID重新填充细胞。在一些实施例中,所述细胞的特征在于以下标志物中的一个或多个(如2个、3个、4个或5个中的任何一个)标志物:Lin
在一些实施例中,根据本文中所描述的包括双链供体核酸的工程化细胞中的任何工程化细胞,所述双链供体核酸进一步包括侧接所述外源核酸序列的第一末端的所述核酸酶的第二识别序列。在一些实施例中,所述双链供体核酸进一步包括侧接所述外源核酸序列的第二末端的第三识别序列。在一些实施例中,所述双链供体核酸被配置成使得经切割的双链供体核酸以期望的朝向插入到所述靶基因座中不会在经修饰的靶基因座中产生所述核酸酶的识别序列,并且所述经切割的双链供体核酸以其它朝向插入到所述靶基因座中在所述经修饰的靶基因座中产生所述核酸酶的识别序列。
在一些实施例中,根据本文中所描述的包括双链供体核酸的工程化细胞中的任何工程化细胞,所述双链供体核酸是双链病毒基因组。在一些实施例中,所述双链病毒基因组是腺病毒基因组、慢病毒基因组(例如,慢病毒RNA基因组的dsDNA中间体)或腺相关病毒(AAV)基因组。在一些实施例中,所述AAV基因组是自身互补AAV(scAAV)基因组。在一些实施例中,所述scAAV基因组是scAAV6基因组。在一些实施例中,所述慢病毒基因组是整合酶缺陷型慢病毒基因组。
在一些实施例中,根据本文中所描述的包括核酸酶或对所述核酸酶进行编码的核酸的工程化细胞中的任何工程化细胞,所述核酸酶是RNA引导的核酸内切酶(RGEN)。在一些实施例中,所述RGEN是Cas9核酸酶。在一些实施例中,所述工程化细胞进一步包括能够引导所述RGEN切割所述靶基因座中的所述第一识别序列的gRNA。在一些实施例中,所述gRNA能够引导所述RGEN切割所述供体核酸中的一个或多个识别序列。在一些实施例中,所述工程化细胞包括包括所述RGEN和所述gRNA的核糖核蛋白(RNP)。在一些实施例中,所述工程化细胞包括对所述RGEN进行编码的核酸。在一些实施例中,对所述RGEN进行编码的所述核酸是mRNA或质粒。
在一些实施例中,根据本文中所描述的包括RGEN或对所述RGEN进行编码的核酸的工程化细胞中的任何工程化细胞,所述靶基因座和所述双链供体核酸中的所述核酸酶的所述识别序列中的每个识别序列是原间隔子序列。在一些实施例中,所述工程化细胞进一步包括靶向所述原间隔子序列中的一个或多个原间隔子序列的一个或多个gRNA。在一些实施例中,所述靶基因座和所述双链供体核酸中的所述原间隔子中的每个原间隔子是相同的,并且所述工程化细胞包括靶向所述原间隔子序列的一个gRNA。
在一些实施例中,本文中所描述的工程化细胞包括:i)第一核酸,所述第一核酸包括第一原间隔子;以及ii)gRNA,所述gRNA包括间隔子,其中所述第一原间隔子是与所述间隔子不完全匹配的DAP,并且其中所述第一原间隔子与所述间隔子匹配的程度足以允许在所述第一原间隔子处对所述第一核酸进行修饰。在一些实施例中,所述DAP的长度比所述间隔子短至少约1个(如至少约2个、3个或更多个中的任何一个)核苷酸。在一些实施例中,所述DAP包括与所述间隔子的至少约1个(如至少约2个、3个或更多个中的任何一个)核苷酸错配。在一些实施例中,所述工程化细胞进一步包括包括第二原间隔子的第二核酸,其中所述第二原间隔子与所述间隔子完全匹配。
在一些实施例中,根据本文中所描述的工程化细胞中的任何工程化细胞,所述工程化细胞包括:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割外源核酸要插入其中的所述工程化细胞中的靶基因座中的第一原间隔子;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在一侧或两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述第一原间隔子和所述第二原间隔子与所述gRNA间隔子完全匹配。在一些实施例中,所述靶基因座中的所述第一原间隔子与所述gRNA间隔子完全匹配,并且所述供体核酸中的所述第二原间隔子是与所述gRNA间隔子不完全匹配的DAP。在一些实施例中,所述靶基因座中的所述第一原间隔子是与所述gRNA间隔子不完全匹配的DAP,并且所述供体核酸中的所述第二原间隔子与所述gRNA间隔子完全匹配。在一些实施例中,所述供体核酸包括所述第二原间隔子侧接在两侧上的所述外源核酸。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。在一些实施例中,所述工程化细胞缺乏同源性定向修复(HDR)所必需的机制。在一些实施例中,所述工程化细胞是HSC,如LT-HSC。在一些实施例中,所述工程化细胞是SCID重现填充细胞。在一些实施例中,所述工程化细胞的特征在于以下标志物中的一个或多个(如2个、3个、4个或5个中的任何一个)标志物:Lin
在一些实施例中,根据本文中所描述的工程化细胞中的任何工程化细胞,所述工程化细胞包括:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割外源核酸要插入其中的所述工程化细胞中的靶基因座中的第一原间隔子,并且其中所述第一原间隔子与所述gRNA间隔子完全匹配;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,其中所述第二原间隔子是与所述gRNA间隔子不完全匹配的DAP,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。
在一些实施例中,根据本文中所描述的工程化细胞中的任何工程化细胞,所述工程化细胞包括:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割外源核酸要插入其中的所述工程化细胞中的靶基因座中的第一原间隔子,并且其中所述第一原间隔子是与所述gRNA间隔子不完全匹配的DAP;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,其中所述第二原间隔子与所述gRNA间隔子完全匹配,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。
在一些实施例中,所述工程化细胞是HSC,包含LT-HSC和短期移植HSC(ST-HSC)两者,如是CD34
可以根据已知技术收集HSC,并通过已知技术富集或贫化,如与抗体的亲和力结合,如流式细胞术和/或免疫抗原选择。在一些实施例中,所述HSC是从患者获得的自体HSC。
在一些实施例中,所述工程化细胞是T细胞或能够分化成T细胞的前体细胞。在一些实施例中,所述工程化细胞是CD3
可以根据已知技术收集淋巴细胞(T淋巴细胞),并通过已知技术富集或贫化,如与抗体的亲和力结合,如流式细胞术和/或免疫抗原选择。在一些实施例中,所述T细胞是从患者获得的自体T细胞。
在一些实施例中,本公开进一步提供了包括如本文中所描述的工程化细胞的组合物。
在一些实施例中,本文中提供了一种将包括插入在靶基因座处的外源核酸序列的经编辑的HSC移植在个体中的方法,所述方法包括向所述个体施用根据本文中所描述的实施例中的任何实施例的经编辑的HSC的群体。在一些实施例中,所述经编辑的HSC在所述个体中存在至少约1周、2周、3周、4周、5周、6周、7周、8周、9周、10周、11周、12周、13周、14周、15周、16周或更多周中的任何一个。在一些实施例中,所述经编辑的HSC的群体根据本文中所描述的方法中的任何方法制备。在一些实施例中,所述个体中的经编辑的HSC的移植量等于或大于使用同源依赖性机制制备的对应的经编辑的HSC的移植量。在一些实施例中,所述经编辑的HSC的群体含有在源自从所述个体获得的HSC的输入群体的HSC的输出群体中。在一些实施例中,从所述个体获得的所述HSC的输入群体包括HSC的混合群体,所述HSC的混合群体包括LT-HSC和ST-HSC,并且移植的所述经编辑的HSC的群体包括经编辑的LT-HSC。在一些实施例中,所述方法包括向所述个体施用所述HSC的输出群体。
在一些实施例中,根据本文中所描述的将包括插入在靶基因座处的外源核酸序列的经编辑的HSC移植在个体中的方法中的任何方法,所述经编辑的HSC通过包括以下的方法制备:(a)将核酸酶或对所述核酸酶进行编码的核酸引入到所述HSC中,其中所述靶基因座包括所述核酸酶的第一识别序列;以及(b)将双链供体核酸引入到所述HSC中,其中所述双链核酸包括外源核酸序列并且被配置成通过NHEJ插入到所述靶基因座中。在一些实施例中,所述HSC是长期移植造血干细胞(LT-HSC)。在一些实施例中,所述HSC是SCID重新填充细胞。在一些实施例中,所述HSC的特征在于以下标志物中的一个或多个(如2个、3个、4个或5个中的任何一个)标志物:Lin
在一些实施例中,根据本文中所描述的将包括插入在靶基因座处的外源核酸序列的经编辑的HSC移植在个体中的方法中的任何方法,所述双链供体核酸进一步包括侧接所述外源核酸序列的第一末端的所述核酸酶的第二识别序列。在一些实施例中,所述双链供体核酸进一步包括侧接所述外源核酸序列的第二末端的第三识别序列。在一些实施例中,所述双链供体核酸在引入到所述细胞中之后在所述第二识别序列和/或所述第三识别序列处被切割。在一些实施例中,所述双链供体核酸被配置成使得经切割的双链供体核酸以期望的朝向插入到所述靶基因座中不会在经修饰的靶基因座中产生所述核酸酶的识别序列,并且所述经切割的双链供体核酸以其它朝向插入到所述靶基因座中在所述经修饰的靶基因座中产生所述核酸酶的识别序列。
在一些实施例中,根据本文中所描述的将包括插入在靶基因座处的外源核酸序列的经编辑的HSC移植在个体中的方法中的任何方法,所述双链供体核酸是双链病毒基因组。在一些实施例中,所述双链病毒基因组是腺病毒基因组、慢病毒基因组(例如,慢病毒RNA基因组的dsDNA中间体)或腺相关病毒(AAV)基因组。在一些实施例中,所述AAV基因组是自身互补AAV(scAAV)基因组。在一些实施例中,所述scAAV基因组是scAAV6基因组。在一些实施例中,所述慢病毒基因组是整合酶缺陷型慢病毒基因组。
在一些实施例中,根据本文中所描述的将包括插入在靶基因座处的外源核酸序列的经编辑的HSC移植在个体中的方法中的任何方法,所述核酸酶是RNA引导的核酸内切酶(RGEN)。在一些实施例中,所述RGEN是Cas9核酸酶。在一些实施例中,制备所述经编辑的HSC的所述方法进一步包括将能够引导所述RGEN切割所述靶基因座中的所述第一识别序列的gRNA引入到所述HSC中。在一些实施例中,所述gRNA能够引导所述RGEN切割所述供体核酸中的一个或多个识别序列。在一些实施例中,制备所述经编辑的HSC的所述方法包括将包括所述RGEN和所述gRNA的核糖核蛋白(RNP)引入到所述HSC中。在一些实施例中,制备所述经编辑的HSC的所述方法包括将对所述RGEN进行编码的核酸引入到所述HSC中。在一些实施例中,对所述RGEN进行编码的所述核酸是mRNA或质粒。
在一些实施例中,根据本文中所描述的将包括插入在靶基因座处的外源核酸序列的经编辑的HSC移植在个体中的方法中的任何方法,所述靶基因座和所述双链供体核酸中的所述核酸酶的所述识别序列中的每个识别序列是原间隔子序列。在一些实施例中,制备所述经编辑的HSC的所述方法进一步包括将靶向所述原间隔子序列中的一个或多个原间隔子序列的一个或多个gRNA引入到所述HSC中。在一些实施例中,所述靶基因座和所述双链供体核酸中的所述原间隔子中的每个原间隔子是相同的,并且所述方法包括将靶向所述原间隔子序列的一个gRNA引入到所述细胞中。
在一些实施例中,根据本文中所描述的制备在将经编辑的HSC移植在个体中的方法中使用的包括插入在靶基因座处的外源核酸序列的所述经编辑的HSC的方法中的任何方法,所述HSC基因组包括所述靶基因座中的第一原间隔子,并且所述方法包括将以下引入到所述HSC中:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割所述靶基因座中的所述第一原间隔子;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在一侧或两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述第一原间隔子和所述第二原间隔子与所述gRNA间隔子完全匹配。在一些实施例中,所述靶基因座中的所述第一原间隔子与所述gRNA间隔子完全匹配,并且所述供体核酸中的所述第二原间隔子是与所述gRNA间隔子不完全匹配的DAP。在一些实施例中,所述靶基因座中的所述第一原间隔子是与所述gRNA间隔子不完全匹配的DAP,并且所述供体核酸中的所述第二原间隔子与所述gRNA间隔子完全匹配。在一些实施例中,所述DAP的长度比所述gRNA间隔子短至少约1个(如至少约2个、3个或更多个中的任何一个)核苷酸。在一些实施例中,所述DAP包括与所述gRNA间隔子的至少约1个(如至少约2个、3个或更多个中的任何一个)核苷酸错配。在一些实施例中,所述供体核酸包括所述第二原间隔子侧接在两侧上的所述外源核酸。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。在一些实施例中,所述方法包括将包括所述RGEN和所述gRNA的RNP引入到所述HSC中。在一些实施例中,所述方法包括将对所述RGEN进行编码的核酸引入到所述HSC中。在一些实施例中,对所述RGEN进行编码的所述核酸是mRNA或质粒。在一些实施例中,所述RGEN是Cas9。
在一些实施例中,根据本文中所描述的制备在将经编辑的HSC移植在个体中的方法中使用的包括插入在靶基因座处的外源核酸序列的所述经编辑的HSC的方法中的任何方法,所述HSC基因组包括所述靶基因座中的第一原间隔子,并且所述方法包括将以下引入到所述HSC中:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割所述靶基因座中的所述第一原间隔子,并且其中所述第一原间隔子与所述gRNA间隔子完全匹配;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,其中所述第二原间隔子是与所述gRNA间隔子不完全匹配的DAP,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。
在一些实施例中,根据本文中所描述的制备在将经编辑的HSC移植在个体中的方法中使用的包括插入在靶基因座处的外源核酸序列的所述经编辑的HSC的方法中的任何方法,所述HSC基因组包括所述靶基因座中的第一原间隔子,并且所述方法包括将以下引入到所述HSC中:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割所述靶基因座中的所述第一原间隔子,并且其中所述第一原间隔子是与所述gRNA间隔子不完全匹配的DAP;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,其中所述第二原间隔子与所述gRNA间隔子完全匹配,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。
在一些实施例中,根据本文中所描述的制备在将经编辑的HSC移植在个体中的方法中使用的包括插入在靶基因座处的外源核酸序列的所述经编辑的HSC的方法中的任何方法,所述核酸酶或对所述核酸酶进行编码的核酸在所述供体核酸被引入到所述HSC中之前被引入到所述HSC中。在一些实施例中,所述核酸酶或对所述核酸酶进行编码的核酸在所述供体核酸被引入到所述HSC中之前不超过1小时被引入到所述HSC中。在一些实施例中,所述核酸酶或对所述核酸酶进行编码的核酸在所述供体核酸被引入到所述HSC中之前不超过5分钟被引入到所述HSC中。在一些实施例中,将所述核酸酶或对所述核酸酶进行编码的核酸引入到所述HSC中包括将包括RGEN和gRNA的RNP引入到所述HSC中。在一些实施例中,所述供体核酸是双链病毒基因组,例如scAAV基因组。
在一些实施例中,根据本文中所描述的制备在将经编辑的HSC移植在个体中的方法中使用的包括插入在靶基因座处的外源核酸序列的所述经编辑的HSC的方法中的任何方法,所述方法包括在所述供体核酸被引入到所述HSC中之前将包括RGEN和gRNA的RNP引入到所述HSC中。在一些实施例中,所述RNP在所述供体核酸被引入到所述HSC中之前不超过1小时被引入到所述HSC中。在一些实施例中,所述RNP在所述供体核酸被引入到所述HSC中之前不超过5分钟被引入到所述HSC中。在一些实施例中,所述供体核酸是双链病毒基因组,例如scAAV基因组。
在一些实施例中,根据本文中所描述的制备在将经编辑的HSC移植在个体中的方法中使用的包括插入在靶基因座处的外源核酸序列的所述经编辑的HSC的方法中的任何方法,所述HSC在缺氧条件下进行培养。
在一些实施例中,根据本文中所描述的制备在将经编辑的HSC移植在个体中的方法中使用的包括插入在靶基因座处的外源核酸序列的所述经编辑的HSC的方法中的任何方法,所述HSC在将所述核酸酶或对所述核酸酶进行编码的核酸和所述供体核酸引入到所述HSC前不超过约48小时进行培养。在一些实施例中,所述HSC在将所述核酸酶或对所述核酸酶进行编码的核酸和所述供体核酸引入到所述HSC前不超过约24小时进行培养。在一些实施例中,所述HSC在将所述核酸酶或对所述核酸酶进行编码的核酸和所述供体核酸引入到所述HSC前不超过约2小时进行培养。在一些实施例中,将所述核酸酶或对所述核酸酶进行编码的核酸引入到所述HSC中包括将包括RGEN和gRNA的RNP引入到所述HSC中。在一些实施例中,所述供体核酸是双链病毒基因组,例如scAAV基因组。
在一些实施例中,根据本文中所描述的制备在将经编辑的HSC移植在个体中的方法中使用的包括插入在靶基因座处的外源核酸序列的所述经编辑的HSC的方法中的任何方法,所述HSC在存在Notch配体的情况下进行培养。在一些实施例中,所述Notch配体是δ样Notch配体(DLL)、锯齿状1、锯齿状2或其缀合物。在一些实施例中,所述δ样Notch配体是DLL1、DLL3或DLL4。在一些实施例中,所述Notch配体是Fc-DLL1、Fc-DLL3、Fc-DLL4、Fc-锯齿状1或Fc-锯齿状2。
在一些实施例,本文中提供了一种治疗有需要的受试者的疾病或病状的方法,其中所述疾病或病状的特征在于功能性蛋白质的缺陷表达,所述方法包括向所述受试者施用根据本文中所描述的方法中的任何方法进行编辑以表达的所述蛋白质的功能性形式的细胞。
在一些实施例中,所述疾病是重症综合性免疫缺陷(SCID),并且所述方法包括向所述受试者施用根据本文中所描述的方法中的任何方法进行编辑以表达在所述受试者中突变的蛋白质的功能性形式的HSC的群体。在一些实施例中,对所述HSC进行编辑以表达涉及淋巴发育的蛋白质,例如IL2Rg、RAG1或IL7R。在一些实施例中,对所述HSC进行编辑以表达涉及淋巴细胞增殖和/或代谢的蛋白质,例如ADA或PNP。在一些实施例中,所述疾病或病状是高雪氏病、法布里病、黏多糖贮积症I-IX型或肾上腺脑白质营养不良。
在一些实施例中,根据治疗有需要的受试者的疾病或病状的方法中的任何方法,所述经编辑的细胞通过包括以下的方法制备:(a)将核酸酶或对所述核酸酶进行编码的核酸引入到所述细胞中,其中所述靶基因座包括所述核酸酶的第一识别序列;以及(b)将双链供体核酸引入到所述细胞中,其中所述双链核酸包括外源核酸序列并且被配置成通过NHEJ插入到所述靶基因座中。在一些实施例中,所述细胞缺乏同源性定向修复(HDR)所必需的机制。在一些实施例中,所述细胞是造血干细胞(HSC),如长期移植造血干细胞(LT-HSC)。在一些实施例中,所述细胞是SCID重新填充细胞。在一些实施例中,所述细胞的特征在于以下标志物中的一个或多个(如2个、3个、4个或5个中的任何一个)标志物:Lin
在一些实施例中,根据治疗有需要的受试者的疾病或病状的方法中的任何方法,所述双链供体核酸进一步包括侧接所述外源核酸序列的第一末端的所述核酸酶的第二识别序列。在一些实施例中,所述双链供体核酸进一步包括侧接所述外源核酸序列的第二末端的第三识别序列。在一些实施例中,所述双链供体核酸在引入到所述细胞中之后在所述第二识别序列和/或所述第三识别序列处被切割。在一些实施例中,所述双链供体核酸被配置成使得经切割的双链供体核酸以期望的朝向插入到所述靶基因座中不会在经修饰的靶基因座中产生所述核酸酶的识别序列,并且所述经切割的双链供体核酸以其它朝向插入到所述靶基因座中在所述经修饰的靶基因座中产生所述核酸酶的识别序列。
在一些实施例中,根据治疗有需要的受试者的疾病或病状的方法中的任何方法,所述双链供体核酸是双链病毒基因组。在一些实施例中,所述双链病毒基因组是腺病毒基因组、慢病毒基因组(例如,慢病毒RNA基因组的dsDNA中间体)或腺相关病毒(AAV)基因组。在一些实施例中,所述AAV基因组是自身互补AAV(scAAV)基因组。在一些实施例中,所述scAAV基因组是scAAV6基因组。在一些实施例中,所述慢病毒基因组是整合酶缺陷型慢病毒基因组。
在一些实施例中,根据治疗有需要的受试者的疾病或病状的方法中的任何方法,所述核酸酶是RNA引导的核酸内切酶(RGEN)。在一些实施例中,所述RGEN是Cas9核酸酶。在一些实施例中,制备所述经编辑的细胞的所述方法进一步包括将能够引导所述RGEN切割所述靶基因座中的所述第一识别序列的gRNA引入到所述细胞中。在一些实施例中,所述gRNA能够引导所述RGEN切割所述供体核酸中的一个或多个识别序列。在一些实施例中,制备所述经编辑的细胞的所述方法包括将包括所述RGEN和所述gRNA的核糖核蛋白(RNP)引入到所述细胞中。在一些实施例中,制备所述经编辑的细胞的所述方法包括将对所述RGEN进行编码的核酸引入到所述细胞中。在一些实施例中,对所述RGEN进行编码的所述核酸是mRNA或质粒。
在一些实施例中,根据治疗有需要的受试者的疾病或病状的方法中的任何方法,所述靶基因座和所述双链供体核酸中的所述核酸酶的所述识别序列中的每个识别序列是原间隔子序列。在一些实施例中,制备所述经编辑的细胞的所述方法进一步包括将靶向所述原间隔子序列中的一个或多个原间隔子序列的一个或多个gRNA引入到所述细胞中。在一些实施例中,所述靶基因座和所述双链供体核酸中的所述原间隔子中的每个原间隔子是相同的,并且所述方法包括将靶向所述原间隔子序列的一个gRNA引入到所述细胞中。
在一些实施例中,根据本文中所描述的制备在治疗有需要的受试者的疾病或病状的方法中使用的包括插入在靶基因座处的外源核酸序列的经编辑的细胞的方法中的任何方法,所述细胞基因组包括所述靶基因座中的第一原间隔子,并且所述方法包括将以下引入到所述细胞中:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割所述靶基因座中的所述第一原间隔子;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在一侧或两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述第一原间隔子和所述第二原间隔子与所述gRNA间隔子完全匹配。在一些实施例中,所述靶基因座中的所述第一原间隔子与所述gRNA间隔子完全匹配,并且所述供体核酸中的所述第二原间隔子是与所述gRNA间隔子不完全匹配的DAP。在一些实施例中,所述靶基因座中的所述第一原间隔子是与所述gRNA间隔子不完全匹配的DAP,并且所述供体核酸中的所述第二原间隔子与所述gRNA间隔子完全匹配。在一些实施例中,所述DAP的长度比所述gRNA间隔子短至少约1个(如至少约2个、3个或更多个中的任何一个)核苷酸。在一些实施例中,所述DAP包括与所述gRNA间隔子的至少约1个(如至少约2个、3个或更多个中的任何一个)核苷酸错配。在一些实施例中,所述供体核酸包括所述第二原间隔子侧接在两侧上的所述外源核酸。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。在一些实施例中,所述方法包括将包括所述RGEN和所述gRNA的RNP引入到所述细胞中。在一些实施例中,所述方法包括将对所述RGEN进行编码的核酸引入到所述细胞中。在一些实施例中,对所述RGEN进行编码的所述核酸是mRNA或质粒。在一些实施例中,所述RGEN是Cas9。
在一些实施例中,根据本文中所描述的制备在治疗有需要的受试者的疾病或病状的方法中使用的包括插入在靶基因座处的外源核酸序列的经编辑的细胞的方法中的任何方法,所述细胞基因组包括所述靶基因座中的第一原间隔子,并且所述方法包括将以下引入到所述细胞中:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割所述靶基因座中的所述第一原间隔子,并且其中所述第一原间隔子与所述gRNA间隔子完全匹配;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,其中所述第二原间隔子是与所述gRNA间隔子不完全匹配的DAP,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。
在一些实施例中,根据本文中所描述的制备在治疗有需要的受试者的疾病或病状的方法中使用的包括插入在靶基因座处的外源核酸序列的经编辑的细胞的方法中的任何方法,所述细胞基因组包括所述靶基因座中的第一原间隔子,并且所述方法包括将以下引入到所述细胞中:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割所述靶基因座中的所述第一原间隔子,并且其中所述第一原间隔子是与所述gRNA间隔子不完全匹配的DAP;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,其中所述第二原间隔子与所述gRNA间隔子完全匹配,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。
在一些实施例中,根据本文中所描述的制备在治疗有需要的受试者的疾病或病状的方法中使用的包括插入在靶基因座处的外源核酸序列的经编辑的细胞的方法中的任何方法,所述核酸酶或对所述核酸酶进行编码的核酸在所述供体核酸被引入到所述细胞中之前被引入到所述细胞中。在一些实施例中,所述核酸酶或对所述核酸酶进行编码的核酸在所述供体核酸被引入到所述细胞中之前不超过1小时被引入到所述细胞中。在一些实施例中,所述核酸酶或对所述核酸酶进行编码的核酸在所述供体核酸被引入到所述细胞中之前不超过5分钟被引入到所述细胞中。在一些实施例中,将所述核酸酶或对所述核酸酶进行编码的核酸引入到所述细胞中包括将包括RGEN和gRNA的RNP引入到所述细胞中。在一些实施例中,所述供体核酸是双链病毒基因组,例如scAAV基因组。
在一些实施例中,根据本文中所描述的制备在治疗有需要的受试者的疾病或病状的方法中使用的包括插入在靶基因座处的外源核酸序列的经编辑的细胞的方法中的任何方法,所述方法包括在所述供体核酸被引入到所述细胞中之前将包括RGEN和gRNA的RNP引入到所述细胞中。在一些实施例中,所述RNP在所述供体核酸被引入到所述细胞中之前不超过1小时被引入到所述细胞中。在一些实施例中,所述RNP在所述供体核酸被引入到所述细胞中之前不超过5分钟被引入到所述细胞中。在一些实施例中,所述供体核酸是双链病毒基因组,例如scAAV基因组。
在一些实施例中,根据本文中所描述的制备在治疗有需要的受试者的疾病或病状的方法中使用的包括插入在靶基因座处的外源核酸序列的经编辑的细胞的方法中的任何方法,所述细胞在缺氧条件下进行培养。
在一些实施例中,根据本文中所描述的制备在治疗有需要的受试者的疾病或病状的方法中使用的包括插入在靶基因座处的外源核酸序列的经编辑的细胞的方法中的任何方法,所述细胞在将所述核酸酶或对所述核酸酶进行编码的核酸和所述供体核酸引入到所述细胞前不超过约48小时进行培养。在一些实施例中,所述细胞在将所述核酸酶或对所述核酸酶进行编码的核酸和所述供体核酸引入到所述细胞前不超过约24小时进行培养。在一些实施例中,所述细胞在将所述核酸酶或对所述核酸酶进行编码的核酸和所述供体核酸引入到所述细胞前不超过约2小时进行培养。在一些实施例中,将所述核酸酶或对所述核酸酶进行编码的核酸引入到所述细胞中包括将包括RGEN和gRNA的RNP引入到所述细胞中。在一些实施例中,所述供体核酸是双链病毒基因组,例如scAAV基因组。
在一些实施例中,根据本文中所描述的制备在治疗有需要的受试者的疾病或病状的方法中使用的包括插入在靶基因座处的外源核酸序列的经编辑的细胞的方法中的任何方法,所述细胞在存在Notch配体的情况下进行培养。在一些实施例中,所述Notch配体是δ样Notch配体(DLL)、锯齿状1、锯齿状2或其缀合物。在一些实施例中,所述δ样Notch配体是DLL1、DLL3或DLL4。在一些实施例中,所述Notch配体是Fc-DLL1、Fc-DLL3、Fc-DLL4、Fc-锯齿状1或Fc-锯齿状2。
本文中提供了包括本公开中所阐述的用于产生工程化细胞的系统的一个或多个元件的组合物。
在一些实施例中,本文中提供了一种组合物,其包括以下中的一个或多个:(a)核酸酶或对所述核酸酶进行编码的核酸,其中所述核酸酶能够在包括所述核酸酶的第一识别序列的靶基因座处进行介导性基因组编辑;以及(b)双链供体核酸,其中所述双链供体核酸包括外源核酸序列并且被配置成通过NHEJ插入到所述靶基因座中。在一些实施例中,所述组合物进一步包括要编辑的细胞。
在一些实施例中,根据本文中所描述的包括双链供体核酸的组合物中的任何组合物,所述双链供体核酸进一步包括侧接所述外源核酸序列的第一末端的所述核酸酶的第二识别序列。在一些实施例中,所述双链供体核酸进一步包括侧接所述外源核酸序列的第二末端的第三识别序列。在一些实施例中,所述双链供体核酸被配置成使得经切割的双链供体核酸以期望的朝向插入到所述靶基因座中不会在经修饰的靶基因座中产生所述核酸酶的识别序列,并且所述经切割的双链供体核酸以其它朝向插入到所述靶基因座中在所述经修饰的靶基因座中产生所述核酸酶的识别序列。
在一些实施例中,根据本文中所描述的包括双链供体核酸的组合物中的任何组合物,所述双链供体核酸是双链病毒基因组。在一些实施例中,所述双链病毒基因组是腺病毒基因组、慢病毒基因组(例如,慢病毒RNA基因组的dsDNA中间体)或腺相关病毒(AAV)基因组。在一些实施例中,所述AAV基因组是自身互补AAV(scAAV)基因组。在一些实施例中,所述scAAV基因组是scAAV6基因组。在一些实施例中,所述慢病毒基因组是整合酶缺陷型慢病毒基因组。
在一些实施例中,根据本文中所描述的包括核酸酶或对所述核酸酶进行编码的核酸的组合物中的任何组合物,所述核酸酶是RNA引导的核酸内切酶(RGEN)。在一些实施例中,所述RGEN是Cas9核酸酶。在一些实施例中,所述组合物进一步包括能够引导所述RGEN切割所述靶基因座中的所述第一识别序列的gRNA。在一些实施例中,所述gRNA能够引导所述RGEN切割所述供体核酸中的一个或多个识别序列。在一些实施例中,所述组合物包括包括所述RGEN和所述gRNA的核糖核蛋白(RNP)。在一些实施例中,所述组合物包括对所述RGEN进行编码的核酸。在一些实施例中,对所述RGEN进行编码的所述核酸是mRNA或质粒。
在一些实施例中,根据本文中所描述的包括RGEN或对所述RGEN进行编码的核酸的组合物中的任何组合物,所述靶基因座和所述双链供体核酸中的所述核酸酶的所述识别序列中的每个识别序列是原间隔子序列。在一些实施例中,所述组合物进一步包括靶向所述原间隔子序列中的一个或多个原间隔子序列的一个或多个gRNA。在一些实施例中,所述靶基因座和所述双链供体核酸中的所述原间隔子中的每个原间隔子是相同的,并且所述组合物包括靶向所述原间隔子序列的一个gRNA。
在一些实施例中,本文中所描述的组合物包括以下中的一个或多个:i)第一核酸,所述第一核酸包括第一原间隔子;以及ii)gRNA,所述gRNA包括间隔子,其中所述第一原间隔子是与所述间隔子不完全匹配的DAP,并且其中所述第一原间隔子与所述间隔子匹配的程度足以允许在所述第一原间隔子处对所述第一核酸进行修饰。在一些实施例中,所述DAP的长度比所述间隔子短至少约1个(如至少约2个、3个或更多个中的任何一个)核苷酸。在一些实施例中,所述DAP包括与所述间隔子的至少约1个(如至少约2个、3个或更多个中的任何一个)核苷酸错配。在一些实施例中,所述组合物进一步包括包括第二原间隔子的第二核酸,其中所述第二原间隔子与所述间隔子完全匹配。
在一些实施例中,根据本文中所描述的组合物中的任何组合物,所述组合物包括以下中的一个或多个:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割外源核酸要插入其中的靶基因座中的第一原间隔子;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在一侧或两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述第一原间隔子和所述第二原间隔子与所述gRNA间隔子完全匹配。在一些实施例中,所述靶基因座中的所述第一原间隔子与所述gRNA间隔子完全匹配,并且所述供体核酸中的所述第二原间隔子是与所述gRNA间隔子不完全匹配的DAP。在一些实施例中,所述靶基因座中的所述第一原间隔子是与所述gRNA间隔子不完全匹配的DAP,并且所述供体核酸中的所述第二原间隔子与所述gRNA间隔子完全匹配。在一些实施例中,所述供体核酸包括所述第二原间隔子侧接在两侧上的所述外源核酸。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。例如,在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。在一些实施例中,所述组合物进一步包括包括所述靶基因座的细胞。在一些实施例中,所述细胞缺乏同源性定向修复(HDR)所必需的机制。在一些实施例中,所述细胞是造血干细胞(HSC),如长期移植造血干细胞(LT-HSC)。在一些实施例中,所述细胞是SCID重新填充细胞。在一些实施例中,所述细胞的特征在于以下标志物中的一个或多个(如2个、3个、4个或5个中的任何一个)标志物:Lin
在一些实施例中,根据本文中所描述的组合物中的任何组合物,所述组合物包括以下中的一个或多个:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割外源核酸要插入其中的靶基因座中的第一原间隔子,并且其中所述第一原间隔子与所述gRNA间隔子完全匹配;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,其中所述第二原间隔子是与所述gRNA间隔子不完全匹配的DAP,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。在一些实施例中,所述组合物进一步包括包括所述靶基因座的细胞。
在一些实施例中,根据本文中所描述的组合物中的任何组合物,所述组合物包括以下中的一个或多个:a)RGEN或对所述RGEN进行编码的核酸;b)gRNA,所述gRNA包括间隔子或对所述gRNA进行编码的核酸,其中所述gRNA能够靶向所述RGEN以切割外源核酸要插入其中的靶基因座中的第一原间隔子,并且其中所述第一原间隔子是与所述gRNA间隔子不完全匹配的DAP;以及c)双链供体核酸,其中所述供体核酸包括第二原间隔子侧接在两侧上的所述外源核酸,其中所述gRNA能够靶向所述RGEN以切割所述供体核酸中的所述第二原间隔子,其中所述第二原间隔子与所述gRNA间隔子完全匹配,并且其中所述供体核酸被配置成使得所述外源核酸能够通过NHEJ插入到所述靶基因座中。在一些实施例中,所述供体核酸被配置成使得:i)所述经切割的供体核酸以期望的朝向插入到所述经切割的靶基因座中不会产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子,并且ii)所述经切割的供体核酸以其它朝向插入到所述经切割的靶基因座中产生侧接能够被由所述gRNA引导的所述RGEN切割的所述外源核酸的原间隔子。在一些实施例中,所述靶基因座中的所述第一原间隔子处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述第二原间隔子处于反向朝向。在一些实施例中,所述组合物进一步包括包括所述靶基因座的细胞。
本文中还提供了包括如本公开中所阐述的制备的经基因修饰的细胞(如哺乳动物细胞)的组合物。
本文中还提供了包含工程化细胞和/或用于产生本文中所提供和所描述的工程化细胞的系统元件的试剂盒和系统。因此,例如,本文中提供了一种试剂盒,其包括以下中的一个或多个:如本文中所描述的蛋白质序列;如本文中所描述的表达载体;和/或如本文中所描述的细胞。
基因组靶向核酸或引导RNA
本公开提供了一种基因组靶向核酸,其可以将相关多肽(例如,定点多肽或DNA核酸内切酶)的活性指导靶核酸内的特异性靶序列。在一些实施例中,基因组靶向核酸是RNA。基因组靶向RNA在本文中被称为“引导RNA”或“gRNA”。引导RNA至少可以具有与所关注的靶核酸序列杂交的间隔子序列以及CRISPR重复序列。在II型系统中,gRNA还具有被称作tracrRNA序列的第二RNA。在II型引导RNA(gRNA)中,CRISPR重复序列和tracrRNA序列彼此杂交以形成双链体。在V型引导RNA(gRNA)中,crRNA形成双链体。在这两种系统中,双链体可以结合定点多肽,使得引导RNA和定点多肽形成复合体。基因组靶向核酸借助于其与定点多肽的相关而提供对复合体的靶特异性。基因组靶向核酸因此指导定点多肽的活性。
在一些实施例中,基因组靶向核酸是双分子引导RNA。在一些实施例中,基因组靶向核酸是单分子引导RNA。双分子引导RNA可以具有两个RNA链。第一链在5′到3′的方向上具有任选的间隔子扩展序列、间隔子序列和最小CRISPR重复序列。第二链具有最小tracrRNA序列(与最小CRISPR重复序列互补)、3′tracrRNA序列和任选的tracrRNA扩展序列。II型系统中的单分子引导RNA(sgRNA)在5′到3′的方向上具有任选的间隔子扩展序列、间隔子序列、最小CRISPR重复序列、单分子引导接头、最小tracrRNA序列、3′tracrRNA序列和任选的tracrRNA扩展序列。任选的tracrRNA扩展可以具有对引导RNA的另外的功能(例如,稳定性)有帮助的元素。单分子引导接头可以将最小CRISPR重复和最小tracrRNA序列连接形成发夹结构。任选的tracrRNA扩展具有一个或多个发夹。V型系统中的单分子引导RNA(sgRNA)在5′到3′的方向上具有最小CRISPR重复序列和间隔子序列。
示例性基因组靶向核酸在WO2018002719中进行了描述。
供体DNA或供体模板
定点多肽(如DNA核酸内切酶)可以在核酸(例如,基因组DNA)中引入双链断裂或单链断裂。双链断裂可以刺激细胞的内源DNA修复途径(例如,同源依赖性机制(HDR)或非同源末端连接(NHEJ)或替代性非同源末端连接(A-NHEJ)或微同源性介导末端连接(MMEJ))。NHEJ可以在不需要同源模板的情况下修复经切割的靶核酸。这有时可能在靶核酸中在切割位点处引起小型缺失和插入(插入缺失)并且可能导致破坏或改变基因表达。
当在发生双链断裂的细胞的细胞核内以足够的浓度提供外源DNA分子时,外源DNA可以在NHEJ修复过程期间插入在双链断裂处并且因此成为基因组的永久添加物。将核酸酶靶位点包含在外源DNA中会极大地刺激其在NHEJ介导的DNA修复期间插入到靶位点中。在一些实施例中,这些外源DNA分子被称为供体模板。如果供体模板任选地含有转基因的编码序列以及相关的调节序列(如启动子、增强子、polyA序列和/或剪接受体序列(在本文中也称为“供体盒”),则转基因可以从基因组中的整合核酸表达,从而产生持续细胞的寿命之久的永久性表达。此外,当细胞分裂时,供体DNA模板的整合核酸可以被传递到子细胞。
在一些实施例中,可以通过各种不同的方法将供体DNA与核酸酶一起供应或者独立供应,例如通过转染、纳米颗粒、微注射、或病毒转导。
在一些实施例中,根据本文中所描述的包括外源核酸序列的供体模板中的任何供体模板,gRNA靶位点侧接在所述外源核酸序列的一侧或两侧上。例如,此种供体模板可以包括具有外源核酸序列的gRNA靶位点5′和/或外源核酸序列的gRNA靶位点3′的外源核酸序列。在一些实施例中,所述供体模板包括具有外源核酸序列的gRNA靶位点5′的外源核酸序列。在一些实施例中,所述供体模板包括具有外源核酸序列的gRNA靶位点3′的外源核酸序列。在一些实施例中,所述供体模板包括具有外源核酸序列的gRNA靶位点5′和外源核酸序列的gRNA靶位点3′的外源核酸序列。在一些实施例中,所述供体模板包括具有外源核酸序列的gRNA靶位点5′和外源核酸序列的gRNA靶位点3′的外源核酸序列,并且所述两个gRNA靶位点包括相同的序列。在一些实施例中,所述供体模板包括至少一个gRNA靶位点,并且所述供体模板中的所述至少一个gRNA靶位点包括与所述供体模板的所述外源核酸序列要整合到其中的靶基因座中的gRNA靶位点相同的序列。在一些实施例中,所述供体模板包括具有外源核酸序列的gRNA靶位点5′和外源核酸序列的gRNA靶位点3′的外源核酸序列,并且所述供体模板中的所述两个gRNA靶位点包括与所述供体模板的所述外源核酸序列要整合到其中的靶基因座中的gRNA靶位点相同的序列。在一些实施例中,所述靶基因座中的所述gRNA靶位点处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述gRNA靶位点处于反向朝向。
在一些实施例中,所述供体模板是双链供体核酸。在一些实施例中,所述双链供体核酸包括外源核酸序列并且被配置成通过NHEJ插入到靶基因座中。在一些实施例中,所述双链供体核酸进一步包括侧接所述外源核酸序列的第一末端的第一核酸酶的第一识别序列。在一些实施例中,所述双链供体核酸包括侧接所述外源核酸序列的第二末端的第二核酸酶的第二识别序列。在一些实施例中,所述第一和第二核酸酶是相同的核酸酶。在一些实施例中,所述第一和第二识别序列是相同的识别序列。在一些实施例中,所述双链供体核酸被配置成使得经切割的双链供体核酸以期望的朝向插入到所述靶基因座中不会在经修饰的靶基因座中产生所述核酸酶的识别序列,并且所述经切割的双链供体核酸以其它朝向插入到所述靶基因座中在所述经修饰的靶基因座中产生所述核酸酶的识别序列。在一些实施例中,所述第一和第二核酸酶是RGEN,并且所述第一和第二识别序列是原间隔子序列。
在一些实施例中,本文中所描述的双链供体核酸包括在一个或两个末端上侧接有原间隔子的外源核酸序列。在一些实施例中,所述外源核酸序列在其5′端上侧接有原间隔子。在一些实施例中,所述外源核酸序列在其3′端上侧接有原间隔子。在一些实施例中,所述外源核酸序列在其5′和3′端上侧接有原间隔子。在一些实施例中,靶基因座中的原间隔子序列处于正向朝向,所述供体核酸中的所述外源核酸处于正向朝向,并且所述供体核酸中的所述原间隔子处于反向朝向。
在一些实施例中,本文中所描述的双链供体核酸包括在一个或两个末端上侧接有与gRNA的间隔子不完全匹配的延迟作用原间隔子(DAP)的外源核酸序列,其中所述DAP与所述间隔子匹配的程度足以允许通过由所述gRNA引导的RGEN在所述DAP处对所述供体核酸进行修饰。在一些实施例中,所述DAP的长度比所述间隔子短至少约1个(如至少约2个、3个或更多个中的任何一个)核苷酸。在一些实施例中,所述DAP包括与所述间隔子的至少约1个(如至少约2个、3个或更多个中的任何一个)核苷酸错配。例如,所述gRNA可以包括来自SEQID NO:8的多核苷酸序列的间隔子,并且所述DAP可以包括来自SEQ ID NO:16-28中任何一个的多核苷酸序列的原间隔子。
在一些实施例中,根据本文中所描述的使用双链供体核酸的方法中的任何方法,所述双链供体核酸是双链病毒基因组。在一些实施例中,所述双链病毒基因组是腺病毒基因组、慢病毒基因组(例如,慢病毒RNA基因组的dsDNA中间体)或腺相关病毒(AAV)基因组。在一些实施例中,所述AAV基因组是自身互补AAV(scAAV)基因组。在一些实施例中,所述scAAV基因组是scAAV6基因组。在一些实施例中,所述慢病毒基因组是整合酶缺陷型慢病毒基因组。
对定点多肽或DNA核酸内切酶进行编码的核酸
因此,在一些实施例中,基因组编辑的方法和组合物可以使用对定点多肽或DNA核酸内切酶进行编码的核酸序列。对所述定点多肽进行编码的所述核酸序列可以是DNA或RNA。如果对所述定点多肽进行编码的所述核酸序列是RNA,则其可以与gRNA序列共价连接或以单独的序列存在。在一些实施例中,可以使用所述定点多肽或DNA核酸内切酶的肽序列替代其核酸序列。
载体
另一方面,本公开提供了一种核酸,所述核酸具有对本公开的基因组靶向核酸进行编码的核苷酸序列、本公开的定点多肽和/或实施本公开的方法的实施例所需的任何核酸或蛋白质分子。在一些实施例中,此种核酸是载体(例如,重组表达载体)。
所设想的表达载体包含但不限于基于牛痘病毒、脊髓灰质炎病毒、腺病毒、腺相关病毒、SV40、单纯性疱疹病毒、人类免疫缺陷病毒、逆转录病毒(例如,鼠类白血病病毒、脾坏死病毒、以及源自于如劳斯肉瘤病毒、哈威肉瘤病毒、禽白血病病毒、慢病毒、人类免疫缺陷病毒、骨髓及外骨髓增生性肉瘤病毒和乳腺肿瘤病毒等逆转录病毒的载体)的病毒载体以及其它重组载体。设想用于真核靶细胞的其它载体包含但不限于载体pXT1、pSG5、pSVK3、pBPV、pMSG和pSVLSV40(法玛西亚公司(Pharmacia))。设想用于真核靶细胞的另外的载体包含但不限于载体pCTx-1、pCTx-2和pCTx-3。其它载体只要与宿主细胞相容就可以使用。
在一些实施例中,载体具有一个或多个转录和/或翻译控制元件。根据所利用的宿主/载体系统,表达载体中可以使用许多适合的转录和翻译控制元件中的任何元件,包含组成型和诱导型启动子、转录增强子元件、转录终止子等。在一些实施例中,载体是自我失活载体,其使病毒序列或者CRISPR机械或其它元素的组分失活。
适合的真核启动子(即,在真核细胞中起作用的启动子)的非限制性实例包含来自以下的那些启动子:巨细胞病毒(CMV)立即早期、单纯性疱疹病毒(HSV)胸苷激酶、早期和晚期SV40、来自逆转录病毒的长末端重复(LTR)、人延伸因子-1启动子(EF1)、具有与鸡β-肌动蛋白启动子(CAG)融合的巨细胞病毒(CMV)增强子的混合构建体、鼠类干细胞病毒启动子(MSCV)、磷酸甘油酸激酶-1基因座启动子(PGK)、以及小鼠金属硫蛋白-I。
为了表达小型RNA(包含结合Cas核酸内切酶使用的引导RNA),如RNA聚合酶III启动子等各种启动子(包含例如U6和H1启动子)会是有利的。对这种启动子的描述和用于增强这种启动子的使用的参数在本领域中是已知的,并且另外的信息和方法正在进行定期描述;参见例如,Ma,H等人,《分子疗法-核酸(Molecular Therapy-Nucleic Acids)》,3,e161(2014年)doi:10.1038/mtna.2014.12。
表达载体还可以含有用于翻译起始的核糖体结合位点以及转录终止子。表达载体还可以包含用于扩增表达的适当序列。表达载体还可以包含对与定点多肽融合由此产生融合蛋白非天然标签(例如,组氨酸标签、血球凝聚素标签、绿色荧光蛋白等)进行编码的核苷酸序列。
在一些实施例中,启动子是诱导型启动子(例如,热休克启动子、四环素调控的启动子、类固醇调控的启动子、金属调控的启动子、雌激素受体调控的启动子等)。在一些实施例中,启动子是组成型启动子(例如,CMV启动子、UBC启动子)。在一些实施例中,启动子是受空间限制和/或时间限制的启动子(例如,组织特异性启动子、细胞类型特异性启动子等)。在一些实施例中,如果基因要在将所述基因插入到基因组中之后在基因组中存在的内源启动子下表达,则载体不具有要在宿主细胞中表达的至少一个基因的启动子。
由于NHEJ和/或HDR而产生的对靶DNA的修饰可能导致例如突变、缺失、改变、整合、基因校正、基因置换、基因标记、转基因插入、核苷酸缺失、基因破坏、易位和/或基因突变。将非天然核酸整合到基因组DNA中的过程是基因组编辑的实例。
定点多肽是在基因组编辑中用于对DNA进行切割的核酸酶。定点多肽可以作为以下中的任一项施用于细胞或患者:一个或多个多肽或对所述多肽进行编码的一个或多个核酸。
在CRISPR/Cas或CRISPR/Cpf1系统的背景下,定点多肽可以结合到引导RNA,所述引导RNA进而指定靶DNA中多肽针对的位点。在本文中的CRISPR/Cas或CRISPR/Cpf1系统的实施例中,定点多肽是如DNA核酸内切酶等核酸内切酶。此种RNA引导的定点多肽在本文中也被称为RNA引导的核酸内切酶或RGEN。
示例性定点多肽在WO2018002719中进行了描述。
在一些实施例中,5′边界和/或3′边界的定位相对于特定参考基因座的移位用于促进或增强基因编辑的特定应用,这部分地取决于选择用于编辑的核酸内切酶系统,如本文中进一步描述和说明的。
在此种靶序列选择的第一非限制性方面中,许多核酸内切酶系统具有引导潜在靶位点的初始选择以供切割的规则或标准,如在CRISPR II型或V型核酸内切酶的情况下,邻近DNA切割位点的特定位置中的PAM序列基序的要求。
在靶序列选择或优化的另一非限制方面,相对于中靶活性的频率而评估靶序列和已经遍及核酸内切酶的特定组合的“脱靶”活性的频率(即,在除了所选靶序列之外的位点处发生DSB的频率)。在一些情况下,相对于其它细胞,已经在期望基因座处被正确编辑的细胞可以具有选择性优势。选择性优势的说明性但非限制性实例包含获取如以下等属性:增强的复制率、持久性、对某些条件的抗性、增强的成功移植率或者在引入到患者体内之后的体内持久性、以及与维持这种细胞或增大这种细胞的数量或活力相关的其它属性。在其它情况下,可以通过用于鉴别、分类或以其它方式选择已经被正确编辑的细胞的一种或多种筛选方法来肯定地选择已经在期望基因座处被正确编辑的细胞。选择性优势和定向选择方法两者可以利用与校正相关的表型。在一些实施例中,可以对细胞进行两次或更多次编辑以产生第二修饰,所述第二修饰产生了用于选择或纯化预期细胞群体的新表型。可以通过为可选择或可筛选标记物添加第二gRNA来产生这种第二修饰。在一些情况下,可以使用含有cDNA以及还有可选择标记物的DNA片段在期望的基因座处对细胞进行正确编辑。
在实施例中,无论是任何选择性优势适用还是将在特定情况下应用任何定向选择,还通过考虑脱靶频率来引导靶序列选择,以便提高应用的效率和/或降低在除了期望靶之外的位点处发生不期望改变的可能性。如本文中和本领域中进一步描述和说明的,脱靶活性的发生受大量因素的影响,所述因素包含靶位点与各种脱靶位点之间的相同点和不通电以及所使用的特定核酸内切酶。可获得辅助预测脱靶活性的生物信息学工具,并且这种工具也可以频繁用于鉴别最可能的脱靶活性位点,然后可以在实验环境中对所述位点进行评估以评价脱靶活性相对于中靶活性的频率,由此允许选择具有较高相对中靶活性的序列。本文提供了这种技术的说明性实例,并且其它技术在本领域中是已知的。
靶序列选择的另一方面涉及同源重组事件。共享同源性区域的序列可以充当导致插入序列缺失的同源重组事件的焦点。这种重组事件发生在染色体和其它DNA序列的正常复制过程期间,并且还在合成DNA序列的其它时间发生,如在双链断裂(DSB)修复的情况下,所述DSB在正常细胞复制周期期间有规律地发生,但还可以通过各种事件(如UV光以及DNA断裂的其它诱导物)的发生或某些药剂(如各种化学诱导物)的存在得到增强。许多这种诱导物使DSB在基因组中任意发生,并且DSB在正常细胞中有规律地诱导和修复。在修复期间,可以完全保真地重构原始序列,然而,在一些情况下,在DSB位点处引入小型插入或缺失(被称为“插入缺失”)。
还可以在特定位置处特异性地诱导DSB,如本文所描述的核酸内切酶系统的情况一样,所述DSB可以用于在所选染色体位置处引起定向或优先基因修饰事件。可以在多种情形下利用同原序列在DNA修复(以及复制)的背景下经受重组的趋势,并且所述趋势是如CRISPR等基因编辑系统的一个应用的基础,在所述应用中,使用同源定向修复将通过使用“供体”多核苷酸提供的所关注的序列插入到期望染色体定位中。
还可以使用特定序列之间的区域来产生期望的缺失,所述区域可以是可以具有少到十个碱基对或更少的小型“微同源性”区域。例如,在与附近序列具有微同源性的位点处引入单个DSB。在修复这种DSB的正常过程期间,高频率发生的结果是,由于DSB和伴随的细胞修复过程所促进的重组导致插入序列缺失。
然而,在一些情形下,选择同源性区域内的靶序列还可能引起大得多的缺失,包含基因融合(当缺失处于编码区域中时),考虑到特定情形,所述缺失可以是或可以不是期望的。
本文所提供的实例进一步展示了对用于产生DSB的各种靶区域的选择以及对此种区域内的特异性靶序列的选择,所述DSB被设计成插入本文中所描述的一个或多个系统组分,所述特异性靶序列被设计成使脱靶事件相对于中靶事件最小化。
在一些实施例中,引入到细胞中的多核苷酸具有可以单独地或组合地使用的一种或多种修饰,例如以增强活性、稳定性或特异性;改变递送;减少宿主细胞中的先天免疫应答;或用于其它增强,如本文中进一步描述的和本领域已知的。
在一些实施例中,在CRISPR/Cas9/Cpf1系统中使用修饰后多核苷酸,在这种情况下,可以对引导RNA(单链引导或双链引导)和/或对引入到细胞中的Cas或Cpf1核酸内切酶进行编码的DNA或RNA进行修饰,如下所描述和说明的。可以在CRISPR/Cas9/Cpf1系统中使用这种修饰后多核苷酸来编辑任何一个或多个基因组座位。
将CRISPR/Cas9/Cpf1系统用于非限制性地说明这种用途的目的,可以使用对引导RNA的修饰来增强具有引导RNA和Cas或Cpf1核酸内切酶的CRISPR/Cas9/Cpf1基因组编辑复合体的形成和稳定性,所述引导RNA可以是单分子引导或双分子。对引导RNA的修饰还可以或可替代地用于增强基因组编辑复合体与基因组中的靶序列之间的相互作用的发起、稳定性或动力学,这可以例如用于提高中靶活性。对引导RNA的修饰还可以或可替代地用于增强特异性,例如,中靶位点处的基因组编辑相较于其它(脱靶)位点处的效应的相对速率。
修饰还可以或可替代地用于例如通过增加引导RNA被细胞中存在的核糖核酸酶(RNA酶)降解的抗性来提高引导RNA的稳定性,由此使引导RNA在细胞中的半衰期增加。在Cas或Cpf1核酸内切酶被引入到待通过需要转译以生成核酸内切酶的RNA进行编辑细胞中的实施例中,提高引导RNA半衰期的修饰特别有用,这是因为使在RNA对核酸内切酶进行编码的同时引入的引导RNA的半衰期增加可以用于增加引导RNA和编码后Cas或Cpf1核酸内切酶共存于细胞中的时间。
修饰还可以或可替代地用于降低引入到细胞中的RNA引起先天性免疫应答的可能性或程度。已经在包含小干扰RNA(siRNA)在内的RNA干扰(RNAi)的背景下很好地表征的这种应答如下文和本领域中描述的往往与RNA的半衰期的降低相关和/或与细胞因子或和免疫应答相关的其它因子的引出相关。
还可以对引入到细胞中的对核酸内切酶进行编码的RNA进行一种或多种类型的修饰,包含但不限于增强RNA的稳定性的修饰(如通过提高细胞中存在的RNA酶对其进行的降解)、增强对所得产物(即,核酸内切酶)的翻译的修饰、和/或降低引入到细胞中的RNA引起先天性免疫应答的可能性或程度的修饰。
同样可以使用如前述和其它修饰等修饰的组合。在例如CRISPR/Cas9/Cpf1的情况下,可以对引导RNA进行一种或多种类型的修饰(包含以上例示的修饰)和/或可以对编码Cas核酸内切酶的RNA进行一种或多种类型的修饰(包含以上例示的修饰)。
示例性经修饰的核酸在WO2018002719中进行了描述。
在一些实施例中,本文中所提供的方法中所使用的任何核酸分子(例如,本公开的对基因组靶向核酸进行编码的核酸和/或定点多肽)被包装到递送媒剂的表面中或上以便递送到细胞。所设想的递送媒剂包含但不限于纳米球、脂质体、量子点、纳米颗粒、聚乙二醇颗粒、水凝胶和胶束。如本领域中描述的,可以使用各种靶向部分来增强这种媒剂与期望的细胞类型或位置的优先相互作用。
将本公开的复合体、多肽和核酸引入到细胞中可以通过以下方式发生:病毒或噬菌体感染、转染、缀合、原生质体融合、脂质转染、电穿孔、核转染、磷酸钙沉淀、聚乙烯亚胺(PEI)介导的转染、DEAE右旋糖酐介导的转染、脂质体介导的转染、粒子枪技术、磷酸钙沉淀、直接微注射、纳米颗粒介导的核酸递送等。
示例性递送方法和试剂在WO2018002719进行了描述。
上文已经参考具体的替代方案描述了本公开。然而,在本公开的范围内,除上文所描述的以外的其它替代方案同样是可能的。在本公开的范围内,可以提供与上文所描述的方法步骤不同的方法步骤。本文中所描述的不同特征和步骤可以以不同于所描述的特征和步骤的其它组合来组合。
关于在本文中使用复数和/或单数术语,本领域的技术人员可以根据上下文和/或应用的需要将复数翻译成单数和/或将单数翻译成复数。为了清楚起见,本文中可明确地阐述各种单数/复数排列。
本领域技术人员将理解,一般来说,本文中并且尤其在所附权利要求(例如,所附权利要求的主体)中使用的术语总体上旨在作为“开放式”术语(例如,术语“包含(including)”应当被理解为“包含但不限于”、术语“具有”应当被理解为“至少具有”、术语“包含(includes)”应当被理解为“包含但不限于”等)。
另外,在以马库西(Markush)组的方式描述本公开的特征或方面的情况下,本领域技术人员将认识到,本公开也由此以马库西组中的任何单个成员或成员子组的形式进行描述。
第一到第十一方面的替代方案的特征中的任何特征均适用于本文中所标识的所有方面和替代方案。此外,第一到第十一方面的替代方案的特征中的任何特征可以以任何方式与本文中所描述的其它替代方案部分或全部独立地组合,例如,一个、两个或三个或更多个替代方案可以全部或部分地组合。进一步地,可以使第一到第十一方面的替代方案的特征中的任何特征对其它方面或替代方案而言是任选的。尽管以上根据各种示例替代方案和实施方案进行了描述,但是应当理解,在一个或多个单独替代方案中描述的各种特征、方面和功能并不局限于其对结合其描述的特定替代方案的适用性,而是可以单独或以各种组合的方式应用于本申请的一个或多个其它替代方案,无论此类替代方案是否被描述,也无论此类特征是否被呈现为所描述的替代方案的一部分。因此,本申请的广度和范围不应受到任何上文所描述的示例替代方案的限制。
本文中所引用的所有参考文献都以全文引用的方式并入本文中。在通过引用的方式并入的公开和专利或专利申请与本说明书中所包含的公开内容相抵触的情况下,本说明书意欲替代和/或优先于任何这类矛盾材料。在通过引用的方式并入本文中的公开和专利或专利申请与本说明书中所包含的公开内容相抵触的情况下,本说明书意欲替代和/或优先于任何这类矛盾材料。
以下所附描述中阐述了本公开的一个或多个实施例的细节。但是与本文所描述的材料和方法类似或等效的任何材料和方法也可以用于实践或测试本公开。根据描述,本公开的其它特征、目的和优点将变得显而易见。在描述中,除非上下文另有明确规定,否则单数形式还包含复数形式。除非另外定义,否则本文所使用的所有技术术语和科学术语均具有与本公开所属领域的普通技术人员通常所理解的含义相同的含义。在冲突的情况下,以本说明书为准。
应当理解,本文中所描述的实例和实施例仅是出于说明性目的,并且根据其进行的各种修改或改变将启发本领域的技术人员并且将被包含在本申请的精神与权限范围内和所附权利要求书的范围内。本文所引用的所有出版物、专利和专利申请均出于所有目的以其整体通过并入。
本文中所提供的公开的一些实施例通过以下非限制性实例进一步说明。
实例
执行这个研究以在K562细胞中测定在有和没有供体切割的情况下刺激的NHEJ介导的靶向整合的可行性。在有和没有CRISPR/Cas9识别位点的情况下克隆带有依赖于内源PPP1R12C启动子进行表达的GFP表达盒的质粒供体载体以在体内进行供体切割。
在这些实验中,在第-1天,用1.50、2.75和3.50pmol的1切口质粒供体(pCR2.1-TOPO-psAAVS1-SA-P2A-H2Bj-Venus-BGHpA-psSCRAM)或3.50pmol的0切口质粒供体(pCR2.1-TOPO-psSCRAM-SA-P2A-H2Bj-Venus-BGHpA-psSCRAM)对三十万个K562细胞进行核转染。pCR2.1-TOPO:载体质粒主链;psSCRAM:用PAM加扰的原间隔子序列;psAAVS1:与具有PAM的Cas9/gRNA RNP所切割的基因组DNA序列相同的原间隔子序列;SA:剪接受体;P2A:肽切割信号序列;H2Bi-Venus:与使细胞核中的GFP稳定的组蛋白H2B融合的经修饰的GFP;以及BGHpA:牛生长激素聚腺苷酸化序列。二十四小时后,在有或没有RNP的情况下对每种条件下的K562细胞进行核转染。RNP是12pmol Cas9(Feldan)和60pmol AAVS1引导RNA(Axolabs)的复合体。使用针对K562细胞系的Lonza 4D
流式细胞术结果示出于图1A和1B中。如通过GFP
将在D7时提取的gDNA用于内-外式PCR(in-out PCR)以进行整合检测(参见图2中的示意图)。使用10μl AmpliTaq
执行这个研究以在人CD3
STIM后(分裂)T细胞靶向整合
表1
条件一式两份
将Pan CD3
以50,000vg/细胞的MOI使用来自VBL(CBGU004)的NHEJ-TI病毒(SEQ ID NO:6)并且以50,000vg/细胞的MOI使用来自VBL(CBGGU014)的HDR-TI病毒(SEQ ID NO:7)。RNP包含GeneArt v2 Cas9 1pmol/10,000个细胞和Synthego gRNA(SEQ ID NO:8)2.5pmol/10,000个细胞。
按照制造商的建议,将Lonza 4D
细胞培养
在这些实验中,将二十万个细胞/条件(总共320万个细胞)解冻,并将DMSO洗掉(将1ml冷冻细胞解冻并在10ml培养基中稀释)。将细胞以350xg旋转10分钟,抽吸上清液,并且然后轻拍管以重悬细胞。用活化珠以一百万个细胞/ml添加培养基,并将细胞培养48小时。
珠耗竭
解冻后第二天,将细胞收集到50ml锥形管中并剧烈移液以解离成团的细胞。将含有细胞的管放置在磁性支架上并温育10分钟,然后将上清液轻轻移液到其它50ml锥形管中。将含有细胞的管再次放置在磁性支架上并温育10分钟,然后将上清液轻轻移液到其它50ml锥形管中。将管以350xg离心10分钟,抽吸出上清液,并将细胞以一百万个细胞/ml重悬并在核转染前培养至少两小时。
RNP核转染
将细胞收集到50ml锥形管中并以350xg离心10分钟,在此期间制备RNP复合体。将先前等分的RNP复合体解冻,并制备20∶50pmol的Cas9∶gRNA/10τl核转染试剂的P3核转染试剂+RNP主混合物。在适当的孔/条件下,将10μl核转染试剂/孔等分到16孔核转染条。将收集到的细胞以200,000个细胞/10μl(20,000个细胞/μl)重悬于P3核转染试剂中,并将10μl含有细胞的核转染试剂分配到16孔核转染条的每个孔,达到20μl的总体积。
病毒转导
核转染前,制备病毒转导培养基。如下制备无血清培养基的含有病毒的主混合物:a.80μl总体积且50,000vg/细胞病毒;b.320μl(+额外)且400亿(vg+额外)。还制备仅培养基对照。将80μl转导培养基或对照等分到96孔板的孔。
核转染后,用100μl移液管抽吸80μl的转导培养基,并将其轻轻转移到16孔核转染条的孔中。抽吸出100μl的转导培养基/核转染培养基混合物,并将其移液回到96孔板的对应的孔中。将细胞(现在以2×10
无STIM(非分裂)T细胞靶向整合
表2
条件一式三份
将Pan CD3
以50,000vg/细胞的MOI使用来自VBL(CBGU004)的NHEJ-TI病毒(SEQ ID NO:6)并且以50,000vg/细胞的MOI使用来自VBL(CBGGU014)的HDR-TI病毒(SEQ ID NO:7)。RNP包含GeneArt v2 Cas9 1pmol/10,000个细胞和Synthego gRNA(SEQ ID NO:8)2.5pmol/10,000个细胞。
按照制造商的建议,将Lonza 4D
细胞培养
在这些实验中,将五百万个细胞/条件(总共1.2亿个细胞)解冻,并将DMSO洗掉(将5ml冷冻细胞解冻并在50ml培养基中稀释)。将细胞以350xg旋转10分钟,抽吸上清液,并且然后轻拍管以重悬细胞。以两百万到五百万个细胞/ml添加培养基,并将细胞培养24小时。
RNP核转染
将细胞收集到50ml锥形管中并以350xg离心10分钟,在此期间制备RNP复合体。将先前等分的RNP复合体解冻,并制备200∶500pmol的Cas9∶gRNA/50μl核转染试剂的P3核转染试剂+RNP主混合物。在适当的条件下,将50μl核转染试剂等分到100-μl的核转染比色皿。将收集到的细胞以2,000,000个细胞/50μl重悬于P3核转染试剂中,并将50μl含有细胞的核转染试剂分配到每个核转染比色皿,达到100μl的总体积。
病毒转导
核转染前,制备病毒转导培养基。如下制备无血清培养基的含有病毒的主混合物:a.900μl总体积且50,000vg/细胞病毒;b.4800μl(+额外)且10亿(vg+额外)。还制备仅培养基对照。将900μl转导培养基或对照等分到24孔板的孔。
核转染后,用转移移液管抽吸~500μl的转导培养基,并将其轻轻转移到核转染比色皿中。抽吸出所有的转导培养基/核转染培养基混合物,并将其移液回到24孔板的对应的孔中。将细胞培养最多两周,并在第2天(D2)、第4天(D4)、第7天(D7)和第14天(D14)通过流式细胞术对其进行分析。在第2天(D2)时收集基因组DNA以测定切割效率并在第7天(D7)时收集以测定供体整合。
结果示出于图3A、图3B、图4、图5A、图5B和图5C。HDR-TI在经活化的T细胞中是有利的(图3A和3B),而NHEJ-TI在未经活化的T细胞中是有利的(其中没有可检测到的HDR-TI;图5A和5B)。进一步地,如图5C中所示出的,经NHEJ编辑的未经活化的T细胞主要是CD4
执行这个研究以在人CD34
表3
每个条件使用二十万个CD34
按照制造商的建议,将Lonza 4D
细胞培养
使用前立即将等分的培养基和细胞因子解冻。将解冻的细胞因子和小分子添加到StemSpan SFEM II以产生完全培养基,将所述完全培养基温热到37℃。将足够用于200,000个细胞/条件的hCD34
RNP核转染
将Lonza 4D
AAV感染
将AAV在冰上解冻。将解冻的细胞因子和小分子在使用前立即添加到StemSpanSFEM II以产生完全培养基,将所述完全培养基温热到37℃。将细胞收集到15ml锥形管中,并取出100μl(总共1∶100)细胞并稀释到1ml(1∶10稀释度)以使用Vi-Cell XR测量活力和细胞浓度。将细胞以90xg旋转9分钟,在此期间,在低结合蛋白试管中制备AAV稀释液。通过将50μl完全培养基添加到96孔板的每个孔来制备培养板,并将对应量的AAV稀释液添加到每个孔。倒出上清液,并将细胞重悬于50μl乘以条件数量的完全培养基中。将50μl的细胞添加到每个孔,并将细胞放置回加湿的37℃常氧温育箱中持续两小时。然后将细胞收集到1.5ml无菌eppendorf管中,并以90xg旋转10分钟,在此期间,通过将0.7ml完全培养基添加在24孔板的每个孔中来制备培养板。倒出上清液,并将细胞重悬于300μl完全培养基中并转移到所制备的培养板。
条件特异性方案
方案1(P1)
方案1(P1)首先执行AAV处理,然后进行RNP处理。用AAV处理细胞,并在两小时后将其收集到1.5ml无菌Eppendorf管中。将细胞以90xg旋转10分钟,在此期间,制备核转染试剂和RNP以及每孔含900μl完全培养基的24孔培养板。将细胞重悬于20μl P3+/-RNP中,并将100μl的细胞转移到所制备的24孔培养板。将细胞在常氧温育箱中培养最多+5天,每两天添加一次培养基。
方案2(P2)
方案2(P2)首先执行RNP处理,然后进行AAV处理。在有或没有RNP的情况下对细胞进行核转染,并将100μl的细胞转移到所制备的培养板。允许细胞静置一小时,然后用AAV处理两小时。然后将细胞收集、旋转并重悬于新鲜培养基中,并将其在常氧温育箱中培养最多+5天,每两天添加一次培养基。
数据收集
TIDE分析
将细胞收集到1.5ml微离心管中。然后冲洗细胞,并用1ml PBS收集剩余的培养基。通过以350xg离心5分钟使细胞沉淀,并倒出上清液。如果总体积超过1.2ml,则在同一管中重复步骤1-4。按照制造商的方案,使用Qiagen
使用10τl AmpliTaq
然后如下对经纯化的PCR产物进行测序。按照制造商的方案使用Qiagen PCR纯化试剂盒(目录号28106)进行PCR净化。将经纯化的PCR产物提交给Sequetech进行Sanger测序。使用巢式引物进行测序:AAVS1 TIDE-4R:cctctccatcctcttgctttctttg(SEQ ID NO:12);和AAVS1TIDE-4F:aactgcttctcctcttgggaagt(SEQ ID NO:13)。
使用TSUNAMI Batch TIDE分析(54.234.74.37/home/或54.158.189.0/home/处的网页)对CRISPR/Cas9切割效率进行INDEL分析。上传所需要的数据文件以开始分析:CSV文件列表-含有四列且无标题的“.csv”文件(样品名称列表-用于在输出文件中进行标记;预期的gRNA序列-表示紧邻PAM序列(不包含PAM)上游的预期的gRNA序列的20nt(5′-3′)DNA字符串;测试样品名称;对照样品名称);测序文件(.ab1或.scf文件)。输入以下参数以进行分析:左边界:默认值为100bp;右边界:断裂位点处设置的默认值-10bp;分解窗口:测定用于进行分解的序列段(默认值设置是对于所上传的序列而言可能的最大窗口);插入缺失大小范围:设置要建模的插入缺失的最大大小。默认值为10;P值阈值:默认值为p<0.001。然后生成结果并对输出中的质量度量进行评估,并且如果需要的话,调整参数(断裂位点之前的平均异常序列信号<10%(对照和测试样品两者);分解结果的R2>0.9)。参考:Brinkman等人,《核酸研究(Nucleic Acids Res.)》2014年12月16日;42(22):e168.doi:10.1093/nar/gku936。
进行内-外式PCR以进行整合检测
将TIDE分析所提取的相同的gDNA用于内-外式PCR以进行整合检测。使用10μlAmpliTaq
TOPO-TA克隆
使用4μl内-外式PCR扩增子、1μl盐溶液和1μ1 TOPO-TA载体(
将TOP10化学感受态细胞在冰上解冻,并将2μl TOPO-TA克隆产物添加到解冻的TOP10化学感受态细胞。将细胞悬浮液通过轻敲混合并在冰上温育5分钟,然后在42℃下加热震荡45秒。然后将细胞在冰上温育5分钟,添加250μl SOC培养基,并将细胞在37℃下在细菌振荡器中温育30分钟。将150μl的细胞平板接种在X-gal涂覆的羧苄青霉素琼脂板上并温育过夜。选择白色菌落用于质粒生长和测序。
流式细胞术
将细胞从细胞培养板收集到5ml FACS管中,并添加至多4ml的FACS缓冲液。将细胞以350xg旋转5分钟,并倒出上清液。添加用于细胞表面抗原的活力染料和/或缀合的抗体,并将细胞在室温下温育20分钟。添加至多4ml的FACS缓冲液,并将细胞以350xg旋转5分钟。倒出上清液并使总体积达到200μl,并将细胞转移到U型底96孔板,并使用Attune高通量系统运行。
结果示出于图6、图7A、图7B、图8A和图8B。对于P1和P2两者,2切口供体的编辑效率高于0切口供体,并且在对应条件下,与P1相比,P2示出更高的编辑效率(图6和7A),从而进一步证实供体切割的优点并且表明首先进行RNP处理、然后进行AAV处理会导致更有效的靶向整合。
执行这个研究以在人CD34
表4:D1编辑条件
表5:D2编辑条件
**一式三份地进行实验
在这些实验中,使用200,000个CD34
RNP包含24pmol的Cas9(Feldan)到120pmol的AAVS1引导RNA(SEQ ID NO:8)(Axolabs)。以20,000vg/细胞的MOI使用scAAV6 2切口NHEJ载体(SEQ ID NO:5)(载体生物实验室),以2×10
按照制造商的建议,将Lonza 4D
细胞培养
使用前立即将等分的培养基和细胞因子解冻。将解冻的细胞因子和小分子添加到SCGM或SFEM II以产生完全培养基,将所述完全培养基温热到37℃。将足够用于200,000个细胞/条件的hCD34
RNP核转染
将Lonza 4D
AAV感染
将AAV在冰上解冻。将解冻的细胞因子和小分子在使用前立即添加到SCGM或SFEMII以产生完全培养基,将所述完全培养基温热到37℃,在此期间,在低结合蛋白管中制备AAV稀释液。制备96孔培养板,并将80μl完全培养基和对应量的AAV稀释液添加到每个孔。将100μl的经核转染的细胞(添加有80μl的拯救培养基)从16孔条转移到所制备的培养板中,并将细胞放置回加湿的37℃缺氧温育箱中持续两小时。然后收集细胞,在此期间,通过将0.7ml完全培养基添加在24孔板的每个孔中来制备培养板。倒出细胞上清液,并将细胞重悬并转移到所制备的24孔培养板。用200μl新鲜培养基和强力移液清洗96孔培养板,并将培养基转移到24孔板的对应孔中。
然后将细胞培养四天,然后将其收集并在1.5ml管中沉淀。按照制造商的方案,使用Machery-Nagel基因组DNA提取试剂盒收集gDNA。
TIDE分析
将细胞收集到1.5ml微离心管中。然后冲洗细胞,并用1ml PBS收集剩余的培养基。通过以350xg离心5分钟使细胞沉淀,并倒出上清液。如果总体积超过1.2ml,则在同一管中重复步骤1-4。按照制造商的方案,使用Qiagen
使用10μl AmpliTaq
然后如下对经纯化的PCR产物进行测序。按照制造商的方案使用Qiagen PCR纯化试剂盒(目录号28106)进行PCR净化。将经纯化的PCR产物提交给Sequetech进行Sanger测序。使用巢式引物进行测序:AAVS1 TIDE-4R:cctctccatcctcttgctttctttg(SEQ ID NO:12);和AAVS1TIDE-4F:aactgcttctcctcttgggaagt(SEQ ID NO:13)。
使用TSUNAMI Batch TIDE分析(54.234.74.37/home/或54.158.189.0/home/处的网页)对CRISPR/Cas9切割效率进行INDEL分析。上传所需要的数据文件以开始分析:CSV文件列表-含有四列且无标题的“.csv”文件(样品名称列表-用于在输出文件中进行标记;预期的gRNA序列-表示紧邻PAM序列(不包含PAM)上游的预期的gRNA序列的20nt(5′-3′)DNA字符串;测试样品名称;对照样品名称);测序文件(.ab1或.scf文件)。输入以下参数以进行分析:左边界:默认值为100bp;右边界:断裂位点处设置的默认值-10bp;分解窗口:测定用于进行分解的序列段(默认值设置是对于所上传的序列而言可能的最大窗口);插入缺失大小范围:设置要建模的插入缺失的最大大小。默认值为10;P值阈值:默认值为p<0.001。然后生成结果并对输出中的质量度量进行评估,并且如果需要的话,调整参数(断裂位点之前的平均异常序列信号<10%(对照和测试样品两者);分解结果的R2>0.9)。参考:Brinkman等人,《核酸研究》2014年12月16日;42(22):e168.doi:10.1093/nar/gku936。
进行内-外式PCR以进行整合检测
将TIDE分析所提取的相同的gDNA用于内-外式PCR以进行整合检测。使用10μlAmpliTaq
流式细胞术
将细胞从细胞培养板收集到5ml FACS管中,并添加至多4ml的FACS缓冲液。将细胞以350xg旋转5分钟,并倒出上清液。添加用于细胞表面抗原的活力染料和/或缀合的抗体,并将细胞在室温下温育20分钟。添加至多4ml的FACS缓冲液,并将细胞以350xg旋转5分钟。倒出上清液并使总体积达到200μl,并将细胞转移到U型底96孔板,并使用Attune高通量系统运行。流式细胞术CD34离体面板包含CD34 BV510;CD90 PerCP-Cy5.5;CD38APC;CD45RAPE;和Ghost Red 780活力染料。
结果示出于图9A、图9B、图9C、图9D、图10A、图10B、图11A、图11B、图11C、图11D、图12A、图12B和图12C。SCGM培养基引起500nm范围内的偏移,从而导致eGFP和CD34-BV510通道中的阴性群体发生偏移。这可以解释明确的eGFP
执行这个研究以在人CD34
表9
**一式三份地进行实验
在这些实验中,使用200,000个CD34
RNP包含比率为10∶25pmol的Cas9(GeneArt V2)和AAVS1引导RNA(SEQ ID NO:8)(Synthego)。以20,000vg/细胞的MOI使用scAAV60切口NHEJ载体(SEQ ID NO:4)(载体生物实验室),以2×10
按照制造商的建议,将Lonza 4D
细胞培养
对于H1编辑条件,解冻后一到两个小时按下文所陈述的操控细胞。对于D1编辑条件,解冻后24小时按下文所陈述的操控细胞。
使用前立即将等分的培养基和细胞因子解冻。将解冻的细胞因子和小分子添加到SFEM II以产生完全培养基,将所述完整培养基温热到37℃。将足够用于200,000个细胞/条件的hCD34
RNP核转染
将Lonza 4D
AAV感染
将AAV在冰上解冻。将解冻的细胞因子和小分子在使用前立即添加到SFEM II以产生完全培养基,将所述完全培养基温热到37℃,在此期间,在低结合蛋白管中制备AAV稀释液。制备96孔培养板,并将80μl完全培养基和对应量的AAV稀释液添加到每个孔。将100μl的经核转染的细胞(添加有80μl的拯救培养基)从16孔条转移到所制备的培养板中,并将细胞放置回加湿的37℃缺氧温育箱中持续两小时。然后收集细胞,在此期间,通过将0.7ml完全培养基添加在24孔板的每个孔中来制备培养板。倒出细胞上清液,并将细胞重悬并转移到所制备的24孔培养板。用200μl新鲜培养基和强力移液清洗96孔培养板,并将培养基转移到24孔板的对应孔中。
然后将细胞培养四天,然后将其收集并在1.5ml管中沉淀。按照制造商的方案,使用Machery-Nagel基因组DNA提取试剂盒收集gDNA。
TIDE分析
将细胞收集到1.5ml微离心管中。然后冲洗细胞,并用1ml PBS收集剩余的培养基。通过以350xg离心5分钟使细胞沉淀,并倒出上清液。如果总体积超过1.2ml,则在同一管中重复步骤1-4。按照制造商的方案,使用Qiagen
使用10μl AmpliTaq
然后如下对经纯化的PCR产物进行测序。按照制造商的方案使用Qiagen PCR纯化试剂盒(目录号28106)进行PCR净化。将经纯化的PCR产物提交给Sequetech进行Sanger测序。使用巢式引物进行测序:AAVS1 TIDE-4R:cctctccatcctcttgctttctttg(SEQ ID NO:12);和AAVS1TIDE-4F:aactgcttctcctcttgggaagt(SEQ ID NO:13)。
使用TSUNAMI Batch TIDE分析(54.234.74.37/home/或54.158.189.0/home/处的网页)对CRISPR/Cas9切割效率进行INDEL分析。上传所需要的数据文件以开始分析:CSV文件列表-含有四列且无标题的“.csv”文件(样品名称列表-用于在输出文件中进行标记;预期的gRNA序列-表示紧邻PAM序列(不包含PAM)上游的预期的gRNA序列的20nt(5′-3′)DNA字符串;测试样品名称;对照样品名称);测序文件(.ab1或.scf文件)。输入以下参数以进行分析:左边界:默认值为100bp;右边界:断裂位点处设置的默认值-10bp;分解窗口:测定用于进行分解的序列段(默认值设置是对于所上传的序列而言可能的最大窗口);插入缺失大小范围:设置要建模的插入缺失的最大大小。默认值为10;P值阈值:默认值为p<0.001。然后生成结果并对输出中的质量度量进行评估,并且如果需要的话,调整参数(断裂位点之前的平均异常序列信号<10%(对照和测试样品两者);分解结果的R2>0.9)。参考:Brinkman等人,《核酸研究》2014年12月16日;42(22):e168.doi:10.1093/nar/gku936。
进行内-外式PCR以进行整合检测
将TIDE分析所提取的相同的gDNA用于内-外式PCR以进行整合检测。使用10μlAmpliTaq
流式细胞术
将细胞从细胞培养板收集到5ml FACS管中,并添加至多4ml的FACS缓冲液。将细胞以350xg旋转5分钟,并倒出上清液。添加用于细胞表面抗原的活力染料和/或缀合的抗体,并将细胞在室温下温育20分钟。添加至多4ml的FACS缓冲液,并将细胞以350xg旋转5分钟。倒出上清液并使总体积达到200μl,并将细胞转移到U型底96孔板,并使用Attune高通量系统运行。流式细胞术CD34离体面板包含CD34 BV510;CD90 PerCP-Cy5.5;CD38APC;CD45RAPE;和Ghost Red 780活力染料。
结果示出于图13中。解冻后一小时编辑的细胞示出成功的NHEJ介导的靶向整合的证据,尽管效率略微较低。然而,相对于D1,当在H1时编辑细胞时,相对细胞性和活力略微增加。在同一天对细胞进行解冻、编辑和注射的方案可以简化技术的临床应用。这对于NHEJ-TI而言将是独特的,因为其不需要HDR介导的TI所需的预刺激步骤。
执行这个研究以在人CD34
表6
**一式两份地进行实验
在这些实验中,使用200,000个CD34
RNP包含24pmol的Cas9(GeneArt V2对比Aldevron SpyFi)到120pmol的AAVS1引导RNA(SEQ ID NO:8)(Synthego)。以20,000vg/细胞的MOI使用scAAV6 2切口NHEJ载体(SEQID NO:5)(载体生物实验室),以2×10
按照制造商的建议,将Lonza 4D
细胞培养
使用前立即将等分的培养基和细胞因子解冻。将解冻的细胞因子和小分子添加到SFEM II以产生完全培养基,将所述完整培养基温热到37℃。将足够用于200,000个细胞/条件的hCD34
RNP核转染
将Lonza 4D
AAV感染
将AAV在冰上解冻。将解冻的细胞因子和小分子在使用前立即添加到SFEM II以产生完全培养基,将所述完全培养基温热到37℃,在此期间,在低结合蛋白管中制备AAV稀释液。制备96孔培养板,并将80μl完全培养基和对应量的AAV稀释液添加到每个孔。将100μl的经核转染的细胞(添加有80μl的拯救培养基)从16孔条转移到所制备的培养板中,并将细胞放置回加湿的37℃缺氧温育箱中持续两小时。然后收集细胞,在此期间,通过将0.7ml完全培养基添加在24孔板的每个孔中来制备培养板。倒出细胞上清液,并将细胞重悬并转移到所制备的24孔培养板。用200μl新鲜培养基和强力移液清洗96孔培养板,并将培养基转移到24孔板的对应孔中。
然后将细胞培养四天,然后将其收集并在1.5ml管中沉淀。按照制造商的方案,使用Machery-Nagel基因组DNA提取试剂盒收集gDNA。
TIDE分析
将细胞收集到1.5ml微离心管中。然后冲洗细胞,并用1ml PBS收集剩余的培养基。通过以350xg离心5分钟使细胞沉淀,并倒出上清液。如果总体积超过1.2ml,则在同一管中重复步骤1-4。按照制造商的方案,使用Qiagen
使用10μl AmpliTaq
然后如下对经纯化的PCR产物进行测序。按照制造商的方案使用Qiagen PCR纯化试剂盒(目录号28106)进行PCR净化。将经纯化的PCR产物提交给Sequetech进行Sanger测序。使用巢式引物进行测序:AAVS1 TIDE-4R:cctctccatcctcttgctttctttg(SEQ ID NO:12);和AAVS1TIDE-4F:aactgcttctcctcttgggaagt(SEQ ID NO:13)。
使用TSUNAMI Batch TIDE分析(54.234.74.37/home/或54.158.189.0/home/处的网页)对CRISPR/Cas9切割效率进行INDEL分析。上传所需要的数据文件以开始分析:CSV文件列表-含有四列且无标题的“.csv”文件(样品名称列表-用于在输出文件中进行标记;预期的gRNA序列-表示紧邻PAM序列(不包含PAM)上游的预期的gRNA序列的20m(5′-3′)DNA字符串;测试样品名称;对照样品名称);测序文件(.ab1或.scf文件)。输入以下参数以进行分析:左边界:默认值为100bp;右边界:断裂位点处设置的默认值-10bp;分解窗口:测定用于进行分解的序列段(默认值设置是对于所上传的序列而言可能的最大窗口);插入缺失大小范围:设置要建模的插入缺失的最大大小。默认值为10;P值阈值:默认值为p<0.001。然后生成结果并对输出中的质量度量进行评估,并且如果需要的话,调整参数(断裂位点之前的平均异常序列信号<10%(对照和测试样品两者);分解结果的R2>0.9)。参考:Brinkman等人,《核酸研究》2014年12月16日;42(22):e168.doi:10.1093/nar/gku936。
进行内-外式PCR以进行整合检测
将TIDE分析所提取的相同的gDNA用于内-外式PCR以进行整合检测。使用10τlAmpliTaq
流式细胞术
将细胞从细胞培养板收集到5ml FACS管中,并添加至多4ml的FACS缓冲液。将细胞以350xg旋转5分钟,并倒出上清液。添加用于细胞表面抗原的活力染料和/或缀合的抗体,并将细胞在室温下温育20分钟。添加至多4ml的FACS缓冲液,并将细胞以350xg旋转5分钟。倒出上清液并使总体积达到200μl,并将细胞转移到U型底96孔板,并使用Attune高通量系统运行。流式细胞术CD34离体面板包含CD34 BV510;CD90 PerCP-Cy5.5;CD38APC;CD45RAPE;和Ghost Red 780活力染料。
结果示出于图14A、图14B、图14C和图15。DZ-100核转染程序比CA-137核转染程序表现更好。使用DZ-100的编辑效率显著较高,尽管细胞的绝对细胞性没有显著差异。GeneArt V2 Cas9比Aldevron的SpyFi Cas9表现更好。用GeneArt V2 Cas9的编辑效率明显著较高,而SpyFi并未提高活力。
执行这个研究以在人CD34
表7
**一式三份地进行实验
在这些实验中,使用200,000个CD34
RNP包含Cas9(GeneArt V2):AAVS1引导RNA(SEQ ID NO:8)(Synthego),比率为:1)Lo:10∶50pmol;或2)Hi:20∶100pmol。以以下两种的MOI使用scAAV6 2切口NHEJ载体(SEQ IDNO:5)(载体生物实验室):1)Lo:20,000vg/细胞;或2)Hi:60,000vg/细胞,以2×10
按照制造商的建议,将Lonza 4D
细胞培养
使用前立即将等分的培养基和细胞因子解冻。将解冻的细胞因子和小分子添加到SFEM II以产生完全培养基,将所述完整培养基温热到37℃。将足够用于200,000个细胞/条件的hCD34
RNP核转染
将Lonza 4D
AAV感染
将AAV在冰上解冻。将解冻的细胞因子和小分子在使用前立即添加到SFEM II以产生完全培养基,将所述完全培养基温热到37℃,在此期间,在低结合蛋白管中制备AAV稀释液。制备96孔培养板,并将80μl完全培养基和对应量的AAV稀释液添加到每个孔。将100μl的经核转染的细胞(添加有80μl的拯救培养基)从16孔条转移到所制备的培养板中,并将细胞放置回加湿的37℃缺氧温育箱中持续两小时。然后收集细胞,在此期间,通过将0.7ml完全培养基添加在24孔板的每个孔中来制备培养板。倒出细胞上清液,并将细胞重悬并转移到所制备的24孔培养板。用200μl新鲜培养基和强力移液清洗96孔培养板,并将培养基转移到24孔板的对应孔中。
然后将细胞培养四天,然后将其收集并在1.5ml管中沉淀。按照制造商的方案,使用Machery-Nagel基因组DNA提取试剂盒收集gDNA。
TIDE分析
将细胞收集到1.5ml微离心管中。然后冲洗细胞,并用1ml PBS收集剩余的培养基。通过以350xg离心5分钟使细胞沉淀,并倒出上清液。如果总体积超过1.2ml,则在同一管中重复步骤1-4。按照制造商的方案,使用Qiagen
使用10μl AmpliTaq
然后如下对经纯化的PCR产物进行测序。按照制造商的方案使用Qiagen PCR纯化试剂盒(目录号28106)进行PCR净化。将经纯化的PCR产物提交给Sequetech进行Sanger测序。使用巢式引物进行测序:AAVS1 TIDE-4R:cctctccatcctcttgctttctttg(SEQ ID NO:12);和AAVS1TIDE-4F:aactgcttctcctcttgggaagt(SEQ ID NO:13)。
使用TSUNAMI Batch TIDE分析(54.234.74.37/home/或54.158.189.0/home/处的网页)对CRISPR/Cas9切割效率进行INDEL分析。上传所需要的数据文件以开始分析:CSV文件列表-含有四列且无标题的“.csv”文件(样品名称列表-用于在输出文件中进行标记;预期的gRNA序列-表示紧邻PAM序列(不包含PAM)上游的预期的gRNA序列的20nt(5′-3′)DNA字符串;测试样品名称;对照样品名称);测序文件(.ab1或.scf文件)。输入以下参数以进行分析:左边界:默认值为100bp;右边界:断裂位点处设置的默认值-10bp;分解窗口:测定用于进行分解的序列段(默认值设置是对于所上传的序列而言可能的最大窗口);插入缺失大小范围:设置要建模的插入缺失的最大大小。默认值为10;P值阈值:默认值为p<0.001。然后生成结果并对输出中的质量度量进行评估,并且如果需要的话,调整参数(断裂位点之前的平均异常序列信号<10%(对照和测试样品两者);分解结果的R2>0.9)。参考:Brinkman等人,《核酸研究》2014年12月16日;42(22):e168.doi:10.1093/nar/gku936。
进行内-外式PCR以进行整合检测
将TIDE分析所提取的相同的gDNA用于内-外式PCR以进行整合检测。使用10μlAmpliTaq
流式细胞术
将细胞从细胞培养板收集到5ml FACS管中,并添加至多4ml的FACS缓冲液。将细胞以350xg旋转5分钟,并倒出上清液。添加用于细胞表面抗原的活力染料和/或缀合的抗体,并将细胞在室温下温育20分钟。添加至多4ml的FACS缓冲液,并将细胞以350xg旋转5分钟。倒出上清液并使总体积达到200μl,并将细胞转移到U型底96孔板,并使用Attune高通量系统运行。流式细胞术CD34离体面板包含CD34BV510;CD90PerCP-Cy5.5;CD38APC;CD45RA PE;和Ghost Red 780活力染料。
结果示出于图16中。RNP水平降低会使编辑效率降低。当与水平提高的RNP一起使用时,提高的AAV水平会显著提高效率,并且不会降低相对活力。
执行这个研究以测定人CD34
在这些实验中,使用200,000个CD34
RNP包含Cas9(GeneArt V2):AAVS1引导RNA(Synthego),比率为20∶50pmol。以5000vp/细胞的MOI使用Ad5/352切口NHEJ载体(Welgen公司(Welgen Inc)),以2×10
按照制造商的建议,将Lonza 4D
如先前所描述被执行RNP核转染和病毒感染。核转染和Ad5/35处理后7天进行针对整合检测的内-外式PCR分析。
结果示出于图17中。所有样品均具有外-外式带,但是如通过内-外式PCR带所证明的,只有用Ad5/35和RNP核转染两者处理的样品示出转基因的整合。
先前的实例示出了CD34 HSC中的NHEJ介导的靶向整合的总体优化编辑条件。对HDR的培养条件进行了优化,从而有必要在HSC中进行细胞循环。然而,在HSC中诱导细胞增殖通常会诱导分化,从而耗尽LT-HSC的级分。NHEJ介导的TI不需要细胞循环和生长。此处对基质蛋白是否可以在维持有效靶向整合的同时帮助维持LT-HSC表型进行了检查。对使用肌腱蛋白C(一种基质蛋白)和DLL1-Fc涂层来诱导NOTCH信号传导进行了检查。这两种因素均与骨髓微环境、HSC发育和维持相关。
表8
**一式三份地进行实验
在这些实验中,使用200,000个CD34
如下制备培养板(经组织培养处理的24孔板)。1.对照板(低附着板)。2.肌腱蛋白C:1μg/cm
RNP包含Cas9(GeneArt V2):AAVS1引导RNA(SEQ ID NO:8)(Synthego),比率为10∶25pmol。以20,000vg/细胞的MOI使用scAAV6 0切口NHEJ载体(SEQ ID NO:4)(载体生物实验室),以2×10
按照制造商的建议,将Lonza 4D
细胞培养
如下制备涂覆有肌腱蛋白C的细胞培养板。将100μg的解冻的肌腱蛋白C在24ml冷PBS中稀释,并通过用0.22μm PVDF膜过滤而灭菌,并将0.5ml/孔的PBS-TenC混合物添加到24孔板的孔。将板用石蜡膜覆盖,并在4℃下温育过夜。在使用前立即抽吸PBS-TenC混合物。
如下制备涂覆有DLL1-Fc的细胞培养板。通过将50μg的DLL1-Fc在12ml冷PBS中稀释而将DLL1-Fc在PBS中重构(制造商的方案),并将0.5ml/孔的PBS-DLL1-Fc混合物添加到24孔板的孔。将板用石蜡膜覆盖,并在4℃下温育过夜。在使用前立即抽吸PBS-DLL1-Fc混合物。
如下制备涂覆有肌腱蛋白C和DLL1-Fc的细胞培养板。将50μg的解冻的肌腱蛋白C在12ml冷PBS中稀释,并通过用0.22μm PVDF膜过滤而灭菌。添加50μg重构的DLL1-Fc,并将0.5ml/孔的PBS-TenC-DLL1-Fc混合物添加到24孔板的孔。将板用石蜡膜覆盖,并在4℃下温育过夜。在使用前立即抽吸PBS-TenC-DLL1-Fc混合物。
使用前立即将等分的培养基和细胞因子解冻。将解冻的细胞因子和小分子添加到SFEM II以产生完全培养基,将所述完整培养基温热到37℃。将足够用于200,000个细胞/条件的hCD34
RNP核转染
将Lonza 4D
AAV感染
将AAV在冰上解冻。将解冻的细胞因子和小分子在使用前立即添加到SFEM II以产生完全培养基,将所述完全培养基温热到37℃,在此期间,在低结合蛋白管中制备AAV稀释液。制备96孔培养板,并将80μl完全培养基和对应量的AAV稀释液添加到每个孔。将100μl的经核转染的细胞(添加有80τl的拯救培养基)从16孔条转移到所制备的培养板中,并将细胞放置回加湿的37℃缺氧温育箱中持续两小时。然后收集细胞,在此期间,通过将0.7ml完全培养基添加在24孔板的每个孔中来制备培养板。倒出细胞上清液,并将细胞重悬并转移到所制备的24孔培养板。用200μl新鲜培养基和强力移液清洗96孔培养板,并将培养基转移到24孔板的对应孔中。
然后将细胞培养四天,然后将其收集并在1.5ml管中沉淀。按照制造商的方案,使用Machery-Nagel基因组DNA提取试剂盒收集gDNA。
TIDE分析
将细胞收集到1.5ml微离心管中。然后冲洗细胞,并用1ml PBS收集剩余的培养基。通过以350xg离心5分钟使细胞沉淀,并倒出上清液。如果总体积超过1.2ml,则在同一管中重复步骤1-4。按照制造商的方案,使用Qiagen
使用10μl AmpliTaq
然后如下对经纯化的PCR产物进行测序。按照制造商的方案使用Qiagen PCR纯化试剂盒(目录号28106)进行PCR净化。将经纯化的PCR产物提交给Sequetech进行Sanger测序。使用巢式引物进行测序:AAVS1 TIDE-4R:cctctccatcctcttgctttctttg(SEQ ID NO:12);和AAVS1TIDE-4F:aactgcttctcctcttgggaagt(SEQ ID NO:13)。
使用TSUNAMI Batch TIDE分析(54.234.74.37/home/或54.158.189.0/home/处的网页)对CRISPR/Cas9切割效率进行INDEL分析。上传所需要的数据文件以开始分析:CSV文件列表-含有四列且无标题的“.csv”文件(样品名称列表-用于在输出文件中进行标记;预期的gRNA序列-表示紧邻PAM序列(不包含PAM)上游的预期的gRNA序列的20nt(5′-3′)DNA字符串;测试样品名称;对照样品名称);测序文件(.ab1或.scf文件)。输入以下参数以进行分析:左边界:默认值为100bp;右边界:断裂位点处设置的默认值-10bp;分解窗口:测定用于进行分解的序列段(默认值设置是对于所上传的序列而言可能的最大窗口);插入缺失大小范围:设置要建模的插入缺失的最大大小。默认值为10;P值阈值:默认值为p<0.001。然后生成结果并对输出中的质量度量进行评估,并且如果需要的话,调整参数(断裂位点之前的平均异常序列信号<10%(对照和测试样品两者);分解结果的R2>0.9)。参考:Brinkman等人,《核酸研究》2014年12月16日;42(22):e168.doi:10.1093/nar/gku936。
进行内-外式PCR以进行整合检测
将TIDE分析所提取的相同的gDNA用于内-外式PCR以进行整合检测。使用10μlAmpliTaq
流式细胞术
将细胞从细胞培养板收集到5ml FACS管中,并添加至多4ml的FACS缓冲液。将细胞以350xg旋转5分钟,并倒出上清液。添加用于细胞表面抗原的活力染料和/或缀合的抗体,并将细胞在室温下温育20分钟。添加至多4ml的FACS缓冲液,并将细胞以350xg旋转5分钟。倒出上清液并使总体积达到200μl,并将细胞转移到U型底96孔板,并使用Attune高通量系统运行。流式细胞术CD34离体面板包含CD34 BV510;CD90 PerCP-Cy5.5;CD38APC;CD45RAPE;和Ghost Red 780活力染料。
结果示出于图18A和18B中。相对于对照细胞,在基质蛋白上培养细胞不会提高经编辑的细胞的活力和绝对细胞性。有趣的是,在具有LT-HSC表型(CD34
执行这个研究以在人CD34
在本研究中,在以下条件下,使用总共20只小鼠。培养对照:三只小鼠;仅RNP:三只小鼠;仅scAAV6 0切口:三只小鼠;仅scAAV6 2切口小鼠:三只小鼠;RNP+scAAV6 0切口:四只小鼠;和RNP+scAAV6 2切口:四只小鼠。
使用500,000个CD34
RNP包含Cas9(GeneArt V2):AAVS1引导RNA(SEQ ID NO:8)(Synthego),比率为50∶250pmol。以60,000vg/细胞的MOI使用scAAV60切口NHEJ载体(SEQ ID NO:4)(载体生物实验室)或scAAV62切口NHEJ载体(SEQ ID NO:5)(载体生物实验室),以2×10
按照制造商的建议,将Lonza 4D
实验时间线如下。第0天(D0)-将细胞解冻:1000万个动员CD34
细胞培养
使用前立即将等分的培养基和细胞因子解冻。将解冻的细胞因子和小分子添加到SFEM II以产生完全培养基,将所述完整培养基温热到37℃。将足够用于500,000个细胞/小鼠的hCD34
RNP核转染
将Lonza 4D
AAV感染
将AAV在冰上解冻。将解冻的细胞因子和小分子在使用前立即添加到SFEM II以产生完全培养基,将所述完全培养基温热到37℃,在此期间,在低结合蛋白管中制备AAV稀释液。通过将750μl或1ml完全培养基和对应量的AAV稀释液添加到T75烧瓶来制备培养烧瓶。将600μl的经核转染的细胞(添加有500μl的拯救培养基)从转染烧瓶转移到所制备的AAV感染培养烧瓶中,并将细胞放置回加湿的37℃缺氧温育箱中持续六小时。然后将细胞转移到15ml锥形管并以90xg旋转10分钟,抽吸上清液,并将细胞重悬于7.5ml或10ml中并转移到T75烧瓶以继续培养过夜、保留等分试样的细胞继续培养以进行编辑分析。
将细胞收集并在15ml锥形管中沉淀,抽吸上清液,并将细胞重悬于165μl或220μl注射缓冲液(PBS+0.5%BSA)中。将10μl细胞等分试样以1∶100稀释,并使用Vi-Cell对其进行计数。将剩余的细胞保持在冰上,直到注射的时间为止。从将细胞解冻、操控期间到进行制备以便注射的细胞损失的水平比预期的要大,并且每只小鼠最多仅接受200,000个细胞。
细胞的编辑效率如下:
D2 eGFP水平:培养对照:0.31% eGFP
D3 eGFP水平:培养对照:0.064% eGFP
D4 eGFP水平:培养对照:0.24% eGFP
这些数据进一步证实,当使用供体切割时,编辑效率会提高。
图19中示出了来自在D2时注射了通过scAAV6 0切口或scAAV6 2切口的NHEJ介导的靶向整合在D1时进行编辑的人CD34
在这个研究中,NHEJ介导的靶向整合方案得到了进一步优化。对通过NHEJ-TI修饰的CD34
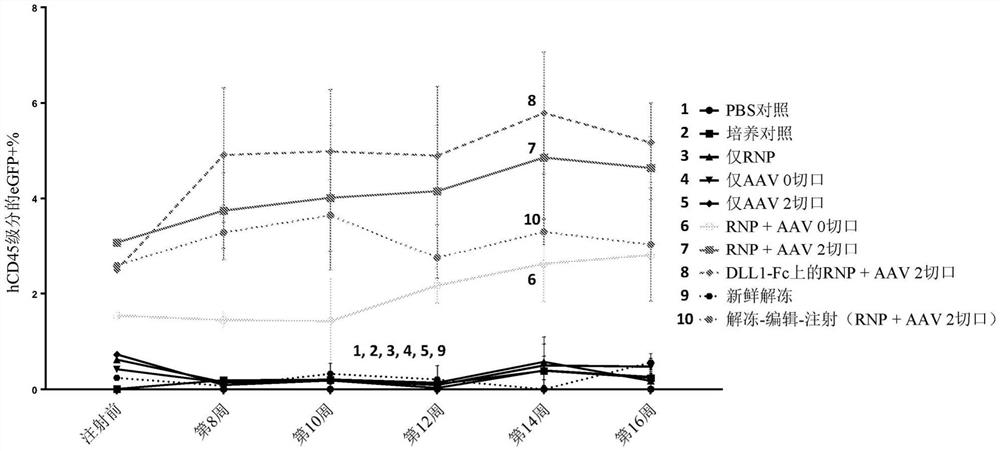
在这个实验中,使用了三十六只小鼠:1)PBS对照:三只小鼠;2)培养对照:三只小鼠;3)仅RNP:三只小鼠;4)仅scAAV6 0切口:三只小鼠;5)仅scAAV6 2切口:三只小鼠;6)RNP+scAAV6 0切口:四只小鼠;7)RNP+scAAV6 2切口:四只小鼠;8)DLL1涂覆板上的RNP+scAAV62切口:四只小鼠;9)新鲜解冻:三只小鼠;10)RNP+scAAV62切口(D0编辑-解冻-注射):四只小鼠。
在D1+1条件下使用一百万个CD34
RNP包含Cas9(Feldan):AAVS1引导RNA(SEQ ID NO:8)(Synthego),比率为50∶250pmol。以50,000vg/细胞的MOI使用scAAV6 0切口NHEJ载体(SEQ ID NO:4)(载体生物实验室)和scAAV6 2切口NHEJ载体(SEQ ID NO:5)(载体生物实验室),以2×10
按照制造商的建议,将Lonza 4D
研究中所使用的实验时间线如下。第0天(D0):将细胞解冻;D1+1注射:4000万个CD34+细胞(GCSF动员的)。第1天(D1):D1+1对细胞进行操控;RNP和scAAV6感染的核转染。第2天(D2):对小鼠进行注射;早晨-以200cGy对小鼠进行辐照;D0解冻-编辑-注射条件:对细胞进行操控;下午-D1+1条件:对小鼠进行注射;D0条件:对小鼠进行注射。第8、10、12和14周:中期放血。第16周:终点分析。
细胞培养
使用前立即将等分的培养基和细胞因子解冻。将解冻的细胞因子和小分子添加到SFEM II以产生完全培养基,将所述完整培养基温热到37℃。将足够用于1,600,000个细胞/小鼠的hCD34
RNP核转染
将Lonza 4D
AAV感染
将AAV在冰上解冻。将解冻的细胞因子和小分子在使用前立即添加到SFEM II以产生完全培养基,将所述完全培养基温热到37℃,在此期间,在低结合蛋白管中制备AAV稀释液。通过将750μl或1ml完全培养基和对应量的AAV稀释液添加到T75烧瓶来制备培养烧瓶。将600μl的经核转染的细胞(添加有500μl的拯救培养基)从转染烧瓶转移到所制备的AAV感染培养烧瓶中,并将细胞放置回加湿的37℃缺氧温育箱中持续六小时。然后将细胞转移到15ml锥形管并以90xg旋转10分钟,抽吸上清液,并将细胞重悬于7.5ml或10ml培养基中并转移到T75烧瓶以继续培养过夜、保留等分试样的细胞继续培养以进行编辑分析。
将细胞收集并在15ml锥形管中沉淀,抽吸上清液,并将细胞重悬于165μl或220μl注射缓冲液(PBS+0.5%BSA)中。将10μl细胞等分试样以1∶100稀释,并使用Vi-Cell对其进行计数。将剩余的细胞保持在冰上,直到注射的时间为止。
DLL1-Fc条件特异性方案:1)如先前在实例9中所描述的,用DLL1-Fc涂覆T75烧瓶;2)将细胞解冻并在DLL1-Fc涂覆板上培养过夜;3)为了分离细胞进行操控,收集上清液,对板进行洗涤并将其与1mM含EDTA的PBS一起温育5分钟,温育两次;4)如上文所描述的对细胞进行编辑;5)RNP核转染后,在新的DLL1-Fc涂覆的T75烧瓶中进行AAV感染;6)将细胞培养过夜;7)如上文所描述的制备细胞以进行注射,但是再次对板进行洗涤并将其在1mM含EDTA的PBS中温育5分钟,温育两次。
解冻-编辑-注入条件特异性方案:1)将细胞在注射的当天解冻;2)将细胞在低附着T75烧瓶中的完全培养基中静置一小时;3)如上文所描述的对细胞进行操控;4)AAV感染两小时后,将细胞收集而不是稀释,并制备细胞以进注射。
每只小鼠接受所需数量的细胞(对于培养对照和新鲜解冻,500,000个细胞/小鼠,对于其他条件,1,000,000个细胞/小鼠)。结果示于图21、图22A-22D、图23A-23D、图24A-24D、图25A-25D、图26A-26D、图27A、图27B、图28A-28C和图29A-29C。
细胞的初始编辑效率如下:培养对照:0.01%GFP
16周后骨髓移植百分比:培养对照:38%±27%hCD45
16周后骨髓GFP
序列表
- 用于进行NHEJ介导的基因组编辑的组合物和方法
- 用于通过单倍体诱导来进行基因组编辑的方法和组合物
