一种印第安纳沙门氏菌SInCYZ及其应用
文献发布时间:2024-04-18 19:58:21
技术领域
本发明属于生物工程技术领域,具体涉及一种印第安纳沙门氏菌SInCYZ及其在细菌适应性研究的应用。
背景技术
细菌的适应性(fitness)是指细菌为了适应不同的生存环境(如抗生素、温度、渗透压、pH等)进而繁衍后代,包括侵袭力、致病能力和生长能力都发生较大改变,目前关于细菌适应性研究主要集中在耐药细菌的适应性代价(fitnesscost)。对于细菌适应性的评价,其“黄金标准”是竞争性实验,通常按照不同生长环境又可分为体外竞争或体内竞争。体外竞争一般在培养基中进行,需将耐药菌和敏感菌按比例混合培养,一定时间后测定两种细菌数量的变化,计算竞争指数,进而评价细菌的适应性。体内竞争主要是设计动物感染模型,通过测定脏器中不同细菌的数量来评价适应性。细菌竞争性实验需选取具有特定耐药性标签的菌株和不具有该耐药性的敏感菌株,方便筛选计数。但对于革兰氏阴性菌而言,由于其耐药性通常是由可接合型耐药质粒介导,极易发生水平转移,如果选用含耐药质粒的革兰氏阴性菌进行竞争性实验,容易导致敏感菌获取耐药质粒后无法通过抗性培养基进行筛选区分。
印第安纳沙门氏菌是近年来在我国逐步流行的一种沙门氏菌血清型,其主要特征是具有广泛流行性和多重耐药性,因而对该病原进行适应性研究具有重要的科学意义。然而研究表明,目前我国流行的印第安纳沙门氏菌通常含有大型耐药质粒(PrevalenceandantimicrobialresistanceofSalmonellaentericaserovarIndianainChina(1984–2016).Zoonoses andPublicHealth.2017;64:239–251),由于此类耐药质粒接合效率较高,因而不适合开展印第安纳沙门氏菌的适应性研究。
发明内容
本发明的目的在于提供一株可用于印第安纳沙门氏菌适应性研究的参考菌株,可以用于评价细菌在体外或体内适应能力的差异。
本发明技术方案如下:
一种印第安纳沙门氏菌SInCYZ,是从历年来收集、保存的600余株印第安纳沙门氏菌菌种中,经多年反复筛选验证后获得的一株不含质粒的多重耐药菌株,其遗传性状稳定,不与其它细菌发生耐药基因水平转移,可用作印第安纳沙门氏菌适应性研究的参考菌株。
印第安纳沙门氏菌SInCYZ(SalmonellaIndianaSInCYZ)已于2023年5月12日送中国典型培养物保藏中心(中国.武汉.武汉大学)保藏,名称及鉴别特征:印第安纳沙门氏菌(SalmonellaIndiana),株号:SInCYZ,保藏编号:CCTCCNO.M2023745。
本发明的提供了所述的印第安纳沙门氏菌用于细菌适应性研究的应用。
本发明提供的印第安纳沙门氏菌SInCYZ具有遗传性状稳定,抗性标记丰富,不与其它细菌发生耐药基因水平转移,可以广泛用于印第安纳沙门氏菌竞争性实验的参考菌株。
附图说明
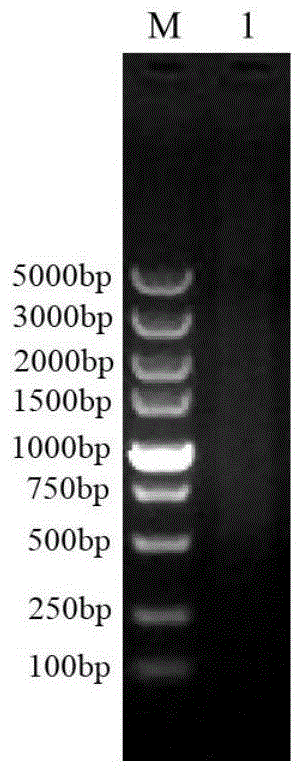
图1为实施例1中抽提质粒的琼脂糖凝胶电泳检测结果。图中:M为TakaraDNA分子量标准Marker(100~5000bp),泳道1为SInCYZ;
图2为实施例1中S1-PFGE的检测结果。图中:M为PFGEMarker,泳道1为SInCYZ;
图3为实施例2中SInCYZ的PCR-RFLP琼脂糖凝胶电泳检测结果。图中:M为DL-2000marker,泳道1为SInCYZ(酶切前),泳道2为ATCC51959(酶切前),泳道3为SInCYZ(酶切后),泳道4为ATCC51959(酶切后),泳道5为空白对照。
具体实施方式
下面结合实施例和附图对本发明做进一步的说明,以下所述,仅是对本发明的较佳实施例而已,并非对本发明做其他形式的限制,任何熟悉本专业的技术人员可能利用上述揭示的技术内容加以变更为同等变化的等效实施例。凡是未脱离本发明方案内容,依据本发明的技术实质对以下实施例所做的任何简单修改或等同变化,均落在本发明的保护范围内。
实施例1印第安纳沙门氏菌SInCYZ生物学特性研究
1)分离纯化与染色镜检
印第安纳沙门氏菌SInCYZ菌株于2014年12月从江苏省扬州市的发病肉鸡盲肠中分离所得。其具体分离方法为:无菌采集盲肠样品加入SBG磺胺增菌液中37℃过夜培养,再接种木糖赖氨酸脱氧胆盐琼脂37℃过夜培养,挑取带金属光泽黑色中心的菌落,接种于LB琼脂培养基,37℃培养24小时。将纯培养后的细菌进行革兰氏染色镜检,然后用光学显微镜观察,呈两端稍圆的细长杆菌。
2)生化鉴定
从LB琼脂平板上挑取菌落,进行生化鉴定试验。微量生化鉴定管购自杭州微生物试剂有限公司,按照说明书进行操作。结果菌株的各项生化指标(见表1)均符合沙门氏菌的生化特性。
表1.SInCYZ生化鉴定结果
3)血清学分型
从LB琼脂平板上挑取菌落至生理盐水中,用比浊法调整细菌浓度至每毫升1.0×10
表2.SInCYZ血清学分型结果
注:“+”代表发生凝集,“-”代表未发生凝集。
4)耐药性测试
采用肉汤稀释法结合纸片扩散法,测试SInCYZ对常见药物敏感性,根据Clinicaland LaboratoryStandardsInstitute(CLSI),USNationalAntimicrobialResistanceMonitoringSystem(NARMS)和EuropeanCommitteeonAntimicrobialSusceptibilityTesting(EUCAST)等国际细菌耐药性检测标准进行结果判定。结果见表3,由表可见SInCYZ对氨苄西林、头孢唑啉、头孢噻肟、头孢曲松、头孢他啶、氨曲南、链霉素、庆大霉素、卡那霉素、阿米卡星、四环素、萘啶酸、环丙沙星、磺胺异恶唑、甲氧苄啶、甲氧苄啶/磺胺异恶唑、氯霉素和利福平共18种药物具有抗药性。
表3.SInCYZ耐药性测试结果
5)质粒检测
将SInCYZ经LB肉汤增菌后,使用细菌基因组DNA提取试剂盒(天根生化科技(北京)有限公司)提取细菌基因组DNA进行Illumina测序,同时将灭活的细菌进行Pacbio测序(均由南京派森诺基因科技有限公司完成),上述序列拼接后发现该菌株只有染色体序列,但没有发现质粒序列。进一步将SInCYZ序列通过质粒在线查找工具PlasmidFinder(http://cge.cbs.dtu.dk/services/PlasmidFinder/)检索后仍未发现质粒信息。进一步使用质粒小提试剂盒(天根生化科技(北京)有限公司)或通过S1-PFGE方法也未能在SInCYZ菌株中发现任何质粒(图1、2)。
6)耐药基因水平转移
选取SInCYZ作为供体菌,C600和EC600作为受体菌,分别采用肉汤接合法和滤膜接合法进行耐药基因水平转移实验,所有实验均重复三次,只要有一次转移成功即判定可以水平转移。配置不同抗性组合的平板进行筛选,每种平板均含2种抗生素,C600为受体菌的使用高浓度链霉素(2mg/ml)加另外一种抗生素筛选,EC600为受体菌的使用高浓度利福平(2.5mg/ml)加另外一种抗生素筛选,结果如表4所示。可以发现无论使用哪种受体菌、接合方法或筛选药物均未发现SInCYZ发生耐药基因的水平转移。
表4.SInCYZ耐药基因水平转移测试
注:“-”:阴性,“/”:未测试,AMP:氨苄西林,CTX:头孢噻肟,ATM:氨曲南,STR:链霉素,KAN:卡那霉素,TET:四环素,CIP:环丙沙星,SUL:磺胺异恶唑,CHL:氯霉素,RIF:利福平。
7)遗传稳定性测试
使用LB肉汤对SInCYZ进行连续过夜传代,每传5代接种1次LB琼脂,从琼脂上随机挑选10个菌落按药敏试验要求测试耐药性状。累计传100代,接种20次LB琼脂,测试200个菌落的耐药性状,结果所有菌落均与原代细菌具有相同的耐药性,表明SInCYZ具有良好的遗传稳定性。
实施例2SInCYZ与ATCC51959的肉汤培养竞争实验
将SInCYZ与印第安纳沙门氏菌ATCC51959冻干菌种复苏后在琼脂平板划线培养,挑选单克隆菌株分别接种LB试管肉汤,37℃摇床培养至对数中期,分别以1:1比例接种LB锥形瓶肉汤,37℃、200r/m震荡培养,24h后将混合菌液在灭菌生理盐水中依次进行10倍倍比稀释,取100μl分别在LB琼脂平板、含氯霉素的LB琼脂平板上铺板,37℃过夜培养计数,试验设置3个平行。含氯霉素的LB琼脂平板的菌数即为SInCYZ菌数,LB琼脂平板的菌数落减去含氯霉素的LB琼脂平板的菌数即为ATCC51959菌数。
此外,根据SInCYZ与ATCC51959基因组序列差异,建立一种鉴别上述2种细菌的PCR-RFLP方法,其中扩增引物为F:5-GCGCGTCTGGACATTTGATA-3,R:5-GAATTCGGCTTTGCTCAAGTC-3;扩增条件:94℃预变性5min;94℃变性30s;58℃退火30s;72℃延伸30s;共30个循环,最后72℃延伸8min;将扩增产物用SspI限制性内切酶进行酶切后,进行琼脂糖凝胶电泳检测。结果如图3所示,SInCYZ因含有SspI酶切位点,其扩增产物可以被酶切为215bp和422bp两个条带,而ATCC51959因没有该酶切位点所以仍为一个条带(637bp)。通过该方法对抗性平板上随机挑选的菌落进行检测,进一步验证结果的准确性。
根据结果统计竞争指数W=ln(RF/RI)/ln(SF/SI),RI和SI表示0h菌液中耐药菌(SInCYZ)和敏感菌(ATCC51959)的数量,RF和SF表示24h菌液中耐药菌和敏感菌的数量。经统计W=0.42,表明在肉汤培养竞争实验中,SInCYZ的适应性弱于ATCC51959。
实施例3SInCYZ与ATCC51959对肠上皮细胞入侵的竞争实验
将鼠肠上皮细胞IEC-6按1×10
根据结果统计竞争指数W=ln(RF/RI)/ln(SF/SI),RI和SI表示接种菌液中耐药菌(SInCYZ)和敏感菌(ATCC51959)的数量,RF和SF表示孵育后细胞内耐药菌和敏感菌的数量。经统计W=1.25,表明在肠上皮细胞入侵的竞争实验中,SInCYZ的适应性强于ATCC51959。
实施例4SInCYZ与ATCC51959在巨噬细胞内生存的竞争实验
将鼠巨噬细胞RAW264.7按1×10
根据结果统计竞争指数W=ln(RF/RI)/ln(SF/SI),RI和SI表示接种菌液中耐药菌(SInCYZ)和敏感菌(ATCC51959)的数量,RF和SF表示孵育后细胞内耐药菌和敏感菌的数量。经统计W=1.07,表明在巨噬细胞内生存的竞争实验中,SInCYZ的适应性强于ATCC51959。
实施例5SInCYZ与ATCC51959对小鼠感染的体内竞争实验
将SInCYZ与ATCC51959菌液以1:1比例混合后用灭菌PBS进行倍比稀释至约为2.5×10
尽管已经示出和描述了本发明的实施例,对于本领域的普通技术人员而言,可以理解在不脱离本发明的原理和精神的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由所附权利要求及其等同物限定。
- 一种鸡伤寒沙门氏菌弱毒分离株及其应用
- 一种快速检测畜禽粪便中印第安纳沙门氏菌的LAMP试剂盒
- 一种印第安纳沙门氏菌PCR检测试剂盒及其非诊断性检测方法
