含有脐带血单个核细胞培养上清的脑神经损伤治疗剂
文献发布时间:2023-06-19 19:23:34
技术领域
本发明涉及一种含有脐带血单个核细胞培养上清的脑损伤治疗剂。
背景技术
围产期的新生儿脑损伤是一种疾病,每1000名新生儿中就会有1~2人并发,这种疾病会导致此后的终身脑性瘫痪,不仅对本人,对抚养家庭也会造成沉重的负担。
导致脑性瘫痪的围产期脑损伤包括缺氧缺血性脑病、脑出血、脑室周围白质软化等,这些主要病症的炎症病症是细胞内Ca升高、线粒体功能障碍引起的活性氧升高、巨噬细胞活化及伴随其的高细胞因子血症。早产儿尤其容易并发脑出血,症状最重,生命预后差。
低温疗法被认为是一种有效的治疗方法,但据说在接受治疗的8~9名儿童中只有1名有效。并且,目前除了低温疗法外,没有确定的治疗方法。
到目前为止,已经推进了将自体骨髓来源的间充质干细胞直接给予脑性瘫痪患者的临床研究,并报道了其有效性(非专利文献1)。另外,虽然有给予脐带来源细胞的报道,但一部分运动机能并没有得到显著改善(非专利文献2)。并且,有报告称,通过向新生儿脑出血模型小鼠给予脐带血来源细胞,显著改善了运动机能障碍(专利文献1)。
现有技术文献
非专利文献
非专利文献1:Cytotherapy 2013Dec;15(12):1549-62
非专利文献2:Cytotherapy 2015 17(2):224-231
专利文献
专利文献1:国际公开第2017/204231号。
发明内容
发明要解决的技术问题
在由脑出血或缺血等引起的脑神经损伤中,不仅要治疗出血或缺血,还要促进由于该原因而受损的神经细胞等的保护或再生。为了此类神经细胞等的保护或再生,考虑给予脐带来源的细胞,但根据从脐带采集的方法、所得的细胞特性也不同,从而不清楚来自脐带的所有细胞是否都会有这种效果。另外,在脑神经损伤中,虽然设想通过腰椎穿刺进行蛛网膜下腔给药,但是这种给药方法具有高风险,因此提供一种给药途径更容易且有效的治疗剂成为问题。
解决技术问题的技术方案
本发明人为解决上述问题进行了深入的研究,结果发现,脐带血单个核细胞的培养上清通过促进脑神经干细胞向脑损伤部位的归巢、脑神经干细胞的分化和成熟,可以再生脑神经,且对脑神经损伤有效,从而完成了本发明。
即,本发明涉及以下内容:
(1)一种脑神经损伤治疗剂,该治疗剂含有脐带血单个核细胞的培养上清作为有效成分。
(2)如(1)所述的脑神经损伤治疗剂,其中,所述培养上清中含有细胞因子和趋化因子。
(3)如(1)或(2)所述的脑神经损伤治疗剂,其中,含有IL-6、CXCL1、CXCL7、CXCL8和CCL2。
(4)如(1)~(3)中任一项所述的脑神经损伤治疗剂,其中,所述培养上清是将脐带血单个核细胞培养1~3天得到的。
(5)如(1)~(4)中任一项所述的脑神经损伤治疗剂,其中,培养开始时的脐带血单个核细胞的密度为5×10
(6)如(1)~(5)中任一项所述的脑神经损伤治疗剂,其中,所述脑神经损伤不是遗传性疾病。
(7)如(1)~(6)中任一项所述的脑神经损伤治疗剂,其中,所述脑神经损伤为运动障碍(左旋多巴诱导的异动症、慢性或迟发性运动障碍、或口面运动障碍)、下肢不宁综合征(药物诱发性或特发性)、药物诱发性肌张力障碍、舞蹈病(亨廷顿病、毒素诱发性舞蹈病、小舞蹈病(Sydenham)、妊娠舞蹈病、威尔逊病、药物诱发性舞蹈病、或代谢性或内分泌性舞蹈病)、面部痉挛(运动性、言语性、简单性、复杂性或图雷特综合征等)、肌张力障碍(急性、全身性、局灶性、节段性、性、中间性、心因性或急性肌张力障碍反应等)、Sodemytopic帕金森病、刻板运动障碍(自闭症、遗传性或儿童相关运动障碍等)、强迫性障碍、嗜睡症(猝倒等)、传染性海绵状脑病(克罗伊茨费尔特-雅各布病或库鲁病等)、痴呆症(阿尔茨海默病、路易体痴呆、血管性痴呆、匹克氏病或酒精性痴呆等)、神经棘红细胞增多症、发作或痉挛、手足徐动症(亨廷顿病、呼吸停止、新生儿黄疸或脑卒中相关等)、或儿童脑性瘫痪。
(8)一种(1)~(7)中任一项所述的脑神经损伤治疗剂的制造方法,该方法包括a:培养脐带血单个核细胞的工序;以及b:回收所述脐带血单个核细胞的培养上清的工序。
(9)一种药物组合物,该组合物包含(1)~(7)中任一项所述的脑神经损伤治疗剂。
(10)如(9)所述的药物组合物,其中,该组合物为冻干制剂。
(11)一种脑神经再生促进剂,该促进剂含有脐带血单个核细胞的培养上清作为有效成分。
(12)如(11)所述的脑神经再生促进剂,其中,所述脑神经再生促进剂为脑神经前体细胞增殖促进剂、脑神经前体细胞归巢促进剂、脑神经前体细胞分化成熟促进剂、或它们的组合。
(13)如(11)或(12)所述的脑神经再生促进剂,其中,所述培养上清中含有细胞因子和趋化因子。
(14)如(11)~(13)中任一项所述的脑神经再生促进剂,其中,含有IL-6、CXCL1、CXCL7、CXCL8和CCL2。
(15)如(11)~(14)中任一项所述的脑神经再生促进剂,其中,所述培养上清是将脐带血单个核细胞培养1~3天得到的。
(16)如(11)~(15)中任一项所述的脑神经再生促进剂,其中,培养开始时的脐带血单个核细胞的密度为5×10
(17)如(11)~(16)中任一项所述的脑神经再生促进剂,其中,所述脑神经再生发生于非遗传性疾病的脑神经损伤中。
(18)如(11)~(17)中任一项所述的脑神经再生促进剂,其中,所述脑神经再生发生于运动障碍(左旋多巴诱导的异动症、慢性或迟发性运动障碍、或口面运动障碍)、下肢不宁综合征(药物诱发性或特发性)、药物诱发性肌张力障碍、舞蹈病(亨廷顿病、毒素诱发性舞蹈病、小舞蹈病、妊娠舞蹈病、威尔逊病、药物诱发性舞蹈病、以及代谢性和内分泌性舞蹈病)、面部痉挛(运动、言语、简单、复杂以及图雷特综合征等)、肌张力障碍(急性、全身性、局灶性、节段性、性、中间性、心因性以及急性肌张力障碍反应等)、Sodemytopic帕金森病、刻板运动障碍(自闭症、遗传性以及儿童相关运动障碍等)、强迫性障碍、嗜睡症(猝倒等)、传染性海绵状脑病(克罗伊茨费尔特-雅各布病以及库鲁病等)、痴呆症(阿尔茨海默病、路易体痴呆、血管性痴呆、匹克氏病、酒精性痴呆等)、神经棘红细胞增多症、发作以及痉挛、手足徐动症(亨廷顿病、呼吸停止、新生儿黄疸以及脑卒中相关等)、或儿童脑性瘫痪中。
(19)一种(11)~(18)中任一项所述的脑神经再生促进剂的制造方法,该方法包括a:培养脐带血单个核细胞的工序;以及b:回收所述脐带血单个核细胞的培养上清的工序。
(20)一种药物组合物,该组合物包含(11)~(18)中任一项所述的脑神经再生促进剂。
(21)如(20)所述的药物组合物,其中,该组合物为冻干制剂。
发明效果
根据本发明,可以提供一种含有脐带血单个核细胞培养上清的脑神经损伤治疗剂。通过混合多个供体的细胞培养上清,本制剂可制成均质的脑神经损伤治疗剂,且与含有细胞的制剂相比,更易于制造、储存、给药。
附图的简单说明
图1显示了脐带血单个核细胞和神经前体细胞共培养的神经再生。与(1)单独培养相比,(2)共培养时,在培养的第3天和第7天,神经前体细胞的增殖、存活、移动(迁移)、分化和成熟增强。
图2显示了脐带血单个核细胞培养上清的神经再生(体外)。与仅添加(1)培养基相比,添加(2)培养上清时,在培养的第3天和第7天,神经前体细胞的增殖、存活、移动(迁移)、分化和成熟增强。
图3显示了脐带血单个核细胞培养上清的神经再生(脑室下带)。与仅给予(1)培养基相比,将(2)培养上清给予缺氧处理儿童脑性瘫痪模型小鼠时,脑室下带的神经前体细胞的增殖增强((a)、(b)vs(c)、(d))。
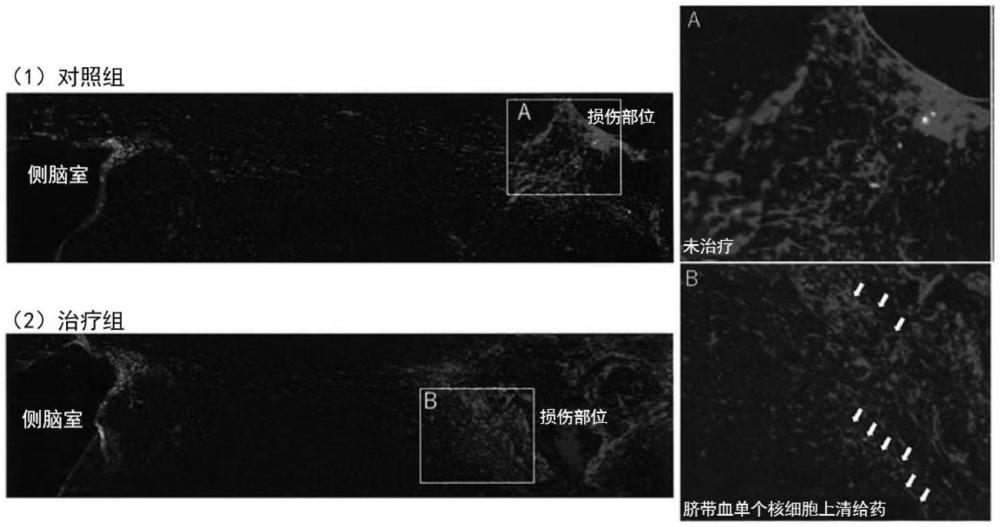
图4显示了脐带血单个核细胞培养上清的神经再生(脑损伤部位)。与仅给予(1)培养基相比,将(2)培养上清给予缺氧处理儿童脑性瘫痪模型小鼠时,神经前体细胞向脑损伤部位周围的归巢、以及脑损伤部位周围的神经前体细胞向神经元的分化和成熟增强。((B)箭头)。
具体实施方式
以下将根据具体的实施方式对本发明进行详细说明。但是,本发明并不限于以下的实施方式,在不脱离本发明精神的范围内,本发明可以任意的方式实施。
另外,本发明中引用的专利公报、专利申请公开公报、以及非专利文献等,出于所有目的,其整体通过引用并入本发明。
本发明中,适用于数值的“~”是指在规定的参考值以上、且在规定的参考值以下的范围内的数值范围。
脐带血单个核细胞
本发明中,“脐带”是连接胎儿和胎盘的白色管状组织,表示不含胎盘的组织。本发明的脐带没有特别限制,只要是取自哺乳动物的脐带即可,例如灵长类哺乳动物的脐带。更优选人的脐带。
本发明中,“脐带血”是指脐带中含有的胎儿血,“人脐带血”是指可以从人脐带获得的血液。人脐带血可以从阴道分娩和剖腹产分娩的、包括胎盘和脐带的产后组织中适当地去除胎盘并回收的脐带制备。另外,人脐带血也可以从脐带血库获得,例如,兵库脐带血库。
本发明中,“脐带血单个核细胞”是指脐带血所含细胞中的单个核细胞。脐带血单个核细胞可以从脐带血中分离出来,该分离方法包括比重离心法(例如可以使用Lympholye、Ficoll-Paque、Percoll、Lymphoprep)、使用细胞分选仪的方法、使用抗体的免疫磁分离法、免疫比重离心法等。并且,也可以使用透析膜从脐带血中分离单个核细胞。此外,也可以使用全血单个核细胞浓缩用纯细胞分选系统(Pure Cell Select System;注册商标,PALL)、血细胞除去用净化器(Cellsorba E,注册商标,旭化成)和血小板制剂用白细胞除去过滤器(Sepacell PL,注册商标,PLX-5B-SCD、旭化成)等,但没有特别限制。与脐带血来源的各种干细胞不同,脐带血单个核细胞不需要继代培养或详细的细胞分级分离,易于制备。
2.培养上清的制备
脐带血单个核细胞的“培养”可以按照常规方法进行,例如以下方式。在培养容器中,根据需要在含有钠、钾、钙、镁、磷、氯、氨基酸、维生素、激素、细胞因子、抗生素、脂肪酸、糖或根据目的添加的其他化学成分、或血清等生物成分的基础培养基中加入脐带血单个核细胞,在CO
只要不抑制脐带血单个核细胞的增殖、维持和存活、蛋白质的分泌等,可以使用任何培养基(也称为培养液)。另外,除Dulbecco改良Eagle培养基(DMEM)外,Iscove改良Dulbecco培养基(IMDM)、HamF12培养基(HamF12)、RPMI1640培养基等可以用作基础培养基。并且,也可以并用两种以上的基础培养基。作为混合培养基的一例可例举等量混合IMDM和HamF12的培养基(例如,IMDM/HamF12)。另外,作为可以添加到培养基中的成分,可例举血清(胎牛血清、人血清、马血清、绵羊血清等)、血清替代物(Knockout血清替代物等)、各种条件培养基、牛血清白蛋白、人血清白蛋白、抗生素、各种维生素、深层海水和各种矿物质。
本发明中,用于制备脑神经损伤治疗剂的脐带血单个核细胞的培养基优选不含血清的培养基。不含血清可以防止朊病毒等的感染风险,并防止混入牛血清白蛋白等异源蛋白质,从而提高脑神经损伤治疗剂的安全性。例如,通过在不含血清的培养基(无血清培养基)中培养脐带血单个核细胞,可以制备不含血清成分的培养上清。
本发明中,用于制备脑神经损伤治疗剂的培养基可以含有深层海水。“深层海水”一般是指超过200米深度的海水,据说它起源于格陵兰岛周围由于盐度差异引起的垂直下沉的、称为“羽流”的全球洋流,它在地球上循环了几个世纪,从未与大气接触过。由于该深层海水几乎不受阳光照射,并且处于低温高压的状态,因此细菌少,且富含无机营养盐(矿物质)等。通过含有深层海水,可以调整培养上清的分泌蛋白量,与不含深层海水的情况相比,可以制备活性更高的脑神经损伤治疗剂。培养基中所含深层海水的浓度(v/v),例如为1%、2%、3%、4%、5%、6%、7%、8%、9%、10%、15%、20%、25%、30%、40%、50%、60%、70%或80%以上;以及90%、80%、70%、60%、50%、45%、40%、35%、30%、25%、20%、15%或10%以下;1~85%、5~85%、10%~85%、15%~85%、20%~85%、25%~85%、30%~85%、40%~85%、50%~85%、60%~85%、70%~85%、80%~85%、1~75%、5~75%、10%~75%、15%~75%、20%~75%、25%~75%、30%~75%、40%~75%、50%~75%、60%~75%、70%~75%、1~45%、5~45%、10%~45%、15%~45%、20%~45%、25%~45%、30%~45%、40%~45%、1~10%或5~10%的范围;73%或81%。
获得脐带血单个核细胞的培养上清的培养时间,例如可以为5小时~7天、1天~6天、1天~5天、1天~4天、1天~3天或1天~2天,也可以为0.5天、1天、2天、3天、4天、5天、6天或7天。培养温度例如为36℃~38℃,例如为37℃,CO
为了获得脐带血单个核细胞的培养上清,培养开始时脐带血单个核细胞的密度,例如可以为1×10
培养后,通过分离去除细胞成分,即可得到脐带血单个核细胞的培养上清。本发明中,培养上清不仅是指从培养液中分离去除细胞成分而得到的上清本身,适当进行各种处理(例如离心处理、浓缩、溶剂置换、透析、冷冻、干燥、冷冻干燥、稀释、脱盐、保存等)的培养上清也包括在此范围内。培养上清的处理方法将在后面进行详细说明。本发明中,培养上清不含细胞成分。因此,本发明中的培养上清不含用于培养的脐带血单个核细胞,不是细胞医疗用组合物。
本发明中,脐带血单个核细胞在培养基中分泌细胞因子、趋化因子等。培养上清中所含的蛋白质,可例举对脑神经再生重要的Interleukin(IL)-6、C-X-C基序趋化因子配体(C-X-C Motif Chemokine Ligand、CXCL)1、CXCL7、CXCL8(也称为IL-8)和C-C基序趋化因子配体(CCL)2(也称为MCP-1)。
本发明中,脐带血单个核细胞的培养上清中还可以含有以下一种或两种以上蛋白质:
TNF超家族成员14(也称为LIGHT)、白细胞介素(IL)-1a、IL-1b、IL-2、IL-3、IL-4、IL-5、IL-7、IL-10、IL-12p40/70、IL-13、IL-15、IL-16、干扰素(IFN)-g、肿瘤坏死因子(TNF)-a、TNF-b等细胞因子;
C-X-C基序趋化因子配体(CXCL)1/2/3(也称为GROa/b/g)、CXCL6、CXCL9(也称为MIG)、CXCL10(也称为IP-10)、CXCL12(也称为SDF-1)、CXCL13、C-C基序趋化因子配体(CCL)1、CCL4、CCL5、CCL7、CCL8、CCL11、CCL13、CCL15、CCL17、CCL18、CCL20(也称为LARC)、CCL22、CCL23、CCL24、CCL26、C-X3-C基序趋化因子配体(CX3CL)1(也称为FKN)等趋化因子;
血管生成素、脑源性神经营养因子(BDNF)、表皮细胞生长因子(EGF)、成纤维细胞生长因子(FGF)-4、FGF-6、FGF-7、FGF-9、FMS样酪氨酸激酶3配体(FLT-3L)、胶质细胞源性神经营养因子(GDNF)、粒细胞-巨噬细胞集落刺激因子(GM-CSF)、粒细胞集落刺激因子(G-CSF)、肝细胞生长因子(HGF)、胰岛素样生长因子(IGF)-1、胰岛素样生长因子结合蛋白(IGFBP)-2、IGFBP-1、IGFBP-4、IGFBP-3、血小板衍生生长因子(PDGF)-BB、胎盘生长因子(PLGF)、转化生长因子(TGF)-b1、TGF-b2、TGF-b3、血小板生成素(TPO)、干细胞因子(SCF)、巨噬细胞集落刺激因子(M-CSF)、神经营养因子(NT)-3、NT-4、血管内皮生长因子(VEGF)-A等生长因子/相关因子;
瘦蛋白、白血病抑制因子(LIF)、巨噬细胞移动抑制因子(MIF)、骨桥蛋白(OPN)、骨保护素(OPG)、抑瘤素M(OSM)、金属蛋白酶组织抑制因子(TIMP)-1、TIMP-2等其他介质。
本发明中,脐带血单个核细胞的培养上清中可含的因子在以下方面对神经再生很重要。本发明的培养上清含有这些因子的一部分或全部,适合大脑或中枢神经的再生(Boruczkowski等人、Int.J.Mol.Sci.2019 20,2433;Watson等人、Neuroscience Letters2020 715,134533;Wang等人、Stem Cell Research&Therapy 2017 8,26;Baba等人、PLOSONE 2019 14(9)e0221111;Wang等人、Acta Medica Okayama 2012 66(6)429等):
a)神经前体细胞的增殖和存活:BDNF、CCL5、CXCL1、CXCL7、CXCL8、CX3CL1、EGF、FGF-9、G-CSF、IGF-1、IL-6、OPN等;
b)神经前体细胞的分化和成熟:BDNF、CCL11、CXCL1、CXCL7、CXCL9、CXCL12、CX3CL1、FGF-4、FGF-9、GDNF、GM-CSF、IL-1b、LIF、OPN、SCF、TGF-b3等;
c)神经前体细胞的迁移:CCL2、CCL11、CCL20、CXCL1、CXCL7、CXCL8、CXCL12、EGF、IGF-1等;
d)神经营养:GDNF、NGF、NT-4/5等;
e)星形胶质细胞的活性化等:BDNF、IFN-g、IL-1a、IL-1b等;
f)小胶质细胞的活性化等:CCL17、CXCL10、瘦蛋白等。
g)少突胶质细胞的再生等:CXCL1、CXCL7、CXCL8、CXCL12、CX3CL1、EGF、M-CSF、NT-4、IGFBP-4等;
h)血管生成:血管生成素、CCL2、CXCL5、CXCL6、CXCL7、CXCL8、Groa/b/c、HGF、IGF-1、IL-6、VEGF、SCF等;
i)抗炎症:CCL4、IL-10、IL-13、TGF-b2等。
本发明中,作为脐带血单个核细胞培养上清的、细胞因子和趋化因子(以及生长因子等)的混合物,可以作为脐带血单个核细胞培养上清的一部分、或从脐带血单个核细胞培养上清中分离出来的细胞因子和趋化因子(以及生长因子等)的混合物使用。从脐带血单个核细胞培养上清中分离出来的细胞因子和趋化因子(以及生长因子等)的混合物中,可以用一种或多种已知对应的基因重组等细胞因子和趋化因子(以及生长因子等)替换细胞因子和趋化因子(以及生长因子等)的一部分,或者也可以添加对应的基因重组等细胞因子和趋化因子(以及生长因子等)。
3.脑神经损伤治疗剂
本发明的脑神经损伤治疗剂通过含有脐带血单个核细胞的培养上清,对脑神经损伤起到再生神经组织的效果。这种程度的效果可以取代传统脐带血干细胞移植的部分或全部效果。另外,令人吃惊的是,本发明的脑神经损伤治疗剂通过促进脑室下带的神经前体细胞的增殖、向脑神经损伤部位的归巢、脑神经损伤部位的神经细胞的分化和成熟,对脑神经的神经组织起到普遍广泛的神经再生效果。因此,本发明的脑神经损伤治疗剂不限于特定的脑神经损伤,对于广泛的脑神经损伤,可以作为脑神经再生促进剂用于治疗脑神经损伤、减轻症状等。由于本发明的脑神经损伤治疗剂用在脑神经损伤发病之前,因此即使该脑神经损伤处于患病未知阶段,通过给药至对象也可以有效抑制对象的脑神经损伤的恶化。因此,通过习惯性地使用本发明的脑神经损伤治疗剂,可以在发病前治疗多方面的脑神经损伤,预防、延缓或减轻发病。即,本发明中,“治疗”的范围不仅包括根治脑神经损伤引起的症状和异常的处理,还包括即使不能根治,却减轻症状和异常、或者与不进行处理的情况相比延缓症状和异常的处理,还包括预防、延缓或减轻发病的处理。
由于本发明的脑神经损伤治疗剂促进神经再生,因此可适用于多方面的脑神经损伤。例如,脑神经损伤是非遗传性疾病的脑神经损伤。本发明的脑神经损伤治疗剂没有限制,可例举运动障碍(左旋多巴诱导的异动症、慢性和迟发性运动障碍、以及口面运动障碍)、下肢不宁综合征(药物引起以及特发性)、药物诱发性肌张力障碍、舞蹈病(亨廷顿病、毒素诱发性舞蹈病、小舞蹈病、妊娠舞蹈病、威尔逊病、药物诱发性舞蹈病、以及代谢性和内分泌性舞蹈病)、面部痉挛(运动性、言语性、简单性、复杂性以及图雷特综合征等)、肌张力障碍(急性、全身性、局灶性、节段性、性、中间性、心因性以及急性肌张力障碍反应等)、Sodemytopic帕金森病、刻板运动障碍(自闭症、遗传性以及儿童相关运动障碍等)、强迫性障碍、嗜睡症(猝倒等)、传染性海绵状脑病(克罗伊茨费尔特-雅各布病以及库鲁病等)、痴呆症(阿尔茨海默病、路易体痴呆、血管性痴呆、匹克氏病以及酒精性痴呆等)、神经棘红细胞增多症、发作以及痉挛、手足徐动症(亨廷顿病、呼吸停止、新生儿黄疸以及脑卒中相关等)、以及儿童脑性瘫痪。
所述脑神经损伤治疗剂的给药对象代表性的为靶组织具有损伤的人类患者,还设想适用于人以外的哺乳动物(包括宠物动物、家畜、实验动物。具体而言,例如,小鼠、大鼠、豚鼠、仓鼠、猴子、牛、猪、山羊、绵羊、狗、猫等)。
所述脑神经损伤的发生部位没有特别限制。所述疾病的发生部位为整个或部分大脑,大脑包括前脑和脑干,前脑具有大脑和间脑,脑干具有中脑和菱脑。大脑具有嗅脑、扁桃、纹状体、海马和大脑新皮层等,间脑具有上丘脑、丘脑、下丘脑、丘脑腹、脑下垂体、松果体和第三脑室等。中脑具有中脑盖、大脑脚、前顶盖和中脑水管,菱脑具有脑桥、小脑和延髓等。所述脑神经损伤的发生部位可以是这些部位的任何一个。
使用本发明的脑神经损伤治疗剂的治疗方法,包括鼻腔给予脐带血单个核细胞培养上清以修复大脑的损伤部位。根据本治疗方法,能够以微创方式有效地恢复因儿童脑性瘫痪等脑神经损伤而受损的部位。
4.制造方法
本发明还提供一种脑神经损伤治疗剂的制造方法,该方法包括
a:培养脐带血单个核细胞的工序,以及
b:回收所述脐带血单个核细胞的培养上清的工序。
该制造方法还可以包括对所述回收的培养上清进行选自离心处理、浓缩、溶剂置换、透析、冷冻、干燥、冷冻干燥、稀释和脱盐中的一种以上处理的工序。通过包括这样的工序,脑神经损伤治疗剂的处理、保存、运输变得容易。并且,所述制造方法还可以包括对所述回收的培养上清添加附加成分的工序。通过添加这样的附加成分,可以改变脑神经损伤治疗用组合物整体的物性,提高其特性。并且,所述制造方法还可以包括从脐带血制备脐带血单个核细胞体细胞的工序。对于各工序和附加成分等,本发明的脑神经损伤治疗剂的说明书中记载的事项直接适用。在包括对所述回收的培养上清进行选自离心处理、浓缩、溶剂置换、透析、冷冻、干燥、冷冻干燥、稀释和脱盐中的一种以上处理的工序、以及对所述回收的培养上清添加附加成分的工序两者的情况下,可以先进行两工序的任一者,在可能的情况下也可以同时进行。
在上述工序b中,回收脐带血单个核细胞的培养上清。例如,可以用滴液吸管、移液管等吸取培养液并回收。回收的培养上清直接或经过一种以上处理后用作本发明的脑神经损伤治疗剂的有效成分。上述处理的例子包括离心处理、浓缩、溶剂置换、透析、制剂化、冷冻、干燥、冷冻干燥、稀释、脱盐、保存(例如,4℃、-80℃)。另外,脐带血单个核细胞的培养上清无需复杂、高度的纯化即可达到预期效果。因此,本发明的脑神经损伤治疗剂可以通过简单的工序制造。不需要复杂的纯化工序也有利于避免纯化伴随的活性降低。
本发明的脐带血单个核细胞培养上清可源自来自多个供体的脐带血单个核细胞。即,可以混合培养来自多个供体的脐带血单个核细胞,并回收培养上清,也可以混合来自各个供体的脐带血单个核细胞的培养上清,也可以经过一种以上处理(离心处理、浓缩、溶剂置换、透析、制剂化、冷冻、干燥、冷冻干燥、稀释、脱盐、保存)后,混合来自各个供体的脐带血单个核细胞的培养上清。但是,由于本发明的脐带血单个核细胞培养上清可能发生过度的混合淋巴细胞反应,因此优选不混合培养来自多个供体的脐带血单个核细胞。另外,来自多个供体的脐带血单个核细胞的培养上清的优点在于它可以作为均质的脑神经损伤治疗剂生产。
<脐带血单个核细胞培养上清的浓缩方法>
本发明的脑神经损伤治疗用组合物可以制剂化。
用于制剂化的脐带血单个核细胞培养上清的浓缩方法,可以适用通常用于浓缩培养上清的方法。浓缩方法的示例可例举以下两种方法。
1.离心柱浓缩法
使用Amicon Ultra Centrifugal Filter Units-10K(Millipore制)浓缩培养上清。具体操作步骤如下。
(i)将培养上清(最多15mL)加入Amicon Ultra Centrifugal Filter Units-10K,以×4000g离心约60分钟,浓缩至200μL。
(ii)将培养上清等量的无菌PBS加入上述管中,再次以×4000g离心约60分钟,将基础液替换为PBS。
(iii)所得200μL溶液回收到微量试管中,得到浓缩脐带血单个核细胞培养上清。
2.乙醇沉淀浓缩法
通过乙醇沉淀法浓缩培养上清。具体操作步骤如下。
(i)向5mL培养上清中加入45mL的100%乙醇,混合,-20℃放置60分钟。
(ii)4℃,以x15000g离心15分钟。
(iii)除去上清液,加入10mL的90%乙醇,充分搅拌。
(iv)4℃,以x15000g离心5分钟。
(iii)除去上清液,将所得颗粒溶解于500μL无菌水,回收到微量试管中,作为浓缩脐带血单个核细胞培养上清。
<脐带血单个核细胞培养上清的冷冻干燥方法>
另外,本发明的脑神经损伤治疗剂中的脐带血单个核细胞培养上清也可以是经冷冻干燥的。由此,得到良好的保存稳定性。脐带血单个核细胞培养上清的冷冻干燥方法,可以适用通常用于冷冻干燥培养上清的方法。冷冻干燥方法的示例可例举例如以下方法。冷冻干燥制造的培养上清可以作为粉末制剂使用,或者用适当的溶剂如水重构后使用。
(i)将上述方法中得到的脐带血单个核细胞培养上清或浓缩脐带血单个核细胞培养上清在-80℃冷冻2小时至半天。
(ii)冷冻后,打开样品管的盖子,放入冷冻干燥机中。
(iii)冷冻干燥1~2天。
(iv)所得样本作为冷冻干燥的脐带血单个核细胞培养上清(可-80℃保存)。
5.药物组合物
根据适用对象的情况,在维持预期治疗效果的前提下,本发明的脑神经损伤治疗剂还可以含有其他附加成分作为药物组合物。附加可含的成分示例如下。
(i)生物可吸收材料
透明质酸、胶原蛋白、纤维蛋白原(例如,bolheal(注册商标))等可用作有机生物可吸收材料。
(ii)凝胶材料
凝胶材料优选使用生物相容性高的材料,可以使用透明质酸、胶原蛋白或纤维蛋白胶等。可以选择使用各种透明质酸和胶原蛋白,但优选采用适合本发明的脑神经损伤治疗剂的适用目的(适用组织)的透明质酸和胶原蛋白。使用的胶原蛋白优选可溶性的(酸溶性胶原蛋白、碱溶性胶原蛋白、酶溶性胶原蛋白等)。
(iii)其他
还可以含有制剂上可接受的其他成分(例如,载体、赋形剂、崩解剂、缓冲剂、乳化剂、助悬剂、镇痛剂、稳定剂、保存剂、防腐剂、生理盐水等)。赋形剂可以使用乳糖、淀粉、山梨醇、D-甘露醇、白砂糖等。崩解剂可以使用淀粉、羧甲基纤维素、碳酸钙等。缓冲剂可以使用磷酸盐、柠檬酸盐、乙酸盐等。乳化剂可以使用阿拉伯胶、海藻酸钠、黄芪胶等。助悬剂可以使用单硬脂酸甘油酯、单硬脂酸铝、甲基纤维素、羧甲基纤维素、羟甲基纤维素、十二烷基硫酸钠等。镇痛剂可以使用苯甲醇、氯丁醇、山梨糖醇等。稳定剂可以使用丙二醇、抗坏血酸等。保存剂可以使用苯酚、苯扎氯铵、苯甲醇、氯丁醇、对羟基苯甲酸甲酯等。防腐剂可以使用苯扎氯铵、对羟基苯甲酸、氯丁醇等。还可以含有抗生素、pH调节剂、生长因子(例如,表皮细胞生长因子(EGF)、神经生长因子(NGF)、脑源性神经营养因子(BDNF))等。
本发明的药物组合物的最终形态没有特别限制。形态的例子包括液体状(液状、凝胶状等)和固体状(包括粉末状、细粒、颗粒状等冻干制剂)。本发明的药物组合物可以具有适合吸入的形态,例如,可以通过喷雾器或扩散器雾化的液体形态。脑神经损伤的相关部位是大脑,考虑到血脑屏障的存在,本发明的脑神经损伤治疗用组合物期望采取能够鼻腔给药、脑室内给药或髓腔内给药的形式。例如,鼻腔给药可以以喷雾状或粉末状的形式进行。与使用脐带血单个核细胞和脐带血干细胞的情况相比,脐带血单个核细胞的培养上清在前期准备和储存方面具有优势,据说特别适合脑神经损伤急性期和亚急性期的治疗。此外,脐带血单个核细胞的培养上清非常有用,因为它不含细胞成分,可以克服免疫排斥的问题。
不过,在一些实施方案中,除了脐带血单个核细胞的培养上清外,本发明的脑神经损伤治疗剂还可以含有脐带血单个核细胞、脐带血干细胞、ES细胞、iPS细胞或间充质干细胞等,或者也可以与这些干细胞等组合使用。通过追加使用这些干细胞等,某些情况下可以提高治疗效果。
本发明还提供了一种在脑神经损伤发病前抑制对象脑神经损伤发病的方法,该方法包括以能够抑制所述脑神经损伤发病的有效量、向脑神经损伤发病前的对象给予本发明的脑神经损伤治疗剂。所述对象可以是人或人以外的哺乳动物(包括宠物动物、家畜、实验动物。具体而言,例如,小鼠、大鼠、豚鼠、仓鼠、猴子、牛、猪、山羊、绵羊、狗、猫等)。所述对象可以是被确定具有脑神经损伤发病风险的对象。这种风险可以通过基因诊断、系谱分析等确定。具有如下示例,例如,统计表明特定基因中特定等位基因或SNP的存在与感染特定疾病的概率相关。
只要以能维持预期的治疗效果为前提,本发明的脑神经损伤治疗剂的给药剂量没有限制,例如,换算成未处理的培养上清的量,为0.1mL/kg/日~100mL/kg/日、1mL/kg/日~100mL/kg/日或5mL/kg/日~100mL/kg/日,换算成未处理的培养上清的蛋白质的量,为0.1mg/kg/日~1000mg/kg/日,另外,也可以为1mg/kg/日~100mg/kg/日。并且,给药方法没有特别限制。例如,所述脑神经损伤治疗剂的给药优选为非口服给药,非口服给药可以是全身性给药也可以是局部给药。只要以能维持预期的治疗效果为前提,所述脑神经损伤治疗剂的给药方法没有限制,可例举静脉给药、动脉给药、门静脉给药、皮内给药、皮下给药、肌肉内给药、腹腔内给药、经肺给药(经肺吸收)、脑室内给药、髓腔内和鼻腔给药等。其中,优选微创的鼻腔给药。此外,根据脑室内给药、髓腔内和鼻腔给药,在脑神经损伤的治疗中特别有效,因为无需担心穿过血脑屏障的可能性。给药时间表,例如可以采用一天一次~几次、两天一次、或者三天一次等。在制定给药时间表时,可以考虑对象的性别、年龄、体重、病情等。
6.脑神经再生促进剂
本发明的脐带血单个核细胞培养上清是一种脑神经再生促进剂。“脑神经再生”可以指由于大脑中神经前体细胞的增加、分化和成熟而在神经修复或神经发育过程中发生的各种现象中的至少一种。因此,神经再生优选包括原有神经功能完全或部分恢复的现象。是否实现了有效的神经再生可以通过公知的方法来确认。例如,将具有神经损伤且给予神经再生促进剂的患病的人或家畜与具有神经损伤且未给予神经再生促进剂的患病的人或家畜进行比较,如果给予神经再生促进剂的患病的人或家畜的损伤神经功能的恢复程度较高,则可以判断已经实现了有效的神经再生。如下面的实施例所示,神经功能的恢复可以以对刺激的反应、运动功能、认知功能的恢复等为指标进行评价,运动功能的恢复,例如旋转杆实验(Oh等人、Exp.Mol.Med.201850(4),22;Kossatz等人、Front.Pharmacol.2018 9,376)、Y迷宫实验(Miedel等人、J.Vis.Exp.2017(123);Sarnyai等人、Proc.Natl.Acad.Sci.USA.2000 97(26),14731)、挂线试验(Aartsma-Rus等人、J.Vis.Exp.2014(85))等,可以用公知的方法检查。
神经再生发生于神经产生缺陷来源的细胞,可以发生于治疗对象部位本来就存在的细胞(内源性细胞),例如也可以发生于与神经再生促进剂一同移植的细胞(外源性细胞)。这些细胞可例举神经细胞、神经前体细胞、胚胎干细胞、诱导多能干细胞、间充质干细胞、血管内皮细胞、血管内皮前体细胞、造血干细胞等。
本发明的脐带血单个核细胞培养上清是一种脑神经再生促进剂,可以是一种脑神经前体细胞增殖促进剂。“脑神经前体细胞增殖促进剂”是促进脑内神经前体细胞增殖的药剂。是否实现了有效的脑神经前体细胞增殖可以通过公知的方法来确认。例如,如下面的实施例所示,可以通过添加脑神经前体细胞分化和成熟促进剂,观察脑或脑源性神经前体细胞的增殖情况来进行评价。神经前体细胞可以是从活体采集的细胞,也可以是从iPS等干细胞分化的细胞,也可以使用细胞系(例如A172、B65、C6、KS-1、N2A、PC12、SH-SY5Y、SKN-BE2、T98G、U251、U87、YH-13)。
本发明的脐带血单个核细胞培养上清是一种脑神经再生促进剂,可以是一种脑神经前体细胞归巢促进剂。“脑神经前体细胞归巢促进剂”是促进神经前体细胞向脑损伤部位归巢的药剂。是否实现了有效的脑神经前体细胞归巢可以通过公知的方法来确认。例如,将具有神经损伤且给予脑神经前体细胞归巢促进剂的患病的人或家畜与具有神经损伤且未给予脑神经前体细胞归巢促进剂的患病的人或家畜进行比较,如果在给予脑神经前体细胞归巢促进剂的患病的人或家畜中,观察到脑神经前体细胞从海马的颗粒细胞下带、脑室下带向脑损伤部位的移动较多的情况下,则可以判断已经实现了有效的脑神经前体细胞归巢。另外,在并用神经前体细胞等细胞进行给药的情况下,根据所给予的细胞在脑损伤部位的聚集情况,也可以进行同样的判断。如下面的实施例所示,脑神经前体细胞的归巢可以使用脑神经前体细胞的标记物(例如DCX(双皮质素)、SOX2(SRY(性别决定区Y)-box 2)、PAX6(配对box 6))为指标进行评价。
本发明的脐带血单个核细胞培养上清是一种脑神经再生促进剂,可以是一种脑神经前体细胞分化和成熟促进剂。“脑神经前体细胞分化和成熟促进剂”是一种促进脑内神经前体细胞轴突延伸、分化成熟为神经细胞的药剂。
是否实现了有效的脑神经前体细胞分化和成熟可以通过公知的方法来确认。例如,如下面的实施例所示,可以通过添加脑神经前体细胞分化成熟促进剂,观察脑或脑源性神经前体细胞的轴突延伸、或测定延伸的轴突长度来进行评价。神经前体细胞可以是从活体采集的细胞,也可以是从iPS等干细胞分化的细胞,也可以使用细胞系(例如A172、B65、C6、KS-1、N2A、PC12、SH-SY5Y、SKN-BE2、T98G、U251、U87、YH-13)。
本发明的脑神经再生促进剂包括细胞因子、趋化因子等。作为细胞因子、趋化因子等,可例举对脑神经再生重要的Interleukin(IL)-6、C-X-C基序趋化因子配体(CXCL)1、CXCL7、CXCL8(也称为IL-8)和C-C基序趋化因子配体(CCL)2(也称为MCP-1)。
本发明的脑神经再生促进剂还可以含有以下一种或两种以上蛋白质:
TNF超家族成员14(也称为LIGHT)、白细胞介素(IL)-1a、IL-1b、IL-2、IL-3、IL-4、IL-5、IL-7、IL-10、IL-12p40/70、IL-13、IL-15、IL-16、干扰素(IFN)-g、肿瘤坏死因子(TNF)-a、TNF-b等细胞因子;
C-X-C基序趋化因子配体(CXCL)1/2/3(也称为GROa/b/g)、CXCL6、CXCL9(也称为MIG)、CXCL10(也称为IP-10)、CXCL12(也称为SDF-1)、CXCL13、C-C基序趋化因子配体(CCL)1、CCL4、CCL5、CCL7、CCL8、CCL11、CCL13、CCL15、CCL17、CCL18、CCL20(也称为LARC)、CCL22、CCL23、CCL24、CCL26、C-X3-C基序趋化因子配体(CX3CL)1(也称为FKN)等趋化因子;
血管生成素、脑源性神经营养因子(BDNF)、表皮细胞生长因子(EGF)、成纤维细胞生长因子(FGF)-4、FGF-6、FGF-7、FGF-9、FMS样酪氨酸激酶3配体(FLT-3L)、胶质细胞源性神经营养因子(GDNF)、粒细胞-巨噬细胞集落刺激因子(GM-CSF)、粒细胞集落刺激因子(G-CSF)、肝细胞生长因子(HGF)、胰岛素样生长因子(IGF)-1、胰岛素样生长因子结合蛋白(IGFBP)-2、IGFBP-1、IGFBP-4、IGFBP-3、血小板衍生生长因子(PDGF)-BB、胎盘生长因子(PLGF)、转化生长因子(TGF)-b1、TGF-b2、TGF-b3、血小板生成素(TPO)、干细胞因子(SCF)、巨噬细胞集落刺激因子(M-CSF)、神经营养因子(NT)-3、NT-4、血管内皮生长因子(VEGF)-A等生长因子/相关因子;
瘦蛋白、白血病抑制因子(LIF)、巨噬细胞移动抑制因子(MIF)、骨桥蛋白(OPN)、骨保护素(OPG)、抑瘤素M(OSM)、金属蛋白酶组织抑制因子(TIMP)-1、TIMP-2等其他介质。
本发明中,用于制备脑神经再生促进剂的培养基可以含有深层海水。“深层海水”一般是指超过200米深度的海水,据说它起源于格陵兰岛周围由于盐度差异引起的垂直下沉的、称为“羽流”的全球洋流,它在地球上循环了几个世纪,从未与大气接触过。由于该深层海水几乎不受阳光照射,并且处于低温高压的状态,因此细菌少,且富含无机营养盐(矿物质)等。通过含有深层海水,可以调整培养上清的分泌蛋白量,与不含深层海水的情况相比,可以制备活性更高的脑神经损伤治疗剂。培养基中所含深层海水的浓度(v/v),例如为1%、2%、3%、4%、5%、6%、7%、8%、9%、10%、15%、20%、25%、30%、40%、50%、60%、70%或80%以上、以及90%、80%、70%、60%、50%、45%、40%、35%、30%、25%、20%、15%或10%以下、1~85%、5~85%、10%~85%、15%~85%、20%~85%、25%~85%、30%~85%、40%~85%、50%~85%、60%~85%、70%~85%、80%~85%、1~75%、5~75%、10%~75%、15%~75%、20%~75%、25%~75%、30%~75%、40%~75%、50%~75%、60%~75%、70%~75%、1~45%、5~45%、10%~45%、15%~45%、20%~45%、25%~45%、30%~45%、40%~45%、1~10%或5~10%的范围、73%或81%。
获得作为脑神经再生促进剂的、脐带血单个核细胞的培养上清的培养时间,例如可以为5小时~7天、1天~6天、1天~5天、1天~4天、1天~3天或1天~2天,也可以为0.5天、1天、2天、3天、4天、5天、6天或7天。培养温度例如为36℃~38℃,例如为37℃,CO
为了获得作为脑神经再生促进剂的、脐带血单个核细胞的培养上清,培养开始时脐带血单个核细胞的密度,例如可以为1×10
由于本发明的脑神经再生促进剂促进神经再生,因此可适用于多方面的脑神经损伤。例如,脑神经损伤是非遗传性疾病的脑神经损伤。本发明的脑神经损伤治疗剂没有限制,可例举运动障碍(左旋多巴诱导的异动症、慢性和迟发性运动障碍、以及口面运动障碍)、下肢不宁综合征(药物引起以及特发性)、药物诱发性肌张力障碍、舞蹈病(亨廷顿病、毒素诱发性舞蹈病、小舞蹈病、妊娠舞蹈病、威尔逊病、药物诱发性舞蹈病、以及代谢性和内分泌性舞蹈病)、面部痉挛(运动性、言语性、简单性、复杂性以及图雷特综合征等)、肌张力障碍(急性、全身性、局灶性、节段性、性、中间性、心因性以及急性肌张力障碍反应等)、Sodemytopic帕金森病、刻板运动障碍(自闭症、遗传性以及儿童相关运动障碍等)、强迫性障碍、嗜睡症(猝倒等)、传染性海绵状脑病(克罗伊茨费尔特-雅各布病以及库鲁病等)、痴呆症(阿尔茨海默病、路易体痴呆、血管性痴呆、匹克氏病以及酒精性痴呆等)、神经棘红细胞增多症、发作以及痉挛、手足徐动症(亨廷顿病、呼吸停止、新生儿黄疸以及脑卒中相关等)、以及儿童脑性瘫痪。
本发明还提供一种脑神经再生促进剂的制造方法,该方法包括
a:培养脐带血单个核细胞的工序,以及
b:回收所述脐带血单个核细胞的培养上清的工序。
该制造方法还可以包括对所述回收的培养上清进行选自离心处理、浓缩、溶剂置换、透析、冷冻、干燥、冷冻干燥、稀释和脱盐中的一种以上处理的工序。通过包括这样的工序,脑神经再生促进剂的处理、保存、运输变得容易。并且,所述制造方法还可以包括对所述回收的培养上清添加附加成分的工序。通过添加这样的附加成分,可以改变脑神经再生促进用组合物整体的物性,提高其特性。并且,所述制造方法还可以包括从脐带血制备脐带血单个核细胞体细胞的工序。对于各工序和附加成分等,本发明的脑神经损伤治疗剂的说明书中记载的事项直接适用。在包括对所述回收的培养上清进行选自离心处理、浓缩、溶剂置换、透析、冷冻、干燥、冷冻干燥、稀释和脱盐中的一种或多种处理的工序、以及对所述回收的培养上清添加附加成分的工序两者的情况下,可以先进行两工序的任一者,在可能的情况下也可以同时进行。
根据适用受试者的情况,在维持预期治疗效果的前提下,本发明的脑神经再生促进剂还可以含有其他附加成分作为药物组合物。附加可含的成分示例如下。
(i)生物可吸收材料
透明质酸、胶原蛋白、纤维蛋白原(例如,bolheal(注册商标))等可用作有机生物可吸收材料。
(ii)凝胶材料
凝胶材料优选使用生物相容性高的材料,可以使用透明质酸、胶原蛋白或纤维蛋白胶等。可以选择使用各种透明质酸和胶原蛋白,但优选采用适合本发明的脑神经再生促进剂的适用目的(适用组织)的透明质酸和胶原蛋白。使用的胶原蛋白优选可溶性的(酸溶性胶原蛋白、碱溶性胶原蛋白、酶溶性胶原蛋白等)。
(iii)其他
还可以含有制剂上可接受的其他成分(例如,载体、赋形剂、崩解剂、缓冲剂、乳化剂、助悬剂、镇痛剂、稳定剂、保存剂、防腐剂、生理盐水等)。赋形剂可以使用乳糖、淀粉、山梨醇、D-甘露醇、白砂糖等。崩解剂可以使用淀粉、羧甲基纤维素、碳酸钙等。缓冲剂可以使用磷酸盐、柠檬酸盐、乙酸盐等。乳化剂可以使用阿拉伯胶、海藻酸钠、黄芪胶等。助悬剂可以使用单硬脂酸甘油酯、单硬脂酸铝、甲基纤维素、羧甲基纤维素、羟甲基纤维素、十二烷基硫酸钠等。镇痛剂可以使用苯甲醇、氯丁醇、山梨糖醇等。稳定剂可以使用丙二醇、抗坏血酸等。保存剂可以使用苯酚、苯扎氯铵、苯甲醇、氯丁醇、对羟基苯甲酸甲酯等。防腐剂可以使用苯扎氯铵、对羟基苯甲酸、氯丁醇等。还可以含有抗生素、pH调节剂、生长因子(例如,表皮细胞生长因子(EGF)、神经生长因子(NGF)、脑源性神经营养因子(BDNF))等。
本发明的脑神经再生促进剂的药物组合物的最终形态没有特别限制。形态的例子包括液体状(液体状、凝胶状等)和固体状(粉末状、细粒、颗粒状等,包括冻干制剂)。本发明的药物组合物可以具有适合吸入的形态,例如,可以通过喷雾器或扩散器雾化的液体形态。脑神经损伤的相关部位是大脑,考虑到血脑屏障的存在,本发明的脑神经再生促进用组合物应该是采取鼻腔给药、脑室内给药或髓腔内的形式。例如,鼻腔给药可以以喷雾状或粉末状的形式进行。与脐带血单个核细胞和脐带血干细胞相比,脐带血单个核细胞的培养上清在前期准备和保存方面具有优势,据说特别适合脑神经损伤急性期和亚急性期的治疗。此外,脐带血单个核细胞的培养上清非常有用,因为它不含细胞成分,可以克服免疫排斥的问题。
实施例
以下将基于实施例对本发明进行详细说明。另外,本发明不限定于此。
实施例1:脐带血单个核细胞以及培养上清的制备
1)人脐带血单个核细胞的制备
脐带血单个核细胞如下所示进行制备。即,将1mL肝素钠注射液(1000U/mL)置于50mL聚丙烯管中,采集获得高知大学医学部附属医院妇产科知情同意提供的人脐带血约30mL。采集的人脐带血用Hank's平衡盐溶液(HBSS)稀释3倍。将稀释的脐带血小心地铺在预先加入了15mL Lympholyte-H(Cedarlane公司制)的50mL聚丙烯管中,以800×g离心分离20分钟。收集分离的单个核细胞层,加入HBSS,以300×g离心分离10分钟,洗涤细胞。在得到的单个核细胞中加入1mL的细胞冷冻保存液STEM-CELL BANKER(TAKARABIO公司制)进行悬浮,在-80℃的超低温冰箱中冷冻保存。冷冻保存的细胞在使用开始时进行冷冻融化,然后根据实验目的,用添加HBSS或10%胎牛血清(FBS)的各种细胞培养液进行洗涤。
2)人脐带血单个核细胞的培养
将脐带血单个核细胞以2×10
实施例2:脐带血单个核细胞和神经前体细胞共培养的神经再生
1)神经前体细胞的制备
将出生1周龄左右的NOD/SCID小鼠(Charles River Laboratories Japan,Inc.:NOD.CB17-Prkdc
2)共培养
将实施例1制备的人脐带血单个核细胞和实施例2制备的神经前体细胞分别悬浮于NeuroCult Basal完全培养基(StemCell Technologies公司制)中,使用μ-slidechemotaxis(Ibidi公司制),在37℃、5%CO
由以上结果可知,脐带血单个核细胞在制备状态(即由于未分离干细胞而包含各种细胞的状态)下,会分泌增强神经前体细胞的增殖、存活、移动(迁移)、分化和成熟的因子。
实施例3:基于脐带血单个核细胞培养上清的神经再生(体外)
对神经前体细胞的效果
将实施例2制备的神经前体细胞悬浮于NeuroCult Basal完全培养基(StemCellTechnologies公司制)中,接种于μ-slide chemotaxis(Ibidi公司制)中,加入50%(v/v)实施例1所得的人脐带血单个核细胞的培养上清,在37℃、5%CO
由以上结果可知,脐带血单个核细胞在制备状态(即、由于未分离干细胞而包含各种细胞的状态)下,会分泌增强神经前体细胞的增殖、存活、移动(迁移)、分化和成熟的因子,脐带血单个核细胞的培养上清促进了神经再生。
培养上清中所含因子
用抗体阵列(RayBiotech制,Human Cytokine Array C5)检查实施例1制备的脐带血单个核细胞培养上清中含有的因子(n=6)。如表1所示,培养上清中含有IL-1b、IL-6等细胞因子;CCL2、CCL5、CXCL1、CXCL5、CXCL7、CXCL8、GROa/b/g等趋化因子;BDNF、EGF等生长因子;骨桥蛋白(OPN)等,认为这些因子促进神经再生。此外,当在以8%、41%、73%、81%浓度添加了深层海水的培养基中制备培养上清时,这些因子的一部分或全部的浓度增加。
表1
实施例4:基于脐带血单个核细胞培养上清的神经再生(体内)
1)小鼠缺氧再灌注处理儿童脑性瘫痪模型的构建
使用ICR小鼠(Charles River Laboratories Japan,Inc.,Crl:CD1),根据Rice-Vannucci等人的方法制作缺氧再灌注治疗儿童脑性瘫痪模型小鼠(Wang等人,J MaternFetal Neonatal Med.2015;28(7):842-7)。用2%异氟烷麻醉出生后9天的小鼠(雌雄),用脑动脉瘤夹(Mizuho公司制)梗塞右侧颈动脉。将个体置于8%氧浓度下120分钟,然后取下脑动脉夹,使血流再灌注。
基于脐带血培养上清的治疗
将10μL实施例1制备的脐带血培养上清每隔一天鼻腔给药至缺氧处理儿童脑性瘫痪模型小鼠,持续2周。使用治疗后的小鼠进行旋转杆实验(室町机械株式会社制,MK-610A),测定小鼠从在300秒内加速到80rpm的旋转杆上落下为止的时间,培养上清给药组显示出恢复趋势(治疗前、治疗1周后和治疗2周后的步行时间分别为健康小鼠步行时间的72%、90%、112%(n=9))。
病理评估
将100mg/kg的溴脱氧尿苷(BrdU)给予治疗后的缺氧再灌注处理儿童脑性瘫痪模型小鼠(n=3),并标记增殖细胞。然后取出小鼠的大脑,用4%多聚甲醛溶液固定。使用切片机(Leica公司制)制备12μm厚的冷冻切片。使用兔抗小鼠双皮质素(Dcx)抗体(Abcam公司制,1:1000倍稀释使用)和Alexa Fluor 488标记的山羊抗兔IgG抗体(Themo FisherScientific Waltham公司制,1:1000倍稀释使用)对神经前体细胞进行免疫染色,使用小鼠抗小鼠胶质纤维酸性蛋白(GFAP)抗体(BD Biosciences公司制,Cat.No.556329、1:50倍稀释使用)和Alexa Flour 555标记的山羊抗小鼠IgG抗体(Cell Signaling Technology公司制,1:500倍稀释使用)对胶质细胞进行免疫染色,使用抗BrdU抗体(Abcam公司制,1:500倍稀释使用)和Alexa Flour 555标记的山羊抗大鼠IgG抗体(Cell Signaling Technology公司制,1:1000倍稀释使用)对增殖细胞进行免疫染色。
如图3所示,培养上清给药组中,在脑室下带区域确认到Dcx/BrdU共阳性增殖的神经前体细胞,神经前体细胞的数量与对照组(与制备脐带血单个核细胞培养上清时使用的培养基同量的鼻腔给药组)相比,增加了2.1倍(治疗组:397个细胞/切片,对照组:189个细胞/切片)。研究发现,这些神经前体细胞会随着时间的推移在脑损伤部位附近移动和积累(归巢)。
如图4所示,在缺氧处理儿童脑性瘫痪模型小鼠的脑损伤部位周围观察到星形胶质细胞的聚集,但在培养上清给药组中,在星形胶质细胞周围确认到Dcx/BrdU共阳性增殖的神经前体细胞,其显示出许多神经元样的细胞形态(治疗组:61个细胞/切片,对照组:32个细胞/切片)。
对缺氧处理儿童脑性瘫痪模型小鼠的大脑进行免疫染色的结果认为,给予脐带血单个核细胞培养上清会促进脑室下带的神经前体细胞的增殖,同时会促进向脑损伤部位的归巢、向神经元的分化和成熟。
综上所述,脐带血单个核细胞在制备状态(即由于未分离脐带血干细胞而包含各种细胞的状态)下,会分泌增强神经前体细胞的增殖、存活、移动和归巢、分化和成熟的因子,脐带血单个核细胞的培养上清可以使神经再生,可用于治疗儿童脑性瘫痪等脑神经损伤。
- 包含胎儿附属物来源组织细胞培养上清的脑神经损伤治疗剂
- 一种从脐带血分离总有核细胞与单个核细胞的方法
