新型α-糖苷酶抑制剂及其应用
文献发布时间:2023-06-19 09:29:07
技术领域
本发明涉及两种新型α-糖苷酶抑制剂及其应用,2-(4-氟苯甲酰胺基)-N-(呋喃-2-基甲基)苯甲酰胺和22-((1H-苯并[d]咪唑-2-基)甲基)硫基) -5-乙酰基-4-(4-甲氧基苯基)-6-甲基烟腈作为α-糖苷酶抑制剂的应用。
背景技术
糖尿病是一种由于胰岛素分泌不足、胰岛素作用受损或胰岛素抵抗所引起的体内血糖持续在较高水平从而极易发生如:心脏病、肾病(肾功能衰竭、尿毒症)、足病(溃疡、感染、坏疽)、脑病(脑血管病变)、眼病(视网膜病变、模糊不清、失明)等慢性并发症的一种与遗传、生活习惯等相关的常见病;通常表现为即多饮、多食、多尿、体重减少;根据世界卫生组织的划分,糖尿病分为:1型糖尿病(即胰岛素依赖型糖尿病)、2型糖尿病(即非胰岛素依赖型糖尿病)。2型糖尿病患者人数占总体患者数的90%以上,餐后高血糖是引起2型糖尿病并发症的主要原因。
α-糖苷酶存在人体小肠刷状绒毛上,其功能是将经胰腺淀粉酶水解形成的线性糖链和分支糊精链如小的寡糖、麦芽糖、麦芽三糖等进一步分解成α-1,6和α-1,4糖苷键连接的寡糖。α-糖苷酶抑制剂的结构类似于单糖或者寡糖,其结构中一般含有氮、硫等杂原子,可与糖苷酶的活性位点紧密结合,亲和力比α-糖苷酶的正常底物强,因此,糖苷酶抑制剂和寡糖竞争糖苷酶结合位点,通过占据糖苷酶活性空腔,减少寡糖的消化吸收速率从而达到控制血糖的效果。因此,α-糖苷酶是开发治疗糖尿病药物的靶标。
目前临床上常用的α-糖苷酶抑制剂类药物有阿卡波糖、伏格列波糖、米格列醇等,但是这些药物都存在一定的缺陷,比如阿卡波糖虽然是目前应用最广泛的抗糖尿病药物之一,但是阿卡波糖对非活性成分过敏者禁用,因碳水化合物在肠道中发酵往往会引起胃胀气、腹部不适,会对少部分患者的肝细胞造成一定的损伤,有些患者会出现黄疸,会引起转氨酶升高。
因此亟需开发新型疗效好、副作用低的α-糖苷酶抑制剂。
在新药开发过程中,虚拟筛选被证明是一种非常快速、有效的药物先导物的发现手段。我们基于α-糖苷酶与阿卡波糖的复合物晶体结构建立了α-糖苷酶抑制剂的虚拟筛选方法,采用分子对接的虚拟筛选方法对商业化合物库(SPECS)进行了虚拟筛选,获得了潜在的α-糖苷酶抑制剂的候选化合物,后期通过α-糖苷酶酶活抑制活性筛选实验发现购买得到的化合物中有两个化合物,能够抑制α-糖苷酶的活性,并且能够与α-糖苷酶结合、对正常肝细胞(LO2细胞)没有毒性作用。这两个化合物具有开发成为治疗糖尿病药物的良好应用前景。
发明内容
本发明的目的是提供两种新型α-糖苷酶抑制剂。
本发明的第一方面,提供了如图1和图2所示的化合物,或其药学上可接受的盐、水合物、溶剂化物或前药。
本发明的第二方面,一种药物组合物,所述药物组合物包含第一方面所述的图1和图2所示的化合物,或其药学上可接受的盐、水合物、溶剂化物或前药,和药学上可接受的载体。
本发明的第三方面,提供了第一方面所述的图1和图2所示的化合物或其药学上可接受的盐、水合物、溶剂化物或前药用途,用于:(i)制备α-糖苷酶抑制剂;(ii)制备预防和/或治疗α-糖苷酶相关疾病的药物;(iii)制备预防和/或治疗糖尿病的药物;(iv)制备预防和/或治疗2型糖尿病的药物。
药学上可接受的载体必须可与配方的其他成分兼容,且不会对其接受者有害,一般为适当载剂、稀释剂及赋形剂是为本领域技术人员所公知且包括诸如碳水化合物、蜡、水溶性及/或泡胀性聚合物、亲水性或疏水性材料、明胶、油、溶剂、水及类似物。所使用的特定载剂、稀释剂或赋形剂将取决于给予本发明化合物的方式及目的。溶剂通常是基于本领域技术人员所认为安全给予哺乳动物的溶剂(GRAS)而选择。通常,安全溶剂为无毒水性溶剂(诸如水)及其他可溶于水或与水可混溶的无毒溶剂。适当水性溶剂包括水、乙醇、丙二醇、聚乙二醇(例如PEG400或PEG300)等及其混合物。还可包括一或多种缓冲剂、稳定剂、表面活性剂、湿润剂、润滑剂、乳化剂、悬浮剂、防腐剂、抗氧化剂、不透明剂、助滑剂、加工助剂、着色剂、甜味剂、香料、调味剂及其他提供药物(即本发明化合物或其医学组合物)精美外观或有助于制造药物产品(即用于制备药剂)的已知添加剂。
有益效果:本发明的化合物,在体外能够抑制α-糖苷酶,并且可以与α-糖苷酶结合、对正常肝细胞(LO2细胞)没有毒性作用,能够用于制备预防和/或治疗糖尿病的药物。
附图说明
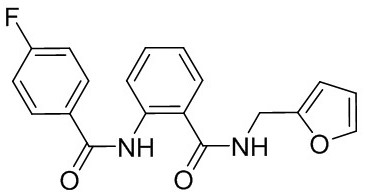
图1为化合物2-(4-氟苯甲酰胺基)-N-(呋喃-2-基甲基)苯甲酰胺(编号37)的结构式。
图2为化合物22-((1H-苯并[d]咪唑-2-基)甲基)硫基) -5-乙酰基-4-(4-甲氧基苯基)-6-甲基烟腈(编号44)的结构式。
图3为化合物抑制α-葡萄糖苷酶活性的IC
图4为α-糖苷酶与化合物不同浓度共孵育情况下的荧光发射光谱的变化情况。
图5为α-糖苷酶与化合物共孵育时的荧光淬灭的斯特恩-沃尔默图表。
图6为α-糖苷酶与图1所示化合物的结合模式图。
图7为α-糖苷酶与图2所示化合物的结合模式图。
具体实施方式
下面对本发明的实施例作详细说明,本实施例在以本发明技术方案为前提下进行实施,给出了详细的实施方式和具体的操作过程,但本发明的保护范围不限于下述的实施例。
本申请的发明人经过对商业化合物库的虚拟筛选及活性研究,发现了两种新型α-糖苷酶抑制剂,能够有效抑制α-糖苷酶的活性,与α-糖苷酶结合、对正常肝细胞(LO2细胞)没有毒性作用。在此基础上,完成了本发明。
实施例1 化合物对α-糖苷酶活性的影响。
对硝基苯-α-葡萄糖苷(4-Nitrophenyl α-D-glucopyranoside,PNPG)是α-葡萄糖苷酶的特异性底物。PNPG经α-葡萄糖苷酶水解产生对硝基苯酚,在405 nm呈特异性吸收。通过对比麦芽根酶解产物加入前后体系中对硝基苯酚的生成量,即可得到其对α-葡萄糖苷酶活性的抑制作用。
配制2.5 mmol/L的PNPG溶液;0.3 U/mL α-葡萄糖苷酶溶液;0.2 mol/L Na
样品组:依次添加 20 μL上述(b)中的PBS缓冲液,20 μL不同麦芽根酶解液,20 μL0.3U/mL α-葡萄糖苷酶溶液于37℃孵育5 min,后加入20 μL 2.5 mmol/L PNPG 溶液,于37℃反应30 min后加80 μL 0.2mol/L Na
背景组:依次添加40 μL上述(b)中的PBS缓冲液,20 μL不同麦芽根酶解液于37℃孵育5 min,后加入20 μL 2.5 mmol/L PNPG溶液,于37℃反应30 min后加80 μL 0.2mol/LNa
阴性组:依次添加 40 μL上述(b)中的PBS缓冲液,20 μL 0.3 U/mL α-葡萄糖苷酶溶液于37℃孵育5 min,后加入20 μL 2.5 mmol/L PNPG溶液,于37℃反应30 min后加80 μL0.2mol/L Na
空白组:添加80 μL上述(b)中的PBS缓冲液,于37℃孵育5 min,不添加其他试剂继续孵育30 min后添加80 μL 0.2mol/L Na
每组做3个平行,于酶标仪中检测405 nm处的吸光度,以此计算出样品的酶抑制率。
计算公式: α-葡萄糖苷酶抑制率%=[1-(
根据抑制曲线求得化合物的IC
实施例2 化合物与α-糖苷酶结合。
荧光淬灭实验用来验证活性化合物与α-糖苷酶的结合。通过配置有恒温槽和10mm石英比色皿的萤光分光光谱仪(Agilent Cary Eclipse)来检测加入不同浓度的化合物后,α-糖苷酶的荧光信号的变化 (发射光谱检测波长为320-500 nm,和激发波长为290nm)。α-糖苷酶的浓度为1U/mL, 化合物的浓度从256 μM 开始等倍稀释,直到0。共孵育条件是37℃, 30 min, PH = 7.0的PBS缓冲液。实验结果如图4和图5所示,结果表明图1和图2所示的化合物能够和α-糖苷酶结合。
实施例3 化合物对正常肝细胞(LO2细胞)的毒性作用。
采用含10%胎牛血清的DMEM培养基,于37℃、5% CO2饱和湿度的培养箱中常规培养。以2×10
实施例4 化合物与α-糖苷酶的结合模式。
分子对接的结果如图6和图7所示,从图上可以看出,图1和图2所示的化合物均能很好的与α-糖苷酶结合。疏水相互作用、氢键相互作用和Pi-Pi堆积是保持两者结合的主要相互作用。
显然,本领域的技术人员可以对本发明进行各种改动和变型而不脱离本发明的精神和范围。这样,倘若本发明的这些修改和变型属于本发明权利要求及其等同技术的范围之内,则本发明也意图包含这些改动和变型在内。
