一种铜纳米粒子包覆碳点实时监测型抑菌水凝胶及制备方法和应用
文献发布时间:2023-06-19 18:29:06
技术领域
本发明属于新材料技术领域,具体涉及一种铜纳米粒子包覆碳点实时监测型抑菌水凝胶及制备方法和应用。
背景技术
伤口敷料,是用于手术后、外伤及其他皮肤损害中包扎伤口的用品,用以覆盖伤口并促进伤口愈合的材料。从目前的研究来看,伤口敷料被分为两类。一类是传统敷料,被动覆盖创面和吸收渗出物,为创面提供有限的保护作用;现有技术中大部分传统的伤口敷料功能单一,仅能抑制细菌生长,促进伤口愈合,而不具备刺激反应或者监测的能力。极少的伤口敷料能够实现早期检测伤口的状态,如温度、pH值、炎症因子以及细菌分泌的毒素和酶等物理化学指标。而在实际应用时,需要伤口敷料能够对这些变化作出反应,从而积极地改变伤口环境,以适当的方式加速伤口痊愈。
另一类是智能敷料,智能伤口敷料是一系列通过使用内置传感器或智能材料的伤口敷料,如刺激响应材料和自愈材料,可以与伤口互动,感知伤口状况或环境变化并做出反应。伤口愈合是一个动态的过程,伴随着各种化学和物理变化。伤口在完全愈合之前经历分子水平变化的多个阶段,而分子水平的任何变化都可能破坏正常的伤口愈合过程。在愈合过程中,伤口部位的温度、pH值、氧气水平、葡萄糖水平和许多其他因素都会影响伤口愈合。因此在近些年,已经开发出了在分子水平上监测伤口状态变化的伤口敷料,以帮助伤口愈合。Yue Zhao,Zuhao Li等人开发了具有刺激响应特性的透明导电超分子水凝胶(YueZhao,Zuhao Li,Qiuju Li,Longfei Yang,et al.Transparent ConductiveSupramolecular Hydrogels with Stimuli-Responsive Properties for On-DemandDissolvable Diabetic Foot Wound Dressings.Macromolecular.Rapid Communication,2020,2000441),能够将按需溶解的伤口敷料用于糖尿病足,这种多功能超分子水凝胶在按需可溶解伤口敷料的设计中提供了新的思路。Ning Tang等人制备了具有抗菌活性的高效自愈多功能敷料,用于无缝合伤口闭合和感染伤口监测(Ning Tang,Rongjun Zhang,Youbin Zheng,et al.Highly Efficient Self-Healing Multifunctional Dressingwith Antibacterial Activity for Sutureless Wound Closure and Infected WoundMonitoring.Advanced.Materials,2021,2106842),该敷料内的集成传感器阵列可以实时监测伤口区域的温度、pH和葡萄糖水平,从而提供可靠和及时的伤口状况信息。最终,所报告的多功能敷料在个性化监测和治疗方法方面、数字化和其他以人为本的医疗保健解决方案方面以及管理伤口愈合相关负担方面都具有很高的价值。综上,智能伤口敷料与创面之间存在着多种形式的相互作用能够反映伤口愈合过程中的变化,控制伤口感染,防止发展为慢性伤口,促进伤口自主愈合,智能伤口敷料的出现为伤口愈合提供了一种新的策略。
虽然现有技术中的智能伤口敷料可以与伤口互动,感知伤口状况或环境变化并做出反应,从而提供可靠和及时的伤口状况信息;但是伤口敷料本身的状态变化也是至关重要的,关于实时监测型伤口敷料的研究至今几乎没有,具备监测能力的抑菌智能伤口敷料的开发也较少,且目前的研究几乎不关注伤口敷料本身的状态变化,如伤口敷料的使用情况、抑菌剂的扩散情况。
发明内容
为了克服上述现有技术的缺点,本发明的目的在于提供一种铜纳米粒子包覆碳点实时监测型抑菌水凝胶及制备方法和应用,解决现有技术中伤口敷料不能实时监测抑菌剂扩散情况的技术问题。
为了达到上述目的,本发明采用以下技术方案予以实现:
本发明公开了一种铜纳米粒子包覆碳点实时监测型抑菌水凝胶,由CuNPs、CQDs和PVA组成;CQDs包覆在CuNPs表面得到CuNPs@CQDs,CuNPs@CQDs填充在PVA的三维孔隙中得到CuNPs@CQDs-PVA复合水凝胶。
优选地,CuNPs@CQDs-PVA复合水凝胶的断裂伸长率达701.81%±7.28%。
优选地,CuNPs@CQDs-PVA复合水凝胶的吸水量达自身重量的350%以上。
本发明还公开了上述铜纳米粒子包覆碳点实时监测型抑菌水凝胶的制备方法,包括以下步骤:
1)先将CuNPs溶液与多巴胺溶液充分混匀,离心、洗涤,再与CQDs溶液充分混匀,离心、洗涤,加入去离子水制得CuNPs@CQDs溶液;
所述CuNPs溶液:多巴胺溶液:CQDs溶液的体积比为(1~3):(1~3):(1~6);
2)在PVA溶胶中加CuNPs@CQDs溶液,搅拌均匀,用硼酸溶液交联,静置除气泡,均匀喷洒Na
所述PVA溶胶与CuNPs@CQDs溶液的体积比为:(5~15):(3~9)。
优选地,步骤1)中,CuNPs溶液是由每0.1~0.6g的CuNPs溶于5~30mL去离子水制得;多巴胺溶液是由每5~120mg的多巴胺溶于5~30mL去离子水制得,CQDs溶液是由每1~6g的CQDs溶于20~50mL去离子水制得。
优选地,步骤1)中,两步充分混匀的条件均为:20~40℃下震荡10~30h。
优选地,步骤2)中,PVA溶胶是由每1~2.5g的PVA加入10mL去离子水中,在80~95℃下加热溶解制得;CuNPs@CQDs溶液是由每0.1~0.5g的CuNPs@CQDs加入1~5mL去离子水中制得。
优选地,步骤1)中,CuNPs溶液按以下方法制得:将每0.1~0.6g硫酸铜溶于8~50mL去离子水中,在75~90℃下加热溶解,加入氨水,生成铜氨络合物,再加入抗坏血酸溶液和环糊精溶液,至生成红棕色沉淀,继续搅拌均匀,离心得到CuNPs,加入去离子水得到CuNPs溶液。
优选地,步骤1)中,CQDs溶液按以下方法制得:将尿素和柠檬酸溶解于去离子水中,再加入十六烷基三甲基溴化铵,超声溶解,将所得混合液加热,再加入去离子水溶解,离心除去不溶性杂质,得到CQDs溶液;
所述尿素:柠檬酸:十六烷基三甲基溴化铵的质量比为(1~4):(1~2):(0.02~0.2)。
本发明还公开了上述铜纳米粒子包覆碳点实时监测型抑菌水凝胶在制备伤口敷料中的应用。
与现有技术相比,本发明具有以下有益效果:
本发明公开了一种铜纳米粒子包覆碳点实时监测型抑菌水凝胶,由CuNPs、CQDs和PVA三部分组成。CuNPs能抑制细菌生长,促进伤口愈合,但CuNPs易聚集,易氧化;CQDs具有优异的还原性,包覆在CuNPs表面,可减缓CuNPs的氧化速度,且CQDs在紫外光照射下发射出蓝色荧光,CQDs的荧光圈能够代表CuNPs的扩散圈,从而实现用CQDs的荧光来实时监测抑菌剂CuNPs扩散的目的;PVA水凝胶作为抑菌药物的载体,拥有大的三维孔隙,CuNPs@CQDs均匀填充在PVA水凝胶的三维孔隙中,且PVA吸水性强,可降解,无毒害,具有优异的生物相容性;由CuNPs、CQDs和PVA三部分组成的CuNPs@CQDs-PVA水凝胶拥有极好的荧光性能,更大的孔隙,更强的吸水性,能够吸收更多的伤口渗出液,在抑制细菌生长,促进伤口愈合的同时,还能通过观察CuNPs@CQDs-PVA复合水凝胶的荧光强弱变化来判断水凝胶的使用状况,实现对伤口敷料使用情况的实时监测,并及时对伤口进行精准给药,加速伤口愈合。
进一步地,CuNPs@CQDs-PVA复合水凝胶的延展性非常好,断裂伸长率达701.81%±7.28%。
进一步地,CuNPs@CQDs-PVA复合水凝胶的吸水性非常好,吸水量达自身重量的350%以上,有利于吸收伤口渗出液。
本发明还公开了铜纳米粒子包覆碳点实时监测型抑菌水凝胶的制备方法,先将CuNPs溶液与多巴胺溶液充分混匀,多巴胺氧化后形成聚多巴胺,并充分包裹CuNPs,再将混合液与CQDs溶液充分混匀,多巴胺及CQDs都具有优异的还原性,利用多巴胺的粘附性,使CQDs包裹在CuNPs上,制得的CuNPs@CQDs可减缓CuNPs的氧化速度,且能通过CQDs的荧光变化,可以实时监测到CuNPs的扩散情况,将PVA溶胶加入到CuNPs@CQDs溶液中混匀,并加入硼酸溶液和Na
本发明制备的铜纳米粒子包覆碳点实时监测型抑菌水凝胶CuNPs@CQDs-PVA作为伤口敷料使用时,CuNPs@CQDs稳定存在于PVA水凝胶中,可以长时间使用而不缺失抑菌性,在伤口敷料领域具有很好的应用潜力。
附图说明
图1为本发明实施例1制得的CuNPs@CQDs-PVA在制备过程中各阶段材料的形貌图;其中,(a)和(b)为CuNPs的SEM图像,(c)为CQDs的TEM图像,(d)为CuNPs@CQDs粒子的SEM图像,(e)和(f)为PVA的SEM图像,(g)、(h)和(i)为CuNPs@CQDs-PVA的SEM图像,(j)、(k)和(l)分别为CuNPs@CQDs-PVA中Cu、C和O元素的mapping图像;
图2为本发明实施例1制得的材料的红外和机械性能分析图;其中,(a)为CuNPs@CQDs/PVA和PVA水凝胶的红外分析图,(b)为CuNPs@CQDs/PVA和PVA水凝胶的机械性能测试图;
图3为本发明实施例1制得的材料的紫外可见漫反射图;其中,(a)为CQDs和CuNPs@CQDs溶液的紫外-可见光吸收光谱,(b)为CuNPs@CQDs-PVA膜的紫外-可见光吸收光谱;
图4为本发明实施例1制得的材料的稳态荧光图;其中,(a)为CQDs溶液的稳态荧光图;(b)为CuNPs@CQDs-PVA的稳态荧光图;
图5为本发明实施例1制得的材料的溶胀性能及可生物降解曲线;其中,(a)是PVA和CuNPs@CQDs-PVA水凝胶的溶胀性曲线,(b)是PVA和CuNPs@CQDs-PVA水凝胶的可生物降解性曲线;
图6为本发明实施例1制得的CQDs的浸渍时间及浸渍浓度对CuNPs@CQDs荧光圈的影响图;其中,(a)是CQDs的浸渍时间为0h、6h、12h、18h、24h和30h时对CuNPs@CQDs荧光圈的影响图,(b)是CQDs的浸渍浓度为4%、6%、8%、10%、12%和14%时对CuNPs@CQDs荧光圈的影响图;
图7为本发明实施例1制得的CuNPs@CQDs/PVA水凝胶随时间增加的荧光圈及铜扩散圈图,其中,(a)是CuNPs@CQDs/PVA水凝胶在20min、4h、8h、12h、24h和36h时的荧光圈图,(b)是CuNPs@CQDs/PVA水凝胶在20min、4h、8h、12h、24h和36h时的铜扩散圈图;
图8为本发明实施例1制得的CuNPs@CQDs-PVA水凝胶的抑菌性能图,其中,(a)是CuNPs@CQDs的添加量分别为0g、0.1g、0.2g、0.3g、0.4g和0.5g时对CuNPs@CQDs-PVA水凝胶抑菌性能的影响试验图,(b)是CuNPs-PVA和CuNPs@CQDs-PVA水凝胶分别在12h、24h和36h时的抑菌持久性试验图,(c)是CuNPs@CQDs-PVA水凝胶在制备阶段各产物的抑菌性试验图;
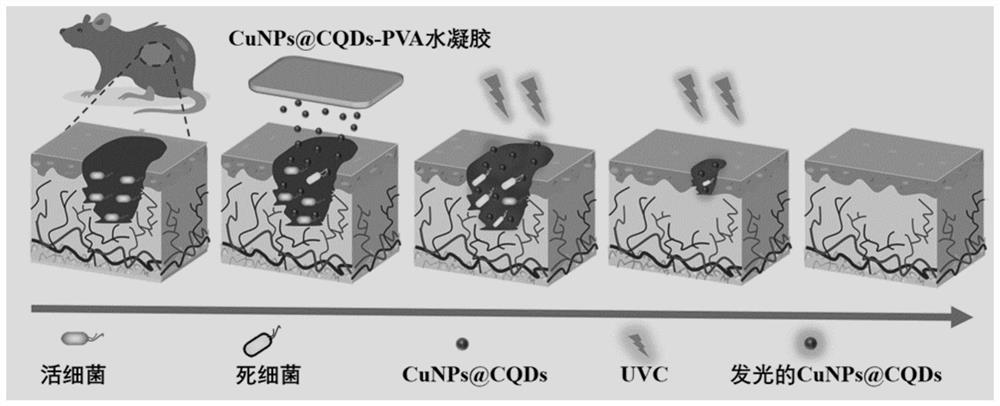
图9为本发明公开的CuNPs@CQDs-PVA水凝胶的抑菌与监测机理图。
具体实施方式
为了使本技术领域的人员更好地理解本发明方案,下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分的实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都应当属于本发明保护的范围。
需要说明的是,本发明的说明书和权利要求书及上述附图中的术语“第一”、“第二”等是用于区别类似的对象,而不必用于描述特定的顺序或先后次序。应该理解这样使用的数据在适当情况下可以互换,以便这里描述的本发明的实施例能够以除了在这里图示或描述的那些以外的顺序实施。此外,术语“包括”和“具有”以及他们的任何变形,意图在于覆盖不排他的包含,例如,包含了一系列步骤或单元的过程、方法、系统、产品或设备不必限于清楚地列出的那些步骤或单元,而是可包括没有清楚地列出的或对于这些过程、方法、产品或设备固有的其它步骤或单元。
下面结合具体实施例对本发明做进一步详细描述:
本发明公开了一种CuNPs@CQDs-PVA水凝胶的制备方法,具体包括以下步骤:
1)CuNPs的合成:首先,在8~50mL去离子水中加入0.1~06g硫酸铜溶解,加热到75~90℃,滴加50~300uL氨水生成铜氨络合物,将配置好的0.5~1.5g/25mL抗坏血酸和0.1~0.5g/25mL环糊精溶液快速加入,观察溶液颜色由蓝色变为暗黄色,最终生成红棕色沉淀,再搅拌2~8分钟,离心得到铜纳米粒子;
2)碳量子点(CQDs)的制备:将1~4g尿素和1~2g柠檬酸溶解于10~40mL去离子水中,加入0.02~0.2g十六烷基三甲基溴化铵(CTAB),CTAB作为分散剂,超声溶解,将所得混合液至于微波炉中高温加热2~6分钟,之后加入20~50mL去离子水溶解CQDs,并以8000~10000rpm的速率离心,除去不溶性杂质,得到CQDs;
3)CuNPs@CQDs的制备:将步骤1)制备好的0.1~0.6g片状CuNPs溶于5~30mL去离子水中,再加入5~30mL浓度为1~4mg/mL的多巴胺溶液,在20~40℃摇床中以一定速率震荡10~30h,离心洗涤三次后,与20~50mL步骤2)制得的CQDs溶液混合后,在20~40℃摇床中以一定速率震荡10~30h,再离心洗涤三次,最终以3~7mL溶液的形式保存;
4)CuNPs@CQDs-PVA水凝胶的制备:在10mL去离子水中加入1~2.5g PVA,80~95℃水浴加热并搅拌10~30分钟,至PVA完全溶解,向PVA溶胶中加入0~8mL的CuNPs@CQDs溶液,搅拌均匀,用1~3mL的0.75wt.%的硼酸溶液交联,倒入六孔培养板静置除气泡。最后将事先配置好的50~200mL的10wt.%的Na
实施例1
1)CuNPs的合成:首先,在25mL去离子水中加入0.4g硫酸铜,85℃下加热溶解,滴加150uL氨水生成铜氨络合物,将配置好的1.1g/25mL抗坏血酸、0.25g/25mL环糊精溶液快速加入,溶液颜色由蓝色变为暗黄色,最终生成红棕色沉淀,搅拌5分钟,离心得到铜纳米粒子;
2)CQDs的制备:将2g尿素、1g柠檬酸溶解于20mL去离子水中,加入0.2g分散剂十六烷基三甲基溴化铵(CTAB),超声溶解;将所得混合液至于微波炉中高温加热5分钟,得到CQDs,之后加入30mL去离子水溶解CQDs,以8000rpm的速率离心,除去不溶性杂质;
3)CuNPs@CQDs的制备:将制备好的0.4g片状CuNPs溶液加入10mL水中,与10mL浓度为2mg/mL的多巴胺溶液混合,在37℃摇床中以一定速率震荡24h;离心洗涤三次后与30mLCQDs溶液混合,在37℃摇床中以一定速率震荡24h;离心洗涤三次,最终以5mL溶液的形式保存;
4)CuNPs@CQDs-PVA水凝胶的制备:将2g PVA加入10mL去离子水中,85℃水浴加热并搅拌15分钟至溶解完全;向PVA溶胶中加入3mL的CuNPs@CQDs溶液,搅拌均匀,用0.75wt.%的硼酸溶液交联,倒入六孔培养板静置除气泡;最后将事先配置好的10wt.%的Na
实施例2
1)CuNPs的合成:首先,在25mL去离子水中加入0.3g硫酸铜,83℃下加热溶解,滴加200uL氨水生成铜氨络合物,将配置好的1.5g/25mL抗坏血酸、0.3g/25mL环糊精溶液快速加入,溶液颜色由蓝色变为暗黄色,最终生成红棕色沉淀,搅拌5分钟,离心得到铜纳米粒子;
2)CQDs的制备:将1.6g尿素、0.8g柠檬酸溶解于20mL去离子水中,加入0.2g分散剂十六烷基三甲基溴化铵(CTAB),超声溶解;将所得混合液至于微波炉中高温加热3分钟,得到CQDs,之后加入40mL去离子水溶解CQDs,以8000rpm的速率离心,除去不溶性杂质;
3)CuNPs@CQDs的制备:将制备好的0.3g片状CuNPs溶液加入15mL水中,与15mL浓度为2mg/mL的多巴胺溶液混合,在32℃摇床中以一定速率震荡20h;离心洗涤三次后与30mLCQDs溶液混合,在37℃摇床中以一定速率震荡20h;离心洗涤三次,最终以5mL溶液的形式保存;
4)CuNPs@CQDs-PVA水凝胶的制备:将1.5g PVA加入10mL去离子水中,90℃水浴加热并搅拌15分钟至溶解完全;向PVA溶胶中加入3mL的CuNPs@CQDs溶液,搅拌均匀,用0.75wt.%的硼酸溶液交联,倒入六孔培养板静置除气泡;最后将事先配置好的10wt.%的Na
实施例3
1)CuNPs的合成:首先,在25mL去离子水中加入0.5g硫酸铜,90℃下加热溶解,滴加250uL氨水生成铜氨络合物,将配置好的1.1g/25mL抗坏血酸、0.25g/25mL环糊精溶液快速加入,溶液颜色由蓝色变为暗黄色,最终生成红棕色沉淀,搅拌5分钟,离心得到铜纳米粒子;
2)CQDs的制备:将2.3g尿素、1.3g柠檬酸溶解于20mL去离子水中,加入0.15g分散剂十六烷基三甲基溴化铵(CTAB),超声溶解;将所得混合液至于微波炉中高温加热4分钟,得到CQDs,之后加入30mL去离子水溶解CQDs,以8000rpm的速率离心,除去不溶性杂质;
3)CuNPs@CQDs的制备:将制备好的0.3g片状CuNPs溶液加入8mL水中,与8mL浓度为2mg/mL的多巴胺溶液混合,在37℃摇床中以一定速率震荡24h;离心洗涤三次后与30mLCQDs溶液混合,在37℃摇床中以一定速率震荡24h;离心洗涤三次,最终以5mL溶液的形式保存;
4)CuNPs@CQDs-PVA水凝胶的制备:将2.3g PVA加入10mL去离子水中,88℃水浴加热并搅拌15分钟至溶解完全;向PVA溶胶中加入6mL的CuNPs@CQDs溶液,搅拌均匀,用0.75wt.%的硼酸溶液交联,倒入六孔培养板静置除气泡;最后将事先配置好的10wt.%的Na
实施例4
1)CuNPs的合成:首先,在25mL去离子水中加入0.2g硫酸铜,80℃下加热溶解,滴加100uL氨水生成铜氨络合物,将配置好的1.1g/25mL抗坏血酸、0.25g/25mL环糊精溶液快速加入,溶液颜色由蓝色变为暗黄色,最终生成红棕色沉淀,搅拌5分钟,离心得到铜纳米粒子;
2)CQDs的制备:将3g尿素、1.5g柠檬酸溶解于20mL去离子水中,加入0.05g分散剂十六烷基三甲基溴化铵(CTAB),超声溶解;将所得混合液至于微波炉中高温加热4分钟,得到CQDs,之后加入30mL去离子水溶解CQDs,以8000rpm的速率离心,除去不溶性杂质;
3)CuNPs@CQDs的制备:将制备好的0.2g片状CuNPs溶液加入10mL水中,与10mL浓度为3mg/mL的多巴胺溶液混合,在37℃摇床中以一定速率震荡28h;离心洗涤三次后与30mLCQDs溶液混合,在37℃摇床中以一定速率震荡20h;离心洗涤三次,最终以5mL溶液的形式保存;
4)CuNPs@CQDs-PVA水凝胶的制备:将1.6g PVA加入10mL去离子水中,86℃水浴加热并搅拌15分钟至溶解完全;向PVA溶胶中加入4mL的CuNPs@CQDs溶液,搅拌均匀,用0.75wt.%的硼酸溶液交联,倒入六孔培养板静置除气泡;最后将事先配置好的10wt.%的Na
实施例5
1)CuNPs的合成:首先,在25mL去离子水中加入0.6g硫酸铜,88℃下加热溶解,滴加260uL氨水生成铜氨络合物,将配置好的1.1g/25mL抗坏血酸、0.25g/25mL环糊精溶液快速加入,溶液颜色由蓝色变为暗黄色,最终生成红棕色沉淀,搅拌5分钟,离心得到铜纳米粒子;
2)CQDs的制备:将3.5g尿素、1.7g柠檬酸溶解于20mL去离子水中,加入0.18g分散剂十六烷基三甲基溴化铵(CTAB),超声溶解;将所得混合液至于微波炉中高温加热4分钟,得到CQDs,之后加入30mL去离子水溶解CQDs,以8000rpm的速率离心,除去不溶性杂质;
3)CuNPs@CQDs的制备:将制备好的0.3g片状CuNPs溶液加入10mL水中,与24mL浓度为2mg/mL的多巴胺溶液混合,在37℃摇床中以一定速率震荡26h;离心洗涤三次后与30mLCQDs溶液混合,在37℃摇床中以一定速率震荡26h;离心洗涤三次,最终以5mL溶液的形式保存;
4)CuNPs@CQDs-PVA水凝胶的制备:将2g PVA加入10mL去离子水中,75℃水浴加热并搅拌30分钟至溶解完全;向PVA溶胶中加入7.5mL的CuNPs@CQDs溶液,搅拌均匀,用0.75wt.%的硼酸溶液交联,倒入六孔培养板静置除气泡;最后将事先配置好的10wt.%的Na
下面结合附图对本发明做进一步详细描述:
(1)对本发明实施例1制得材料的形貌及结构进行了分析测试;
参见图1中(a)和(b)为CuNPs的SEM图像,从图中可以看出,所制备的CuNPs是片状的,平均厚度为285.3nm;(c)为CQDs的TEM图像,从图中可以看出,CQDs的粒径在5nm以下,表明所制备的确实是量子点;(d)为CuNPs@CQDs粒子的SEM图像,从图中可以看出,CuNPs在制备过程中在外力作用下由片状碎裂为更小的不规则的粒子,以多巴胺为粘附剂包裹CQDs,并粘附在CuNPs的表面;(e)和(f)为PVA的SEM图像,从(e)图可以看出PVA水凝胶的表面形貌呈现凹凸不平的沟壑及多孔结构,这是因为使用Na
(2)对本发明实施例1制得的材料的红外和机械性能进行分析测试;
参见图2中(a)为CuNPs@CQDs/PVA和PVA水凝胶的红外分析图,从图中可以看出,CuNPs@CQDs的加入没有改变PVA的峰形,但峰强增大,对于纯的PVA水凝胶来说,在3700~3000cm
表1:机械性能测试
参见表1为本发明实施例1制得的CuNPs@CQDs-PVA及PVA水凝胶的机械性能测试,从表中可以看出PVA水凝胶及CuNPs@CQDs-PVA的延展性都非常好,断裂伸长率分别可达731.25%±6.78%和701.81%±7.28%,这使其作为伤口敷料有更大的应用价值。
(3)对本发明实施例1制得的材料进行紫外可见漫反射分析测试;
参见图3中(a)为CQDs、CuNPs@CQDs溶液的紫外-可见光吸收光谱,从图中可以看出,CQDs、CuNPs@CQDs溶液对200~255nm的远紫外光有强吸收,吸光度为0.875a.u以上,CQDs溶液在200~280nm范围内有一个宽的吸收,在250nm左右有明显的吸收峰,可能含有两个共轭双键,对应于芳香族sp
(4)对本发明实施例1制得的材料进行稳态荧光分析测试;
参见图4中(a)为CQDs溶液的稳态荧光图;从图中可以看出,在365nm波长的激发光下,CQDs溶液的发射峰在555nm左右;(b)为CuNPs@CQDs-PVA的稳态荧光图;从图中可以看出,CuNPs@CQDs-PVA的发射峰蓝移到460nm;而将CQDs溶液、CuNPs@CQDs-PVA干膜置于透明玻璃瓶中,其在自然光下和利用365nm紫外灯照射后的光学照片如图所示,在紫外光下,CQDs溶液和CuNPs@CQDs-PVA膜发射出蓝色荧光;这表明所制备的材料具有极好的荧光性能。
(5)对本发明实施例1制得的材料进行溶胀性能及可生物降解测试;
参见图5中(a)是PVA、CuNPs@CQDs-PVA水凝胶的溶胀性曲线,CuNPs@CQDs的加入增强了PVA水凝胶的吸水性,推测是CuNPs@CQDs的加入使PVA水凝胶产生了更多的三维孔隙;当溶胀平衡时,PVA、CuNPs@CQDs-PVA的吸水量可达自身重量的350%以上,可吸收更多伤口渗出液,这是作为伤口敷料的一个重要性能;作为水凝胶,其保水性尤为重要;(b)是PVA、CuNPs@CQDs-PVA水凝胶的可生物降解性曲线,CuNPs@CQDs-PVA水凝胶以类似于传统敷料的方式抑制暴露伤口上的致病菌,在短时间(从几个小时到几天)使用中,抑菌水凝胶需要保持稳定的状态,不被人体体液中的生物酶降解,确保正常使用;因此,我们对PVA、CuNPs@CQDs-PVA水凝胶进行了PBS溶液降解试验,大量研究表明PVA易于生物降解,我们的测试数据证实了这一点,在降解30天后,PVA失重率达到28%并趋于稳定,而CuNPs@CQDs-PVA水凝胶的降解速率相对PVA来说较慢,推测是因为CuNPs@CQDs填补了原始PVA水凝胶的三维孔隙,接触面减少所致。以上数据足以证明CuNPs@CQDs-PVA水凝胶作为伤口敷料使用时的稳定性。
(6)对本发明实施例1制得的材料进行抑菌性测试;
本实验中,涉及到的抑菌实验具体方法如下:
1)抑菌实验开始前准备工作
实验台清洁干净后,用紫外灯杀菌消毒1h。
固体培养基的配置(500mL):5.0g蛋白胨、2.5g氯化钠、1.5g牛肉膏、6g琼脂,加热溶解于500mL去离子水中,调节pH在7.5左右。
将固体培养基以及实验所用玻璃仪器等置入高压灭菌蒸汽锅中处理20分钟左右。
菌种的活化:适量固体培养基倒入已灭菌试管并放置斜面使其冷却,取冷藏的细菌菌种,用灭菌的接种环刮取斜面菌种呈W字涂至新的试管斜面,并在37℃恒温培养箱中活化细菌24h。待长出一层细菌后将斜面用0.9%的生理盐水刚好没过斜面,刮下斜面菌种溶于生理盐水中,最后将此液体倒入灭菌的锥形试管中,得到菌悬液。
2)抑菌圈法抑菌实验过程
配置固体培养基,同50mL离心管、若干培养皿、若干3mL和1mL移液枪枪头一起置于高压蒸汽灭菌锅中灭菌20分钟。待灭菌完毕,趁热将培养基分别倒入无菌培养皿中,使其静置冷却凝固。
用移液枪移取0.25mL菌悬液放入离心管中,添加10mL无菌水,此即为10
取若干支1mL无菌移液枪头,分别吸取10
将水凝胶切成直径为9mm的圆盘,放置在涂有大肠杆菌悬浮液的固体平板培养基上。膜在37℃恒温生化培养箱中培养。24h后测定抑菌区大小,计算抑菌活性比,计算公式如下:
其中A是测量的抑菌圈大小,A
3)抑菌测试结果
①CQDs的浸渍时间及浸渍浓度对CuNPs@CQDs荧光圈的影响
利用CuNPs@CQDs-PVA水凝胶在紫外光下的荧光来监测伤口敷料的使用情况及抑菌剂的扩散,在这个研究中,荧光是十分关键的观察方式。因此探究了CQDs的浸渍时间及浸渍浓度对CuNPs@CQDs-PVA水凝胶荧光圈的影响。参见图6中(a),在控制其他变量、条件下,随浸渍时间的增长,荧光圈逐渐增大,这是因为时间越长,在多巴胺粘附下,有更多的CQDs包覆CuNPs。考虑时间成本,以24h为最佳浸渍时间。之后,改变CQDs的浸渍浓度;参见图6中(b),在相同浸渍时间下,浸渍高浓度的CQDs,CuNPs@CQDs-PVA水凝胶的荧光圈变大、荧光强度得到增强。最终以12% CQDs为最佳浸渍浓度。
②CuNPs@CQDs/PVA水凝胶随时间增加的荧光圈及铜扩散圈
膜、水凝胶等块状伤口敷料以覆盖皮肤表面的方式对伤口进行给药,而药物需要从敷料扩散到皮肤,再在皮肤上向更宽的范围扩散。本研究利用碳点光致发光的特点来标记CuNPs的扩散。参见图7中(a),以无荧光的DMAA水凝胶作为扩散基质,将CuNPs@CQDs-PVA水凝胶分别放置在DMAA水凝胶上20min、4h、8h、12h、24h、36h,然后用365nm紫外光照射并拍照,最后取出CuNPs@CQDs-PVA水凝胶;参见图7中(b),用铜试剂溶液均匀涂布DMAA水凝胶,5min后拍照观察铜扩散圈。随着CuNPs@CQDs-PVA水凝胶放置在DMAA水凝胶上的扩散时间的增长,DMAA水凝胶上荧光圈及铜扩散圈随之变大。对比图7中(a)和(b)图,发现CuNPs@CQDs-PVA水凝胶在DMAA水凝胶上的荧光圈与铜扩散圈的变化是一致的,这能够表明CuNPs@CQDs是稳定存在于PVA水凝胶中的,CuNPs与CQDs同步扩散,因此CQDs的荧光圈能够代表CuNPs的扩散圈,即能够实现用CQDs的荧光来标记抑菌剂CuNPs的扩散。
③CuNPs@CQDs-PVA水凝胶的抑菌性能
伤口敷料的抑菌性一直以来都是至关重要的。CuNPs@CQDs的添加量影响着CuNPs@CQDs-PVA水凝胶的抑菌率,参见图8中(a),随着CuNPs@CQDs添加的量增多,抑菌性增强,当添加量为0.3g时,抑菌性达到最佳;参见图8中(b),对CuNPs-PVA、CuNPs@CQDs-PVA水凝胶的抑菌持久性进行测试,发现CuNPs-PVA、CuNPs@CQDs-PVA水凝胶在12h、24h、36h时均表现出良好的的抑菌耐久性,表明CuNPs@CQDs-PVA水凝胶作为伤口敷料可以长时间使用,而不缺失抑菌性;参见图8中(c),是对CuNPs@CQDs-PVA水凝胶在各制备阶段的产物的抑菌性分析,PVA、CQDs-PVA水凝胶没有抑菌性,而CuNPs-PVA、CuNPs@CQDs-PVA水凝胶有较好的抑菌性,这表明CuNPs是发挥抑菌作用的关键物质。
(7)对本发明实施例1制得的材料进行抑菌和监测机理分析;
参见图9为本发明实施例1~5制得的CuNPs@CQDs-PVA水凝胶的抑菌与监测机理图,当CuNPs@CQDs-PVA水凝胶做为伤口敷料使用时,其CuNPs@CQDs抑菌剂具有优异的抑菌性,可破坏细菌细胞膜,发生溶胞作用,引起细胞溶解和死亡,快速杀灭伤口上的细菌,以防感染。此外,CuNPs@CQDs具有良好的荧光性能,在紫外光照射下发出蓝色的荧光,这可以很好的监测CuNPs@CQDs药物的扩散情况,及时对伤口给予精准给药,这使得CuNPs@CQDs-PVA水凝胶在伤口敷料中有了更大的应用价值。
铜(Cu)是一种经济高效的抗菌剂,可有效杀死金属表面的病原体,从而破坏细菌的呼吸链和基因复制;同时,铜纳米颗粒(CuNPs)的氧化还原特性,能够对包括脂质和蛋白质在内的细胞造成损伤,对微生物具有一定的杀伤力;碳量子点作为一种新发现的纳米材料,具有许多优异的性能,如低细胞毒性、非常好的生物相容性、高荧光量子产率、稳定的水分散体、优异的化学稳定性,已经在许多领域进行了广泛研究,如药物递送、细胞成像、传感、光电子材料、以及催化作用等;CuNPs易聚集、易氧化,受金属离子猝灭碳点荧光机理的启发,CuNPs氧化后可猝灭CQDs荧光,多巴胺及CQDs具有优异的还原性,以多巴胺为粘附剂包裹CQDs,并包覆在CuNPs表面,可减缓CuNPs的氧化速度。利用PVA优异的生物相容性能,可以作为抑菌药物的载体,将CuNPs@CQDs均匀填充在PVA水凝胶的三维孔隙中,制得一种CuNPs@CQDs-PVA水凝胶,实现了对伤口敷料状态变化的实时监测。
本发明制备的铜纳米粒子包覆碳点实时监测型抑菌水凝胶与传统的伤口敷料相比,制得的CuNPs@CQDs-PVA水凝胶在紫外光下发射出蓝色荧光,具有极好的荧光性能,不仅能抑制细菌生长,促进伤口愈合,还能通过观察CuNPs@CQDs-PVA水凝胶的荧光强弱来判断水凝胶的使用状况,实现对伤口敷料状态变化的实时监测,并及时对伤口给予精准给药。CuNPs@CQDs-PVA水凝胶的延展性非常好,断裂伸长率可达701.81%±7.28%,吸水量可达自身重量的350%以上,有利于吸收伤口渗出液。CuNPs@CQDs稳定存在于PVA水凝胶中的,CuNPs与CQDs同步扩散,CQDs的荧光圈能够代表CuNPs的扩散圈,从而实现用CQDs的荧光来标记抑菌剂CuNPs扩散的目的。CuNPs@CQDs-PVA水凝胶作为伤口敷料可以长时间使用,而不缺失抑菌性,使其在伤口敷料领域具有很好的应用潜力。
以上内容仅为说明本发明的技术思想,不能以此限定本发明的保护范围,凡是按照本发明提出的技术思想,在技术方案基础上所做的任何改动,均落入本发明权利要求书的保护范围之内。
- 一种石墨烯包覆铜纳米粒子复合材料导电油墨及其制备方法
- 一种具有pH响应性的席夫碱共聚物包覆的介孔二氧化硅载药纳米粒子及其制备方法和应用
- 一种碳点修饰二氧化硅纳米粒子基水凝胶复合材料的制备方法及应用
- 一种纳米级碳包覆Mo-Mo2C的异质纳米粒子及其制备方法和应用
