鉴定淫羊藿次生代谢途径中黄酮醇类新化合物的方法
文献发布时间:2023-06-19 19:28:50
技术领域
本发明属于天然产物技术领域,具体涉及鉴定淫羊藿次生代谢途径中黄酮醇类新化合物的方法。
背景技术
淫羊藿(Epimedium brevicornu Maxim)是小檗科(Berberidaceae)淫羊藿属(Epimedium)的多年生草本植物,淫羊藿的主要有效成分是以2-苯基色原酮为母核,在C-8、C-7、C-5、C-3、C-4'位上具有异戊烯基、羟基、糖基、甲氧基的黄酮醇类衍生物。迄今对淫羊藿的物质基础研究已较为深入,主要集中在黄酮醇类成分(如:淫羊藿苷、朝藿定、淫羊藿次苷等);据统计已报道的淫羊藿黄酮醇类成分有70余种,黄酮有20余种。
秦伟瀚等结合淫羊藿黄酮醇成分次生代谢规律及高分辨质谱,构建以巫藿苷为特征产物的生源合成途径,推导验证淫羊藿新化合物的化学结构(秦伟瀚、阳勇、郭延垒、李卿、刘翔.基于巫藿苷为主要代谢产物的生源途径推导及淫羊藿新化合物鉴定分析研究[J].天然产物研究与开发,2020,32(9):11.)。秦伟瀚等还将淫羊藿黄酮次生代谢规律和高分辨质谱法相结合,推导验证淫羊藿新成分的化学结构。通过查阅淫羊藿化学相关文献,构建箭叶淫羊藿素的生源合成途径,推导可能存在的代谢产物(秦伟瀚,阳勇,郭延垒,等.基于箭叶淫羊藿素为主要代谢产物的生源途径推导及淫羊藿新化合物鉴定研究[J].药学学报,2020,55(9):6.)。秦伟瀚等又结合高分辨质谱法探讨淫羊霍特征药效黄酮的质谱裂解规律,并运用该规律鉴定新化合物的化学结构(秦伟瀚,阳勇,李卿,等.基于高分辨质谱法的淫羊藿特征药效黄酮质谱裂解规律及新化合物鉴定研究[J].天然产物研究与开发,2021(033-009).)。
发明内容
本发明为进一步明确淫羊藿特征药效物质-黄酮醇类化合物结构,采用了构建淫羊藿次生代谢途径,通过高分辨质谱鉴定新化合物的方法,该方法鉴定出了2种黄酮醇类新成分及12种黄酮醇类新化合物。
本发明具体采用以下技术方案:
鉴定淫羊藿次生代谢途径中黄酮醇类新化合物的方法,包括以下步骤:
S1:根据淫羊藿黄酮醇类成分的次生代谢规律,构建黄酮醇类成分生物合成途径,推导生物合成途径中可能存在的代谢物,并构建新化合物筛查数据库。
所构建的黄酮醇类成分生物合成途径包括:
途径1:以去甲淫羊藿素为母核在C-3、C-7、C-4’位进行糖苷化、甲基化途径;
途径2:以去甲淫羊藿素C-8位异戊烯基双键水合产物为母核在C-3、C-7、C-4’位进行糖苷化、甲基化途径;
途径3:以去甲淫羊藿素C-8位异戊烯基双键加氢产物为母核在C-3、C-7、C-4’位进行糖苷化、甲基化途径;
途径4:以去甲淫羊藿素C-7位和C-8位基团加成产物为母核在C-3、C-4’位进行糖苷化、甲基化途径。
上述途径中,糖苷化是指:葡萄糖苷、鼠李糖苷、木糖苷的单糖苷化、双糖苷化、叁糖苷化或肆糖苷化。
其中,构建新化合物筛查数据库是将代谢产物信息代入PeakView软件后分析获得。
S2:制备不同品种批次的淫羊藿样品提取液,用质谱仪采集不同品种批次样品数据,将满足质量误差小于5ppm、同位素分布正确且含有二级碎片的离子作为目标化合物,结合已知化合物数据库及二级碎片裂解规律,鉴定验证推导的新化合物的化学结构。
其中,采用50%的乙醇水溶液对淫羊藿样品粉末进行超声提取30min,过滤。其中,50%的乙醇水溶液和淫羊藿样品粉末的比例为2mL:0.1g。
上述方法验证的新化合物包括:结构式分别为M1、M2、M3、M5、M6、M7、M8、M9、M11、M12、M13、M14所示的新化合物:
/>
/>
采用上述方法还鉴定验证了2个结构式如M4和M10所示的新成分:
本发明的有益效果为:
本发明通过构建淫羊藿黄酮醇次生代谢网络推导出的化合物结构达100余个,结合高分辨质谱在15个品种54批次淫羊藿样品中鉴定出了2种新成分及12种新化合物,可能与品种样本数量、生长环境、采集时间、加工方式等因素有关。
本发明通过分析总结淫羊藿中含异戊烯基黄酮醇类成分次生代谢规律可以发现,母核(去甲淫羊藿素)羟基甲基化基本发生在C-4’位,葡萄糖苷化多发生在C-7位,而鼠李糖苷化则多发生在C-3位,表明黄酮醇生物合成途径存在多种相似的生化反应类型。
附图说明
图1为淫羊藿特征黄酮醇代谢途径1。
图2为淫羊藿特征黄酮醇代谢途径2。
图3为淫羊藿特征黄酮醇代谢途径3。
图4为淫羊藿特征黄酮醇代谢途径4。
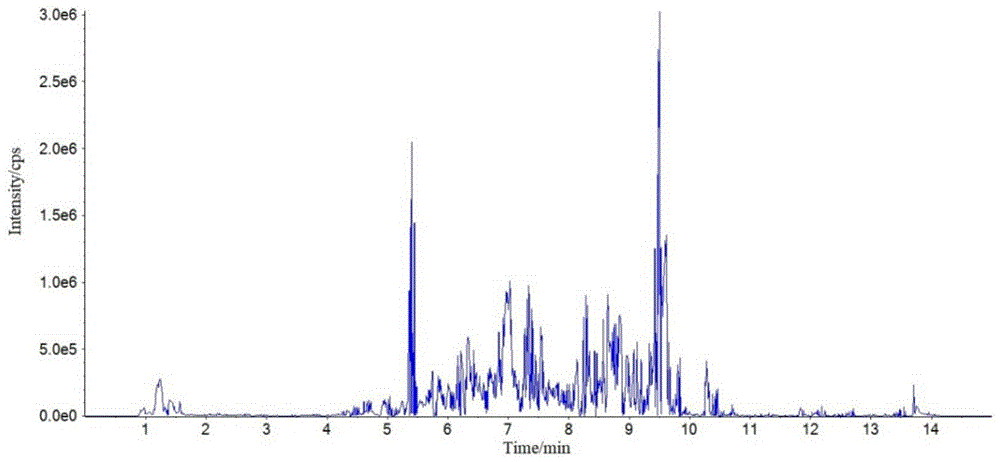
图5为样品总离子流图。
图6为化合物M1的提取离子图(A)及二级碎片裂解规律图(B)。
图7为化合物M2的提取离子图(A)及二级碎片裂解规律图(B)。
图8为化合物M3的提取离子图(A)及二级碎片裂解规律图(B)。
图9为化合物M4的提取离子图(A)及二级碎片裂解规律图(B)。
图10为化合物M5的提取离子图(A)及二级碎片裂解规律图(B)。
图11为化合物M6的提取离子图(A)及二级碎片裂解规律图(B)。
图12为化合物M7的提取离子图(A)及二级碎片裂解规律图(B)。
图13为化合物M8的提取离子图(A)及二级碎片裂解规律图(B)。
图14为化合物M9的提取离子图(A)及二级碎片裂解规律图(B)。
图15为化合物M10的提取离子图(A)及二级碎片裂解规律图(B)。
图16为化合物M11的提取离子图(A)及二级碎片裂解规律图(B)。
图17为化合物M12的提取离子图(A)及二级碎片裂解规律图(B)。
图18为化合物M13的提取离子图(A)及二级碎片裂解规律图(B)。
图19为化合物M14的提取离子图(A)及二级碎片裂解规律图(B)。
具体实施方式
下面通过具体实施方式对本发明进行更加详细的说明,以便于对本发明技术方案的理解,但并不用于对本发明保护范围的限制。
本实施例中所述新成分是该化合物已经被鉴定出来但没有在淫羊藿中发现,新化合物是没有鉴定出来的化合物。
(一)仪器与试药
1、仪器
LC-30A型超高效液相色谱仪(日本,岛津公司):二元高压泵、自动进样器、柱温箱;Triple TOF
2、试药
对照品淫羊藿苷(批号:489-32-7)、淫羊藿次苷I(批号:56725-99-6)、淫羊藿次苷II(批号:113558-15-9)、朝藿定A(批号:110623-72-8)、朝藿定B(批号:110623-73-9)、朝藿定C(批号:110642-44-9)、箭叶淫羊藿苷A(批号:118525-35-2)、箭叶淫羊藿苷B(批号:118525-36-3)、鼠李糖淫羊藿次苷II(批号:135293-13-9)、宝藿苷II(批号:55395-07-8)、淫羊藿属苷A(批号:39012-04-9)、去甲淫羊藿素(批号:28610-31-3)、宝藿苷V(批号:118544-18-6)、粗毛淫羊藿苷(批号:143601-07-4),质量分数均大于98%,均购于成都埃法生物科技有限公司;乙腈(色谱级,德国Merck公司)、甲酸(色谱级,美国ACS公司),其余试剂为分析纯。不同品种淫羊藿样品采自于重庆、四川、湖北、湖南等地,经鉴定为小檗科多年生草本植物淫羊藿的地上部分。54批样品信息见表1。
表1淫羊藿样品采集信息
(二)实验方法
1、质谱条件
电喷雾离子源(ESI),正离子模式采集数据,喷雾电压(IS):+5500V;雾化气压力(GS1):0.37MPa;气帘气压力(CUR):0.16MPa;辅助气压力(GS2):0.37MPa;离子源温度(TEMP):600℃;簇裂解电压(DP):60V;碰撞能量(CE):45V;碰撞能量滚动区间(CES):15V;检测模式为IDA(信息关联采集模式),多重质量亏损(MMDF)和动态背景扣除(DBS)为触发二级的条件,满足该条件优先进行二级扫描。
2、样品溶液制备
取淫羊藿样品粉末约0.1g,精密称定,置5mL试管中,精密加入50%的乙醇水溶液2mL,密塞,称定质量,超声处理(功率:600W)30min,放冷,再次称定质量,用50%乙醇溶液补足减失质量,涡旋混匀,过滤,精密量取续滤液1mL提取液于10mL容量瓶中,加色谱甲醇定容至刻度,摇匀,用0.22μm微孔滤膜滤过于进样瓶中,即得。
3、数据分析处理
根据淫羊藿黄酮醇类成分的次生代谢规律构建其生物合成途径,推导可能存在的代谢产物,并将代谢产物信息代入PeakView软件,构建新化合物筛查数据库;提取分析Q-TOF采集的不同品种批次样品数据,将满足质量误差小于5ppm、同位素分布正确且含有二级碎片的离子作为目标化合物,结合软件Formula Finder、Mass Calculators等功能、在线数据库(SciFinder、Reaxys、ChemSpider、Metlin、HMDB)及二级碎片裂解规律,鉴定验证推导化合物的化学结构。
(三)黄酮醇类实验鉴定结果
1、黄酮醇途径新成分、新化合物鉴定结果
本实施例根据黄酮醇的次生代谢规律,构建了4条代谢途径。
途径1为以去甲淫羊藿素为母核在C-3、C-7、C-4’位进行糖苷化、甲基化途径(图1),该途径已知成分有41种,结合高分辨质谱法共鉴定出了2个新化合物(M1、M2)。
途径2为以去甲淫羊藿素C-8位异戊烯基双键水合产物为母核在C-3、C-7、C-4’位进行糖苷化、甲基化途径(图2),该途径共涉及到21个化合物,其中有4个为已知成分,分别为Noricarliin、Maohuoside A、Icaritin-3-O-α-rhamnoside、Wanepimedoside A,结合高分辨质谱法共鉴定出了1个新化合物(M3)和1个新成分(M4)。
途径3为以去甲淫羊藿素C-8位异戊烯基双键加氢产物为母核在C-3、C-7、C-4’位进行糖苷化、甲基化途径(图3),该途径共涉及到21个化合物,已知成分仅ICARISID II,结合高分辨质谱法共鉴定出了4个新化合物(M5~M8)。
途径4为以去甲淫羊藿素C-7位和C-8位基团加成产物为母核在C-3、C-4’位进行糖苷化、甲基化途径(图4),该途径共涉及到22个化合物,其中有3个为已知成分,分别为Anhydrocicaritin、Ikarisoside E、Acuminatin,结合高分辨质谱法共鉴定出了6个新化合物(M9,M11~M14)和1个新成分(M10)。上述鉴定结果见表2,样品的总离子流图见图5。
表2淫羊藿黄酮醇类新化合物、新成分鉴定结果表
2、新成分、新化合物的高分辨质谱验证分析
新化合物M1,分子式为C
新化合物M2,分子式为C
新化合物M3,分子式为C
新成分M4,分子式为C
新化合物M5,分子式为C
新化合物M6,分子式为C
新化合物M7,分子式为C
新化合物M8,分子式为C
新化合物M9,分子式为C
新成分M10,分子式为C
新化合物M11,分子式为C
新化合物M12,分子式为C
新化合物M13,分子式为C
新化合物M14,分子式为C
3、黄酮醇途径新化合物推导过程
(1)途径1推导过程
该途径存在两种单糖苷成分,即母核(去甲淫羊藿素)在C-7位键合葡萄糖苷的Epimedoside C和C-3位键合鼠李糖苷的Baohuoside II,由次生代谢规律图(图1)可知,Epimedoside D的C-3位键合有一分子的木糖苷,据此推测可能存在母核上键合木糖苷的化合物,将该化合物分子式代入PeakView软件,对15个品种淫羊藿样品的一级、二级质谱进行提取,并结合在线数据库、二级碎片和质谱裂解规律进行分析,并未发现单加木糖苷及其甲基化产物。Epimedoside D的C-7位还键合有一分子葡萄糖苷,而其它含木糖苷成分均连接在C-3位鼠李糖苷之上,提示木糖苷不能直接键合在母核上面,只有在C-7位羟基结合葡萄糖苷之后才能发生该生化反应。
由图1可知,以Baohuoside II为底物,生成的双糖苷化合物均有文献报道,而以Epimedoside C为底物的双糖苷产物仅发现Hexandraside E和Epimedoside A,再结合Epimedoside D的化学结构,推测可能存在含C-3位木糖苷、C-7位葡萄糖苷的双糖苷化合物,并由此鉴定出了M1和M2。
由于该途径存在着叁糖苷和肆糖苷化合物,本实施例根据次生代谢规律也进行了相应分析,但未鉴定出一种该类成分,这可能与淫羊藿品种、生长环境、代谢积累、酶活性等多种因素相关。
(2)途径2推导过程
由该途径次生代谢规律图(图2)可以看出,母核(Noricarliin)是去甲淫羊藿素C-8位异戊烯基的双键加成一分子水所得,分析途径中其它3个已知成分结构,均为C-3、C-7位羟基糖苷化以及C-4’位羟基甲基化产物,据此推测该途径是母核在糖基转移酶和甲基转移酶的催化作用下发生一系列的生物化学反应,生成单糖苷、双糖苷及甲基化产物。Noricarliin的C-4’位羟基结合甲基后生成M3;母核的C-7、C-4’位羟基键合葡萄糖苷和甲基可以生成Maohuoside A,故推测在生物合成Maohuoside A之前可能有未被甲氧化的M4存在,结合PeakView软件、二级碎片和质谱裂解规律也验证了2个新化合物的推导结果,在该途径中未鉴定出含木糖的单糖苷和除Wanepimedoside A外的双糖苷化合物。相较于去甲淫羊藿素结构,该途径母核C-8位异戊烯基发生了双键水合加成,但C-3、C-7、C-4’位羟基活性依然存在,作为底物在转移酶的催化作用下同样有可能发生多种生化反应,结合4个已知成分的化学结构就能佐证上述推论。从该途径的17个未知成分中仅鉴定出2个新化合物,可能与底物含量和关键酶活性较低有关。
(3)途径3推导过程
由该途径次生代谢规律图(图3)可以看出,母核(M5)为去甲淫羊藿素C-8位异戊烯基双键加氢后产物,整个途径推导过程与途径2一致。母核C-4’位羟基甲基化生成M6,M7是母核键合一分子葡萄糖苷并甲基化产物,M8为C-3、C-7位羟基分别键合鼠李糖苷、葡萄糖苷的双糖苷化合物;结合PeakView软件、二级碎片和质谱裂解规律验证了4个新化合物的推导结果,在此途径中未鉴定出含有木糖的单糖苷及双糖苷化合物。在淫羊藿的62个已知黄酮醇类成分中,仅ICARISID II的C-8位异戊烯基双键被还原,也是该途径中唯一的已知成分,在植物体内存在着大量的氧化还原酶类,加氢是常见的还原反应类型,据此推测去甲淫羊藿素C-8位上异戊烯基可能会发生双键加氢反应,并形成一系列的代谢产物。通过分析高分辨质谱数据发现,鉴定出的4个新化合物二级质谱仅M6有脱去C
(4)途径4推导过程
由于该途径母核(M9)的C-8位异戊烯基与C-7位的羟基成环,导致C-7位羟基不能再与糖苷结合,故而能发生糖苷化的活性基团仅为C-3位羟基,而C-4’位羟基只能发生甲基化,C-5位羟基则不具反应活性。由次生代谢网络图(图4)可知,去甲淫羊藿素C-7、C-8位环化可以生成M9,M9的C-4’位再发生甲基化可生成Anhydrocicaritin。参比Ikarisoside E和Acuminatin的结构,可以发现,Acuminatin是由Ikarisoside E的C-4’位甲基化所生成,而与M9相较,C-7、C-8位基团环化后会再一次脱氢形成双键,C-3位则结合一分子鼠李糖苷。据此推测M9的基团成环脱氢后可生成M10,而M10的C-4’位可以再甲基化生成M11,同时M10的C-3位羟基还可以发生糖苷化反应。根据以上推导结果,采用ChemDraw软件构建途径中所有化合物的结构式,并将化合物信息导入PeakView软件,对15个品种淫羊藿的50个批次样品数据进行提取分析,结合在线数据库、二级碎片及质谱裂解规律,鉴定出M10的C-3位羟基还可以结合葡萄糖苷(M12)进而C-4’位羟基甲基化(M13)产物;并且在Ikarisoside E结构的基础上可以再键合1分子葡萄糖或鼠李糖生成两个双糖苷化合物(M14)。由于母核的C-7位羟基被屏蔽,导致该基团糖苷化活性丧失,由该途径推导结果可以看出,C-3位没有鉴定出含木糖苷的化合物,这也与其它途径推导结果一致。该途径没有探讨叁糖苷化合物,是因为在淫羊藿已知黄酮醇成分中没有发现在C-3位结合糖苷数量有超过2个的成分。
以上所述之实施例,只是本发明的较佳实施例而已,并非限制本发明的实施范围,故凡依本发明专利范围所述的构造、特征及原理所做的等效变化或修饰,均应包括于本发明申请专利范围内。
