一种氮杂蒽醌类生物碱的制备方法及应用
文献发布时间:2023-06-19 11:34:14
技术领域
一种氮杂蒽醌类生物碱的制备方法及应用,属于氮杂蒽醌类生物碱制备及应用技术领域。
背景技术
氮杂蒽醌类生物碱scorpinone是由真菌代谢产生的聚酮化合物的衍生物,最早是从一株海洋真菌中发现(Miljkovic A., Mantle P. G., Williams D. J., Rassing B.,Scorpinone, a new natural azaanthraquinone produced by a Bispora-liketropical fungus[J]. Journal of Natural Products, 2001, 64, 1251–1253)。其具有重要生物学活性天然生物碱的母核结构,通常的结构包括苯并[g]喹啉-5,10-二酮、吡啶并[3,2-g]喹啉-5,10-二酮等或其衍生物,其中最简单的氮杂蒽醌类生物碱是Cleistopholine。氮杂蒽醌类生物碱平面结构式见式(I)。
植物内生真菌是一种特殊生境微生物,是指在其生活史的一定阶段或者全部阶段无症状地存在于植物表皮细胞层以下的内部组织中,而不使宿主植物表现明显病害症状的真菌(Wilson D. Endophyte: The Evolution of a Term, and Clarification of ItsUse and Definition [J]. Oikos, 1995, 73(2): 274-276)。
发明内容
本发明所要解决的技术问题是:克服现有技术的不足,提供一种成本低,生产过程绿色环保且易于规模化的氮杂蒽醌类生物碱的制备方法及应用。
本发明解决其技术问题所采用的技术方案是:一种氮杂蒽醌类生物碱的制备方法,其特征在于:包括以下步骤:
1)从中药赤芍中分离得到内生真菌;
2)按重量份:马铃薯200份,酵母膏8~12份,蛋白胨5~7份,葡萄糖25~35份,KH
3)取大米与水配匀灭菌后加入步骤2)所得种子液培养40天,大米:水:种子液按重量比1.5:1.5~2.0:0.18~0.22;
4)取步骤3)所得培养液加入1.4~1.6倍体积的乙酸乙酯浸泡50~70min,然后超声25~35分钟过滤取滤液,重复3次,滤液减压浓缩,去除溶剂,得浸膏,浸膏经常压硅胶柱色谱梯度洗脱7次,依次得组分F1~F7,F7经Flash柱色谱梯度洗脱5次,依次得组分F7-1~F7-5,F7-5经HPLC半制备色谱分离得氮杂蒽醌类生物碱。
通过真菌发酵提取的方式获得氮杂蒽醌类生物碱,真菌培养成本低,提取简单,产量高,绿色环保,易于规模化。
优选的,步骤4)所述的常压硅胶柱色谱洗脱条件为:依次采用石油:醚丙酮体积比=100:1、50:1、30:1、20:1、10:1、5:1、1:1洗脱。此洗脱条件洗脱更充分,同时损失最少。
优选的,步骤4)所述的Flash柱色谱采用C18柱,洗脱条件为依次采用30%、40%、50%、60%、65%体积浓度的甲醇水溶液洗脱。此洗脱条件洗脱更充分,同时损失最少。
优选的,步骤4)所述的HPLC半制备色谱分离条件为:采用ES-C18色谱柱,体积浓度50% 的甲醇水溶液,检测器波长设为280 nm。
优选的,步骤2)灭菌前培养液分装至500ml三角瓶,每瓶装培养液150ml。更易于菌株培养。
优选的,步骤2)与步骤3)中的灭菌采用115℃,在68kPa下灭菌30min。配合上述分装条件,培养效果更好。
优选的,步骤2)所述的旋转培养采用155转/min。
一种上述的氮杂蒽醌类生物碱的应用,其特征在于:用于制备抗炎药物。
本发明所述的氮杂蒽醌类生物碱机器可药用盐可根据现有技术来制备成口服药物制剂、注射剂等。
与现有技术相比,本发明所具有的有益效果是:本发明所述的氮杂蒽醌类生物碱通过真菌发酵获得,不仅产量高,而且绿色环保,利于可持续的工业化生产,成本低。同时,氮杂蒽醌类生物碱抑制脂多糖(LPS)诱导小鼠巨噬细胞RAW264.7释放一氧化氮(NO)的IC
附图说明
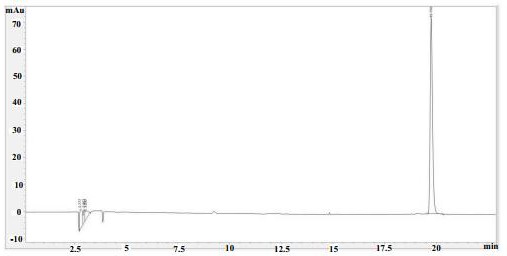
图1为实施例1所得产品色谱图。
具体实施方式
下面结合实施例对本发明做进一步说明,实施例1是本发明的最佳实施例。
实施例1
一种氮杂蒽醌类生物碱的制备方法,包括以下步骤:
1)从中药赤芍(Paeonia lactiflora Pall.)中分离得到内生真菌,该菌的纯菌种利用NCBI-BlastN 2.0.6 +,通过核酸序列的比对鉴定为Ophiosimulans tanaceti 菌株;
2)制备菌种液体种子液:按重量份:马铃薯200g,酵母膏10g,蛋白胨6g,葡萄糖30g,KH
3)菌株固体发酵:取30个1L三角瓶,每1L三角瓶装大米150g、纯净水180ml,大米与水配匀后,115 ℃,68 kPa,灭菌30分钟,每瓶加入步骤2)所得种子液20ml室温培养40天;
4)提取分离:每瓶固体发酵物加入500ml乙酸乙酯浸泡50~70min,然后超声30分钟过滤取滤液,重复3次,滤液减压浓缩,去除溶剂,得总浸膏30g,浸膏经常压硅胶柱色谱梯度洗脱7次,洗脱条件为:依次采用石油:醚丙酮体积比=100:1、50:1、30:1、20:1、10:1、5:1、1:1洗脱,依次得到组分F1~F7,F7经Flash柱色谱梯度洗脱5次,Flash柱色谱采用C18柱,洗脱条件为依次采用30%、40%、50%、60%、65%体积浓度的甲醇水溶液洗脱,依次得组分F7-1~F7-5,F7-5经HPLC半制备色谱分离,HPLC半制备色谱分离条件为:采用ES-C18色谱柱,体积浓度50% 的甲醇水溶液,检测器波长设为280 nm。得到氮杂蒽醌类生物碱scorpinone(保留时间为19 .8min,103 mg)。
实施例2
一种氮杂蒽醌类生物碱的制备方法,在实施例1的基础上,步骤2)所用KH
实施例3
一种氮杂蒽醌类生物碱的制备方法,在实施例1的基础上,步骤3)采用大米150g、纯净水200ml,种子液22ml进行君主固体发酵,其他条件与实施例1相同。
实施例4
一种上述的氮杂蒽醌类生物碱的应用,用于制备抗炎药物。
采用Griess 法考察化合物抑制 LPS 诱导小鼠巨噬细胞 RAW 264.7 释放 NO 能力。取生长状态良好且处于对数生长期的细胞,将浓度为 1 ×106 cell•mL-1 的RAW264.7细胞接种于 96 孔板内,在 37 ℃、 5% CO2 培养箱中培养 24 h。 24 h 后,加入含有LPS(终浓度 0.5 µg•mL-1)不同药物浓度的培养基,同时设空白组和 LPS 组,于37 ℃、5% CO
结果表明,氮杂蒽醌类生物碱scorpinone及含有氮杂蒽醌类生物碱scorpinone的Ophiosimulans tanaceti 菌株发酵提取物均可显著抑制LPS诱导小鼠巨噬细胞RAW264.7释放NO,IC
因此,可以证明本发明所得的氮杂蒽醌类生物碱具有药理活性。按照常规技术手段,与药学上可接受的载体、和/或赋形剂,制成适用于口服或注射等应用形式制剂,例如,按常规技术,加入药物可接受的载体和/或赋形剂制成片剂、胶囊剂、粉剂、糖浆剂、针剂等。
对比例1
一种氮杂蒽醌类生物碱的制备方法,在实施例1的基础上,KH
性能测试
检测实施例1所得产品,性状为黄色粉末;核磁共振检测结果为:
ESI-MS:[M]
色谱图见图1。
可证明所得产品为氮杂蒽醌类生物碱 scorpinone且纯度大于98%。
以上所述,仅是本发明的较佳实施例而已,并非是对本发明作其它形式的限制,任何熟悉本专业的技术人员可能利用上述揭示的技术内容加以变更或改型为等同变化的等效实施例。但是凡是未脱离本发明技术方案内容,依据本发明的技术实质对以上实施例所作的任何简单修改、等同变化与改型,仍属于本发明技术方案的保护范围。
- 一种氮杂蒽醌类生物碱的制备方法及应用
- 一种手性3.3.1氮杂桥环吲哚生物碱衍生物及其制备方法和应用
