治疗滤泡型淋巴瘤的方法
文献发布时间:2023-06-19 11:57:35
本申请要求2018年11月30日提交的美国临时申请62/773,678的优先权,该申请的公开内容据此全文以引用方式并入。
技术领域
本文提供了治疗滤泡型淋巴瘤(FL)和基因突变的方法,该方法可用于预测受试者对用依鲁替尼治疗滤泡型淋巴瘤的无反应。
背景技术
滤泡型淋巴瘤的基因图谱是复杂的。除了标志t(14;18)易位导致BCL2过表达外,分子遗传学研究也已经鉴定了许多基因中的复发性体细胞突变。此类突变可降低受试者对治疗的反应。
发明内容
本文提供了治疗受试者的滤泡型淋巴瘤(FL)的方法,该方法包括向受试者施用治疗有效量的依鲁替尼,从而治疗FL,其中受试者在选自以下的一个或多个基因中不具有如表2中所定义的一个或多个突变:AHNAK、ARID1A、ATP6AP1、BCL9L、CLTC、CNOT1、EP400、KDM2B、MYBBP1A、NACA、NBPF1、NBPF10、NCOA4、NEDD4L、PRDM16、SOCS1和TBL1XR1。
还提供了预测患有滤泡型淋巴瘤的受试者中对依鲁替尼无反应的可能性的方法,该方法包括分析来自受试者的样本中选自以下的一个或多个基因中的如表2中所定义的突变中的一个或多个突变:AHNAK、ARID1A、ATP6AP1、BCL9L、CLTC、CNOT1、EP400、KDM2B、MYBBP1A、NACA、NBPF1、NBPF10、NCOA4、NEDD4L、PRDM16、SOCS1和TBL1XR1,其中一个或多个基因中的突变中的一个或多个突变指示对依鲁替尼无反应。
附图说明
当结合附图阅读时,进一步理解发明内容以及下文的具体实施方式。出于示出本发明所公开方法的目的,附图中所示的是本发明方法的示例性实施方案;然而,所述方法不限于所公开的具体实施方案。在附图中:
图1示出了在DAWN研究患者中具有反应者数据(N=83)的突变基因的数量。
图2示出了来自DAWN研究的>10%的样本(75个基因)中突变的基因的热图。
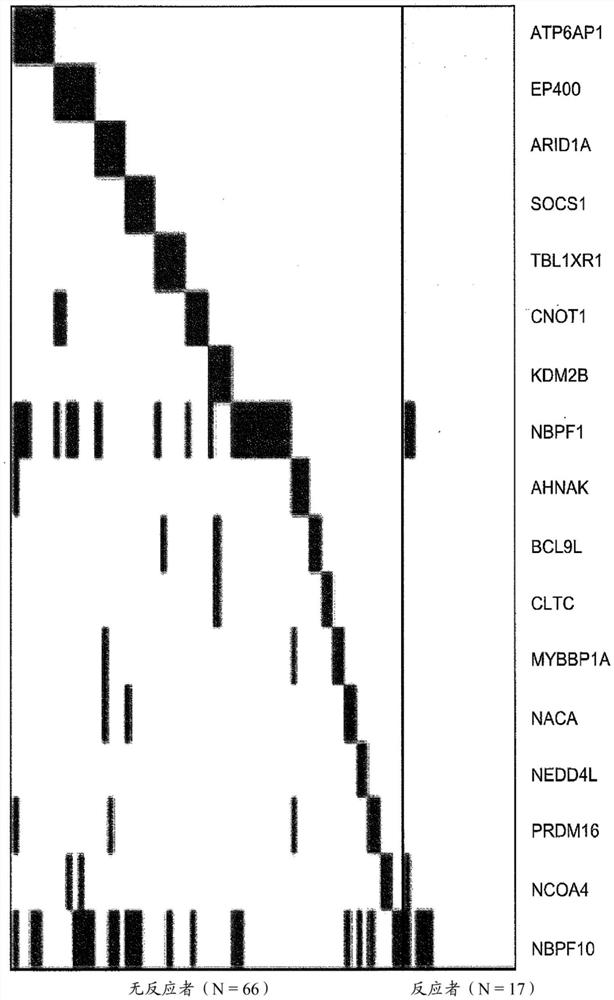
图3示出了来自DAWN研究的排序的无反应者基因突变的热图。
图4示出了基于交叉验证研究的预测的反应者的平均ORR。
图5是DAWN患者中ATP6AP1基因中的体细胞突变的示例性图。
图6是DAWN患者中EP400基因中的体细胞突变的示例性图。
图7是DAWN患者中的ARID1A基因中的体细胞突变的示例性图。
图8是DAWN患者中SOCS1基因中的体细胞突变的示例性图。
图9是DAWN患者中TBL1XR1基因中的体细胞突变的示例性图。
具体实施方式
结合形成本公开一部分的附图,并参考以下具体实施方式,可更容易地理解本发明所公开的方法。应当理解,本发明所公开的方法不限于本文所描述和/或示出的具体方法,并且本文所用的术语仅用于以举例方式描述具体实施方案,并不旨在限制受权利要求书保护的方法。
除非另外特别说明,否则关于可能的机制或作用模式或改善原因的任何描述仅旨在出于示例性目的,并且本发明所公开的方法不受任何此类建议的机制或作用模式或改善原因的正确或错误的约束。
当本文列举或建立数值范围时,该范围包括其端值以及该范围内的所有单独整数和分数,并且也包括其中由那些端值以及内部整数和分数的所有各种可能组合形成的较窄范围中的每一者,以在相同程度上形成所述范围内的较大数值组的亚组,如同明确列举了那些较窄范围中的每一者一样。不旨在将方法的范围限于当限定范围时所列举的特定值。所有范围均包括端值在内并且可组合。
当前面使用“约”将值表示为近似值时,应当理解,该具体值构成了另一个实施方案。提及具体数值至少包括该具体值,除非上下文另有明确规定。
应当理解,本发明所公开的方法的某些特征为清楚起见在本文各单独实施方案的上下文中进行描述,但也可以组合形式提供在单个实施方案中。相反地,本文所公开的方法的各种特征为简明起见在单个实施方案的上下文中进行描述,也可分开地或以任何子组合形式提供。
如本文所用,单数形式“一个”、“一种”和“该”包括复数形式。
与说明书的各方面相关的各种术语在说明书和权利要求书中通篇使用。除非另外指明,否则此类术语被赋予本领域的普通含义。其它具体定义的术语应按照与本文所提供的定义相符的方式理解。
当参考数值范围、截止值或特定值使用时,术语“约”用于指示所列举的值可与所列出的值相差多达10%。因此,术语“约”用于涵盖与指定值相差±10%或更小的变化、±5%或更小的变化、±1%或更小的变化、±0.5%或更小的变化、或者±0.1%或更小的变化。
术语“包含”旨在包括由术语“基本上由……组成”和“由……组成”涵盖的示例;类似地,术语“基本上由……组成”旨在包括由术语“由……组成”所涵盖的示例。
美国和其它国家批准用于多种B细胞恶性肿瘤的布鲁顿酪氨酸激酶(BTK)的第一类口服共价抑制剂依鲁替尼破坏恶性B细胞的粘附、增殖、归巢和生存所必需的信号传导途径。
“治疗(Treat、treatment)”及类似的术语包括降低症状的严重性和/或频率、消除症状和/或症状的根本原因、降低症状的频率或可能性和/或其根本原因、以及改善或补救由滤泡型淋巴瘤直接或间接造成的损害。治疗包括对所施用的药剂(依鲁替尼)的完全反应和部分反应。治疗也包括与未接受治疗的受试者的预期生存期相比延长生存期。
如本文所用,短语“治疗有效量”是指如本文所述的有效实现特定生物学或治疗结果(诸如但不限于本文所公开、描述或例示的生物学或治疗结果)的依鲁替尼的量。治疗有效量可根据以下因素而变化:诸如个体的疾病状态、年龄、性别和体重,以及组合物在受试者中引发期望的反应的能力。治疗有效量的示例性指标包括例如患者健康状况改善、肿瘤负荷减少、滤泡型淋巴瘤生长被遏止或减慢、以及/或者滤泡型淋巴瘤细胞没有向身体其它部位转移。
如本文所用,术语“受试者”旨在表示人。“受试者”和“患者”在本文中可互换使用。
本文使用以下缩写:布鲁顿酪氨酸激酶(BTK);复发性或难治性(R/R);总反应率(ORR);总生存期(OS);滤泡型淋巴瘤(FL);完全反应(CR);以及部分反应(PR)。
本文提供了治疗受试者的滤泡型淋巴瘤(FL)的方法,该方法包括:向受试者施用治疗有效量的依鲁替尼,从而治疗FL,其中受试者在选自以下的一个或多个基因中不具有如表2中所定义的一个或多个突变:AHNAK、ARID1A、ATP6AP1、BCL9L、CLTC、CNOT1、EP400、KDM2B、MYBBP1A、NACA、NBPF1、NBPF10、NCOA4、NEDD4L、PRDM16、SOCS1和TBL1XR1。
AHNAK、ARID1A、ATP6AP1、BCL9L、CLTC、CNOT1、EP400、KDM2B、MYBBP1A、NACA、NBPF1、NBPF10、NCOA4、NEDD4L、PRDM16、SOCS1和TBL1XR1中的一者或多者中的表2中提供的突变与对依鲁替尼治疗无反应相关联,如本文所公开的。因此,该方法包括向受试者施用治疗有效量的依鲁替尼,从而治疗FL,其中受试者在选自以下的一个或多个基因中不具有如表2中所定义的一个或多个突变:AHNAK、ARID1A、ATP6AP1、BCL9L、CLTC、CNOT1、EP400、KDM2B、MYBBP1A、NACA、NBPF1、NBPF10、NCOA4、NEDD4L、PRDM16、SOCS1和TBL1XR1。该方法可对在如表2中提供的AHNAK、ARID1A、ATP6AP1、BCL9L、CLTC、CNOT1、EP400、KDM2B、MYBBP1A、NACA、NBPF1、NBPF10、NCOA4、NEDD4L、PRDM16、SOCS1和TBL1XR1中的1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16个或所有17个中不具有如表2中所定义的一个或多个突变及其各种组合的受试者进行。
本发明还公开了治疗受试者的滤泡型淋巴瘤(FL)的方法,该方法包括:向患有FL但在选自以下的一个或多个基因中不具有如表2中所定义的一个或多个突变的受试者施用治疗有效量的依鲁替尼,从而治疗FL:AHNAK、ARID1A、ATP6AP1、BCL9L、CLTC、CNOT1、EP400、KDM2B、MYBBP1A、NACA、NBPF1、NBPF10、NCOA4、NEDD4L、PRDM16、SOCS1和TBL1XR1。
还提供了治疗在选自以下的一个或多个基因中不具有如表2中所定义的一个或多个突变的受试者的滤泡型淋巴瘤(FL)的方法:AHNAK、ARID1A、ATP6AP1、BCL9L、CLTC、CNOT1、EP400、KDM2B、MYBBP1A、NACA、NBPF1、NBPF10、NCOA4、NEDD4L、PRDM16、SOCS1和TBL1XR1,该方法包括向受试者施用治疗有效量的依鲁替尼,从而治疗FL。
依鲁替尼的治疗有效量可包括约420mg至约840mg。例如,依鲁替尼的治疗有效量可包括约420mg、440mg、460mg、480mg、500mg、520mg、540mg、560mg、580mg、600mg、620mg、640mg、660mg、680mg、700mg、720mg、740mg、760mg、780mg、800mg、820mg或840mg。在一些实施方案中,依鲁替尼的治疗有效量为560mg。
在一些实施方案中,FL为复发性/难治性(R/R)FL。
适用于治疗的受试者包括在施用之前具有如下情况的受试者:
·具有1级、2级或3a级非转化FL的诊断;
·已用≥2条先前的治疗线进行了治疗;
·对使用含抗CD20单克隆抗体的化学免疫疗法方案的最后一条先前的治疗线是R/R的;或
·它们的任何组合。
在一些实施方案中,受试者可具有部分反应。在一些实施方案中,受试者可具有完全反应。
还提供了依鲁替尼在制造药物中的用途,该药物用于治疗在选自以下的一个或多个基因中不具有如表2中所定义的一个或多个突变的受试者的滤泡型淋巴瘤(FL):AHNAK、ARID1A、ATP6AP1、BCL9L、CLTC、CNOT1、EP400、KDM2B、MYBBP1A、NACA、NBPF1、NBPF10、NCOA4、NEDD4L、PRDM16、SOCS1和TBL1XR1。
还提供了用于治疗在选自以下的一个或多个基因中不具有如表2中所定义的一个或多个突变的受试者的滤泡型淋巴瘤(FL)的用途的依鲁替尼:AHNAK、ARID1A、ATP6AP1、BCL9L、CLTC、CNOT1、EP400、KDM2B、MYBBP1A、NACA、NBPF1、NBPF10、NCOA4、NEDD4L、PRDM16、SOCS1和TBL1XR1。
提供了预测患有滤泡型淋巴瘤的受试者中对依鲁替尼无反应的可能性的方法,该方法包括:分析来自受试者的样本中选自以下的一个或多个基因中的如表2中所定义的一个或多个突变:AHNAK、ARID1A、ATP6AP1、BCL9L、CLTC、CNOT1、EP400、KDM2B、MYBBP1A、NACA、NBPF1、NBPF10、NCOA4、NEDD4L、PRDM16、SOCS1和TBL1XR1,其中一个或多个基因中的突变指示对依鲁替尼无反应。
AHNAK、ARID1A、ATP6AP1、BCL9L、CLTC、CNOT1、EP400、KDM2B、MYBBP1A、NACA、NBPF1、NBPF10、NCOA4、NEDD4L、PRDM16、SOCS1和TBL1XR1中的一者或多者中的表2中提供的突变指示对依鲁替尼治疗无反应,如本文所公开的。如表2中提供的AHNAK、ARID1A、ATP6AP1、BCL9L、CLTC、CNOT1、EP400、KDM2B、MYBBP1A、NACA、NBPF1、NBPF10、NCOA4、NEDD4L、PRDM16、SOCS1和TBL1XR1中的1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16个或所有17个中的突变及其各种组合可指示对依鲁替尼治疗无反应。
在一些实施方案中,该方法包括分析来自受试者的样本中选自以下的一个或多个基因中的如表2中所定义的一个或多个突变:AHNAK、ARID1A、ATP6AP1、BCL9L、CLTC、CNOT1、EP400、KDM2B、MYBBP1A、NACA、NBPF1、NBPF10、NCOA4、NEDD4L、PRDM16、SOCS1和TBL1XR1,其中一个或多个基因中缺少一个或多个突变指示对依鲁替尼有反应。
在一些实施方案中,将预测患有滤泡型淋巴瘤的受试者中对依鲁替尼无反应的可能性的方法与后续的滤泡型淋巴瘤治疗相结合。因此,提供了治疗受试者中滤泡型淋巴瘤(FL)的方法,该方法包括:分析来自受试者的样本中选自以下的一个或多个基因中的如表2中所定义的一个或多个突变:AHNAK、ARID1A、ATP6AP1、BCL9L、CLTC、CNOT1、EP400、KDM2B、MYBBP1A、NACA、NBPF1、NBPF10、NCOA4、NEDD4L、PRDM16、SOCS1和TBL1XR1,其中一个或多个基因中的一个或多个突变指示对依鲁替尼无反应;以及如果受试者在一个或多个基因中不具有一个或多个突变,则施用治疗有效量的依鲁替尼,从而治疗FL。
来自受试者的合适样本包括含有感兴趣的基因的任何生物样本,包括但不限于全血样本和肿瘤活检样本。
提供以下实施例以进一步描述本文所公开的实施方案中的一些。这些实施例旨在说明而非限制本发明所公开的实施方案。
DAWN研究(NCT01779791)评估了在患有复发性/难治性(R/R)滤泡型淋巴瘤(FL)的患者中的依鲁替尼单一疗法的疗效和安全性。依鲁替尼的总反应率(ORR)为20.9%(95%置信区间[CI],13.7-29.7),未达到主要终点。然而,反应者经历了长持续时间的反应(中值19.4个月)。对来自DAWN研究的样本进行基因学研究,以确定是否可使用体细胞突变来鉴定将对依鲁替尼有反应或无反应的FL患者。
DAWN试验的详细方法公布于Gopal AK等人,J Clin Oncol.2018;36:2405-2412中。简而言之,DAWN是一项针对年龄≥18岁且具有1级、2级或3a级非转化FL的诊断的患者中对依鲁替尼(560mg,每天一次)的多中心单臂2期研究,该患者已用≥2条先前的治疗线进行了治疗并且对使用含抗CD20单克隆抗体的化学免疫疗法方案的最后一条先前的治疗线是R/R的。主要终点是总反应率(ORR=完全反应[CR]+部分反应[PR]),由独立审查委员会使用国际工作组修订的《恶性淋巴瘤的反应标准》进行评估。
对88个福尔马林固定石蜡包埋的肿瘤样本(LabCorp,Burlington,NC)进行全外显子组测序,该肿瘤样本来自在依鲁替尼治疗后的反应者或无反应者。应用多个过滤器来排除潜在的种系变体,并使用已知与癌症有关的1216个基因的定制小组进行进一步分析。使用费舍尔精确检验鉴定富含反应者或无反应者的变体。基于数据库中针对非同义单核苷酸多态性功能预测(dbNSFP)的元分析支持向量机(metaSVM)注释,将变体标记为“有害的”。分类器以用贪心算法排序的可变数量的基因来构建,该贪心算法选择在每次迭代时将允许从患者池中移除最多数量的无反应者的基因,同时严重罚分反应者的移除。首先通过DAWN数据集内的10倍交叉验证评估分类结果,随后(参见Bartlett NL等人,Blood.2018;131:182-190)。
收集全血样本和肿瘤活检样本,并将全血和血浆级分用于基因分析。
从88名患有FL的受试者的FFPE样本(每个样本来自不同的受试者)产生外显子组数据。这些受试者中的八十三名被指示为在依鲁替尼治疗后的“反应者”(CR+PR)或“无反应者”(SD+PD)。
使用Nimblegen试剂盒产生全外显子组数据,并使用KAPA构建试剂盒进行测序文库。使用Illumina HiSeq2500平台进行测序,其中每个样本的目标为100倍的覆盖范围。
总共88个FFPE FL样本已进行全外显子组测序,并且首先由LabCorp分析。通过生成变体等位基因频率(VAF)直方图来定性评估(a)数据中体细胞与种系变体的存在程度和(b)在调用集中是否正确表示低VAF变体,从而检查LabCorp分析的结果。由于在VAF=0.5和VAF=1.0附近观察到大的峰,因此推断大部分变体可能是杂合的或纯合的种系变体;由于在VAF直方图的低端处只看到很少的变体,因此确定应使用特定富集低VAF变体的程序。
为了纠正在LabCorp数据中看到的潜在问题,使用原始FASTQ序列数据文件在DNAnexus上运行了一个内部外显子组分析管道。使用FastQC 1.0.0评估质量,使用BWA软件包0.5.9中的BWA-MEM算法将序列与hs37d5基因组构建进行比对,使用GATK 3.5外显子组管道重新校准比对,并且用MuTect 1.1.7、SnpEff 4.2(使用GRCh37.75数据库)和GEMINI0.20.0(通过使用非TCGA gnomAD和ExAC参考进行修正)对变体进行注释。过滤非同义编码变体(在R中定义为is_coding=“1”&impact!=“synonymous_variant”),以减少将测序人工痕迹和种系变体纳入关联分析中的可能性。(a)基于dbNSFP中的MetaSVM注释,将变体标记为“有害的”,和/或(b)基于它们是否存在于Bartlett CTEP研究中所用的个人癌症小组中的基因,将变体标记为“个人基因”变体。
该外显子组测序评估的主要目标是从体细胞突变中鉴定反应者/无反应者。为了实现这一点,仅用“个人基因”进行分析,并在Bartlett CTEP数据集中(使用个人ACE扩展癌症小组针对FL数据生成的数据集)测试。在更受限制的(“个人基因”)和完整的全外显子组数据集中,对所有可能的体细胞变体以及仅那些推断为有害的基因变体进行统计分析。利用基于贪心算法(具有错误分类罚分)的无反应者基因排序和使用基因突变状态的反应者/无反应者合并,开发了使用可变基因数量的多个分类器。首先通过数据集内的10倍交叉验证评估分类结果;随后,基于在Bartlett CTEP FL受试者研究中预测的反应者组的总依鲁替尼反应率来评估分类器的子集。
外显子组数据是从88名患者的石蜡包埋的肿瘤样本中产生的。总共鉴定到974,686个非同义变体。在滤除潜在误差和可能的种系突变后,变体的数量减少至13,554。可获得83名患者的反应数据,包括17名反应者和66名无反应者。
经过滤的变体的最终VAF直方图显示,在由LabCorp返回的原始变体集中看到在0.5和1.0处峰的显著降低,表明体细胞与种系变体的比率高得多。EZH2-Y646和STAT6-D419(已知的体细胞FL相关突变)的VAF值降至0.4以下,表明如果变体在dbSNP中而不是在COSMIC中,则排除不低于该阈值的变体将是合理的。dbSNP中而非COSMIC集中的变体大部分落入0.5和1.0附近的区域,表明它们中的许多可能是种系突变。作为对经过滤的变体的最终分布的检查,检查存在于数据集内的COSMIC(“已知体细胞”)变体的VAF分布,并发现其具有类似的分布(然而,注意,在COSMIC中存在可能几乎完全是种系的已知污染变体,占0.5左右的小峰)。每个样本中突变基因的数量从100以下变化到500以上,并且在无反应者NR受试者中差异更大,这可能是由于样本量较大所致。
在图2中提供了从全外显子组测序鉴定的变体频率的总模式。在>10%的患者中存在75个具有推定突变的基因,包括先前与FL有关的那些基因中的许多(例如CREBBP、BCL2和KMT2D)。图2的左图示出了在每个基因中具有突变的个体的百分比,而右图示出了在83名患者中可获得反应者数据的这些基因中的突变分布。
由于来自无反应者的样本数量比来自反应者的样本数量更多,单变量分析主要产生在依鲁替尼反应者中显着富集的大部分变体,但数量非常少,例如FANCA、HISTH1B、ANXA6和PARP10(表1)。有趣的是,作为肿瘤抑制子的BTG1中具有变体的2名患者也对依鲁替尼有反应。在单变量分析中鉴定出很少的无反应者基因,包括NBPF1、ATP6AP1、EP400和CNOT1(这些基因中的突变可激活绕过BTK的途径,包括mTOR和JAK/STAT途径)。
Inf=无穷大
*结果仅针对p值<0.2的基因示出。
因为限定反应者的基因很少,所以将更多无反应者患者中突变的基因作为分类器开发的目标。选择一组基因并通过选择允许在每次迭代中推断最多附加的无反应者直到覆盖所有无反应者的基因来排序。从选定的小组中,开发了17个分类器模型,包括ATP6AP1、EP400、ARID1A、SOCS1、TBL1XR1、CNOT1和KDM2B中的变体(图3)。
由图4中的实线示出的预测的反应者的平均ORR(“预测的反应者的平均ORR”)基于针对17个不同反应者/无反应者分类模型的10倍交叉验证,显示了随着添加更多基因,预测的ORR增加。如图3所示,每个模型由用于构建该模型的基因的数量来限定,其中按照新信息量减少的顺序添加基因。图4中的虚线(“ORR”)表示整个患者群体的ORR,无论其分类如何。
前5个排序基因(ATP6AP1、EP400、ARID1A、SOCS1和TBL1XR1)的突变状态在预测缺乏反应方面最具信息。这些基因中的突变仅存在于无反应者中并在下文进行描述。
ATP6AP1-在ATP6AP1基因中看到的大多数突变存在于ATP-合酶S1区域中(图5)。
EP400-7名无反应者患者在EP400基因中具有体细胞突变,并且这些患者中的5名具有由metaSVM标记为“有害”的突变(图6)。EP400编码组蛋白乙酰化酶复合物组分。
ARID1A-在DAWN数据集中发生推定的肿瘤抑制子ARID1A中的5个突变,并且这些突变中的2个导致过早终止密码子的形成(图7)。
SOCS1-在DAWN研究中观察到的6个SOCS1突变中的大多数被metaSVM预测为有害并且在SH2结构域中(图8)。
TBL1XR1-TBLXR1基因中的5个推定的体细胞突变中的4个被metaSVM预测为有害的;其余的变体代表过早的终止密码子的获得(图9)。
CARD11-CARD11包含存在于6名患者中的8种变体。每个CARD11变体被单独鉴定,即使CARD11在该分析中不是排序最高的基因。在此处应用过滤后,总共留下了来自2名患者的4个变体(T117P、D230N、C351S和S352P),并且可能是有害的,尽管它们未被metaSVM识别为是有害的。在滤除的变体中,有1个的变体等位基因频率(VAF)<0.05(VAF=0.04672897),有1个属于非癌症体细胞突变目录(COSMIC)dbSNP组,经受了VAF<0.4过滤器(VAF=0.49371981),而其它在dbSNP中被标记为“仅种系”,这表明CARD11的大部分趋势是由种系变体引起的。
表2中提供了在反应者和无反应者中鉴定出的体细胞突变。
*获得的终止密码子;**终止密码子丢失。
对来自2期DAWN试验的患者中的基因的突变分析得出了对R/R FL中的依鲁替尼反应和抗性机制的见解。
本领域的技术人员将会知道可对本发明的优选实施方案作出许多改变和修改,而且此类改变和修改可在不脱离本发明的实质的情况下进行。因此,所附权利要求书旨在覆盖落入本发明的真实实质和范围内的所有此类等同变化。
本文档所引用或描述的每项专利、专利申请和公布的公开内容均据此全文以引用方式并入本文。
实施方案的以下列表旨在补充而不是替换或取代先前的描述。
实施方案1.依鲁替尼在制造药物中的用途,所述药物用于治疗在选自以下的一个或多个基因中不具有如表2中所定义的一个或多个突变的受试者的滤泡型淋巴瘤(FL):AHNAK、ARID1A、ATP6AP1、BCL9L、CLTC、CNOT1、EP400、KDM2B、MYBBP1A、NACA、NBPF1、NBPF10、NCOA4、NEDD4L、PRDM16、SOCS1和TBL1XR1。
实施方案2.用于治疗在选自以下的一个或多个基因中不具有如表2中所定义的一个或多个突变的受试者的滤泡型淋巴瘤(FL)的用途的依鲁替尼:AHNAK、ARID1A、ATP6AP1、BCL9L、CLTC、CNOT1、EP400、KDM2B、MYBBP1A、NACA、NBPF1、NBPF10、NCOA4、NEDD4L、PRDM16、SOCS1和TBL1XR1。
实施方案3.一种治疗受试者的滤泡型淋巴瘤(FL)的方法,所述方法包括向所述受试者施用治疗有效量的依鲁替尼,从而治疗所述FL,其中所述受试者在选自以下的一个或多个基因中不具有如表2中所定义的一个或多个突变:AHNAK、ARID1A、ATP6AP1、BCL9L、CLTC、CNOT1、EP400、KDM2B、MYBBP1A、NACA、NBPF1、NBPF10、NCOA4、NEDD4L、PRDM16、SOCS1和TBL1XR1。
实施方案4.一种治疗在选自以下的一个或多个基因中不具有如表2中所定义的一个或多个突变的受试者的滤泡型淋巴瘤(FL)的方法:AHNAK、ARID1A、ATP6AP1、BCL9L、CLTC、CNOT1、EP400、KDM2B、MYBBP1A、NACA、NBPF1、NBPF10、NCOA4、NEDD4L、PRDM16、SOCS1和TBL1XR1,所述方法包括向所述受试者施用治疗有效量的依鲁替尼,从而治疗所述FL。
实施方案5.根据实施方案2-4中任一项所述的用途或方法,其中依鲁替尼的所述治疗有效量包括约420mg至约840mg。
实施方案6.根据实施方案5所述的用途或方法,其中依鲁替尼的所述治疗有效量包括560mg。
实施方案7.根据前述实施方案中任一项所述的用途或方法,其中所述FL为复发性/难治性(R/R)FL。
实施方案8.根据前述实施方案中任一项所述的用途或方法,其中在所述施用之前,所述受试者具有1级、2级或3a级非转化FL的诊断。
实施方案9.根据实施方案8所述的用途或方法,其中在所述施用之前,所述受试者已用≥2条先前的治疗线进行了治疗。
实施方案10.根据实施方案9所述的用途或方法,其中在所述施用之前,所述受试者对使用含抗CD20单克隆抗体的化学免疫疗法方案的最后一条先前的治疗线是R/R的。
实施方案11.根据前述实施方案中任一项所述的用途或方法,其中所述受试者具有部分反应或完全反应。
实施方案12.一种预测患有滤泡型淋巴瘤的受试者中对依鲁替尼无反应的可能性的方法,所述方法包括分析来自所述受试者的样本中选自以下的一个或多个基因中的如表2中所定义的一个或多个突变:AHNAK、ARID1A、ATP6AP1、BCL9L、CLTC、CNOT1、EP400、KDM2B、MYBBP1A、NACA、NBPF1、NBPF10、NCOA4、NEDD4L、PRDM16、SOCS1和TBL1XR1,其中所述一个或多个基因中的所述一个或多个突变指示对依鲁替尼无反应。
实施方案13.根据实施方案12所述的方法,还包括如果所述受试者在所述一个或多个基因中不具有所述一个或多个突变,则施用治疗有效量的依鲁替尼,从而治疗所述FL。
- 治疗滤泡型淋巴瘤的方法
- 用淋巴毒素(LT)途径抑制物治疗滤泡性淋巴瘤
