一种用于治疗淀粉样蛋白脑神经疾病的组合物和其治疗方法
文献发布时间:2023-06-19 11:57:35
技术领域
本发明涉及一种用于治疗淀粉样蛋白脑神经疾病的组合物和其治疗方法。
背景技术
退行性脑疾病为一种由于中枢神经系统神经细胞的退行性变化而引起各种症状的疾病,例如运动和感觉功能受损、如记忆、学习和计算推理等高级功能受到抑制。常见的疾病包括阿尔茨海默氏病(Alzheimer's disease)、帕金森氏病(Parkinson's disease)和记忆障碍等。在退行性脑疾病中,神经细胞的死亡是由于快速或缓慢进行的坏死(necrosis)或凋亡(apoptosis)而发生的。因此,为了开发预防、控制和治疗中枢神经系统疾病的方法,需要理解神经细胞的死亡机制。
另一方面,作为一种具有代表性的退行性脑疾病,阿尔茨海默氏病的重要病理特征是称为老年斑(senile plaque)的肽聚集体的形成,其引起突触功能障碍和神经细胞死亡。这些老年斑的主要成分为具有40个至42个氨基酸长度的淀粉样蛋白-β(amyloid-beta)。淀粉样蛋白-β单体很容易自组装成(self-assemble)寡聚物、原纤维(protofibril)和富含β-折叠的纤维,并与神经毒性的发病有关。
淀粉样蛋白-β斑块与神经毒性之间的相关性尚不明确,但淀粉样蛋白-β自组装成中间寡聚物或聚集体被认为与如阿尔茨海默氏病的脑神经疾病的发病有关。
另外,Tau蛋白由四个部分组成:N-末端突出部分、脯氨酸(proline)聚集结构域、微管结合结构域和C-末端(Mandelkow et al.,Acta.Neuropathol.,103,26-35,1996),并且已知当Tau蛋白在中枢神经系统的神经细胞中异常过度磷酸化或异常修饰时,会引起退行性脑疾病,例如帕金森氏病和Tau蛋白病(tauopathy)。
因此,提出抑制淀粉样蛋白-β聚集、降解其聚集体或减少异常过度磷酸化的Tau蛋白作为治疗如阿尔茨海默氏病和帕金森氏病的退行性脑疾病的良好方法。
发明内容
【技术问题】
本发明的一实施例提供一种用于抑制和/或降解淀粉样蛋白-β聚集的药物组合物,其包括选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其药学上可接受的盐中的至少一种作为有效成分。
本发明的另一实施例提供一种用于降解(和/或抑制聚集)Tau蛋白和/或抑制Tau蛋白磷酸化的药物组合物,其包括选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其药学上可接受的盐中的至少一种作为有效成分。
本发明的另一实施例提供一种抑制和/或降解淀粉样蛋白-β聚集的方法,其包括:将至少一种选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其药学上可接受的盐的药学有效量施用于需要抑制和/或降解淀粉样蛋白-β聚集的对象。所述方法可以进一步包括:在所述施用步骤前,确认需要抑制和/或降解淀粉样蛋白-β聚集的对象。
本发明的另一实施例提供一种降解(和/或抑制聚集)Tau蛋白和/或抑制Tau蛋白磷酸化的方法,其包括:将至少一种选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其药学上可接受的盐的药学有效量施用于需要降解(和/或抑制聚集)Tau蛋白和/或抑制Tau蛋白磷酸化的对象。所述方法可以进一步包括:在所述施用步骤前,确认需要降解(和/或抑制聚集)Tau蛋白和/或抑制Tau蛋白磷酸化的对象。
本发明的另一实施例提供一种用于预防和/或治疗退行性脑疾病(neurodegenerative brain disease)的药物组合物,其包括选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其药学上可接受的盐中的至少一种作为有效成分。
本发明的另一实施例提供一种预防和/或治疗退行性脑疾病的方法,其包括:将至少一种选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其药学上可接受的盐的药学有效量施用于需要预防和/或治疗退行性脑疾病的对象。所述方法可以进一步包括:在所述施用步骤前,确认需要预防和/或治疗退行性脑疾病的对象。
本发明的另一实施例提供一种用于保护脑神经的药物组合物,其包括选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其药学上可接受的盐中的至少一种作为有效成分。
本发明的另一实施例提供一种脑神经细胞的保护方法,其包括:将至少一种选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其药学上可接受的盐的药学有效量施用于需要保护脑神经细胞的对象。所述方法可以进一步包括:在所述施用步骤前,确认需要保护脑神经细胞的对象。
本发明的另一实施例提供一种用于预防或改善认知障碍或改善记忆力的药物组合物,其包括选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其药学上可接受的盐中的至少一种作为有效成分。
本发明的另一实施例提供一种预防或改善认知障碍或改善记忆力的方法,其包括:将至少一种选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其药学上可接受的盐的药学有效量施用于需要预防或改善认知障碍或改善记忆力的对象。所述方法可以进一步包括:在所述施用步骤前,确认需要预防或改善认知障碍或改善记忆力的对象。
本发明的另一实施例提供一种用于抑制和/或降解淀粉样蛋白-β聚集的保健功能性食品,其包括选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其食品学上可接受的盐中的至少一种作为有效成分。
本发明的另一实施例提供一种用于降解(和/或抑制聚集)Tau蛋白和/或抑制Tau蛋白磷酸化的保健功能性食品,其包括选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其食品学上可接受的盐中的至少一种作为有效成分。
本发明的另一实施例提供一种用于预防和/或改善退行性脑疾病的保健功能性食品,其包括选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其食品学上可接受的盐中的至少一种作为有效成分。
本发明的另一实施例提供一种用于保护脑神经细胞的保健功能性食品,其包括选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其食品学上可接受的盐中的至少一种作为有效成分。
本发明的另一实施例提供一种用于预防或改善认知障碍或改善记忆力的保健功能性食品,其包括选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其食品学上可接受的盐中的至少一种作为有效成分。
【技术方案】
在本说明书中,通过确认选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其药学上可接受的盐中的至少一种的抑制淀粉样蛋白-β聚集、降解淀粉样蛋白-β的活性、降解(和/或抑制聚集)Tau蛋白的活性和/或抑制Tau蛋白过度磷酸化的效果,确认所述化合物在治疗退行性脑疾病(neurodegenerative brain disease)中的作用,并提出所述化合物在抑制和/或降解淀粉样蛋白-β聚集的活性,和/或降解(和/或抑制聚集)Tau蛋白和/或抑制Tau蛋白磷酸化,和/或预防和/或治疗退行性脑疾病方面的新用途。由于所述选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其药学上可接受的盐中的至少一种其血脑屏障(Blood-Brain Barrier,BBB)通透性高,因此可以在大脑中有效发挥抑制和/或降解淀粉样蛋白-β聚集,和/或降解(和/或抑制聚集)Tau蛋白和/或抑制Tau蛋白磷酸化,和/或预防和/或治疗退行性脑疾病的活性。
由此,本发明的一实施例提供一种用于抑制和/或降解淀粉样蛋白-β聚集的药物组合物,其包括选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其药学上可接受的盐中的至少一种作为有效成分。
本发明的另一实施例提供一种用于降解(和/或抑制聚集)Tau蛋白和/或抑制Tau蛋白磷酸化的药物组合物,其包括选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其药学上可接受的盐中的至少一种作为有效成分。
本发明的另一实施例提供一种抑制和/或降解淀粉样蛋白-β聚集的方法,其包括:将至少一种选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其药学上可接受的盐的药学有效量施用于需要抑制和/或降解淀粉样蛋白-β聚集的对象。所述方法可以进一步包括:在所述施用步骤前,确认需要抑制和/或降解淀粉样蛋白-β聚集的对象。
本发明的另一实施例提供一种降解(和/或抑制聚集)Tau蛋白和/或抑制Tau蛋白磷酸化的方法,其包括:将至少一种选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其药学上可接受的盐的药学有效量施用于需要降解(和/或抑制聚集)Tau蛋白和/或抑制Tau蛋白磷酸化的对象。所述方法可以进一步包括:在所述施用步骤前,确认需要降解(和/或抑制聚集)Tau蛋白和/或抑制Tau蛋白磷酸化的对象。
本发明的另一实施例提供一种用于预防和/或治疗退行性脑疾病的药物组合物,其包括选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其药学上可接受的盐中的至少一种作为有效成分。
本发明的另一实施例提供一种预防和/或治疗退行性脑疾病的方法,其包括:将至少一种选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其药学上可接受的盐的药学有效量施用于需要预防和/或治疗退行性脑疾病的对象。所述方法可以进一步包括:在所述施用步骤前,确认需要预防和/或治疗退行性脑疾病的对象。
本发明的另一实施例提供一种用于预防或改善认知障碍或改善记忆力的药物组合物,其包括选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其药学上可接受的盐中的至少一种作为有效成分。
本发明的另一实施例提供一种预防或改善认知障碍或改善记忆力的方法,其包括:将至少一种选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其药学上可接受的盐的药学有效量施用于需要预防或改善认知障碍或改善记忆力的对象。所述方法可以进一步包括:在所述施用步骤前,确认需要预防或改善认知障碍或改善记忆力的对象。
本发明的另一实施例提供一种用于抑制和/或降解淀粉样蛋白-β聚集的保健功能性食品,其包括选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其食品学上可接受的盐中的至少一种作为有效成分。
本发明的另一实施例提供一种用于降解(和/或抑制聚集)Tau蛋白和/或抑制Tau蛋白磷酸化的保健功能性食品,其包括选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其食品学上可接受的盐中的至少一种作为有效成分。
本发明的另一实施例提供一种用于预防和/或改善退行性脑疾病的保健功能性食品,其包括选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其食品学上可接受的盐中的至少一种作为有效成分。
本发明的另一实施例提供一种用于保护脑神经细胞的保健功能性食品,其包括选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其食品学上可接受的盐中的至少一种作为有效成分。
本发明的另一实施例提供一种用于预防或改善认知障碍或改善记忆力的保健功能性食品,其包括选自利福霉素(Rifamycin)、三氟丙嗪(Triflupromazine)及其食品学上可接受的盐中的至少一种作为有效成分。
下面将更详细描述本说明书提供的发明。
本发明人已经证实,利福霉素或其药学上可接受的盐抑制淀粉样蛋白-β聚集(参见实施例1和图1),并且在淀粉样蛋白-β的聚集被诱导时,对其进行降解(参见实施例2、实施例3、图3、图5和图7)。
另外,在本发明的利福霉素的阿尔茨海默氏病动物模型中确认了淀粉样蛋白斑块和Tau磷酸化的减少效果,其结果发现,淀粉样蛋白斑块的数量和斑块的总面积减少(参见实施例4和图8至图10)。
另外,确认了本发明的利福霉素改善阿尔茨海默氏病动物模型中的认知功能和记忆力(参见实施例6、图13和图14)。
另外,本发明人已经证实,三氟丙嗪或其药学上可接受的盐抑制淀粉样蛋白-β聚集(参见实施例1和图2),并且在淀粉样蛋白-β的聚集被诱导时,对其进行降解(参见实施例2、图4和图6)。
此外,在本发明的三氟丙嗪的阿尔茨海默氏病动物模型中确认了淀粉样蛋白斑块和Tau磷酸化的减少效果,其结果发现,淀粉样蛋白斑块的数量和斑块的总面积减少(参见实施例4和图11),降解总Tau蛋白,并抑制Tau蛋白的磷酸化(参见实施例5和图12)。
在本说明书中,已经确认由于利福霉素或三氟丙嗪不仅抑制淀粉样蛋白-β聚集并降解已聚集的聚集体,而且降解Tau蛋白并抑制Tau的磷酸化,因此具有各种退行性脑疾病的治疗效果,例如阿尔茨海默氏病、帕金森氏病等。
在本说明书中,术语“利福霉素(Rifamycin)”可以是指一组多个利福霉素衍生物。所述利福霉素可以选自利福平(rifampicin)、利福布汀(rifabutin)、利福喷丁(rifapentine)、利福拉齐(rifalazil)、利福昔明(rifaximin)、利福定(rifamdin)、利福霉素B、利福霉素S和利福霉素SV中的一种。
利福喷丁也可以称为3-[[(4-环戊基-1-哌嗪基)亚氨基]甲基]-利福霉素(3-[[(4-Cyclopentyl-1-piperazinyl)imino]methyl]-rifamycin),并且可以由以下化学式1表示。
【化学式1】
利福平可以为5,6,9,17,19,21-六羟基-23-甲氧基-2,4,12,16,18,20,22-七甲基-8-[N-(4-甲基-1-哌嗪基)甲亚氨酰基]-2,7-(环氧十五碳环[1,11,13]三烯亚氨基)-萘并[2,1-b]呋喃-1,11(2H)-二酮21-醋酸酯(5,6,9,17,19,21-hexahydroxy-23-methoxy-2,4,12,16,18,20,22-heptamethyl-8-[N-(4-methyl-1-piperazinyl)formimidoyl]-2,7-
(epoxypentadeca[1,11,13]trienimino)-naphtho[2,1-b]furan-1,11(2H)-dione 21-acetate),并且可以由以下化学式2表示。
【化学式2】
利福布汀可以为(S,12E,14S,15R,16S,17R,18R,19R,20S,21S,22E,24Z)-6,16,18,20-四羟基-1′-异丁基-14-甲氧基-7,9,15,17,19,21,25-七甲基-螺[9,4-(环氧十五碳环[1,11,13]三烯亚氨基)-2H-呋喃并[2′,3′:7,8]萘[1,2-二咪唑-2,4′-哌啶]-5,10,26-(3H,9H)-三酮-16-醋酸酯((S,12E,14S,15R,16S,17R,18R,19R,20S,21S,22E,24Z)-6,16,18,20-tetrahydroxy-1'-isobutyl-14-methoxy-7,9,15,17,19,21,25-heptamethyl-spiro[9,4-
(epoxypentadeca[1,11,13]trienimino)-2H-furo[2',3':7,8]naphth[1,2-diimidazole-2,4'-piperidine]-5,10,26-(3H,9H)-trione-16-acetate),并且可以由以下化学式3表示。
【化学式3】
利福拉齐可以为(2S,16Z,18E,20S,21S,22R,23R,24R,25S,26R,27S,28E)-5,12,21,23-四羟基-27-甲氧基-2,4,16,20,22,24,26-七甲基-10-[4-(2-甲基丙基)哌嗪-1-基]-1,6,15-三氧代-1,2-二氢-6H-2,7-(环氧十五碳环[1,11,13]三烯亚氨基)[1]苯并呋喃并[4,5-a]吩恶嗪-25-基醋酸酯((2S,16Z,18E,20S,21S,22R,23R,24R,25S,26R,27S,28E)-5,12,21,23-tetrahydroxy-27-methoxy-2,4,16,20,22,24,26-heptamethyl-10-[4-(2-methylpropyl)piperazin-1-yl]-1,6,15-trioxo-1,2-dihydro-6H-2,7-(epoxypentadeca[1,11,13]trienoimino)[1]benzofuro[4,5-a]phenoxazin-25-ylacetate),并且可以由以下化学式4表示。
【化学式4】
利福昔明可以为[2S-(2R*,16Z,18E,20R*,21R*,22S*,23S*,24S*,25R*,26S*,27R*,22E)]-25-乙酰基氧基)-5,6,21,23-四羟基-27-甲氧基-2,4,11,16,20,22,24,26-八甲基-2,7-(环氧十五碳环[1,11,13]三烯亚氨基)苯并呋喃并[4,5-e]pyrido[1,2-a]苯并咪唑-1,15(2H)-二酮([2S-(2R*,16Z,18E,20R*,21R*,22S*,23S*,24S*,25R*,26S*,27R*,22E)]-25-acetyloxy)-5,6,21,23-tetrahydroxy-27-methoxy-2,4,11,16,20,22,24,26-octamethyl-2,7-(epoxypentadeca[1,11,13]trienimino)benzofuro[4,5-e]pyrido[1,2-a]benzimidazole-1,15(2H)-dione),并且可以由以下化学式5表示。
【化学式5】
利福霉素B可以为{[(2S,12Z,14E,16S,17S,18R,19R,20R,21S,22R,23S,24E)-21-(乙酰基氧基)-5,6,17,19-四羟基-23-甲氧基-2,4,12,16,18,20,22-七甲基-1,11-二氧代-1,2-二氢-2,7-(环氧十五碳环[1,11,13]三烯亚氨基)萘并[2,1-b]呋喃-9-基]氧代}醋酸({[(2S,12Z,14E,16S,17S,18R,19R,20R,21S,22R,23S,24E)-21-(acetyloxy)-5,6,17,19-tetrahydroxy-23-methoxy-2,4,12,16,18,20,22-heptamethyl-1,11-dioxo-1,2-dihydro-2,7-(epoxypentadeca[1,11,13]trienoimino)naphtho[2,1-b]furan-9-yl]oxy}acetic acid),并且可以由以下化学式6表示。
【化学式6】
利福霉素S可以为5,17,19,21-四羟基-23-甲氧基-2,4,12,16,18,20,22-七甲基-2,7-(环氧十五碳环[1,11,13]三烯亚氨基)萘并[2,1-b]呋喃-1,6,9,11(2H)-四酮21-醋酸酯(5,17,19,21-Tetrahydroxy-23-methoxy-2,4,12,16,18,20,22-heptamethyl-2,7-(epoxypentadeca[1,11,13]trienimino)naphtho[2,1-b]furan-1,6,9,11(2H)-tetrone21-Acetate),并且可以由以下化学式7表示。
【化学式7】
利福霉素S可以为5,6,9,17,19,21-六羟基-23-甲氧基-2,4,12,16,18,20,22-七甲基-2,7-(环氧十五碳环[1,11,13]三烯亚氨基)萘并[2,1-b]呋喃-1,11(2H)-二酮21-醋酸酯(5,6,9,17,19,21-Hexahydroxy-23-methoxy-2,4,12,16,18,20,22-heptamethyl-2,7-(epoxypentadeca[1,11,13]trienimino)naphtho[2,1-b]furan-1,11(2H)-dione 21-acetate),并且可以由以下化学式8表示。
【化学式8】
利福啶可以为3-[[[4-(2-甲基丙基)-1-哌嗪基]亚氨基]甲基]利福霉素(3-[[[4-(2-Methylpropyl)-1-piperazinyl]imino]methyl]rifamycin),并且可以由以下化学式9表示。
【化学式9】
三氟丙嗪(Triflupromazine,二甲基({3-[2-(三氟甲基)-10H-吩噻嗪-10-基]丙基})胺(dimethyl({3-[2-(trifluoromethyl)-10H-phenothiazin-10-yl]propyl})amine);CAS No.146-54-3;参见化学式10)主要用于治疗精神/情绪障碍,例如精神分裂症等。然而,尚无有关三氟丙嗪对抑制和/或降解淀粉样蛋白-β聚集的活性,和/或降解(和/或抑制聚集)Tau蛋白和/或抑制Tau蛋白磷酸化,和/或预防和/或治疗退行性脑疾病的效果的报道。
【化学式10】
人淀粉样蛋白-β(amyloid-beta)是一种包括约36个至43个氨基酸的肽分子,也是在阿尔茨海默氏病患者的大脑中表达的淀粉样蛋白斑块的主要成分,并且已知与阿尔茨海默氏病的发病有关。所述淀粉样蛋白-β肽分子可以通过用β分泌酶(beta secretase)和γ分泌酶(gamma secretase)切割淀粉样蛋白前体蛋白(amyloid precursor protein(APP);UniProtKB P05067)而获得。淀粉样蛋白-β肽分子聚集形成神经细胞毒性寡聚物,导致退行性脑疾病。
另外,Tau蛋白由四个部分组成,其包括N-末端突出部分、脯氨酸(proline)聚集结构域、微管结合结构域和C-末端(Mandelkow et al.,Acta.Neuropathol.,103,26-35,1996),已知当Tau在中枢神经系统的神经细胞中异常过度磷酸化或异常修饰时,会引起退行性脑疾病,例如帕金森氏病和Tau蛋白病(tauopathy)。
本文使用的术语“退行性脑疾病”是指与大脑退行性变化有关的所有疾病,尤其是用于全面描述由脑和/或脑神经细胞中淀粉样蛋白-β的聚集、Tau蛋白的聚集和Tau蛋白的过度磷酸化中的至少一种因素引起的所有疾病(脑疾病)。在一实施例中,退行性脑疾病病例可以为阿尔茨海默氏病(Alzheimer's disease)、帕金森氏病、亨廷顿氏病、轻度认知障碍(mild cognitive impairment)、脑淀粉样血管病、唐氏综合症、淀粉样蛋白脑卒中(stroke)、系统性淀粉样蛋白疾病、荷兰(Dutch)型淀粉样变性病、尼曼-皮克病、老年性痴呆、肌萎缩侧索硬化(amyotrophic lateral sclerosis)、脊髓小脑萎缩(SpinocerebellarAtrophy)、多发性抽动症(Tourette'sSyndrome)、弗里德利希共济失调(Friedrich'sAtaxia)、马查多-约瑟夫病(Machado-Joseph's disease)、路易体痴呆(Lewy BodyDementia)、肌张力障碍(Dystonia)、进行性核上性麻痹(Progressive SupranuclearPalsy)或额颞叶痴呆(Frontotemporal Dementia)等,但不限于此,其可以为由淀粉样蛋白-β的聚集(aggregation)、Tau蛋白的聚集和/或Tau蛋白的磷酸化引起的任何疾病。
如本文所用,术语“治疗”包括病理症状的减轻或改善,疾病部位的减少,疾病进展的延迟或缓解,疾病状态或症状的改善、减轻或稳定,部分或完全恢复,生存期的延长和其他有益治疗结果等的所有含义。术语“预防”包括对没有特定疾病的对象起作用以预防所述特定疾病的发病、延迟其发病时期或降低其发病频率的所有机制和/或效果的含义。术语“保护脑神经细胞”包括抑制脑神经细胞的损伤和/或死亡的所有机制和/或效果的含义。
所述药学上或食品学上可接受的盐可以不受限制地从药学领域中常用的所有盐中选择和使用。在一具体实施例中,所述药学上可接受的盐可以选自使用如盐酸、溴酸、磺酸、氨基磺酸、磷酸、硝酸等的无毒性无机酸;或如乙酸、丙酸、琥珀酸、乙醇酸、硬脂酸、乳酸、酒石酸、柠檬酸、对甲苯磺酸、甲磺酸等的有机酸形成的盐中的至少一种,例如可以为盐酸盐,但不限于此。
本说明书提供的药物组合物可用于选自以下类型的对象(患者):
(1)与正常水平相比,淀粉样蛋白-β的聚集水平更高或可能更高的对象(患者);
(2)与正常水平相比,Tau蛋白的聚集水平更高或可能更高的对象(患者);
(3)与正常水平相比,Tau蛋白的磷酸化水平更高或可能更高的对象(患者);以及
(4)属于所述(1)至(3)中的至少一项的对象(患者)。
所述淀粉样蛋白-β或Tau蛋白的聚集水平可以指淀粉样蛋白-β聚集体或Tau蛋白聚集体的量(浓度)或淀粉样蛋白-β聚集体或Tau蛋白聚集体在总淀粉样蛋白-β或总Tau蛋白中的比率。
所述Tau蛋白的磷酸化水平可以指磷酸化后的Tau蛋白的量(浓度)或磷酸化后的Tau蛋白在总Tau蛋白的比率。
所述“正常”可以指与施用所述药物组合物的对象(患者)相同类型的个体中不具有前述定义的“退行性脑疾病”的个体或者从所述个体中分离和/或培养的脑组织或脑细胞(脑神经细胞)。
在一实施例中,除了所述有效成分(利福霉素、三氟丙嗪或其药学上可接受的盐)以外,所述药物组合物还可以包括选自药学上可接受的载体、赋形剂、稀释剂、填充剂、增量剂、湿润剂、崩解剂、乳化剂(表面活性剂)、润滑剂、甜味剂、调味剂、悬浮液、保存剂等中的至少一种佐剂。所述佐剂可以根据所述药物组合物所施用的剂型进行适当调节,并且可以包括选自药学领域中常用的所有佐剂中的至少一种。在一具体实施例中,所述药学上可接受的载体通常在药物的制剂化中使用,并且可以为选自乳糖、右旋糖、蔗糖、海藻糖、精氨酸、组氨酸、山梨糖醇、甘露醇、淀粉、阿拉伯胶、磷酸钙、藻酸盐、明胶、硅酸钙、微晶纤维素、聚乙烯吡咯烷酮、纤维素、水、糖浆、甲基纤维素、羟苯甲酯、羟苯丙酯、滑石、硬脂酸镁、矿物油等中的至少一种,但不限于此。
所述有效成分(利福霉素、三氟丙嗪或其药学上可接受的盐)的有效量,或所述药物组合物可以以口服或非口服方式给药。在非口服给药的情况下,可以通过静脉内注射、皮下注射、肌内注射、腹膜内注射、内皮给药、鼻内给药、肺内给药、直肠内给药或病变部位局部给药等来进行。在口服给药的情况下,所述药物组合物可以包衣活性成分以防止活性成分在胃中降解,或者可以配制成可防止在胃中降解的剂型。
另外,本文所用的术语“有效成分”可以是指本文所述的物质(例如,利福霉素、三氟丙嗪或其药学上可接受的盐)用于实现本文所述的药理学活性(例如,治疗退行性脑疾病)的生理活性物质,这与出于利用利福霉素或三氟丙嗪的已知活性(例如,分别为抗生活性、治疗精神分裂症)来治疗本文所述疾病的目的而单独施用利福霉素或三氟丙嗪、与其他物质组合施用或者另外施用不同。即,利福霉素或三氟丙嗪可以作为用于直接治疗退行性脑疾病的单一有效成分施用。
如本文所述,术语“药学有效量”可以指在药物组合物中可以表现出所需药理学效果的有效成分(利福霉素、三氟丙嗪或其药学上可接受的盐)的含量或剂量。所述药学有效量或有效成分可以根据诸如制剂化方法、给药方式、患者的年龄、体重、性别、病理状况、饮食、给药时间、给药间隔、给药途径、排泄速度和反应敏感性等因素适当地确定。例如,所述有效成分的日剂量或单剂量范围可以为0.0001mg/kg至1000mg/kg(体重)、0.001mg/kg至500mg/kg、0.01mg/kg至100mg/kg、0.1mg/kg至50mg/kg或0.5mg/kg至20mg/kg,但不限于此。所述日剂量或单剂量可以以单位剂量的形式配制成单一制剂,或者通过适当地划分用量来配制,或者通过将其装入多剂量容器来制备。
所述药物组合物中有效成分(即,利福霉素、三氟丙嗪或其药学上可接受的盐)的含量可以根据药物组合物的使用形式、患者的状况、所需效果等适当地调整,例如,按重量百分比计可以为0.0001%至99.9%、0.001%至99.9%、0.01%至99.9%、0.1%至99.9%、0.5%至99.9%、1%至99.9%、5%至99.9%、10%至99.9%、15%至99.9%、20%至99.9%、25%至99.9%、30%至99.9%、35%至99.9%、40%至99.9%、45%至99.9%、50%至99.9%、55%至99.9%、0.0001%至90%、0.001%至90%、0.01%至90%、0.1%至90%、0.5%至90%、1%至90%、5%至90%、10%至90%、15%至90%、20%至90%、25%至90%、30%至90%、35%至90%、40%至90%、45%至90%、50%至90%、55%至90%、0.0001%至70%、0.001%至70%、0.01%至70%、0.1%至70%、0.5%至70%、1%至70%、5%至70%、10%至70%、15%至70%、20%至70%、25%至70%、30%至70%、35%至70%、40%至70%、45%至70%、50%至70%、55%至70%、0.0001%至50%、0.001%至50%、0.01%至50%、0.1%至50%、0.5%至50%、1%至50%、5%至50%、10%至50%、15%至50%、20%至50%、25%至50%、30%至50%、35%至50%、40%至50%、45%至50%、0.0001%至40%、0.001%至40%、0.01%至40%、0.1%至40%、0.5%至40%、1%至40%、5%至40%、10%至40%、15%至40%、20%至40%、25%至40%、30%至40%或35%至40%,但不限于此。
所述药物组合物可以为水性或油性介质中的溶液、悬浮液、糖浆剂或乳化剂的形式,或者可以配制成散剂、粉剂、颗粒剂、片剂或胶囊剂等的形式,并且为了进行制剂化,可以进一步包括分散剂或稳定剂。
所述药物组合物的施用对象可以为包括人类、猴子等的灵长类动物;包括小鼠、大鼠等的啮齿类动物;包括狗、猫、牛、猪、绵羊、山羊、马等的哺乳类动物;或从所述哺乳类动物中分离出的细胞、组织或其培养物。
所述保健功能性食品是使用容易在日常膳食中缺乏的营养素、对人体有用的原料或成分(以下称为“功能性原料”)制备的食品,并且是指有助于维持健康、预防和/或改善某些疾病或症状的任何食品,对其最终产品形式没有特别限制。例如,所述保健功能性食品可以选自各种食品、饮料组合物、食品添加剂等,但不限于此。
所述保健功能性食品中有效成分(即,利福霉素、三氟丙嗪或其药学上可接受的盐)的含量可以根据食品的形式、所需用途等适当地调整,没有特别限制,例如,按重量百分比计可以为食品总重量的0.0001%至99%、0.0001%至95%、0.0001%至90%、0.0001%至80%、0.0001%至50%、0.001%至99%、0.001%至95%、0.001%至90%、0.001%至80%、0.001%至50%、0.01%至99%、0.01%至95%、0.01%至90%、0.01%至80%、0.01%至50%、0.1%至99%、0.1%至95%、0.1%至90%、0.1%至80%、0.1%至50%、0.1%至30%、0.1%至10%、1%至99%、1%至95%、1%至90%、1%至80%、1%至50%、1%至30%、1%至10%、10%至99%、10%至95%、10%至90%、10%至80%、10%至50%、10%至30%、25%至99%、25%至95%、25%至90%、25%至80%、25%至50%、25%至30%、40%至99%、40%至95%、40%至90%、40%至80%、40%至50%、50%至99%、50%至95%、50%至90%、50%至80%、60%至99%、60%至95%、60%至90%或60%至80%,但不限于此。
所述保健功能性食品可以进一步包括选自各种营养素、维生素、矿物(电解质)、如合成风味剂或天然风味剂等的风味剂、着色剂、增味剂(奶酪、巧克力等)、果胶酸或其盐、海藻酸或其盐、有机酸、保护性胶体增稠剂、pH调节剂、稳定剂、防腐剂、甘油、醇和用于碳酸饮料的碳酸化剂等中的至少一种。相对于所有保健功能性食品的100重量份,这些添加剂的比例通常在0.001重量份至约20重量份的范围内选择,但不限于此。
【有益效果】
本说明书中提供的技术通过使用利福霉素、三氟丙嗪或其药学上可接受的盐作为有效成分,不仅可以实现优异的淀粉样蛋白-β聚集的抑制和/或降解效果,还可以降解(和/或抑制聚集)Tau蛋白,并抑制Tau蛋白的过度磷酸化,由于其血脑屏障通透性高,因此可使其成功地作用于脑组织,有效地应用于预防和/或治疗与淀粉样蛋白-β聚集、Tau蛋白聚集、和/或过度磷酸化的Tau蛋白有关的各种退行性脑疾病。
附图说明
图1为通过硫黄素T分析(Thioflavin T analysis)确认抑制淀粉样蛋白-β聚集(Inhibition of Aβaggregation)的结果图表,其显示利福喷丁对抑制淀粉样蛋白-β聚集的效果(对照组:Aβ
图2为通过硫黄素T分析确认抑制淀粉样蛋白-β聚集(Inhibition of Aβaggregation)的结果图表,其显示三氟丙嗪盐酸盐对抑制淀粉样蛋白-β聚集的效果(对照组:Aβ
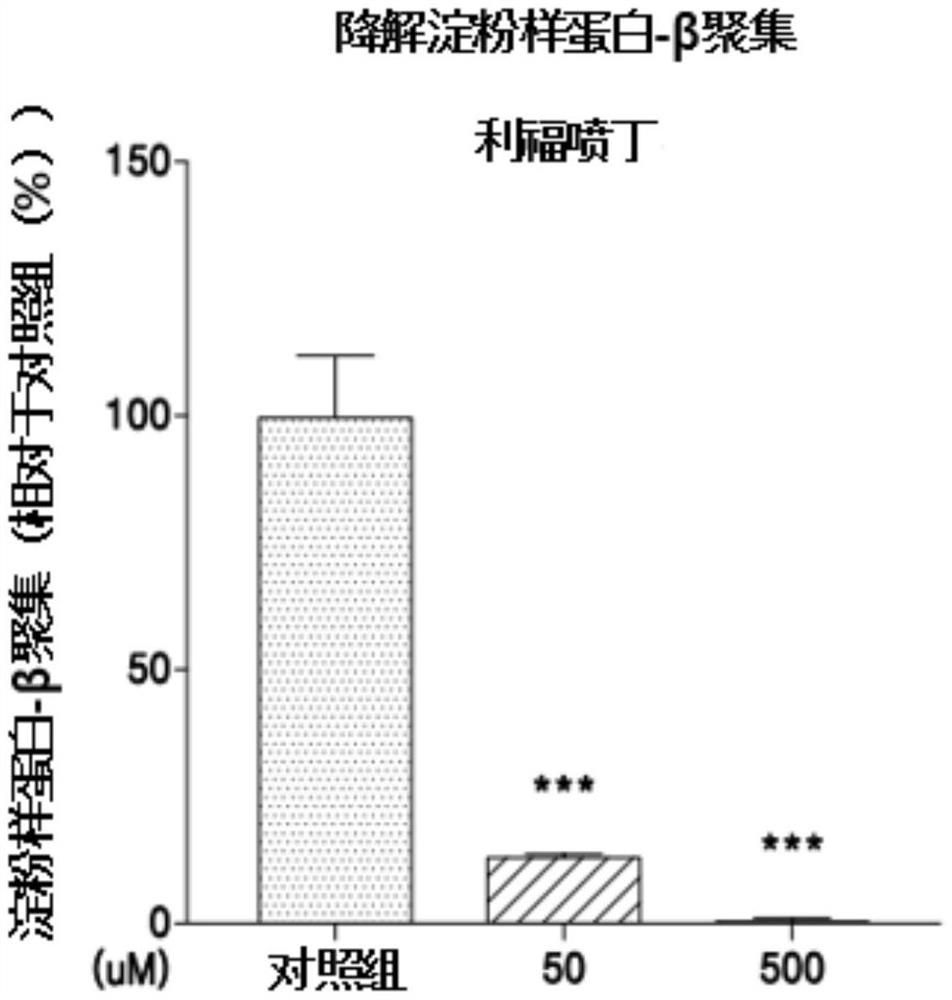
图3为通过硫黄素T分析确认降解淀粉样蛋白-β聚集(Aβdisaggregation)的结果图表,其显示利福喷丁对降解淀粉样蛋白-β聚集的效果(对照组:Aβ
图4为通过硫黄素T分析确认降解淀粉样蛋白-β聚集(Aβdisaggregation)的结果图表,其显示三氟丙嗪盐酸盐对降解淀粉样蛋白-β聚集的效果(对照组:Aβ
图5为通过基于PICUP的SDS-PAGE来确认降解淀粉样蛋白-β聚集(Aβdisaggregation)结果的电泳图像,其显示利福喷丁对降解淀粉样蛋白-β聚集的效果。
图6为通过基于PICUP的SDS-PAGE来确认降解淀粉样蛋白-β聚集(Aβdisaggregation)结果的电泳图像,其显示三氟丙嗪盐酸盐对降解淀粉样蛋白-β聚集的效果。
图7为通过硫黄素T分析确认降解淀粉样蛋白-β聚集(Aβdisaggregation)的结果图表,其显示利福喷丁和利福霉素系衍生物(利福平、利福布汀、利福霉素SV、利福定、利福霉素S、利福昔明、利福霉素B)对降解淀粉样蛋白-β聚集的效果(对照组:Aβ
图8为通过在转基因的阿兹海默氏痴呆动物(APP/PS1 TG)中使用6E10抗体来确认降解淀粉样蛋白-β斑块的结果的组织染色照片,其显示利福喷丁对降解淀粉样蛋白-β聚集的效果。
图9为通过在转基因的阿兹海默氏痴呆动物(APP/PS1 TG)中使用6E10抗体来确认降解淀粉样蛋白-β斑块的结果的图表,其显示利福喷丁对降解淀粉样蛋白-β聚集的效果。这是通过计算脑半球中总淀粉样蛋白-β斑块的数量、脑半球的海马(hippocampus)中淀粉样蛋白-β斑块的数量以及脑半球的大脑皮质(cortex)部位中淀粉样蛋白-β斑块的数量而获得的值,与施用溶媒(vehicle)的TG小鼠相比,利福喷丁施用组中的所述值显着减少。
图10为通过在转基因的阿兹海默氏痴呆动物(APP/PS1 TG)中使用6E10抗体来确认降解淀粉样蛋白-β斑块的结果的图表,其显示利福喷丁对降解淀粉样蛋白-β聚集的效果。这是通过计算脑半球中总淀粉样蛋白-β斑块的总面积、脑半球的海马(hippocampus)中淀粉样蛋白-β斑块的总面积以及脑半球的大脑皮质(cortex)部位中淀粉样蛋白-β斑块的总面积而获得的值,与施用溶媒(vehicle)的TG小鼠相比,利福喷丁施用组中的所述值显着减少。
图11为通过在转基因的阿尔茨海默氏病动物模型(5X FAD)中使用硫黄素T分析来确认降解淀粉样蛋白-β斑块结果的组织染色照片,其显示三氟丙嗪盐酸盐对降解淀粉样蛋白-β聚集的效果。
图12为通过在转基因的阿尔茨海默氏病动物模型(5X FAD)中使用SDS-PAGE来确认磷酸化Tau蛋白结果的电泳照片,其显示三氟丙嗪盐酸盐对抑制Tau蛋白磷酸化的效果。
图13为在转基因的阿兹海默氏痴呆动物(APP/PS1 TG)中施用利福喷丁后第8周时进行Y-迷宫测试(Y-maze test)的结果,这是测量实验动物抓住周围的线索并依次进入迷宫的相对频率的自发变换(spontaneous alteration)(%)值,这表明与阴性对照组TG-Veh组相比,记忆力的数值改善得更接近阳性对照组WT-Veh。
图14为在转基因的阿兹海默氏痴呆动物(APP/PS1 TG)中施用利福喷丁后第8周时进行新物体识别试验(Novel Object Recognition)的结果,这是测量实验动物搜索新物体的频率的偏好指数(Preference Index)值,这表明与阴性对照组TG-Veh组相比,记忆力的数值改善得更接近阳性对照组WT-Veh。
具体实施方式
下面将参考实施例更详细地描述本发明,这些实施例仅是示例性的,并不旨在限制本发明的范围。本领域技术人员显然可以在不脱离本发明要旨的范围内修改以下描述的实施例。
实施例1:抑制淀粉样蛋白-β聚集试验(Aβaggregation inhibition test)
将利福喷丁溶解于二甲基亚砜(DMSO)以使其浓度为5mM。然后,将所述化合物用6%二甲基亚砜(在蒸馏水中)稀释并使用。
将三氟丙嗪盐酸盐(以下所有实施例中使用的三氟丙嗪为三氟丙嗪盐酸盐)溶解于二甲基亚砜(dimethyl sulfoxide)以使其浓度为5mM。然后,将所述化合物用6%二甲基亚砜(在蒸馏水中)稀释并使用。
通过将人Aβ
另一方面,将硫黄素-T(Sigma-Aldrich)溶解于50mM甘氨酸缓冲液(pH8.5)以使其浓度为5mM。然后,使用50mM甘氨酸缓冲液(pH8.5)将其稀释至5μM,并在避光的暗室保存。
分别将所准备的淀粉样蛋白-β溶液放入1.5mL微量离心分离管中以使其浓度为50μM,并且对于每个1.5mL微量离心分离管,将利福喷丁和三氟丙嗪处理为2μM的浓度,然后在37℃下反应72小时。
将完成反应的反应液以25μL的量分别添加到96孔荧光分析板的每个孔中,然后将所准备的硫黄素-T溶液以75μL的量分别添加到每个孔中。在室温的暗室条件下进行5分钟反应后,使用多模式酶标仪(multi-mode microplate reader)在450nm激发(excitation)和485nm发射(emission)下测量荧光值。
将仅处理淀粉样蛋白-β以聚集72小时的组(对照组)的荧光值转换为%值并将其表示为100,并且将所测得的荧光值转换为其相对值,其结果如图1和图2所示。
图1显示利福喷丁的抑制淀粉样蛋白-β聚集效果(对照组:Aβ
图2显示三氟丙嗪的抑制淀粉样蛋白-β聚集效果(对照组:Aβ
另外,通过使用50μM的淀粉样蛋白-β对20μM的各种化合物进行与上述相同的试验,测量淀粉样蛋白-β聚集程度,并将其结果表示为相对于对照组(100%)的相对值,如下表1所示。
【表1】
如上表1所示,可以确认利福喷丁和三氟丙嗪抑制淀粉样蛋白-β聚集活性的效果显著高于其他化合物。
实施例2:降解淀粉样蛋白-β聚集试验(Aβdisaggregation test)
2.1、准备试料
将利福喷丁溶解于二甲基亚砜(DMSO)以使其浓度为5mM。然后,将所述化合物用6%二甲基亚砜(在蒸馏水中)稀释并使用。
将三氟丙嗪盐酸盐溶解于二甲基亚砜以使其浓度为5mM。然后,将所述化合物用6%二甲基亚砜(在蒸馏水中)稀释并使用。
通过将Aβ
另一方面,将硫黄素-T溶解于50mM甘氨酸缓冲液(pH8.5)以使其浓度为5mM。然后,使用50mM甘氨酸缓冲液(pH8.5)将其稀释至5μM,并在避光的暗室保存。
2.2、通过硫黄素T分析的降解淀粉样蛋白-β聚集试验
将所述实施例2.1中准备的淀粉样蛋白-β溶液分别放入每个1.5mL微量离心分离管中,以使其浓度为25μM,然后在37℃下反应72小时。
对于所述每个1.5mL微量离心分离管,将利福喷丁和三氟丙嗪分别处理为50μM或500μM的不同浓度,然后在37℃下反应72小时。
将完成反应的反应液以25μL的量分别添加到96孔荧光分析板的每个孔中,然后将所准备的硫黄素-T溶液以75μL的量分别添加到每个孔中。在室温的暗室条件下进行5分钟反应后,使用多模式酶标仪(multi-mode microplate reader)在450nm激发(excitation)和485nm发射(emission)下测量荧光值。
将仅处理淀粉样蛋白-β以聚集72小时的组(对照组)的荧光值转换为%值并将其表示为100,并且将所测得的荧光值转换为其相对值,其结果如图3和图4所示。
图3显示利福喷丁的降解淀粉样蛋白-β聚集效果(对照组:Aβ
图4显示三氟丙嗪的降解淀粉样蛋白-β聚集效果(对照组:Aβ
2.3、通过SDS-PAGE分析的降解淀粉样蛋白-β聚集试验
为了确认在所述实施例2.1准备的试料中降解淀粉样蛋白-β的聚集,如下进行SDS-PAGE分析。
更详细地,在琥珀试管(Axygen,MCT-150-X)中,使用未修饰蛋白质的光催化交联(Photo-induced cross-linking of unmodified proteins,PICUP)缓冲液(0.1M磷酸钠(pH7.4))制备硫酸铵(APS,200mM)和三联吡啶氯化钌六水合物(Tris(2,2'-bipyridyl)dichlororuthenium(II)hexahydrate,Ru,10mM)的储备液(stock)。将所述储备液在PICUP缓冲液中稀释10倍(APS:20mM/Ru:1mM)。将所述实施例2.1中准备的每个试料以10μL分别分配到0.5mL试管(Axygen,PCR-05-C)的底部。将APS(20mM)1μL分配到试管壁上,而将Ru(1mM)1μL分配到试管帽上。此时,为了防止反应进行,不将试料与APS和Ru混合。关闭试管帽并使用离心机旋转后,将试管从离心机中取出,并使用白炽灯每秒曝光3次。向每个试管加入5X还原样品缓冲液(reducing Sample buffer)(w/5%β-巯基乙醇)3μL。将试料在95℃至100℃下加热5分钟,然后在冰上冷却。
然后,将所述经PICUP处理的试料加载到4%至20%(w/v)的Tris-甘氨酸凝胶上,并在100V下进行电泳1小时30分钟。分离完成电泳的凝胶,并通过银染来确认。
所获得的电泳结果示于图5和图6。在图5和图6中,除了最左侧的大小标记泳道外,第一泳道(淀粉样蛋白-β聚集体(-)+化合物(-))显示Aβ
实施例3:利福霉素系衍生物的降解淀粉样蛋白-β聚集试验(Aβdisaggregationtest)
3.1、准备试料
将化合物(利福喷丁、利福平、利福布汀、利福霉素SV、利福霉素B、利福霉素S、利福昔明、利福定;以上利福霉素系衍生物)溶解于二甲基亚砜以使其浓度为5mM。然后,将所述化合物用6%二甲基亚砜(在蒸馏水中)稀释并使用。
通过将Aβ
另一方面,将硫黄素-T溶解于50mM甘氨酸缓冲液(pH8.5)以使其浓度为5mM。然后,使用50mM甘氨酸缓冲液(pH8.5)将其稀释至5μM,并在避光的暗室保存。
3.2、通过硫黄素T分析的降解淀粉样蛋白-β聚集试验
将所述实施例3.1中准备的淀粉样蛋白-β溶液分别放入每个1.5mL微量离心分离管中,以使其浓度为50μM,然后在37℃下反应72小时。
对于所述每个1.5mL微量离心分离管,将利福喷丁系衍生物分别处理为50μM的浓度,然后在37℃下反应48小时。
将完成反应的反应液以25μL的量分别添加到96孔荧光分析板的每个孔中,然后将所准备的硫黄素-T溶液以75μL量分别添加到每个孔中。在室温的暗室条件下进行5分钟反应后,使用多模式酶标仪(multi-mode microplate reader)在450nm激发(excitation)和485nm发射(emission)下测量荧光值。
将仅处理淀粉样蛋白-β以聚集72小时的组(对照组)的荧光值转换为%值并将其表示为100,并且将所测得的荧光值转换为其相对值,其结果如图7所示。
图7显示包括利福喷丁的利福霉素系衍生物的降解淀粉样蛋白-β聚集效果(对照组:Aβ
实施例4:口服给药利福喷丁对APP/PS1 TG小鼠的淀粉样蛋白斑块减少效果的确认
4.1、准备APP/PS1 TG小鼠模型
转基因小鼠(APP/PS1 TG;阿尔茨海默氏病动物模型;B6C3-Tg(APPswe,PSEN1dE)85Dbo/Mmjax)和野生型小鼠(WT)均来自杰克逊实验室(Jackson Laboratory,美国缅因州巴港)。APP/PS1 TG小鼠与野生型小鼠杂交并保持为双半合子(double hemizygotes)。根据杰克逊实验室的标准聚合酶链式反应(PCR)条件,通过使用尾部DNA(tail DNA)的PCR分析来确认所有基因型。在动物饲养室的每个塑料笼里放入一只小鼠,交替进行12小时的明暗循环,将温度保持在21±1℃,并且使小鼠自由摄取食物和水。
4.2、用利福喷丁处理小鼠模型
将利福喷丁以200mg/kg的浓度每周一次(TG,RP 200QW)或以50mg/kg的浓度每两天一次(TG,RP 50QOD)口服给予10个月龄的APP/PS1 TG小鼠9周。将相同量的溶媒(vehicle,Veh)(蒸馏水中0.5%MC)施用于对照组。所述施用是通过使用用于口服给药的探针(sonde),根据小鼠的体重将其溶解于10ml/kg(v/w)的溶媒来进行的。
4.3、准备脑组织样品
使用2%阿佛丁(Avertin)(20mg/g,i.p.麻醉小鼠。用0.9%氯化钠灌注所述小鼠并切除其大脑。在4℃下,将所述半脑在4%多聚甲醛(pH7.4)中固定过夜。对用多聚甲醛固定的大脑进行脱水过程,以使用石蜡制备组织块。
4.4、免疫组织化学染色
将所述实施例4.3中准备的用石蜡固定的脑组织切成5μm至6μm厚的切片,以进行免疫组织化学染色。在组织切片用脱蜡(dewax)、补水(rehydrate)和1%过氧化氢处理以去除内源性过氧化物酶(endogenous peroxidase)后,为了抑制非特异性反应,使用10%(v/v)正常山羊血清(goat normal serum)进行阻断(blocking)过程60分钟,然后使用Aβ抗体将斑块染色(过夜,4℃)。第二天用磷酸盐缓冲液(PBS)洗涤后,使用ABC试剂盒(VectastinABC试剂盒,Vector Laboratories)进行二抗染色,然后在显微镜下观察。如图8的淀粉样蛋白-β斑块的染色图和图9以及图10的图表所示,与对照组小鼠(TG-Veh)相比,在施用利福喷丁的小鼠中所述斑块数量和总斑块面积减少。
实施例5:口服给药三氟丙嗪对5X FAD小鼠的淀粉样蛋白斑块和磷酸化Tau减少效果的确认
5.1、准备5X FAD小鼠模型
转基因小鼠(5XFAD;阿尔茨海默氏病动物模型;B6SJL-Tg(APPSwFlLon,PSEN1*M146L*L286V)6799Vas/Mmjax)和野生型小鼠得自杰克逊实验室(美国缅因州巴港)。5X FAD小鼠与野生型小鼠杂交并保持为双半合子(double hemizygotes)。根据杰克逊实验室的标准聚合酶链式反应(PCR)条件,通过使用尾部DNA(tail DNA)的PCR分析来确认所有基因型。在动物饲养室的每个塑料笼里放入4只至6只小鼠,交替进行12小时的明暗循环,将温度保持在21±1℃,并且使小鼠自由摄取食物和水。
5.2、在小鼠模型中处理三氟丙嗪
将三氟丙嗪以50mg/kg的浓度每两天一次口服给予7个月龄的5X FAD小鼠3周。将相同量的溶媒(vehicle)(磷酸盐缓冲液中1%(w/v)二甲基亚砜)施用于对照组。所述施用是通过使用用于口服给药的探针,根据小鼠的体重将其溶解于10ml/kg(v/w)的溶媒来进行的。
5.3、准备脑组织样品
使用2%(w/v)阿佛丁(20mg/g,i.p.麻醉小鼠。用0.9%(w/v)氯化钠灌注所述小鼠并切除其大脑。在4℃下,将所述半脑在4%(w/v)多聚甲醛(pH7.4)中固定过夜。为了进行冷冻保存,将大脑浸泡于30%(w/v)蔗糖中48小时。将所述其他半脑解剖成皮质和海马区域,并在含有1x蛋白酶抑制剂鸡尾酒的裂解缓冲液(10mM Tris-氯化氢,320mM蔗糖中的5mM乙二胺四乙酸(EDTA),pH7.4)中的冰上进行均匀化30分钟。将所述样品在4℃下,以13500rpm进行离心分离30分钟。使用BCA蛋白分析试剂盒(thermoFisher,cat#232250),根据制造商的说明测量裂解液的浓度。所述吸光度在560nm处读取。
5.4、免疫组织化学染色和ThS染色
为了用硫黄素S(thioflavin S,ThS)对冷冻的脑进行染色,使用低温恒温器(Leica CM1800)将脑切成35μm厚的组织切片,然后对Aβ斑块进行染色。在乙醇(50%(v/v))中以500uM的浓度进行ThS染色7分钟。并且将所述切片依次在100%、90%和70%(v/v)的乙醇中洗涤10秒钟,然后放入磷酸盐缓冲液中。使用Leica DM2500荧光显微镜获得图像。如图11所示,将对照组小鼠(vehicle,磷酸盐缓冲液中的1%(w/v)二甲基亚砜)与施用本发明的三氟丙嗪的小鼠进行比较,在施用三氟丙嗪的小鼠中的斑块数量和总斑块面积减少。
5.5、蛋白印迹试验(Western blot Assay)方法
通过蛋白印迹(Western blot)分析确认了Aβ斑块和Tau的变化,其中Tau为阿尔茨海默氏痴呆症和帕金森氏病的主要致病蛋白质。通过SDS-PAGE分离所准备的组织的样品,并转移至聚偏氟乙烯(PVDF)膜。使用一抗将所述膜在4℃下处理过夜。作为一抗,使用可检测总Tau(T-Tau)和磷酸化Tau(P-Tau)的抗体,并使用与辣根过氧化酶(HRP)共轭(conjugated)的二抗进行检测。根据制造商的说明,使用ECL化学发光底物(ClarityWestern ECL substrte,Bio-Rad)进行所述印迹显影。
所获得的蛋白印迹结果如图12所示。如图12所示,将对照组小鼠(Tg veh,磷酸盐缓冲液中的1%(w/v)二甲基亚砜)与施用三氟丙嗪的转基因小鼠(Tg TFP,n=4)进行比较,已经确认在施用三氟丙嗪的小鼠中,大脑皮质(cortex)和海马(hippocampus)组织中的T-Tau(Total Tau)和P-Tau(磷酸化Tau)均减少。这些结果表明,三氟丙嗪在作为阿尔茨海默氏病动物模型的转基因动物(Tg)中具有降低总Tau蛋白水平并抑制Tau蛋白磷酸化的效果。另一方面,在野生型小鼠(Wt)中,施用三氟丙嗪后,未观察到总Tau(T-Tau)和磷酸化Tau(P-Tau)显着减少。
实施例6:口服给药利福喷丁对APP/PS1 TG小鼠的认知功能改善效果的确认
6.1、准备APP/PS1 TG小鼠模型
转基因小鼠(APP/PS1 TG;阿尔茨海默氏病动物模型;B6C3-Tg(APPswe,PSEN1dE)85Dbo/Mmjax)和野生型小鼠均来自杰克逊实验室(Jackson Laboratory,美国缅因州巴港)。这些APP/PS1 TG小鼠与野生型小鼠杂交并保持为双半合子(double hemizygotes)。根据杰克逊实验室的标准聚合酶链式反应(PCR)条件,通过使用尾部DNA(tail DNA)的PCR分析来确认所有基因型。在动物饲养室的每个塑料笼里放入一只小鼠,交替进行12小时的明暗循环,将温度保持在21±1℃,并且使小鼠自由摄取食物和水。
6.2、用利福喷丁处理小鼠模型
将利福喷丁以200mg/kg的浓度每周一次或以50mg/kg的浓度每两天一次口服给予10个月龄的APP/PS1 TG小鼠9周。将相同量的溶媒(vehicle)(蒸馏水中0.5%MC)施用于对照组。所述施用是通过使用用于口服给药的探针,根据小鼠的体重将其溶解于10ml/kg(v/w)的溶媒来进行的。
6.3、Y迷宫测试(Y-maze test)
安装迷宫框以进行Y迷宫测试,所述迷宫框是通过将相同的三个40厘米长(壁高15厘米)的臂(arm)以120度的角度排列而制成的所述实验是利用啮齿类动物探索习性的本能进行的行为实验,是一种侧重于探索新领域的高可能性的方法。记住刚搜索过的臂(arm)而不进入相同臂的次数越多,记忆力的数值就显示为越高。提供每个个体8分钟的搜索时间,并且最终结果表示为自发变换(%)值。通过以下公式计算自发变换(Spontaneousalteration)(%)。
【公式】
自发变换(%)=三联体数(The number oftriplet)/(进臂总次数(total armentry)-2)
行为模式的分析是通过使用SMART VIDEO TRACKING软件(美国Panlab)来进行。试验中获得的所有数据均以平均值±标准误差平均值(mean±Standard Error Mean(SEM))表示,并进行作为比较对象组的药物施用组之间的比较和药物施用组与药物未施用组的比较,以使用学生t检验(student’s t-test)进行组间分析。根据如图13所示,在转基因的阿兹海默氏痴呆动物(APP/PS1 TG)中施用利福喷丁后第8周时进行Y-迷宫测试(Y-mazetest)的结果,可以确认与阴性对照组(TG-Veh)相比,测量实验动物抓住周围的线索并依次进入迷宫的相对频率的自发变换(spontaneous alteration)(%)值改善得更接近阳性对照组(WT-Veh)。
6.4、新物体识别试验(Novel Object Recognition)
新物体识别试验在40cm×40cm的丙烯酸笼中使用两个不同的物体来评估记忆力。在使实验动物适应丙烯酸笼的内部后,将两个物体放置在某个位置以使其自由识别,然后测量搜索每个物体所需的时间。向每个个体提供24小时的延迟时间,并且在同一位置上仅将一个物体更改为另一个物体。此时,由于将更改后的物体识别为新物体,因此搜索时间越长,可以判断其记忆力越好。如果不记得24小时之前的物体,则无法区分新物体和现有物体,从而会均一地搜索两个物体。使实验动物总共自由探索10分钟的时间,并将其结果表示为偏好指数(preference index)(新物体探索时间/总探索时间(Novel object exploringtime/total exploring time))。分析通过使用SMART VIDEO TRACKING软件(美国Panlab)来进行。试验中获得的所有数据均以平均值±标准误差平均值(mean±Standard ErrorMean(SEM))表示,并进行作为比较对象组的药物施用组之间的比较和药物施用组与药物未施用组的比较,以使用学生t检验(student’s t-test)进行组间分析。根据如图14所示在转基因的阿兹海默氏痴呆动物(APP/PS1 TG)中施用利福喷丁后第8周时进行新物体识别试验(Novel Object Recognition)的结果,测量实验动物搜索新物体的频率的偏好指数(Preference Index)的值增加,从而可以确认与阴性对照组(TG-Veh)相比,记忆力的数值改善得更接近阳性对照组WT-Veh。
- 一种用于治疗淀粉样蛋白脑神经疾病的组合物和其治疗方法
- 用于淀粉样蛋白积聚性疾病的探针、用于染色淀粉样蛋白的试剂、用于治疗或预防淀粉样蛋白积聚性疾病的药物、以及用于诊断神经原纤维缠结的探针以及用于染色神经原纤维缠结的试剂
