一种吴茱萸碱衍生物及其制备方法与作为PGAM1抑制剂的应用
文献发布时间:2024-04-18 19:58:26
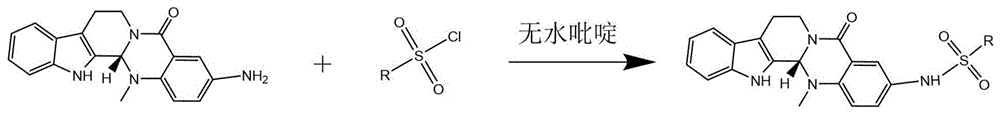
技术领域
本发明属于药物技术,具体涉及一种含有吴茱萸碱结构单元的PGAM1抑制剂的制备方法与应用。
背景技术
目前已有IDH[X. Tang, C.C. Lin, I. Spasojevic, et al. A joint analysisof metabolomics and genetics of breast cancer, Breast Cancer Res, 16 (2014)415.]和PKM2[D. Anastasiou, Y. Yu, W.J. Israelsen, et al. Pyruvate kinase M2activators promote tetramer formation and suppress tumorigenesis, Nat ChemBiol, 8 (2012) 839-847.]小分子靶向作为抗癌药物的报道,这也表明调节癌细胞代谢可能成为一种新的癌症治疗手段。磷酸甘油酸突变酶1(Phosphoglycerate Mutase 1,PGAM1)是糖酵解途径将3-磷酸甘油酸(3PG)转化为2-磷酸甘油酸(2PG)的第8步的关键酶。由于PGAM1同时调节糖酵解和生物合成,开发针对PGAM1的抑制剂被认为是一种双重抑制分解代谢和合成代谢的癌症治疗方法。但是现有PGAM1抑制剂有一定的缺点,例如:在体内的代谢和稳定性不理想,导致药物的生物利用度降低或药物在体内的持续时间较短。这可能需要通过药物化学的优化来解决。类似于其他抗肿瘤药物,PGAM1抑制剂面临肿瘤细胞对药物的耐药性问题。这可能需要结合其他治疗策略,如联合用药或药物组合治疗,来克服耐药性。由于PGAM1在正常细胞中也起着重要的生理功能,抑制剂会对正常细胞产生不良影响。因此,需要进一步评估抑制剂的安全性和毒副作用,以确保其在临床应用中的可行性。
发明内容
本发明公开了一种含有吴茱萸碱结构单元的PGAM1抑制剂的制备方法与应用。目前,化疗仍作为癌症治疗的首选手段。虽然化疗药物治疗效果好,但毒副作用大,会产生耐药性。很多天然植物提取物被证明可有效治疗恶性肿瘤,其作用机制有别于传统化疗药,逐渐引起了肿瘤制药界的关注。然而,化疗药物和天然植物提取物均只针对单个药物靶点,易发生代偿性调节。本发明报道了含有吴茱萸碱结构单元的PGAM1抑制剂的设计、合成和药物研究,公开所合成的化合物对人多种细胞系细胞活性和凋亡等的影响,并进一步探讨其机制。
本发明采用如下技术方案:
一种吴茱萸碱衍生物,其化学结构式如下:
。
上述吴茱萸碱衍生物的制备方法为以下步骤,将3-氨基吴茱萸碱与磺酰氯中间体反应,制备所述吴茱萸碱衍生物;所述磺酰氯中间体的化学结构式 如下:
。
本发明中,R为芳基、取代芳基、取代杂环基中的一种或几种。优选的,芳基为苯基、稠环苯基或者联苯基;取代苯基中,取代基包括烷基、烷氧基、卤代烷基、卤代烷氧基、卤素、酰基、酯基中的一种或几种;取代杂环基中,取代基包括卤代烷基、酯基中的一种或几种;杂环基为氧杂环基。进一步优选的,取代基中,烷基为具有1~10个碳原子的直链、支链或环烷基;稠环苯基包括2~10个苯环;酰基包括丙烯酰基、丁烯酰基、乙酰基、对甲苯磺酰基、苯甲酰基。
本发明中,反应在有机碱的催化作用下进行;反应的时间为1~10小时,温度为0~60℃。优选的,有机碱为吡啶及其衍生物;反应的时间为2~6小时,温度为室温。
本发明中,3-氨基吴茱萸碱与磺酰氯中间体的摩尔比为1∶(1~2)。
本发明公开了一种药物组合物,包含治疗有效量的一种或多种上述吴茱萸碱衍生物以及药学上可接受的赋形剂、载体或稀释剂。上述药学上可接受的盐包括有机酸盐或无机酸盐;其中无机酸包括:盐酸、硫酸、磷酸、二磷酸、氢溴酸或硝酸;有机酸包括:乙酸、马来酸、富马酸、酒石酸、琥珀酸、乳酸、对甲苯磺酸、水杨酸或草酸。赋形剂、载体或稀释剂为常规产品。
本发明公开了上述吴茱萸碱衍生物或其药学上可接受的盐或者上述药物组合物在制备PGAM1抑制剂或者作为PGMA1抑制剂的应用;或在制备抗肿瘤药物或者抗肿瘤细胞药物中的应用。
作为示例,本发明公开了一种含有吴茱萸碱结构单元的PGAM1抑制剂,其制备方法为,将3-氨基吴茱萸碱溶解于无水吡啶中,然后加入相应的苯磺酰氯,在室温下搅拌;反应完成后,先用展开剂进行点板观察,用20%HCl,乙酸乙酯萃取悬浮液,直至完全除去吡啶,接着用无水Na2SO4进行干燥,蒸发后得到固体化合物。
本发明成功设计并合成了含有吴茱萸碱结构单元的PGAM1抑制剂,然后在体外实验评估其生物活性。合成的吴茱萸碱衍生物对H460和PC9具有较强的抑制活性。作为具体的实验:MTT结果显示,吴茱萸碱衍生物能抑制细胞活力和增殖,且呈剂量和时间依赖性,其中化合物13对肺癌细胞H460的抑制活性(IC
附图说明
图1为含有吴茱萸碱结构单元的PGAM1抑制剂的合成路线;
图2为采用MTT法测定不同化合物作用于H460、PC9细胞的细胞毒性结果;
图3为采用MTT法测定不同化合物作用于PC9/GR、H1299和SW620细胞的细胞毒性结果;
图4为化合物13的细胞凋亡结果,采用不同浓度的化合物作用于H460细胞;
图5为阳性药物的细胞凋亡结果,采用不同浓度的化合物作用于H460细胞。
具体实施方式
本发明将不同原料通过化学方式键合,获得毒副作用降低,药理作用相加或协同的新化合物。反应过程中涉及到的原料及试剂,除了特殊说明之外,均为分析纯,均从SigmaAldrich Trading Co. Ltd.购买。核磁共振波谱仪为德国公司Bruker AVANCE400和Bruker AVANCE500型,TMS做内标物,溶剂采用DMSO-
本发明公开了3-氨基吴茱萸碱与苯磺酰氯发生亲核取代反应,得到含有吴茱萸碱结构单元的PGAM1抑制剂。还公开了上述含有吴茱萸碱结构单元的PGAM1抑制剂在制备抗肿瘤药物中的应用。优选的肿瘤为肺癌。终产物合成路线如图1所示。将3-氨基吴茱萸碱溶解于无水吡啶中,然后加入相应的苯磺酰氯,在室温下搅拌;反应完成后,先用展开剂(CH2Cl2:CH3OH=10:1)进行点板观察,用20%HCl(20mL),乙酸乙酯(20mL)萃取悬浮液,直至完全除去吡啶,接着用适量无水 Na
实施例一 含有吴茱萸碱结构单元的PGAM1抑制剂的制备
2-氟-N-(14-甲基-5-氧代-5,7,8,13,13b,14-六氢吲哚[2',3':3,4]吡啶并[2,1-b] 喹唑啉-3-基)苯磺酰胺(1)
将3-NH-EVO(100mg,1mmol)盛入10mL反应瓶中,加入无水吡啶(3mL),搅拌至完全溶解,再加入2-氟苯磺酰氯(91.66mg,1.5mmol),在室温下搅拌4h,薄层色谱监测反应过程。反应完成后,加20%稀盐酸(20mL),再加乙酸乙酯(20mL),萃取3次,直至完全除去吡啶,加无水硫酸钠干燥,减压蒸馏得到棕黄色固体51 mg,产率:44.8%。M.p= 25℃;R f = 0.33(二氯甲烷:甲醇= 10:1)。
。
其他化合物也以类似的方法合成,改变磺酰氯即可,具体参见表1,薄层色谱监测反应过程。
4-氯-N-(14-甲基-5-氧代-5,7,8,13,13b,14-六氢吲哚[2',3':3,4]吡啶并[2,1-b] 喹唑啉-3-基)苯磺酰胺(2)
黄色固体(45mg),产率:38.8%。
3-溴-N-(14-甲基-5-氧代-5,7,8,13,13b,14-六氢吲哚[2',3':3,4]吡啶并[2,1-b]喹唑啉-3-基)苯磺酰胺(3)
黄色固体(113毫克),产率:98%。
3-溴-N-(14-甲基-5-氧代-5,7,8,13,13b,14-六氢吲哚[2',3':3,4]吡啶并[2,1-b]喹唑啉-3-基)苯磺酰胺(4)
黄色固体(61mg),产率:53.4%。
2-溴-N-(14-甲基-5-氧代-5,7,8,13,13b,14-六氢吲哚[2',3':3,4]吡啶并[2,1-b]喹唑啉-3-基)苯磺酰胺(5)
黄色固体(65mg),产率:56.3%。
4-碘-N-(14-甲基-5-氧代-5,7,8,13,13b,14-六氢吲哚[2',3':3,4]吡啶并[2,1-b]喹唑啉-3-基)苯磺酰胺(6)
黄色固体(81mg),产率70.8%。
2,4,6-三氯-N-(14-甲基-5-氧代-5,7,8,13,13b,14-六氢吲哚[2',3':3,4]吡啶并[2,1-b]喹唑啉-3-基)苯磺酰胺(7)
橙色固体(86毫克),产率:75.5%。
2,4-二氯-N-(14-甲基-5-氧代-5,7,8,13,13b,14-六氢吲哚[2',3':3,4]吡啶并[2,1-b]喹唑啉-3-基)苯磺酰胺(8)
橙色固体(28mg),产率:24.2%。
4-(氯甲基)-5-(N-(14-甲基-5-氧代-5,7,8,13,13b,14-六氢吲哚[2',3':3,4]吡啶并[2,1-b]喹唑啉-3-基)氨基磺酰基)呋喃-2-羧酸甲酯(9)
黄色固体(104mg),产率:90.0%。
2,4,6-三异丙基-N-(14-甲基-5-氧代-5,7,8,13,13b,14-六氢吲哚[2',3':3,4]吡啶并[2,1-b]喹唑啉-3-基)苯磺酰胺(10)
红棕色固体(63mg),产率:55.0%。
4-(叔丁基)-N-(14-甲基-5-氧代-5,7,8,13,13b,14-六氢吲哚[2',3':3,4]吡啶并[2,1-b]喹唑啉-3-基)苯磺酰胺(11)
黄色固体(35mg),产率:30.4%。
4'-氯-N-(14-甲基-5-氧代-5,7,8,13,13b,14-六氢吲哚[2',3':3,4]吡啶并[2,1-b]喹唑啉-3-基)-[1,1'-联苯]-4-磺酰胺(12)
黄色固体(40mg),产率:35.2%。
N-(14-甲基-5-氧代-5,7,8,13,13b,14-六氢吲哚[2',3':3,4]吡啶并[2,1-b]喹唑啉-3-基)-3-(三氟甲氧基)苯磺酰胺(13)
棕黄色固体(58mg),产率:50.4%.
4-氟-N-(14-甲基-5-氧代-5,7,8,13,13b,14-六氢吲哚[2',3':3,4]吡啶并[2,1-b]喹唑啉-3-基)-3-(三氟甲基)苯磺酰胺(14)
棕色固体(82mg),产率:71.1%。
4-甲基-N-(14-甲基-5-氧代-5,7,8,13,13b,14-六氢吲哚[2',3':3,4]吡啶并[2,1-b]喹唑啉-3-基)苯磺酰胺(15)
黄色固体(35mg),产率:30.0%。
N-(14-甲基-5-氧代-5,7,8,13,13b,14-六氢吲哚[2',3':3,4]吡啶并[2,1-b]喹唑啉-3-基)萘-1-磺酰胺(16)
黄色固体(58mg),产率:50.2%。
N-(14-甲基-5-氧代-5,7,8,13,13b,14-六氢吲哚[2',3':3,4]吡啶并[2,1-b]喹唑啉-3-基)-[1,1'-联苯]-4-磺酰胺(17)
黄色固体(73mg),产率:63.6%。
4-环己基-N-(14-甲基-5-氧代-5,7,8,13,13b,14-六氢吲哚[2',3':3,4]吡啶并[2,1-b]喹唑啉-3-基)苯磺酰胺(18)
黄色固体(81mg),产率:70.5%。
2-氟-N-(14-甲基-5-氧代-5,7,8,13,13b,14-六氢吲哚[2',3':3,4]吡啶并[2,1-b]喹唑啉-3-基)苯磺酰胺(19)
棕黄色固体(31mg),产率27.0%。
N-(14-甲基-5-氧代-5,7,8,13,13b,14-六氢吲哚[2',3':3,4]吡啶并[2,1-b]喹唑啉-3-基)-1-苯基甲磺酰胺(20)
棕黄色固体(44mg),产率:38.0%。
3,5-二氟-N-(14-甲基-5-氧代-5,7,8,13,13b,14-六氢吲哚[2',3':3,4]吡啶并[2,1-b]喹唑啉-3-基)苯磺酰胺(21)
黄色固体(74mg),产率:64.0%。
实施例二 目标化合物体外PGAM1抑制活性的研究
测试了目标化合物对PGAM1酶的抑制活性。PGAM1酶活板是从江苏酶科生物技术有限公司购买的(编号:MK530295A)。试剂、样本和标准品在37℃孵育30分钟。接着,将板子洗涤五次,添加酶标试剂,再次在37℃孵育30分钟,并再次洗涤五次。随后,将A和B两种显色剂(每个孔加入50μL)加入到各个孔中。板子轻轻摇动后,在黑暗中37℃储存10分钟,使颜色得以改变。然后,加入50μL的终止液到每个孔中,使蓝色变为黄色。添加终止液后的15分钟内测量每个孔的OD值。阳性对照选用PGMI-004A。如表2所示,大多数化合物对PGAM1具有良好或极好的抑制活性(IC
实施例三 细胞毒性实验
细胞系H460、PC9、H1299和LO2细胞在含有10% (v/v)胎牛血清和1%青霉素/链霉素(P/S)的RPMI-1640培养基中孵育,PC9/GR、 SW620在含有10% (v/v)胎牛血清和1%青霉素/链霉素(P/S)的DMEM培养基中孵育,温度为37℃,5%CO
采用MTT法测定目标化合物1~21、阳性药PGMI-004A对人细胞系H460、PC9、PC9/GR、H1299、SW620和LO2的体外抗增殖抑制作用。取对数生长期的细胞于96孔细胞板分别给药处理72 h,各药物组中分别设立5个不同浓度组,为2.5、5.0、10.0、20.0、40.0μM。实验结果如图2和图3所示,对于所测定的六种细胞株,目标化合物1~21、阳性药PGMI-004A对H460和PC9具有明显的抑制作用,且剂量依赖方式抑制细胞存活;大多数目标化合物的体外抗肿瘤作用强于PGMI-004A;尤其是化合物13处理H460和PC9达到72小时,IC
实施例四 细胞凋亡分析
为了更好地探究MTT实验中观察到的不同化合物抗增殖活性抑制是否与诱导细胞凋亡的能力有关,采用流式细胞仪和Annexin V-FITC/碘化丙啶(PI)法研究化合物13的肿瘤细胞凋亡。H460细胞分别在2.5、5和10 μM的浓度下孵育。如图4所示,化合物13有效诱导H460细胞系凋亡,且呈浓度依赖性。随着给药浓度的增加,化合物13诱导的H460细胞凋亡率分别为:14.71%、30.88%、33.84%;阳性药PGMI-004A的凋亡率分别为:5.19%、5.40%、7.89%,参见图5。结果表明,化合物13能有效诱导细胞凋亡,其作用强于PGAM1抑制剂PGMI-004A。
结论
在3-NH-EVO引入苯磺酰氯取代基,设计并合成了具有不同取代基的PGAM1抑制剂(1~21)。用氢谱、碳谱和质谱分析了这些衍生物的结构。
本发明产物效果较好,尤其是含有取代基氟的化合物表现出更好的效果。本发明产物提高了药物的亲脂性,从而提高了药物在各种生物膜上的生物利用度和通透性,从而使药物与细胞受体、蛋白质和酶等各自的靶标结合。值得注意的是,化合物13能有效抑制5种癌细胞的增殖,其IC
综上所述,本发明扩展了EVO的结构类型,并发现其有抑制PGAM1的作用,为进一步开发更有效的抗肿瘤药物提供了新的方向。
- 中压制备色谱且纯化高纯吴茱萸碱和吴茱萸次碱的方法
- 一种含硫醚的三唑希夫碱杨梅素衍生物、其制备方法及用途
- 一种喜树碱衍生物及其在制备抗炎症药物中的应用
- 一种罗丹明类酰腙衍生物及其制备方法和应用以及一种荧光探针
- 一种吴茱萸次碱衍生物及其制备方法和应用
- 一种吴茱萸碱衍生物及其制备方法和应用
