用于低剂量放射治疗的肿瘤靶向性载体及其制备方法和肿瘤靶向药物
文献发布时间:2023-06-19 10:55:46
技术领域
本发明涉及抗肿瘤生物纳米医药技术领域,具体涉及一种用于低剂量放射治疗的肿瘤靶向性载体,本发明还涉及一种用于低剂量放射治疗的肿瘤靶向性载体的制备方法,本发明还涉及一种包括前述用于低剂量放射治疗的肿瘤靶向性载体的肿瘤靶向药物。
背景技术
放射疗法(RT)是用于治疗癌症的三种主要方法之一,它依赖于高能X射线或γ射线的靶向递送,诱导DNA损伤和肿瘤细胞凋亡,从而促进肿瘤消融。尽管RT是一种常见的治疗方式,但RT伴随着严重的副作用,其功效可能会受限于肿瘤微环境(TME)内的氧缺乏,导致无法完全根除靶肿瘤。目前很多临床试验试图通过高压氧疗法(HBO)克服RT的氧依赖性,以改善RT的治疗效果。然而, HBO也有严重的副作用,包括气压伤和高氧性癫痫发作等,因此该方法的实用性不强。最近有研究报道了肿瘤细胞内产生O
发明内容
有鉴于此,本发明提供了一种用于低剂量放射治疗的肿瘤靶向性载体,本发明还提供了一种用于低剂量放射治疗的肿瘤靶向性载体的制备方法,本发明还提供了一种用于低剂量放射治疗的药物,以解决现有放射疗法存在的肿瘤靶向性差、肿瘤细胞反射敏感性低等缺陷。
第一方面,本发明提供了一种用于低剂量放射治疗的肿瘤靶向性载体,包括厌氧菌以及吸附于所述厌氧菌上的黑磷量子点。
优选的,所述厌氧菌为大肠杆菌或者沙门氏菌。
本发明用于低剂量放射治疗的肿瘤靶向性载体包括厌氧菌以及吸附于所述厌氧菌上的黑磷量子点。该用于低剂量放射治疗的肿瘤靶向性载体采用的材料都是生物相容性材料,不会对人体产生副作用。该用于低剂量放射治疗的肿瘤靶向性载体由于具有厌氧菌,借助于厌氧菌的厌氧趋向性,使得该肿瘤靶向性载体能够精确定位到肿瘤细胞。该用于低剂量放射治疗的肿瘤靶向性载体采用了黑磷量子点(BPQD),具有高的光热转换效率,通过光热作用达到靶向治疗低氧肿瘤细胞的效果。另一方面,黑磷量子点(BPQD)也具有放射疗法增敏作用,两者协同,能够显著提高放射治疗的疗效,由此可以实现低剂量的治疗肿瘤,具有巨大的临床应用潜力。
第二方面,本发明还提供了一种用于低剂量放射治疗的肿瘤靶向性载体的制备方法,包括以下步骤:
提供厌氧菌和黑磷量子点,对所述厌氧菌进行表面氨化处理,将表面氨化处理的厌氧菌与黑磷量子点混合以使黑磷量子点吸附到厌氧菌上,制得用于低剂量放射治疗的肿瘤靶向性载体。
本发明用于低剂量放射治疗的肿瘤靶向性载体的制备方法具有步骤简单,成本低,可用于大规模工业化生产等优点。
优选的,所述黑磷量子点的制备方法如下:提供黑磷粉末并将黑磷粉末溶于 N-甲基吡咯烷酮中,将黑磷粉末的N-甲基吡咯烷酮分散系依次进行探头超声和水浴超声,将水浴超声后的分散系先进行初级离心收集上清液,再对上清液进行次级离心收集沉淀,得到黑磷量子点。
优选的,所述黑磷粉末的N-甲基吡咯烷酮分散系中黑磷的浓度为0.25~ 5mg/ml。
优选的,所述探头超声的功率为600~2400W,所述探头超声的时间为1~5 h,所述探头超声的频率为19~25kHz;
所述探头超声为脉冲探头超声,所述脉冲探头超声设置为工作2s,间隔4s。
优选的,所述水浴超声的功率为150~500W,所述水浴超声的时间为5~20 h,所述水浴超声的温度为4℃以下。
优选的,所述初级离心的转速为5000~8000rpm,所述初级离心的时间为 10~30min,所述次级离心的转速为10000~15000rpm,所述次级离心的时间为10~30min。
优选的,所述氨化处理的具体方法为:提供氨化试剂和厌氧菌的PBS溶液,将所述氨化试剂和厌氧菌的PBS溶液混匀、离心,制得表面氨化处理的厌氧菌;
所述氨化试剂为DSPE-PEG-NH
优选的,所述PEG的平均分子量为2000。
优选的,所述氨化试剂与厌氧菌的PBS溶液的质量体积之比为0.1~5mg/ml,所述厌氧菌的PBS溶液中厌氧菌的浓度为10
优选的,所述表面氨化处理的厌氧菌与黑磷量子点搅拌混匀20~60min,所述搅拌的转数为100~500rpm。
优选的,表面氨化处理的厌氧菌与黑磷量子点搅拌混匀后,3500~7500rpm 离心2~10min,沉淀即为用于低剂量放射治疗的肿瘤靶向性载体。
第三方面,本发明还提供了一种用于低剂量放射治疗的药物,包括如本发明第一方面所述的用于低剂量放射治疗的肿瘤靶向性载体。
本发明用于低剂量放射治疗的药物包括用于低剂量放射治疗的肿瘤靶向性载体,同时具有肿瘤光热治疗、光动力治疗效果,另外也能增强反射治疗的敏感度,提升反射疗法的疗效。
本发明的优点将会在下面的说明书中部分阐明,一部分根据说明书是显而易见的,或者可以通过本发明实施例的实施而获知。
附图说明
为更清楚地阐述本发明的内容,下面结合附图与具体实施例来对其进行详细说明。
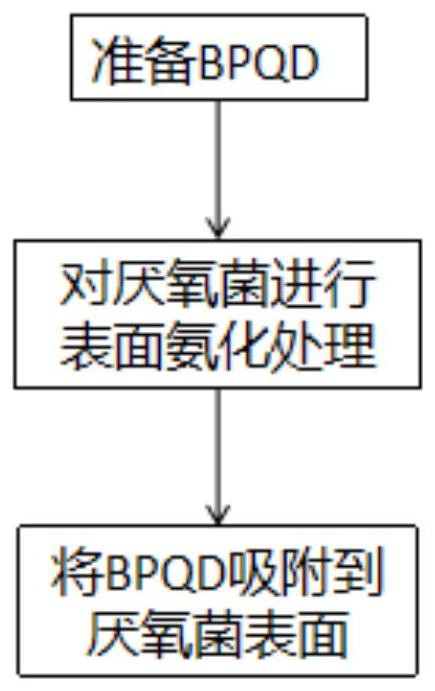
图1为本发明一实施方式提供的用于低剂量放射治疗的肿瘤靶向性载体的制备流程图;
图2为本发明提供的光照试验结果图;
图3为本发明提供的细胞存活率试验结果图;
图4为低氧环境光照下的细胞存活率试验结果图;
图5为光热和低剂量放射条件下常氧环境下的细胞存活率试验结果图;
图6为光热和低剂量放射条件下低氧环境下的细胞存活率试验结果图。
具体实施方式
以下所述是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也视为本发明的保护范围。
第一方面,本发明提供了一种用于低剂量放射治疗的肿瘤靶向性载体,包括厌氧菌以及吸附于所述厌氧菌上的黑磷量子点。
优选的,所述厌氧菌为大肠杆菌或者沙门氏菌。
第二方面,本发明还提供了一种用于低剂量放射治疗的肿瘤靶向性载体的制备方法,包括以下步骤:
提供厌氧菌和黑磷量子点,对所述厌氧菌进行表面氨化处理,将表面氨化处理的厌氧菌与黑磷量子点混合以使黑磷量子点吸附到厌氧菌上,制得用于低剂量放射治疗的肿瘤靶向性载体。
优选的,所述黑磷量子点的制备方法如下:提供黑磷粉末并将黑磷粉末溶于 N-甲基吡咯烷酮中,将黑磷粉末的N-甲基吡咯烷酮分散系依次进行探头超声和水浴超声,将水浴超声后的分散系先进行初级离心收集上清液,再对上清液进行次级离心收集沉淀,得到黑磷量子点。
优选的,所述黑磷粉末的N-甲基吡咯烷酮分散系中黑磷的浓度为0.25~ 5mg/ml。
优选的,所述探头超声的功率为600~2400W,所述探头超声的时间为1~5 h,所述探头超声的频率为19~25kHz;
所述探头超声为脉冲探头超声,所述脉冲探头超声设置为工作2s,间隔4s。
优选的,所述水浴超声的功率为150~500W,所述水浴超声的时间为5~20 h,所述水浴超声的温度为4℃以下。
优选的,所述初级离心的转速为5000~8000rpm,所述初级离心的时间为 10~30min,所述次级离心的转速为10000~15000rpm,所述次级离心的时间为10~30min。
优选的,所述氨化处理的具体方法为:提供氨化试剂和厌氧菌的PBS溶液,将所述氨化试剂和厌氧菌的PBS溶液混匀、离心,制得表面氨化处理的厌氧菌;
所述氨化试剂为DSPE-PEG-NH
优选的,所述PEG的平均分子量为2000。
优选的,所述氨化试剂与厌氧菌的PBS溶液的质量体积之比为0.1~5mg/ml,所述厌氧菌的PBS溶液中厌氧菌的浓度为10
优选的,所述表面氨化处理的厌氧菌与黑磷量子点搅拌混匀20~60min,所述搅拌的转数为100~500rpm。
优选的,表面氨化处理的厌氧菌与黑磷量子点搅拌混匀后,3500~7500rpm 离心2~10min,沉淀即为用于低剂量放射治疗的肿瘤靶向性载体。
第三方面,本发明还提供了一种用于低剂量放射治疗的药物,包括如本发明第一方面所述的用于低剂量放射治疗的肿瘤靶向性载体。
以下通过具体的实施例详细阐述用于低剂量放射治疗的肿瘤靶向性载体的制备方法以及制得的用于低剂量放射治疗的肿瘤靶向性载体。
实施例1
如图1所示,用于低剂量放射治疗的肿瘤靶向性载体的制备方法,包括以下步骤:
(1)超声剥离制备黑磷量子点(BPQD)
将25mg的BP粉末添加到装有25ml NMP(N-甲基吡咯烷酮)的50ml密封锥形管中,并在1200W的功率下用脉冲探头超声3h,超声频率设为22kHz,脉冲探头超声的脉冲设为工作2s,间隔4s。探头超声结束后,将脉冲探头超声后的分散系转移至水浴超声中继续超声分散,水浴超声的功率为300W,水浴超声的时间为 10h,水浴超声的温度保持在4℃以下。将经过两步超声分散后的分散系先以7000 rpm离心20分钟,轻轻倒出含黑磷量子点(BPQD)的上清液。然后,将含有黑磷量子点(BPQD)的上清液继续以12000rpm离心20分钟,得到黑磷量子点(BPQD)。
(2)对厌氧菌进行表面氨化处理
将1ml的含有大肠杆菌(1×10
(3)制备肿瘤靶向性载体
向上述1ml氨基修饰的厌氧菌的PBS溶液中添加300μg黑磷量子点(BPQD), 200rpm搅拌30min,搅拌混匀后再次对混合液进行离心,离心转速为5000rpm,离心时间为3min,收集沉淀即为用于低剂量放射治疗的肿瘤靶向性载体(BPQD- Esc,BE)。
实施例2
用于低剂量放射治疗的肿瘤靶向性载体的制备方法,包括以下步骤:
(1)超声剥离制备黑磷量子点(BPQD)
将6.25mg的BP粉末添加到装有25ml NMP(N-甲基吡咯烷酮)的50ml密封锥形管中,并在2400W的功率下用脉冲探头超声1h,超声频率设为25kHz,脉冲探头超声的脉冲设为工作2s,间隔4s。探头超声结束后,将脉冲探头超声后的分散系转移至水浴超声中继续超声分散,水浴超声的功率为150W,水浴超声的时间为20h,水浴超声的温度保持在2℃以下。将经过两步超声分散后的分散系先以 8000rpm离心10分钟,轻轻倒出含黑磷量子点(BPQD)的上清液。然后,将含有黑磷量子点(BPQD)的上清液继续以15000rpm离心10分钟,得到黑磷量子点 (BPQD)。
(2)对厌氧菌进行表面氨化处理
将1ml的含有大肠杆菌(1×10
(3)制备肿瘤靶向性载体
向上述1ml氨基修饰的厌氧菌的PBS溶液中添加100μg黑磷量子点(BPQD), 200rpm搅拌30min,搅拌混匀后再次对混合液进行离心,离心转速为5000rpm,离心时间为3min,收集沉淀即为用于低剂量放射治疗的肿瘤靶向性载体(BPQD- Esc,BE)。
实施例3
(1)超声剥离制备黑磷量子点(BPQD)
将125mg的BP粉末添加到装有25ml NMP(N-甲基吡咯烷酮)的50ml密封锥形管中,并在600W的功率下用脉冲探头超声5h,超声频率设为19kHz,脉冲探头超声的脉冲设为工作2s,间隔4s。探头超声结束后,将脉冲探头超声后的分散系转移至水浴超声中继续超声分散,水浴超声的功率为500W,水浴超声的时间为5h,水浴超声的温度保持在0℃以下。将经过两步超声分散后的分散系先以5000 rpm离心30分钟,轻轻倒出含黑磷量子点(BPQD)的上清液。然后,将含有黑磷量子点(BPQD)的上清液继续以10000rpm离心30分钟,得到黑磷量子点(BPQD)。
(2)对厌氧菌进行表面氨化处理
将1ml的含有沙门氏菌(1×10
(3)制备肿瘤靶向性载体
向上述1ml氨基修饰的厌氧菌的PBS溶液中添加500μg黑磷量子点(BPQD),100rpm搅拌60min,搅拌混匀后再次对混合液进行离心,离心转速为5000rpm,离心时间为3min,收集沉淀即为用于低剂量放射治疗的肿瘤靶向性载体(BPQD- Esc,BE)。
效果实施例:
采用本发明实施例1所制备的黑磷量子点-大肠杆菌肿瘤靶向性载体(BE)进行性能测试,进而验证本发明的这种载体及药物的效果。
(1)RT及激光治疗
在缺氧条件下进行放射治疗(RT)和激光辐照试验,分别设置以下六个对照组:第一组,PBS+L,仅有808nm激光辐照;第二组,RT(2Gy),2Gy的X射线照射量;第三组,BE,采用实施例1制备的用于低剂量放射治疗的肿瘤靶向性载体进行治疗;第四组,BE+L,采用实施例1制备的用于低剂量放射治疗的肿瘤靶向性载体联合808nm激光辐照进行治疗;第五组,BE+RT,采用实施例1制备的用于低剂量放射治疗的肿瘤靶向性载体联合2Gy X射线照射进行治疗;第六组, BE+L+RT,采用实施例1制备的用于低剂量放射治疗的肿瘤靶向性载体联合808nm 激光照射、2Gy X射线照射进行治疗。具体测试过程中,将第一、四和六组的细胞暴露于808nm激光下辐射,将第二、五和六组中的细胞暴露于2Gy X射线下照射,辐照时间均为10分钟。
结果如图2所示,相对于BE+RT(第五组)和BE+L(第四组)处理组中的细胞,进行BE+L+RT(第六组)处理的细胞表现出具有明显更高的DSB数量。一方面,BPQD的光热作用会破坏细胞DNA结构进而引发细胞凋亡,另一方面,BE中的BPQDs也具有放射疗法致敏作用,从而形成更多的γ-H2AX病灶。相对于单一 RT治疗组,BE+L+RT治疗组中的γ-H2AX多了4.56倍,这表明BE在缺氧条件下可以作为高效放射增敏剂。
(2)细胞存活试验
图3为细胞常氧(氧气含量为21%)条件下的细胞存活试验结果,图4为细胞缺氧(低氧,氧气含量为2%)条件下的细胞存活试验结果。细胞存活试验结果表明,在常氧条件下,CT26细胞对放疗非常敏感,而BE放疗的敏化作用似乎不太明显(敏化增强率(SER)=0.999)。在缺氧条件下,CT26细胞对放射疗法非常不敏感,即使在6Gy的高强度X射线辐射下,其存活率也约为69%。而添加 BE后,放射治疗的增敏效果非常明显(SER=1.17),在6Gy辐射下CT26细胞的存活率仅为~31%。该结果表明BE具有良好放射疗法敏化能力。
图5为常氧环境下光热和低剂量放射条件下的细胞存活率试验结果,图6为低氧(缺氧)环境下光热和低剂量放射条件下的细胞存活率试验结果。在光热和低剂量放疗(2Gy)的双重处理下,低氧和常氧条件下肿瘤细胞的生长均受到显着抑制,并且克隆数明显减少。体外实验的结果充分证明,本发明制备的BE具有有效的光热、放射疗法互补的能力,能够实现低剂量的放射疗法。
由于大肠杆菌的低氧趋向性,使他们能够选择性地在肿瘤中积累和复制,本发明的BE中的大肠杆菌的没有被破坏,因而本发明制备的BE具有良好的肿瘤靶向能力。
本发明还评估了BE在体内的抗肿瘤活性。将携带CT26肿瘤的小鼠随机分为六个不同的治疗组:(1)PBS+L组、(2)RT组、(3)BE+L组、(4)BE+RT组、(5) BPQD+L+RT组、(6)BE+L+RT组。仅RT和L治疗不足以明显抑制肿瘤生长;在 BE+L组和BE+RT组中,肿瘤的生长受到非常明显的抑制,这与该制剂的放射增敏剂和PTT活性相一致。并且BPQDs+L+RT组治疗显示出与BE+L和BE+RT组观察到的抗肿瘤功效相当。在BE+L+RT治疗组中,观察到了小鼠的最大肿瘤生长停滞,这与BE有效消融肿瘤组织的能力相一致。在整个研究过程中,未观察到治疗小鼠的明显体重变化,表明该治疗方法不会引起明显的全身毒性。因此,BE具有高度的生物相容性,并促进PTT和低剂量RT的协同治疗效果。
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
- 用于低剂量放射治疗的肿瘤靶向性载体及其制备方法和肿瘤靶向药物
- 用于低剂量放射治疗的肿瘤靶向性载体、药物及制备方法
