一种核酸级联放大诱导三维纳米结构形成检测氯霉素的方法
文献发布时间:2023-06-19 12:24:27
技术领域
本发明属于生物工程技术领域,具体地,涉及一种核酸级联放大诱导三维纳米结构形成检测氯霉素的方法。
背景技术
在当今社会,抗生素作为药物,具有一定抑菌和杀菌作用。在人类和动物的治疗中起着重要的作用。但是,如果人体中的抗生素含量过高,则会造成严重的不良影响。氯霉素(CAP)是一种广谱抗生素,具有成本低,抗菌效果好等优点。它已被广泛用于治疗人类和畜牧业的疾病,并且可以治疗由伤寒杆菌,大肠杆菌和流感杆菌引起的感染。肉类,牛奶等其他食品中含有一定量的CAP。但是,如果长时间食用这些食物,则人体中氯霉素的含量最终将超过标准,从而损害了人体的健康。典型的不良反应主要是抑制骨髓的造血功能,导致再生障碍性贫血,并具有一定的致癌性。一些国家完全禁止在水产品,家禽和其他粮食中使用含有CAP的药物。因此,设计一种简单,廉价且准确的动物源食品中氯霉素检测策略非常重要。
目前,已经出现了一些检测CAP的方法,包括色谱法、荧光、比色法、化学发光和电化学。其中,由于比色法具有简单,成本低,速度快的优点,因此使用比色法检测CAP更为普遍。然而,普通比色法具有特别明显的缺点,即其灵敏度不够高。因此,设计基于比色法的目标检测策略所面临的挑战是试图避免其灵敏度差的缺点。近年来,为了提高检测CAP策略的灵敏度,许多信号放大方法,例如酶促信号放大,包括滚环扩增(RCA),聚合酶链反应(PCR),以及环介导的等温扩增(LAMP)和无酶信号扩增,包括链置换扩增(SDA),催化发夹装配(CHA)和杂交链反应(HCR)。尽管这些酶信号放大方法具有更高的效率和更好的灵敏度,但是由于存在生物酶,其对系统环境的要求非常严格,并且其成本更高。因此,相对而言,无酶信号放大方法更为普遍,因为它们的放大倍数仍然可以达到100倍,并且其成本也相对较低。徐等人已经报道了使用HCR辅助扩增法检测卡那霉素的比色聚集测定,其LOD为0.68μM。已证明比色法可用于实际样品中卡那霉素的检测。由于食物中残留的抗生素最终将通过食物链传递给人类,因此检测食物中微量的抗生素也至关重要。如果您设计的策略仅依靠CHA或HCR扩增方法,则很难检测痕量的分析物。
发明内容
发明目的:本发明的目的是提供了一种核酸级联放大诱导三维纳米结构形成检测氯霉素的方法,该方法由于G-四链体和三维DNA立方体网状结构的结合,具有增强的类过氧化物酶催化活性,所以能够实现对牛奶中的抗生素进行超灵敏检测。
技术方案:本发明所述的一种核酸级联放大诱导三维纳米结构形成检测氯霉素的方法,具体操作步骤如下:
(1.1)、通过水热合成法和高温煅烧法,制备Ni-Fe LDO,再通过一锅法,在Ni-FeLDO的表面修饰单链DNA;
(1.2)、根据目标物抗生素样本,设计适合于目标物抗生素样本的适配体和DNA寡核苷酸链,并用缓冲溶液配制不同浓度的DNA寡核苷酸链;
(1.3)、对DNA寡核苷酸链进行预退火处理;
(1.4)、将经过预退火处理的DNA寡核苷酸链加入到待检测的目标物抗生素样本中进行混合,孵育,从而得到HCR产物和G-四链体;
(1.5)、将得到的HCR产物和修饰有单链DNA的Ni-Fe LDO进行混合,孵育,从而得到三维DNA/Ni-Fe LDO立方体网状结构;
(1.6)、再将得到的G-四链体与得到的三维DNA/Ni-Fe LDO立方体网状结构进行混合,孵育;
(1.7)、孵育结束后,将带有负电荷的G-四链体结合在带有正电的三维DNA/Ni-FeLDO立方体网状结构的表面;最后,进行磁性分离,去掉上清液,进行TMB显色反应实验,最终实现对目标物抗生素样本的超灵敏定量检测。
进一步的,在步骤(1.1)中,所述的水热合成法的反应条件:在烘箱60℃下反应48小时;
所述高温煅烧法的反应条件:在500℃下反应8小时。
进一步的,在步骤(1.2)中,所述的目标物抗生素样本是氯霉素,所述目标物抗生素样本的适配体是通过指数富集的配体技术挑选出来的,是一种DNA链;
另外,所述的缓冲溶液是由0.01M PBS和1mM EDTA,100mM KCl配制而成的。
进一步的,在步骤(1.3)中,所述DNA寡核苷酸链进行预退火处理的操作条件是:在95℃下反应5min,然后冷却至25℃的室温,待用。
进一步的,在步骤(1.4)中,所述经过预退火处理的DNA寡核苷酸链加入到待检测的目标物抗生素样本中进行混合孵育的条件是:孵育温度为37℃,反应时间是2小时。
进一步的,在步骤(1.5)中,将HCR产物与修饰有单链DNA的Ni-Fe LDO进行混合孵育的条件是:在25℃下反应1小时。
进一步的,在步骤(1.6)中,将G-四链体与三维DNA/Ni-Fe LDO立方体网状结构进行孵育的条件是:在25℃下反应30分钟。
进一步的,在步骤(1.7)中,最终的TMB显色反应,其缓冲溶液是0.1MNaAc/HAc溶液,pH范围从3.5到5.5。
进一步的,本方法的操作过程均在避光的条件下进行,且在水浴锅中进行。
本发明依靠基于Ni-Fe LDO纳米片(NSs)和无酶扩增方法(包括催化发夹装配(CHA)和杂交链反应(HCR),本发明开发了一种用于检测氯霉素(CAP)的超灵敏比色测定法;由于G-四链体被Ni-Fe LDO NSs表面吸附,其类过氧化物酶样催化活性得到了明显的增强;而且,通过磁分离的效果,信号背景值将被有效地降低;因此,本发明可实现对超痕量的目标CAP定量检测;在最佳条件下,得到显示出0.1fM至0.1nM的宽线性范围,具有良好的线性(r
有益效果:本发明与现有技术相比,本发明将G-四链体可以通过配位作用和Ni-FeLDO结合在一起,并且复合材料具有显著增强的类过氧化物酶催化活性;最重要的是,本发明在检测实际样品中具有潜在的应用价值,而G-四链体和Ni-Fe LDO NSs的组合可以有效提高其催化活性的想法在生物学分析领域具有一定的潜在价值。
附图说明
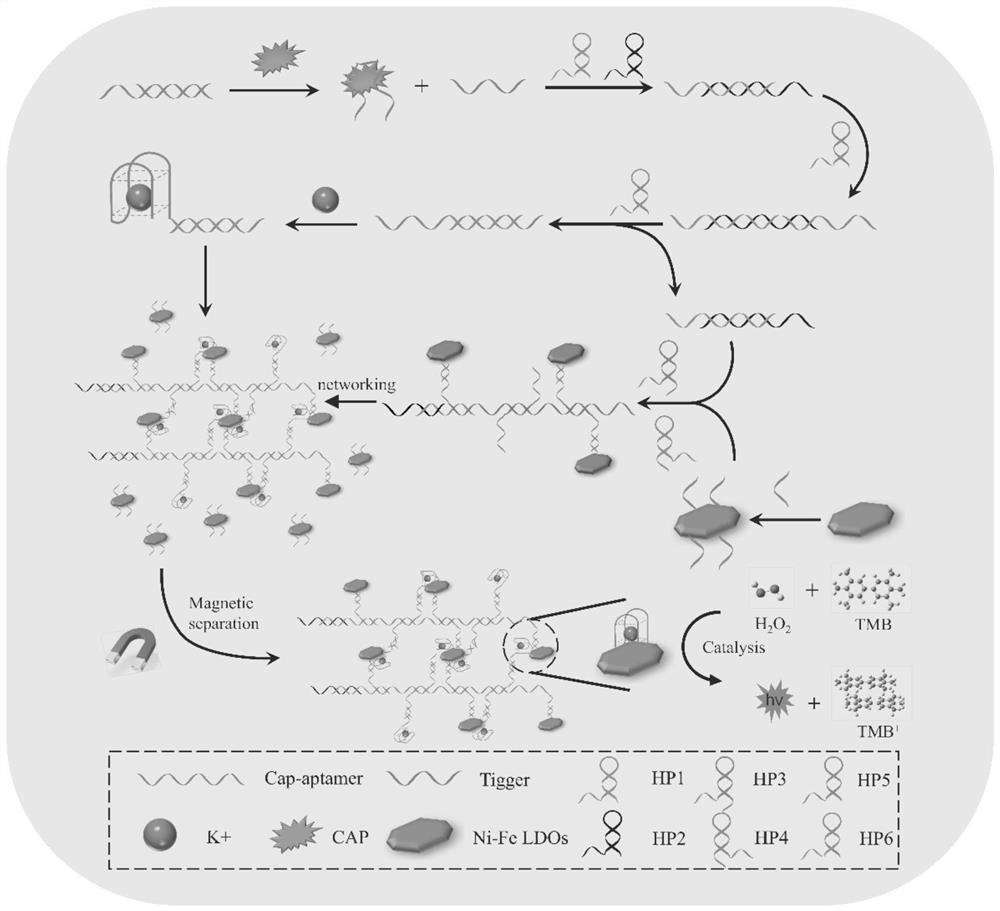
图1是本发明的操作流程图;
图2中(a和b)是本发明中不同尺寸的Ni-Fe LDO NSs的TEM图;(c和d)是本发明中三维Ni-Fe LDO/DNA NW在不同尺度下的TEM图;
图3是本发明中相关实验条件的优化示意图;其中,目标氯霉素的浓度为0.01nM,(a)是K
图4(a)是本发明中在最佳实验条件下检测目标氯霉素的校准图;(b)是本发明中对应于目标氯霉素浓度变化的UV-vis光谱图;在652nm处记录溶液的吸光度值。
具体实施方式
以下结合附图和具体实施例,对本发明做出进一步说明。
本发明所述的一种核酸级联放大诱导三维纳米结构形成检测氯霉素的方法,具体操作步骤如下:
(1.1)、通过水热合成法和高温煅烧法,从而制备Ni-Fe LDO,再通过一锅法,在Ni-Fe LDO的表面修饰单链DNA;
(1.2)、根据目标物抗生素样本,设计适合于目标物抗生素样本的适配体和DNA寡核苷酸链,并用缓冲溶液配制不同浓度的DNA寡核苷酸链;
(1.3)、对DNA寡核苷酸链进行预退火处理;
(1.4)、将经过预退火处理的DNA探针加入到待检测的目标抗生素样本中进行混合,孵育,从而得到HCR产物和G-四链体;
(1.5)、将得到的HCR产物和修饰有单链DNA的Ni-Fe LDO进行混合,孵育,从而得到三维DNA/Ni-Fe LDO立方体网状结构;
(1.6)、将得到的G-四链体与三维DNA/Ni-Fe LDO立方体网状结构进行混合,孵育;
(1.7)、孵育结束后,具有三维的DNA/Ni-Fe LDO立方体网状结构已经形成,同时溶液中产生大量的G-四链体,将带有负电荷的G-四链体结合在带有正电的DNA/Ni-Fe LDO立方体网状结构的表面;最后,对其进行磁性分离,去掉上清液,在一定环境条件下,进行TMB显色反应实验,最终实现对目标物抗生素样本CAP的超灵敏定量检测。
进一步的,在步骤(1.1)中,所述的水热合成法的反应条件:烘箱60℃下反应48小时;
所述高温煅烧法的条件:在500℃下反应8小时;
所述合成的Ni-Fe LDH是呈片状的,具有一定的类过氧化物酶催化活性,然后通过高温煅烧,可以将Ni-Fe LDH煅烧成Ni-Fe LDO;所述的Ni-Fe LDO既具有强磁性又具有增强的类过氧化物酶催化活性;
另外,由于Ni-Fe LDO本身容易聚集,所以表面修饰单链DNA的过程中,需要在涡旋振荡器上面低速震荡,以保证二者能够充分的接触。
进一步的,在步骤(1.2)中,所述的目标物抗生素样本是氯霉素,所述目标物抗生素样本的适配体是通过指数富集的配体技术挑选出来的,是一种DNA链;
另外,所述的缓冲溶液是由0.01M PBS和1mM EDTA,100mM KCl配制而成的。
进一步的,在步骤(1.3)中,所述DNA寡核苷酸链进行预退火处理的操作条件是:在95℃下反应5min,然后冷却至25℃的室温,待用。
进一步的,在步骤(1.4)中,所述目标物抗生素样本是CAP,为了降低背景干扰值,其孵育温度为37℃;其中,CAP-aptamer,probe 1和probe 2之间的反应时间是2小时。
进一步的,在步骤(1.5)中,将HCR产物与修饰有单链DNA的Ni-Fe LDO进行混合孵育的条件是:在25℃下反应1小时。
进一步的,在步骤(1.6)中,将G-四链体与三维DNA/Ni-Fe LDO立方体网状结构进行孵育的条件是:在25℃下反应30分钟。
进一步的,在步骤(1.7)中,最终的TMB显色反应,其缓冲溶液是0.1MNaAc/HAc溶液,pH范围从3.5到5.5。
进一步的,在TMB显色反应中,震荡不能太剧烈,为了防止吸附在DNA/Ni-Fe LDO网状结构表面的G-四链体脱落。
进一步的,本方法的操作过程均在避光的条件下进行,且在水浴锅中进行。
具体的,一种核酸级联放大诱导三维纳米结构形成检测氯霉素的方法,包括以下步骤:
这种用于检测CAP的比色策略涉及一种编码探针,它是CAP适配体/触发的杂交探针;此外,这些HP1、HP2、HP3、HP4、HP5和HP6的DNA发夹探针是触发CHA和HCR信号放大的原料;信号放大的整个分析过程如下:在存在目标CAP的情况下,由于目标CAP及其适配体(CAP-适体),释放的触发器与HP1杂交,暴露了HP1的开放序列后,由于HP1和HP2之间的结合能力强于HP1和触发器,原来与HP1杂交的触发器又被释放以参与下一个周期信号放大,并且CHA反应的该信号放大完成;长单链分别暴露在CHA产物的两端,这将作为新的启动子序列分别触发HCR和CHA反应。在存在HP3的情况下,它将与HP1/HP2复合链杂交,并形成三元HP1/HP2/HP3复合物;当在此混合溶液中添加HP4时,将形成HP3/HP4双链,并释放HP1/HP2双链;由于可以形成G-四链体的HP3/HP4杂合体的序列被暴露,因此在K
采用超微量紫外分光光度计对最终的信号进行检测。
所述的杂交缓冲液是由0.01M PBS,1mM EDTA-2Na,100mM KCl,pH 7.5;Ni-Fe LDO表面修饰的ssDNA是由饱和PBS缓冲液制备的,整个修饰过程都是在饱和PBS体系下进行的。
通过上述方法,该发明实验了对牛奶中残留氯霉素的超灵敏检测;示例中,对氯霉素的检测限为11.6aM,其线性范围为0.1fM到0.1nM;所建立的方法适用于对多种实际样品中残留氯霉素的检测。
采用上述方法,对不同加标氯霉素浓度的牛奶样品进行了检测,具体实例如下:
在优化的实验条件下,研究了该策略在新鲜牛奶样品中检测目标CAP的实际应用;从一家超市购买了这种新鲜的牛奶,以前的报告中报道了牛奶样品的制备方法;进行如下:将400μL新鲜牛奶和1000μL冰乙腈放入2ml离心管中;然后,将其置于涡旋振荡器上并摇动1分钟,以确保它们均匀混合;最后,将离心管转移至4℃的冰箱中反应1h;反应1小时后,可以清楚地发现分层现象,并且在离心管底部出现大量白色沉淀;将该溶液以12000rpm离心3分钟,并取出上清液用于进一步的实验;然后,将990μL的上清液添加到2mL离心管中,并将10μL的10fM,100fM,1pM和10pM目标CAP分别添加到该管中;最后,将这些不同浓度的牛奶样品在使用前保存在4℃的冰箱中;如表1所示,它表明未能检测出牛奶样品中的残留CAP;该结果证明该牛奶符合标准。为了证明本发明可以有效地检测实际样品中的残留CAP,对添加了不同浓度目标CAP的牛奶样品进行了回收率实验;分别以0.1fM,1fM,10fM和100fM的目标CAP加标牛奶样品。如表1所示,通过公式计算,可得到101.4%至102.3%的良好回收率,以上结果表明,本方法对牛奶实际样品中目标CAP的分析具有一定的实用性。
表1牛奶中残留氯霉素的检测
- 一种核酸级联放大诱导三维纳米结构形成检测氯霉素的方法
- 级联侵入信号放大反应结合纳米金-寡核苷酸探针可视化核酸检测方法
