基于石墨烯的介电泳传感器和方法
文献发布时间:2023-06-19 09:47:53
相关申请的交叉引用
本申请要求于2018年6月5日提交的美国申请序列号第62/680,777号的优先权。该在前申请的公开内容被视为本申请的公开内容的一部分,并且以其整体被包含在本申请中。
技术背景
根据世界卫生组织,每年有5.5亿人由于食源性肠道疾病而生病,并且230,000人死于这些疾病。来自沙门氏菌属和大肠杆菌(E.coli)的感染是这些肠道疾病中最常见的几种。沙门氏菌属是在动物中发现的细菌,如果摄入,则可能引起严重的健康问题。对于诸如幼儿、老年人和具有弱化的免疫系统的人之类的具有高并发症风险的人而言此类问题是特别严重的。类似地,大肠杆菌是一种大肠菌,取决于细菌的品种和人的易感性,大肠杆菌可引起人类的疾病或甚至死亡。在明尼苏达州和全国各地,沙门氏菌属和大肠杆菌的爆发仍然是对公众健康的持续威胁。
通常使用的病原体细菌DNA的测试方法包括培养和/或聚合酶链反应(PCR)分析,这是用于使用一系列重复的扩增序列来扩增靶标DNA分子的实验室技术。PCR具有优异的灵敏度,但是需要几十个循环来确定特定物种的存在或不存在,这既耗时又昂贵,并且通常需要初始富集培养步骤。正在开发检测食品或临床样品中病原体生物的日益快速和灵敏的方法。具体而言,因为沙门氏菌属作为食源性病原体的重要性,已经在寻求用于快速测量这种细菌的方法,最近的进展已经进一步提高了使用其他方法的检测速度和灵敏度,但是这些方法仍然达不到手持式系统所需的速度和灵敏度。
手持式系统的DNA检测的一种特别有前途的方法涉及使用基于石墨烯的传感器,并且文献中的许多报告已经表明,石墨烯可以提供一种出色的替代方法来选择性地感测DNA。石墨烯是sp
由于其单层性质,石墨烯可以对吸附的生物分子提供优异的灵敏度,并且还可以官能化以选择性地提供给化学活性靶标。
传统的石墨烯传感器使用简单的扩散过程来将颗粒吸引到表面。这可能很慢。另一方面,介电泳(DEP)可用于将颗粒吸引到高电场梯度的区域,但是不提供方便的选择性感测手段。在本发明中,描述了一种传感器,该传感器通过使用在表面上用探针材料官能化的石墨烯解决了如何在基于DEP的传感器内实现选择性的问题。它还提供了一种方法来分离相对较大的DEP吸引偏置电压和通常较小的感测偏置电压。
发明内容
在某些方面,本发明的特征在于一种利用表面官能化以实现特异性和选择性感测的石墨烯边缘介电泳(DEP)传感器。在一些方面,本发明的特征在于一种检测所述传感器的选择性响应的方法。
在一些实施例中,基于石墨烯的DEP传感器使用在石墨烯或相邻表面(或基材)上的表面官能化来实现选择性。基于石墨烯的DEP传感器可以使用随时间变化的激励来进行DEP吸引,这使得能够独立于DEP AC激励读出传感器响应。
除了其他优点,实施例可以使用基于DEP的石墨烯传感器来实现对一系列靶标分子或生物颗粒的选择性。实施例还可以使得能够在存在旨在将颗粒吸引到石墨烯边缘的相对较大的AC激励的情况下读出传感器响应。
以下附图和描述阐述了本发明的一个或多个实施例的细节。本公开的其他特征、对象以及优点将根据说明书、附图以及权利要求书而显而易见。
附图说明
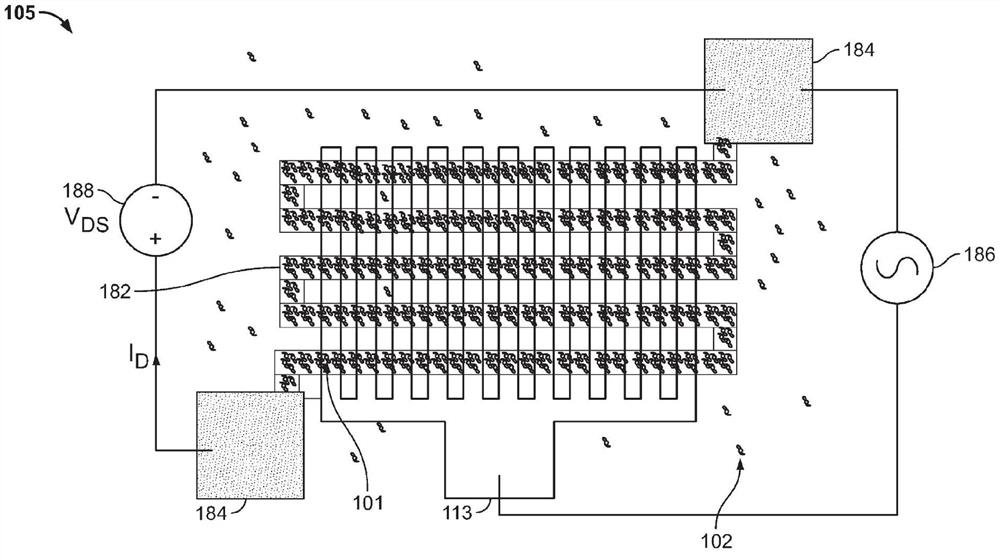
图1a-1c是示出基于电阻的DEP传感器的俯视图的示意图。图1a示出了在含有靶标的溶液中的具有附着在石墨烯表面上的探针的传感器。图1b示出了经由施加的AC偏置使用DEP将靶标吸引到石墨烯边缘的传感器。图1c示出了在移除DEP激励之后靶标结合到附近探针,从而实现传感器读数。
图2a-2c是示出基于电容的DEP传感器的俯视图的示意图。图2a示出了在含有靶标的溶液中的具有附着在石墨烯表面上的探针的传感器。图2b示出了经由施加的AC偏置使用DEP将靶标吸引到石墨烯边缘的传感器。图2c示出了在移除DEP激励之后靶标结合到附近探针以使得能够进行传感器读出。
图3示出了所施加的电压信号和对基于电阻的DEP传感器的预期响应的曲线图。
图4示出了所施加的电压信号和对基于电容的DEP传感器的预期响应的曲线图。
图5a和图5b示出了具有变化的AC偏置的基于电容的DEP传感器的预期响应的曲线图。
图6a-6e示出了石墨烯边缘DEP镊的制造过程。图6a示出了栅极氧化物凹陷和栅极金属图案化。图6b示出了石墨烯转移。图6c示出了石墨烯图案化成俘获区段。图6d示出了接触部金属化和剥离。图6e示出了使用探针物体进行表面官能化。
各个附图中相同的附图标记指示相同的要素。
具体实施方式
图1a示出了石墨烯边缘介电泳传感器105的实施例。特定传感器在电阻感测模式下操作,如我们先前已经在2017年6月16日提交的题为“Electrodes formed from 2Dmaterials for dielectrophoresis and systems and methods for utilizing thesame(用于介电泳的由2D材料形成的电极和使用该电极的系统和方法)”的临时申请第62/521,096号中和在2018年6月18日提交的美国2018/0361400中描述的,这两个专利的全部内容都通过引用结合于此。
DEP传感器105包括第一指状电极113、石墨烯电极182和接触部184。接触部184被电耦合到石墨烯电极182。DEP传感器105是三端子设备,其中第一指状电极113用作栅极电极,并且两个接触部184用作源极端子和漏极端子。石墨烯电极182被布置成蛇形形状以增加与第一指状电极113的交叉位点。增加交叉位点导致可以俘获颗粒的边缘的数量增加。例如,石墨烯电极180的蛇形条带的宽度可在100nm到5μm的范围,并且第一指状电极113的宽度可在0.1μm到5μm的范围。
石墨烯电极182与第一指状电极113电隔离。例如,可将类似于绝缘层130的绝缘层布置在第一指状电极113和石墨烯电极182之间。因此,DEP传感器105的示例层叠可以以所列出的顺序包括:第一指状电极113、绝缘层、以及石墨烯电极182。绝缘层可充当由石墨烯电极182和第一指状电极113形成的3端子FET设备的“栅极氧化物”。
接触部184可以由各种导电材料形成。导电材料的示例包括金属、硅化物、或合金,诸如金、钯、铂、钨、铬、钛、铱、钼、铝、或铜。在一些实施方式中,可以堆叠不同的导电材料层以形成接触部184。
可以通过以下操作来对DEP传感器105进行电测量:经由接触部184在石墨烯电极182的两端之间施加DC电压、或AC电压、或它们两者(被统称为“测量电压”),并且测量当在第一指状电极113(“栅极电极”)和石墨烯电极182之间施加AC电压(“俘获电压”)以引起DEP俘获时产生的漏极电流(ID)。可通过电压源186施加俘获电压,并且可通过源表188测量电压,该源表188被配置成施加电压并测量相应电流。最初,以一定频率在栅极电极113和石墨烯电极182之间施加俘获电压,该频率不对应于对特定类型颗粒的DEP俘获(例如,1MHz),并且没有颗粒被俘获。
测量电压通常小于俘获电压,以减轻由漏极电流ID的流动引起的跨石墨烯电极184的两个端子的电压降。例如,测量电压可以比俘获电压的幅度小10到100倍。
在一些实施方式中,除了AC电压之外,俘获电压还可具有DC偏置。DC偏置可用于例如偏置石墨烯电极182以控制其电导率。
如图1a所示,表面探针101附着到石墨烯电极182,其中探针被设计成与靶标102具有选择性反应。探针和靶标可以是分子、蛋白质、适体、抗体、脂质、囊泡、细胞衍生的颗粒、官能化的纳米颗粒或整个细胞的任何互补对,所述探针和靶标具有以下性质:可将探针附着到石墨烯的表面,并且靶标是可极化的颗粒,使得可以使用DEP将该靶标吸引到石墨烯表面并且该靶标可以选择性地附着到石墨烯上的表面探针。
这样的探针/靶标对的示例是具有互补匹配的单链DNA分子。另一个示例是使用生物素或生物素标记的蛋白质来官能化石墨烯,以用于检测链霉亲和素靶标。
可使用传感器检测靶标到探针的选择性附着。这可以使用石墨烯边缘DEP几何形状来使用先前在临时专利申请第62/521,096号和美国2018/0361400中描述的电容感测方式或电阻感测方式中的任一者来实现。可以使用“吸引并侦听(attract-and-listen)”模式来实现感测,其中首先使用DEP激励将靶标颗粒吸引到石墨烯表面,然后关闭激励并且使用较小的信号来评估石墨烯传感器响应。
在图1a-1c中示出了该模式的图,其示出了DNA检测,其中在DEP吸引脉冲之前,靶标DNA被吸引到其中边缘跨过栅极边缘的石墨烯区域。在释放DEP脉冲之后,如图1c所示,靶标DNA可在石墨烯表面附近附着到靶标DNA,由此产生电响应。可使用图1a-1c所示的电阻配置或图2a-2c所示的电容配置来实现该响应。
图2F示出了集成了石墨烯变容二极管的DEP设备204的俯视图。DEP设备204包括第一指状电极213、第二指状电极233和石墨烯电极280。石墨烯电极280被电耦合到第二指状电极233。石墨烯电极280已经被细分为数个较小的指状物以增加石墨烯电极280在第一指状电极213上的边缘和交叉的数量,在所述边缘和交叉处颗粒可被俘获。例如,细分的指状物的宽度可在100nm到5μm的范围。
石墨烯电极280与第一指状电极213电隔离。例如,可将类似于绝缘层130的绝缘层布置在第一指状电极213和石墨烯电极280之间。因此,DEP传感器204的示例层叠可以以所列出的顺序包括:第一指状电极213、绝缘层、石墨烯电极280、以及第二指状电极233。进一步,在第一指状电极213、绝缘层、以及石墨烯电极280之间可存在其他材料层。
第一指状电极213和第二指状电极233可由各种导电材料形成。导电材料的示例包括金属、硅化物、或合金,诸如金、钯、铂、钨、铬、钛、铱、钼、铝、或铜。在一些实施方式中,可以堆叠不同的导电材料层以形成第一电极213和第二电极233。这样的堆叠可有利于改善金属与绝缘层或石墨烯之间的粘附性,以及改善到石墨烯电极的电接触的质量。
最初,以一定频率在第一指状电极213(“栅极电极”)和耦合到石墨烯电极280的第二指状电极233之间施加AC偏置,该频率不对应于对特定类型颗粒的DEP俘获(例如,1MHz),并且作为结果没有颗粒被俘获。可以通过电压源216施加AC偏置。
在图3中示出了针对电阻感测模式的所施加的电压(下部曲线图)和预期的响应(上部曲线图)。此处,可以通过施加DC漏极到源极电压V
在图4中,示出了基于电容的传感器的感测场景。此处,使用小的AC栅极偏置来以简单双端子配置读出传感器。再次,为了加速设备响应,可以施加较大的AC偏置,然后再次减小,以读出传感器电容响应。类似于电阻传感器,还可以通过扫描栅极电压并监测狄拉克电压来实现读出,该狄拉克电压是电容最小处的栅极电压。
如图5所示,在一些实施例中,该场景被重复并且用于不同浓度的目标分析物,与允许分析物通过简单的扩散过程移动到表面相比,具有加速响应的益处。这也不同于一种替代模式的感测,其中DEP信号被连续地施加并且传感器响应与DEP信号同时被读出。可以使用类似的脉冲序列来执行负DEP,其中在传感器被暴露于含靶标流体之后,不需要的颗粒被从表面排斥。除了激励的频率将使得溶液中的某些颗粒将被排斥之外,感测模态将是相似的。
通常,本文公开的传感器和技术可在各种应用中实现。例如,它们可以被部署在照护点(point of care)传感器中。在一些实施例中,实施例被部署在基于DNA的条形码传感器中。
以如下方式来制造基于DEP的传感器并且验证它们的俘获能力。现有的石墨烯可变电容器(或“变容二极管”)的制造工艺(参见例如M.A.Ebrish、H.Shao和S.J.Koester,“Operation of multi-finger graphene quantum capacitance varactors usingplanarized local bottom gate electrodes(使用平面化的局部底部栅极电极操作多指石墨烯量子电容变容二极管)”,Appl.Phys.Lett.100,143102(2012))经修改以使其适于在石墨烯表面附近俘获大密度的颗粒。
在图6a-6e中示出了石墨烯边缘DEP传感器的示例制造工艺。设备制造开始于在硅晶片上通过热氧化来生长厚SiO
接下来,石墨烯被图案化成一系列窄条带,从而产生大量可俘获分子的边缘。使用光学光刻,条带小至2μm宽,具有4μm间距。使用电子束光刻,条带窄至100nm,具有200nm间距。在图6c示出了图案化的石墨烯的示意图。接下来,如图6d所示,图案化Cr/Au(10/100nm)金属化以形成到石墨烯的欧姆接触部。设备制造还可包括诸如SU-8之类的厚(若干微米)隔离层,该隔离层仅在有源设备区域上方被图案化和开口,以形成用于在测试期间进行流体限制的微小体积。最后,如图6e所示,施加官能化以将探针附着到石墨烯表面。
可探索不同的设备几何形状来确定最优结构以实现同时俘获和感测。在该设备优化中存在若干因素。这些因素包括:(1)为了实现足够有效的俘获所需的边缘数量;(2)电容或电阻感测;以及(3)激励的最优序列以吸引和感测DNA片段。
可以使用在1mM KCl缓冲液中过滤的DNA样本来测试传感器(参见,例如A.Barik、Y.Zhang、R.Grassi、B.P.Nadappuram、J.B.Edel、T.Low、S.J.Koester和S.-H.Oh,“Graphene-edge dielectrophoretic tweezers for trapping of biomolecules(用于俘获生物分子的石墨烯边缘介电泳镊)”,Nat.Commun.8,1867(2017)),然而,可以研究具有诸如细胞膜蛋白质残基之类的附加的颗粒的更复杂介质。对于食源性病原体检测,DNA样本可包括鼠伤寒沙门氏菌(Salmonella typhimurium)的片段。基于用于获取样本的PCR方法的类型(基于凝胶、赛博格林(cybergreen)、或实时),所述片段的长度在1kb到100bp范围变化。
该示例展示了两个主要元素:(1)在石墨烯上的探针DNA的表面官能化,以及(2)使用图6(d)中示出的设备结构来进行感测验证。
1-芘丁酸N-羟基琥珀酰亚胺酯(1-pyrenebutyric acid N-hydroxysuccinimideester,PBASE)被附着到石墨烯表面。PBASE的芘端通过π-π互连附着到石墨烯,同时琥珀酰亚胺部分从石墨烯向外延伸,实现与探针DNA的结合。为了附着探针,DNA的5’端经修改以包括胺基。该经修改的DNA被暴露于溶液中的PBASE覆盖的石墨烯,并且允许与琥珀酰亚胺交联以形成稳定的官能化层。通常,通过将整个基材浸泡在诸如乙腈之类的含探针DNA的溶液中来实现官能化过程,尽管可以容易地修改该工艺以使用基于喷嘴的打印或3D打印来在同一芯片上实现局部官能化的设备。
可首先使用原子力显微镜(AFM)和拉曼光谱在毯状石墨烯层上验证探针DNA与石墨烯表面的附着。可通过识别特定于官能化物质的峰,以及通过对证明石墨烯中电子或空穴浓度(hole concentration)的系统变化的G和2D峰中的偏移进行分析这两者来使用拉曼光谱验证石墨烯上的官能化分子。在已经使用这些技术验证官能化之后,DNA探针被附着到传感器设备结构上的石墨烯。在这些结构中,通过分析在狄拉克电压中的偏移来进一步验证探针DNA附着。据信狄拉克点偏移是表面官能化附着的可靠指示符,如已经使用芘硼酸(pyrene boronic acid)官能化证明的(参见,例如参考Y.Zhang、R.Ma、X.Zhen、Y.C.Kudva、P.Bühlmann和S.J.Koester,“Capacitive sensing of glucose in electrolytes usinggraphene quantum capacitance varactors(使用石墨烯量子电容变容二极管在电解质中电容感测葡萄糖)”,ACS Appl.Mater.Interfaces 9,38863–38869(2017))。此处,可使用浓度不断增加的含探针DNA的溶液并且将狄拉克点作为浓度的函数监测,来验证石墨烯官能化。该验证是重要的,因为可存在来自设备处理的残留物,并且经由拉曼的裸石墨烯与来自电气测试的设备石墨烯的等效掺杂结果的比较为后续感测提供了重要的验证。
以如下方式验证石墨烯设备的DEP增强感测。使用具有标准磷酸盐缓冲盐水(PBS)的大致0.1×浓度的中到高电导率KCl溶液。在初始测试中,在1nM降到1fM的范围的浓度下评估从大肠杆菌和鼠伤寒沙门氏菌PCR提取的100-1000bp DNA片段。探针DNA由单链DNA组成,并且靶标DNA由具有与探针匹配的互补碱基对的单链DNA组成。
使用流动池(flow cell)几何形状来测试样本。在测试过程中,将包含靶标DNA的溶液在预官能化的传感器的暴露区域上循环。流动池几何形状允许在变化的DNA浓度下测试单个设备。
由于SU-8层隔离了传感器的外在区域并且仅允许有源传感器区域与测试溶液相互作用,所以由缓冲溶液的导电性引起的寄生效应被最小化。然而,如果这样的问题持续存在,则应该可进一步稀释感测溶液。使用一种测试芯片,该测试芯片允许使用标准探针台的设备的测试,其中探针位于测试液体中远离有源设备区域的位置。另外,所有感测试验都利用差分感测,其中“空白”传感器(仅使用芘官能化)被用作控制设备。通过从没有受体的电极减去信号,可以排除背景信号、漂移问题和温度变化。此类差分感测在DEP中可能是重要的,在DEP中,由于由AC激励引起的流体运动可能会产生热效应。
基于图1a-1c和图2a-2c中示出的两种类型的传感器几何形状描述了两个主感测协议。第一个是图1a-1c中示出的基于电阻的几何形状。在该几何形状中,石墨烯被图案化为石墨烯数次跨过多指埋入式电极的形状。石墨烯可以以蛇形几何形状布置,以增加在特定区域内的栅极边缘交叉的数量。在该几何形状中,在石墨烯蛇形的端部之间施加小的DC或AC偏置(在100mV的量级上)。通过针对各种DNA浓度监测V
在建立该基线之后,评估石墨烯边缘DEP感测。例如,在每个浓度处,监测DC响应达5分钟以建立基线,并且随后AC激励被添加到栅极电极达规定时间(例如,5分钟),并且被移除,并且再次监测DC响应。AC电压大约以零为中心(没有DC分量),并且基于依赖于俘获的研究来确定峰-峰值和频率。在该几何形状中,重要的是在俘获期间将V
所评估的第二设备几何形状是图2a-2c中所示的变容二极管几何形状。该几何形状以并联配置操作并且使得在栅极边缘处的石墨烯中的小断裂不影响性能。设备还在V
最后,评价传感器对干扰颗粒的选择性,以便模拟在实际生物培养中感测的效果。因为DNA分子比蛋白质和脂质具有更高的电极化性,所以期望可发现最优的DEP频率范围和电压以选择性地浓缩DNA分子,同时排除不想要的干扰物和碎片。
已经描述了数个实施例。然而,应当理解,可以进行各种修改而不脱离本发明的精神和范围。相应地,其他实施例也在所附权利要求的范围内。
- 基于石墨烯的介电泳传感器和方法
- 一种基于光介电泳的石墨烯批量化装配方法
