一种评估患者对PD-1单抗产品敏感性的检测盒及其应用
文献发布时间:2023-06-19 11:49:09
技术领域
本发明涉及生物技术与医学领域,尤其涉及一种评估患者对PD-1单抗产品敏感性的检测盒及其应用。
背景技术
恶性黑素瘤是由皮肤和其他器官黑素细胞产生的肿瘤,早期黑素瘤患者预后较好,治疗以手术为主;晚期黑素瘤的治疗效果差,死亡率高。其自然病程中出现的与淋巴细胞浸润相关的肿瘤自发回缩或消退现象,以及黑素瘤对各种免疫治疗较好的临床反应均提示了黑素瘤是一种免疫原性肿瘤。且T细胞数量和活性受损是肿瘤免疫逃避的一个重要机制,免疫抑制性分子程序性细胞死亡受体1(PD-1)通路研究在免疫靶向治疗中具有里程碑式的意义,代表药物有nivolumab、pembrolizumab等,2012年美国临床肿瘤学会年会报告的数据显示抗PD-1的免疫治疗对以黑素瘤为主的多种肿瘤有效。
PD-1是第二代免疫检查点临床靶点,它是CD28超家族的一员,是含288个氨基酸的细胞膜蛋白,表达于活化T细胞的抑制性受体,高表达于黑素瘤抗原特异性T细胞,其配体PD-L1表达于抗原呈递细胞及肿瘤细胞。PD-1与配体结合后抑制具有抗肿瘤能力的细胞毒性T细胞的活性,并下调T细胞应答,从而诱导和维持外周免疫耐受,保护组织避免免疫攻击,同时也能减弱感染性免疫和肿瘤免疫。抗PD-1抗体和抗PD-L1抗体通过竞争性地与PD-1及PD-L1结合,从而解除T细胞的免疫抑制状态,进而有效的治疗黑素瘤。虽然PD-1单抗疗法在治疗黑素瘤上有一定的疗效,部分患者对PD-1单抗疗法存在严重的治疗抵抗,严重削弱了治疗效果并影响患者预后。
A20作为肿瘤坏死因子α(tumor necrosis factorα,TNFα)诱导内皮细胞反应中的一个诱导性表达蛋白,还有一个更重要的功能是作为NF-κB的负调控因子。大多数细胞中A20都是低表达的,当NF-κB被TNFα等炎性因子活化后,会与A20启动子区的NF-κB受体结合,A20会迅速被活化并且负调控NF-κB、MAPK等通路,从而改变IFNγ、TNFα、IL-12、IL10、IL-15和IL-21在内的多种细胞因子的表达水平。有关研究表明,部分肿瘤对烷化剂产生耐药的分子机制,发现NF-κB通路上的几个基因改变与耐药密切相关,而A20被认为是烷化剂引起DNA损伤从而导致NF-κB通路激活的重要调控因素。
因此目前急需一种快速评估患者对PD-1单抗产品敏感性的检测盒,提前发现对PD-1免疫疗法具有潜在高反应性的患者,以实现PD-1单抗疗法的精准治疗,也对提高PD-1单抗疗法的临床疗效具有重要意义。
发明内容
针对以上问题,本发明提供了一种评估患者对PD-1单抗产品敏感性的检测盒及其应用,提前发现并筛选对PD-1免疫疗法具有潜在高反应性的患者,以实现PD-1单抗疗法的精准治疗,也对提高PD-1单抗疗法的临床疗效具有重要意义。
为了实现上述发明目的,本发明提供以下技术方案:
一种评估患者对PD-1单抗产品敏感性的检测盒的应用,所述检测盒包括生物标志物,通过检测试剂盒内的生物标志物表达量来评估患者对PD-1单抗产品敏感性,所述生物标志物为A20蛋白。
优选地,所述患者为黑素瘤患者。
优选地,所述生物标志物的表达量通过非靶向蛋白质质谱检测。
本发明所述的敏感性是指包括患者对治疗黑素瘤的PD-1单抗产品的治疗敏感和治疗抵抗。
PD-1单抗产品包括但不限于Nivolumab、Atezolizumab、Pembrolizumab。
本发明还公开了一种评估患者对PD-1单抗产品敏感性的检测盒,所述检测盒包括生物标志物,通过检测生物标志物的表达量来评估患者对PD-1单抗产品敏感性,所述生物标志物为A20蛋白。
优选地,所述检测盒中含有生物标志物的样本全部来源于患者,在操作时应避免带入其他蛋白质影响检测结果。
优选地,所述样本来自黑素瘤患者原发灶瘤团内。
本发明公开的检测盒的制备方法如下:
(1)从患者原发灶内获得肿瘤组织,采用PBS缓冲液清洗干净,于-80℃的温度下保存存样;
(2)送样前,将肿瘤组织置于含有RBC裂解缓冲液的离心管中,于100℃加热5min,冷却至室温后进行超声处理,超声处理完后后于4℃、12000rpm下;离心15min,得到上清液;
(3)从上清液中浓缩收取蛋白质提取物得到生物标志物,置于检测盒盒体内,得到检测盒,将检测盒进行非靶向蛋白质质谱检测后,需在后续判断该黑素瘤患者是否对PD-1单抗治疗存在敏感性或治疗抵抗;
进一步,对检测盒内的A20蛋白的表达含量进行判断,判断标准如下:
通过非靶向蛋白质质谱检测获得的A20蛋白的表达含量,若检测含量小于1×10
有益效果:
1、本发明通过检测黑素瘤患者原发灶内A20蛋白表达量评估患者对PD-1单抗产品敏感性,提前发现并筛选对PD-1免疫疗法具有潜在高反应性的患者,以实现PD-1单抗疗法的精准治疗,也对提高PD-1单抗疗法的临床疗效具有重要意义。
2、本发明为判断黑素瘤患者是否对PD-1单抗治疗敏感或者抵抗提供了新的新方法,可以作为PD-1单抗治疗前判断治疗效果的参考依据,为制定个性化治疗提供意见基础,在医药学领域的应用前景广阔。
3、本发明的检测结果可靠,检测时间较短,检测方法简单易操作,具有广阔的应用前景。
附图说明
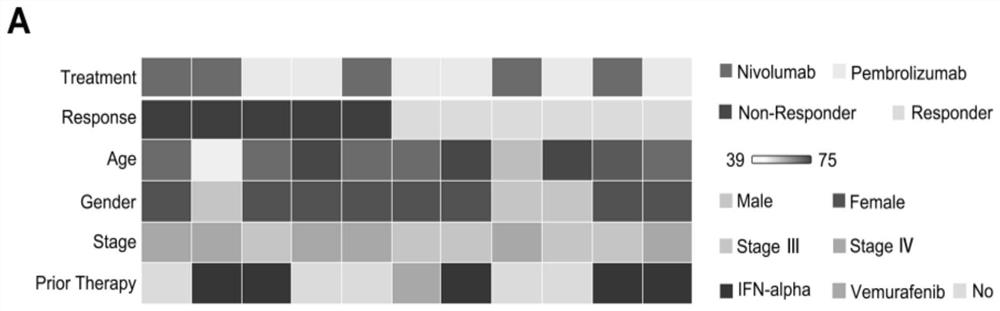
图1:PD-1单抗治疗后患者的敏感性图;
图2:PD-1单抗治疗后患者的A20蛋白表达量图。
具体实施方式
以下将结合具体实施例对本发明进行详细说明:
随机选取11位黑素瘤患者进行实验。
一、检测盒的制备:
(1)从11位患者的原发灶内分别获得肿瘤组织20mg,采用PBS缓冲液清洗干净,于-80℃的温度下保存存样;
(2)送样前,将肿瘤组织分别置于含有RBC裂解缓冲液的离心管中,于100℃加热5min,冷却至室温后进行超声处理,超声处理完后后于4℃、12000rpm下;离心15min,得到上清液;
(3)从上述上清液中浓缩收取蛋白质提取物得到生物标志物,将生物标志物置于检测盒盒体内,得到检测盒,将检测盒内的样本进行非靶向蛋白质质谱检测;
(4)记录上述检测盒通过非靶向蛋白质质谱检测获得的A20蛋白的表达含量。
得到的实验数据如表1所示:
表1
根据判断规则:若检测含量小于1×10
本发明的实施例公开的是一种评估患者对PD-1单抗产品敏感性的检测盒及其制备方法与评判标准,为了确定上述评判结果的准确性,进行验证,验证方法如下:
验证:将步骤(4)所得结果与RECIST结果进行对比可验证A20蛋白含量判断PD-1治疗效果的抵抗性和敏感性的结果可靠性。
判断依据RECIST(实体瘤的疗效评价标准),具体评价标准如下:
完全缓解(CR):所有靶病灶消失,全部病理淋巴结(包括靶结节和非靶结节)短直径必须减少至<10mm。
部分缓解(PR):靶病灶直径之和比基线水平减少≥30%。
疾病稳定(SD):靶病灶减小的程度没达到PR,增加的程度也没达到PD水平,介于两者之间,研究时可以直径之和的最小值作为参考。
疾病进展(PD):以整个实验研究过程中所有测量的靶病灶直径之和的最小值为参照,直径和相对增加≥20%(如果基线测量值最小就以基线值为参照);除此之外,必须满足靶病灶直径和的绝对值增加至少5mm(出现一个或多个新病灶也视为疾病进展)。
基线时,由研究者通过体检和影像学(CT)评估肿瘤负荷。
治疗敏感组患者定义为达到CR和PR患者之和;治疗抵抗组患者定义为PD患者。
对上述11位患者进行PD-1单抗治疗,上述患者中每人使用的药物Nivolumab、Atezolizumab、Pembrolizumab中的任意一种。
服用6周后得到的临床参数如图1所示,结果显示5位患者存在治疗抵抗,6位患者为治疗敏感患者,与检测盒判断的结果相同。
进一步验证,通过对上述11位患者的原发灶瘤团组织进行蛋白质谱分析,比对治疗抵抗患者和敏感患者瘤团中蛋白表达量,发现A20蛋白在治疗抵抗患者中表达水平显著升高,如图2所示,差异倍数经过Log2标准化后在5倍左右,表明A20表达水平升高与患者治疗抵抗高度相关,再次验证检测盒结果正确。
综上可知:
1、通过检测黑素瘤患者原发灶内A20蛋白表达量评估患者对PD-1单抗产品敏感性,可以筛选出对PD-1免疫疗法具有潜在高反应性的患者,以实现PD-1单抗疗法的精准治疗,也对提高PD-1单抗疗法的临床疗效具有重要意义。
2、本发明制备的检测盒检测PD-1单抗产品敏感性结果与RECIST结果一致,说明检测正确率高,检测结果可靠。
3、为患者制定个性化治疗提供意见基础,在医药学领域的应用前景广阔。
以上实施例仅用以说明本发明的技术方案而非限制,尽管参照较佳实施例对本发明进行了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的宗旨和范围,其均应涵盖在本发明的权利要求范围当中。本发明未详细描述的技术、形状、构造部分均为公知技术。
- 一种评估患者对PD-1单抗产品敏感性的检测盒及其应用
- 基因组合及其在制备评估受试者对戈利木单抗药物敏感性产品中的应用
