一种禽流感壳聚糖纳米颗粒疫苗的制备方法
文献发布时间:2023-06-19 11:54:11
技术领域
本发明涉及生物制品技术领域,具体涉及一种禽流感壳聚糖纳米颗粒疫苗的制备方法。
背景技术
禽流感是一种由甲型流感病毒引起的禽类高发性疾病,以精神沉郁,食欲减退,咳嗽、喷嚏等呼吸道症状为主要临床症状。目前,H9N2引起的禽流感在我国呈地方流行,虽然死亡率低,但感染的蛋鸡容易出现输卵管功能异常,产褪色蛋、畸形蛋、砂皮蛋、软壳蛋,鸡群产蛋率下降30%~80%,病程持续时间长的可达月余,造成严重的经济损失。近几年我国也接连发生,给养禽业造成了巨大的经济损失。疫苗接种仍然是当前预防和控制H9N2禽流感的主要手段,而纳米颗粒是指粒子直径大小在1~1000nm之间的微小颗粒。因其本身物理和生物学的特性,使其广泛应用到食品、化工、检测、纺织与机械、生物医学等方面。纳米颗粒经过精密加工,不仅能够被设计成病毒自然的形态(病毒样颗粒),还能够同时装载多种抗原,因此纳米颗粒在疫苗方面的应用前景广阔。
传统禽流感疫苗一般分为三种,灭活疫苗、弱毒活疫苗和基因工程疫苗。传统疫苗存在一定的局限性,如减毒活疫苗可能出现“毒力返祖”的情况,灭活疫苗产生免疫力的持续时间短,质粒DNA疫苗可能整合到免疫动物染色体,免疫应激反应剧烈等。
发明内容
本发明的目的在于克服现有技术中减毒活疫苗可能出现“毒力返祖”的情况,灭活疫苗产生免疫力的持续时间短,质粒DNA疫苗可能整合到免疫动物染色体,免疫应激反应剧烈等问题,提供一种禽流感壳聚糖纳米颗粒疫苗的制备方法。
本发明的目的通过以下技术方案予以实现:
一种禽流感壳聚糖纳米颗粒疫苗的制备方法,包括以下步骤:
S1.制备壳聚糖溶液和三聚磷酸钠溶液;
S2.制备灭活病毒液;
S3.将灭活病毒液逐滴滴加至壳聚糖溶液中得到病毒/壳聚糖混合溶液;再以0.1~0.5mL/min的流速,在不断以800~1500rpm/min的转速搅拌的条件下,将三聚磷酸钠溶液加入到所述病毒/壳聚糖混合溶液中;
S4.在1~8℃条件下,将步骤S3的最后得到的混合溶液,以8000~13000g/min的转速离心20~50min得到壳聚糖-禽流感纳米颗粒;将得到的壳聚糖-禽流感纳米颗粒分散在磷酸缓冲溶液中。
壳聚糖溶液的配制:将壳聚糖固体颗粒溶解在2%的乙酸水溶液中直至溶液透明,并不断用磁力搅拌器搅拌直至完全溶解。溶解后,将壳聚糖溶液用去离子水稀释,用NaOH将溶液的pH调节至5.4。再将溶液通过0.22μm过滤器过滤,得到用于实验的壳聚糖溶液。
三聚磷酸钠溶液的配制:将三聚磷酸钠固体颗粒溶解在去离子水中,并不断用磁力搅拌器搅拌直至完全溶解。再用0.22μm过滤器过滤,得到用于实验的三聚磷酸钠溶液。
根据离子交联的原理,带正电的壳聚糖和带负电的三聚磷酸钠之间的分子内和分子间作用力交联形成纳米颗粒。
优选地,所述步骤S1中,壳聚糖溶液的浓度为0.5%~2%(w/v);所述三聚磷酸钠的浓度为0.5%~1.5%(w/v)。
优选地,所述步骤S3中,灭活病毒的浓度为0.05%~0.15%(mg/v),灭活病毒与壳聚糖溶液的体积比为1:(1~3)。
优选地,所述步骤S3中,病毒/壳聚糖混合溶液与三聚磷酸钠溶液的体积比为(4~6):1。
优选地,所述步骤S4中,利用超声5~15min将得到的壳聚糖-禽流感纳米颗粒分散在磷酸缓冲溶液中。
优选地,所述灭活病毒为H9N2禽流感病毒。
所述禽流感壳聚糖纳米颗粒疫苗的制备方法得到的禽流感壳聚糖纳米颗粒疫苗。
与现有技术相比,本发明具有以下技术效果:
本发明公开的一种禽流感壳聚糖纳米颗粒疫苗的制备方法,具有安全性高、制备方便的特点,制备简单快速,高效省时,有利于推广应用,同时本发明制备的疫苗具有特异性强,毒副作用小,在预防H9N2禽流感方面有很大潜力,有望作为一种新型纳米疫苗应用于临床,具有良好的疫苗开发潜力。另外,本发明提供的方法能够应用于更广大的范围,可以选择不同的病毒种类,或将某病毒进行基因工程改造,从而利用其抗原区域进行疫苗的制备。
附图说明
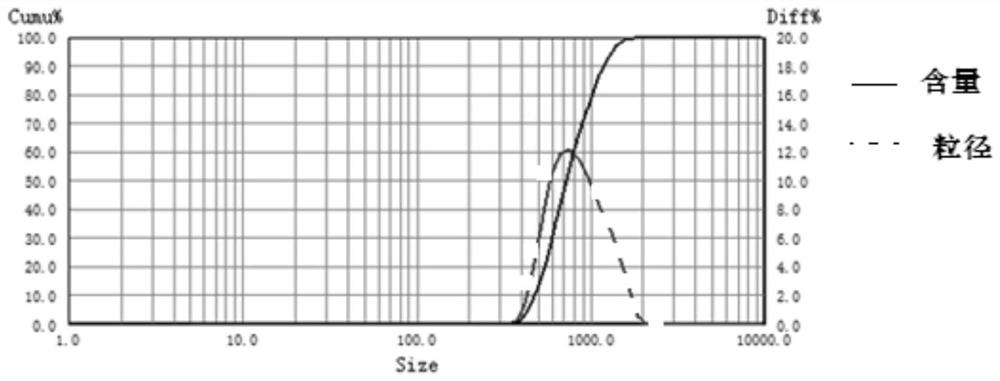
图1本发明实施例1壳聚糖纳米颗粒疫苗的尺寸及尺寸大小分布图;
图2本发明实施例1壳聚糖纳米颗粒疫苗的形态表征电镜图;
图3不同浓度比的壳聚糖纳米颗粒疫苗引发SPF白羽鸡体液免疫反应的抗体滴度的HI分析结果图;
图4不同浓度比的壳聚糖纳米颗粒疫苗引发SPF白羽鸡淋巴细胞增殖情况的分析结果图。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
除特殊说明,本实施例、对比例以及实验例中所用的设备均为常规实验设备,所用的材料、试剂无特殊说明均为市售得到,无特殊说明的实验方法也为常规实验方法。
实施例1
一种禽流感壳聚糖纳米颗粒疫苗的制备方法,包括以下步骤:
S1.制备浓度为1%(w/v)壳聚糖溶液和浓度为1%(w/v)三聚磷酸钠溶液;
S2.制备灭活病毒液;利用SPF鸡胚扩增病毒,收集其尿囊液,将收获的病毒尿囊液用甲醛灭活,终浓度为0.1%,在37℃,400rpm/min摇床中反应48h,并用0.22μm过滤器过滤;
S3.将2.5mL灭活病毒液逐滴加入到5.0mL壳聚糖溶液中得到病毒/壳聚糖混合溶液;再以1/6mL/min的流速,在不断以1000rpm/min的转速搅拌的条件下,将三聚磷酸钠溶液加入到所述病毒/壳聚糖混合溶液中,其中,壳聚糖溶液与三聚磷酸钠溶液的体积比为5:1;
S4.在4℃条件下,将步骤S3的最后得到的混合溶液,以10000g/min的转速离心30min得到壳聚糖-禽流感纳米颗粒;将得到的壳聚糖-禽流感纳米颗粒分散在磷酸缓冲溶液中并超声处理10mim。
所述禽流感壳聚糖纳米颗粒疫苗的制备方法得到的禽流感壳聚糖纳米颗粒疫苗。
实施例2
一种禽流感壳聚糖纳米颗粒疫苗的制备方法,包括以下步骤:
S1.制备浓度为0.5%(w/v)壳聚糖溶液和浓度为0.5%(w/v)三聚磷酸钠溶液;
S2.制备灭活病毒液;利用SPF鸡胚扩增病毒,收集其尿囊液,将收获的病毒尿囊液用甲醛灭活,终浓度为0.1%,在37℃,400rpm/min摇床中反应48h,并用0.22μm过滤器过滤;
S3.将2.5mL灭活病毒液逐滴加入到2.5mL壳聚糖溶液中得到病毒/壳聚糖混合溶液;再以0.2mL/min的流速,并不断以1000rpm/min的转速搅拌的条件下,将三聚磷酸钠溶液加入到所述病毒/壳聚糖混合溶液中,其中,壳聚糖溶液与三聚磷酸钠溶液的体积比为4:1;
S4.在1℃条件下,将步骤S3的最后得到的混合溶液,以13000g/min的转速离心20min得到壳聚糖-禽流感纳米颗粒;将得到的壳聚糖-禽流感纳米颗粒分散在磷酸缓冲溶液中并超声处理10mim。
所述禽流感壳聚糖纳米颗粒疫苗的制备方法得到的禽流感壳聚糖纳米颗粒疫苗。
实施例3
一种禽流感壳聚糖纳米颗粒疫苗的制备方法,包括以下步骤:
S1.制备浓度为2%(w/v)壳聚糖溶液和浓度为1.5%(w/v)三聚磷酸钠溶液;
S2.制备灭活病毒液;利用SPF鸡胚扩增病毒,收集其尿囊液,将收获的病毒尿囊液用甲醛灭活,终浓度为0.1%,在37℃,400rpm/min摇床中反应48h,并用0.22μm过滤器过滤;
S3.将2.5mL灭活病毒液逐滴加入到7.5mL壳聚糖溶液中得到病毒/壳聚糖混合溶液;再以0.5mL/min的流速,并不断以800rpm/min的转速搅拌的条件下,将三聚磷酸钠溶液加入到所述病毒/壳聚糖混合溶液中,其中,壳聚糖溶液与三聚磷酸钠溶液的体积比为6:1;
S4.在8℃条件下,将步骤S3的最后得到的混合溶液,以8000g/min的转速离心50min得到壳聚糖-禽流感纳米颗粒;将得到的壳聚糖-禽流感纳米颗粒分散在磷酸缓冲溶液中并超声处理10mim。
所述禽流感壳聚糖纳米颗粒疫苗的制备方法得到的禽流感壳聚糖纳米颗粒疫苗。
对比例1
一种禽流感壳聚糖纳米颗粒疫苗的制备方法,包括以下步骤:
S1.制备浓度为1%(w/v)壳聚糖溶液和浓度为1%(w/v)三聚磷酸钠溶液;
S2.制备灭活病毒液;利用SPF鸡胚扩增病毒,收集其尿囊液,将收获的病毒尿囊液用甲醛灭活,终浓度为0.1%,在37℃,400rpm/min摇床中反应48h,并用0.22μm过滤器过滤;
S3.将2.5mL灭活病毒液逐滴加入到5.0mL壳聚糖溶液中得到病毒/壳聚糖混合溶液;再以1/6mL/min的流速,并不断以1000rpm/min的转速搅拌的条件下,将三聚磷酸钠溶液加入到所述病毒/壳聚糖混合溶液中,其中,壳聚糖溶液与三聚磷酸钠溶液的体积比为8:1;
S4.在4℃条件下,将步骤S3的最后得到的混合溶液,以10000g/min的转速离心30min得到壳聚糖-禽流感纳米颗粒;将得到的壳聚糖-禽流感纳米颗粒分散在磷酸缓冲溶液中并超声处理10mim。
所述禽流感壳聚糖纳米颗粒疫苗的制备方法得到的禽流感壳聚糖纳米颗粒疫苗。
与实施例1相比,本对比例中病毒/壳聚糖混合溶液与三聚磷酸钠溶液的体积比不同。
对比例2
一种禽流感壳聚糖纳米颗粒疫苗的制备方法,包括以下步骤:
S1.制备浓度为1%(w/v)壳聚糖溶液和浓度为1%(w/v)三聚磷酸钠溶液;
S2.制备灭活病毒液;利用SPF鸡胚扩增病毒,收集其尿囊液,将收获的病毒尿囊液用甲醛灭活,终浓度为0.1%,在37℃,400rpm/min摇床中反应48h,并用0.22μm过滤器过滤;
S3.将2.5mL灭活病毒液逐滴加入到5.0mL壳聚糖溶液中得到病毒/壳聚糖混合溶液;再以1/6mL/min的流速,并不断以1000rpm/min的转速搅拌的条件下,将三聚磷酸钠溶液加入到所述病毒/壳聚糖混合溶液中,其中,壳聚糖溶液与三聚磷酸钠溶液的体积比为2:1;
S4.在4℃条件下,将步骤S3的最后得到的混合溶液,以10000g/min的转速离心30min得到壳聚糖-禽流感纳米颗粒;将得到的壳聚糖-禽流感纳米颗粒分散在磷酸缓冲溶液中并超声处理10mim。
所述禽流感壳聚糖纳米颗粒疫苗的制备方法得到的禽流感壳聚糖纳米颗粒疫苗。
与实施例1相比,本对比例中病毒/壳聚糖混合溶液与三聚磷酸钠溶液的体积比不同。
实验例1
颗粒的尺寸及分布:如图1所示,利用丹东百特仪器有限公司的BT-90纳米激光粒度分布仪测量疫苗的颗粒尺寸和颗粒尺寸分布。图中横坐标为纳米颗粒疫苗的尺寸大小,纵坐标为某一尺寸下所占的百分比。从图中得出颗粒尺寸范围:300-900nm,纳米尺寸越小有助于帮助疫苗进入细胞和增强免疫。如图2所示,透射电子显微镜FEI/Talos L120c测量禽流感纳米颗粒疫苗的表征。图中大圆圈为超薄碳网,小圆圈(黑色)为电镜下禽流感纳米颗粒疫苗的形态表征。
实验例2
将60只4周龄的SPF白羽鸡随机分为六组,每组10只。每组各用0.5mL实施例或对比例组的壳聚糖纳米颗粒疫苗对鸡进行皮下免疫(S/C),其中一组作为阴性对照组。第一次免疫之后隔3周对鸡进行第二次免疫,免疫方案如表1所示。
表1免疫方案
特异性抗体的测定(HI实验):根据OIE手册公布的血凝抑制(HI)试验进行。HI实验是指从带有测试禽流感疫苗的免疫组和对照组收集的血清样本中进行的,以检测样本中是否存在针对H9N2的抗体。第一次免疫后3周内,每周测量一次,第二次免疫后每2周测量一次。利用一次性真空采集管采集3-5mL血液,然后收集血清做HI实验。将测试的血清以2倍系列稀释液稀释,并与等体积的每种含4个HA单位的禽流感抗原(Ags)混合。之后混合物中加入等体积的0.5%火鸡红细胞(RBC),检查稀释液对血凝的抑制作用。血清抗体的滴度是最高稀释度的倒数,最高稀释度可完全抑制禽流感病毒的血凝作用。结果见图3。图中横坐标为第一次免疫后的天数,纵坐标为HI值(抗体滴度值)。与其他实验组比较:实施例1的值最高,引起的体液免疫更强,诱导机体产生了更强的抗体滴度。
淋巴细胞分离与增值的测定:(从每组中选择3只鸡)使用XTT细胞增殖测定试剂盒进行淋巴细胞增殖测定。在第一次免疫疫苗后第14天,用肝素(20IΜ/mL)通过翅静脉穿刺从每只鸡中采集血液用于淋巴细胞增殖测定。鸡外周血中淋巴细胞的分离是用淋巴细胞分离液进行操作的。淋巴细胞增殖情况结果见图4。图中横坐标为组别,每组包括四个数值,纵坐标为OD值。与其他实验组比较:实施例1的值更高,引起的细胞免疫更强,刺激淋巴细胞等产生了更强的免疫反应。
以上所述,仅为本发明较佳的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,根据本发明的技术方案及其发明构思加以等同替换或改变,都应涵盖在本发明的保护范围之内。
- 一种禽流感壳聚糖纳米颗粒疫苗的制备方法
- 一种高致病性H7N9禽流感病毒、疫苗、检测试剂以及病毒、疫苗的制备方法
