一种测定烟草样品的淀粉含量的方法
文献发布时间:2023-06-19 19:05:50
技术领域
本发明涉及烟草领域,具体涉及一种测定烟草样品的淀粉含量的方法。
背景技术
碳水化合物是绿色植物光合作用的主要产物,主要包括淀粉、纤维素、果胶等,淀粉是植物最主要的能量储存形式,广泛存在于烟草的茎叶中。淀粉反映的是烟草品质的重要指标,提高烤烟的质量水平必须平衡好烤烟烟叶中淀粉含量与烟碱、含氮化合物含量之间的关系,适宜的淀粉含量是提高卷烟香吃味质量的重要指标。但是,烟叶中含有较高的淀粉将会影响烟草的燃烧速度和燃烧完全性,产生的刺激性、焦糊气味和杂气等,对烟草的色、香、味产生不良影响,因此,准确测定烟草中的淀粉含量对评控卷烟烟气质量具有重要意义。
目前,烟草行业主要采用行业标准方法《YC/T 216-2013烟草及烟草制品淀粉的测定连续流动法》检测淀粉含量,该方法采用高氯酸萃取烟草中的淀粉。
发明内容
发明人发现行业标准方法《YC/T 216-2013烟草及烟草制品淀粉的测定连续流动法》检测淀粉含量存在检测重复性不高、回收率不高的问题,特别是待测溶液的存储时间较长时(比如隔夜),检测准确度不高。
发明人经过大量理论分析和实践验证,发现导致传统方法存在技术缺陷的原因是其使用高氯酸萃取烟草中的淀粉。发明人发现由于高氯酸具有强氧化性,会破坏烟草中纤维素和木质素等碳水化合物成分,从而使检测结果偏高。
鉴于上述发现,本申请提供一种新型测定烟草样品的淀粉含量的方法。
在第一方面,本申请提供一种测定烟草样品的淀粉含量的方法,包括
(1)将烟草样品置于乙醇-饱和氯化钠溶液中萃取,萃取后固液分离,收集固体残留物;
(2)将固体残留物置于浓度85-95wt%(例如88wt%、90wt%、92wt%)的二甲基亚砜水溶液中萃取,萃取后固液分离,收集萃取液;
(3)测定萃取液中淀粉的含量,并据此换算烟草样品的淀粉含量。
在一些实施方案中,步骤(1)中,所述乙醇-饱和氯化钠溶液中乙醇的含量为75-85wt%。
在一些实施方案中,步骤(2)中,所述二甲基亚砜水溶液中二甲基亚砜的含量为90wt%。
在一些实施方案中,测定萃取液中淀粉的含量可以采用本领域已知的任一种方法,例如连续流动法。例如可以参考《YC/T 216-2013烟草及烟草制品淀粉的测定连续流动法》中规定的连续流动法。
在一些实施方案中,步骤(3)中,向萃取液中加入盐酸水溶液,然后稀释是,然后进行用连续流动法进行检测。
在一些实施方案中,步骤(1)中,所述萃取分2-3次进行,其中每次萃取具有以下特征
(a1)萃取的温度为20-40℃;
(a2)萃取的总时间为50-70min;
(a3)萃取为超声辅助萃取,超声功率为300-400W;
(a4)每1g待萃取物使用40-60mL乙醇-饱和氯化钠溶液萃取。
在一些实施方案中,步骤(2)中,所述萃取分2-3次进行,其中每次萃取具有以下特征
(b1)萃取的温度为40-60℃;
(b2)萃取的总时间为5-7h;
(b3)萃取为超声辅助萃取,超声功率为330-370W(例如350W);
(b4)每1g待萃取物使用40-60mL二甲基亚砜水溶液萃取。
在一些实施方案中,步骤(1)中,所述萃取具有以下特征:
(c1)用25mL 80%乙醇-饱和氯化钠溶液萃取0.50g烟草样品,萃取温度为20~30℃,萃取在超声振荡器中进行,萃取时间30min;
(c2)将上一步产物固液分离,用2mL 80%乙醇-饱和氯化钠溶液洗涤固体残余物,再固液分离,收集固体残余物;
(c3)用25mL 80%乙醇-饱和氯化钠溶液萃取上一步所得固体残余物,萃取温度为20~30℃,萃取在超声振荡器中进行,萃取时间30min;
(c4)将上一步产物固液分离,用2mL 80%乙醇-饱和氯化钠溶液洗涤固体残余物,再固液分离,收集固体残余物。
在一些实施方案中,步骤(2)中,所述萃取具有以下特征:
(d1)用25mL 90wt%二甲基亚砜水溶液萃取上一步所得固体残余物,萃取温度为50℃,萃取在超声振荡器中进行,萃取时间2h;
(d2)将上一步产物固液分离,收集固体残余物和萃取液;
(d3)重复步骤(d1)-(d2),重复3次;
(d4)合并萃取液。
在一些实施方案中,采用的连续流动法测定萃取液中淀粉的含量。
在一些实施方案中,其中,步骤(3)包括:移取500μL提取液于5mL容量瓶中,再加入50μL 15%HCl水溶液,用水定容至5mL,摇匀,采用的连续流动法进行检测。
在一些实施方案中,采用紫外分光光度法测定萃取液中淀粉的含量。
在一些实施方案中,所述紫外分光光度法中,使用含有二甲基亚砜的水溶液作为参比溶液。
在一些实施方案中,所述紫外分光光度法中,使用含有二甲基亚砜和显色剂的水溶液作为参比溶液。
在上述实施方案中,参比溶液用于消除试剂等非测定物质对入射光吸收的影响。
在一些实施方案中,将烟草样品的二甲亚砜萃取液、水和显色剂按照5-15:35-45:1(例如10:40:1)的配比混合,作为紫外分光光度法的待测样品溶液。
在一些实施方案中,运用双波长分光光度法测定直链淀粉和支链淀粉的含量,其中,直链淀粉的测定双波长为490-500nm和590-600nm;支链淀粉的测定双波长为540-550nm和720-730nm。
在一些实施方案中,运用双波长分光光度法测定直链淀粉和支链淀粉的含量,其中,直链淀粉的测定双波长为493和595nm;支链淀粉的测定双波长为541和728nm。
在一些实施方案中,所述烟草样品选自烟叶、烟梗、烟草薄片中的一种或多种。
在一些实施方案中,所述测定烟草样品的淀粉含量的方法包括以下一种或多种:
(1)测定烟草样品的直链淀粉含量;
(2)测定烟草样品的支链淀粉含量;
(3)测定烟草样品的直链淀粉和支链淀粉总含量。
有益效果
本申请的一项或多项技术方案具有以下一项或多项有益效果:
(1)测定烟草样品的淀粉含量的方法重复性高;
(2)测定烟草样品的淀粉含量的方法加标回收率高;
(3)测定烟草样品的淀粉含量的方法中萃取液的稳定性高,久置后检测结果依然很准确。
附图说明
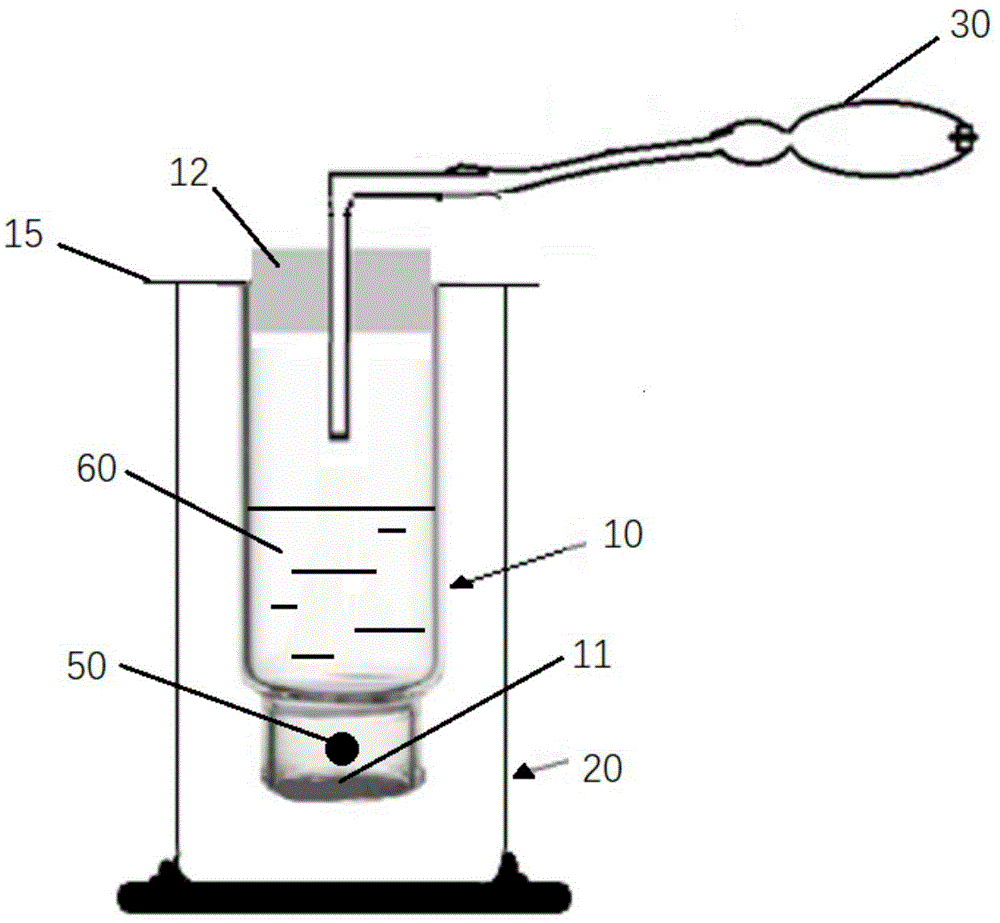
图1示出本申请一个实施例的具有双层嵌套结构的萃取装置。
具体实施方式
下面将结合实施例对本发明的实施方案进行详细描述,但是本领域技术人员将会理解,下列实施例仅用于说明本发明,而不应视为限定本发明的范围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用菌种、试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规产品。
图1示出一个具有双层嵌套结构的萃取装置。如图所示,该萃取装置包括砂芯内管10和外管20,砂芯内管10套接在外管20内。内管10和外管20之间通过位于内管10和外管20管口之间的支持柱15固定连接。内管10的管底为砂芯滤芯(孔径300μm),砂芯内管10的管口处设有玻璃塞12,玻璃塞12上设有通孔,通孔12可供双链加压球30伸入砂芯内管10内,向砂芯内管10内施加气压。在萃取的过程中,将样品50置于砂芯内管10内,然后向砂芯内管10内加入萃取液60,进行萃取,萃取后,通过双链加压球30向砂芯内管50施加气压,促进萃取液透过砂芯11被排出到外管20,固体残渣则保留在砂芯内管10内,从而实现了固液分离。
下面,结合具体实施例进一步详述本申请的测定烟草样品的淀粉含量的方法。
实施例1
1.取0.50g烟草样品置于砂芯内管10中,取25mL 80wt%乙醇-饱和氯化钠溶液加入砂芯内管10中。
2.将砂芯内管10套于外管20中,室温下将萃取装置放入超声振荡器中超声萃取30min。
3.取出萃取装置,用双链加压球30向砂芯内管10加压,滤出萃取液,用2mL 80%乙醇-饱和氯化钠溶液洗涤砂芯内管10内的固体残渣,再用双链加压球30加压弃去洗涤液。重复以上操作1次。
4.向砂芯内管10的固体残渣中加入25mL 90wt%二甲基亚砜水溶液,在50℃下超声提取2h。
5.取出砂芯内管10,用双链加压球加压滤出萃取液,转移萃取液到100mL烧杯。
6.重复三次90wt%二甲基亚砜水溶液萃取过程,收集合并萃取液,混合均匀。
7.取500μL萃取液,置于5mL容量瓶中,再加入50μL 15%盐酸/水溶液,用水定容至刻度,摇匀,参照《YC/T 216-2013烟草及烟草制品淀粉的测定连续流动法》中有关连续流动法的规定进行检测。
对比例1
参照《YC/T 216-2013烟草及烟草制品淀粉的测定连续流动法》对烟草样品进行检测。
数据分析
1、重复性实验(测试用样品为初烤烟叶)
按照实施例1的方法进行了日内重复性和日间重复性的检测,结果如下表1和2所示。
表1日内重复性实验(n=5)
表2日间重复性实验(n=7)
2、加标回收率实验(测试用样品为复烤烟叶)
采用加标法测定方法的回收率。准确取样品0.50g于砂芯提取套管中,加25mL80%乙醇-饱和氯化钠溶液超声萃洗两次后,加入低、中、高三个浓度的混合标样(直链淀粉:支链淀粉=1:4),向砂芯提取套管样品残渣中加入25mL 90wt%二甲基亚砜水溶液,50℃温下超声(功率350W)提取2h,重复三次90wt%二甲基亚砜水溶液萃取过程,收集合并萃取液,混合均匀后,准确移取500μL提取液于5mL容量瓶中,再加入50μL 15%盐酸水溶液,用水定容后进样检测,结果见表3。本申请方法的加标回收率在96.72~100.89%。
表3回收率实验
3、对比实验
应用实施例1和对比例1的方法分别检测了烤烟、白肋烟、香料烟、烟草薄片、梗丝等5个烟样淀粉含量,并将两种方法处理好的试液,静置过夜,再次检测淀粉含量(注:实施例1的萃取液上机检测前才稀释、加酸后定容),结果见表4、5。
表4过夜前的检测数据
表5过夜后的检测数据
变化值=过夜后淀粉含量-过夜前淀粉含量
对比例1的方法中,待测溶液在酸性条件下,淀粉会逐渐少量转化为可溶性糖类,使检测结果降低。
在实施例1的方法中,二甲基亚砜水溶液中的淀粉较为稳定,静置过夜后检测结果变化不大。
因此,由于减少了因高氯酸萃取,破坏纤维素、木质素等大分子碳水化合物而带入的葡萄糖类似物,本申请的方法检测更准确、稳定。
4、对比实验(测试用样品为复烤烟叶)
以复烤烟叶为测试对象,参照实施例1的测试操作,但是采用不同浓度的二甲基亚砜(DMSO)水溶液。
发明人发现,当二甲基亚砜溶解淀粉时,淀粉易发生快速溶胀,形成表面凝胶层,阻止二甲基亚砜穿透淀粉颗粒,影响溶解效果,加入水可以阻止淀粉颗粒的快速溶胀。不同浓度的二甲基亚砜/水体系对烟叶中淀粉的萃取效果不同。取相同的复烤烟叶样品分别用相同体积的不同浓度的二甲基亚砜水溶液萃取,检测结果如下表:
表6
如表6所示,当DMSO水溶液的浓度为90%时,测得的淀粉含量最高。这说明90%的DMSO水溶液能够最为充分地溶解萃取淀粉。
实施例2
采用二甲亚砜萃取-双波长分光光度法测定烟草样品的淀粉含量,双波长分光光度法的优点在于一次可以同时获得直链淀粉、支链淀粉和总淀粉含量3个数据。
以下采用用Evolution 220紫外-可见分光光度计测定烟草样品的淀粉含量。
2.1双波长的确定
经大量实验发现,以下双波长的优选值能够带来准确的检测结果:
(1)直链淀粉的测定双波长为493和595nm;
(2)支链淀粉的测定双波长为541和728nm。
2.2标准曲线的绘制
分别移取1、2、3、4、5mL的直链淀粉标准溶液和支链淀粉标准溶液对应混合于25mL容量瓶中,用90%二甲亚砜定容,制成五个混合淀粉标准工作液,再从五个混合淀粉标准工作液中分别移取1mL液体,加入100μL碘/碘化钾显色溶液,用0.1M盐酸分别定容至5mL。以1mL 90%二甲亚砜加100μL碘/碘化钾显色溶液,用0.1M盐酸定容至5mL的溶液作为参比溶液,分别测定直链淀粉双波长493和595nm的吸光度,支链淀粉双波长541和728nm的吸光度。
以直链淀粉含量为横坐标,直链淀粉双波长吸光度差值(λ
以支链淀粉含量为横坐标,支链淀粉双波长吸光度差值(λ
在以上步骤中,以1mL 90%二甲亚砜加100μL碘/碘化钾显色溶液,用0.1M盐酸定容至5mL的溶液作为参比溶液是关键的。由于萃取样品的二甲亚砜溶液在直链和支链淀粉的测定波长上有吸收,用水作参比无法去除二甲亚砜在测定波长上的吸收干扰,会导致差值变小(甚至变为负值),使其与浓度相关性变差(标线R
另外,实验中发现二甲亚砜萃取液中萃取的淀粉在没有加水稀释电离情况下,与显色剂中碘/碘化钾显色不明显,因此,二甲亚砜萃取液加水稀释及加入显色剂量配比是检测结果稳定可靠的关键。选取一个烟叶样品经前述方式萃取出烟叶淀粉后,根据不同的萃取液、水、显色剂比例,设计了两组实验,结果如下表:
表7不同萃取液与水配比对结果实验
表8不同显色剂的量对结果影响实验
结果显示,二甲亚砜萃取液与水的配比为10:40,且显色剂的量为100μL时,相当于二甲亚砜萃取液、水和显色剂的配比为10:40:1,取得的检测效果最佳,淀粉含量检出值高。
2.3双波长法测定烟草淀粉组分含量的精密度评价
对同一样品进行直链、支链淀粉含量的测定,重复6次,计算平均值和相对标准偏差(RSD%),结果表明,总体重复性良好,可用于直链淀粉含量测定。
表7方法的重复性试验
2.4回收率
在已测得直链淀粉和支链淀粉含量的烟草样品中,选择福建永定C1F-C02(直链淀粉含量为1.508%,支链淀粉含量为3.261%),添加准确称量的直链淀粉和支链淀粉标准品,按前述方法测定添加了标准品的烟草样品中淀粉的含量,计算回收率(表8)。
回收率计算公式如下:
回收率=[(测得的淀粉含量-样品中淀粉的含量)/淀粉标准品加入量]×100%
表8方法的加标回收率
由表8可知,直链淀粉的平均回收率为94.47%,支链淀粉的平均回收率为95.00%。表明用二甲亚砜萃取-双波长分光光度法测定烟草中的直链淀粉和支链淀粉含量的准确性。
2.5样品测定
采用本试验方法对福建永定C3F-B01、福建长汀C3F-B01、福建清流C3F-B01、福建尤溪C3F-B01、福建顺昌C3F-B01等5种不同复烤原烟淀粉含量进行测定。结果如表9所示,不同品种烟草中其直链和支链淀粉含量不同,支链淀粉/直链淀粉的比值变化范围在2.24-3.24之间。
表9不同复烤原烟淀粉含量测定结果
尽管本发明的具体实施方式已经得到详细的描述,但本领域技术人员将理解:根据已经公开的所有教导,可以对细节进行各种修改和变动,并且这些改变均在本发明的保护范围之内。本发明的全部范围由所附权利要求及其任何等同物给出。
