一种地衣芽孢杆菌及其培养方法和应用
文献发布时间:2024-04-18 19:52:40
技术领域
本发明涉及微生物技术领域,具体涉及一种地衣芽孢杆菌及其培养方法和应用。
背景技术
餐厨垃圾在人们生活中经常见到,在世界垃圾中,餐厨垃圾占生活垃圾总量的10-20%。
餐厨垃圾是食物垃圾中最主要的种类,餐厨垃圾的主要包括淀粉类、动物脂肪类、食物纤维类等物质,即城市生活垃圾中有机物的主要成分。在家庭生活垃圾中,餐厨垃圾占了30%左右,餐厨垃圾中主要以菜叶、果皮为主,碳水化合物含量占据50%,泔脚则以动物脂肪、淀粉和蛋白质为主,还包含较高的盐分,易于被功能性微生物利用,出现腐烂、发臭的现象。
我国主要餐厨垃圾处理的方式:1.粉碎直排处理-同时也是欧美国家处理少量餐厨垃圾的主要方法,对餐厨垃圾直接进行破碎处理,排入市政管道下水管网,但易产生水污染,水处理成本较高;2.填埋处理-操作简单,处理较快,可降解组分,稳定时间短,但不可提高资源化利用水平,易造成环境污染;3.能源化处理-主要是将餐厨垃圾进行燃烧或热分解等进行处理,但易造成空气或环境污染;4.肥料化和饲料化处理-基本都是利用微生物进行好氧和厌氧发酵,杀掉或保留原菌进行资源化处理,有利于环境物质大循环,减少碳排放,提高物质能源利用率。
但目前微生物发酵,都是选择外用的添加菌,导致效果不佳,若是可以直接分离出餐厨垃圾中的分解菌在进行扩大化培养,会更有利于餐厨垃圾的处理。
发明内容
为此,本发明提供一种地衣芽孢杆菌及其培养方法和应用,该菌具有耐高温,并可降解餐厨废弃物中油脂和纤维素的功能,可在45~82℃快速生长的特性。
为了提高餐厨垃圾资源化利用效率,筛选有利于降解纤维及油脂微生物可加速餐厨垃圾资源化的进程,不仅可在一定程度提高餐厨资源化利用率,还可减少处理餐厨垃圾能源利用量。
本发明由餐厨自然堆肥过程中,分离筛选同时具有高温降解油脂和纤维素功能的菌株。
为了实现上述目的,本发明提供如下技术方案:
根据本发明的第一方面提供一种地衣芽孢杆菌,所述地衣芽孢杆菌命名为BGB-84F,于2022年9月21日,保藏于中国微生物菌种保藏管理委员会普通微生物中心,保藏地址:北京市朝阳区北辰西路1号院3号,中国科学院微生物研究所,其保藏编号为CGMCCNo.25764。
进一步的,所述地衣芽孢杆菌的16SrDNA基因序列如SEQ ID No.1所示。
进一步的,所述地衣芽孢杆菌分离于餐厨垃圾中。
进一步的,所述地衣芽孢杆菌包括先将餐厨垃圾取样培养基培养,待平板长出菌落后,从平板上刮取少量菌落,用无菌水稀释后涂布平板培养;如无单克隆菌落出现,则需反复在平板涂布平板纯化,直到出现单克隆菌落为止,多次纯化,待菌落形态统一,无其他不同形态菌落出现,则得到纯化的地衣芽孢杆菌。
根据本发明的第二方面提供如上所述的地衣芽孢杆菌在降解餐厨废弃物油脂中的应用。
根据本发明的第三方面提供如上所述的地衣芽孢杆菌在降解餐厨废弃物纤维素中的应用。
根据本发明的第四方面提供如上所述的地衣芽孢杆菌在降解餐厨废弃物中的应用。
根据本发明的第五方面提供的微生物菌剂,所述菌剂包括如上所述的地衣芽孢杆菌BGB-84F,或含有如上所述的地衣芽孢杆菌BGB-84F的冻干粉。
进一步的,所述地衣芽孢杆菌BGB-84F的含量不少于:(1-9)×10
本发明具有如下优点:
运用本发明的分离纯化方法,经若干次反复纯化,在营养固体培养基中划线培养,得到单一菌株,得到的菌株经培养具有降解油脂和纤维素的能力,最后分离纯化得到分解餐厨垃圾功能的菌株系。
本发明的餐厨废弃物菌株同时具有降解油脂和纤维素的特性,餐厨垃圾降解油脂和纤维素试验发现,与不接种相比,接种该菌株可显著降低餐厨垃圾中油脂和纤维素含量,45℃以下不生长,可在45~82℃正常生长,能够显著降解餐厨废弃物中的油脂和纤维素,可用于实际生产。
附图说明
为了更清楚地说明本发明的实施方式或现有技术中的技术方案,下面将对实施方式或现有技术描述中所需要使用的附图作简单地介绍。显而易见地,下面描述中的附图仅仅是示例性的,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据提供的附图引伸获得其它的实施附图。
本说明书所绘示的结构、比例、大小等,均仅用以配合说明书所揭示的内容,以供熟悉此技术的人士了解与阅读,并非用以限定本发明可实施的限定条件,故不具技术上的实质意义,任何结构的修饰、比例关系的改变或大小的调整,在不影响本发明所能产生的功效及所能达成的目的下,均应仍落在本发明所揭示的技术内容得能涵盖的范围内。
图1为本发明实施例1提供的光学显微镜下×1000,地衣芽孢杆菌BGB-84F照片;
其中,A-摇瓶摇菌菌株增殖体,B-摇瓶摇菌菌株孢子体;
图2为本发明实施例1提供的地衣芽孢杆菌BGB-84F,60℃培养在营养琼脂培养基上的菌落形态;
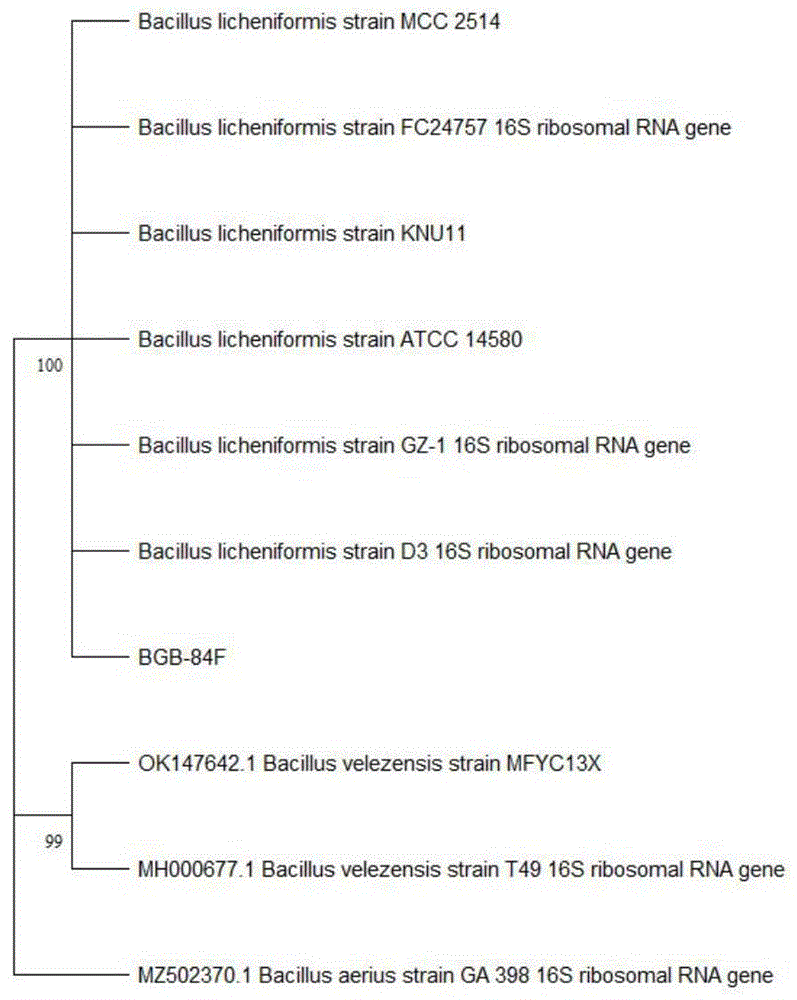
图3为本发明实施例1提供的基于16SrDNA序列构建的系统发育树;
图4为本发明实施例1提供的地衣芽孢杆菌BGB-84F在油脂培养基上的生长情况;其中,A-60℃培养实验组,B-60℃培养对照组;
图5为本发明实施例1提供的地衣芽孢杆菌BGB-84F在纤维素刚果红培养基上的生长情况;其中,A-60℃实验组,B-60℃对照组,C-30℃对照组,D-60℃营养琼脂培养;
图6为本发明实施例1提供的菌株降解油脂和纤维素效果图表,
其中,A-BGB-84F对油脂的降解效果;B-BGB-84F对纤维素的降解效果。
具体实施方式
以下由特定的具体实施例说明本发明的实施方式,熟悉此技术的人士可由本说明书所揭露的内容轻易地了解本发明的其他优点及功效,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
菌种保藏说明:本发明的地衣芽孢杆菌,菌株为BGB-84F,于2022年9月21日,保藏于中国微生物菌种保藏管理委员会普通微生物中心,保藏地址:北京市朝阳区北辰西路1号院3号,中国科学院微生物研究所,其保藏编号为CGMCC No.25764。
实验材料:
供试材料:餐厨垃圾(已破碎,未发酵降解)
供试菌株:地衣芽孢杆菌BGB-84F
主要试验仪器和器材:
超净工作台、高压灭菌锅、恒温振荡培养箱、500mL锥形瓶、镊子、培养皿、玻璃棒、接种环、1.5mL离心管、打孔器、涂布棒等。
试验药品和试剂
(1)试验药品:蛋白胨、H2O、NaCl、酵母粉、牛肉膏、芝麻油、中性红生物染料、硝酸钠、磷酸氢二钠、磷酸二氢钾、硫酸镁、氯化钾、酸水解酪蛋白、刚果红、纤维素粉、琼脂。
(2)试验试剂:
1)营养液体培养基:称取蛋白胨10g、牛肉膏5g、NaCl10g,溶于1L纯水中,pH:6.8-7.5,121℃,30min,灭菌;
2)营养琼脂培养基:加入20g琼脂,其他同表1,121℃,30min,灭菌;
3)PDA培养基:土豆200g、葡萄糖20g/L、琼脂15g/L,水1000mL,自然pH值。称取去皮土豆200g,土豆切成小块放入锅中,加水1000ml,在加热器上加热至沸腾,维持20-30min,用可用6层纱布趁热在烧杯上过滤,取上清液补充水分到1000ml。加入20g葡萄糖、15g琼脂,充分溶解,121℃,30min灭菌,倒板,放置备用。
4)高氏Ⅰ号固体培养基:称取可溶性淀粉20g、KNO
5)油脂培养基:称取蛋白胨10g、氯化钠5g、牛肉膏5g、芝麻油10g、1:6中性红水溶液1mL、琼脂25g于1L纯水中,pH:6.8-7.5,121℃,30min,灭菌,并于超净台倒平板,待用。
6)纤维素刚果红培养基:称取酵母粉0.5g、刚果红试剂0.2g、硝酸钠1.0g、磷酸氢二钠1.2g、磷酸二氢钾0.9g、硫酸镁0.5g、氯化钾0.5g、酸水解酪蛋白0.5g、纤维素粉5.0g、琼脂18g于1L纯水中,pH:6.9-7.1,121℃,30min,灭菌,并于超净台倒平板,待用。
7)餐厨废弃物:将上述已粉碎餐厨垃圾放入500mL锥形瓶,每瓶放置200g,121℃,30min,灭菌,检测初始油脂含量为15.5%,初始纤维素含量为20.20%。
实施例1
本实施例提供地衣芽孢杆菌BGB-84F菌株的分离、纯化、鉴定:
1.餐厨样品采集:采集来自北京大工村餐厨垃圾处理厂,并进行日期及其他信息登记;在餐厨垃圾粉碎后,自然堆肥发酵起始、升温、后期三个时期进行样品采集;
2.目标菌种初步分离:样品采集送至实验室,称取上述采集的样品10g,无菌条件下加入到预先灭菌的盛有100ml生理盐水的三角瓶中,于25℃,30min,160rpm振荡后,静置15min,按照比例稀释至10
待平板长出菌落后,用灭菌的枪头从平板上刮取少量菌落,用无菌水稀释后涂布平板培养。如无单克隆菌落出现,则需反复在平板涂布平板纯化,直到出现单克隆菌落为止,多次纯化,待菌落形态统一,无其他不同形态菌落出现为止。
编号,记录,-80℃保存。
3.初步鉴定:将分离纯化得到的菌株于显微镜下镜检并观察,见图1。
4.菌株性质:
1)形态特征
菌株:营养细胞呈杆状、圆端,多数为单个、少数成对或链状排列,细胞壁为革兰阳性结构。最佳生长温度为55~70℃,最高正常生长温度为65~75℃,最低生长温度为45~50℃,需氧或兼性厌氧。在营养琼脂培养基55℃培养16h的菌落呈透明色,表面光滑湿润,边缘整齐,挑取为粘稠状或冻状(见图2)。
2)培养特性
菌株最适生长条件为:pH=7.0,温度55~60℃,转速180r/min,可利用广泛的碳源和氮源。
3)功能特性
在餐厨废弃物堆肥中,主要功能为可在高温下快速繁殖,并对餐厨废弃物中油脂和纤维素具有一定的降解作用。菌体来源于自然环境,而又被释放到土壤中,对人、动物和植物无害,不会污染环境,还可在一定情况下丰富自然界菌群结构,提高自然界菌群多样性。
5.菌株的16SrDNA序列测序
为鉴定本菌株的系统发育地位,对所分离菌株的16SrDNA序列进行测序。
对菌株单克隆菌液进行PCR特异性扩增,引物分别为27F和1492R,酶选用2×starMix。PCR扩增产物做电泳成像技术进行检测,观察其是否具有条带,将剩余PCR扩增产物用于序列测定。测序结果如SEQ ID NO:1所示。其PCR反应体系如表1:
表1
从NCBI(GenBank)数据库中获取多个参比菌株序列,运用软件BioEdit和MEGA11对分离菌株和参比菌株的16S rDNA序列进行分析,构建分离菌株与参比菌株的系统发育树。从而确定芽孢杆菌株系为地衣芽孢杆菌(Bacillus licheniformis)的菌株系(见图3),并命名为地衣芽孢杆菌BGB-84F(嘉博文84号)。
实施例2
本实施例提供一种地衣芽孢杆菌BGB-84F的餐厨垃圾降解油脂和纤维素试验:
1.菌株培养
将实施例1中-80℃保存的供试菌株3次活化后转接于营养液体培养基培养,培养至对数期,其菌株的生长情况用核酸蛋白测定仪检测,利用OD值估算含菌量,并利用稀释涂布平板计数,用无菌水稀释至1~9×10
2.菌株产脂肪酶及纤维素酶实验
将上述菌含量为1~9×10
观察结果,由图4和图5可见,培养20h,油脂培养基红色平板转变为橙色(脂肪酶可将脂肪水解为甘油和脂肪酸改变培养基的pH,可通过观察菌板的颜色判断菌种是否出现红色斑点来说明这种菌可产生分解油脂的酶),纤维素刚果红培养基出现透明圈(刚果红能与培养基中的纤维素形成红色复合物,已降解的纤维素不能产生红色复合物),可证实菌株代谢脂肪酶及纤维素酶。
3.菌株降解厨余垃圾中油脂和纤维素实验
将已灭菌的锥形瓶及餐厨废弃物接入上述已培养并稀释菌数为(1~9)×10
油脂降解结果如表2,检测结果显示,与对照相比,处理组在24h、48h、72h可油脂降解量分别为19.8%、32%、43.7%。与对照相比,菌株可显著降低物料中油脂含量,菌株降解油脂图见图6A。
表2
纤维素降解结果如表3,检测结果显示,与对照相比,处理组在24h、48h、72h纤维素降解量分别为24%、57.9%、71.1%。与对照相比,菌株可显著降低物料中纤维素含量,菌株降解纤维素图表见图6B。
表3
对比例1
实验材料
高温纤维素降解菌BGB-85F(专利申请号CN202210483248.2)、高温油脂降解菌BGB-83R(专利申请号CN202210069251.X)、BGB-84F
餐厨废弃物及菌悬液制作见实施例2中方法,参照实施例2中,接种后混匀,菌量均为同等菌量(1~9)×10
实验结果如表4所示,随着时间进行,实验处理对纤维素降解率越来越高,实验处理中纤维素降解效率最高的为T3处理,其72h纤维素降解率达到73.36%,T1处理次之,降解效率达到58.91%,而利用专一降解纤维素与专一油脂降解菌复合降解纤维素效仅达到39.30%,其中处理T2专一性油脂降解菌几乎不降解纤维素。
专一性降解纤维素菌BGB-85F降解纤维素效果高于BGB-84F,但BGB-85F与BGB-83R复合之后降解效果显著低于BGB-84F。
表4
实验结果如表5所示,随着实验的进行,菌株对油脂的降解率越来越高,在实验处理进行至72h为最好。其中T2处理油脂降解率达到81.9%,T1次之为66.84%,T4处理降解率为42.7%,其中纤维素降解菌T3处理几乎不降解油脂。
专一性降解油脂菌(BGB-83R)降解油脂效率高于BGB-84F,但BGB-83R与BGB-85F复合之后,综合降解油脂效率显著低于单一菌株。
因此,利用BGB-84F降解油脂与纤维素效率显著高于BGB-83R与BGB-85F复合菌剂效果。
表5
由此可见,BGB-84F降解效果较专一性降解油脂或纤维素菌较低;但是地衣芽孢杆菌BGB-84F可同时降解油脂和纤维素,其在高温情况下降解油脂和纤维素较复合专一性降解油脂和纤维素菌效果好,具有显著性差异。可能因为本菌株在高温情况下生长,无其他菌种竞争,而在高温条件下生长,专一性降解油脂和纤维素菌复合之后,产生较大的竞争关系,导致降解油脂和纤维素效果低于BGB-84F。
虽然,上文中已经用一般性说明及具体实施例对本发明作了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
/>
/>
