一种缓冲液及其在中枢神经特异性蛋白检测试剂盒中的应用
文献发布时间:2023-06-19 11:47:31
技术领域
本发明属于免疫检测技术领域,具体涉及一种缓冲液及其在中枢神经特异性蛋白检测试剂盒中的应用。
背景技术
创伤性脑损伤(traumatic brain injury,TBI)后准确评估中枢神经系统受损严重程度和预后对临床治疗十分重要。目前尚没有一种较为准确的手段来评估TBI的严重程度,也难以判断预后。中枢神经系统损伤所引起的认知功能障碍、运动功能障碍、感觉功能障碍、情绪情感障碍等,严重影响患者的生活质量。
S100-β是一种分子量为21KD的酸性钙结合蛋白,主要由星形胶质细胞产生,通过半胱氨酸残基形成二硫键,以二聚体活性形式大量存在于中枢神经系统中。其含量能反映TBI的程度并对预后进行评估。临床上通过检测S100-β蛋白的表达,能够对脑损伤程度进行判断,同时可对患者的预后情况进行评估。
目前临床上对于创伤性脑损伤的严重程度和术后恢复情况大多通过影像学观察和行为评分进行评估,缺乏足够的精准性和灵敏度。
而现有技术中对脑损伤的检测中利用试剂盒的方法也存在有多种,如中国专利申请CN109266739A公开一种检测脑损伤的miRNA标志物、试剂盒,所述标志物为miR-9、miR-124、miR-128a和miR-128b中的任意一种或多种;所述试剂盒用于检测脑脊液中microRNA标志物的含量;所述标志物和试剂盒,可用于脑损伤辅助诊断。
中国专利申请CN107202890A公开一种用于轻中度脑损伤的快速诊断试剂及含有该试剂的试剂盒及该试剂盒的制备和检测方法,该试剂和试剂盒包括S100、GFAP、UCHL1分别制得的单克隆捕获抗体;所述试剂盒还包括检测抗体,S100、GFAP、UCHL1分别制得的多克隆抗体。
中国专利申请CN109856403A公开一种S100-β蛋白时间分辨荧光免疫层析检测试剂盒采用镧系元素螯合物标记荧光微球后,进而标记S100-β单克隆抗体。
但试剂盒的使用普遍存在灵敏度较差,或者制备过程复杂、检测时间长、成本高等情况。本发明旨在解决现有技术中存在的脑损伤检测试剂盒的灵敏度差、检测时间慢等问题。
发明内容
为克服以上技术问题,本发明提供了一种缓冲液,该缓冲液可以应用在中枢神经特异性蛋白检测试剂盒中,用于检测脑损伤,具有较高的灵敏度,并且可以在较短时间内完成检测。
为实现以上目的,本发明提供的技术方案如下:
一种缓冲液,包括如下组分:4-羟乙基哌嗪乙磺酸(HEPES)、氯化钠(NaCl)、氯化钾(KCl)、硫酸镁(MgSO
优选地,按照重量份数计,所述缓冲液包括如下组分:HEPES 1.0-10份、氯化钠5-10份、氯化钾0.5-5份、硫酸镁0.1-10份、BSA 4.0-30份、海藻糖10-100份、甘氨酸4.0-20份、Casein 0.5-25份、甘油20-200份。
优选地,按照重量份数计,所述缓冲液包括如下组分:HEPES 3.0-10份、氯化钠9份、氯化钾0.5-5份、硫酸镁0.1-10份、BSA 4.0-27份、海藻糖10-100份、甘氨酸4.0-18份、Casein 0.5-25份、甘油20-200份。
优选地,所述缓冲液的制备方法,包括以下步骤:
(1)称取HEPES、NaCl、KCl、MgSO
(2)使用滤膜进行过滤,即得缓冲液。
优选地,所述pH值在6.5-8.2之间。
优选地,所述滤膜孔径为0.22μm。
本发明的另一目的在于提供所述缓冲液在制备中枢神经特异性蛋白检测试剂中的应用。
本发明的目的还在于提供一种中枢神经特异性蛋白检测试剂盒,所述试剂盒中包括所述缓冲液。
优选地,所述试剂盒包括:检测试剂条、质控品、校准品。
优选地,所述质控品的制备方法为:将S100-β重组蛋白作为校准品的原料,以所述缓冲液将其溶解,充分混合后配制而成。
优选地,所述校准品的制备方法为:将S100-β重组蛋白作为质控品的原料,以所述缓冲液将其溶解,充分混合后配制而成。
优选地,所述检测试剂条包括试剂A、试剂B、试剂C、清洗液、发光底物、测读孔位、反应孔位、清洗孔位、洗脱套、吸头。
其中,所述试剂A为碱性磷酸酶标记的S100-β抗体溶液;
所述试剂B为生物素标记的S100-β抗体溶液;
所述试剂C为链霉亲和素标记的磁微粒溶液;
所述清洗液为:含非离子型表活性剂的三羟甲基氨基甲烷(Tris)缓冲液;
优选地,所述清洗液的组成为:Tween-20的浓度为0.5-5%(w/v),TritonX-100的浓度为0.05-0.5%(v/v),其余为水。
所述发光底物为ALP催化的发光底物。
优选地,所述试剂A的制备方法为:将酶标记S100-β抗体偶联物作为试剂A的原料,使用缓冲液A将其溶解后配制而成。
优选地,所述试剂B的制备方法为:将生物素化S100-β抗体偶联物作为试剂B的原料,,使用缓冲液B将其溶解后配制而成。
优选地,所述试剂C的制备方法为:将链霉亲和素磁微粒偶联物作为试剂C的原料,使用缓冲液C将其溶解后配制而成。
优选地,按照重量份数计,所述缓冲液A、缓冲液B和缓冲液C的组成均为:
三羟甲基氨基甲烷3.5-15份、氯化钠9.0份、牛血清白蛋白1.0-50份、牛血清10-100份、羊血清1.0-20份、马血清1.0-20份。
所述缓冲液A、缓冲液B和缓冲液C的pH值为5.8-7.6。
优选地,所述酶标记S100-β抗体偶联物的制备方法,包括以下步骤:
(1)抗体活化:称取2IT,用缓冲液1溶解,加入抗体溶液中进行活化、震荡、反应,再加入缓冲液2,反应后使用PD10脱盐柱除去过量的2IT,制得活化后的抗体溶液;
(2)碱性磷酸酶的活化:称取SMCC、用DMF溶解,震荡、反应,制得SMCC溶液,在SMCC溶液中加入ALP,震荡,反应,再加入缓冲液2,反应,使用PD10脱盐柱除去过量的SMCC,制得活化后的ALP溶液;
(3)抗体和ALP的连接:在抗体溶液中的加入ALP溶液,震荡、反应,制得酶标抗体偶联物;
(4)酶标抗体偶联物的终止和纯化:称取马来酰亚胺用DMF溶解,用缓冲液1稀释,得到马来酰亚胺溶液;反应;
取乙醇胺,用缓冲液1溶解,震荡,使用超滤浓缩管将酶标抗体偶联物浓缩;使用蛋白纯化分析仪和Superdex 200制备级2.6/60凝胶柱进行抗体纯化;使用缓冲液2洗脱;制得纯化的酶标抗体偶联物。
优选地,所述生物素化S100-β抗体偶联物的制备方法,包括以下步骤:
用PBS配制生物素溶液,震荡,反应后,加入脱盐柱中,加入等体积的PBS缓冲液开始洗脱;制得纯化后的生物素化抗体偶联物。
优选地,所述链霉亲和素磁微粒偶联物的制备方法,包括以下步骤:
将磁微粒用缓冲液3清洗后,重悬,在磁微粒溶液中加入链霉亲合素,反应;再在磁微粒溶液中加入EDC,反应后,进行磁性分离;使用缓冲液4将分离后的磁微粒重悬,将磁性分离后的磁微粒-链霉亲合素连接物充分混匀后,在室温下混匀反应1-4小时;再对连接物进行磁性分离,使用缓冲液5将分离后的磁微粒重悬,制得链霉亲和素磁微粒偶联物。
本发明的另一目的在于提供所述试剂盒的检测方法,所述方法包括以下步骤:
S1:免疫反应:将样本、试剂A、试剂B、试剂C依次加入反应孔位,反应;
S2:磁分离及清洗:在孔位加入清洗液,将免疫反应的产物用磁力吸出反应孔位,在清洗孔位脱磁,清洗。
S3:读值:在测度孔位加入发光底物;用自研仪器检测相对发光强度(RLU);
S4:根据检测的校准品数值可获得一条S100-β浓度-发光值标准曲线;该曲线使用四参数Logistic方程拟合;
S5:样本的检测值可以和这条曲线上获得唯一的浓度值对应,从而实现对未知样本的浓度检测。
与现有技术比,本发明的技术优势在于:
(1)本发明提供的缓冲液对试剂盒的检测灵敏度具有较大的影响。本发明提供的试剂盒对中枢神经特异性蛋白检测试剂盒检测的灵敏度达到50皮克/毫升(50×10
(2)本发明配合全自动仪器进行检测,只需加入该有样品的采血管,18分钟即可得到准确结果;远优于传统化学发光30分钟的反应时间或酶联免疫法1-2小时的反应时间。
(3)本发明提供的试剂盒具有更高的精准度和灵敏度和特异性。与其他的方法学相比,灵敏度高、线性宽、反应时间短、准确率高。
(4)抗原缓冲液对S100-β具有较好的保护作用,液体状态下在常温(10-30℃)环境下可以保持活性7天、在2-8℃条件下可保持活性6个月、在-20条件下可保持活性12个月。在冻干条件下可保持活性3年。
附图说明
图1:S100-β检测试剂条示意图;
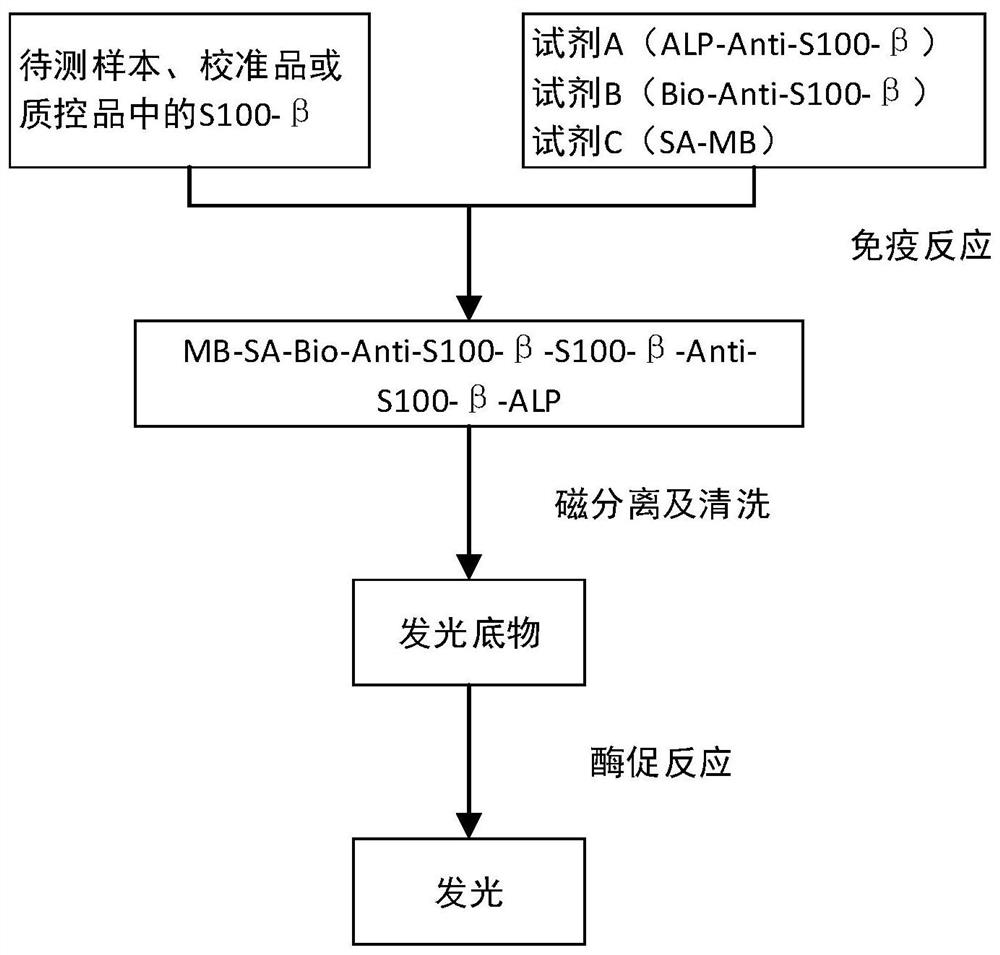
图2:试剂盒使用时的反应流程图;
图3:试剂盒制备工艺流程图;
附图中标记的具体含义如下:1:样本孔位;2:吸头;3:洗脱套;4:清洗液;5:发光底物;6:试剂B;7:试剂C;8:试剂A;9:稀释孔位1;10:稀释孔位2;11:反应孔位;12:清洗孔位1;13:清洗孔位2;14:清洗孔位3;15:测读孔。
现结合附图和实施例对本发明作进一步说明:
具体实施方式
下面通过具体实施例对本发明进行说明,以使本发明技术方案更易于理解、掌握,但本发明并不局限于此。下述实施例中所述实验方法,如无特殊说明,均为常规方法;所述试剂和材料,如无特殊说明,均可从商业途径获得。
1、缓冲液的制备
实施例1
一种缓冲液,按照重量份数计,所述缓冲液包括如下组分:HEPES 3.0g、氯化钠9g、氯化钾2g、硫酸镁5g、BSA 27g、海藻糖40g、甘氨酸18g、Casein 15g、甘油100ml。
所述缓冲液的制备方法,包括以下步骤:
(1)称取HEPES、NaCl、KCl、MgSO
(2)使用0.22μm滤膜进行过滤,即得缓冲液。(记为缓冲液S1)
实施例2
一种缓冲液,按照重量份数计,所述缓冲液包括如下组分:HEPES 1.0g、氯化钠5g、氯化钾0.5g、硫酸镁10g、BSA 30g、海藻糖10g、甘氨酸20g、Casein 0.5g、甘油20ml。
所述缓冲液的制备方法,包括以下步骤:
(1)称取HEPES、NaCl、KCl、MgSO
(2)使用0.22μm滤膜进行过滤,即得缓冲液。(记为缓冲液S2)
实施例3
一种缓冲液,按照重量份数计,所述缓冲液包括如下组分:HEPES 10g、氯化钠10g、氯化钾5g、硫酸镁0.1g、BSA 4.0g、海藻糖100g、甘氨酸4.0g、Casein 25g、甘油200ml。
所述缓冲液的制备方法,包括以下步骤:
(1)称取HEPES、NaCl、KCl、MgSO
(2)使用0.22μm滤膜进行过滤,即得缓冲液。(记为缓冲液S3)
对比例1
与实施例1相比,区别在仅于pH值不同。
一种缓冲液,组成同实施例1。
所述缓冲液的制备方法,包括以下步骤:
(1)称取HEPES、NaCl、KCl、MgSO
(2)使用0.22μm滤膜进行过滤,即得缓冲液。(记为缓冲液D1)
对比例2
与实施例1相比,区别仅在于海藻糖和甘氨酸的用量不同。
一种缓冲液,按照重量份数计,所述缓冲液包括如下组分:HEPES 3.0g、氯化钠9g、氯化钾2g、硫酸镁5g、BSA 27g、海藻糖8g、甘氨酸50g、Casein 15g、甘油100ml。
所述缓冲液的制备方法,步骤同实施例1。(记为缓冲液D2)
对比例3
与实施例1相比,区别仅在于将HEPES替换为PIPES(1,4-哌嗪二乙磺酸)。
一种缓冲液,按照重量份数计,所述缓冲液包括如下组分:PIPES 3.0g、氯化钠9g、氯化钾2g、硫酸镁5g、BSA 27g、海藻糖40g、甘氨酸18g、Casein 15g、甘油100ml。
所述缓冲液的制备方法,包括以下步骤:
(1)称取PIPES、NaCl、KCl、MgSO
(2)使用0.22μm滤膜进行过滤,即得缓冲液。(记为缓冲液D3)
对比例4
与实施例1相比,区别仅在于将甘油替换为丙二醇。
一种缓冲液,按照重量份数计,所述缓冲液包括如下组分:HEPES 3.0g、氯化钠9g、氯化钾2g、硫酸镁5g、BSA 27g、海藻糖40g、甘氨酸18g、Casein 15g、丙二醇100ml。
所述缓冲液的制备方法,包括以下步骤:
(1)称取HEPES、NaCl、KCl、MgSO
(2)使用0.22μm滤膜进行过滤,即得缓冲液。(记为缓冲液D4)
2、中枢神经特异性蛋白检测试剂盒的制备
2.1缓冲液
除实施例1-3以及对比例1-4所制备的缓冲液以外,中枢神经特异性蛋白检测试剂盒的制备过程中使用的缓冲液还包括以下缓冲液:
(1)缓冲液1
称取15g的乙醇胺、6.0g的NaCl加入到纯化水中搅拌至完全溶解,调试PH值在7.3-7.6之间并定容至1000ml,用0.22μm的滤膜进行过滤。
(2)缓冲液2
称取75g的甘氨酸加入到纯化水中搅拌至完全溶解,定容至1000ml,用0.22μm的滤膜进行过滤。
(3)缓冲液3
称取30.0g的MES加入到纯化水中搅拌至完全溶解,调试PH值在4.0-7.0之间并定容至1000ml,用0.22μm的滤膜进行过滤。
(4)缓冲液4
称取6.0g的Tris、9.0g的NaCl、15g的牛血清白蛋白加入到纯化水中搅拌至完全溶解,调试PH值在6.4-8.5之间并定容至1000ml,用0.22μm的滤膜进行过滤。
(5)缓冲液5
称取4.0g的Tris、9.0g的NaCl加入到纯化水中搅拌至完全溶解,调试PH值在7.0-7.8之间并定容至1000ml,用0.22μm的滤膜进行过滤。
(6)缓冲液6
称取7g的Tris、9.0g的NaCl、30g的牛血清白蛋白、50mL的牛血清、10mL的羊血清、10mL的马血清加入到纯化水中搅拌至完全溶解,调试PH值在5.8~7.6之间并定容至1000ml,用0.22μm的滤膜进行过滤。
2.2试剂盒组分
S100-β试剂盒由检测试剂条、校准品、质控品、二维码组成;其中检测试剂条由一系列溶液和附件组成一个整体,可以独立检测一个样本,校准品由含有两个浓度的S100-β抗原和缓冲液配制而成,用于校准标准曲线;质控品由含有两个浓度的S100-β抗原和缓冲液配制而成;二维码中录入了当批次的标准曲线。
表1试剂盒主要组分
2.3试剂条组分
检测试剂条由试剂A、试剂B、试剂C、清洗液、发光底物、测读孔、洗脱套、吸头组成(试剂条的示意图见图1)。
试剂A为碱性磷酸酶标记的S100-β抗体溶液,浓度为0.8μg/mL;试剂B为生物素标记的S100-β抗体溶液,浓度为1.2μg/mL;试剂C为链霉亲合素标记的磁微粒溶液,浓度为0.4mg/mL;清洗液用于反应过程的清洗;发光底物为ALP催化的发光底物;测读孔用于最终的检测读值。
表2试剂条主要组分
2.4试剂盒的制备:
2.4.1校准品、质控品的制备
将S100-β重组蛋白作为校准品的原料,以缓冲液(本发明提供的缓冲液S1-S3或缓冲液D1-D4中的任一种)将其溶解,充分混合后配制成2个校准品,浓度为1ng/mL、100ng/mL。
将S100-β重组蛋白作为质控品的原料,以缓冲液(同校准品的缓冲液)将其溶解,充分混合配制成质控品。浓度为20ng/mL。
2.4.2试剂A的制备
(1)酶标记S100-β抗体偶联物的制备
称取6mg 2-亚氨基硫烷盐酸盐(2IT),用缓冲液1溶解至13.76mg/mL,按比例(1mg抗体加入15μL 2IT溶液)将2IT溶液加入抗体溶液中进行活化,震荡混匀后在室温下反应30分钟,终止活化,按1mg抗体加入15μL缓冲液2的比例,将缓冲液2加入抗体溶液中,室温反应10min,使用PD10脱盐柱除去过量的2IT,收集活化后的抗体。
称取3mg SMCC,用DMF溶解至6.69mg/mlL,按比例在ALP溶液中加入SMCC溶液(1mgALP加入30μL SMCC溶液),震荡混匀后,室温下反应30分钟,终止活化,按1mg ALP加入30μL缓冲液2的比例,将缓冲液2加入ALP溶液中,室温反应10min;使用PD10脱盐柱除去过量的SMCC,收集活化后的ALP。
按比例在抗体溶液中的加入ALP溶液(1.0mg抗体加入1.5mg ALP),震荡混匀后,将混合物,6℃环境中反应16小时。
称取6mg马来酰亚胺,用DMF溶解至9.7mg/mL,按1/10比例,用缓冲液1稀释,得到0.97mg/mL马来酰亚胺溶液,按1mg抗体加入10μL 0.97mg/mL马来酰亚胺溶液比例加入该溶液,在室温下反应15分钟。准确量取6μL乙醇胺,用缓冲液1溶解至100mM(即在6μL乙醇、胺加入994μL缓冲液1)。按1mg抗体加入30μL 100mM乙醇胺溶液的比例加入该溶液,震荡混匀。使用超滤浓缩管将待纯化的抗体偶联物浓缩至2mg/mL。使用纯化蛋白分析仪和Superdex200制备级2.6/60凝胶柱进行抗体纯化,洗脱液为缓冲液2。纯化后的液体为酶标抗体偶联物。
(2)试剂A的制备
将酶标记S100-β抗体偶联物作为试剂A的原料,以缓冲液6将其充分混匀配制成试剂A。
2.4.3试剂B的制备
(1)生物素化S100-β抗体偶联物的制备
按比例在抗体溶液中的加入10mM生物素溶液(1.0mg抗体加入26.68μL 10mM生物素),震荡混匀后,将混合物在室温环境中反应1小时。
将需要脱盐的抗体偶联物加入脱盐柱中。当抗体偶联物完全进入柱料前,使用0.02M PBS补足柱料体积。柱内液体完全进入柱料时,加入等体积的0.02M PBS缓冲液开始洗脱。收集等体积蛋白洗脱液并测试浓度。纯化后的液体为生物素化抗体偶联物。
(2)试剂B的制备:将生物素化S100-β抗体偶联物作为试剂B的原料,以缓冲液6将其充分混匀配制成试剂B。
2.4.4试剂C的制备
(1)将链霉亲合素磁微粒偶联物的制备
将磁微粒用缓冲液3清洗后,重悬至10mg/mL。按磁微粒与链霉亲合素质量比100:10的比例在磁微粒溶液中加入链霉亲合素。充分混合后,在室温下混匀反应10分钟。按磁微粒与(3-二甲氨基丙基)乙基碳二亚胺盐酸盐(EDC)质量比100:50的比例在磁微粒溶液中加入EDC。充分混合后,在室温下混匀反应1小时。
对连接物进行磁性分离。使用缓冲液4将分离后的磁微粒重悬至10mg/mL。充分混匀后,在室温下混匀反2小时。再对连接物进行磁性分离,使用缓冲液5将分离后的磁微粒重悬至10mg/mL,保存于6℃环境下。
(2)试剂C的制备
将链霉亲合素磁微粒偶联物作为试剂C的原料,以缓冲液6将其充分混匀配制成试剂C。
3、效果例
3.1本发明所述试剂盒的检测原理
本试剂盒采用双抗体夹心法测定S100-β的含量。样本中S100-β和试剂A中的S100-β酶标抗体及试剂B中的S100-β生物素化抗体结合,形成“三明治”夹心结构。在夹心结构中加入试剂C,使夹心结构中的生物素和试剂C中的链霉亲合素结合形成“抗原-抗体-磁微粒”复合物。经洗涤,在复合物中加入发光底物,发光底物被复合物中的酶催化裂解,形成不稳定的激发态中间体,当激发态中间体回到基态时便发出光子。产生的光子数与样本中S100-β的浓度成正相关。
采用北京美联泰科生物技术有限公司自研的全自动化学发光免疫分析仪进行检测。反应所需样本量为30μL,自动检验流程为:
A.免疫反应:将30μL样本、50μL试剂A、50μL试剂B、50μL试剂C依次加入反应孔位,在37℃条件下反应20min。
B.磁分离及清洗:在1号清洗孔位加入300μL清洗液,将含磁微粒的混合物用磁力吸出反应孔位,在1号清洗孔位脱磁。清洗2min后;在2号和3号清洗孔位分别进行1次磁分离及清洗。
C.读值:在测读孔位加入150uL发光底物,将含磁微粒的混合物用磁力吸出3号清洗孔位,在测读孔位脱磁;ALP催化的发光底物发光后检测相对发光强度(RLU)。
D.根据检测的校准品数值可获得一条S100-β浓度-发光值标准曲线。该曲线使用四参数Logistic方程拟合。
E.样本的检测值可以和这条曲线上获得唯一的浓度值对应,从而实现对未知样本的浓度检测。
3.2检测指标
3.2.1准确度
将浓度约为20ng/mL(允许偏差±10%)的中枢神经特异性蛋白(S100-β)液(A)加入到浓度范围0ng/mL-0.1ng/mL的样本B中,所加入S100-β抗原与样本B之间的体积比例为1:9,根据公式(1)计算回收率R,其回收率应在85%~115%范围内。
式中:
R—回收率;
V—样品A液的体积;
V
C—血清样品B液加入A液后的3次测量平均值;
C
C
3.2.2灵敏度
将不含任何分析物的样本重复测试20次,得到20次测试结果的浓度值,计算其平均值
3.2.3线性区间
将接近线性区间上限的高值样本与接近线性区间下限的低值样本或零浓度样本混合成不少于5个稀释浓度,其中低值浓度的样本须接近线性区间的下限。对每一浓度的样本各重复测试3次得到发光值,记录各样品的测量结果,并计算各样品3次测量值的平均值(y
式中:
r————相关系数;
x
y
3.2.4重复性
同批号试剂盒重复测试质控品10次,计算10次测试结果的平均值
式中:s——样本测试值的标准差;
3.2.5批间差
用3个批号的试剂盒分别重复测试质控品10次,计算30次测试结果的平均值
3.2.6特异性实验
在不含任何分析物的样本中加入浓度为200ng/mL的S100-α样本。测3次取均值,其测定结果不高于0.1ng/mL。
按照3.2.1-3.2.6的方法检测实施例1-3及对比例1-3的缓冲液应用到试剂盒时的效果,结果见下表3:
表3效果数据
由此可知,本发明提供的试剂盒具有更高的精准度和灵敏度和特异性。且缓冲液的组成及其有效成分的用量对其效果具有较大的影响。
上述详细说明是针对本发明其中之一可行实施例的具体说明,该实施例并非用以限制本发明的专利范围,凡未脱离本发明所为的等效实施或变更,均应包含于本发明技术方案的范围内。
- 一种缓冲液及其在中枢神经特异性蛋白检测试剂盒中的应用
- 一种缓冲液及其在神经元特异性烯醇化酶检测试剂盒中的应用
