脆性X综合征FMR1基因检测引物、试剂盒及其应用
文献发布时间:2023-06-19 12:08:44
技术领域
本发明涉及基因检测技术领域,尤其涉及一种脆性X综合征FMR1基因检测引物、试剂盒及其应用。
背景技术
脆性X综合征(Fragile X Syndrome,FXS),又称Martin-Bell综合征,表现为智力低下,语言及行为能力障碍等。FXS是一种不完全显性的单基因遗传疾病,主要由位于X染色体的FMR1基因5’端非翻译区CGG三核苷酸重复数异常所致。美国医学与遗传学会指南将CGG重复数分为四个等级:小于45为正常;45~54为中间型;55~200为前突变;大于200为完全突变。当CGG重复数大于200时,常伴有序列的异常甲基化,导致FMR1基因功能缺失,使FMR1基因编码的FMRP蛋白表达降低,无法正常调控神经元靶mRNA翻译,导致脆性X综合征的发生。临床表现为重度智力障碍、发育迟缓、自闭症等症状。
FXS发病率仅次于唐氏综合征,成为第二大遗传性智力障碍疾病。男性发病率约为女性的1.5倍。目前,FXS检测的分子生物学方法包括Southen杂交、普通PCR扩增结合Sanger测序和三引物TP-PCR法。传统的Southern blot方法,技术较繁琐,耗时较长,对样本质量要求较高,不适合常规高通量检测。由于目标区域GC含量高,普通PCR扩增和Sanger测序法无法确定CGG重复数。Warner等人发明的三引物TP-PCR法试剂组分复杂,无法得到稳定且准确的目标扩增产物,特别是含有一条完全突变序列的染色体的女性,由于另一条正常染色体的影响,完全突变CGG重复序列结构异常,无法有效扩增全部目标片段。市售的商品化试剂盒,普遍使用多条扩增引物,或全长扩增和重复扩增双体系,通常不能同时兼顾扩增特异性、检测速度和结果判定准确性。
发明内容
针对现有技术中所存在的不足,本发明提供了一种脆性X综合征FMR1基因检测引物、试剂盒及其应用,以解决相关技术中传统脆性X综合征FMR1基因检测效率低准确度低的技术问题。
本发明提供了一种脆性X综合征FMR1基因检测引物,包括用于扩增FMR1基因5’非编码区CGG重复区域的上游特异性引物F1或F2,其核苷酸序列如SEQ ID No:1或4所示;
用于扩增FMR1基因5’非编码区CGG重复区域的下游特异性引物R1或R2,其核苷酸序列如SEQ ID No:2或5所示;以及,
用于扩增CGG重复区域的引物CGG-F或CCG-R,其核苷酸序列如SEQ ID No:3或6所示;
其中,所述用于扩增FMR1基因5’非编码区CGG重复区域的上游特异性引物F1或F2、所述用于扩增FMR1基因5’非编码区CGG重复区域的下游特异性引物R1或R2及所述用于扩增CGG重复区域的引物CGG-F或CCG-R的体积比为50~200:50~200:1。
表1各核苷酸序列
可选地,所述用于扩增CGG重复区域的引物CGG-F或CCG-R为:
用于扩增CGG重复区域的引物的5’端的碱基序列为SEQ ID No:1或SEQ ID No:5所示;
用于扩增CGG重复区域的引物的3’端的碱基序列为CGGCGGCGGCGGCGG或CCGCCGCCGCCGCCG;
在上述5’端碱基序列和3’端碱基序列中间插入CG或AG碱基,以构成引物CGG-F或CCG-R。
本发明还提供了一种试剂盒,包括如上所述的脆性X综合征FMR1基因检测引物。
可选地,所述试剂盒还包括PCR扩增体系反应液和毛细管电泳体系试剂。
可选地,所述毛细管电泳体系试剂包括内标DNA分子片段和去离子甲酰胺。
可选地,所述PCR扩增体系反应液包括DNA聚合酶、缓冲液、dNIP混合液及PCR增强剂。
可选地,所述试剂盒还包括正常质控品、中间型质控品、前突变型质控品和完全突变型质控品中的一种或几种;
其中,所述正常质控品的CGG重复数小于45个;
所述中间型质控品的CGG重复数为45~54个;
所述前突变型质控品的CGG重复数为55~200个;
所述完全突变型质控品的CGG重复数大于200个。
可选地,所述质控品包括28、45、103及大于200个CGG重复数的质控品。
本发明还提供了一种如上所述的脆性X综合征FMR1基因检测引物在检测脆性X综合征FMR1基因CGG重复数的应用。
相比于现有技术,本发明具有如下有益效果:
本发明技术中,通过优化设计脆性X综合征FMR1基因检测引物序列,提高了CGG重复数的检测效率和检测准确性;并且整个体系组分简单、特异性强、成本低廉。
附图说明
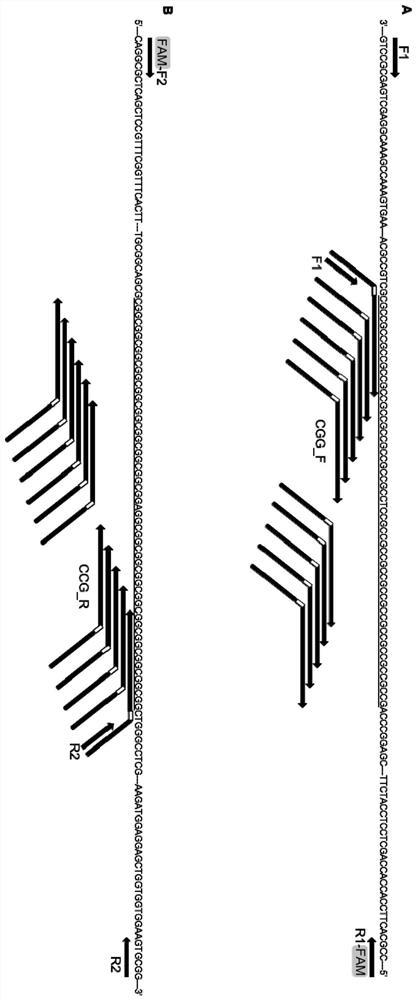
图1为本发明一实施例中的脆性X综合征FMR1基因检测引物的检测原理图;
图2至图4为本发明一实施例中不同配比引物群的PCR结果数据图;
图5至图6为本发明一实施例中不同配比的毛细管电泳结果数据图;
图7至图15为本发明一实施例中的临床数据结果图。
本发明目的的实现、功能特点及优点将结合实施例,参照附图做进一步说明。
具体实施方式
为了使本发明的目的、技术方案及有益效果更加清楚明白,下面结合附图及实施例对本发明中的技术方案进一步说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
本发明提供了一种脆性X综合征FMR1基因检测引物,包括用于扩增FMR1基因5’非编码区CGG重复区域的上游特异性引物F1或F2,其核苷酸序列如SEQ ID No:1或4所示;
用于扩增FMR1基因5’非编码区CGG重复区域的下游特异性引物R1或R2,其核苷酸序列如SEQ ID No:2或5所示;以及,
用于扩增CGG重复区域的引物CGG-F或CCG-R,其核苷酸序列如SEQ ID No:3或6所示;
其中,所述用于扩增FMR1基因5’非编码区CGG重复区域的上游特异性引物F1或F2、所述用于扩增FMR1基因5’非编码区CGG重复区域的下游特异性引物R1或R2及所述用于扩增CGG重复区域的引物CGG-F或CCG-R的体积比为50~200:50~200:1。具体参见表1。
应当理解,本发明中引物的设计,拟在FMR1基因的5’非编码区的CGG重复区域上下游约200bp碱基片段内设计上游引物和下游引物,并同时设计CGG重复区域的引物,形成用以进行PCR扩增的引物群。进一步地,拟通过该引物群的组合,形成最佳配比的引物群,以快速、精准地进行脆性X综合征FMR1基因的检测,有利于临床医学及其研究。
可选地,所述用于扩增CGG重复区域的引物CGG-F或CCG-R为:
用于扩增CGG重复区域的引物的5’端的碱基序列为SEQ ID No:1或SEQ ID No:5所示;
用于扩增CGG重复区域的引物的3’端的碱基序列为CGGCGGCGGCGGCGG或CCGCCGCCGCCGCCG;
在上述5’端碱基序列和3’端碱基序列中间插入CG或AG碱基,以构成引物CGG-F或CCG-R。
可选地,所述SEQ ID No:2或者所述SEQ ID No:4序列5’端标记有荧光修饰。
本发明还提供了一种试剂盒,包括如上所述的脆性X综合征FMR1基因检测引物。
可选地,所述试剂盒还包括PCR扩增体系反应液和毛细管电泳体系试剂。
可选地,所述毛细管电泳体系试剂包括内标DNA分子片段和去离子甲酰胺。
可选地,所述PCR扩增体系反应液包括DNA聚合酶、缓冲液、dNIP混合液及PCR增强剂。
可选地,所述试剂盒还包括正常质控品、中间型质控品、前突变型质控品和完全突变型质控品中的一种或几种;
其中,所述正常质控品的CGG重复数小于45个;
所述中间型质控品的CGG重复数为45~54个;
所述前突变型质控品的CGG重复数为55~200个;
所述完全突变型质控品的CGG重复数大于200个。
可选地,所述质控品包括28、45、103及大于200个CGG重复数的质控品。
本发明还提供了一种如上所述的脆性X综合征FMR1基因检测引物在检测脆性X综合征FMR1基因CGG重复数的应用。
为进一步阐述本发明提供的脆性X综合征FMR1基因检测引物的性能,选用以下实施例进行详细阐述。应当理解,下列实施例仅用于说明本发明中脆性X综合征FMR1基因检测引物的效果,并不限制本发明的脆性X综合征FMR1基因检测引物。
需要说明的是,下述实施例中所使用的实验方法如无特殊说明,均为常规方法。下述实施例中所用的材料、试剂、器材等,如无特殊说明,均可从商业途径获得。
实施例1制备脆性X综合征FMR1基因CGG重复数的试剂盒
1、实验操作:
1.1引物设计:
在FMR1基因CGG重复序列的上游和下游200bp内设计一对特异性引物上游引物F1(SEQ ID NO:1)和下游引物R1(SEQ ID NO:2),并在FMR1基因CGG重复序列内设计CGG序列动态扩增引物CGG-F(SEQ ID NO:3),进行PCR扩增,并得到扩增产物,其核苷酸序列如SEQ IDNO.7所示(具体参见序列表)。
1.2 PCR扩增体系:
①PCR扩增体系反应液试剂包括DNA聚合酶、反应缓冲液、PCR增强剂及dNTP混合液;其中,
DNA聚合酶为5U/μL的Advantage@-GC Genomic LA Polymerase;
反应缓冲液为2×Advantage@GC Melt Buffer(5mM MgCl2);
PCR增强剂为5×Q-Solution;
dNTP混合液为10mM dATP、10mM dTTP、10mM dCTP、10mM dGTP、10mM 7-deaza-dGTP。
②PCR扩增体系如下:
③扩增PCR仪程序如下:(设置缓慢升温速率为2.5℃/sec;缓慢降温速率为1.5℃/sec)
1.3毛细管电泳体系:
毛细管电泳体系为8.7uL去离子甲酰胺和0.3uL DNA分子内标ROX-1200。
1.4获得CGG重复数:
按1.2中PCR反应得到的PCR产物和1.3中得到的毛细管电泳体系的体积比为1:8~10分别取PCR产物和毛细管电泳体系,混合;95℃变性3min,冰上冷却,得到混合物;然后用ABI3730XL将混合物进行毛细管电泳,其中,毛细管长度为50cm,进样电压2.5kV、20秒,电泳时间4000秒。然后利用GeneMapper分析,片段分子大小标记为Peaki,将y=Peaki代入公式y=2.8008x+216.6,R
实施例2不同配比引物群的PCR扩增实验
2.1实验操作:
按体积比为50:50:1、100:100:1及500:500:1分别取上游引物片段、下游引物片段及CGG重复数引物片段,以配制不同配比的引物群;然后于实施例1中的PCR扩增体系中扩增,得到如图2至图4所示的结果数据。
2.2结果分析:
由图2和图4可知,在上游引物片段:下游引物片段:CGG重复数引物片段的体积比范围为50~200:50~200:1形成的引物群,通过PCR扩增,均能得到本发明所需的PCR扩增产物;当上游引物片段:下游引物片段:CGG重复数引物片段的体积比为500:500:1时,扩增后得到的产物不符合本发明后续毛细管电泳所需的PCR产物需求。说明,引物群中上游引物片段、下游引物片段及CGG重复数引物片段的比例,影响PCR扩增后的产物。
实施例3不同PCR产物和毛细管电泳体系配比的组合实验
3.1实验操作:
分别按1:8和1:12的体积比分别取通过PCR扩增得到的PCR产物和毛细管电泳体系,混合,95℃变性3min,冰上冷却,得到混合物;然后用ABI3730XL将混合物进行毛细管电泳,其中,毛细管长度为50cm,进样电压2.5kV、20秒,电泳时间4000秒;再后利用GeneMapper分析,得到CGG重复数,并得到如图5和图6所示的结果数据。
3.2结果分析:
由图5和图6可知,PCR产物和毛细管电泳体系的配比对CGG重复数的测定有影响。
实施例4临床试验
4.1实验操作:
按表2所示的基因来源,分别用市售基因组DNA提取试剂盒提取样本外周血基因组DNA,提取的DNA浓度为50~100ng/uL,OD260/230>2.0,OD260/280>1.8;然后将上述基因组用引物群进行PCR扩增,得PCR扩增产物;再后按1:9的体积比分别取上述PCR扩增产物和毛细管电泳体系,混合,95℃变性3min,冰上冷却,得到混合物;然后用ABI3730XL将混合物进行毛细管电泳,其中,毛细管长度为50cm,进样电压2.5kV、20秒,电泳时间4000秒;再后利用GeneMapper分析,得到CGG重复数,并得到如图7和图15所示的结果数据。
表2不同基因来源的CGG重复数测试实验
4.2结果分析:
由图7至9可知,对正常型男性NM的基因进行检测,得到其CGG重复数为28;对正常女性纯合HF的基因进行检测,得到其CGG重复数为28;对正常女性杂合HetF的基因进行检测,得到其CGG重复数为28/29。
由图10和图11可知,对中间型男性IM的基因进行检测,得到其CGG重复数为45;对中间型女性IF的基因进行检测,得到其CGG重复数为29/53。
由图12和图13可知,对前突变型男性PM的基因进行检测,得到其CGG重复数为103;对前突变型女性PF的基因进行检测,得到其CGG重复数为28/79。
由图14和图15可知,对完全突变型男性FM的基因进行检测,得到其CGG重复数大于200;对完全突变型女性FF的基因进行检测,得到其CGG重复数大于200。
综上,通过由本发明设计的脆性X综合征FMR1基因检测引物群扩增得到的PCR产物和毛细管电泳体系进行毛细管电泳,可精准快速地检测出待测基因的CGG重复数。
最后说明的是,以上实施例仅用以说明本发明的技术方案而非限制,尽管参照较佳实施例对本发明进行了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的宗旨和范围,其均应涵盖在本发明的权利要求范围当中。
- 脆性X综合征FMR1基因检测引物、试剂盒及其应用
- 一种脑胶质瘤突变基因检测引物组合物、试剂盒及试剂盒的应用
