抗体组合物及应用、检测血液中YKL-40浓度的方法
文献发布时间:2023-06-23 06:30:03
技术领域
本发明涉及YKL-40浓度检测领域,具体而言,涉及抗体组合物及应用、检测血液中YKL-40浓度的方法。
背景技术
长期以来,癌症是危及全世界人类健康最主要的疾病之一,全球每年近1900万人确诊为癌症患者,每年癌症死亡率是960万人。因此,如何精准诊断、有效治疗肿瘤是拯待急需解决的问题。在临床诊断癌症时,除了病人出现的体症外,最重要的诊断一环就是肿瘤的检测,包括损伤性与非损伤性检测;前者有肿瘤活检、X-射线等;后者有血液、尿液、消化道分泌液等。随着高端科技的迅猛发展,尤其分子和基因检测技术的不断提升;近20年来,对肿瘤病人血液中的细胞、蛋白、DNA等检测进行了各种尝试,并获得一些成就。对肿瘤病人的血液高表达蛋白有了许多报道,提出检测血液蛋白可以作为诊断癌症病人的标记物,比如CA125、CA19-9等抗原蛋白。但是,目前在临床上公认为肿瘤的血液标记物,能体现肿瘤在体内的存在或进展,却十分有限。所以,研发检测血液蛋白的试剂盒对肿瘤的诊断有着重要的临床价值,对指示早期治疗也有着深远意义。
YKL-40(基因名为CHI3L1)是分泌性糖蛋白,其分子由383个氨基酸构成(40KDa),属几丁质酶基因家族。临床报道YKL-40的表达与多种肿瘤恶变有显著的正相关;例如转移性乳腺癌、直肠癌、肝癌、肺癌、胰腺癌、子宫颈癌、恶性胶质母细胞等多种实体瘤,患者的血浓度YKL-40是显著上升;而且,高浓度YKL-40与肿瘤转移和患者低存活率是密切相关的,提示YKL-40是肿瘤恶变的标志物。其病理机制是与肿瘤血管再生相关;能刺激乳腺癌、直肠癌、脑肿瘤等肿瘤的血管再生,从而促进肿瘤的繁殖和转移。有文献报道,正常人血液YKL-40浓度维持在约50纳克/毫升(ng/ml),而肿瘤病人升高到100纳克/毫升以上,甚至达到200-300纳克/毫升。因此,在癌症病人的诊断中,检测血液YKL-40的浓度受到越来越多的关注。
目前,生产检测YKL-40的试剂盒的企业,均分布于美国,每个试剂盒价格在600-1000美元,含有一个96孔板,可以检测25个样本(每个样本3次重复)。如果检测100例或更大规模病人筛选,昂贵的费用对开展临床研究,还是病人自己承担的费用都是重要考虑的因素。
有鉴于此,特提出本发明。
发明内容
本发明的一个方面,涉及抗体组合物,包括以下组分:
YKL-40重组蛋白、抗YKL-40鼠源单抗、抗YKL-40兔源多抗、山羊抗体共轭辣根过氧化酶、3,3’,5,5’-四甲基联苯胺和硫酸。
所述抗体组合物的组分与YKL-40能特异的结合和反应,可用于检测血液中YKL-40浓度,特异性高,灵敏性高,检测成本低,有利于临床病人的诊断。
本发明的另一个方面,还涉及试剂盒,包括所述的抗体组合物。
本发明的另一个方面,还涉及检测血液中YKL-40浓度的方法,使用所述的抗体组合物或所述的试剂盒,包括以下步骤:
a、将抗YKL-40鼠源单抗加入至96孔板后3~5℃过夜;移去所述96孔板中的所述抗YKL-40鼠源单抗,冲洗所述96孔板;
b、向所述96孔板中加入待测血液样本,于3~5℃冰箱过夜;移去所述96孔板中的所述待测血液样本,冲洗所述96孔板;
c、向所述96孔板中加入抗YKL-40兔源性多抗,于3~5℃静置过夜;移去所述96孔板中的所述抗YKL-40兔源性多抗,冲洗所述96孔板;
d、向所述96孔板中加入山羊抗体共轭辣根过氧化酶,室温放置1.5~2.5h;移去所述96孔板中的所述山羊抗体共轭辣根过氧化酶,向所述96孔板中加入3,3’,5,5’-四甲基联苯胺,进行震荡培养;
e、向所述震荡培养结束后的培养体系中加入硫酸,在450nm波长处检测加入所述硫酸后培养体系的吸光度;
f、利用YKL-40重组蛋白制作YKL-40浓度与吸光度相关的标准曲线。
所述检测血液中YKL-40浓度的方法,使用所述的抗体组合物,该方法的灵敏性高,检测成本低,有利于临床病人的诊断。
与现有技术相比,本发明的有益效果为:
(1)本发明提供的抗体组合物,包括YKL-40重组蛋白、抗YKL-40鼠源单抗、抗YKL-40兔源多抗、山羊抗体共轭辣根过氧化酶和3,3’,5,5’-四甲基联苯胺,以上组分与YKL-40能特异的结合和反应,可用于检测血液中YKL-40浓度,特异性高,灵敏性高,检测成本低,有利于临床病人的诊断。
(2)本发明提供的检测血液中YKL-40浓度的方法,使用所述的抗体组合物,该方法的灵敏性高,检测成本低,有利于临床病人的诊断。
(3)本发明提供的试剂盒,使用所述的抗体组合物,可用于检测血液中YKL-40浓度,特异性高,灵敏性高,检测成本低,有利于临床病人的诊断。
附图说明
为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
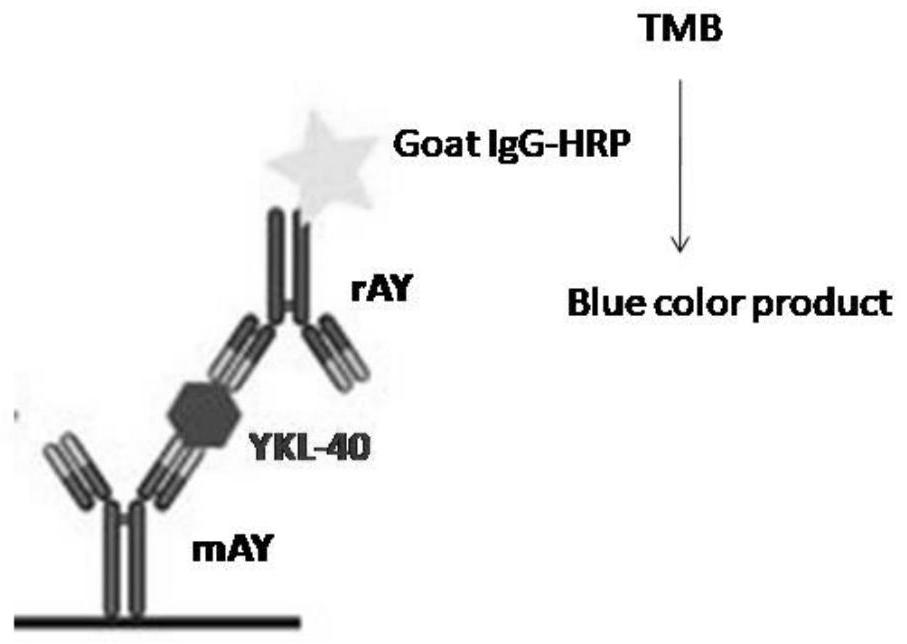
图1为抗体组合物检测YKL-40的原理示意图。
具体实施方式
下面将结合附图和具体实施方式对本发明的技术方案进行清楚、完整地描述,但是本领域技术人员将会理解,下列所描述的实施例是本发明一部分实施例,而不是全部的实施例,仅用于说明本发明,而不应视为限制本发明的范围。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
本发明的一个方面,涉及抗体组合物,包括以下组分:
YKL-40重组蛋白、抗YKL-40鼠源单抗、抗YKL-40兔源多抗、山羊抗体共轭辣根过氧化酶、3,3’,5,5’-四甲基联苯胺和硫酸。
所述的抗体组合物的组分与YKL-40能特异的结合和反应,可用于检测血液中YKL-40浓度,特异性高,灵敏性高,检测成本低,有利于临床病人的诊断。
该抗体组合物不仅仅局限于肿瘤病人血清YKL-40的检测,它也可用于多种疾病的病人,只要病人血液或分泌液(比如尿液、关节液,腹水等)YKL-40是升高的都可以纳入检测范围。因为,最近越来越多的研究表明有多种人类疾病产生高血液浓度的YKL-40,包括老年性痴呆(AD)、慢性关节炎、肠道炎症、II型糖尿病等。因此,该抗体组合物对多种疾病的诊断有着广泛的前景和显著的经济效益。
该抗体组合物检测YKL-40的原理如图1所示,抗YKL-40鼠源单抗(mAY,棕色)先黏附于96孔板,然后加入含有YKL-40的血清样本(红色),再引入抗YKL-40兔源多抗(rAY,蓝色),最后加山羊抗体共轭辣根过氧化酶和反应底物,检测产物的吸光度。
优选地,所述YKL-40重组蛋白的制备方法包括以下步骤:
将YKL-40全基因序列(DNA)引入到pFAST-BAC1质粒(Bac-to-Bac系统,ThermoFisher公司)中,然后,引入杆状病毒质粒,产生杆状病毒传染于昆虫Sf9细胞,收集分泌YKL-40蛋白的细胞上清液,在所述收集分泌YKL-40蛋白的细胞上清液中分离、纯化得到所述YKL-40重组蛋白。
优选地,所述抗YKL-40鼠源单抗的制备方法包括以下步骤:
将所述YKL-40重组蛋白注射于小鼠,分离所述小鼠脾脏的免疫B细胞,然后与小鼠淋巴瘤的腹水肿瘤细胞进行杂交培养,筛选能产生与YKL-40蛋白特异结合的抗体杂交瘤细胞,培养并收集所述抗体杂交瘤细胞的上清液,在所述抗体杂交瘤细胞的上清液中分离、纯化得到所述抗YKL-40鼠源单抗。抗YKL-40鼠源单抗可来自于本申请人实验室杂交瘤细胞培养后收集。
优选地,所述抗YKL-40兔源多抗的制备方法包括以下步骤:
将所述YKL-40重组蛋白C末端的肽段注射于兔的血液中,收集所述2个兔的血清;4周后,每周从兔耳收取血清,共收集50~100mL,用分离血清蛋白IgG的试剂盒(BioRad产品),从所述兔的血清中分离、纯化得到所述抗YKL-40兔源多抗。
优选地,由C端至N端,所述YKL-40重组蛋白C末端的肽段包括:CGQDLRFPLTNAIKDALAAT。
优选地,所述抗YKL-40鼠源单抗的浓度为0.3~1.0mg/ml(例如0.3mg/ml、0.5mg/ml、0.8mg/ml或1.0mg/ml)。
优选地,所述抗YKL-40兔源性多抗的浓度为0.3~1.0mg/ml(例如0.3mg/ml、0.5mg/ml、0.8mg/ml或1.0mg/ml)。
优选地,所述山羊抗体共轭辣根过氧化酶的浓度为0.5~0.8mg/ml(例如0.5mg/ml、0.6mg/ml、0.7mg/ml或0.8mg/ml)。可从Thermofisher公司购置。
优选地,所述3,3’,5,5’-四甲基联苯胺在0.05M磷酸-柠檬酸盐缓冲液(pH为5.0)中的浓度为0.2-0.4mM(例如0.2mM、0.3mM或0.4mM)。可从Merk/Sigma公司购置。
优选地,所述硫酸的浓度为1.8~2.2M(例如1.8M、1.9M、2.0M、2.1M或2.2M)。
本发明的另一个方面,还涉及试剂盒,包括所述的抗体组合物。
所述试剂盒,使用所述的抗体组合物,可用于检测血液中YKL-40浓度,特异性高,灵敏性高,检测成本低,有利于临床病人的诊断。
本发明的另一个方面,还涉及检测血液中YKL-40浓度的方法,使用所述的抗体组合物,包括以下步骤:
a、将抗YKL-40鼠源单抗加入至96孔板后3~5℃过夜;移去所述96孔板中的所述抗YKL-40鼠源单抗,冲洗所述96孔板;洗完后可以保存在4℃冰箱4周或-20℃冰箱6个月;
b、向所述96孔板中加入待测血液样本,于3~5℃冰箱过夜;移去所述96孔板中的所述待测血液样本,冲洗所述96孔板;
c、向所述96孔板中加入抗YKL-40兔源性多抗,于3~5℃静置过夜;移去所述96孔板中的所述抗YKL-40兔源性多抗,冲洗所述96孔板;
d、向所述96孔板中加入山羊抗体共轭辣根过氧化酶,室温放置1.5~2.5h(例如1.5h、1.7h、1.9h、2.0h、2.1h、2.3h或2.5h);移去所述96孔板中的所述山羊抗体共轭辣根过氧化酶,向所述96孔板中加入3,3’,5,5’-四甲基联苯胺,进行震荡培养;
e、向所述震荡培养结束后的培养体系中加入硫酸,在450nm波长处检测加入所述硫酸后培养体系的吸光度;
f、利用YKL-40重组蛋白制作YKL-40浓度与吸光度相关的标准曲线。
所述的检测血液中YKL-40浓度的方法,使用所述的抗体组合物,该方法的灵敏性高,检测成本低,有利于临床病人的诊断。
优选地,所述抗YKL-40鼠源单抗的浓度为0.3~1.0mg/ml(例如0.3mg/ml、0.5mg/ml、0.8mg/ml或1.0mg/ml)。
优选地,所述抗YKL-40兔源性多抗的浓度为0.3~1.0mg/ml(例如0.3mg/ml、0.5mg/ml、0.8mg/ml或1.0mg/ml)。
优选地,所述山羊抗体共轭辣根过氧化酶的浓度为0.5~0.8mg/ml(例如0.5mg/ml、0.6mg/ml、0.7mg/ml或0.8mg/ml)。
优选地,所述3,3’,5,5’-四甲基联苯胺在0.05M磷酸-柠檬酸盐缓冲液(pH为5.0)中的浓度为0.2-0.4mM(例如0.2mM、0.3mM或0.4mM)。
优选地,所述硫酸的浓度为1.8~2.2M(例如1.8M、1.9M、2.0M、2.1M或2.2M)。
优选地,所述抗YKL-40鼠源单抗、所述待测血液样本和所述抗YKL-40兔源性多抗的体积比为50:90~110:45~55(例如50:90:55、50:100:53、50:105:50或50:110:45);
和/或,所述抗YKL-40鼠源单抗、所述山羊抗体共轭辣根过氧化酶、所述3,3’,5,5’-四甲基联苯胺的体积比为50:45~55:95~105(例如50:45:105、50:48:102、50:50:98或50:55:95);
和/或,所述抗YKL-40鼠源单抗和所述硫酸的体积比为50:8~12(例如50:8、50:10、50:11或50:12)。
优选地,所述震荡培养的时间为13~17min(例如13min、14min、15min、16min或17min)。
优选地,所述震荡培养在摇床上进行,所述摇床的频率为110~130rpm/min(例如110rpm/min、115rpm/min、120rpm/min、125rpm/min或130rpm/min)。
下面将结合具体的实施例和对比例对本发明的实施方案进行详细描述。
实施例1
本实施例提供的检测血液中YKL-40浓度的方法,包括以下步骤:
a、首先,抗YKL-40鼠源单抗以1:500稀释(抗体浓度0.5毫克/毫升,mg/ml)制备;在96孔板上加入抗YKL-40鼠源单抗50微升,将该孔板放置于4℃冰箱过夜;之后,移去抗体,用100微升PBS(磷酸缓冲液)洗孔板;
b、加入病人血清样本100微升,再放置于4℃冰箱过夜;吸取血清,用100微升PBS洗孔板三次;然后,加入抗YKL-40兔源多抗50微升(以1:250稀释,抗体浓度0.5mg/ml),再放置于4℃冰箱过夜;
c、移去抗体,清洗孔板,然后加入山羊识别兔源IgG的抗体50微升以1:1000稀释,为市场上购买;该山羊抗体是共轭辣根过氧化酶(horseradish peroxidase,HRP),在96孔板中放置于室温2小时;移去该抗体后,加入反应底物3,3’,5,5’-四甲基联苯胺(3,3’,5,5’-Tetramethylbenzidine,TMB)100μl(临时制备),放置于室温摇床(120转/分钟)15分钟;加入10μl 2M的H
d、分别配制浓度为0ng/ml、25ng/ml、50ng/ml、100ng/ml、200ng/ml、400ng/ml的标准YKL-40重组蛋白溶液,检测YKL-40重组蛋白不同浓度对应的吸光度,相应的吸光值分别为0、0.22、0.48、0.95、1.60、2.58,得到YKL-40蛋白浓度与吸光度相关的标准曲线,相关性r=0.989;根据血清样本检测到的吸光值,计算出样本中的YKL-40浓度。
实施例2
本实施例提供的检测血液中YKL-40浓度的方法,包括以下步骤:
a、同实施例1;
b、加入病人血清样本90微升,再放置于4℃冰箱过夜;吸取血清,用100微升PBS洗孔板三次;然后,加入抗YKL-40兔源多抗55微升(以1:250稀释,抗体浓度0.5mg/ml),再放置于4℃冰箱过夜;
c、移去抗体,清洗孔板,然后加入山羊识别兔源IgG的抗体45微升以1:1000稀释,为市场上购买;该山羊抗体是共轭辣根过氧化酶(horseradish peroxidase,HRP),在96孔板中放置于室温2.5小时;移去该抗体后,加入反应底物3,3’,5,5’-四甲基联苯胺(3,3’,5,5’-Tetramethylbenzidine,TMB)105μl(临时制备),放置于室温摇床(120转/分钟)15分钟;加入8μl 2M的H
d、分别配制浓度为0ng/ml、25ng/ml、50ng/ml、100ng/ml、200ng/ml、400ng/ml的标准YKL-40重组蛋白溶液,检测YKL-40重组蛋白不同浓度对应的吸光度,相应的吸光值分别为0、0.20、0.45、1.05、1.58、2.45,得到YKL-40蛋白浓度与吸光度相关的标准曲线,相关性r=0.979。
实施例3
本实施例提供的检测血液中YKL-40浓度的方法,包括以下步骤:
a、同实施例1;
b、加入病人血清样本110微升,再放置于4℃冰箱过夜;吸取血清,用100微升PBS洗孔板三次;然后,加入抗YKL-40兔源多抗45微升(以1:250稀释,抗体浓度0.5mg/ml),再放置于4℃冰箱过夜;
c、移去抗体,清洗孔板,然后加入山羊识别兔源IgG的抗体55微升以1:1000稀释,为市场上购买;该山羊抗体是共轭辣根过氧化酶(horseradish peroxidase,HRP),在96孔板中放置于室温1.5小时;移去该抗体后,加入反应底物3,3’,5,5’-四甲基联苯胺(3,3’,5,5’-Tetramethylbenzidine,TMB)95μl(临时制备),放置于室温摇床(120转/分钟)15分钟;加入12μl 2M的H
d、分别配制浓度为0ng/ml、25ng/ml、50ng/ml、100ng/ml、200ng/ml、400ng/ml的标准YKL-40重组蛋白溶液,检测YKL-40重组蛋白不同浓度对应的吸光度,相应的吸光值分别为0、0.18、0.40、0.96、1.98、2.55,得到YKL-40蛋白浓度与吸光度相关的标准曲线,相关性r=0.963;根据血清样本检测到的吸光值,计算出样本中的YKL-40浓度。
实施例4
本实施例提供的检测血液中YKL-40浓度的方法,步骤c,摇床频率为130转/分钟,震荡时间为13分钟;步骤d,分别配制浓度为0ng/ml、25ng/ml、50ng/ml、100ng/ml、200ng/ml、400ng/ml的标准YKL-40重组蛋白溶液,检测YKL-40重组蛋白不同浓度对应的吸光度,相应的吸光值分别为0、0.21、0.38、0.85、1.88、2.35,得到YKL-40蛋白浓度与吸光度相关的标准曲线,相关性r=0.960;根据血清样本检测到的吸光值,计算出样本中的YKL-40浓度;其他同实施例1。
实施例5
本实施例提供的检测血液中YKL-40浓度的方法,步骤c,摇床频率为110转/分钟,震荡时间为17分钟;步骤d,分别配制浓度为0ng/ml、25ng/ml、50ng/ml、100ng/ml、200ng/ml、400ng/ml的标准YKL-40重组蛋白溶液,检测YKL-40重组蛋白不同浓度对应的吸光度,相应的吸光值分别为0、0.24、0.55、1.01、1.98、2.85,得到YKL-40蛋白浓度与吸光度相关的标准曲线,相关性r=0.981;根据血清样本检测到的吸光值,计算出样本中的YKL-40浓度;其他同实施例1。
对比例1
本对比例与实施例1的区别仅在于步骤c,山羊抗体共轭辣根过氧化酶在96孔板中放置于室温3小时。
对比例2
本对比例与实施例1的区别仅在于步骤c,摇床频率为140转/分钟,震荡时间为10分钟。
实验例
检测1例高YKL-40表达的癌症病人的血液样本,已知该血液样本的浓度为162ng/ml,利用本发明提供的实施例和对比例提供的检测血液中YKL-40浓度的方法对该血液样本进行检测,得到的检测结果见表1。
表1
从表1中数据可看出使用含有抗体组合物的试剂盒,检测血液中YKL-40浓度的检测结果准确,特异性高,灵敏性高,检测成本低,有利于临床病人的诊断。
尽管已用具体实施例来说明和描述了本发明,然而应意识到,以上各实施例仅用以说明本发明的技术方案,而非对其限制;本领域的普通技术人员应当理解:在不背离本发明的精神和范围的情况下,可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围;因此,这意味着在所附权利要求中包括属于本发明范围内的所有这些替换和修改。
