β-氨基酸衍生物、含其之激酶抑制剂与医药组合物以及其用途
文献发布时间:2023-06-19 11:54:11
技术领域
本揭露系关于一种新颖之化合物,且特别是关于一种新颖之β-氨基酸衍 生物、含其之激酶抑制剂与医药组合物以及其用途。
背景技术
为了将眼球维持在一定的形状,以保持眼睛光学功能及新陈代谢,睫状 体会分泌房水来执行这个工作。当房水排出的通路受阻、蓄积,就会造成眼 压的升高,而眼压是青光眼最重要的风险因素。
目前已知房水引流主要通过以下三种途径:(1)Schlemm管路径(最主要(conventional pathway));(2)葡萄膜-巩膜路径(少量),约10%-20%;(3)虹 膜表面吸收(微量)。而目前常用青光眼药物的降眼压机制为:(a)减少房 水生成,如β受体阻滞剂、碳酸酐酶抑制剂、α受体激动剂等;(b)增加房水 排出(葡萄膜巩膜途径),如摄护腺素类似物、α受体激动剂等。
Rho/ROCK途径在细胞骨架的调节方面扮演重要角色。Rho/ROCK抑制 剂可以通过调节小梁网组织中肌动蛋白细胞骨架、细胞外基质以及 Schlemm’s管内皮细胞的功能,进而达成降低眼压之目的。
当前,一些医药公司已开始探索ROCK抑制剂对人体中降眼压的影响, 并相继研发新药物。在评估人体临床安全性与有效性后,目前市售ROCK抑 制剂之降眼压药物包括Ripasudil(K-115)与Netarsudil(AR-13324)等。在 Ripasudil III期临床试验中发现,轻度结膜充血为最常见的不良反应,其发生 率高达75%,且结膜炎、点状角膜炎等也有发生。Netarsudil(AR-13324)为 ROCK/去甲肾上腺素转运蛋白(norepinephrine transporter,NET)抑制剂化合 物,除了作为ROCK抑制剂的作用外,还有抑制去甲肾上腺素的作用,具有持续降眼压的作用,并且局部耐受性好,但其仍有结膜充血反应。此外, Netarsudil(AR-13324)在临床三期试验ROCKET1、ROCKET2(总计1,167位 病患)对眼压>25mmHg的青光眼病患之药效不如青光眼常规治疗药物 Timolol,在<25mmHg的病患则是药效与Timolol相当。
基于目前已知ROCK抑制剂在应用于降低眼压仍存在各种不同的副作 用,以及长期使用单一机制药物可能衍生药效降低问题,使得病人无法长期 使用单一种药物,因此目前仍亟需开发具有新标靶或多标靶之新颖降眼压药 物,以达成有效降低眼压并减少副作用之效果。
发明内容
本揭露提供一种式(I)所示之化合物或其药学上可接受之盐或酯(ester)、 水合物(hydrate)、溶剂合物(solvate)或结晶物(crystalline form):
本揭露也提供一种激酶抑制剂,包括上述式(I)所示之化合物或其药学上 可接受之盐或酯、水合物、溶剂合物或结晶物。
本揭露还提供一种医药组合物,包括一有效量之上述式(I)所示之化合物 或其药学上可接受之盐或酯、水合物、溶剂合物或结晶物。
又,本揭露提供一种上述式(I)所示之化合物或其药学上可接受之盐或 酯、水合物、溶剂合物或结晶物作为激酶抑制剂之用途。
本揭露也提供一种上述式(I)所示之化合物或其药学上可接受之盐或酯、 水合物、溶剂合物或结晶物用于制备一药物之用途,其中该药物系用于受益 于一激酶之抑制的一体内相关应用,且该激酶系择自由以下所组成之群组的 至少一个:Rho相关的蛋白激酶(Rho-associated protein kinase,ROCK)、肌凝 蛋白轻链激酶-4(myosin light chainkinase 4,MYLK-4)、与有丝分裂原活化蛋 白激酶-19(mitogen-activated proteinkinase 19,MAPK19,YSK-4)。
此外,本揭露更提供一种上述式(I)所示之化合物或其药学上可接受之盐 或酯、水合物、溶剂合物或结晶物之用途,其系用于制备降低眼压之药物。
为了让本发明之上述和其他目的、特征、和优点能更明显易懂,下文特 举较佳实施例,并配合所附图示,作详细说明如下:
附图说明
第1A图显示,在正常眼压兔眼中,不同浓度之本揭露之化合物于第1天 投药之眼压测定结果。
第1B图显示,在正常眼压兔眼中,不同浓度之本揭露之化合物于第3天 投药之眼压测定结果。
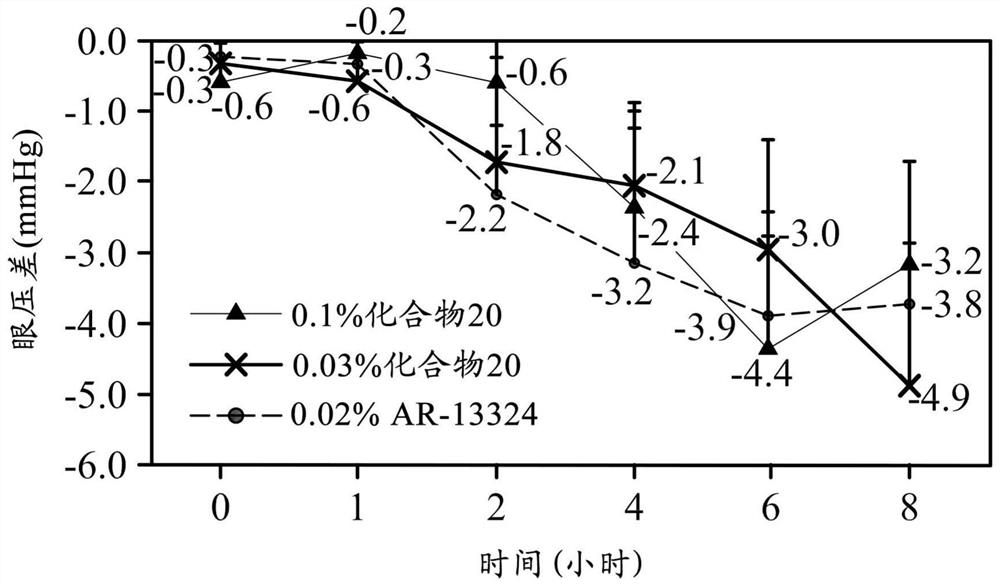
第2图显示,在正常眼压兔眼中,本揭露之化合物与市售药物的降眼压 功效。
第3A图显示,本揭露之化合物与市售药物之眼刺激评估的分数。
第3B图显示,于眼刺激评估中,以本揭露之化合物与市售药物处理之兔 眼的照片。
第3C图显示,于眼刺激评估中,以本揭露之化合物连续投药7天之兔眼, 角膜无呈现混浊受损的照片。
第4图显示,在正常眼压兔眼中,本揭露之化合物之药物浓度在标的组 织8小时内均达到标靶作用药效IC
第5图显示,在正常眼压兔眼中,本揭露之化合物之安全边际(safety margin)测试的结果。
第6图显示,在正常眼压猕猴中,本揭露之化合物与市售药物的降眼压 功效。
第7图显示,在高渗透压食盐水诱导高眼压兔眼中,本揭露之化合物与 市售药物的降眼压功效。*:t-test,p-value<0.05(相较于生理食盐水);#: t-test,p-value<0.05(相较于载剂);φ:t-test,p-value<0.05(相较于市 售药物(AR-13324))。
第8图显示,在磁珠诱导高眼压兔眼中,本揭露之化合物与市售药物的 降眼压功效。
第9图显示,在磁珠诱导高眼压兔眼中,肌凝蛋白轻链激酶-4(myosin lightchain kinase 4,MYLK-4)之表现。
第10图显示,磁珠诱导高眼压兔眼之组织切片的免疫组织化学染色。
实施方式
本揭露提供一种新颖之β氨基酸衍生物,并同时提供此新颖之β氨基酸衍 生物之药学上可接受之盐或酯、水合物、溶剂合物或结晶物。
上述本揭露之新颖之β氨基酸衍生物,可包括以下式(I)所示之化合物, 但不限于此:
于上方所示之式(I)中,X可为单键或O;Y可为NH或C=O;Z可为C=O、 C=S、NH、
于本揭露中,上述式(I)所示之化合物可以个别光学异构物、个别手性异 构物之混合物或消旋化合物之形式存在,且可包括,但不限于,下方表1中 所示之化合物。
表1、式(I)所示之化合物的例子
在一实施例中,本揭露之式(I)所示之化合物可为上述之化合物7,其为 一消旋化合物(racemic compound)。在另一实施例中,本揭露之式(I)所示之化 合物可为上述之化合物20,其为一S型化合物,进一步言之,为一S型镜像异 构物(S-Enantiomer)。
在一实施例中,上述本揭露之新颖之β氨基酸衍生物或此新颖之β氨基酸 衍生物之药学上可接受之盐或酯、水合物、溶剂合物或结晶物,可具有抑制 一激酶的功效,但不限于此。上述激酶的例子可包括,但不限于,肌凝蛋白 轻链激酶-4(myosin light chainkinase 4,MYLK-4)、有丝分裂原活化蛋白激酶 -19(mitogen-activated protein kinase19,MAPK19,YSK-4)、Rho相关的蛋白激 酶(Rho-associated protein kinase,ROCK)或上述之任意组合。Rho相关的蛋白 激酶则可包括,但不限于,Rho相关的蛋白激酶-1(Rho-associated protein kinase-1,ROCK-1)。
在一实施例中,上述本揭露之新颖之β氨基酸衍生物或此新颖之β氨基酸 衍生物之药学上可接受之盐或酯、水合物、溶剂合物或结晶物,可具有抑制 肌凝蛋白轻链激酶-4的功效。
又,上述本揭露之新颖之β氨基酸衍生物或此新颖之β氨基酸衍生物之药 学上可接受之盐或酯、水合物、溶剂合物或结晶物也可具有加成性标靶抑制 作用。因此,在另一实施例中,上述本揭露之新颖之β氨基酸衍生物或此新 颖之β氨基酸衍生物之药学上可接受之盐或酯、水合物、溶剂合物或结晶物, 可具有抑制有丝分裂原活化蛋白激酶-19的功效。
又,在另一实施例中,上述本揭露之新颖之β氨基酸衍生物或此新颖之β 氨基酸衍生物之药学上可接受之盐或酯、水合物、溶剂合物或结晶物,可具 有同时抑制肌凝蛋白轻链激酶-4与Rho相关的蛋白激酶的功效。
又,在另一实施例中,上述本揭露之新颖之β氨基酸衍生物或此新颖之β 氨基酸衍生物之药学上可接受之盐或酯、水合物、溶剂合物或结晶物,可具 有同时抑制有丝分裂原活化蛋白激酶-19与Rho相关的蛋白激酶的功效。
此外,在另一实施例中,上述本揭露之新颖之β氨基酸衍生物或此新颖 之β氨基酸衍生物之药学上可接受之盐或酯、水合物、溶剂合物或结晶物, 可具有同时抑制肌凝蛋白轻链激酶-4、有丝分裂原活化蛋白激酶-19与Rho相 关的蛋白激酶的功效。
在另一实施例中,上述本揭露之新颖之β氨基酸衍生物或此新颖之β氨基 酸衍生物之药学上可接受之盐或酯、水合物、溶剂合物或结晶物,可具有降 低眼压之功效。在一特定实施例中,上述本揭露之新颖之β氨基酸衍生物或 此新颖之β氨基酸衍生物之药学上可接受之盐或酯、水合物、溶剂合物或结 晶物可经由肌凝蛋白轻链激酶-4、有丝分裂原活化蛋白激酶-19、Rho相关的 蛋白激酶或上述之任意组合而达成降低眼压之功效。
由于上述本揭露之新颖之β氨基酸衍生物或此新颖之β氨基酸衍生物之 药学上可接受之盐或酯、水合物、溶剂合物或结晶物,可具有降低眼压之功 效,因此其可应用于一高眼压症(ocular hypertension)或一具有高眼压症之疾 病的治疗及/或预防。上述高眼压症系指眼压大于正常范围的症状。例如,人 类正常眼压为约10-21mmHg,高眼压症为眼压大于约21mmHg的症状,如 大于约22mmHg、大于约25mmHg、大于约30mmHg等,但不限于此。
在一实施例中,上述本揭露之新颖之β氨基酸衍生物或此新颖之β氨基酸 衍生物之药学上可接受之盐或酯、水合物、溶剂合物或结晶物,可应用于眼 压大于约25mmHg,如大于约30mmHg之高眼压症的治疗及/或预防。
基于前述,本揭露也提供一种激酶抑制剂,其可包括任何上述本揭露之 新颖之β氨基酸衍生物或此新颖之β氨基酸衍生物之药学上可接受之盐或酯、 水合物、溶剂合物或结晶物,但不限于此。
于本揭露之激酶抑制剂中,上述本揭露之新颖之β氨基酸衍生物或此新 颖之β氨基酸衍生物之药学上可接受之盐或酯、水合物、溶剂合物或结晶物, 可具有抑制一激酶的功效,而于此所述之激酶可包括,但不限于,肌凝蛋白 轻链激酶-4、有丝分裂原活化蛋白激酶-19、Rho相关的蛋白激酶或上述之任 意组合。Rho相关的蛋白激酶则可包括,但不限于,Rho相关的蛋白激酶-1。
于本揭露之激酶抑制剂中,在一实施例中,上述本揭露之新颖之β氨基 酸衍生物或此新颖之β氨基酸衍生物之药学上可接受之盐或酯、水合物、溶 剂合物或结晶物,可具有抑制肌凝蛋白轻链激酶-4及/或有丝分裂原活化蛋白 激酶-19之功效。于本揭露之激酶抑制剂中,在另一实施例中,上述本揭露 之新颖之β氨基酸衍生物或此新颖之β氨基酸衍生物之药学上可接受之盐或 酯、水合物、溶剂合物或结晶物,除了抑制肌凝蛋白轻链激酶-4及/或有丝分 裂原活化蛋白激酶-19之功效外,还可具有抑制Rho相关的蛋白激酶的功效。
在一实施例中,本揭露之激酶抑制剂可包括上述化合物7(其为一消旋 化合物)或化合物20(其为一S型化合物)。于此特定实施例中,本揭露之 激酶抑制剂可具有同时抑制肌凝蛋白轻链激酶-4、有丝分裂原活化蛋白激酶 -19与Rho相关的蛋白激酶的功效。
此外,基于前述,本揭露也可提供一种任何上述本揭露之新颖之β氨基 酸衍生物或此新颖之β氨基酸衍生物之药学上可接受之盐或酯、水合物、溶 剂合物或结晶物作为激酶抑制剂之用途。
而于本揭露之此用途中,关于上述本揭露之新颖之β氨基酸衍生物或此 新颖之β氨基酸衍生物之药学上可接受之盐或酯、水合物、溶剂合物或结晶 物的激酶抑制功效相关说明同前方所述,因此不于此赘述。
于本揭露之此用途中,在一特定实施例中,上述本揭露之新颖之β氨基 酸衍生物,可为上述化合物7(其为一消旋化合物)或化合物20(其为一S型 化合物)。于此特定实施例中,前述激酶抑制剂可具有同时抑制肌凝蛋白轻 链激酶-4、有丝分裂原活化蛋白激酶-19与Rho相关的蛋白激酶的功效。
此外,本揭露还提供一种医药组合物,其可包括,但不限于,任何上述 本揭露之新颖之β氨基酸衍生物或此新颖之β氨基酸衍生物之药学上可接受 之盐或酯、水合物、溶剂合物或结晶物。
而于本揭露之医药组合物中,关于上述本揭露之新颖之β氨基酸衍生物 或此新颖之β氨基酸衍生物之药学上可接受之盐或酯、水合物、溶剂合物或 结晶物的所有相关叙述同前方所述,因此不于此赘述。
在一实施例中,本揭露之医药组合物可包括上述化合物7,其为一消旋 化合物。在另一实施例中,本揭露之医药组合物可包括上述化合物20,其为 一S型化合物。
又,在一实施例中,上述本揭露之医药组合物,还可包括一药学上可接 受之载体或盐类,但不限于此。
上述药学上可接受之载体可包括,但不限于溶剂、分散媒(dispersion medium)、套膜(coating)、抗菌与抗真菌试剂与一等渗透压与吸收延迟 (absorption delaying)试剂等与药学投予相容者。对于不同的给药方式,可利 用一般方法将药学组合物配制成剂型(dosage form)。
又,上述药学上可接受之盐类可包括,但不限于盐类包括无机阳离子, 例如,碱金属盐类,如钠、钾或胺盐,碱土金族盐类,如镁、钙盐,含二价 或四价阳离子之盐类,如锌、铝或锆盐。此外,也可是为有机盐类,如二环 己胺盐类、甲基-D-葡糖胺,氨基酸盐类,如精胺酸、离胺酸、组织胺酸、 麸胺酸酰胺。
再者,本揭露之医药组合物可被投予至一需要此医药组合物之一个体, 但不限于此。而本揭露之医药组合物的给药途径可包括非口服、口服、经由 吸入喷雾(inhalationspray)或藉由植入贮存器(implanted reservoir)的方式,但 不限于此。非口服可包括,但不限于,涂擦患部、皮下(subcutaneous)、皮内 (intracutaneous)、静脉内(intravenous)、肌肉内(intramuscular)、关节内 (intraarticular)动脉(intraarterial)、滑囊(腔)内(intrasynovial)、胸骨内 (intrasternal)、蜘蛛膜下腔(intrathecal)、疾病部位内(intralesional)注射、眼部 外用(external ophthalmic use)、眼内注射(intraocular)以及灌注技术等。
而涂擦之局部使用的形式可包括软膏、乳剂、液剂、凝胶等,但不限于 此。又,眼部外用之使用的形式可包括,但不限于,眼用滴剂、眼用软膏、 眼用凝胶等。
此外,上述需要被投予此医药组合物之个体可包括,但不限于,一脊椎 动物。又,上述脊椎动物可包括鱼类、两栖类、爬虫类、鸟类或哺乳类,但 不限于此。哺乳类的例子可包括,但不限于,人类、猩猩、猴子、马、驴、 狗、猫、兔子、天竺鼠、大鼠与小鼠。在一实施例中,上述个体可为人类。
在一实施例中,上述本揭露之医药组合物可用于受益于任一激酶抑制任 一体内(in vivo)相关应用,例如受益于任一激酶之抑制任一疾病或病征的治 疗及/或预防,而于此所述之激酶的例子,可包括,但不限于,肌凝蛋白轻链 激酶-4、有丝分裂原活化蛋白激酶-19、Rho相关的蛋白激酶或上述之任意组 合。
又,上述体内相关应用可包括,但不限于,一眼科相关应用及/或肺部相 关应用等。眼科相关应用的例子可包括,视神经的保护,及/或高眼压、青光 眼、眼中风、黄斑部病变、黄斑部水肿、糖尿病视网膜病变、角膜内皮细胞 损伤、角膜纤维化或上述之任意组合的预防及/或治疗等,但不限于此。其中 青光眼可包括剥脱性青光眼(exfoliationglaucoma,XFG)、隅角开放性青光眼 (open angle glaucoma)、隅角闭锁性青光眼(angle-closure glaucoma)、继发型 青光眼(secondary glaucoma)、先天型青光眼(congenitalglaucoma)等,但不限 于此。又,上述肺部相关应用的例子可包括,但不限于,肺动脉高压、慢性 阻塞性肺病(chronic obstructive pulmonary disease,COPD)、病因不明性肺纤维化、肺气肿、肺癌或上述之任意组合等的预防及/或治疗。
此外,本揭露之医药组合物可被调制成一医药制剂,但不限于此。在一 实施例中,本揭露之医药组合物可被调制成一眼用制剂,但不限于此。上述 眼用制剂的例子可包括,但不限于,眼用滴剂、眼用软膏、眼用凝胶、眼内 注射剂等。在一特定实施例中,本揭露之医药组合物可被调制成一眼用滴剂。
此外,本揭露也可提供一种任何上述本揭露之新颖之β氨基酸衍生物或 此新颖之β氨基酸衍生物之药学上可接受之盐或酯、水合物、溶剂合物或结 晶物用于制备一药物之用途,其中上述药物系用于受益于一激酶之抑制的一 体内相关应用。上方所述激酶的例子可包括,但不限于,肌凝蛋白轻链激酶 -4、有丝分裂原活化蛋白激酶-19、Rho相关的蛋白激酶或上述之任意组合。
在一实施例中,于本揭露之上述用途中,所采用为化合物7,其为一消 旋化合物。在一实施例中,于本揭露之上述用途中,所采用为化合物20,其 为一S型化合物。
又于本揭露之上述用途中,上述体内相关应用可包括,但不限于,一眼 科相关应用及/或肺部相关应用等。眼科相关应用的例子可包括,视神经的保 护,及/或高眼压、青光眼、眼中风、黄斑部病变、黄斑部水肿、糖尿病视网 膜病变、角膜内皮细胞损伤、角膜纤维化或上述之任意组合的预防及/或治疗 等,但不限于此。其中青光眼可包括剥脱性青光眼、隅角开放性青光眼、隅 角闭锁性青光眼、继发型青光眼、先天型青光眼等,但不限于此。又,上述 肺部相关应用的例子可包括,但不限于,肺动脉高压、慢性阻塞性肺病、病 因不明性肺纤维化、肺气肿、肺癌或上述之任意组合等的预防及/或治疗。
在一实施例中,于本揭露之上述用途中,上方所述之体内相关应用可为 青光眼的预防及/或治疗。
于本揭露之上述用途中,在另一实施例中,一药学上可接受之载体或盐 类,可与任何上述本揭露之新颖之β氨基酸衍生物或此新颖之β氨基酸衍生物 之药学上可接受之盐或酯、水合物、溶剂合物或结晶物一起制备上述药物。
关于所述之药学上可接受之载体或盐类,可参见前方本揭露之医药组合 物中之药学上可接受之载体或盐类的相关说明,因此不于此赘述。
另外,本揭露也提供一种任何上述本揭露之新颖之β氨基酸衍生物或此 新颖之β氨基酸衍生物之药学上可接受之盐或酯、水合物、溶剂合物或结晶 物用于制备降低眼压的药物的用途。
在一实施例中,于本揭露之上述用途中,所采用为化合物7,其为一消 旋化合物。在一实施例中,于本揭露之上述用途中,所采用为化合物20,其 为一S型化合物。
又,在一实施例中,于上述本揭露之用途中,上述降低眼压之药物可用 于一高眼压症或一具有高眼压症之疾病的治疗及/或预防。而关于所述高眼压 症或具有高眼压症之疾病的相关说明与叙述,可参见前方所述,因此不于此 赘述。
在一实施例中,于上述本揭露之用途中,上述降低眼压之药物可为一青 光眼之治疗药物。而上述青光眼可包括,但不限于,剥脱性青光眼、隅角开 放性青光眼、隅角闭锁性青光眼、继发型青光眼、先天型青光眼等。
又,在一实施例中,于上述本揭露之用途中,上述降低眼压之药物可为 一眼用制剂。而眼用制剂可包括,但不限于,眼用滴剂、眼用软膏、眼用凝 胶、眼内注射剂等。在一特定实施例中,上述降低眼压之药物可为一眼用滴 剂。
于本揭露之上述用途中,在另一实施例中,一药学上可接受之载体或盐 类,可与任何上述本揭露之新颖之β氨基酸衍生物或此新颖之β氨基酸衍生物 之药学上可接受之盐或酯、水合物、溶剂合物或结晶物一起制备上述降低眼 压之药物。
关于所述之药学上可接受之载体或盐类,可参见前方本揭露之医药组合 物中之药学上可接受之载体或盐类的相关说明,因此不于此赘述。
实施例
实施例1
β氨基酸衍生物之合成
1.化合物1与化合物2之合成
化合物1与化合物2之合成方案如以下方案1所示。
方案1
(1)合成例1
在氩气下,对密封管中之1-溴-4-硝基苯(1-bromo-4-nitrobenzene)(210mg,1.04mmol)、1-Boc-4-吡唑硼酸频哪醇酯(1-Boc-4-pyrazoleboronic acid pinacolester)(305mg,1.04mmol)、PdCl
对叔丁基4-(3-(2-(二甲基氨基)乙氧基)-4-硝基苯基)-1H-吡唑(1a)(360 mg)在MeOH(8mL)中的溶液添加10%Pd/C,并将前述反应之混合物于H
将2-叠氮基-3-((叔丁氧基羰基)氨基)丙酸 (2-azido-3-((tert-butoxycarbonyl)amino)propanoic acid)(1.2eq)、HATU(1.5eq) 与DIPEA(2eq)溶解于DMF(0.1M)中,且加入叔丁基-(4-氨基-3-(2-(二甲 基氨基)乙氧基)苯基)-1H-吡唑(1b)(1.0eq),以形成一混合物并于室温搅 拌1小时。以水激发反应,并以EtOAc萃取。收集有机层并以Na
将1,4-二噁烷中之4M HCl(20eq)与4-(4-(2-(2-叠氮基-3-((叔丁氧 基羰基)氨基)丙酰胺基)苯基)-1H-吡唑-1-甲酸叔丁酯(1c)(1eq)于室温 下搅拌1小时。经由过滤收集白色固体,并将其以1,4-二噁烷与DCM清洗。 将白色固体真空干燥以获得N-(4-(1H-吡唑-4-基)苯基)-3-氨基-2-叠氮基 丙酰胺二盐酸盐)(N-(4-(1H-pyrazol-4-yl)phenyl)-3-amino-2-azidopropanamide dihydrochloride)(1)。
(2)合成例2
将叔丁基4-(4-(2-(2-叠氮基-3-((叔丁氧基羰基)氨基)丙酰胺基) 苯基)-1H-吡唑-1-羧酸酯(1c)(1eq)、苯基乙炔(phenyl acetylene)(1.1eq)、硫 酸铜(II)(0.2eq)与(+)-Na-L-抗坏血酸盐((+)-Na-L-ascorbate)(0.2eq)于THF与2-3滴H
化合物2的制备方法与化合物1的制备方法相似。区别在于,化合物叔丁 基4-(4-(2-(2-叠氮基-3-((叔丁氧基羰基)氨基)丙酰胺基)苯基)-1H- 吡唑-1-羧酸酯被置换为化合物叔丁基4-(4-(3-((叔丁氧基羰基)氨基) -2-(4-苯基-1H-1,2,3-三唑-1-基)丙酰胺基)苯基)-1H-吡唑-1-羧酸酯,以 获得产物N-(4-(1H-吡唑-4-基)苯基)-3-氨基-2-(4-苯基-1H-1,2,3-三唑-1- 基)丙烯酰胺二盐酸盐 (N-(4-(1H-pyrazol-4-yl)phenyl)-3-amino-2-(4-phenyl-1H-1,2,3-triazol-1-yl) propenamide dihydrochloride)(2)。
2.化合物3至化合物5之合成
化合物3至化合物5之合成方案如以下方案2所示。
方案2
(3)合成例3
化合物3a的制备方法与化合物1c的制备方法相似。区别在于,化合物2- 叠氮基-3-((叔丁氧基羰基)氨基)丙酸被置换为化合物叔丁基4-(4-(3- (((叔丁氧基羰基)氨基)-2-羟基丙酰胺基)苯基)-1H-吡唑-1-羧酸酯 (tert-butyl 4-(4-(3-((tert-butoxycarbonyl)amino)-2-hydroxypropanamido)phenyl)-1H-pyrazo le-1-carboxylate)(3a)。最终产物N-(4-(1H-吡唑-4-基)苯基)-3-氨基-2-羟 基丙酰胺二盐酸盐 (N-(4-(1H-pyrazol-4-yl)phenyl)-3-amino-2-hydroxypropanamidedihydrochloride)(3)的合成方法与化合物1相似。
(4)合成例4
对10mL THF中之化合物3a(1eq)、苯酚(1eq)与PPh
(5)合成例5
化合物N-(4-(1H-吡唑-4-基)苯基)-3-氨基-2-(4-(三氟甲基)苯氧 基)丙烯酰胺二盐酸盐 (N-(4-(1H-pyrazol-4-yl)phenyl)-3-amino-2-(4-(trifluoromethyl)
phenoxy)propenamide dihydrochloride)(5)的合成方法与化合物4相似。
3.化合物6之合成
化合物6之合成方案如以下方案3所示。
方案3
(6)合成例6
对化合物3a(1eq)在10mL THF中之零度溶液添加NaH(1.5eq)。将前述 混合物于零度下搅拌1小时,之后逐滴加入BnBr(1.5eq)。将前述反应混合物 于室温下搅拌6小时。将反应以水激发并以EtOAc进行萃取。收集有机层并以 Na
最终产物N-(4-(1H-吡唑-4-基)苯基)-3-氨基-2-(苄氧基)丙酰胺二 盐酸盐(N-(4-(1H-pyrazol-4-yl)phenyl)-3-amino-2-(benzyloxy) propanamidedihydrochloride)(6)的合成方法与化合物1相似。
4.化合物7与化合物8之合成
化合物7之合成方案如以下方案4所示。
方案4
(7)合成例7
中间化合物7a与8a的制备方法与化合物1c的制备方法相似。
中间化合物叔丁基4-(4-(3-(((叔丁氧基羰基)氨基)-2-苯基丙酰 胺基)苯基)-1H-吡唑-1-羧酸酯(tert-butyl 4-(4-(3-((tert-butoxycarbonyl)amino)-2-phenylpropanamido)phenyl)-1H-pyrazol e-1-carboxylate)(7a)为白色粉末。
中间化合物叔丁基4-(4-(3-((叔丁氧基羰基)氨基)-2-(4-氟苯基) 丙酰胺基)苯基)-1H-吡唑-1-羧酸酯(tert-butyl 4-(4-(3-((tert-butoxycarbonyl)amino)-2-(4-fluorophenyl)propanamido)phenyl)-1 H-pyrazole-1-carboxylate)(8a)为白色粉末。
最终化合物7与8的制备方法与化合物1的制备方法相似。
最终化合物N-(4-(1H-吡唑-4-基)苯基)-3-氨基-2-苯基丙酰胺二盐酸 盐(N-(4-(1H-pyrazol-4-yl)phenyl)-3-amino-2-phenylpropanamide dihydrochloride)(7)为白色粉末。
最终化合物N-(4-(1H-吡唑-4-基)苯基)-3-氨基-2-(4-氟苯基)丙酰 胺二盐酸盐(N-(4-(1H-pyrazol-4-yl)phenyl)-3-amino-2-(4-fluorophenyl) propanamidedihydrochloride)(8)为白色粉末。
5.化合物9之合成
(8)合成例8
化合物9f之合成方案如以下方案5所示。
方案5
对碘酚(9a)(100g,454.5mmol)在DCM(1000mL)中的溶液添加咪唑 (imidazole)(68g,999.9mmol),然后逐滴加入TIPSC1(87.3g,454.5mmol)。将 前述混合物搅拌16小时,然后倒入冰/水中,以DCM进行萃取。以盐水清洗 有机层,且将其以Na
对化合物9b(140g,372.3mmol)在二噁烷(1500mL)中的溶液添加2-氰基 乙酸乙酯(ethyl 2-cyanoacetate)(63.1g,558.8mmol)、吡啶甲酸(picolinic acid)(13.8g,111.7mmol)、Cs
对化合物9c(22g,60.9mmol)在MeOH/THF(2:1,660mL)中的溶液于 -20℃添加CoCl
对化合物9e(10g,21.5mmol)在EtOH/H
(9)合成例9
化合物9之合成方案如以下方案6所示。
方案6
中间化合物9g的制备方法与化合物1c的制备方法相似。
中间化合物叔丁基4-(4-(3-((叔丁氧基羰基)氨基)-2-(4-((三 异丙基甲硅烷基)氧基)苯基)丙酰胺基)苯基)-1H-吡唑-1-羧酸酯(tert-butyl 4-(4-(3-((tert-butoxycarbonyl)amino)-2-(4-((triisopropylsilyl)oxy)phenyl)propan amido)phenyl)-1H-pyrazole-1-carboxylate)(9g)为白色粉末。
对叔丁基4-(4-(3-((叔丁氧基羰基)氨基)-2-(4-((三异丙基甲 硅烷基)氧基)苯基)丙酰胺基)苯基)-1H-吡唑-1-羧酸酯(9g)(1030mg,1.52 mmol)在THF(10mL)中且经搅拌的溶液添加在THF溶液中之1M TBAF(3.03 mL,3.03mmol)。将所产生之混合物在室温下搅拌1小时。以水激活反应并以 EtOAc进行萃取。收集有机层并以Na
最终化合物9的制备方法与化合物1的制备方法相似。
最终化合物N-(4-(1H-吡唑-4-基)苯基)-3-氨基-2-(4-羟基苯基)丙 酰胺二盐酸盐(N-(4-(1H-pyrazol-4-yl)phenyl)-3-amino-2-(4-hydroxyphenyl) propanamidedihydrochloride)(9)为白色粉末。
6.化合物10之合成
(10)合成例10
化合物10之合成方案如以下方案7所示。
方案7
对叔丁基4-(4-(3-(((叔丁氧基羰基)氨基)-2-(4-羟苯基)丙酰 胺基)苯基)-1H-吡唑-1-羧酸酯(tert-butyl 4-(4-(3-((tert-butoxycarbonyl)amino)-2-(4-hydroxyphenyl)propanamido)phenyl)- 1H-pyrazole-1-carboxylate)(9h)(356mg,0.68mmol)、2,4-二甲基苯甲酸 (2,4-dimethylbenzoic acid)(103mg,0.68mmol)与NEt
于20mL小瓶中装入叔丁基4-(4-(3-((叔丁氧基羰基)氨基)-2-(4- ((2,4-二甲基苯甲酰基)氧基)苯基)丙酰胺基)苯基)-1H-吡唑-1-羧酸 酯(tert-butyl 4-(4-(3-((tert-butoxycarbonyl)amino)-2-(4-((2,4-dimethylbenzoyl)oxy)phenyl)propanamido)phenyl)-1H-pyrazole-1-carboxylate)(10a)(350mg,0.54mmol)与在 二噁烷中之4M HCl溶液(2.7mL)。将所产生之混合物在室温下搅拌1小时。 在减压下移除溶剂以获得所需的化合物4-(1-((4-(1H-吡唑-4-基)苯基) 氨基)-3-氨基-1-氧丙烷-2-基)苯基2,4-二甲基苯甲酸酯二盐酸盐 (4-(1-((4-(1H-pyrazol-4-yl)phenyl)amino)-3-amino-1-oxopropan-2-yl)phenyl 2,4-dimethylbenzoate dihydrochloride)(10),其为白色粉末(271mg,96%)。
7.化合物11之合成
(11)合成例11
化合物11g之合成方案如以下方案8所示。
方案8
对2-(4-(羟甲基)苯基)乙酸(2-(4-(hydroxymethyl)phenyl)acetic acid)(5233mg,31.49mmol)在CH
对甲基2-(4-(羟甲基)苯基)乙酸盐(11b)(5674mg,31.49mmol)在CH
对甲基2-(4-(((三异丙基甲硅烷基)氧基)甲基)苯基)乙酸盐(11c) (10.60g,31.49mmol)在THF(50mL)中之-78℃溶液,逐滴添加LiHMDS (47.30mL,47.23mmol)。于30分钟后,于相同温度逐滴添加在THF(50mL) 中之溴甲基邻苯二甲酰亚胺(bromo-methylphthalimide)(11.34g,47.23 mmol)。移除-78℃冰浴,将溶液回温至室温并搅拌。2小时后,藉由加入 NH
对甲基3-(1,3-二氧代异吲哚啉-2-基)-2-(4-((((三异丙基甲硅烷 基)氧基)甲基)苯基)丙酸酯(11d)(4.39g,8.86mmol)在MeOH(30mL)与 EtOH(50mL)的搅拌溶液中加入水合肼(hydrazine hydrate)(2.22g,44.29 mmol),并将溶液回流2小时。过滤固体,并蒸发溶剂。藉由急速层析法(0 至50百分比EtOAc/己烷)纯化残留物,以获得甲基3-氨基-2-(4-((((三 异丙基甲硅烷基)氧基)甲基)苯基)丙酸酯(methyl 3-amino-2-(4-(((triisopropylsilyl)oxy)methyl)phenyl)propanoate)(11e)。
对甲基3-氨基-2-(4-((((三异丙基甲硅烷基)氧基)甲基)苯基) 丙酸酯(11e)(3.19g,8.74mmol)在CH
对甲基3-((叔丁氧基羰基)氨基)-2-(4-(((三异丙基甲硅烷基) 氧基)甲基)苯基)丙酸酯(11f)(2.07g,4.44mmol)在THF/MeOH(1:1,40mL) 中的溶液加入NaOH(8.88mL,17.76mmol),并在室温下搅拌2小时。将混合 物以1N HCl中和并以EtOAc萃取。将有机层以盐水清洗,以Na
(12)合成例12
化合物11之合成方案如以下方案9所示。
方案9
最终化合物11的合成方法与化合物9相似。
化合物叔丁基4-(4-(3-((叔丁氧基羰基)氨基)-2-(4-(((三异 丙基甲硅烷基)氧基)甲基)苯基)丙酰胺基)苯基)-1H-吡唑-1-羧酸酯(tert-butyl 4-(4-(3-((tert-butoxycarbonyl)amino)-2-(4-(((triisopropylsilyl)oxy)methyl)phenyl )propanamido)phenyl)-1H-pyrazole-1-carboxylate)(11h)为白色粉末。
化合物叔丁基4-(4-(4-(3-((叔丁氧基羰基)氨基)-2-(4-(羟甲 基)苯基)丙酰胺基)苯基)-1H-吡唑-1-羧酸酯(tert-butyl 4-(4-(3-((tert-butoxycarbonyl)amino)-2-(4-(hydroxymethyl)phenyl)propanamido) phenyl)-1H-pyrazole-1-carboxylate)(11i)为白色粉末。
最终化合物N-(4-(1H-吡唑-4-基)苯基)-3-氨基-2-(4-(羟甲基)苯 基)丙烯酰胺二盐酸盐 (N-(4-(1H-pyrazol-4-yl)phenyl)-3-amino-2-(4-(hydroxymethyl) phenyl)propenamide dihydrochloride)(11)为白色粉末。
8.化合物12之合成
(13)合成例13
化合物12之合成方案如以下方案10所示。
方案10
最终化合物12的合成方法与化合物10相似。
化合物叔丁基4-(4-(3-((叔丁氧基羰基)氨基)-2-(4-((((2,4- 二甲基苯甲酰基)氧基)甲基)苯基)丙酰胺基)苯基)-1H-吡唑-1-羧酸酯 (tert-butyl 4-(4-(3-((tert-butoxycarbonyl)amino)-2-(4-(((2,4-dimethylbenzoyl)oxy)methyl)p henyl)propanamido)phenyl)-1H-pyrazole-1-carboxylate)(12a)为白色粉末。
化合物2-(4-(1-((4-(1H-吡唑-4-基)苯基)氨基)-3-氨基-1-氧丙 烷-2-基)苄基2,4-二甲基苯甲酸酯二盐酸盐 (4-(1-((4-(1H-pyrazol-4-yl)phenyl)amino)-3-amino-1-oxopropan-2-yl)benzyl 2,4-dimethylbenzoate dihydrochloride)(12)为白色粉末。
9.化合物13之合成
(14)合成例14
化合物13之合成方案如以下方案11所示。
方案11
对叔丁基4-(4-(3-(((叔丁氧基羰基)氨基)-2-(4-(羟甲基)苯 基)丙酰胺基)苯基)-1-H-吡唑-1-羧酸酯(tert-butyl 4-(4-(3-((tert-butoxycarbonyl)amino)-2-(4-(hydroxymethyl)phenyl)propanamido) phenyl)-1H-pyrazole-1-carboxylate)(11i)(100mg,0.19mmol)在CH
在4mL小瓶中装入叔丁基4-(4-(3-(((叔丁氧基羰基)氨基)-2-(4- 甲酰基苯基)丙酰胺基)苯基)叔丁基-1-H-吡唑-1-羧酸酯(13a)(52mg,0.10 mmol)与在二噁烷(1.0mL)中之4M HCl。将所得混合物在室温下搅拌1小时。 于减压下移除溶剂,以获得所需化合物N-(4-(1H-吡唑-4-基)苯基)-3-氨 基-2-(4-甲酰基苯基)丙酰胺二盐酸盐 (N-(4-(1H-pyrazol-4-yl)phenyl)-3-amino-2-(4-formylphenyl)propanamide dihydrochloride)(13)(44mg,90%)。
10.化合物14之合成
(15)合成例15
化合物14之合成方案如以下方案12所示。
方案12
将叔丁基4-(4-(3-(((叔丁氧基羰基)氨基)-2-苯基丙酰胺基)苯 基)-1H-吡唑-1-羧酸酯(7a)(506mg,1.0mmol,1.0eq)与Lawesson试剂(808mg, 2.0mmol,2.0eq)在甲苯(5mL)中的混合物于N
将叔丁基4-(4-(4-(3-(((叔丁氧基羰基)氨基)-2-苯基丙烷硫代 酰胺基)苯基)-1H-吡唑-1-羧酸酯(14a)(520mg,1.0mmol,1.0eq)溶于1mL MeOH,加入HCl/MeOH(3M,5mL)于室温搅拌3小时。将前述反应混合物 浓缩。将残留物藉由快速层析法(DCM/MeOH从100%至10%)纯化,以获 得粗产物(110mg),又将其以DCM和MeOH结晶,并以1N HCl调整pH值至5.0,以获得N-(4-(1H-吡唑-4-基)苯基)-3-氨基-2-苯基丙硫酰胺二盐酸盐 (N-(4-(1H-pyrazol-4-yl)phenyl)-3-amino-2-phenylpropanethioamide dihydrochloride)(化合物14)(75mg,产率:两步骤23%),其为黄色固体。 LCMS(ES,m/z):[M+H]
11.化合物15之合成
(16)合成例16
化合物15之合成方案如以下方案13所示。
方案13
对叔丁基-(4-氨基-3-(2-(二甲基氨基)乙氧基)苯基)-1H-吡唑 (tert-butyl-(4-amino-3-(2-(dimethylamino)ethoxy)phenyl)-1H-pyrazole)(200mg, 0.85mmol,1.0eq)在CH
在20mL小瓶中装入化合物叔丁基4-(4-(3-(2-(2-((叔丁氧基羰基) 氨基)-1-苯基乙基)硫脲基)苯基)叔丁基-1H-吡唑-1-羧酸酯(15b)(353mg, 0.66mmol)与4M HCl于二噁烷(3.3mL)中。将所得混合物在室温下搅拌1小 时。于减压下除去溶剂,以获得化合物1-(4-(1H-吡唑-4-基)苯基)-3-(2- 氨基-1-苯基乙基)硫脲二盐酸盐 (1-(4-(1H-pyrazol-4-yl)phenyl)-3-(2-amino-1-phenylethyl)thiourea dihydrochloride)(15)(244mg,90%),其呈淡黄色粉末状。
12.化合物16之合成
(17)合成例17
化合物16之合成方案如以下方案14所示。
方案14
将叔丁基-(4-氨基-3-(2-(二甲基氨基)乙氧基)苯基)-1H-吡唑(1b)(400 mg,1.54mmol,1.0equiv)与(异硫氰酸根合甲基)苯 ((isothiocyanatomethyl)benzene)(276mg,1.85mmol,1.2eq)于叔丁醇 (t-BuOH)(10mL)中的混合物在N
将叔丁基4-(4-(3-苄硫脲基)苯基)-1H-吡唑-1-羧酸酯(16a)(410mg,1.00 mmol,1.0eq)与CH
将叔丁基4-(4-((((苄基氨基)(甲硫基)亚甲基)氨基)苯基) -1H-吡唑-1-羧酸酯(16b)(370mg,0.88mmol,1.0eq)、氰胺(cyanamide)(110 mg,2.63mmol,3.0eq)与1,4-二氮杂双环[2.2.2]辛烷 (1,4-diazabicyclo[2.2.2]octane)(98mg,0.88mmol,1.0eq)于叔丁醇(10mL)中 之混合物于在N
13.化合物17之合成
(18)合成例18
化合物17之合成方案如以下方案15所示。
方案15
对4-溴苯甲酸(4-bromobenzoic acid)(322mg,1.60mmol)与叔丁基(2-((4- 氟苄基)氨基)乙基)氨基甲酸酯(tert-butyl (2-((4-fluorobenzyl)amino)ethyl)carbamate)(430mg,1.60mmol)在CH
将叔丁基(2-(4-溴-N-(4-氟苄基)苯甲酰胺基)乙基)氨基甲酸酯 (17a)(537mg,1.19mmol)、叔丁基4-(4,4 1,5,5-四甲基-1,3,2-二氧杂硼硼烷-2- 基)-1H-吡唑-1-羧酸酯(tert-butyl 4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-1H-pyrazole-1-carboxylate)(350 mg,1.19mmol)、PdCl
对叔丁基4-(4-((2-((叔丁氧基羰基)氨基)乙基)(4-氟苄基氨 基甲酰基)苯基)-1H-吡唑-1-羧酸酯(17b)(300mg,0.56mmol)与1,4-二噁烷 (1mL)的混合物加入在1,4-二噁烷(2.78mL)中之4M HCl。将前述之反应混合 物在室温下搅拌1小时。将反应混合物浓缩。将残留物以DCM(6mL)处理并 过滤。收集滤饼,以获得N-(2-氨基乙基)-N-(4-氟苄基)-4-(1H-吡唑-4- 基)苯甲酰胺二盐酸盐 (N-(2-aminoethyl)-N-(4-fluorobenzyl)-4-(1H-pyrazol-4-yl)benzamide dihydrochloride)(17,200mg,87%),其为浅黄色固体。
14.化合物18之合成
(19)合成例19
化合物18之合成方案如以下方案16所示。
方案16
对4-(4,4,5,5-四甲基-1,3,2-二氧杂硼硼烷-2-基)-1H-吡唑-1-甲酸叔丁酯(tert-butyl 4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-1H-pyrazole-1-carboxylate)(154 0mg,5.24mmol)在THF(15mL)于0℃且经搅拌的溶液加入2M NaOH
对叔丁基4-羟基-1H-吡唑-1-羧酸酯(18a)(965mg,5.24mmol)与1-氟-4-硝 基苯(1-fluoro-4-nitrobenzene)(739mg,5.24)在DMF(10mL)中且经搅拌的溶液 加入K
对叔丁基4-(4-硝基苯氧基)-1H-吡唑-1-羧酸酯(18b)(140mg,0.46mmol) 于MeOH(5mL)与EtOAc(5mL)中的溶液中加入10%Pd/C(49mg,0.046 mmol)。将前述之反应混合物于H
对3-((叔丁氧基羰基)氨基)-2-苯基丙酸 (3-((tert-butoxycarbonyl)amino)-2-phenylpropanoic acid)(114mg,0.43mmol) 与叔丁基4-(4-氨基苯氧基)-1H-吡唑-1-羧酸酯(118mg,0.43mmol)在CH
对叔丁基4-(4-(3-(((叔丁氧基羰基)氨基)-2-苯基丙酰胺基)苯 氧基)-1H-吡唑-1-羧酸酯(18d)(110mg,0.21mmol)与1,4-二噁烷(1mL)的混合 物,加入在1,4-二噁烷(1.05mL)中之4M HCl。将前述之反应混合物在室温下 搅拌1小时。将反应混合物浓缩。将残留物以DCM(5mL)处理并过滤。收集 滤饼,以获得N-(4-(((1H-吡唑-4-基)氧基)苯基)-3-氨基-2-苯基丙酰 胺二盐酸盐(N-(4-((1H-pyrazol-4-yl)oxy)phenyl)-3-amino-2-phenylpropanamide dihydrochloride)(18)(82mg,22%),其为白色固体。
15.化合物19之合成
(20)合成例20
化合物19之合成方案如以下方案17所示。
方案17
对在密封管中之4-溴-2-氟苯胺(4-bromo-2-fluoroaniline)(1211mg,6.37mmol)、1-Boc-4-吡唑硼酸频哪醇酯(1-Boc-4-pyrazoleboronic acid pinacol ester)(1875mg,6.37mmol)、PdCl
对3-((叔丁氧基羰基)氨基)-2-苯基丙酸 (3-((tert-butoxycarbonyl)amino)-2-phenylpropanoic acid)(346mg,1.31mmol) 与叔丁基4-(4-氨基-3-氟苯基)-1H-吡唑-1-羧酸酯(19a)(362mg,1.31mmol) 在DMF(2mL)中且经搅拌的溶液,加入DIPEA(569μL,3.26mmol)与 HATU(596mg,1.57mmol)。将前述之反应混合物在室温下搅拌2小时。 藉由减压移除溶剂,接着将残留物以制备逆相高效液相色层分析(80%ACN, 20%H
对溶于1,4-二噁烷(1mL)之叔丁基4-(4-(3-(((叔丁氧基羰基)氨 基)-2-苯基丙酰胺基)-3-氟苯基)-1H-吡唑-1-羧酸酯(19b)(315mg,0.60 mmol),加入在1,4-二噁烷(4.0mL)中之4M HCl。将前述之反应混合物在室温 下超音波处理30分钟。藉由过滤收集白色粉末、以DCM洗涤并干燥,以获得 3-氨基-N-(2-氟-4-(1H-吡唑-4-基)苯基)-2-苯基丙酰胺二盐酸盐 (3-amino-N-(2-fluoro-4-(1H-pyrazol-4-yl)phenyl)-2-phenylpropanamide dihydrochloride)(19)(230mg,96%)。
16.化合物20与化合物21之合成
(21)合成例21
化合物20与21之合成方案如以下方案18所示。
方案18
对4-(4-(3-(((叔丁氧基羰基)氨基)-2-苯基丙酰胺基)苯基)-1H- 吡唑-1-甲酸叔丁酯(tert-butyl 4-(4-(3-((tert-butoxycarbonyl)amino)-2-phenylpropanamido)phenyl)-1H-pyrazol e-1-carboxylate)(15g,29.6mmol,1.0eq)在MeOH(150mL)中的溶液加入 HCl/MeOH(150mL)。将前述混合物于室温隔夜搅拌。将混合物浓缩并将残 留物溶于H
分离条件:
管柱:ChiralPak AD-H Daicel chemical Industries,Ltd,250*30mm I.D.,10 μm
移动相A:Supercritical CO
A:B=60:40于50mL/分钟
管柱温度:38℃
喷嘴压力:100Bar;喷嘴温度:60℃;蒸发温度:20℃;微调温度(Trimmer Temp):25℃;波长:220nm
对H
对H
实施例2
体外功效测试
A.对Rho相关的蛋白激酶(Rho-associated protein kinase,ROCK)之抑制 功效测试
测试上方所合成之各化合物对于ROCK的抑制效果
A-1.方法
1.以DMSO将10mM之测试化合物稀释为1mM,接着再稀释为300nM。 Netarsudil(AR-13324)为市售降眼压药物,AR-13503为AR-13324之活性代谢 物。
2.将上述300nM之测试化合物进行系列稀释,以分别获得浓度为100 nM、33nM、11nM、3.7nM、1.2nM以及0.4nM的测试化合物。
3.将1μL之上述经系列稀释的测试化合物加入49μL之经调整之ROCK 反应缓冲溶液(Modified ROCK reaction buffer)(含0.1M KCl、0.01M MgCl
4.将20μL之上述配制样本加入平底之96孔盘,并于每孔中加入20μL ROCK ATP缓冲溶液。
5.将上述96孔盘放置于回旋式震荡器上,于室温下反应90分钟。
6.接着,将40μL Kinase-Glo luminescent kinase assay solution(Promega,RV6712)加入上述96孔盘,并将96孔盘置于回旋式震荡器上,于室温下反应 10分钟。
7.以SpectraMax M5 microplate reader测定96孔盘之各孔的冷光数值,并 以下方公式计算ROCK抑制率(%)。
最大值=在无任何测试化合物存在下,利用上述方法所测得之值(酵 素与基质完全反应的状况下所测得之值为最大值)
最小值=在无酵素存在下,利用上述方法所测得之值(无酵素与基质 反应所测得之值为最小值)
抑制率(%)=(实验组(添加测试化合物之组所测得的值)-最小值)/(最 大值-最小值)*100%
A-2.结果
结果如表2所示。
表2
注:++++++代表IC
B.对肌凝蛋白轻链激酶-4(myosin light chain kinase 4,MYLK-4)之抑制 功效测试
实验流程系参考ThermoFisher Scientific所提供之LanthaScreen Eu KinaseBinding Assay Screening Protocol and Assay Conditions。
B-1.材料制备
将配制于100%DMSO中之测试化合物储存溶液(1mM),进行3倍系列 稀释10次,以备测定其对MYLK-4的IC
激酶/抗体混合物(Kinase/Antibody Mixture),预先以激酶缓冲液(KinaseBuffer)稀释为2X工作浓度。
B-2.分析方法
1.于白色384微孔平盘(Greiner,Cat.NO.784207)中加入激酶缓冲液3.84 μL,接着加入上述激酶/抗体混合物8.0μL,再加入追踪剂(AlexaFluor labeled Tracer)4.0μL,之后加入上述经稀释之适当浓度测试化合物160nL,并使培 养盘震荡30秒。
2.接着将培养盘放置在室温下培养60分钟,再以萤光盘分析器 (fluorescenceplate reader)读取并分析数据。并以下公式计算各孔洞中之反应 液的发射比。
发射比(emission eatio,ER)=AF647发射(665nm)/铕发射(europium emission)(615nm)
此外,于上述分析中同时设置有LanthaScreen Eu激酶之结合分析的对照 组:抑制0%对照组(0%displacement control),反应中不含已知抑制剂,作为 最大发射比(maximum emission ratio);抑制100%对照组(100%displacement control),包含最高浓度之已知抑制剂,作为最小发射比(minimum emission ratio);其中,已知抑制剂为Sunitinib。
LanthaScreen Eu Kinase之结合分析的反应成份如表3所示。已知抑制剂Sunitinib之IC
表3、LanthaScreen Eu激酶之结合分析的反应成份
3.测试化合物于不同浓度对MYLK-4的抑制率可依据以下公式获得:
抑制%=[(ER
4.根据上方所得测试化合物于不同浓度对MYLK-4的抑制率,计算出测 试化合物于MYLK-4的IC
B-3.结果
结果如表4所示。
表4、测试化合物之MYLK-4IC
注:++++++代表IC
C.对YSK-4之抑制功效测试
实验流程系参考ThermoFisher Scientific所提供之Z’-LYTE ScreeningProtocol and Assay Conditions。
C-1.材料制备
将配制于100%DMSO中之测试化合物储存溶液(1mM),进行3倍系列 稀释10次,以用于测定测试化合物对YSK-4的IC
胜肽/激酶抗体混合物(Peptide/Kinase Mixture),预先以激酶缓冲液 (KinaseBuffer)稀释为2X工作浓度。
ATP溶液,预先以激酶缓冲液(50mM HEPES pH 7.5,0.01%BRIJ-35,10 mM MgCl
显影剂溶液为新颖PKC脂质混合物(Novel PKC Lipid Mix),其含有2 mg/mLPhosphatidyl Serine、0.2mg/mL DAG于20mM HEPES,pH 7.4与0.3% CHAPS,预先以显影缓冲液稀释10倍。
C-2.分析方法
1.于黑色384孔盘(Corning,Cat.NO.4514)中加入上述经稀释之适当浓度 测试化合物100nL、激酶缓冲液2.4μL,接着加入上述胜肽/激酶混合物5μL, 再加入ATP溶液2.5μL,并使培养盘震荡30秒。
2.接着将培养盘放置在室温下培养60分钟。
3.之后加入显影剂溶液5μL,并于黑暗中使培养盘震荡30秒,再以萤光 盘分析器(fluorescence plate reader)读取并分析数据。
此外,针对激酶制作以下对照组,并将其与激酶置于于同一培养盘上:
(1)0%磷酸化对照组(100%抑制对照组)
最大发射比由0%磷酸化对照组(100%抑制对照组)所建立,其不包含 ATP,且因此不显示激酶活性。该对照组在显影反应中产生100%经裂解的胜 肽。
(2)100%磷酸化对照组
由与胜肽基质序列相同的合成磷酸化胜肽作为100%磷酸化对照组。此 对照组在显影反应中产生非常低百分比的裂解胜肽。
依据0%磷酸化对照组与100%磷酸化对照组计算在特定反应孔(实验组) 中达到的磷酸化百分比。
Z’-LYTE Screening Kinase之结合分析反应所使用的Z’-LYTE substrate种 类为Ser/Thr 07胜肽,ATP反应浓度为5μM(YSK4的Km)。本分析中作为对照 用的已知抑制剂为Staurosporine。于系统中IC
对背景萤光的校正=萤光强度
发射比=香豆素(Coumarin)发射(445nm)/萤光素发射(520nm)(使用针对 背景萤光之校正值)
%磷酸化=1-(发射比x F
%抑制=(1–%磷酸化
C100%:100%磷酸化对照组之平均香豆素发射讯号
C0%:0%磷酸化对照组之平均香豆素发射讯号
F100%:100%磷酸化对照组之平均萤光素发射讯号
F0%:0%磷酸化对照组之平均萤光素发射讯号
DRI:显应反应干扰(Development Reaction Interference)
TCFI:测试化合物的萤光干扰(Test Compound Fluorescence Interference)
C-3.结果
结果如表5所述。
表5、测试化合物之YSK4 IC
注:++++++代表IC
整合前述结果可知,本揭露上述合成之化合物对于ROCK、MYLK-4与 YSK4,均具有抑制功效,且具有加成性标靶抑制作用,特别是化合物7与化 合物20。
又,由于目前已知经由抑制之ROCK表现可达成保护视神经(参见,如 Rothschildet al.,ROCK-1mediates diabetesinduced retinal pigment epithelial andendothelial cell blebbing:Contribution to diabetic retinopathy.ScientificReports.(2017)7:8834.与Tanna et al.,Rho Kinase Inhibitors as a NovelTreatment for Glaucoma and Ocular Hypertension.Ophthalmology.(2018) 125:1741-1756.)与减缓或治疗高眼压(参见,如Tanna et al.,Rho Kinase Inhibitors as a NovelTreatment for Glaucoma and Ocular Hypertension. Ophthalmology.(2018)125:1741-1756)、青光眼压(参见,如Tanna et al.,Rho Kinase Inhibitors as a Novel Treatmentfor Glaucoma and Ocular Hypertension. Ophthalmology.(2018)125:1741-1756)、眼中风(参见,如Yi et al.,Protective Effects of Intravitreal Injection of the Rho-Kinase Inhibitor Y-27632in a Rodent Model of Nonarteritic Anterior IschemicOptic Neuropathy(rAION).J Ophthalmol.(2020)2020:1485425.与Nourinia R,etal.ROCK inhibitors for the treatment of ocular diseases.Br J Ophthalmol 2018;102:1-5.)、黄斑部病变(参 见,如Sadiq et al.Pharmacological agents indevelopment for diabetic macular edema Int J Retin Vitr(2020)6:29.)、黄斑部水肿(参见,如Sadiq et al. Pharmacological agents in development for diabeticmacular edema Int J Retin Vitr(2020)6:29.)、糖尿病视网膜病变(参见,如NouriniaR,et al.ROCK inhibitors for the treatment of ocular diseases.Br J Ophthalmol2018;102:1-5)、 角膜内皮细胞损伤(Fuchs endothelial corneal dystrophy,FECD)(参见,如 Okumura et al.The ROCK Inhibitor Eye Drop Accelerates CornealEndothelium Wound Healing Invest Ophthalmol Vis Sci.(2013)54:2439-2502.)、角膜纤维 化(参见,如
此外,目前也已知经由抑制之ROCK表现可达成减缓或治疗肺动脉高压 (参见,如Zhang et al.,Effects of Fasudil on Patients with Pulmonary HypertensionAssociated with Left Ventricular Heart Failure with Preserved EjectionFraction:A Prospective Intervention Study.Can Respir J.(2018)2018: 314825)、慢性阻塞性肺病(COPD)(参见,如Liu et al.,Influence of Rho kinase inhibitorFasudil on late endothelial progenitor cells in peripheral blood of COPDpatients with pulmonary artery hypertension.Bosn J Basic Med Sci.(2014) 14(1):40-4)、病因不明性肺纤维化(参见,如Knipe et al.,The Rho Kinase IsoformsROCK1 and ROCK2 Each Contribute to the Development of Experimental PulmonaryFibrosis.Am J Respir Cell Mol Biol.(2018)58(4): 471-481.)、肺气肿(参见,如Bewley et al.,Differential Effects of p38,MAPK, PI3K or Rho Kinase Inhibitorson Bacterial Phagocytosis and Efferocytosis by Macrophages in COPD.PLoS One.(2016)11(9):e0163139.)、肺癌(参见,如 Vigil et al.,ROCK1 and ROCK2 are Requiredfor Non-Small Cell Lung Cancer Anchorage-Independent Growth andInvasion.Cancer Res.(2012)15:72(20).)等 之功效,因此具有抑制ROCK之功效的本揭露上述合成之化合物,也可应用 于肺部相关疾病与症状,如肺动脉高压、慢性阻塞性肺病、病因不明性肺纤 维化、肺气肿及/或肺癌的预防及/或治疗等。
实施例3
于正常兔之降眼压模型之最大效应(maximal effect,Emax)剂量评估
A.化合物20
1.方法
动物:雄性纽西兰白兔(n=7/每组);
测试化合物配方:0.01%化合物20;0.03%化合物20;0.1%化合物20;
投药:对每只实验动物于右眼(投药眼)滴入50μL测试化合物并于左 眼(对照眼)滴入50μL载剂(vehicle)(不含测试化合物)。将上述3种配方 每天投药一次,连续3天。
在第1天与第3天投药前(0小时)以及投药后2、4、6与8小时以Tono-Vet (iCare)测量每只动物之眼压。
2.结果
结果如第1A图与第1B图,以及表6与表7所示。
表6、第1天投药之眼压测定结果
最大眼压下降幅度%=(对照眼之眼压-投药眼之眼压)/对照眼之眼压 *100
表7、第3天投药之眼压测定结果
最大眼压下降幅度%=(对照眼之眼压-投药眼之眼压)/对照眼之眼压 *100
第1A图与表6显示于第1天投药之眼压测定结果。第1B图与表7显示于第 3天投药之眼压测定结果。
结果显示,化合物20在降眼压效果方面呈现剂量依赖作用(dose dependenteffect),其中投予0.03%化合物20之组与投予0.1%化合物20之组的 降眼压幅度与趋势相近。
又,连续给药3天,投予0.03%化合物20之组有些许药效累积的现象(第 3天比第1天之降眼压幅度平均增加近1mmHg)(参见表6与表7),但投予 0.03%化合物20之组的降眼压幅度与投予0.1%化合物20之组的降眼压幅度相 近(参见表7)。此结果显示,化合物20于浓度0.03%应已接近此模型之眼压 测试极限,因此其所显示之药效(Emax)累积差异不大。
本实验所呈现之数据,系已去除不合格之数据(已去除第1天两眼之眼 压差≥2mmHg(n=1)与第3天给药前两眼之眼压差>5mmHg之白兔(n=1)), 并去除反弹性高眼压之数据(n=3)。每组n值≥3;另外投予0.01%化合物20之 组的n值为6。
由上述结果可知,浓度0.03%应已为化合物20于正常眼压兔之模型中的 最大效应(maximal effect,Emax)剂量。
B.化合物4、5、7、8、11、12与14
以与对于化合物20之类似方法,确认化合物4、5、7、8、11、12与14于 正常眼压兔之模型中的最大效应剂量。
结果显示化合物4、5、7与8之最大效应剂量皆为1%,而化合物11、12 与14之最大效应剂量分别为0.5%、0.25%与0.5%。
实施例4
于正常眼压兔之模型中之降眼压功效评估
A.化合物20
1.材料与方法
实验动物:纽西兰大白兔,雄性,体重大于2公斤。纽西兰大白兔系购 自惠钧养殖场。经过一周检疫期后,以温度16-22℃及30-70%相对湿度 (Relative Humidity,RH)、8小时白天/16小时黑夜之环境条件,饲养于瑞德生 物科技有限公司。
实验方法:
(1)降眼压功效评估
于将12只纽西兰大白兔(2.0-4.0kg)秤重并分组后(每组n=3-6),将大白 兔以包巾固定。待大白兔呈现稳定状态后,拉开其右眼下眼睑,将50μL的 测试样本(含0.1%或0.03%化合物20之眼滴剂),滴入大白兔右眼的结膜囊 内,阖上眼睑,维持大白兔安定状态至少2分钟,并避免大白兔甩头导致眼 药流出眼部;左眼给予载剂(不含测试化合物),作为对照组。以0.02% AR-13324作为比较基准(benchmark),以评估测试化合物的药效竞争性。眼 压侦测时间点为给药前(0小时)及给药后1、2、4、6与8小时。
(2)刺激性评估
眼压测量完毕后即进行兔眼外观拍照,并依据经济合作暨发展组织(Organization for Economic Cooperation and Development,OECD)所规定之眼 刺激性试验准则(OECD/OCDE 405)评估测试物质对大白兔眼睛角膜、虹膜或 结膜造成的刺激状态(adverse event)。
OECD/OCDE 405对于角膜、虹膜或结膜之评分方式如表8所示。
表8、眼刺激等级
可能的最大值:4
*应注意角膜混浊区域
(3)角膜观察
以0.1%化合物20之眼滴剂为测试样本,实验方法与上方「(1)降眼压功 效评估」中所记载之实验方法相同。进行7日连续投药(每日一次),之后 以裂隙灯观察角膜状态。
(4)候选药物于投药后存在于房水(aqueous humor,AH)之含量分析 将正常兔投予化合物20,并于不同时间点确认化合物于房水中之含量。
2.结果
降眼压功效评估之结果如第2图所示。
依据第2图可知,含0.1%化合物20之眼滴剂与含0.03%化合物20之眼滴剂 的最大效应(Emax)显示于投药后6-8小时,而其最大降眼压幅度为约4.4-4.9 mmHg,且眼刺激性轻微。
又,此结果也显示,于正常眼压兔之模型中含0.03%化合物20之眼滴剂 已达最大降眼压作用。
眼刺激性评估结果如第3A图、第3B图与第3C图所示。
由第3A图与第3B图可知,化合物20在最大效应剂量(0.1%)下之眼刺激性 仍低于AR-13324(0.02%)。
此外,第3C图显示,连续给药7天,角膜仍无破损与混浊。
化合物20于投药后存在于虹膜与睫状体及房水之含量分析结果如第4图 所示。针对虹膜与睫状体,化合物20之浓度系以单位ng/g进行测定;针对房 水,化合物20之浓度系以单位ng/mL进行测定。
依据第4图可知,于投药后化合物20在房水中之含量可达ROCK抑制需 求。
B.化合物4、5、7、8、11、12与14
1.方法
(1)降眼压功效评估
以与对于化合物20之类似方法,确认化合物4、5、7、8、11、12、14、 20与21(使用最大效应剂量)于正常眼压兔之模型中的降眼压功效。
(2)安全边际(safety margin)测试
以化合物7为代表,将含2%化合物7之眼滴剂投予兔眼(一天3剂, 每次间隔3小时,并于给药前以及每次给药后1小时观察)。另含0.04%化 合物7之眼滴剂投予兔眼(一天1剂,并于给药前以及给药后1小时与6小 时观察)。依据上述经济合作暨发展组织所规定之眼刺激性试验准则 OECD/OCDE 405,对化合物7之眼刺激性进行评估。
2.结果
降眼压功效评估之结果如表9所示。
表9、降眼压功效评估结果
安全边际(safety margin)测试结果如第5图与表10所示。
表10、安全边际测试结果
由第5图与表10可知,AR-133247于治疗指数为2时,OECD405整体分数 为4,而化合物7于治疗指数为3时,OECD405整体分数为2,因此化合物7之 安全边际优于AR-13324。
实施例5
猕猴动物模式
1.材料与方法
将含0.1%或0.03%化合物20之眼滴剂投予正常猕猴。以0.02%AR-13324 作为基准,以评估测试化合物的药效竞争性。以气动式眼压测定仪(Model 30
2.结果
结果如第6图所示。
依据第6图可知,化合物20可在正常眼压弥猴达到与AR-13324相当或更 优之降眼压作用,且无明显红眼症等副作用。
实施例6
于高渗透压食盐水(hypertonic saline)所诱导之高眼压兔模型(急性高眼 压模型)中的降眼压功效评估
1.材料与方法
实验动物:纽西兰大白兔,雄性,体重2.0-3.0kg。纽西兰大白兔于试验 前购自合格之实验动物兔场,饲养于交通大学动物中心。
测试样本:含0.1%化合物20之眼滴剂
负对照组(negative control)1:生理食盐水
负对照组2:不含测试物质的载剂(含有5%甘露醇(mannitol)、20mM硼 酸(boricacid)与0.125%壬苯醇醚-9(nonoxynol-9))
实验方法:将雄性纽西兰大白兔于秤重与分组后进行麻醉。将160μL高 渗透压食盐水(5%NaCl)注入于麻醉状况下的大白兔左右眼玻璃体内,以使 兔眼成为高眼压状态。接着,将50μL生理盐水(0.9%NaCl)、含0.1%化合物 20之眼滴剂、用于制备化合物20之眼滴剂的载剂(不含化合物20)与含0.02% AR-13324之眼滴剂,分别滴入各组别的兔左右眼内。眼压侦测(IOP)时间点 为麻醉前(0小时)以及投药后0.5、1、1.5、3与5小时。以生理食盐水与不 含测试物质之载剂作为负对照组,以含0.02%AR-13324之眼滴剂作为基准(benchmark),以评估化合物20于高渗透压食盐水诱导高眼压兔之模型中的降 眼压功效。
2.结果
结果如第7图与表11所示。
表11、于高眼压兔模型中之降眼压测试结果
最大眼压差:于记录到最大反应之时间点,个体之眼压读数与负对照组 1(生理食盐水)之平均眼压读数之差异(J Ocul Pharmacol Ther.2010 Apr;26(2):125-132)
结果显示,于高渗透压食盐水诱导高眼压兔之模型中,含0.1%化合物20 之眼滴剂可降低眼压约18.0±6.8mmHg,而含0.02%AR-13324之眼滴剂降低 眼压约7.7±4.2mmHg。显示化合物20的降眼压功效相较于AR-13324明显较佳(t-test,p<0.05)。而载剂相较于生理食盐水于统计上(t-test)并无明显差异。 AR-13324相较于生理食盐水或载剂,在统计上(t-test)也无显著差异。
实施例7
于磁珠诱导高眼压兔之模型(眼压>30mmHg的高眼压模型)中的降眼 压功效评估
剥脱性青光眼(exfoliation glaucoma,XFG)被认为比原发性隅角开放性 青光眼(primary open angle glaucoma)更严重。剥脱性青光眼与原发性隅角开 放性青光眼之最大眼压(38.2vs 26.9mmHg)、最小眼压(24.7vs 18.4mmHg) 与平均眼压变化(13.5vs8.5mmHg)在统计学上具显著差异。又,目前并无已 知的饮食疗法、药物或其他干预措施可以防止剥脱性综合征(exfoliation syndrome)的发生或减慢其发展(Progress inRetinal and Eye Research Vol.19, No.3,pp.345to 368,2000)。由上述可知,剥脱性青光眼之眼压可以达到>30 mmHg,且目前对其并无有效药物,因此,于此提供眼压>30mmHg的高眼 压模型以评估本揭露之化合物应用于剥脱性青光眼与眼压>30mmHg的高 眼压之治疗的可行性。
A.化合物20
1.材料与方法
实验动物:纽西兰大白兔,雄性,体重2.0-3.0kg。纽西兰大白兔于试验 前购自惠钧养殖场,饲养于交通大学动物中心。
测试样本:含0.03%或0.1%化合物20之眼滴剂
负对照组1:不含测试化合物20的载剂(含有5%甘露醇、20mM硼酸 与0.125%壬苯醇醚-9)
负对照组2:不含测试化合物AR-13324的载剂(含有4.7%D-甘露醇与 0.05%硼酸)
实验方法:将雄性纽西兰大白兔于秤重与分组后以Zoletil 50 0.2mL/kg 进行麻醉纽西兰大白兔。将50μL磁珠溶液(50mg/mL,磁珠粒径10μm)注 入于麻醉状况下的大白兔左右眼前眼房内,以使兔眼成为高眼压状态。眼前 房注射结束后,立即在眼周套入强力铷铁磁铁环处理10-20分钟,以使磁珠 完全堵住眼房水排水组织。以抗生素消毒眼球后,提供保湿眼膏进行眼球恢 复,并待眼压升高。约3天后,眼压可以达到>30mmHg的高眼压,并可以持 续至少10天。在眼压达到目标眼压>30mmHg的高眼压后,将含0.03%或0.1% 化合物20之眼滴剂(右眼)、用于制备化合物20之眼滴剂的载剂(不含化合 物20)(左眼)、含0.02%AR-13324之眼滴剂(右眼)与用于制备AR-13324 眼滴剂的载剂(不含AR-13324)(左眼),分别滴入一滴(约35μL)于各 组别的兔左右眼内。眼压侦测(IOP)时间点为给药前(0小时)以及给药后2、 4、6与8小时,实验连续进行2天。以含0.02%AR-13324之眼滴剂作为基准, 以评估化合物20于磁珠诱导高眼压兔之模型(眼压>30mmHg的高眼压模 型)中的降眼压功效。
2.结果
结果如表12与第8图所示。
表12、化合物20于磁珠诱导高眼压兔之模型中的降眼压测试结果
结果显示,于磁珠诱导高眼压兔之模型(眼压>30mmHg的高眼压模型) 中,含0.03%化合物20之眼滴剂可降低眼压约5.7±0.6mmHg(降低约 15.3%),而含0.1%化合物20之眼滴剂可降低眼压约12.1±1.4mmHg(降低 约28.8%)。亦即含0.03%化合物20之眼滴剂与含0.1%化合物20之眼滴剂 的降眼压功效均优于含0.02%AR-13324之眼滴剂(降低眼压约4.3±1.4 mmHg(降低约11.0%)),且含0.1%化合物20之眼滴剂的降眼压功效甚 至可为含0.02%AR-13324之眼滴剂的2倍以上。
B.化合物7
以与对于化合物20之类似方法,确认化合物7(使用最大效应剂量0.5% 与1%)于正常眼压兔之模型中的降眼压功效。
结果如表13所示。
表13、化合物7于磁珠诱导高眼压兔之模型中的降眼压测试结果
依据表12可知,于磁珠诱导高眼压兔之模型(眼压>30mmHg的高眼压 模型)中,含0.5%化合物7之眼滴剂与含1%化合物7之眼滴剂的降眼压功效 也均优于含0.02%AR-13324之眼滴剂,其中含1%化合物7之眼滴剂的降眼压 功效甚至可为含0.02%AR-13324之眼滴剂的3倍以上。
实施例8
1.MYLK-4于细胞之表现
(1)方法
人小梁网(Human Trabecular Meshwork,HTM)细胞(Cat.NO.6590)获自ScienCell Research Laboratories。将HTM细胞维持于小梁网细胞培养基 (TrabecularMeshwork Cell Medium,TMCM)(Cat.NO.6591)中。TMCM 是由500mL基础培养基、10mL FBS(Cat.NO.0010)、5mL小梁网细胞生长补 充剂(TMCGS,Cat.NO.6592)与5mL青霉素/链霉素溶液(P/S,Cat.NO.503) 所调配而成。当细胞生长达到70-80%饱合后,以50μg/mL地塞米松(dexamethasone)(Cat.NO.4902,Sigma)对HTM细胞进行隔夜处理。
通过西方墨点法分析细胞裂解物中之MYLK4与GAPDH的表现。首先收 集细胞,并以1x RIPA(50mM Tris-HCl,pH 7.4、150mM NaCl、0.25%脱 氧胆酸、0.1%NP-40、1mM EDTA,磷酸酶抑制剂和蛋白酶抑制剂混合物) 冲洗。接着,以SDS-PAGE(sodium dodecyl sulfatepolyacrylamide gel electrophoresis,十二烷基硫酸钠聚丙烯酰胺凝胶电泳)分离细胞裂解物,并 转移到PVDF membtane(iBlot
(2)结果
结果如第9图所示。
依据第9图可知,经地塞米松处理之HTM细胞(疾病状态细胞)之 MYLK-4表现量较正常HTM细胞高。
2.MYLK-4于磁珠诱导的疾病标的组织表现
(1)方法
将50μL磁珠溶液(50mg/mL,磁珠粒径10μm)注入于麻醉状况下的大 白兔左右眼之眼前房内,以使兔眼成为高眼压状态。以未经磁珠溶液处理之 大白兔作为对照组。之后将兔子牺牲,取出眼球,并进行组织病理分析。
组织病理判读方法:
显微镜:MoticEasyScan
显微摄影系统:MoticEasyScan
判读方法:
委托远见生物科技股份有限公司进行兔眼球石蜡组织切片之免疫组织 化学染色(immunohistochemical,IHC staining),除针对眼球小梁网(trabecular meshwork)进行结果判读外,并提供判读结果评分表及各不同倍率的显微摄 影照片。
取下之眼球组织经福马林固定后,脱水并进行石蜡包埋,再制成3μm 厚的石蜡组织切片。IHC染色之生物标记为MYLK-4及MLC-2。
根据检体所制成之组织病理切片,分别在20倍、40倍、100倍、200倍及 400倍显微镜下进行组织病灶观察及记录。根据病灶严重度、分布范围及所 占组织的百分比例,参照INHAND(International Harmonization of Nomenclature and Diagnostic Criteria)建议之5级分制评级法进行病灶评分:0 级分代表无明显病理变化、病灶占总体组织1%以下;1级分代表病症极微 (minimal,1-5%);2级分代表病症轻微(mild,6-25%);3级分代表病症中度 (moderate,26-50%);4级分代表病症中高度(moderately severe,51-75%);5级分代表病症严重(severe/high,>76%)。
(2)结果
免疫组织化学染色结果如第10图所示,而评分结果如表14所示。
表14、免疫组织化学染色之评分结果
依据图10及表14可知,无论是疾病状态细胞(经地塞米松处理之HTM 细胞),或者是疾病动物标的组织(经磁珠诱导之兔眼),MYLK-4的表现 量均高于正常细胞与组织,因此推定具MYLK-4抑制功效之本揭露化合物除 了经由ROCK抑制作用,还可藉由抑制MYLK-4而有效降低眼压。
整合前述实验结果可知,相较于AR-13324仅以ROCK为标靶,本揭露之 化合物20可同时以ROCK、MYLK-4与YSK-4为标靶。又,于高渗透压食盐 水诱导高眼压兔之模型(急性高眼压模型)与磁珠诱导高眼压兔之模型(眼 压>30mmHg的高眼压模型)中,本揭露之化合物20的降眼压功效皆优于 AR-13324。此外,本揭露之化合物20在最大效应剂量下,相较于AR-13324 具有较低之刺激性。
虽然本发明已以较佳实施例揭露如上,然其并非用以限定本发明,任何 熟习此技艺者,在不脱离本发明之精神和范围内,当可作些许之更动与润饰, 因此本发明之保护范围当视后附之权利要求所界定者为准。
- β-氨基酸衍生物、含其之激酶抑制剂与医药组合物以及其用途
- 稠合杂环衍生物、含该衍生物的医药组合物及其医药用途
