基因HSF5或/和蛋白HSF5在制备用于诊断特发性不孕不育症的产品中的应用
文献发布时间:2023-06-19 19:30:30
技术领域
本发明涉及分子生物学和医学技术领域,特别涉及基因HSF5或/和蛋白HSF5在制备用于诊断特发性不孕不育症的产品中的应用。
背景技术
不孕不育由遗传因素(基因突变)在导致的配子(精子或卵子)发生障碍中占比重较大。通过探究遗传机制,发现减数分裂的精准完成对遗传信息的稳定传递至关重要。在同源染色体联会阶段,大量减数分裂特异性基因应时空表达并完成特定功能。如何检测不孕不育患者对明确特发性不孕不育的病因及靶向治疗具有重要的实践意义。
因此,需要开发用于诊断特发性不孕不育症的产品。
发明内容
本发明目的是提供基因HSF5或/和蛋白HSF5在制备用于诊断特发性不孕不育症的产品中的应用,可明确诊断特发性不孕不育症,在改善不孕不育方面具有重要的意义。
在本发明的第一方面,提供了基因HSF5或/和蛋白HSF5在制备用于诊断特发性不孕不育症的产品中的应用。
进一步地,所述用于诊断特发性不孕不育症的产品包括:用于检测HSF5基因异常的产品;或/和用于检测蛋白HSF5表达水平异常的产品。
进一步地,所述HSF5基因异常包括:基因序列存在单或多碱基序列缺失、插入或替换。
进一步地,所述用于检测HSF5基因异常的产品包括检测HSF5基因的引物。
进一步地,所述蛋白HSF5表达水平异常包括:HSF5蛋白提前终止表达,或者HSF5蛋白重要功能域中氨基酸缺失、插入或替换。
所述HSF5蛋白重要功能域具体为:单链DNA结合域,其他未知功能域。
进一步地,所述用于检测蛋白HSF5表达水平异常的产品包括:特异性结合所述HSF5蛋白的抗体。
在本发明的第二方面,提供了HSF5蛋白的抗体在制备用于诊断特发性不孕不育症的产品中的应用。
在本发明的第三方面,提供了用于检测HSF5基因异常的引物对在制备用于诊断特发性不孕不育症的产品中的应用。
进一步地,所述用于检测HSF5基因异常的引物对的核苷酸序列如SEQ ID NO:1-SEQ ID NO:12所示。
在本发明的第四方面,提供了一种用于诊断特发性不孕不育症的产品,所述用于诊断特发性不孕不育症的产品包括:用于检测HSF5基因异常的引物对,所述引物对的核苷酸序列如SEQ ID NO:1-SEQ ID NO:12所示。
本发明实施例中的一个或多个技术方案,至少具有如下技术效果或优点:
本申请通过研究发现,敲除模式小鼠(C57bl/6)中Hsf5,雄性小鼠表现为精子缺失和不育;在生精过程中,具体表现为精母细胞发育会阻滞到减数分裂前1期粗线期;而雌性卵巢中不表达该基因,故敲除后雌性配子发育正常且个体可孕。在其他有关哺乳动物的研究中,HSF5蛋白在野猪(Sus scrofa)的卵巢中高表达;但在饲养猪(Duroc pig)中参与雄性精子发生;另外,在马(Equus caballus)的雌性幼体中,HSF5也呈现高表达。而在人的不同组织中,HSF5呈现与小鼠相似的睾丸高表达特征。随后通过实验发现检测基因HSF5异常或/和蛋白HSF5的表达水平异常可用于诊断特发性不孕不育症,因此基因HSF5或/和蛋白HSF5可以在制备用于诊断特发性不孕不育症的产品中应用,可明确诊断特发性不孕不育症,在改善不孕不育方面具有重要的意义。
附图说明
为了更清楚地说明本发明实施例中的技术方案,下面将对实施例描述中所需要使用的附图作一简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其它的附图。
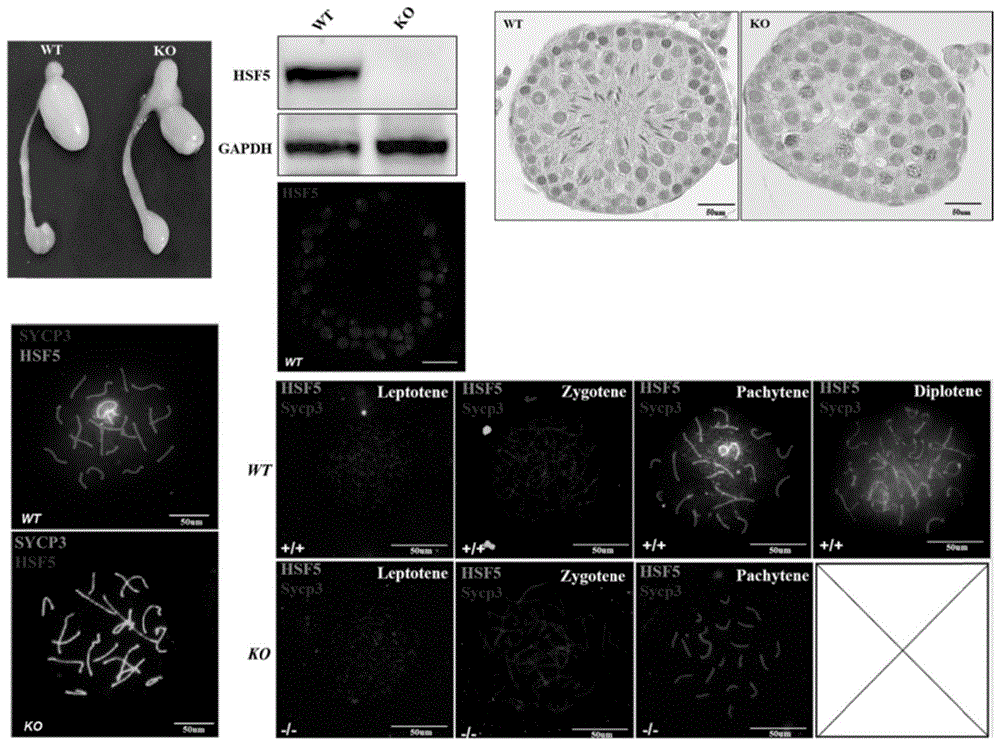
图1为本发明实施例1的结果;
图2为本发明实施例2的结果;
图3为本发明实施例3的结果。
具体实施方式
下文将结合具体实施方式和实施例,具体阐述本发明,本发明的优点和各种效果将由此更加清楚地呈现。本领域技术人员应理解,这些具体实施方式和实施例是用于说明本发明,而非限制本发明。
在整个说明书中,除非另有特别说明,本文使用的术语应理解为如本领域中通常所使用的含义。因此,除非另有定义,本文使用的所有技术和科学术语具有与本发明所属领域技术人员的一般理解相同的含义。若存在矛盾,本说明书优先。
除非另有特别说明,本发明中用到的各种原材料、试剂、仪器和设备等,均可通过市场购买获得或者可通过现有方法获得。
本申请实施例的技术方案为解决上述技术问题,总体思路如下:
本申请发明人在研究中发现,敲除模式小鼠(C57bl/6)中的Hsf5基因,雄性小鼠表现为精子缺失和不育;在生精过程中,具体表现为精母细胞发育会阻滞到减数分裂前1期粗线期;而雌性卵巢中不表达该基因,故敲除后雌性配子发育正常且个体可孕。
实施例1中Hsf5基因敲除导致小鼠睾丸精子发生过程受阻和数量产生严重减少,这导致小鼠生育率下降。
实施例2中纯合敲除Hsf5基因小鼠外显子2、3区段缺失,表明特发性雄性不育与Hsf5基因异常相关。
实施例3中Hsf5基因敲除鼠中HSF5蛋白表达水平和野生小鼠(对照)相比存在明显差异,Hsf5基因敲除鼠中HSF5蛋白表达提前终止,表明特发性雄性不育与Hsf5蛋白表达水平异常相关。
下面将结合实施例及实验数据对本申请的基因HSF5或/和蛋白HSF5在制备用于诊断特发性不孕不育症的产品中的应用进行详细说明。
实施例1
1、材料
收集正常小鼠和Hsf5基因敲除小鼠的睾丸及附睾组织。
2、睾丸大小测量及称重、睾丸组织固定、切片和组织学染色检测精子数量、免疫荧光检测蛋白定位。操作如下:
(1)解剖出完整的小鼠睾丸及附睾组织;摆放整齐后,使用刻度尺进行测量睾丸大小变化并进行统计学分析。
(2)取每只小鼠的单侧睾丸进行石蜡切片前固定、包埋处理;将包埋好的组织进行切片、脱蜡处理。
(3)对石蜡切片进行HE染色,封片处理;观察曲精小管中精子数量变化,并进行统计学分析。
(4)对小鼠单侧睾丸进行总蛋白提取,免疫印迹检测蛋白表达水平。
(5)对小鼠单侧睾丸进行多聚甲醛(4%)固定、蔗糖(30%)脱水处理;包埋后放置-80℃冷却硬化、切片。
(6)对获得的冰冻组织切片进行抗原修复、封闭、抗体孵育和荧光检测;分析蛋白表达差异。
(7)分离小鼠睾丸中的各级生精细胞、低渗处理、固定于粘附载玻片;对玻片负载的细胞进行清洗、封闭、抗体孵育和荧光检测,分析蛋白表达时期及定位差异。
3、结果分析
(1)Hsf5基因敲除小鼠的睾丸尺寸较正常鼠减小,重量降低。
(2)Hsf5基因敲除小鼠的成熟精子数量减少。
(3)Hsf5基因敲除小鼠的睾丸组织中HSF5蛋白表达水平降低。
(4)Hsf5基因敲除小鼠的各级生精细胞中HSF5蛋白的定位异于正常鼠的定位。
4、实验结论
Hsf5基因敲除导致小鼠睾丸精子发生过程受阻和数量产生严重减少,这导致小鼠生育率下降。
实施例2、检测基因组中Hsf5基因序列
1、材料
收集野生和纯合Hsf5基因敲除小鼠的外周血200微升(ul)。
2、提取血液组织基因组
采用血液基因提取试剂盒(品牌:TIANGEN,货号:DP348),具体操作按说明书执行,具体操作如下:
(1)处理血液样品(当选用血液样品为200ul时,无需处理)。
(2)加入200ul缓冲液GB和20ul蛋白酶K(Proteinase K)的预混溶液至上述处理获得的200ul样品中,充分颠倒混匀,56℃放置10分钟(min),其间颠倒混匀数次,溶液应变清亮。
(3)室温放置2-5min后加入350ul缓冲液BD,充分颠倒混匀,此时可能会出现絮状沉淀。
(4)将上一步所得溶液和絮状沉淀都加入一个吸附柱CG2中(吸附柱CG2放入收集管中),12,000转每分钟(rpm)离心30秒(s),倒掉收集管中的废液,将吸附柱CG2放入收集管中;重复本步骤一次。
(5)12,000rpm离心2min,倒掉废液。将吸附柱CG2置于室温放置2min,以彻底晾干吸附材料中残余的漂洗液。
(6)将吸附柱CG2转入1.5毫升(ml)离心管中,向吸附膜中间位置悬空滴加50-200ul洗脱缓冲液TB,室温放置2min,12,000rpm离心2min,将溶液收集到离心管中。
(7)将DNA产物保存至-20℃。
3、PCR扩增Hsf5基因序列
(1)设计小鼠Hsf5基因外显子引物,具体信息如下:
表1
(2)用上述引物扩增目的基因序列,具体操作参数如下:
表2
(3)核酸凝胶电泳,具体试剂及操作参数如下:
表3
(4)通过紫外凝胶成像仪(品牌:北京六一,型号:WD9413B,紫外波长:254nm)找到目的条带并用刀片切下,标记后,附带引物送测序,公司为北京擎科生物技术有限公司。具体物品如下:
(5)将返回测序结果与基因数据库(NCBI Reference Sequence GeneID:124535)中Hsf5基因进行序列比对,使用软件为SnapGene 4.1.9。
4、结果分析
(1)碱基缺失:Hsf5基因外显子序列中碱基发生非3整倍数缺失,编码蛋白必定受到影响,应进一步通过SnapGene软件确定编码蛋白序列,具体需参考蛋白表达及功能验证。
5、实验结论
经测序,纯合敲除Hsf5基因小鼠外显子2、3区段缺失,则特发性雄性不育与Hsf5基因相关。
实施例3、检测Hsf5编码蛋白表达水平
1、获取组织
处死、解剖纯合Hsf5基因敲除小鼠;获取睾丸曲细精管或卵巢组织。
2、制备蛋白样品
具体操作如下:
表4
3、蛋白免疫印迹反应
表5
4、数据计算
通过BCA法蛋白定量,以β-actin(不同细胞内含量变化不大,不受目标蛋白变化影响)作为内参蛋白可对HSF5蛋白进行相对定量(取HSF5蛋白与内参蛋白的比值作为计量值),对照组蛋白取自正常小鼠睾丸组织(可视为正常组织)。将不同样品的显影图像进行灰度处理并计算灰度值或灰度面积(可用软件image J)。
5、结果分析
(1)检测组HSF5蛋白条带位置改变:结合HSF5基因序列信息,表明HSF5蛋白提前终止;但蛋白功能具体是否受影响需要进一步行蛋白互作实验(CO-IP或GST poll-down)证实。
6、实验结论
Hsf5基因敲除鼠中HSF5蛋白表达水平和野生小鼠(对照)相比存在明显差异,表现为表达量下降和对应大小的蛋白痕迹缺失,这提示雄性不育与Hsf5基因突变相关。
综上可知,特发性不孕不育症与基因HSF5异常有关或/和蛋白HSF5表达水平异常有关,表明基因HSF5或/和蛋白HSF5可以在制备用于诊断特发性不孕不育症的产品中进行应用。
应用例1、基因HSF5或/和蛋白HSF5可以在制备用于诊断特发性不孕不育症的产品中的应用
一、检测基因组中HSF5基因序列
1、材料
收集特发性不孕不育患者的外周血200微升(ul)。
2、提取血液组织基因组
采用血液基因提取试剂盒(品牌:TIANGEN,货号:DP348),具体操作按说明书执行,具体操作如下:
(1)处理血液样品(当选用血液样品为200ul时,无需处理)。
(2)加入200ul缓冲液GB和20ul蛋白酶K(Proteinase K)的预混溶液至上述处理获得的200ul样品中,充分颠倒混匀,56℃放置10分钟(min),其间颠倒混匀数次,溶液应变清亮。
(3)室温放置2-5min后加入350ul缓冲液BD,充分颠倒混匀,此时可能会出现絮状沉淀。
(4)将上一步所得溶液和絮状沉淀都加入一个吸附柱CG2中(吸附柱CG2放入收集管中),12,000转每分钟(rpm)离心30秒(s),倒掉收集管中的废液,将吸附柱CG2放入收集管中;重复本步骤一次。
(5)12,000rpm离心2min,倒掉废液。将吸附柱CG2置于室温放置2min,以彻底晾干吸附材料中残余的漂洗液。
(6)将吸附柱CG2转入1.5毫升(ml)离心管中,向吸附膜中间位置悬空滴加50-200ul洗脱缓冲液TB,室温放置2min,12,000rpm离心2min,将溶液收集到离心管中。
(7)将DNA产物保存至-20℃。
3、PCR扩增HSF5基因序列
(1)可供检测人源HSF5基因是否异常的引物序列,如下表6所示:
表6
/>
(2)用上述引物扩增目的基因序列,具体操作参数如下:
表7
(3)核酸凝胶电泳,具体试剂及操作参数如下:
表8
(4)通过紫外凝胶成像仪(品牌:北京六一,型号:WD9413B,紫外波长:254nm)找到目的条带并用刀片切下,标记后,附带引物送测序,公司为北京擎科生物技术有限公司。具体物品如下:
(5)将返回测序结果与基因数据库(NCBI Reference Sequence GeneID:124535)中HSF5基因进行序列比对,使用软件为SnapGene 4.1.9。
4、结果分析
(1)序列完全匹配:表明HSF5基因外显子序列没有突变,可确定特发性不孕不育与HSF5基因无关。
(2)碱基缺失或插入:HSF5基因外显子序列中碱基发生非3整倍数缺失或插入,编码蛋白必定受到影响,故特发性不孕不育与HSF5相关;若发生3整倍数缺失或插入可导致编码蛋白中缺失或插入额外氨基酸残基,且改变位点发生在功能域中可导致HSF5活性降低,进一步通过SnapGene软件确定编码蛋白序列,具体需参考蛋白表达及功能验证。
(4)碱基替换:若HSF5基因外显子序列中碱基发生同义突变(碱基替换后未改变编码氨基酸种类),最终编码蛋白未发生改变,故特发性不孕不育与HSF5基因无关;若HSF5基因外显子序列中碱基发生无义突变(碱基替换后导致蛋白翻译提前终止),最终影响HSF5蛋白活性及功能,故特发性不孕不育与HSF5基因有关。
5、实验结果判定
(1)若经测序,患者编码基因所在区域序列正确,则特发性男性不育与HSF5基因无关。
(2)若患者编码基因出现碱基缺失、插入和替换等造成蛋白翻译提前终止或关键位点功能缺失的情况,则特发性男性不育与HSF5基因有关;需要进一步鉴定。
二、检测HSF5编码蛋白表达水平
1、获取组织
通过睾丸或卵巢穿刺(需要专业医务人员)获取不孕不育患者的曲细精管或卵巢组织。
2、制备蛋白样品
具体操作如下:
表9
3、蛋白免疫印迹反应
表10
4、数据计算
通过BCA法蛋白定量,以β-actin(不同细胞内含量变化不大,不受目标蛋白变化影响)作为内参蛋白可对HSF5蛋白进行相对定量(取HSF5蛋白与内参蛋白的比值作为计量值),对照组(非不孕不育患者)蛋白取自睾丸癌患者的癌旁组织(可视为正常组织)。将不同样品的显影图像进行灰度处理并计算灰度值或灰度面积(可用软件image J)。
5、结果分析
(1)检测组与对照组无差异(位置、含量):表明不孕不育患者HSF5蛋白表达水平与正常人无异,同时,若基因序列正确可进一步排除HSF5异常导致不孕不育的可能性。
(2)检测组HSF5蛋白条带位置改变:结合HSF5基因序列信息,表明HSF5蛋白提前终止,或因插入碱基导致终止密码子丢失而加入新序列;若不伴随表达量增加,提示蛋白功能可能未受影响,若蛋白表达量增加提示突变导致蛋白功能受损;但蛋白功能具体是否受影响需要进一步行蛋白互作实验(CO-IP或GST poll-down)证实。
(3)检测组HSF5蛋白含量增加:提示HSF5蛋白活性降低,结合HSF5基因序列信息(功能域突变)及蛋白互作实验(蛋白结合下降),可提高诊断HSF5导致不孕不育的可能性。
6、实验结果
实验结果判定:
(1)若患者HSF5蛋白表达水平和正常可育者水平相比存在明显差异,表现为表达量下降或对应大小的蛋白痕迹缺失,这提示患者不育与HSF5基因突变相关。
(2)若患者HSF5蛋白表达水平与正常可育者水平相当,应结合基因突变位点,对蛋白功能进行分析,具体可分析蛋白定位时期、与互作蛋白的结合能力等方面,若以上多方面检测异常,则提示患者不育与HSF5基因突变相关。
最后,还需要说明的是,术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的过程、方法、物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种过程、方法、物品或者设备所固有的要素。
尽管已描述了本发明的优选实施例,但本领域内的技术人员一旦得知了基本创造性概念,则可对这些实施例作出另外的变更和修改。所以,所附权利要求意欲解释为包括优选实施例以及落入本发明范围的所有变更和修改。
显然,本领域的技术人员可以对本发明进行各种改动和变型而不脱离本发明的精神和范围。这样,倘若本发明的这些修改和变型属于本发明权利要求及其等同技术的范围之内,则本发明也意图包含这些改动和变型在内。
