用于心脏重塑的心脏起搏治疗的递送
文献发布时间:2023-06-19 09:41:38
本申请要求于2018年6月14日提交的美国临时专利申请第62/684,828号的权益,该申请的公开内容通过引用以其整体并入本文。
技术领域
本公开涉及心脏起搏方法和系统,并且更具体地涉及用于在植入式医疗设备中递送心脏重塑起搏的方法和装置。
背景技术
心力衰竭(HF)是一种复杂的疾病状态,其被广泛地通过心脏无法充分泵送以应对其静脉回流和/或递送足够的输出来满足身体的代谢需求来定义。心力衰竭是一种日益普遍的威胁生命的心血管疾病,由明显的残疾、频繁住院和高死亡率所表征。HF在年龄较大的个体中越来越普遍(高达总人口的10%),并且已成为65岁以上人群住院的最常见原因。HF是住院的主导原因或促成因素,并因此正在成为医疗保健支出的重要促成因素。HF的特定临床表现是由心力衰竭的根本原因所确定的。
术语心力衰竭(HF)广义上是指一种病理生理性疾病,在这种疾病中,心脏功能无法递送足够的血液来满足代谢需求(例如,在体育锻炼期间,或在严重的情况下在休息时),或无法适应静脉回流。随后可以基于患者所表现出的症状,来应用一系列进一步的子分类和/或心脏结构。纽约心脏协会提供了通过症状或客观评估对心力衰竭的示例性分类(I-IV级,A-D级)。心力衰竭也可以通过射血分数来定义。通常,表现出射血分数小于或等于0.35的患者被归类为患有射血分数降低的心力衰竭(HFrEF),而射血分数大于0.35的患者被认为是射血分数保留的心力衰竭(HFpEF)。
充血性心力衰竭症状指示充血性心力衰竭。示例性充血性心力衰竭症状包括:导致容易疲劳和器官功能障碍(例如肾脏)的心输出量降低,以及与肺部充血(导致呼吸困难)或外周充血(导致下肢和腹部肿胀)相关的症状。
基于健康活跃男性与久坐男性以及先前患有心肌梗塞的男性的室性心律失常发生率的比较,在久坐的生活方式与室性心律失常的风险之间标识出可能的相关性。久坐的生活方式的一个结果是,心脏腔室的大小可能会减少,这通常是由于肌肉厚度增加而引起的。因此,在健康久坐的男性中发现在锻炼期间室性心律失常数量最多,等级最高。
患有心力衰竭的所有患者中几乎有一半具有正常的射血分数(EF),通常被称为射血分数保留的心力衰竭(HFpEF)。在患有HFpEF的充血性心力衰竭患者中,每次搏动从心脏左心室泵出的血液量(射血分数)大于50%。HFpEF通常也被称为舒张性心力衰竭或舒张性功能障碍,因为功能缺陷通常与舒张期和心室充盈期间发生的变化有关。患有心力衰竭人群中的大约一半患有HFpEF,而其余人表现出射血分数降低,或者射血分数降低的心力衰竭(HFrEF)。
HFpEF的流行率(prevalence)持续增大,这可能是由于常见风险因素的流行率增大,包括年老、高血压、代谢综合征、肾功能不全和肥胖。HFpEF由异常的舒张功能所表征,这表现为心脏左心室的僵硬度增大、下一次搏动前充满血液时左心室舒张度降低、以及腔室容量减小(这通常是由于肌肉厚度增大所引起的)。对于正经历HFpEF的患者而言,心房纤颤和肺动脉高压的风险增大。
发明内容
本公开涉及一种用于在一段时间内递送能够重塑患者的心脏的起搏治疗的方法和设备。根据本公开的一个示例,一种方法包括递送心脏重塑起搏以刺激患者心脏状况的正常化;响应于所递送的重塑起搏而监测一个或多个参数;响应于该监测,而确定心脏重塑起搏是否对心脏正常化具有影响;以及响应于所确定的对心脏正常化的影响,而调整心脏重塑起搏。
根据本公开的另一示例,一种用于向患者递送心脏重塑起搏的心脏设备包括:壳体;多个电极,该多个电极被电连接到壳体,以递送心脏重塑起搏,以刺激患者心脏状况的正常化;以及处理器,该处理器被定位在壳体内并且被配置成:响应于所递送的重塑起搏而监测一个或多个参数;响应于该监测,而确定心脏重塑起搏是否对心脏正常化具有影响;并且响应于所确定的对心脏正常化的影响,而调整心脏重塑起搏。
在本公开的另一示例中,一种方法包括递送心脏重塑起搏以刺激患者心脏状况的正常化;响应于所递送的心脏重塑起搏,而执行对一个或多个参数的短期监测;监测指示所递送的心脏重塑起搏对心脏正常化的长期影响的一个或多个长期参数;响应于该监测,而确定所递送的心脏重塑起搏对心脏正常化的长期影响;以及响应于短期监测和所确定的对心脏正常化的长期影响中的一者或两者,而调整心脏重塑起搏。
在本公开的另一示例中,用于向患者递送心脏重塑起搏的心脏设备包括:壳体;多个电极,该多个电极被电连接到壳体,以递送心脏重塑起搏,以刺激患者心脏状况的正常化;以及处理器,该处理器被定位在壳体内并且被配置成:响应于所递送的心脏重塑起搏,而执行对一个或多个参数的短期监测;监测指示所递送的心脏重塑起搏对心脏正常化的长期影响的一个或多个长期参数;响应于该监测,而确定所递送的心脏重塑起搏对心脏正常化的长期影响;并且响应于短期监测和所确定的对心脏正常化的长期影响中的一者或两者,而调整心脏重塑起搏。
附图说明
图1是根据本公开的可用于递送起搏治疗的示例性心脏治疗递送系统的示意图。
图2是更详细地示出图1的示例性心脏治疗递送系统的示意图。
图3是根据本公开的示例的植入式医疗设备的示例性配置的示例性功能框图。
图4是根据本公开的植入式医疗设备的电路系统的示例性功能框图。
图5是根据本公开的示例的递送用于心脏重塑的起搏治疗的方法的流程图。
图6是示出重塑起搏对患者的心输出量的影响的图形表示。
图7是根据本公开的示例的递送用于心脏重塑的起搏治疗的方法的流程图。
图8是根据本公开的示例的递送用于心脏重塑的起搏治疗的方法的流程图。
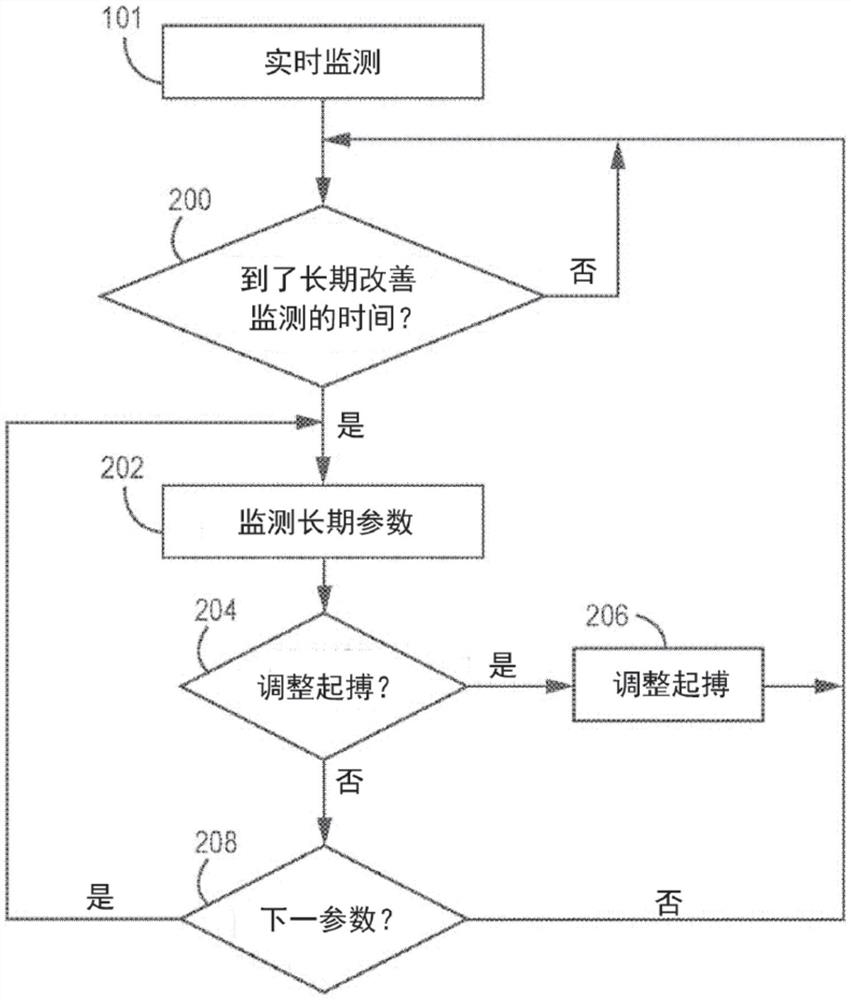
图9是根据本公开的示例的递送重塑起搏治疗的方法的流程图。
具体实施方式
对本领域技术人员将会是显而易见的是,来自一个实施例的元件或过程可与其他实施例的元件或过程结合使用,并且使用本文中所陈述的特征的组合的这种方法、设备和系统的可能实施例不限于附图中所示和/或本文所描述的特定实施例。进一步地,将认识到,本文中所描述的实施例可包括并不一定按比例示出的许多元件。
图1是根据本公开的可用于递送起搏治疗的示例性心脏治疗递送系统的示意图。治疗递送系统10可包括可以耦合至引线18、20、22和编程器24的植入式医疗设备16(IMD)。IMD 16可以是例如经由耦合到引线18、20、22中的一个或多个的电极向患者14的心脏12提供电信号的植入式起搏器、心脏复律器、和/或除颤器。患者14可以是但不一定是人。
引线18、20、22延伸至患者14的心脏12中以感测心脏12的电活动和/或向心脏12递送电刺激。在图1中所示的示例中,右心室(RV)引线18延伸通过一个或多个静脉(未示出)、上腔静脉(未示出)和右心房26,并进入右心室28。左心室(LV)冠状窦引线20延伸通过一个或多个静脉、腔静脉、右心房26,并进入冠状窦30到达与心脏12的左心室32的游离壁相邻的区域。右心房(RA)引线22延伸通过一个或多个静脉和腔静脉,并且进入心脏12的右心房26。在一个示例中,心房引线22可被定位在AV结/隔膜区域附近,以用于希氏束起搏的递送,并且至少一个心室引线18被定位在右心室中或心室引线20被定位在左心室中,如下面描述的。
IMD 16可经由耦合到引线18、20、22中的至少一个的电极来感测伴随于心脏12的去极化和复极化的电信号等。在一些示例中,IMD 16基于在心脏12内感知到的电信号来向心脏12提供起搏治疗(例如起搏脉冲)。IMD 16可操作用于调整与起搏治疗相关联的一个或多个参数,诸如例如脉冲宽度、电压振幅、脉冲串长度等。进一步地,IMD 16可操作用于使用各种电极配置来递送起搏治疗,所述电极配置可以是单极的或双极的。IMD 16还可经由位于引线18、20、22中的至少一个引线上的电极来提供除颤治疗和/或心脏复律治疗。进一步地,IMD 16可检测心脏12的心律失常(诸如,心室28、32的纤颤),并以电脉冲的形式将除颤治疗递送至心脏12。在一些示例中,可对IMD 16进行编程以递送累进的治疗(例如,具有增大的能量水平的脉冲),直到心脏12的纤颤停止为止。
在一些示例中,编程器24可以是手持式计算设备或计算机工作站,该编程器24可由用户(诸如医生、技术人员、另一临床医生、和/或患者)用于与IMD 16通信(例如,对IMD16编程)。例如,用户可以与编程器24交互,以检取关于在IMD 16内的和/或与利用IMD 16所递送的起搏治疗相关联的一个或多个检测到的或指示的故障的信息。IMD 16和编程器24可经由使用本领域已知的任何技术的无线通信来进行通信。通信技术的示例可包括例如低频或射频(RF)遥测,但也可设想其他技术。
图2是更详细地示出图1的示例性心脏治疗递送系统的示意图。引线18、20、22可经由连接器块34电耦合至治疗递送模块(例如,用于递送起搏治疗)、感测模块(例如,一个或多个电极,用以感测或监测心脏12的电活动以用于确定起搏治疗的有效性)、和/或IMD 16的任何其他模块。在一些示例中,引线18、20、22的近侧端可包括电触头,这些电触头电耦合到IMD 16的连接器块34中的相应的电触头。另外,在一些示例中,引线18、20、22可借助于固定螺钉、连接销或另一种适当的机械耦合机构被机械地耦合到连接器块34。
引线18、20、22中的每根引线包括细长的绝缘引线体,该绝缘引线体可以携载通过隔离件(例如管状绝缘鞘)而彼此分开的多个导体(例如,同心盘绕导体、直导体等)。在示出的示例中,双极电极40、42被定位在引线18的远侧端附近。此外,双极电极44、46被定位在引线20的远侧端附近,且双极电极48、50被定位在引线22的远侧端附近。
电极40、44、48可采用环形电极的形式,并且电极42、46、50可采用分别可伸缩地安装在绝缘电极头52、54、56内的可伸长螺旋尖端电极的形式。电极40、42、44、46、48、50中的每一个可电耦合至其相关联的引线18、20、22的引线体内的导体(例如,螺旋的和/或直的)中的相应一个,并由此耦合至引线18、20、22的近侧端上的电触头中的相应一个。
电极40、42、44、46、48、50可进一步被用于感测伴随于心脏12的去极化和复极化的电信号(例如,电描记图(EGM)内的形态波形)。这些感知到的电信号经由相应的引线18、20、22而被传导至IMD 16。在一些示例中,IMD 16还可以经由电极40、42、44、46、48、50递送起搏脉冲,以引起患者的心脏12的心脏组织的去极化。在一些示例中,如图2中所示,IMD 16包括一个或多个壳体电极,诸如壳体电极58,该一个或多个壳体电极可与IMD 16的壳体60(例如,气密密封壳体)的外表面一体地形成或以其他方式耦合至该壳体60。电极40、42、44、46、48、50中的任意电极可与壳体电极58相组合地用于单极感测或起搏。换言之,电极40、42、44、46、48、50、58中的任意电极可被结合使用,以形成感测向量,例如,可用于评估和/或分析起搏治疗的有效性的感测向量。关于2011年12月23日提交并且转让给本发明的受让人的美国专利申请第9,002,454号可看到感测和起搏的配置的示例,该申请的公开内容通过引用整体地结合于此,如通过优选地将LV尖端(即,电极46)-Rv线圈(即,电极62)用于起搏向量和感测向量而加以修改。从LV尖端到RV线圈向量对于执行阻抗测量可能会更好。此阻抗可与LV腔室大小呈负相关,并且可在LV腔室随着重塑起搏舒张时下降。本领域技术人员一般可理解,还可选择其他电极作为起搏和感测向量。
如参照图3和图4进一步详细描述的,壳体60可封围治疗递送模块以及用于监测该患者的心律的感测模块,该治疗递送模块可包括用于生成心脏起搏脉冲和除颤或心脏复律电击的刺激发生器。引线18、20、22还可以分别包括可采取线圈形式的细长电极62、64、66。IMD 16可以经由细长电极62、64、66和壳体电极58的任何组合来向心脏12递送除颤电击。电极58、62、64、66还可以用于向心脏12递送心脏复律脉冲。进一步地,电极62、64、66可以由任何适当的导电材料制成,诸如,但不限于铂、铂合金、和/或已知可用于植入式除颤电极的其他材料。由于电极62、64、66通常不被配置成递送起搏治疗,因此电极62、64、66中的任意电极可用于在起搏治疗期间感测电活动(例如,用于分析起搏治疗有效性)并且可与电极40、42、44、46、48、50、58中的任意电极结合使用。在至少一个实施例中,RV细长电极62可用于在起搏治疗的递送期间感测患者的心脏的电活动(例如,与壳体电极58结合,形成RV细长、线圈、或除颤电极至壳体电极向量)。
图1-2中所示的示例性治疗递送系统10的配置仅是一个示例。在一个示例中,心房引线22被定位在AV结/隔膜区域附近,以用于希氏束起搏的递送,并且心室引线18被定位在右心室中或心室引线20被定位在左心室中,或者可包括心室引线18和20两者,如下面描述的。此外,下面将描述,引线22的电极50可以采用螺旋尖端电极的形式以使得引线能够被固定地接合在AV结/隔膜区域附近,以用于希氏束起搏的递送。
图3是根据本公开的示例的植入式医疗设备的示例性配置的功能框图。如图3所示,IMD 16可以包括控制模块81、治疗递送模块84(例如,其可以包括刺激发生器)、感测模块86和电源90。控制模块81可以包括处理器80、存储器82以及遥测模块88。存储器82可以包括计算机可读指令,当例如由处理器80执行时,这些计算机可读指令使IMD 16和/或控制模块81执行本文所描述的归因于IMD 16和/或控制模块81的各种功能。进一步地,存储器82可包括任何易失性、非易失性、磁的、光的、和/或电的介质,诸如随机存取存储器(RAM)、只读存储器(ROM)、非易失性RAM(NVRAM)、电可擦除可编程ROM(EEPROM)、闪存存储器、和/或任何其他数字介质。下面将详细地描述,存储器82包括与夺获管理(包括根据本公开的夺获管理的方法)有关的计算机指令。此外,存储器82包括用于一个或多个起搏方案(例如,一个或多个起搏算法等)的计算机指令。例如,一个或多个起搏算法以升高的心率起搏心脏达指定的持续时间,然后以第二心率水平起搏心脏达另一预先指定的持续时间。一个或多个其他实施例涉及以第一升高频率和第一持续时间起搏患者的心脏。在一个或多个起搏方案中,起搏器递送第一升高起搏频率(例如,比静息心率高出多达每分钟30个心跳达多至10分钟或多至20分钟)。此后,起搏频率升高到第二升高起搏频率(例如,比第一升高心率高出多达20HBM达多至10或20分钟)。此后,递送第三起搏频率以允许心脏比第二升高起搏频率更慢地搏动。低于第三起搏频率的第四起搏频率通过起搏器被递送到心脏。此后,允许心率逐渐恢复到静息心率水平(在有起搏或没有起搏的情况下)。本文公开了多个其他起搏方案,起搏器可以采用所述多个其他起搏方案以便重塑心脏。
控制模块81的处理器80(也被称为处理器电路)可包括以下各项中的任一项或多项:微处理器、控制器、数字信号处理器(DSP)、专用集成电路(ASIC)、现场可编程门阵列(FPGA)、和/或等效的分立或集成的逻辑电路系统。在一些示例中,处理器80可包括多个部件,诸如以下各项的任意组合:一个或多个微处理器、一个或多个控制器、一个或多个DSP、一个或多个ASIC、和/或一个或多个FPGA、以及其他分立或集成逻辑电路系统。归因于本文中的处理器80的功能可具体化为软件、固件、硬件、或它们的任意组合。
控制模块81可控制治疗递送模块84根据可存储在存储器82中的选定的一个或多个治疗程序向心脏12递送治疗(例如,诸如起搏之类的电刺激治疗)。更具体地,控制模块81(例如处理器80)可控制治疗递送模块84以递送电刺激,诸如例如具有由选定的一个或多个治疗程序(例如起搏治疗程序、起搏恢复程序、夺获管理程序等)指定的振幅、脉冲宽度、频率、或电极极性的起搏脉冲。如所示,治疗递送模块84例如经由相应引线18、20、22的导体或在壳体电极58的情况下经由设置在IMD 16的壳体60内的电导体而被电耦合至电极40、42、44、46、48、50、58、62、64、66。治疗递送模块84可以被配置用于使用电极40、42、44、46、48、50、58、62、64、66中的一个或多个电极生成诸如起搏治疗之类的电刺激治疗并向心脏12递送所述电刺激治疗。
例如,治疗递送模块84可经由分别被耦合到引线18、20、和22的环形电极40、44、48、和/或分别是引线18、20、和22的螺旋尖端电极42、46、和50来递送起搏刺激(例如,起搏脉冲)。进一步地,例如,治疗递送模块84可经由电极58、62、64、66中的至少两个来将除颤电击递送至心脏12。在一些示例中,治疗递送模块84可被配置成以电脉冲形式来递送起搏、心脏复律或除颤刺激。在其他示例中,治疗递送模块84可被配置成以其他信号的形式(诸如,正弦波、方波和/或其他基本上连续的时间信号)来递送这些类型的刺激中的一种或多种。
IMD 16可进一步包括开关模块85,并且控制模块81(例如,处理器80)可使用开关模块85来例如经由数据/地址总线来选择可用的电极中的哪些被用于递送治疗(诸如,用于起搏治疗的起搏脉冲),或可用的电极中的哪些被用于感测。开关模块85可包括开关阵列、开关矩阵、多路复用器、或适用于选择性地将感测模块86和/或治疗递送模块84耦合到一个或多个选定电极的任何其他类型的开关设备。更具体地,治疗递送模块84可包括多个起搏输出电路。可例如使用开关模块85来选择性地将多个起搏输出电路中的每一个起搏输出电路耦合至电极40、42、44、46、48、50、58、62、64、66中的一个或多个(例如,用于向起搏向量递送治疗的一对电极)。即,可使用开关模块85来将每个电极选择性地耦合到治疗递送模块的起搏输出电路中的一个。
感测模块86被耦合(例如,电耦合)至感测装置,该感测装置以及附加的感测装置可以包括电极40、42、44、46、48、50、58、62、64、66以便监测心脏12的电活动,例如,心电图(ECG)/电描记图(EGM)信号等。ECG/EGM信号可用于分析多个起搏事件。更具体地,ECG/EGM信号内的每个起搏事件的一个或多个形态特征可用于确定每个起搏事件是否具有预定水平的有效性。ECG/EGM信号可进一步用于监测心率(HR)、心率变异性(HRV)、心率震荡(HRT)、减速/加速能力、减速序列发生率、T波交替(TWA)、P波到P波的间期(也被称为P-P间期或A-A间期)、R波到R波的间期(也被称为R-R间期或V-V间期)、P波到QRS波群的间期(也被称为P-R间期、A-V间期或P-Q间期)、QRS波群形态、ST段(即,连接QRS波群和T波的段)、T波改变、QT间期、电向量等。
开关模块85还可以与感测模块86一起用于选择使用可用电极中的哪些可用电极来例如感测患者心脏的电活动(例如,使用电极40、42、44、46、48、50、58、62、64、66的任意组合感测患者心脏的一个或多个电向量)。在一些示例中,控制模块81可经由感测模块86内的开关模块(例如,通过经由数据/地址总线来提供信号)来选择用作感测电极的电极。在一些示例中,感测模块86可包括一个或多个感测通道,该一个或多个感测通道中的每一个可包括放大器。
在一些示例中,感测模块86包括通道,该通道包括具有比R波或P波放大器相对更宽的通带的放大器。来自被选择用于耦合至该宽带放大器的选定感测电极的信号可被提供给多路复用器,并随后通过模数转换器转换成多位数字信号以作为EGM存储在存储器82中。在一些示例中,对此类EGM在存储器82中的存储可处于直接存储器存取电路的控制下。控制模块81(例如使用处理器80)可采用数字信号分析技术来表征存储在存储器82中的数字化信号,以分析和/或分类EGM信号的一个或多个形态波形,从而确定起搏治疗的有效性。例如,处理器80可被配置成确定或获得患者心脏的一个或多个电向量内的一个或多个感知到的形态波形的一个或多个特征,并在存储器82内存储该一个或多个特征,以用于在稍后的时间处确定起搏治疗的有效性。
如果IMD 16被配置成生成起搏脉冲以及向心脏12递送起搏脉冲,则控制模块81可包括起搏器计时和控制模块,该起搏器计时和控制模块可被实现为硬件、固件、软件或其任何组合。起搏器计时和控制模块可包括与处理器80(诸如微处理器)分开的一个或多个专用硬件电路(诸如ASIC)、和/或由处理器80的部件(其可以是微处理器或ASIC)执行的软件模块。起搏器计时和控制模块可包括可编程计数器,该可编程计数器控制与DDD、VVI、DVI、VDD、AAI、DDI、DDDR、VVIR、DVIR、VDDR、AAIR、DDIR以及单腔室起搏和双腔室起搏的其他模式相关联的基础时间间期。在前面提到的起搏模式中,“D”可指示双腔室,“V”可指示心室,“I”可指示被禁止的起搏(例如,无起搏),“A”可指示心房,而“R”可指示频率应答性。起搏模式中的第一个字母可指示被起搏的腔室,第二个字母可指示在其中电信号被感知的腔室,而第三个字母可指示在其中提供对感测的响应的腔室。
由控制模块81内的起搏计时和控制模块定义的间期可以包括心房和心室起搏逸搏间期、感知的P波和R波对重新开始逸搏间期的计时无效的不应期、和/或起搏脉冲的脉冲宽度。作为另一示例,起搏器计时和控制模块可定义消隐期,并且从感测模块86提供信号,以消隐一个或多个通道(例如,放大器)达在向心脏12递送电刺激期间和之后的一时段。可响应于存储器82中所存储的数据,确定这些间期的持续时间。控制模块81的起搏器计时和控制模块还可确定心脏起搏脉冲的振幅。
在起搏期间,起搏器计时/控制模块内的逸搏间期计数器可在感测到R波和P波时被重置。治疗递送模块84(例如,包括刺激发生器)可以包括一个或多个起搏输出电路,该一个或多个起搏输出电路例如通过开关模块85被选择性地耦合到适于将双极或单极起搏脉冲递送到心脏12的腔室中的一个腔室的电极40、42、44、46、48、50、58、62或66的任意组合。控制模块81可在由治疗递送模块84生成起搏脉冲时重置逸搏间期计数器,并且由此控制对包括抗快速性心律失常起搏的心脏起搏功能的基本计时。
在一些示例中,控制模块81可作为中断驱动设备而操作,并且可响应于来自起搏器计时和控制模块的中断,其中,该中断可与感知到的P波和R波的出现以及心脏起搏脉冲的生成相对应。可由处理器80执行任何必要的数学计算,并且由起搏器计时和控制模块控制的值或间期的任何更新可在此类中断之后发生。存储器82的一部分可被配置成多个再循环缓冲区,该多个再循环缓冲区能保存一系列测得的间期,可由例如处理器80响应于起搏或感测中断的发生而分析这些测得的间期,以确定患者的心脏12目前是否正表现出房性或室性快速性心律失常。
控制模块81的遥测模块88可以包括用于与诸如本文参考图1描述的编程器24之类的另一设备通信的任何适当的硬件、固件、软件或其任何组合。例如,在处理器80的控制下,遥测模块88可以借助于天线(所述天线可以是内部和/或外部天线)来接收来自编程器24的下行链路遥测并向编程器24发送上行链路遥测。处理器80可例如经由地址/数据总线提供要通过上行链路传送至编程器24的数据和针对遥测模块88内的遥测电路的控制信号。在一些示例中,遥测模块88可以经由多路复用器向处理器80提供所接收的数据。在至少一个实施例中,遥测模块88可以被配置成:如果起搏治疗变得无效或不太有效(例如,不具有预定水平的有效性),则传输警告或警报。
IMD 16的各种部件被进一步耦合到电源90,该电源90可包括可再充电的和不可再充电的电池。可选择不可再充电的电池以维持达若干年,而可再充电的电池可例如每天或每周感应地从外部设备进行充电。
图4是根据本公开的植入式医疗设备的电路系统的示例性功能框图。图4描绘了双极RA引线22、双极RV引线18、以及双极LV CS引线20与植入式脉冲发生器(IPG)电路31耦合,其中没有LA CS起搏/感测电极28和30,该植入式脉冲发生器电路31具有起搏领域所公知的双心室DDD/R类型的可编程模式以及参数。进而,传感器信号处理电路43间接地耦合至计时电路83,并且经由数据和控制总线耦合至微计算机电路系统33。在通常被划分成微计算机电路33和起搏电路的功能框图中示出了IPG电路31。起搏电路包括数字控制器/定时器电路、输出放大器电路51、感测放大器电路55、RF遥测收发器41、活动传感器电路35以及以下描述的多个其他电路和部件。
晶体振荡器电路47为起搏电路提供基本计时时钟,而电池29提供电力。上电复位电路45对电路到电池的用于定义初始的操作条件的初始连接作出响应,并且类似地响应于检测到低电池条件而重置设备的操作状态。参考模式电路37生成用于起搏电路内的模拟电路的稳定的电压参考和电流,而模数转换器ADC和多路复用器电路39使模拟信号和电压数字化,以提供来自感测放大器55的心脏信号的实时遥测,以用于经由RF发射器和接收器电路41进行上行链路传输。电压参考和偏置电路37、ADC和多路复用器39、上电复位电路45和晶体振荡器电路47可对应于在目前市售的植入式心脏起搏器中的目前使用的那些部件中的任意部件。
IPG生成到心脏组织的起搏脉冲。通常,可以将起搏脉冲定时为每个患者的目标心率。为了调整患者的心率,起搏器调整起搏脉冲之间的间期。例如,为了增大患者的心率,减小从起搏器生成的脉冲之间的间期。相反,为了减小患者的心率,增大脉冲之间的间期。在一个或多个实施例中,锻炼方案可以被配置成包括与恢复间期(即,比紧接在前的锻炼间期更低的较低目标心率)交错的锻炼间期(即,比患者的静息心率水平更高的较高目标心率)。用于锻炼心脏的一个目标心率区可以是患者最大心率的50%-85%。在一个或多个实施例中,目标心率区可以被设置为患者最大心率区的75-95%。在一个或多个其他实施例中,目标心率区可被设置为患者最大心率区的105%达短的时间段(例如,多至20分钟或多至30分钟等)。
可以通过使用基本频率来实现运动方案,该运动方案包括与恢复频率间期(也被称为降低的频率间期)交错的一组增大的频率间期,该基本频率可以通过修改每个间期的起搏脉冲来被调整。例如,如果静息心率是基本心率(间期根据该基本心率而被测得),则可以通过以下方式来确定第一增大频率:将该患者的平均静息心率(例如60HBM)加上用于该特定间期的预先指定数量的HBM(例如20HBM等),以获得在第一时间段(例如,10分钟)内的80HBM(即,60HBM+20HBM)。由于目标心率水平现在为80HBM,因此可以减小从起搏器生成的脉冲之间的间期。
起搏器可以被配置成将最大心率水平用作基本心率,并将目标频率从最大心率向下调整至目标心率区(例如最大心率区的50%-85%)。可以通过使用患者的跟踪日常活动或使用已知公式(即220HBPM减去患者的年龄)来确定患者的最大心率。最大心率可取决于多种因素,包括患者的年龄、身体活动和心脏状况。
如果将该IPG编程为频率应答模式,则由一个或多个生理传感器输出的信号被用作频率控制参数(RCP)以导出生理逸搏间期。例如,与在所描绘的示例性IPG电路31中的患者活动传感器(PAS)电路35中获得的患者的活动水平成比例地调整逸搏间期。患者活动传感器35被耦合至IPG壳体,并且可采取本领域熟知的压电晶体换能器的形式,并且其输出信号被处理并用作RCP。传感器316响应于感知到的身体活动而生成电信号,这些电信号由活动电路35处理并被提供给数字控制器/定时器电路83。活动电路35和相关联的传感器316可对应于美国专利第5,052,388号和第4,428,378号中公开的电路系统。
常规的起搏器当前被配置成自动跟踪人的心率达特定时间段(例如1天),并响应于患者的活动而定制起搏脉冲间期。活动传感器全天感测这个人的活动,并且处理器根据患者的活动调整起搏器的起搏频率。在人的心率已被跟踪达一天之后,自动地执行频率分布(profile)优化,如在美敦力手册CLARIA MRI
类似地,可结合诸如氧合传感器、压力传感器、pH传感器和呼吸传感器(所有这些都公知用于提供频率应答起搏能力)之类的替代类型的传感器来实践本发明。替代地,QT时间可用作频率指示参数,在这种情况下不需要额外的传感器。类似地,还可在非频率应答起搏器中实践本发明。
借助于遥测天线57和相关联的RF收发器41来完成去往和来自外部编程器的数据传输,RF收发器41用于解调所接收的下行链路遥测和传输上行链路遥测两者。如起搏领域所公知的,上行链路遥测能力将通常包括用于传输所存储的数字信息(例如,操作模式和参数、EGM直方图、和其他事件、以及指示心房和心室中所感知的和起搏的去极化的发生的心房和/或心室电活动和标记通道脉冲的实时EGM)的能力。
微计算机33包含微处理器80和相关联的系统时钟,并且分别包含处理器上RAM和ROM芯片82A和82B。此外,微计算机电路33包括单独的RAM/ROM芯片82C以提供额外的存储器容量。微处理器80通常以降低的功率消耗模式来进行操作,并且是中断驱动的。微处理器80响应于限定的中断事件而被唤醒,该限定的中断事件可包括由数字定时器/控制器电路83中的定时器生成的A-触发(TIRG)信号、RV-触发信号、LV-触发信号,以及由感测放大器电路55生成的A-事件信号、RV-事件信号和LV-事件信号等等。通过微计算机电路33借助于数据和控制总线306根据编程(programmed-in)的参数值和操作模式来控制由数字控制器/定时器电路83进行倒计时(time out)的间期和延迟的特定值。此外,如果被编程成作为频率应答起搏器来操作,则可以例如每周期或每两秒提供定时中断,以便允许微处理器分析活动传感器数据并更新基本A-A、V-A或V-V逸搏间期(如适用)。此外,微处理器80还可以用于限定可变的、可操作的AV延迟间期以及被递送至每个心室的能量。
在一个实施例中,微处理器80是适合于以常规方式获取并执行存储在RAM/ROM单元82C中的指令的定制微处理器。然而,所设想的是,其他实现可适用于实践本发明。例如,现成的可商购的微处理器或微控制器、或者定制的专用硬接线逻辑或状态机型电路可以执行微处理器80的功能。
数字控制器/定时器电路83在微计算机33的总体控制下进行操作以便控制起搏电路内的计时功能和其他功能,并且包括一组计时电路和相关联逻辑电路,描绘了该一组计时电路和相关联逻辑电路中的与本发明有关的某些电路。所描绘的计时电路包括URI/LRI定时器83A、V-V延迟定时器83B、用于对过去的V-事件到V-事件间期或V-事件到A-事件间期或V-V传导间期进行计时的固有间期定时器83C、用于对A-A、V-A和/或V-V起搏逸搏间期进行计时的逸搏间期定时器83D、用于对自在前的A-事件或A-触发起的A-LVp延迟(或A-RVp延迟)进行计时的AV延迟间期定时器83E、用于对心室后时间段进行计时的心室后定时器83F、以及日期/时间时钟83G。
AV延迟间期定时器83E加载有用于一个心室腔的适当延迟间期(即,使用已知方法所确定的A-RVp延迟或A-LVp延迟),用于对从在前的A-起搏或A-事件的开始进行倒计时。间期定时器83E触发起搏刺激递送,并且可以基于一个或多个先前的心动周期(或来自针对给定患者根据经验导出的数据集)。
事件后定时器83F对在RV-事件或LV-事件或RV-触发或LV-触发之后的心室后时间段或在A-事件或A-触发之后的心房后时间段进行倒计时。事件后时间段的持续时间还可以被选择作为存储在微计算机33中的可编程参数。心室后时间段包括PVARP、心房后心室消隐期(PAVBP)、心室消隐期(VBP)、心室后心房消隐期(PVARP)和心室不应期(VRP),但是也可以至少部分地根据起搏引擎中采用的操作电路系统而适当地定义其他时段。心房后时间段包括心房不应期(ARP)(在所述心房不应期期间,出于重置任何AV延迟的目的而忽略A-事件)以及心房消隐期(ABP)(在所述心房消隐期期间,禁用心房感测)。应当注意的是,心房后时间段和AV延迟的开始可与每个A-事件或A-触发的开始或结束基本上同时开始,或者在A-触发的情况下,可以在A-触发之后的A-起搏结束时开始。类似地,心室后时间段和V-A逸搏间期的开始可以与V-事件或V-触发的开始或结束基本上同时开始,或者在V-触发的情况下,在可以在V-触发之后的V-起搏结束时开始。微处理器80还可选地计算AV延迟、心室后时间段和心房后时间段,其随着响应于RCP(多个)而建立的基于传感器的逸搏间期和/或随着固有心房率而变化。
输出放大器电路51包括RA起搏脉冲发生器(以及LA起搏脉冲发生器,如果提供LA起搏的话)、RV起搏脉冲发生器和LV起搏脉冲发生器,或者与目前在提供心房和心室起搏的市售心脏起搏器中使用的那些中的任一个相对应。为了触发RV-起搏或LV-起搏脉冲的生成,数字控制器/定时器电路83在A-RVp延迟的超时(在RV预激的情况下)时生成RV-触发信号或在A-LVp延迟的超时(在LV预激的情况下)时生成LV-触发,所述A-RVp延迟的超时和A-LVp延迟的超时由AV延迟间期定时器83E(或V-V延迟定时器83B)提供。类似地,在由逸搏间期定时器83D计时的V-A逸搏间期结束时,数字控制器/定时器电路83生成触发RA-起搏脉冲的输出的RA-触发信号(或触发LA-起搏脉冲的输出的LA-触发信号,如果提供的话)。
输出放大器电路51包括开关电路,以用于将来自引线导体和中性罐(IND_CAN)电极20之间的选定起搏电极对耦合至RA起搏脉冲发生器(和LA起搏脉冲发生器,如果提供的话)、RV起搏脉冲发生器和LV起搏脉冲发生器。起搏/感测电极对选择和控制电路53选择要与输出放大器电路51内的心房和心室输出放大器耦合的引线导体和相关联的起搏电极对,以用于完成RA、LA、RV和LV起搏。
感测放大器电路55包含与在用于心房和心室起搏和感测的当代心脏起搏器中目前被采用的那些感测放大器中的任意感测放大器相对应的感测放大器。在本领域中已经普遍的是使用非常高的阻抗的P波和R波感测放大器来放大由心脏去极化波前的通过而跨感测电极对生成的电压差信号。高阻抗感测放大器使用高增益来放大低振幅信号,并且依赖于通带滤波器、时域滤波、以及振幅阈值比较来从背景电噪声中区分P波或R波。数字控制器/定时器电路83控制心房和心室感测放大器55的灵敏度设置。
感测放大器通常在向起搏系统的起搏电极中的任意电极递送起搏脉冲之前、期间和之后的消隐期期间与感测电极解耦合,以避免感测放大器的饱和。感测放大器电路55包括消隐电路,该消隐电路用于在ABP、PVABP和VBP期间将引线导体和IND_CAN电极20的选定对与RA感测放大器(以及LA感测放大器,如果提供的话)、RV感测放大器和LV感测放大器的输入解耦合。感测放大器电路55还包括开关电路,该开关电路用于将选定的感测电极引线导体和IND_CAN电极20耦合至RA感测放大器(以及LA感测放大器,如果提供的话)、RV感测放大器和LV感测放大器。再次,感测电极选择和控制电路53选择待与输出放大器电路51和感测放大器电路55内的心房和心室感测放大器耦合的导体和相关联的感测电极对,以用于沿着所期望的单级和双极感测向量完成RA、LA、RV和LV感测。
由RA感测放大器感知到的RA-感测信号中的右心房去极化或P波导致被传送至数字控制器/定时器电路83的RA-事件信号。类似地,由LA感测放大器(如果提供的话)感知到的LA-感测信号中的左心房去极化或P波导致被传送至数字控制器/定时器电路83的LA-事件信号。由心室感测放大器感知到的RV-感测信号中的心室去极化或R波导致被传送至数字控制器/定时器电路83的RV-事件信号。类似地,由心室感测放大器感知到的LV-感测信号中的心室去极化或R波导致被传送至数字控制器/定时器电路83的LV-事件信号。RV-事件信号、LV-事件信号、以及RA-事件信号、LA-感测信号可以是不应的或非不应的,并且可以不经意地由电噪声信号或异常传导的去极化波触发,而不是由真正的R波或P波触发。
图5是根据本公开的示例的使用起搏器来在一段时间内递送能够重塑心脏的起搏治疗的方法的流程图。在一个或多个实施例中,起搏治疗可导致心脏重塑。根据一个示例,可以使用心房引线22来递送用于心脏重塑的起搏治疗,该心房引线22被定位在AV结/高隔膜区域附近以经由尖端电极50和环形电极48来递送起搏。技术人员理解的是,可以使用其他起搏向量来使心脏起搏(例如,在2018年11月3日提交的美国专利申请第62/581,486号和2018年10月17日提交的美国专利申请第62/573,685号中所述的希氏束治疗,这些专利申请通过引用以其整体被并入)。根据本公开的一个示例,可以在一天中的预定时间处递送重塑起搏治疗。例如,当患者最有可能不活动时(例如,患者睡着或处于仰卧位),可以递送起搏治疗。可以以多种方式确定不活动(例如,检测监测、从具有传感器的穿戴式设备(例如,诸如Garmin
在确定安排重塑起搏治疗的递送时(框100中的“是”),处理器80可以以预定频率和/或持续时间来递送重塑起搏治疗(框102)。例如,处理器80可以使重塑起搏以升高的频率(例如,100bpm达30分钟的持续时间)被递送,或者在另一示例中以升高的频率(例如,100bpm等达特定时间段,例如每天5小时)被递送。在另一示例中,处理器80可以使重塑起搏以初始较低频率(诸如70bpm)被递送,并逐渐将患者的心率增大到例如预定的心率阈值(诸如100bpm)。下面详细描述用于以可变的频率和/或持续时间递送重塑起搏的示例性模式。附加地,以经调整的起搏参数(例如,振幅等)锻炼心脏可以持续一段时间,以增大心率,和/或直到检测到终止状况为止。
一旦发起重塑起搏的递送(框102),处理器80就可以开始监测由所递送的重塑起搏导致的患者的症状(框104)。此外,处理器80可以监测是否已经从患者接收到患者激动信号。患者激动信号的示例可以是由患者发起的并且指示患者由于所递送的重塑起搏而正经历不适的信号,或者是从活动传感器35接收到的并且指示患者不再睡着或处于仰卧位的信号(框106)。如果处理器80确定已经接收到患者激动信号(框106中的“是”),则处理器80暂停重塑起搏治疗的递送(框116),并等待用于重塑起搏的递送的下一个安排的会话(框100)。
基于所监测到的症状(框104),并且如果尚未接收到患者激动信号(框106中的“否”),则处理器80确定所递送的重塑起搏是否导致可测量的影响,该可测量的影响将指示重塑起搏的递送对引起患者心脏状况的某种程度的正常化是有效的。例如,处理器80可以监测一个或多个参数的变化,诸如组织灌注、心房灌注、估计的肺动脉舒张压(ePad)、右心室压力、左心室压力、和压力替代(诸如阻抗),作为重塑起搏正以指示存在某种程度的心脏正常化的方式影响患者心脏的整体状况的指示符。在一个或多个其他实施例中,在一段时间之后自动地递送和/或暂停治疗(例如,在递送起搏后
在一个示例中,为了确定是否存在可测量的正常化影响(框108),处理器80可以确定与患者相关联的灌注是否存在变化。例如,可以通过以下方式来确定组织灌注的变化:在重塑起搏治疗的递送期间测量组织灌注,并且将所测得的组织灌注与在重塑起搏被递送给患者之前(例如,诸如在植入该设备时)确定的非起搏基线组织灌注水平进行比较。尽管下面的描述使用组织灌注作为调整治疗的目标参数,但是也可以使用上面提到的其他参数。
如果当前测得的组织灌注水平相对于基线组织灌注水平没有增大,则处理器80确定所递送的重塑起搏尚未导致指示心脏正常化的可测量的影响(框108中的“否”)。随后作出关于是否调整重塑起搏的递送的确定(在框110),以便增大后续递送的重塑起搏将导致指示心脏正常化的可测量影响的可能性。
图6是示出重塑起搏对患者的心输出量的影响的图形表示。心输出量(CO)是指每分钟由心脏泵送的血液量,并且是心率(HR)或每分钟的搏动次数与每搏输出量(SV)的乘积,所述每搏输出量是每次搏动泵送的血液量,因此CO=HR x SV。如图6所示,心输出量通常随着心率的增大而增大,直到达到心输出量的最大增大113为止。该最大输出量113往往因患者而异,并且对于单个患者可能有所不同,这取决于患者心脏的当前状况。一旦达到最大心输出量113,起搏的心率的任何进一步增大都会导致患者心输出量的减少115,并可能指示对患者心脏状况的有害影响。
因此,为了确定是否调整起搏治疗(图5的框110),当未检测到指示心脏正常化的可测量的影响时(框108中的“否”),处理器80可以在患者的心输出量的斜率被确定为正在增大的情况下,确定调整起搏治疗(框110中的“是”)。处理器80随后可以通过增大重塑起搏的频率和/或持续时间来调整重塑起搏(框112)。典型的干预调整偏好增大最大起搏频率,而增加持续时间作为次级调整将使频率影响变得有症状。然而,如果未确定患者的心输出量的斜率正在增大,则处理器80确定不调整起搏治疗(框110中的“否”)。
一旦处理器80确定调整治疗(框110中的“是”)并因此调整了重塑起搏(框112),或者处理器80确定不调整治疗(框110中的“否”),就作出关于会话时间是否已结束的确定(框114)。例如,处理器80可以确定是否以至少100bpm的频率递送重塑起搏治疗达一定的时间段(例如30分钟等),或者在另一示例中,是否以至少100bpm的频率递送重塑起搏治疗达每天5小时。
如果会话时间尚未结束(框114中的“否”),则处理器80使用相同或经调整的频率和/或持续时间继续递送重塑起搏治疗(框102)。另一方面,如果会话时间已经结束(框114中的“是”),则处理器80暂停重塑起搏治疗的递送(框116),并等待下一个安排的会话以用于重塑起搏的递送(框100)。
如果当前测得的组织灌注水平相对于基线组织灌注水平已增大,则处理器80确定所递送的重塑起搏已导致指示心脏正常化的可测量的影响(框108中的“是”)。随后作出关于该影响是否大于预定的症状避免阈值的确定(框118),该预定的症状避免阈值指示重塑起搏对患者来说过于激进。如果确定该影响大于预定的症状避免阈值(框118中的“是”),则处理器80确定是调整并继续递送经调整的重塑起搏治疗,还是暂停重塑治疗的递送以解决重塑起搏对患者来说过于激进的指示(框120)。
例如,如果在重塑起搏的递送期间发生的室性早搏(PVC)的数量增加,则处理器80可以确定该影响大于预定的症状避免阈值(框118中的“是”),并因此确定重塑治疗过于激进。当增加的PVC是在框118中用于确定重塑起搏过于激进的指示时,处理器80确定不暂停重塑起搏的递送(框120中的“否”),并因此通过将起搏的递送频率降低预定的量来调整起搏治疗(框120中的“是”)。例如,递送频率可以每分钟减少10次搏动。在另一示例中,处理器80可以跟踪原始基线斜率,并且当该斜率偏离基线斜率预定量或预定百分比时暂停治疗。
在另一示例中,如果确定满足收缩性度量(measure)阈值,则处理器80可以确定该影响大于预定的症状避免阈值(框118中的“是”),并且因此确定重塑治疗过于激进。例如,确定是否满足收缩性度量可以包括:确定在所递送的重塑起搏期间,是否存在经由心音传感器感知到的S1和S2心音的振幅减小,或者是否经由心脏传感器感知到S3心音。许多起搏器被配置成检测心音。可从位于明尼苏达州明尼阿波利斯的美敦力公司获得的示例性起搏器AMPLIA
在又另一示例中,如果生物标志物指示符超过生物标志物指示符阈值,则处理器80可以确定该影响大于预定的症状避免阈值(框118中的“是”),并且因此确定重塑治疗过于激进。例如,确定生物标志物指示符是否超过生物标志物指示符阈值可包括:确定用于诊断充血性心力衰竭(CHF)的生物标志物指示符(诸如,脑钠肽(BNP),也被称为B型钠尿肽)是否增加超过指示CHF的预定阈值。当生物标志物指示符是被用于确定重塑治疗过于激进的指示时,处理器80确定由于该指示而暂停重塑起搏的递送(框120中的“是”),并因此暂停重塑起搏治疗的递送(框116),并且等待用于重塑起搏的递送的下一安排的会话(框100)。
在另一示例中,如果确定ST段测量结果满足ST段阈值,则处理器80可以确定该影响大于预定的症状避免阈值(框118中的“是”),并且因此确定重塑治疗过于激进。例如,可以基于由IMD 16感知到的ECG信号或者基于由另一内部或外部监测设备从替代位置感知到的EGM心脏信号,来确定在所递送的重塑起搏期间的ST段测量结果。在一个或多个实施例中,数据被存储(诸如,存储在表格中)到针对患者的存储器中,其中数据将ST段与可接受的起搏治疗结果进行关联从而起搏可以继续和/或ST段与过于激进的起搏治疗相关联以便暂停治疗。将在所递送的起搏期间确定的ST段测量结果与ST阈值(该ST阈值可以在非起搏心脏活动期间被确定)进行比较,并且如果确定发生ST段测量结果的增大,则确定满足ST段阈值。当ST段测量结果的变化是在框118中用于确定重塑治疗过于激进的指示时,处理器80确定不暂停重塑起搏的递送(框120中的“否”),并因此通过将起搏的递送频率降低预定的量来调整起搏治疗(框120中的“是”)。
一旦处理器80为了解决重塑起搏治疗的实例过于激进(框118中的“是”),或为了解决重塑起搏治疗的实例没有导致存在可测量的正常化影响(框108中的“否”),而调整重塑起搏的递送(框112),就作出有关会话时间是否结束的确定(框114)。例如,处理器80可以确定重塑起搏治疗是否已经以至少100bpm的频率被递送达30分钟。在另一示例中,处理器80可以确定重塑起搏治疗是否已经以至少100bpm的频率被递送达每天5个小时持续两周的时间段。如果会话时间尚未结束(框114中的“否”),则处理器80继续递送重塑起搏治疗(框102),并且该治疗继续。另一方面,如果会话时间已经结束(框114中的“是”),则处理器80暂停重塑起搏治疗的递送(框116),并等待下一个安排的递送重塑起搏会话(框100)。
以此方式,根据本公开的示例的用于递送心脏重塑起搏治疗的方法可以包括:处理器80经由心房引线22的尖端电极50和环形电极48感测心脏信号300并监测心脏症状,以确定是否由于所递送的重塑起搏而诱导出不期望的症状。例如,处理器80可以递送心脏重塑起搏以刺激患者心脏状况的正常化,响应于所递送的重塑起搏而监测一个或多个参数,响应于该监测而确定对心脏正常化的影响,并响应于所确定的对心脏正常化的影响而调整重塑起搏。
图7是根据本公开的示例的递送用于心脏重塑的起搏治疗的方法的流程图。根据另一示例,在重塑起搏治疗的实时递送期间,处理器80可基于短期症状避免因素来确定是否由于所递送的重塑起搏而诱导出不期望的症状,并相应地调整或暂停所递送的治疗,如以上所述的。另外,处理器80还可监测长期功效改善因素,以确定是否存在由于在延长的时间段内所递送的重塑起搏治疗而导致的心脏状况的长期改善。具体而言,例如,一旦重塑起搏治疗已被递送达预定的长期时间段(诸如,以至少100bpm的频率被递送达每天5小时持续例如两周的时间段),处理器80就可以开始执行对重塑起搏的影响的长期监测,以确定是否存在朝向心脏正常化的期望水平的改善。
例如,如图7的示例中所示的,对如上所述的所递送的重塑起搏的连续实时监测101期间,处理器80评估所递送的重塑起搏的长期影响,以确定重塑起搏是否已导致患者心脏的成功正常化。例如,一旦处理器80确定到了执行对重塑起搏的长期监测的时间(框200中的“是”),即,例如当确定重塑起搏已经以至少100bpm的频率被递送达每天5小时持续两周的时间段时,处理器80就开始监测与重塑起搏的长期递送相关联的一个或多个长期参数(框202),并且评估所递送的重塑起搏的长期影响,以确定重塑起搏是否已导致患者心脏的成功正常化。随后基于长期参数,作出关于是否调整重塑起搏的确定(框204)。如果处理器80确定长期参数指示应调整重塑起搏(框204中的“是”),则处理器80调整重塑起搏(框206),并等待下一个安排的时间以执行对重塑起搏的长期监测(框200中的“是”)。另一方面,如果处理器80确定长期参数指示不应调整重塑起搏(框204中的“否”),则处理器80可以确定是否监测附加的长期参数(框208)以确定附加的长期参数是否指示重塑起搏已导致患者心脏的成功正常化。
如果附加的长期参数未被确定(框208中的“否”),则处理器80等待下一个安排的时间来执行对重塑起搏的长期监测(框200中的“是”)。如果附加的长期参数要被确定(框208中的“是”),则处理器80监测附加的长期参数(框202),以确定附加的长期参数是否指示重塑起搏已导致患者心脏的成功正常化。随后基于附加的长期参数,作出关于是否调整重塑起搏的确定(框204)。如果处理器80确定附加的长期参数指示应调整重塑起搏(框204中的“是”),则处理器80调整重塑起搏(框206),并等待下一个安排的时间来执行对重塑起搏的长期监测(框200中的“是”)。另一方面,如果处理器80确定该附加的长期参数指示不应调整重塑起搏(框204中的“否”),则处理器80可以确定是否监测附加的长期参数(框208)。
以此方式,在一个示例中,处理器80可监测单个长期参数以确定该长期参数是否指示应调整重塑起搏。在另一示例中,处理器80可以监测多个长期参数以确定这些长期参数中的至少一个是否指示应当调整重塑起搏。
根据一个示例,处理器80可以监测患者的QRS持续时间(框202),以确定QRS持续时间是否由于所递送的重塑起搏而随着时间增大。如果QRS持续时间被确定为增大,则处理器80确定重塑起搏应该被调整(框204中的“是”),并且因此通过降低所递送的重塑起搏的频率和/或持续时间来进行调整(框206),并等待下一个安排的时间来执行对重塑起搏的长期监测(框200中的“是”)。另一方面,如果未确定QRS持续时间增大,则处理器80确定不应调整重塑起搏(框204中的“否”)。
在另一示例中,处理器80可以监测一个或多个昼夜节律参数(框202),以确定是否调整重塑起搏将被递送的时间段。例如,假设处理器80在一天中患者最可能不活动的预定时间期间(诸如,在凌晨12点至凌晨5点之间)递送重塑起搏,如上所述,则处理器80可以将重塑起搏要被递送的时间段划分为预定的时间分段(例如,诸如20分钟时间分段),并针对这些20分钟时间分段中的每一个或针对该分段期间的预定数量的搏动,确定是否发生指示AV阻滞的缺乏从心房到心室的传导达该20分钟时间分段。处理器80随后通过如下方式来调整用于重塑起搏的递送的时间段(框204):在初始递送时段(即,在凌晨12点至凌晨5点之间)中的AV阻滞被确定为可能发生的那些20分钟时间分段期间不递送重塑起搏。
除先前描述的起搏算法外,起搏器还可以使用一个或多个起搏方案来重塑心脏。在另一示例中,处理器80可以仅表征患者全天的昼夜节律,在这些节律期间递送快速起搏,并基于所递送的快速起搏来确定患者的心脏何时可能以更正常的方式传导,从而指示AV阻滞的可能性较小。处理器80随后通过在AV阻滞不太可能发生的那些时段期间递送重塑起搏,来调整用于重塑起搏的递送的时间段(框204)。以这种方式,处理器利用昼夜节律参数来学习或确定何时递送重塑起搏,而不是仅在固定的时间段期间递送重塑起搏。
在另一示例中,处理器80可以监测一个或多个长期参数(框202),以标识是否存在心脏正常化的阈值水平的长期改善。例如,如果患者的心输出量的斜率增大,则处理器80可以确定存在阈值水平的长期改善。如果存在阈值水平的长期改善,则处理器80可以调整重塑起搏的频率和/或持续时间。在另一示例中,如果存在肺动脉压力的期望变化、或阻抗的期望变化(诸如指示心脏腔室舒张的阻抗偏移),则处理器80可以确定存在阈值水平的长期改善。如果存在由于所递送的重塑起搏而导致的阈值水平的长期改善,则处理器80可以增大所递送的重塑起搏的频率和/或持续时间(框206)。
在另一示例中,处理器80可以被编程为利用预定的占空比范围(诸如,在每天4小时的最小时间段与每天8小时的最大时间段之间的范围)来递送重塑起搏。以此方式,如果存在由于所递送的重塑起搏而导致的阈值水平的长期改善,则处理器80可增大所递送的重塑起搏的持续时间(框206),除非已达到最大占空比。一旦已经达到最大占空比,处理器80就可以以最大占空比维持重塑起搏的递送。
图8是根据本公开的示例的递送用于心脏重塑的起搏治疗的方法的流程图。根据另一示例,一旦处理器80确定到了执行对重塑起搏的长期监测的时间(框200中的“是”),处理器80就开始监测与重塑起搏的长期递送相关联的一个或多个长期参数(框202),并且评估所递送的重塑起搏的长期影响,以确定是否应暂停重塑起搏。
如图8中所示,对长期参数的监测(框202)可以包括:处理器80监测参数以确定是暂停重塑起搏的递送(框210中的“是”),还是维持在当前设定的频率和/或持续时间下的重塑起搏的递送(框210中的“否”)。例如,对长期参数的监测(框202)可包括:监测在延长的时间段内到患者的静息心率的恢复,以确定患者的长期静息心率是否发生变化。
例如,处理器80可以确定恢复率,该恢复率与在所递送的重塑起搏期间导致的升高的心率下的重塑起搏的递送之后心率返回到静息心率的时间量相关联。将确定的恢复率与例如在植入时确定的基线恢复率进行比较。如果在例如诸如一星期之类的长期时间段内与所确定的恢复率相关联的时间量没有减少,则处理器80确定长期参数指示重塑起搏不应暂停(框210中的“否”),并且因此以当前的频率和/或持续时间继续或维持重塑起搏的递送。如果与所确定的恢复率相关联的时间量减少,则处理器80确定重塑起搏已导致期望水平的患者心脏状况的正常化,并且因此应当暂停重塑起搏的递送(框210中的“是”),并因此暂停重塑起搏的递送(框212)。
在另一示例中,如果处理器80基于所确定的恢复率确定长期参数指示不应暂停重塑起搏(框210中的“否”),并因此以当前的频率和/或持续时间继续或维持重塑起搏的递送,则处理器80可以确定是否监测附加的长期参数(框214),以确定附加的长期参数是否指示应该暂停重塑起搏。
在另一示例中,对长期参数的监测(框202)可以包括在延长的时间段内监测心脏收缩时间间期(STI),以确定患者的长期STI是否发生变化。将当前的长期STI与例如在植入时确定的基线STI进行比较。如果STI不存在预定的减小,诸如减小30%,则处理器80确定长期参数指示不应暂停重塑起搏(框210中的“否”),并因此以当前的频率和/或持续时间继续或维持重塑起搏的递送。如果当前确定的STI存在预定的减小,则处理器80确定重塑起搏已导致期望水平的患者心脏状况的正常化,并且因此应当暂停重塑起搏的递送(框210中的“是”),并因此暂停重塑起搏的递送(框212)。
在另一示例中,如果处理器80基于所确定的STI的减小确定长期参数指示不应暂停重塑起搏(框210中的“否”),并因此以当前的频率和/或持续时间继续或维持重塑起搏的递送,则处理器80可以确定是否监测附加的长期参数(框214),以确定附加的长期参数是否指示应该暂停重塑起搏。
在另一示例中,对长期参数的监测(框202)可包括:在延长的时间段内监测用于诊断充血性心力衰竭(CHF)的生物标志物指示符(诸如,例如脑钠肽(BNP)),以确定是否存在生物标志物的变化,该生物标志物的变化将指示所递送的重塑起搏已导致期望水平的患者心脏状况的正常化。将在长的时间段内测得的生物标志物与例如在植入时确定的基线测量结果进行比较。如果不存在生物标志物的预定的长期变化,则处理器80确定该长期参数指示不应暂停重塑起搏(框210中的“否”),并因此以当前的频率和/或持续时间继续或维持重塑起搏的递送。如果生物标志物存在预定的长期变化,则处理器80确定重塑起搏已导致期望水平的患者心脏状况的正常化,并且因此应当暂停重塑起搏的递送(框210中的“是”),并因此暂停重塑起搏的递送(框212)。
在另一示例中,如果处理器80基于所确定的STI的减小确定长期参数指示不应暂停重塑起搏(框210中的“否”),并因此以当前的频率和/或持续时间继续或维持重塑起搏的递送,则处理器80可以确定是否监测附加的长期参数(框214),以确定附加的长期参数是否指示应该暂停重塑起搏。
图9是根据本公开的示例的递送重塑起搏治疗的方法的流程图。如图9所示,为了增大重塑起搏的递送将有效地引起期望水平的患者心脏状况的正常化的可能性,处理器80可以在多个间期期间递送重塑起搏,其中多个间期以增大心脏的肌肉耐力的方式改变重塑起搏的频率和/或持续时间。例如,处理器80可以以当前设定的频率递送重塑起搏(框300)达预定的持续时间,并且一旦已经以当前的频率递送重塑起搏达当前的持续时间(框302中的“是”),就确定是否将频率从当前频率调整到下一频率(框304),和/或确定是否将持续时间从当前持续时间调整到下一持续时间(框308)。
以此方式,一旦已经以当前的频率递送重塑起搏达当前的持续时间(框302中的“是”),处理器80就仅调整频率(框306)并以经调整的频率递送下一重塑起搏间期(框312)达当前的持续时间,仅调整持续时间(框310)并以当前的频率并以经调整的下一持续时间递送下一重塑起搏间期(框312),调整当前频率(框306)和持续时间(框310)两者并以经调整的频率递送下一重塑起搏间期(框312)达经调整的持续时间,或不对频率或持续时间进行调整并继续以当前的频率递送下一重塑起搏间期(框312)达当前的持续时间。一旦持续时间在下一重塑起搏的递送期间期满(框302中的“是”),就重复该过程以生成下一重塑起搏递送间期,直到当前重塑起搏递送会话已结束为止。
以此方式,处理器80可以在具有第一频率和第一持续时间的第一间期期间递送重塑起搏,确定是否要调整在第一间期之后的下一间期期间递送重塑起搏期间的第一频率和第一持续时间中的一者或两者,并响应于该确定而在下一间期期间递送重塑起搏,使得下一间期可以包括被递送的重塑起搏具有以下各项中的一项:第一频率与第一持续时间两者、经调整的频率与第一持续时间、第一频率与经调整的持续时间、以及经调整的频率与经调整的持续时间两者。
特别地,在一个示例中,重塑起搏的递送可以包括预热间期,在该预热间期期间,重塑起搏以略高于与患者相关联的静息心率的频率被递送达初始持续时间,随后是积累间期,在该积累间期期间,重塑起搏以增大的频率被递送达相对于初始持续时间较短的持续时间。一旦在积累间期期间完成重塑起搏的递送,重塑起搏就可以使用初始间期的频率和持续时间来被递送,以生成重塑起搏的上/下递送,或者可以以增大的频率、以增大的持续时间、或以增大的频率和持续时间等来被递送。以这种方式,重塑起搏可以以反复上升和/或下降的模式来被递送,以增加肌肉耐力,并由此增大重塑起搏的递送将有效地引起期望水平的患者心脏状况的正常化的可能性。
在一个示例中,重塑起搏的递送可以包括:10分钟的预热间期(第一时间段),在该预热间期期间,重塑起搏以刚好高于患者的静息频率的低频率(用于将心率增大多至高于静息心率每分钟30次心跳(HBM)的第一频率)被递送;随后是3分钟的第一积累间期,在该第一积累间期期间,重塑起搏以最大频率(诸如,高于第一心率多至50HBM)被递送;随后是第二间期(例如2分钟间期),在该第二间期期间,重塑起搏以小于最大频率的频率被递送;随后是第三积累间期(例如2分钟间期),在该第三积累间期期间重塑起搏以最大频率被递送;随后是一分钟时间间期,在该一分钟时间间期期间,重塑起搏以小于最大频率的频率被递送;随后是一分钟时间间期,在该一分钟时间间期期间,重塑起搏以最大频率被递送;随后是1分钟时间间期,在该1分钟时间间期期间,重塑起搏以小于最大频率的频率被递送。随后可以重复该过程。例如,可重复实施此算法高达每天1小时。
在另一示例中,重塑起搏的递送可以包括以相同的频率但是以不同的持续时间递送。例如,重塑起搏的递送可以包括:在两分钟间期(第一间期)期间以给定频率(第一频率)递送重塑起搏;随后是在四分钟间期(第二间期)期间以相同的频率递送重塑起搏;随后是在六分钟间期(第三间期)期间以相同的频率递送重塑起搏;随后是在另一个六分钟间期(第四间期)期间以相同的频率递送重塑起搏;随后是四分钟间期(第五间期)期间以相同的频率递送重塑起搏;以及随后是在两分钟间期(第六间期)期间以相同的频率递送重塑起搏。在另一示例中,递送可以在不同的间期中的每一个之间包括恢复间期(第七间期),在所述恢复间期期间以降低的频率和减少的持续时间递送重塑起搏。可重复实施此算法高达每天1小时。
在另一示例中,可以以步进模式来递送重塑起搏,该步进模式包括:预热间期(允许心率逐渐积累多达20HBM的第一间期),在该预热间期期间重塑起搏以最小频率(例如,将心率提高多达30HBM)被递送;随后是积累间期,在该积累间期期间,重塑起搏以比预热间期期间递送的最小频率更大的第一频率被递送;随后是另一积累间期,在该另一积累间期期间,重塑起搏以第二频率被递送,该第二频率大于最小频率(例如,将心率增大到比第一频率高多达30HBM),并且等于或大于在先前的积累间期期间使用的第一频率。可重复实施此算法高达每天1小时。
在另一个示例中,重塑起搏的递送可以包括:初始间期(多达3至5分钟),在该初始间期期间,重塑起搏以高频率被递送(从而导致心率增大多达50HBM);随后是下一间期,在该下一间期期间,重塑起搏以降低的频率(将HBM从第一间期减小20HBM)被递送,或者重塑起搏的递送可以包括:初始间期,在该初始间期期间,重塑起搏以降低的频率被递送;随后是下一间期,在该下一间期期间,重塑起搏以高频率被递送,可包括两者之间的交替。
以这种方式,重塑起搏的递送可以包括在长或短的时间段(诸如几天或一个或多个星期)内递送的不同频率和/或持续时间模式的多种组合。此外,还可以包括恢复间期,在该恢复间期期间,重塑起搏的递送被抑制达一段时间,或者以降低的频率和/或持续时间被递送以允许可变的模式用于重塑起搏的递送,这还可以包括一个或多个预热间期和一个或多个积累间期的组合,从而导致期望水平的患者心脏状况的正常化。
本公开中所描述的技术(包括归因于IMD 16、编程器24、处理器80、或各构成部件的那些技术)可以至少部分地以硬件、软件、固件或它们的任意组合来实现。例如,这些技术的各方面可在一个或多个处理器内实现,该一个或多个处理器包括一个或多个微处理器、DSP、ASIC、FPGA、或任何其他等效的集成或分立逻辑电路系统,以及具体化在编程器中的此类部件(诸如,医生编程器或患者编程器、刺激器、图像处理设备或其他设备)的任何组合。术语“模块”、“处理器”或“处理电路系统”一般可指独立的或结合其他逻辑电路系统的任何前述逻辑电路系统、或任何其他等效电路系统。
此类硬件、软件和/或固件可在相同的设备内或在分开的设备内实现以支持本公开所描述的各种操作和功能。此外,所描述的单元、模块或部件中的任一者可一起被实现,或可被单独地实现为分立但可互操作的逻辑设备。将不同的特征描绘为模块或单元旨在强调不同的功能方面,且并不一定暗示这种模块或单元必须由分开的硬件或软件部件来实现。而是,与一个或多个模块或单元相关联的功能可由分开的硬件或软件部件来执行,或可集成在共同或分开的硬件或软件部件内。
当在软件中实现时,归因于本公开中描述的系统、设备和技术的功能可具体化为计算机可读介质(诸如,RAM、ROM、NVRAM、EEPROM、闪存存储器、磁数据存储介质、光数据存储介质,等等)上的指令。可由一个或多个处理器执行这些指令以支持本公开中所描述的功能的一个或多个方面。
在一个示例中,本文所述的锻炼方案是在患者正睡觉时执行的,然而,该锻炼方案可以在没有检测到任何患者数据(例如,检测到不活动)的情况下执行。附加地,锻炼方案不用于诊断目的;而是,锻炼心脏是为了重塑心脏。
实施例1:一种方法,包括:
递送心脏重塑起搏,以刺激患者心脏状况的正常化;
响应于所递送的重塑起搏而监测一个或多个参数;
响应于该监测,而确定心脏重塑起搏是否对心脏正常化具有影响;以及
响应于所确定的对心脏正常化的影响而调整心脏重塑起搏。
实施例2:一种用于向患者递送心脏重塑起搏的心脏设备,包括:
壳体;
多个电极,该多个电极被电连接到壳体,以递送心脏重塑起搏,以刺激患者心脏状况的正常化;以及
处理器,该处理器被定位在壳体内并且被配置成用于:
响应于所递送的心脏重塑起搏而确定一个或多个参数,
响应于该监测,而确定心脏重塑起搏是否对心脏正常化具有影响,并且
响应于所确定的对心脏正常化的影响而调整心脏重塑起搏。
实施例3:实施例1-2中任一项所述的方法或设备,其中,响应于该监测而确定心脏重塑起搏是否对心脏正常化具有影响包括:
在重塑起搏治疗的递送期间确定组织灌注;
将所确定的组织灌注与在心脏重塑起搏被递送给患者之前确定的非起搏基线组织灌注水平进行比较,
其中,响应于该监测而确定心脏重塑起搏是否对心脏正常化具有影响包括:响应于该比较而确定心脏重塑起搏是否已对心脏正常化具有影响。
实施例4:实施例3中所述的方法或设备,其中,将所确定的组织灌注与在心脏重塑起搏被递送给患者之前确定的非起搏基线组织灌注水平进行比较包括:确定是否存在组织灌注相对于基线组织灌注水平的增大,
其中,响应于该比较而确定心脏重塑起搏是否已对心脏正常化具有影响包括:响应于存在组织灌注相对于基线组织灌注水平的增大,而确定心脏重塑起搏已对心脏正常化具有影响,并且
其中响应于所确定的对心脏正常化的影响而调整心脏重塑起搏包括:响应于确定组织灌注的增大,而调整心脏重塑起搏。
实施例5:实施例4中所述的方法或设备,其中,响应于存在组织灌注相对于基线组织灌注水平的增大而确定心脏重塑起搏已对心脏正常化具有影响包括:确定心脏输出信号的斜率是否正在增大,并且
其中响应于确定组织灌注的增大而调整心脏重塑起搏包括:响应于确定心脏输出信号的斜率正在增大,而调整心脏重塑起搏。
实施例6:实施例1-5中任一项所述的方法或设备,其中,响应于该监测而确定心脏重塑起搏是否对心脏正常化具有影响包括:确定对心脏正常化的影响是否大于症状避免阈值,并且
其中,响应于所确定的对心脏正常化的影响而调整心脏重塑起搏包括:响应于对心脏正常化的影响大于症状避免阈值,而调整心脏重塑起搏。
实施例7:实施例6中所述的方法或设备,其中确定对心脏正常化的影响是否大于症状避免阈值包括:
确定是否存在在心脏重塑起搏的递送期间发生的室性早搏(PVC)的增加;以及
响应于PVC的增加,而确定对心脏正常化的影响大于症状避免阈值。
实施例8:实施例6-7中所述的方法或设备,其中确定对心脏正常化的影响是否大于症状避免阈值包括:
在心脏重塑起搏的递送期间感测心音信号;以及
响应于以下各项中的一项而确定对心脏正常化的影响大于症状避免阈值:S1和S2心音的振幅的减小、以及响应于感知到的心音信号而感知到S3心音。
实施例9:实施例6-8中所述的方法或设备,其中确定对心脏正常化的影响是否大于症状避免阈值包括:
确定在心脏重塑起搏的递送期间生物标志物指示符的增加是否大于指示心力衰竭的阈值;以及
响应于生物标志物指示符的增加大于指示心力衰竭的阈值,而确定对心脏正常化的影响大于症状避免阈值。
实施例10:实施例9中所述的方法或设备,其中,生物标志物指示符包括脑钠肽。
实施例11:实施例6-10中所述的方法或设备,其中,响应于所递送的重塑起搏而监测一个或多个参数包括感测心脏信号,并且
其中,确定对心脏正常化的影响是否大于症状避免阈值包括:
确定在心脏重塑起搏的递送期间是否存在感知到的心脏信号的ST段测量结果的增大;以及
响应于存在ST段测量结果的增大,而确定对心脏正常化的影响大于症状避免阈值。
实施例12:实施例1-11中任一项所述的方法或设备,其中,一个或多个参数包括:组织灌注、心房灌注、估计的肺动脉压力(ePad)、右心室压力、左心室压力、PVC、ST段测量结果、生物标志物指示符、心音和阻抗。
实施例13:一种方法,包括:
递送心脏重塑起搏,以刺激患者心脏状况的正常化;
响应于所递送的心脏重塑起搏,而执行对一个或多个参数的短期监测;
监测指示所递送的心脏重塑起搏对心脏正常化的长期影响的一个或多个长期参数;
响应于该监测,而确定所递送的心脏重塑起搏对心脏正常化的长期影响;以及
响应于短期监测和所确定的对心脏正常化的长期影响中的一者或两者,而调整心脏重塑起搏。
实施例14:一种用于向患者递送心脏重塑起搏的心脏设备,包括:
壳体;
多个电极,该多个电极被电连接到壳体,以递送心脏重塑起搏,以刺激患者心脏状况的正常化;以及
处理器,该处理器被定位在壳体内并且被配置成用于:
响应于所递送的心脏重塑起搏,而执行对一个或多个参数的短期监测,
监测指示所递送的心脏重塑起搏对心脏正常化的长期影响的一个或多个长期参数,
响应于该监测,而确定所递送的心脏重塑起搏对心脏正常化的长期影响,以及
响应于短期监测和所确定的对心脏正常化的长期影响中的一者或两者,而调整心脏重塑起搏。
实施例15:实施例13-14中一项所述的方法或设备,其中,监测指示所递送的心脏重塑起搏对心脏正常化的长期影响的一个或多个长期参数包括:在心脏重塑起搏的递送期间感测心脏信号,
其中,响应于该监测而确定所递送的心脏重塑起搏对心脏正常化的长期影响包括:
响应于感知到的心脏信号,而确定预定的长期时间段内的QRS持续时间,以及
确定QRS持续时间是否正在增大;并且
其中,响应于短期监测和所确定的对心脏正常化的长期影响中的一者或两者而调整心脏重塑起搏包括:响应于QRS持续时间被确定为正在增大,而调整心脏重塑起搏。
实施例16:实施例13-15中一项所述的方法或设备,其中,方法进一步包括或设备的处理器被进一步配置成执行:
在预定的时间段期间递送心脏重塑起搏;以及
将心脏重塑起搏被递送的时间段划分为预定的时间分段,
其中响应于该监测而确定所递送的心脏重塑起搏对心脏正常化的长期影响包括:针对预定的时间分段中的每一个,确定是否正在发生AV阻滞;并且
响应于短期监测和所确定的对心脏正常化的长期影响中的一者或两者而调整心脏重塑起搏包括:响应于确定发生AV阻滞的预定的时间分段,而调整心脏重塑起搏的递送。
实施例17:实施例13-16中一项所述的方法或设备,其中,响应于该监测而确定所递送的心脏重塑起搏对心脏正常化的长期影响包括:
确定心脏输出信号的斜率是否正在增大;以及
响应于确定心脏输出信号的斜率正在增大,而确定心脏正常化的长期改善。
实施例18:实施例13-17中一项所述的方法或设备,其中,监测指示所递送的心脏重塑起搏对心脏正常化的长期影响的一个或多个长期参数包括:在心脏重塑起搏的递送期间感测心脏信号,
其中,响应于该监测而确定所递送的心脏重塑起搏对心脏正常化的长期影响包括:响应于感知到的心脏信号,而确定是否存在指示心脏腔室的舒张的阻抗的预定变化,
其中,响应于短期监测和所确定的对心脏正常化的长期影响中的一者或两者而调整心脏重塑起搏包括:响应于所确定的阻抗变化,而调整心脏重塑起搏的递送。
实施例19:实施例13-18中一项所述的方法或设备,其中,响应于该监测而确定所递送的心脏重塑起搏对心脏正常化的长期影响包括:确定在心脏重塑起搏的长期递送期间的肺压的变化;并且
其中,响应于短期监测和所确定的对心脏正常化的长期影响中的一者或两者而调整心脏重塑起搏包括:响应于所确定的肺压的变化,而调整心脏重塑起搏的递送。
实施例20:实施例13-19中一项所述的方法或设备,其中,响应于短期监测和所确定的对心脏正常化的长期影响中的一者或两者而调整心脏重塑起搏包括:响应于所确定的长期影响,而调整心脏重塑起搏的占空比。
实施例21:实施例13-20中一项所述的方法或设备,其中,响应于该监测而确定所递送的心脏重塑起搏对心脏正常化的长期影响包括:
确定与在心脏重塑起搏的递送之后心率返回到静息心率的时间量相关联的恢复率;以及
将所确定的恢复率与基线恢复率进行比较,
其中,响应于短期监测和所确定的对心脏正常化的长期影响中的一者或两者而调整心脏重塑起搏包括:响应于该比较,而确定是否暂停心脏重塑起搏的递送。
实施例22:实施例13-21中一项所述的方法或设备,其中,监测指示所递送的心脏重塑起搏对心脏正常化的长期影响的一个或多个长期参数包括:在心脏重塑起搏的递送期间感测心脏信号,
其中,响应于该监测而确定所递送的心脏重塑起搏对心脏正常化的长期影响包括:响应于感知到的心脏信号,而确定是否存在心脏收缩时间间期的预定变化,并且
其中,响应于短期监测和所确定的对心脏正常化的长期影响中的一者或两者而调整心脏重塑起搏包括:响应于所确定的心脏收缩时间间期的变化,而确定是否暂停心脏重塑起搏的递送。
实施例23:实施例13-22中一项所述的方法或设备,其中,响应于该监测而确定所递送的心脏重塑起搏对心脏正常化的长期影响包括:
确定心脏重塑起搏的递送期间的指示心力衰竭的生物标志物指示符的长期变化;
确定生物标志物指示符的长期变化是否指示存在对心脏正常化的长期影响;并且
其中,响应于短期监测和所确定的对心脏正常化的长期影响中的一者或两者而调整心脏重塑起搏包括:响应于生物标志物指示符的长期变化指示存在对心脏正常化的长期影响,而暂停心脏重塑起搏的递送。
实施例24:实施例23中所述的方法或设备,其中,生物标志物指示符包括脑钠肽。
实施例25:实施例13-24中一项所述的方法或设备,其中,监测指示所递送的心脏重塑起搏对心脏正常化的长期影响的一个或多个长期参数包括:在延长的时间段内监测心脏收缩时间间期(STI),以生成长期STI,
其中,响应于该监测而确定所递送的心脏重塑起搏对心脏正常化的长期影响包括:将长期STI与基线STI进行比较,
其中,响应于短期监测和所确定的对心脏正常化的长期影响中的一者或两者而调整心脏重塑起搏包括:响应于该比较,而确定是否暂停心脏重塑起搏的递送。
已经参照说明性实施例提供了本公开,并且本公开不旨在以限制性意义进行解释。如先前所述,本领域技术人员将会认识到,其他各种说明性应用可以使用本文所描述的技术来利用本文所描述的装置和方法的有益特性。说明性实施例的各种修改以及本公开的附加实施例在参照本说明书时将会是显而易见的。
- 用于心脏重塑的心脏起搏治疗的递送
- 用于心脏医疗装置和医疗装置系统中起搏治疗的定时递送的远场P波近实时感测
