一种检测血浆中13种神经酰胺的液质联用方法
文献发布时间:2023-06-19 09:26:02
技术领域
本发明涉及生物化学分析检测技术领域,具体涉及一种检测血浆中13种神经酰胺的液质联用方法。
背景技术
神经酰胺是脂类家族中非常重要的一组代谢分子,存在于包括低密度脂蛋白的所有脂蛋白中。神经酰胺有很高的生物活性,可影响许多生物过程,如细胞膜结构、细胞应激发病以及细胞凋亡等,它是饱和脂肪酸和鞘氨醇的代谢产物,代谢功能异常和血脂异常的病理状态下,神经酰胺未被脂肪吸收而蓄积在组织中。血浆中神经酰胺浓度不仅可以提示心血管类疾病风险,如高血压、心衰、二型糖尿病等,也对动脉粥样硬化斑块活性有提示作用。
神经酰胺按照脂肪酸链长度的不同,至少可分为50种类型,近年来欧美顶级研究机构发现三种特有的神经酰胺分子Cer(16:0)、Cer(18:0)和Cer(24:0),他们与心血管疾病发生高度相关,此后围绕关于神经酰胺作为心血管疾病发生发展方面的机制研究层出不穷。多项已发表的研究已验证了神经酰胺对心血管风险预后的预测价值,血浆神经酰胺预测的风险与传统因子(包括年龄、性别、体重指数、吸烟状态和血液胆固醇)无关。另外对于在其他标志物,比如C反应蛋白(CRP)、apoB和Lp-PLA2进行校正后,神经酰胺的预测价值仍很明显。梅奥诊断的Jeffrey医生在对接受侵入性治疗的ACS患者进行了多中心回顾性研究(n=1637),研究者测定患者基线时的血浆神经酰胺浓度,并对其随访1年,在随访过程中出现心血管相关死亡的51例患者中,血浆神经酰胺浓度显著升高,对之前出现的心肌梗死、糖尿病、胆固醇、HDL-C、LDL-C和GRACE评分进行校正后,神经酰胺的预测能力仍显著。结合3种预测性的血浆神经酰胺及其与第4种神经酰胺的比值,Jeffrey医生团队构建了一套神经酰胺评分系统,并在此后的2项大型观察性研究(每项研究>1500例患者)中使用神经酰胺风险评分系统,结果均表明,与得分≤2分的患者相比,得分10-12分的患者出现时间的风险增加6倍,显示出神经酰胺评分系统精准的预测能力。总之,人体神经酰胺浓度的升高或者降低与心血管类疾病风险息息相关,其在血浆中含量的高低对于评估人体健康是至关重要的。
本发明采用高效液相色谱(HPLC)串联质谱分析技术对血浆中与心血管类疾病风险高度相关的13种神经酰胺类物质的含量进行检测分析,大大提高了检测效率和准确性。
发明内容
为了实现上述目的,本发明提供一种检测血浆中13种神经酰胺的液质联用方法,该方法检测灵敏度高、特异性强、准确且血浆样品前处理过程较简单,7min之内可完成多种神经酰胺的分离和检测,基质效应和精密度满足要求。
为了实现上述目的,本发明采用以下技术方案:
本发明提供一种检测血浆中13种神经酰胺的液质联用方法,采用超高效液相色谱串联质谱技术(LC-MS/MS)对血浆中神经酰胺成分含量检测分析,所述的13种神经酰胺为C16(d18:1/16:0)、C18(d18:1/18:0)、C24(d18:1/24:0)、C24:1(d18:1/24:1(15Z))、C14(d18:1/14:0)、C18:1(d18:1/18:1(9Z))、C20(d18:1/20:0)、C22(d18:1/22:0)、C16(d18:0/16:0)、C18(d18:0/18:0)、C24(d18:0/24:0)、C24:1(d18:0/24:1(15Z))和C24:1Lactosyl(β)Ceramide(d18:1/24:1),所述方法包括以下步骤:
(1)血浆样品的预处理:向血浆样品中加入混合内标液,再经振荡、离心,取上清液,即得待检测血浆样品;
(2)定性和定量检测:采用超高效液相色谱技术将待检测血浆样品中13种神经酰胺进行分离,再利用质谱同位素内标定量法通过比对样品中保留时间、质谱信息,检测样品中是否含有13种神经酰胺,并以分别含有上述13种神经酰胺的溶液作为标准品,对待检测血浆样品中每一种神经酰胺成分进行定量检测;
其中,超高效液相色谱条件为:色谱柱的流速为0.3-0.5mL/min,色谱柱的柱温为30-50℃,色谱柱的进样体积为0.5-2μL,色谱流动相包括流动相A和流动相B,采用流动相梯度洗脱的方式;
质谱条件为:离子源为电喷雾离子源或钠喷离子源,扫描模式为多反应监测的正离子扫描模式,喷雾电压为1-2kV,去溶剂温度为100-150℃,雾化气温度为380-450℃,雾化气流速为760-820L/h,锥孔气流速为130-160L/h,图谱数据采集的质荷比范围为50-1000m/z,采集的扫描频率为0.2-0.3s。
优选地,超高效液相色谱条件为:色谱柱为C18色谱柱,色谱柱规格为:长度100mm,内径2.1mm,颗粒直径为1.7μm,色谱柱的流速为0.4mL/min,色谱柱的柱温为40℃,色谱柱的进样体积为1μL。
优选地,色谱流动相中流动相A为含体积分数0.1%甲酸、1mM/L甲酸铵的水,色谱流动相中流动相B为含体积分数0.1%甲酸、0.2mM/L甲酸铵的乙腈-异丙醇混合液,乙腈-异丙醇混合液中乙腈-异丙醇的体积比为4:3;色谱柱的梯度洗脱条件为:0-0.5min流动相B体积分数为85%,0.5-4.2min流动相B体积分数为99%,4.2-6.5min流动相B体积分数为85%。
优选地,质谱条件为:离子源为电喷雾离子源,喷雾电压为1.5kV,去溶剂温度为120℃,雾化气温度为400℃,雾化气流速为800L/h,锥孔气流速为150L/h。
优选地,血浆样品的预处理过程为:取血浆样品50μL加入至离心管内,再向其中加入800μL的混合内标液,经过漩涡震荡,然后经离心后留上清液,即得待检测血浆样品待用。
优选地,所述血浆样品为人或动物的血浆。
与现有技术相比,本发明具有如下有益效果:本发明方法灵敏度高、特异性强、准确且血浆样品前处理过程较简单,7min之内可完成多种神经酰胺组分的分离和检测,基质效应与精密度满足要求,可用于临床上神经酰胺的定性和定量分析,为临床上心血管疾病的健康评估提供一种可靠的检测方法。
附图说明
下面结合附图与具体实施例对本发明作进一步详细说明。
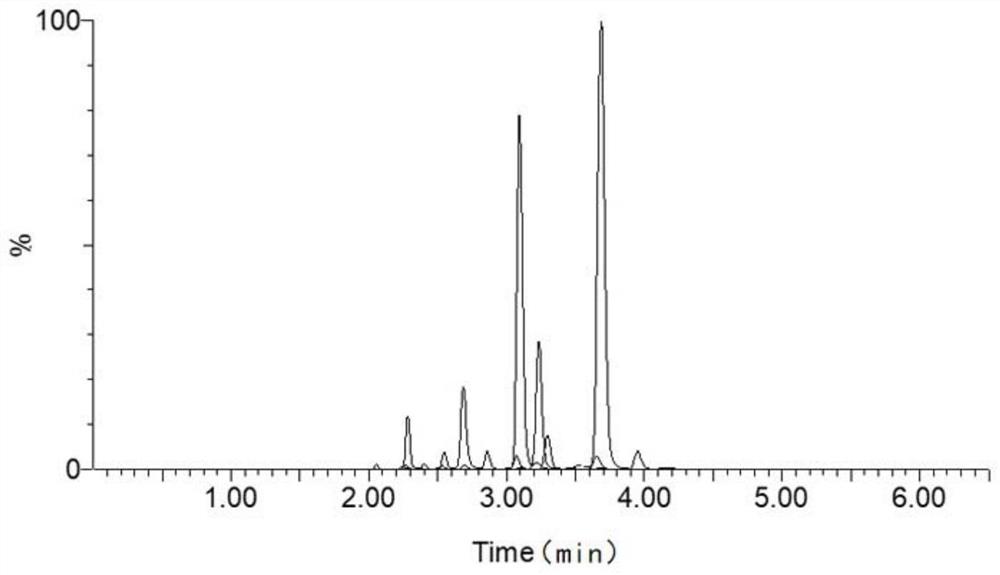
图1为实施例中标准品中13种神经酰胺及4种同位素内标物的总离子流色谱图;
图2为实施例中血浆样品中13种神经酰胺及其4种同位素内标物的总离子流色谱图。
具体实施方式
下面通过具体实施方式来进一步说明本发明的技术方案。本领域技术人员应该明了,所述实施例仅仅是帮助理解本发明,不应视为对本发明的具体限制。
本发明中所采用的血浆样品来自于武汉亚洲心脏病医院2017年12月份门诊的血浆样本。
本发明中所用的仪器包括Xevo TQ-S三重四级杆质谱仪(Waters Corporation);UPLC I-Class超高效液相色谱系统(配自动进样器,Waters Corporation);色谱柱为Waters BEH C18色谱柱(Waters Corporation)。
本发明中试剂耗材包括色谱纯异丙醇(Honeywell,美国);MS级甲醇、乙腈和异丙醇(Fisher,美国);MS级甲酸、甲酸铵(Merck,美国);牛血清白蛋白(BSA)(Merck,美国)。
本发明中标准品:13个神经酰胺的标准品及稳定同位素内标均购自Avanti PolarLipids Inc,纯度均≥99%。
本发明中质控品:含有13个待测神经酰胺分子的空白血浆基质溶液,分低中高三个浓度分别为QC(L)、QC(M)、QC(H),见表1所示。
表1 13种神经酰胺类物质质控品对应浓度(单位μM)
本实施例提供一种检测血浆中13种神经酰胺的液质联用方法,采用超高效液相色谱串联质谱技术对血浆中神经酰胺成分含量检测分析,13种神经酰胺为C16(d18:1/16:0)、C18(d18:1/18:0)、C24(d18:1/24:0)、C24:1(d18:1/24:1(15Z))、C14(d18:1/14:0)、C18:1(d18:1/18:1(9Z))、C20(d18:1/20:0)、C22(d18:1/22:0)、C16(d18:0/16:0)、C18(d18:0/18:0)、C24(d18:0/24:0)、C24:1(d18:0/24:1(15Z))和C24:1Lactosyl(β)Ceramide(d18:1/24:1),包括以下步骤:
(1)血浆样品的预处理:取血浆样品50μL加入至离心管内,再向其中加入800μL的混合内标液,经过漩涡震荡10min,然后在15000r/min条件下离心10min后取上清液,即得待检测血浆样品待用;
混合内标液的配置:分别取1.00mg氘代同位素内标品,包括d7-C16(d18:1/16:0)、d7-C18(d18:1/18:0)、d7-C24(d18:1/24:0)和d7-C24:1(d18:1/24:1(15Z)),依次加入3.67、3.49、3.04、3.05mL甲醇完全溶解,得到浓度均为500μM/L的4种同位素内标溶液,然后用甲醇将这4种同位素内标溶液的浓度分别稀释至50μM/L、100μM/L、150μM/L、150μM/L,然后再取10μL上述溶液加入到100mL异丙醇溶液中,得混合内标液。
(2)定性和定量检测:
采用超高效液相色谱技术将待检测血浆样品中13种神经酰胺进行分离,超高效液相色谱条件为:色谱柱为C18色谱柱,色谱柱规格为:长度100mm,内径2.1mm,颗粒直径为1.7μm,色谱柱的流速为0.4mL/min,色谱柱的柱温为40℃,色谱柱的进样体积为1μL,色谱流动相中流动相A为含体积分数0.1%甲酸、1mM/L甲酸铵的水,色谱流动相中流动相B为含体积分数0.1%甲酸、0.2mM/L甲酸铵的乙腈-异丙醇混合液,乙腈-异丙醇混合液中乙腈-异丙醇的体积比为4:3;色谱柱的梯度洗脱条件为:0-0.5min流动相B体积分数为85%,0.5-4.2min流动相B体积分数为99%,4.2-6.5min流动相B体积分数为85%。
再利用质谱同位素内标定量法,通过比对样品中保留时间、质谱信息,检测样品中是否含有13种神经酰胺,并以分别含有上述13种神经酰胺的溶液作为标准品,以标准品与内标物的浓度比为X轴,标准品与内标物的峰面积比为Y轴,建立校准曲线,对待检测血浆样品中每一种神经酰胺成分进行定量检测;
质谱条件为:离子源为电喷雾离子源,扫描模式为多反应监测的正离子扫描模式,喷雾电压为1.5kV,去溶剂温度为120℃,雾化气温度为400℃,雾化气流速为800L/h,锥孔气流速为150L/h,图谱数据采集的质荷比范围为50-1000m/z,采集的扫描频率为0.25s。;同时监测了目标物C16(d18:1/16:0)(m/z 538.40→264.37)、C18(d18:1/18:0)(m/z 566.44→264.37)、C24(d18:1/24:0)(m/z 650.56→264.37)、C24:1(d18:1/24:1(15Z))(m/z 648.50→264.38)、C14(d18:1/14:0)(m/z 510.40→264.37)、C18:1(d18:1/18:1(9Z))(m/z564.40→264.36)、C20(d18:1/20:0)(m/z 594.44→264.36)、C22(d18:1/22:0)(m/z622.50→264.38)、C16(d18:0/16:0)(m/z 540.40→266.34)、C18(d18:0/18:0)(m/z568.44→266.38)、C24(d18:0/24:0)(m/z 652.56→284.41)、C24:1(d18:0/24:1(15Z)(m/z650.53→284.40)和C24:1Lactosyl(β)Ceramide(d18:1/24:1)(m/z 972.60→264.35)以及同位素内标d7-C16(d18:1/16:0)(m/z 545.44→271.40)、d7-C18(d18:1/18:0)(m/z573.50→271.39)、d7-C24(d18:1/24:0)(m/z 657.56→271.39)和d7-C24:1(d18:1/24:1(15Z))(m/z 655.54→271.39)。各个目标物的去簇电压和碰撞电压参数见表2。
表2 13种神经酰胺物质质谱参数
标准品的配置:分别准确称取C16(d18:1/16:0)2.03mg、C18(d18:1/18:0)2.03mg、C24(d18:1/24:0)2.17mg、C24:1(d18:1/24:1(15Z))5.01mg、C14(d18:1/14:0)5.03mg、C18:1(d18:1/18:1(9Z))5.01mg、C20(d18:1/20:0)5.02mg、C22(d18:1/22:0)5.05mg、C16(d18:0/16:0)5.10mg、C18(d18:0/18:0)5.03mg、C24(d18:0/24:0)5.02mg、C24:1(d18:0/24:1(15Z)5.03mg和C24:1Lactosyl(β)Ceramide(d18:1/24:1)5.01mg,分别加入3.78mL、3.59mL、6.69mL、3.86mL、4.90mL、4.43mL、4.21mL、4.02mL、4.63mL、4.40mL、7.67mL、3.84mL和5.14mL的甲醇,配制成浓度分别为1000、1000、500、2000、2000、2000、2000、2000、2000、2000、1000、2000和1000μM/L的标准品母液;
分别从以上标准品母液中移取120、30、1200、150、3、3、15、60、3、3、30、15、120μL用甲醇定容至3mL,得到浓度分别为40、10、200、100、2、2、10、40、2、2、10、10、40μM/L的混合标准品储备液。
标准品的处理:取15μL混合标准品储备液加入至285μL空白血浆基质溶液中作为第一个高值浓度点;取150μL第一高值浓度点用等体积空白血浆基质溶液稀释得第二高值浓度点,后使用4倍体积的空白血浆基质溶液进行逐级稀释,得其他五个校准浓度点。每个浓度点样品取50μL分装,加入800μL混合内标液,然后涡旋振荡10min,15000r/min条件下离心10min后取600μL上清液,最后移入色谱瓶中上样进行LC-MS/MS分析。
质控品的配制:取混合标准品储备液1μL、5μL、40μL分别用空白血浆基质溶液定容至1000μL得到。
质控品的处理:分别取质控品溶液QC(L),QC(M),QC(H)各50μL于1.5mL离心管中,再向其中加入800μL的混合内标液,经过漩涡震荡10min,然后在15000r/min条件下离心10min后取上清液600μL,最后移入色谱瓶中上样进行LC-MS/MS分析。
超高效液相色谱系统-质谱仪中分析试剂盒上下四周加膜,防震保温,左上方放置流动相A和流动相B,左下方分别放置4*1mL安瓿瓶,分别为标准液和质控品;右边分别放置10mL稀释液和100mL萃取液。分析试剂盒中各组分见表3。
表3 13种神经酰胺类物质分析试剂盒组分的制备
测试结果:
(1)总离子流色谱图:13种神经酰胺的标准品和血浆样品的峰形比较对称,且没有杂峰干扰,说明在此条件下能够得到良好的检测,图1为13种神经酰胺及其4种内标标准品的总离子流色谱图,图2为血浆中13种神经酰胺及其4种内标标准品的总离子流色谱图,这13种物质虽然色谱上没有完全分离开,但结合质谱的特异性,对于LC-MS/MS的检测足以满足定量要求,无需完全分离。
(2)基质效应(matrix effect,ME)和提取回收率(extraction efficiency,EE)考察:由于本实验空白血浆基质为50mg/mL牛血清白蛋白水溶液(5%BSA),且定量标曲由5%BSA配制而得,因此对5%BSA和血浆均进行基质效应和提取回收率考察,基质效应由提取后基质加标和同浓度标样纯溶液相比较而得,浓度越高,基质效应的影响越小,因此高浓度只考察了提取回收率(浓度越高,提取回收率可能越小),测试结果见表4和表5。测试结果显示,13种神经酰胺在5%BSA中几乎无基质效应(均在85%-115%之间),且提取回收率较高(≥80%);同样,13种神经酰胺在血浆中的基质效应经内标校正后,除了C24(d18:0/24:0)在80%以外,其余化合物的基质效应均在88%-105%之间;提取回收率在80%左右。另外C20(d18:1/20:0)低浓度样品的提取回收率较低,应该是加标浓度相对血浆本底浓度较低所致,且高浓度样品提取回收率接近80%。
表4 13种神经酰胺在5%BSA中基质效应和处理效率结果
表5 13种神经酰胺在血浆中基质效应和处理效率结果
(3)校准曲线:采用同位素内标定量法,利用TargetLynx软件以标准物与内标物的浓度比为X轴,标准物与内标物峰面积比为Y轴,建立校准曲线,并计算出血浆中待测物的浓度,13种神经酰胺在各自浓度范围内的线性拟合方程,线性良好,相关系数在0.998以上,满足定量要求,见表6。
表6 13种神经酰胺线性回归方程及线性相关系数
(4)精密度试验:取正常人血浆样品一天内重复处理8批,以同位素内标法定量测定13种神经酰胺的浓度,批内精密度范围为0.80%~11.9%,结果见表7;三日内分3批处理,除C18:1(d18:1/18:1(9Z))以外,计算批间精密度范围为0.18%~10.7%,C18:1(d18:1/18:1(9Z))由于含量非常低(比C24(d18:1/24:0)在血浆中的含量低1000倍),批间精密度为23.7%(一般而言,精密度须在20%以内,对于含量极低的化合物,可放宽至30,结果见表8。
表7批内精密度试验结果(单位μM/L)
表8批间精密度试验结果(单位μM/L)
本发明采用超高效液相色谱串联质谱技术同时测定了人体血浆中13种神经酰胺,同时针对目标物的出峰时间和离子对进行检测,灵敏度高,与此同时,采用同位素内标法定量可以极大的消除基质干扰,而且不受预处理过程、进样体积和流动相等条件的影响,能够达到准确定量。
考察了13种神经酰胺在5%BSA和血浆中的基质效应及提取回收率,13种神经酰胺在5%BSA中几乎无基质效应(均在85%-115%之间),且提取回收率较高(≥80%);同样,13种神经酰胺在血浆中的基质效应经内标校正后,除了C24(d18:0/24:0)在80%以外,其余化合物的基质效应均在88%-105%之间;提取回收率在80%左右。说明5%BSA可作为空白血浆替代基质,用于血浆中神经酰胺的准确定量。
方法的重现性结果表明,日内精密度为0.80%~11.9%,除C18:1(d18:1/18:1(9Z))以外,日间精密度范围为0.18%~10.7%,C18:1(d18:1/18:1(9Z))由于含量非常低(比C24(d18:1/24:0)在血浆中的含量低1000倍),日间精密度为23.7%。一般而言,精密度须在20%以内,对于含量极低的化合物,可放宽至30%。如果使用灵敏度更高的仪器,精密度数据将得到改善。
本发明中的方法灵敏度高、特异性强、准确且前处理过程较简单,7min之内可完成多种神经酰胺的分离和检测,方法稳定性良好,基质效应、提取回收率及精密度,满足要求,可用于临床上血浆中神经酰胺的定量分析,为临床上心血管疾病风险的健康评估提供一种可靠的检测方法。
以上应用了具体个例对本发明进行阐述,只是用于帮助理解本发明,并不用以限制本发明。对于本发明所属技术领域的技术人员,依据本发明的思想,还可以做出若干简单推演、变形或替换。
- 一种检测血浆中13种神经酰胺的液质联用方法
- 一种采用液质联用检测人血浆中呋塞米的方法及应用
